Zusammenfassung 101 L 2 H 3
|
|
|
- Nele Beck
- vor 5 Jahren
- Abrufe
Transkript
1 Zusammenfassung Zusammenfassung In dieser Arbeit gelang zum ersten Mal die Synthese und Charakterisierung von Übergangsmetall koordinierten Anilinoradikalen. Die Eigenschaften der koordinierten Anilinoradikale konnten mit denen der analogen koordinierten Phenoxylradikale verglichen werden. Die makrozyklischen Anilinliganden HL 1, H 2 L 2 und H 3 L 3 wurden synthetisiert. Die aromatischen Ringe der Aniline sind in den ortho- und para-positionen zum Stickstoff mit tert-butylgruppen substituiert. Die Substitution erhöht die Stabilität der Anilinoradikale und macht diese eingehenden Untersuchungen zugänglich. Die Phenolatliganden H 1 L OH,But und H 33 L OH,But sind die Sauerstoffderivate der Liganden HL 1 und H 3 L 3. Ihre Kristallstrukturen zeigen die gleiche Geometrie wie die Komplexe der Anilidliganden. Dies ermöglicht den direkten Vergleich spektroskopischer Eigenschaften von Phenoxyl- und Anilinoradikalen. H 3 C CH 3 H 2 H 2 H 2 H 2 H 2 H 2 HL 1 H 2 L 2 H 3 L 3 Abb.6.1: Die Liganden HL 1, H 2L 2 und H 3L 3 In den Kristallstrukturen der Komplexe mit den Liganden HL 1, H 2 L 2 und H 3 L 3 unterscheiden sich die Anilingruppen. So sind die beiden Aniline im Komplex [H 2 L 2 Cu II ](ClO 4 ) 2 an das Metallzentrum koordiniert. Im Komplex [H 3 L 3 Ga III F 3 ] sind dagegen alle drei Aniline nicht koordiniert. Die Aniline im Komplex [H 3 L 3 Cu II Cl](ClO 4 ) sind alle unterschiedlich. Ein Anilin ist an das Kupferion koordiniert, ein weiteres nur schwach und das letzte ist unkoordiniert. Während in diesen Komplexen der Stickstoff in seiner anilinischen Form vorliegt, sind die
2 102 Zusammenfassung Stickstoffe in den Anilidkomplexen [L 1 Co III (Bu 2 acac)](clo 4 ) und [L 3 Mn IV ](BPh 4 ) deprotoniert. Die Bindungslängen in den aromatischen Ringen der Aniline werden nicht durch die Koordination an Übergangsmetalle beeinflußt, auch der Vergleich mit den Bindungslängen in der Kristallstruktur des Liganden H 2 L 2 zeigt keine Unterschiede. Der aromatische Ring erhält durch die Koordination keinen semichinoiden Charakter. In den Kristallen von [H 3 L 3 Ga III F 3 ] liegen sechs Methanolmoleküle in einer Ringstruktur vor. Das beobachtete Methanolhexamer ist die erste zyklische Methanolstruktur, die röntgenographisch gesichert ist. Die Anilidkomplexe konnten elektrochemisch zu den koordinierten Anilinoradikalen oxidiert werden. Die koordinierten Anilinoradikale zeigen π-π* Übergänge, die im sichtbaren Bereich des elektromagnetischen Spektrums absorbieren. Die Absorptionsbanden liegen im Vergleich zu denen der koordinierten Phenoxylradikale leicht bathochrom verschoben. Im Mangan-Anilinoradikalkomplex ist eine Schwingungsstruktur wie bei den Phenoxylradikalen zu erkennen. Die Kobaltkomplexe mit koordinierten Anilino- oder Phenoxylradikalen zeigen diese Schwingungsstruktur nicht. Das Monoradikal des Komplexes [L 1 Co III (Bu 2 acac)](clo 4 ) zeigt ein S = 1/2 EPR-Spektrum mit einem g-wert von , das im Einklang mit der Formulierung eines organischen Radikals steht. Es werden Hyperfeinkopplungen zum Stickstoff und dem am Stickstoff gebundenen Wasserstoff beobachtet, die denen der unkoordinierten Anilinoradikalen entsprechen. Das zusätzliche Auftreten einer Kobalt-Hyperfeinkopplung zeigt, daß das Anilinoradikal an das Kobaltzentralatom koordiniert ist. Ein weiteres Zeichen für die Koordination des Anilinoradikals ist das Auftreten nur einer benzylischen Hyperfeinkopplung. Dies zeigt, daß die benzylischen Protonen diastereotop sind. Im nicht oxidierten Komplex zeigt sich diese Diastereotopie in den unterschiedlichen Signalen der benzylischen Protonen im 1 H-MR Spektrum. Die Zuordnung der Hyperfeinkopplungen in den EPR-Spektren und der benzylischen Signale im 1 H-MR Spektrum gelang durch den Vergleich mit dem teildeuterierten
3 Zusammenfassung 103 Komplex [L 1d Co III (Bu 2 acac)](clo 4 ), in dem die benzylischen und aromatischen Wasserstoffe deuteriert sind. Die Hyperfeinkopplung zu Deuteronen ist im Vergleich zu der zu Protonen um den Faktor 6.5 kleiner. Der analoge Kobalt-Phenoxylkomplex [ 1 L OH,But Co III (acac)](clo 4 ) zeigt ebenfalls ein S = 1/2 Signal mit einer Hyperfeinkopplung zu nur einem benzylischen Proton. Die Schwingungsbanden in den Resonanz-Raman Spektren konnten durch den Vergleich der deuterierten und nicht deuterierten Anilinoradikale zugeordnet werden. Die Resonanz-Raman Spektren zeigen analog zu den Phenoxylradikalen als charakteristische Bande die Wilson ν 8a Mode. Die Bande der Wilson ν 7a Mode, die bei der Koordination von Phenoxylradikalen stark an Intensität verliert, ist im Spektrum der koordinierten Anilinoradikalen so intensitätsschwach, daß sie nicht beobachtet werden kann. Der Komplex [L 3 Mn IV ](ClO 4 ) konnte elektrochemisch zu den Mono-, Di- und Triradikalkomplexe oxidiert werden. In den EPR-Spektren der Radikalkomplexe beobachtet man eine antiferromagnetische Kopplung der S = 1/2 Spinsysteme mit dem S = 3/2 Spin des Mangan(IV)-Ions. Der unoxidierte Komplex zeigt ein S = 3/2 EPR-Signal mit einer großen ullfeldaufspaltung. Im EPR-Spektrum des Monoradikalkomplexes ist ein Signal des ganzzahligen Spinsystems bei niedrigem Feld zu erkennen. Das koordinierte Diradikal zeigt ein S = 1/2 Signal, welches beim Übergang zum Triradikal stark in der Intensität abnimmt. Das S = 1/2 Signal im Spektrum des koordinierten Diradikals läßt sich mit einem isotropen g-wert und einer Hyperfeinkopplung zum Mangan(IV) simulieren. Die Hyperfeinkopplung weicht von der nach den Methoden der Spinprojektion berechneten ab. Dies wird durch eine elektronische Änderung des Manganions während der zweiten Oxidation erklärt. Das Auftreten einer neuen intensiven Bande bei 570 nm in den UV-Vis Spektren steht damit im Einklang. Die EPR-Spektren der isoelektronischen Chrom(III)-Phenoxylkomplexe zeigen ebenfalls eine starke antiferromagnetische Kopplung der Radikale zu dem Metallzentrum. Die UV-Vis Spektren der Di- und Triradikalkomplexe zeigen ähnliche UV-Vis Spektren wie die Anilinoradikalkomplexe. Die Absorption bei 570 nm wird einem Metall-zu-Radikal Charge-transfer Übergang zugeordnet.
4 104 Zusammenfassung Das elektrochemische Verhalten der Anilino- und Phenoxylradikale zeigt Gemeinsamkeiten. Die Potentialdifferenz zwischen zwei ligandzentrierten Oxidationen kann durch ein einfaches elektrostatisches Modell für eine homogen geladene Kugel in einem Dielektrikum erklärt werden. Die Potentialdifferenz zwischen der ersten Oxidation der Kobalt- und der Mangankomplexe sind für die Oxidationen zum Anilino- und zum Phenoxylradikal nahezu identisch. Die geringere Potentialdifferenz wird mit dem Fehlen einer π-rückbindung vom Liganden zum Metallzentrum in Kobalt(III)-Komplexen erklärt, was zeigt, daß die π-rückbindung vom Phenoxyl- und Anilinoradikal zum Manganion in derselben Größenordnung liegen. In den absoluten Potentialen unterscheiden sich jedoch die Anilinoradikale erheblich von den Phenoxylradikalen. Die Oxidation zum Radikal erfolgt bei den Anilinoradikalen bei einem um ca. 530 mv negativeren Potential als in den vergleichbaren Phenolatkomplexen. Der Vergleich von Anilinoradikalkomplexen mit Phenoxylradikalkomplexen, in denen der aromatische Ring nicht substituiert vorliegt, zeigt, daß die entsprechenden Anilinoradikale stabiler als die Phenoxylradikale sind. Die strukturelle und elektronische Gleichheit der Komplexe [L 3 Mn IV ](BPh 4 ) und [ 3 L An Mn IV ](BPh 4 ) erlaubt es, die Zuordnung der Oxidationen auf den Komplex mit den unsubstituierten Aniliden zu übertragen. Bemerkenswert ist einerseits, daß die Potentiale der ligandzentrierten Oxidationen nicht wesentlich durch die Substitution der Anilide beeinflußt werden, und anderseits, daß die erste ligandzentrierte Oxidation im Komplex [ 3 L An Mn IV ](BPh 4 ) auf der Zeitskala der Cyclovoltammetrie reversibel ist. Die ligandenzentrierten Oxidationen der unsubstituierten Phenolatkomplexe sind dagegen irreversibel. Die erhöhte Stabilität der koordinierten Anilinoradikale gegenüber den koordinierten Phenoxylradikalen kann der niedrigeren Delokalisierung des ungepaarten Elektrons in den aromatischen Ring zugeschrieben werden. Es zeigt sich, daß die EPR-Spektren und die UV-Vis Charakteristika der hier untersuchten Anilino- und Phenoxylradikale nahezu identisch sind. Besonders im Vergleich zwischen den Eigenschaften der Mangan(IV)-Anilinoradikalkomplexe mit
5 Zusammenfassung 105 denen der Chrom(III)-Phenoxylradikalkomplexe erkennt man, daß die Systeme durch die d-elektronenkonfiguration am Metall und den p z -Charakter der Radikale beschrieben werden. Weder die Metalle Mangan oder Chrom noch die spintragenden Zentren Sauerstoff oder Stickstoff in den Radikalliganden können unterschieden werden. Die Elektrochemie der Anilino- und der Phenoxylradikale hingegen unterscheidet sich deutlich. Die leichtere Oxidierbarkeit des Anilids gegenüber dem Phenolat und die erhöhte Stabilität der Anilinoradikale gegenüber den Phenoxylradikalen wird wie bei den unkoordinierten Radikalen mit der höheren Basizität des Anilids erklärt.
5. Schwingungsspektroskopische Untersuchungen
 5. Schwingungsspektroskopische Untersuchungen Die Cyanid- und Thiocyanatliganden gehören als lineare Moleküle ohne Symmetriezentrum zu der Punktgruppe C v. 117 Für das zweiatomige CN - -Molekül gibt es
5. Schwingungsspektroskopische Untersuchungen Die Cyanid- und Thiocyanatliganden gehören als lineare Moleküle ohne Symmetriezentrum zu der Punktgruppe C v. 117 Für das zweiatomige CN - -Molekül gibt es
A. Mezzetti Fragenkatalog X
 Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
7 Kernresonanz-Spektroskopische Untersuchungen
 7 Kernresonanz-Spektroskopische Untersuchungen 79 7 Kernresonanz-Spektroskopische Untersuchungen 7.1 1 H-MR-Signale Die 1 H-MR-Spektroskopie liefert aufgrund der charakteristischen chemischen Verschiebung
7 Kernresonanz-Spektroskopische Untersuchungen 79 7 Kernresonanz-Spektroskopische Untersuchungen 7.1 1 H-MR-Signale Die 1 H-MR-Spektroskopie liefert aufgrund der charakteristischen chemischen Verschiebung
Schuldiges Verhalten bei Metall-Ligand-Komplexen. Allgemeines Verhalten und Charakterisierung
 Schuldiges Verhalten bei Metall-Ligand-Komplexen Allgemeines Verhalten und Charakterisierung 0. Gliederung 1. Definition 2. Mehrkernige Komplexe mit Chinonliganden 3. Analyse der Oxidationsstufen 4. Fazit
Schuldiges Verhalten bei Metall-Ligand-Komplexen Allgemeines Verhalten und Charakterisierung 0. Gliederung 1. Definition 2. Mehrkernige Komplexe mit Chinonliganden 3. Analyse der Oxidationsstufen 4. Fazit
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
Zusammenfassung. Summary
 Radikalhaltige Komplexe als funktionelle Modelle für metalloenzymatische Katalyse Radical Complexes as functional models for metalloenzymatic catalysis Chaudhuri, Phalguni; Wieghardt, Karl; Weyhermüller,
Radikalhaltige Komplexe als funktionelle Modelle für metalloenzymatische Katalyse Radical Complexes as functional models for metalloenzymatic catalysis Chaudhuri, Phalguni; Wieghardt, Karl; Weyhermüller,
1. Zusammenfassung. Zusammenfassung High-spin Verbindungen
 Zusammenfassung 1 1. Zusammenfassung 1.1 High-spin Verbindungen 3-Nitrenodiphenylmethylen (1) und 3,3 -Dinitrenodiphenylmethylen (2) sind gemischte high-spin Verbindungen, die jeweils ein Carbenzentrum
Zusammenfassung 1 1. Zusammenfassung 1.1 High-spin Verbindungen 3-Nitrenodiphenylmethylen (1) und 3,3 -Dinitrenodiphenylmethylen (2) sind gemischte high-spin Verbindungen, die jeweils ein Carbenzentrum
Elektronenspinresonanz-Spektroskopie
 Elektronenspinresonanz-Spektroskopie (ESR-Spektroskopie) engl.: Electron Paramagnetic Resonance Spectroscopy (EPR-Spectroscopy) Stephanie Dirksmeyer, 671197 Inhalt 1. Grundidee 2. physikalische Grundlagen
Elektronenspinresonanz-Spektroskopie (ESR-Spektroskopie) engl.: Electron Paramagnetic Resonance Spectroscopy (EPR-Spectroscopy) Stephanie Dirksmeyer, 671197 Inhalt 1. Grundidee 2. physikalische Grundlagen
5 Die Photolyse von Methyl-Semiquadratsäureamid
 44 5 Die Photolyse von Methyl-Semiquadratsäureamid 5 Die Photolyse von Methyl-Semiquadratsäureamid 5.1 Vorbemerkungen: Methylsemiquadratsäureamid (53) unterscheidet sich von Semiquadratsäureamid (48) nur
44 5 Die Photolyse von Methyl-Semiquadratsäureamid 5 Die Photolyse von Methyl-Semiquadratsäureamid 5.1 Vorbemerkungen: Methylsemiquadratsäureamid (53) unterscheidet sich von Semiquadratsäureamid (48) nur
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+
![Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ Elektronenspektrum von [Ti(H 2 O) 6 ] 3+](/thumbs/66/55543366.jpg) Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Seminar zum Praktikum Anorganische Chemie III III
 Seminar zum Praktikum Anorganische hemie III III Metallorganische hemie Dr. J. Wachter IR-Teil 4 www.chemie.uni-regensburg.de/anorganische_hemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_hemie/wachter/lehre.html
Seminar zum Praktikum Anorganische hemie III III Metallorganische hemie Dr. J. Wachter IR-Teil 4 www.chemie.uni-regensburg.de/anorganische_hemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_hemie/wachter/lehre.html
IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC
 IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Terminübersicht (14 täg.) Gruppe 1 Gruppe 2 1. Seminar
IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Terminübersicht (14 täg.) Gruppe 1 Gruppe 2 1. Seminar
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
4. Zusammenfassung 100 H P P H
 4. Zusammenfassung 100 =XVDQIDVVXQJ Die vorliegende Arbeit beschreibt sowohl die Synthese und Komplexchemie von Zirkoniumphosphaniden sowie der homologen Systeme des Arsens, als auch die erstellung von
4. Zusammenfassung 100 =XVDQIDVVXQJ Die vorliegende Arbeit beschreibt sowohl die Synthese und Komplexchemie von Zirkoniumphosphaniden sowie der homologen Systeme des Arsens, als auch die erstellung von
4 Synthesen antiprionen-aktiver Verbindungen
 4 Synthesen antiprionen-aktiver Verbindungen Quinacrinanaloga (Grundstruktur C) 77 4 Synthesen antiprionen-aktiver Verbindungen 4.1 Synthesen der Quinacrinanaloga (Grundstruktur C) Die Synthesen der Quinacrinanaloga
4 Synthesen antiprionen-aktiver Verbindungen Quinacrinanaloga (Grundstruktur C) 77 4 Synthesen antiprionen-aktiver Verbindungen 4.1 Synthesen der Quinacrinanaloga (Grundstruktur C) Die Synthesen der Quinacrinanaloga
Die Bindung in Übergangsmetallkomplexenn. Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth
 Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
Herstellung und Oxidation von 2,4,6-Tri-tert-butylphenol
 2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
1 Einleitung. Einleitung 1
 Einleitung 1 1 Einleitung Die Supramolekulare Chemie ist die Chemie der intermolekularen Bindung. Sie beschäftigt sich mit Strukturen und Funktionen von Einheiten, die durch Assoziation zweier oder mehrerer
Einleitung 1 1 Einleitung Die Supramolekulare Chemie ist die Chemie der intermolekularen Bindung. Sie beschäftigt sich mit Strukturen und Funktionen von Einheiten, die durch Assoziation zweier oder mehrerer
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden
 Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Spektroskopie-Seminar WS 17/18 5 NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration
 g 4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration a () ϕ ( 2) ϕ ( 2) ϕ ( 1) ψ = ϕ + 1 b a b Heitler-London ( ) ϕ ( 2) + ϕ ( 2) ϕ ( 1) + [ ϕ ( 1) ϕ (
g 4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration a () ϕ ( 2) ϕ ( 2) ϕ ( 1) ψ = ϕ + 1 b a b Heitler-London ( ) ϕ ( 2) + ϕ ( 2) ϕ ( 1) + [ ϕ ( 1) ϕ (
M U S T E R L Ö S U N G
 Prof. Dr. B. König Prof. Dr.. Geyer 3. Klausur zum Praktikum rganische hemie I für Studierende der hemie und der Biochemie im SS 2001 am Donnerstag, dem 26. Juli 2001 M U S T E R L Ö S U G ame:...vorname:...
Prof. Dr. B. König Prof. Dr.. Geyer 3. Klausur zum Praktikum rganische hemie I für Studierende der hemie und der Biochemie im SS 2001 am Donnerstag, dem 26. Juli 2001 M U S T E R L Ö S U G ame:...vorname:...
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 31. Januar 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 31. Januar 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Übersicht. Wasserstoff-Verbindungen
 Allgemeine Chemie - Teil Anorganische Chemie II: 5. Hauptgruppe Übersicht A. Die Stellung der Elemente der 5. Hauptgruppe im Periodensystem. Stickstoff 2.1. Stickstoff-Wasserstoff Wasserstoff-Verbindungen.1.1.
Allgemeine Chemie - Teil Anorganische Chemie II: 5. Hauptgruppe Übersicht A. Die Stellung der Elemente der 5. Hauptgruppe im Periodensystem. Stickstoff 2.1. Stickstoff-Wasserstoff Wasserstoff-Verbindungen.1.1.
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 5: )
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Spektroskopie in der Organischen Chemie. Spin-Entkopplung
 Spin-Entkopplung Spin-Spin-Kopplung zwischen nichtäquivalenten Kernen führt zur Aufspaltung der Signale der Kopplungspartner: im Falle größerer Spinsysteme können komplexe Multiplettsignale entstehen.
Spin-Entkopplung Spin-Spin-Kopplung zwischen nichtäquivalenten Kernen führt zur Aufspaltung der Signale der Kopplungspartner: im Falle größerer Spinsysteme können komplexe Multiplettsignale entstehen.
4.2 Cyclische Verbindungen mit Stickstoffdoppelbindungen (Azoverbindungen)
 4.2 Cyclische Verbindungen mit Stickstoffdoppelbindungen (Azoverbindungen) 4.2.1 Reine Azoverbindungen (22-28) Azoverbindungen stellen in Form der Azofarbstoffe eine sehr alte Klasse von Verbindungen dar.
4.2 Cyclische Verbindungen mit Stickstoffdoppelbindungen (Azoverbindungen) 4.2.1 Reine Azoverbindungen (22-28) Azoverbindungen stellen in Form der Azofarbstoffe eine sehr alte Klasse von Verbindungen dar.
Forschen in der Chemie und Materialwissenschaften 2014
 Forschen in der Chemie und Materialwissenschaften 2014 Untersuchung von reaktiven Zwischenprodukten in Argonmatrizen Jim Widmer, Kantonsschule Trogen Betreuer: Prof. Dr. Thomas Bally, Prof. Andreas Zumbühl
Forschen in der Chemie und Materialwissenschaften 2014 Untersuchung von reaktiven Zwischenprodukten in Argonmatrizen Jim Widmer, Kantonsschule Trogen Betreuer: Prof. Dr. Thomas Bally, Prof. Andreas Zumbühl
Chemische und Magnetische Äquivalenz
 Chemische und Magnetische Äquivalenz Das Aussehen von NMR-Signalen in Mehr-Spinsystemen wird ganz wesentlich davon beeinflusst, ob es äquivalente Kerne gibt oder nicht. ierbei sind zwei wichtige Arten
Chemische und Magnetische Äquivalenz Das Aussehen von NMR-Signalen in Mehr-Spinsystemen wird ganz wesentlich davon beeinflusst, ob es äquivalente Kerne gibt oder nicht. ierbei sind zwei wichtige Arten
Wissenschaftliches Schreiben in der AC
 Wissenschaftliches Schreiben in der AC Saarbrücken, den 05.06.2015 6 Publikationen in Wissenschaftlichen Zeitschriften > 1 Einleitung Inhalte der Übung Wissenschaftliches Schreiben in der AC 1 Einleitung
Wissenschaftliches Schreiben in der AC Saarbrücken, den 05.06.2015 6 Publikationen in Wissenschaftlichen Zeitschriften > 1 Einleitung Inhalte der Übung Wissenschaftliches Schreiben in der AC 1 Einleitung
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
c = Ausbreitungsgeschwindigkeit (2, m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 )
 2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Atommodell. Atommodell nach Bohr und Sommerfeld Für sein neues Atommodell stellte Bohr folgende Postulate auf:
 Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2018/19 www.ruhr-uni-bochum.de/chirality 1 Komplementärfarben Absorbiert eine Probe gelbes
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2018/19 www.ruhr-uni-bochum.de/chirality 1 Komplementärfarben Absorbiert eine Probe gelbes
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie
Aufgabe 1: (18 Punkte)
 Aufgabe 1: (18 Punkte) In der Arbeitsgruppe Hilt wurde folgende Reaktionssequenz durchgeführt: A H 10 H B O O O 1 1 2 2 + 10 3 3 4 4 Δ DA- Produkt 6-9 5 5 6-9 2 Ph Ph Co(dppe) 2 3 3 4 4 Im ersten Reaktionsschritt
Aufgabe 1: (18 Punkte) In der Arbeitsgruppe Hilt wurde folgende Reaktionssequenz durchgeführt: A H 10 H B O O O 1 1 2 2 + 10 3 3 4 4 Δ DA- Produkt 6-9 5 5 6-9 2 Ph Ph Co(dppe) 2 3 3 4 4 Im ersten Reaktionsschritt
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 13. Juli 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 13. Juli 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
Aufbau von Atomen. Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem
 Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
NMR Spektroskopie. Aufgaben
 hemische Verschiebung 1. Zeichnen Sie zu den nachfolgend aufgeführten Stoffen die Strukturformeln! Unterscheiden Sie dann zwischen chemisch äquvalenten und nichtäquivalenten Kernen. Bezeichnen Sie die
hemische Verschiebung 1. Zeichnen Sie zu den nachfolgend aufgeführten Stoffen die Strukturformeln! Unterscheiden Sie dann zwischen chemisch äquvalenten und nichtäquivalenten Kernen. Bezeichnen Sie die
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
C.C. Milisenda, S. Koch und S. Müller, Deutsche Stiftung Edelsteinforschung (DSEF)
 02/12/2016 Smaragde aus Äthiopien C.C. Milisenda, S. Koch und S. Müller, Deutsche Stiftung Edelsteinforschung (DSEF) Im Oktober 2014 konnten wir auf den Münchener Mineralientagen 2 Exemplare von Smaragden
02/12/2016 Smaragde aus Äthiopien C.C. Milisenda, S. Koch und S. Müller, Deutsche Stiftung Edelsteinforschung (DSEF) Im Oktober 2014 konnten wir auf den Münchener Mineralientagen 2 Exemplare von Smaragden
Welche Prinzipien bestimmen die quantenmechanischen Zustände, beschrieben durch ihre Quantenzahlen, die die Elektronen eines Atoms einnehmen?
 phys4.021 Page 1 12. Mehrelektronenatome Fragestellung: Betrachte Atome mit mehreren Elektronen. Welche Prinzipien bestimmen die quantenmechanischen Zustände, beschrieben durch ihre Quantenzahlen, die
phys4.021 Page 1 12. Mehrelektronenatome Fragestellung: Betrachte Atome mit mehreren Elektronen. Welche Prinzipien bestimmen die quantenmechanischen Zustände, beschrieben durch ihre Quantenzahlen, die
LAF-Klausur. Wintersemester 2011/12
 LAF-Klausur Wintersemester 2011/12 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile werden
LAF-Klausur Wintersemester 2011/12 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile werden
Darstellung von Malachitgrün Präparat 5
 Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Kurs "Spektroskopische Methoden in der Anorganischen und Organischen Chemie" Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt 1)
 Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt ) Zum Lösungsmittel: Das Kohlenstoffspektrum zeigt bei 77 ppm drei gleich große äquidistante Signale. Diese stammen von CDC 3. Chemische Verschiebungen
Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt ) Zum Lösungsmittel: Das Kohlenstoffspektrum zeigt bei 77 ppm drei gleich große äquidistante Signale. Diese stammen von CDC 3. Chemische Verschiebungen
Festkörperelektronik 2008 Übungsblatt 4
 Lichttechnisches Institut Universität Karlsruhe (TH) Prof. Dr. rer. nat. Uli Lemmer Dipl.-Phys. Alexander Colsmann Engesserstraße 13 76131 Karlsruhe Festkörperelektronik 4. Übungsblatt 12. Juni 2008 Die
Lichttechnisches Institut Universität Karlsruhe (TH) Prof. Dr. rer. nat. Uli Lemmer Dipl.-Phys. Alexander Colsmann Engesserstraße 13 76131 Karlsruhe Festkörperelektronik 4. Übungsblatt 12. Juni 2008 Die
8 Zusammenfassung der Ergebnisse
 Zusammenfassung der Ergebnisse und Ausblick 131 8 Zusammenfassung der Ergebnisse Die vorliegende Arbeit beschreibt die Synthese, Charakterisierung und beschichtungstechnische Anwendung von Übergangsmetall-substituierten
Zusammenfassung der Ergebnisse und Ausblick 131 8 Zusammenfassung der Ergebnisse Die vorliegende Arbeit beschreibt die Synthese, Charakterisierung und beschichtungstechnische Anwendung von Übergangsmetall-substituierten
Die Primärreaktion der Photosynthese
 Die Primärreaktion der Photosynthese 1. Energetische Betrachtungen Wie ist es energetisch möglich, dass das so energiearme und stabile Wassermolekül in der Primärreaktion der Photosynthese zu Sauerstoff
Die Primärreaktion der Photosynthese 1. Energetische Betrachtungen Wie ist es energetisch möglich, dass das so energiearme und stabile Wassermolekül in der Primärreaktion der Photosynthese zu Sauerstoff
12.8 Eigenschaften von elektronischen Übergängen. Übergangsfrequenz
 phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
Spektroskopische und theoretische Untersuchungen von Übergangsmetallkomplexen mit non-innocent Liganden
 Spektroskopische und theoretische Untersuchungen von Übergangsmetallkomplexen mit non-innocent Liganden Jurema Schmidt Vortrag im Seminar Moderne Anwendungen der magnetischen Resonanz 17.10.2013 Inhalt
Spektroskopische und theoretische Untersuchungen von Übergangsmetallkomplexen mit non-innocent Liganden Jurema Schmidt Vortrag im Seminar Moderne Anwendungen der magnetischen Resonanz 17.10.2013 Inhalt
Was ist Elektrochemie? Elektrochemie. Elektrochemie ist die Lehre von der Beziehung
 Was ist Elektrochemie? Elektrochemie Elektrochemie ist die Lehre von der Beziehung zwischen elektrischen und chemischen Prozessen. 131 Stromleitung in einem Metall Wir haben gelernt, dass die Stromleitung
Was ist Elektrochemie? Elektrochemie Elektrochemie ist die Lehre von der Beziehung zwischen elektrischen und chemischen Prozessen. 131 Stromleitung in einem Metall Wir haben gelernt, dass die Stromleitung
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
1 Der Elektronentransfer: Theorie nach Marcus und Hush
 1 Der Elektronentransfer: Theorie nach Marcus und Hush Betrachtet wird der Elektronentransfer zwischen zwei solvatisierten Spezies in einer Lösung. Es gibt zwei Arten von Elektronentransfer, Reaktionen
1 Der Elektronentransfer: Theorie nach Marcus und Hush Betrachtet wird der Elektronentransfer zwischen zwei solvatisierten Spezies in einer Lösung. Es gibt zwei Arten von Elektronentransfer, Reaktionen
- Allgemeiner Überblick über Magnetismus und magnetische Materialien
 - 1 - Vorl. #1 (22. kt. 2010) Molekulare Nanomagnete: Quantenphysik zum Anfassen WS2010/2011 Prof. liver Waldmann Hochhaus Zi. 202 Tel.: 5717 Sprechstunde: jederzeit (Ihr seid immer herzlich willkommen)
- 1 - Vorl. #1 (22. kt. 2010) Molekulare Nanomagnete: Quantenphysik zum Anfassen WS2010/2011 Prof. liver Waldmann Hochhaus Zi. 202 Tel.: 5717 Sprechstunde: jederzeit (Ihr seid immer herzlich willkommen)
Spektroskopische Methoden in der Organischen Chemie (OC IV) NMR Spektroskopie 1. Physikalische Grundlagen
 NMR Spektroskopie 1. Physikalische Grundlagen Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR Spektroskopie 1. Physikalische Grundlagen Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
Organische Chemie I Molekül der Woche - Azulen
 I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
NMR-Lösungsmittel. 1 H-NMR. Bei der Verwendung der normalen, nichtdeuterierten Lösungsmittel. Spektroskopie in der Organischen Chemie
 NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
Kombinierte Übungen zur Spektroskopie Beispiele für die Bearbeitung
 Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 18. Juli 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 18. Juli 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Chemie der Metalle (Nachklausur)
 Aufgabe 1 2 3 4 5 6 7 8 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Abschlußklausur zur Vorlesung Chemie der Metalle
Aufgabe 1 2 3 4 5 6 7 8 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Abschlußklausur zur Vorlesung Chemie der Metalle
Schriftliche Prüfung BSc Frühling 2014
 Prüfungen Analytische Chemie Samstag, 1. Februar 2014 Schriftliche Prüfung BSc Frühling 2014 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Samstag, 1. Februar 2014 Schriftliche Prüfung BSc Frühling 2014 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Homoaromatizität. Charlotte Over Lara Schultes
 Homoaromatizität Charlotte Over Lara Schultes 02.12.2010 Übersicht 1. Einführung 2. Aromatizität 3. Homoaromatizität 4. Beispiele 4.1 Kationische Homoaromaten 4.2 Neutrale Homoaromaten 4.3 Anionische Homoaromaten
Homoaromatizität Charlotte Over Lara Schultes 02.12.2010 Übersicht 1. Einführung 2. Aromatizität 3. Homoaromatizität 4. Beispiele 4.1 Kationische Homoaromaten 4.2 Neutrale Homoaromaten 4.3 Anionische Homoaromaten
Spektroskopie-Seminar SS NMR-Spektroskopie. C-NMR-Spektroskopie und 2D-Spektroskopie
 13 C-NMR-Spektroskopie und 2D-Spektroskopie 6.1 Allgemeines Kernresonanz: Wechselwirkungen zwischen dem magnetischen Moment von Atomkernen mit einem magnetischen Wechselfeld Nur solche Isotope können untersucht
13 C-NMR-Spektroskopie und 2D-Spektroskopie 6.1 Allgemeines Kernresonanz: Wechselwirkungen zwischen dem magnetischen Moment von Atomkernen mit einem magnetischen Wechselfeld Nur solche Isotope können untersucht
Übergangsmetallkomplexe neuer Thioether- Phenolatliganden. Synthese, Strukturen und Eigenschaften
 CHRIFTENREIHE DE MAX-PLANCK-INTITUT FÜR TRAHLENCHEMIE IN 0932-5131 NR. 139 Übergangsmetallkomplexe neuer Thioether- Phenolatliganden ynthese, trukturen und Eigenschaften Dissertation zur Erlangung des
CHRIFTENREIHE DE MAX-PLANCK-INTITUT FÜR TRAHLENCHEMIE IN 0932-5131 NR. 139 Übergangsmetallkomplexe neuer Thioether- Phenolatliganden ynthese, trukturen und Eigenschaften Dissertation zur Erlangung des
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006
 Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Lösungen 3. Übungsblatt SS 2002
 Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Einführung in die Astronomie und Astrophysik I
 Einführung in die Astronomie und Astrophysik I Teil 8 Jochen Liske Fachbereich Physik Hamburger Sternwarte jochen.liske@uni-hamburg.de Astronomische Nachricht der Woche Astronomische Nachricht der Woche
Einführung in die Astronomie und Astrophysik I Teil 8 Jochen Liske Fachbereich Physik Hamburger Sternwarte jochen.liske@uni-hamburg.de Astronomische Nachricht der Woche Astronomische Nachricht der Woche
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Einführung in die NMR-Spektroskopie. NMR-Spektroskopie. Teil 1: Einführung und Grundlagen der 1 H NMR. Das NMR Spektrometer
 NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ
 Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Grundpraktikum für Biologen 2016
 Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
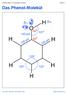 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Fluoreszenzlampenl. René Riedel. Bettina Haves
 Leuchtstoffe in Fluoreszenzlampenl René Riedel Bettina Haves Inhalt 1) Fluoreszenzlampen 2) Fluoreszenz 3) Geschichte der Leuchtstoffe 4) Leuchtstoffe in Fluoreszenzlampen 5) Weitere Anwendungsbereiche
Leuchtstoffe in Fluoreszenzlampenl René Riedel Bettina Haves Inhalt 1) Fluoreszenzlampen 2) Fluoreszenz 3) Geschichte der Leuchtstoffe 4) Leuchtstoffe in Fluoreszenzlampen 5) Weitere Anwendungsbereiche
Redoxreaktionen. Elektrochemische Spannungsreihe
 Elektrochemische Spannungsreihe Eine galvanische Zelle bestehend aus einer Normal-Wasserstoffelektrode und einer anderen Halbzelle erzeugen eine Spannung, die, in 1-molarer Lösung gemessen, als Normal-
Elektrochemische Spannungsreihe Eine galvanische Zelle bestehend aus einer Normal-Wasserstoffelektrode und einer anderen Halbzelle erzeugen eine Spannung, die, in 1-molarer Lösung gemessen, als Normal-
Einführung in die ENDOR- Spektroskopie
 Einführung in die ENDOR- Spektroskopie Institut für Chemie und Biochemie Freie Universität Berlin Stand: 1996 Inhalt (1) 1. Einführung 2. Grundlagen 2.1. ENDOR-Spektroskopie 2.2. TRIPLE-Resonanz 2.3. Spektrometer-Aufbau
Einführung in die ENDOR- Spektroskopie Institut für Chemie und Biochemie Freie Universität Berlin Stand: 1996 Inhalt (1) 1. Einführung 2. Grundlagen 2.1. ENDOR-Spektroskopie 2.2. TRIPLE-Resonanz 2.3. Spektrometer-Aufbau
11. Elektronen im Festkörper
 11. Elektronen im Festkörper 11.1 Elektrische Leitung in Festkörpern 11.2 Freies Elektronengas im Sommerfeld- Modell 11.3 Bändermodell des Festkörpers 11.4 Metalle, Isolatoren und Halbleiter WS 2013/14
11. Elektronen im Festkörper 11.1 Elektrische Leitung in Festkörpern 11.2 Freies Elektronengas im Sommerfeld- Modell 11.3 Bändermodell des Festkörpers 11.4 Metalle, Isolatoren und Halbleiter WS 2013/14
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 29. Januar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 29. Januar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Infrarot Spektroskopie organischer Verbindungen
 Infrarot Spektroskopie organischer Verbindungen Praktikum (B.C. 3.4) Lehrstuhl für Instrumentelle Analytik Michael Deicke Michael.Deicke@uni-jena.de Ziele des Praktikums IR-Spektren organischer Verbindungen
Infrarot Spektroskopie organischer Verbindungen Praktikum (B.C. 3.4) Lehrstuhl für Instrumentelle Analytik Michael Deicke Michael.Deicke@uni-jena.de Ziele des Praktikums IR-Spektren organischer Verbindungen
P105. Konstitution. Massenspektrum 100 % m/z
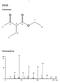 1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
Hallwachs-Experiment. Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe
 Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Auf der rechten Seite sind Beispiele für kovalente Bindungen.
 Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Übungen zu "EMK" Übungen zu EMK - Seite 1 (von 5)
 Übungen zu "EMK" A Voraussage der ablaufenden Reaktion mit Standardpotentialen Welcher Stoff reagiert zu welchem Produkt? Möglichst die vollständige Reaktionsgleichung. E o Werte aus "Rauscher, Voigt".
Übungen zu "EMK" A Voraussage der ablaufenden Reaktion mit Standardpotentialen Welcher Stoff reagiert zu welchem Produkt? Möglichst die vollständige Reaktionsgleichung. E o Werte aus "Rauscher, Voigt".
Spinsysteme. AX 3 -Spinsystem
 Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
