BIOCHEMIE light. Hubert Rehm / Friederike Hammar. 5., korrigierte und erweiterte Auflage 2013
|
|
|
- Kai Mann
- vor 8 Jahren
- Abrufe
Transkript
1 BIEMIE light ubert Rehm / Friederike ammar 5., korrigierte und erweiterte Auflage 2013 VERLAG EURPA-LERMITTEL ourney, Vollmer Gmb & o. KG Düsselberger Straße aan-gruiten Europa-r.: 54425
2 ubert Rehm hat in Tübingen Biochemie und Mathematik studiert und anschließend am Max-Planck- Institut für Psychiatrie über spannungsabhängige Ionenkanäle promoviert. Es folgte ein Jahrzehnt molekularbiologischer Forschung u. a. am ZMB in eidelberg, am entre national de la recherche scientifique in izza, am VA Medical enter in Seattle und an der ET Zürich. eute arbeitet ubert Rehm als freier Wissenschaftsjournalist und Buchautor in Rottweil. Friederike ammar studierte hemie mit Schwerpunkt Biochemie an der Universität Mainz. Während ihrer Doktorarbeit in der Immunologie hatte sie Gelegenheit, hautnah zu erleben, mit welchen Schwierigkeiten besonders Medizinstudenten beim Verständnis biochemischer Zusammenhänge kämpfen. Danach arbeitete sie als freie Wissenschaftsjournalistin für die Themenfelder Biochemie, Biotechnologie, Gentechnik und molekulare Medizin. Sie war in mehreren Projekten der Universität Mainz und anderer Institu tionen mit der Kommunikation biowissenschaftlicher Forschungsergebnisse beschäftigt und arbeitet heute in der Pressestelle eines erstellers von Auto immundiagnostika. 5., korrigierte und erweiterte Auflage 2013 Druck ISB Alle Rechte vorbehalten. Das Werk ist urheberrechtlich geschützt. Jede Verwertung außerhalb der gesetzlich geregelten Fälle muss vom Verlag schriftlich genehmigt werden. Der Inhalt des Werkes wurde sorgfältig erarbeitet. Dennoch übernehmen Autoren und Verlag für die Richtigkeit von Angaben, inweisen und Ratschlägen sowie für eventuelle Druckfehler keine aftung by Verlag Europa-Lehrmittel, ourney, Vollmer Gmb & o. KG, aan-gruiten Satz: Birgit irksena Satzfein, Berlin Umschlaggestaltung: braunwerbeagentur, Radevormwald Druck: Media-Print Informationstechnologie Gmb, Paderborn
3 Vorwort Es ist viel, was man heutzutage vom gemeinen Studenten verlangt: Anatomie, istologie, Physiologie und auch noch Biochemie. Die ähnelt verzweifelt dem Berliner Telefonbuch: Eine Unzahl von ummern und amen, die sich kein Mensch merken kann. Selbst der Professor kennt nur ein paar Seiten. Biochemie-light gibt die wichtigen ummern an. Es beschränkt sich auf das was zählt für Praktika, Klausur und Physikum. Zudem erläutert es Experimente, die in Biochemie-Praktika durchgeführt werden. Mit Biochemie-light wissen Sie, worauf es ankommt, haben den Überblick, verstehen die Zusammenhänge. Sie stehen nicht mehr mit flatternden erven vor den Wälzern mit ihren underten von Seiten und Tausenden von Formeln und Strukturen. Sie vermeiden es, zweitrangige Stoffwechselketten mit sämtlichen Enzymen, ofaktoren und Ionen auswendig zu lernen. Man kann nicht überall alles wissen. Das Büchlein ist ein Konzentrat der Biochemie, es enthält das Überlebensnotwendige, das, was Sie mindestens brauchen, um eine Prüfung zu bestehen. In der fünften Auflage ist das Buch angeschwollen. Das liegt nicht an der Geschwätzigkeit der Autoren, sondern am Fleiß der Forscher. Die haben in den letzten Jahren Ergebnisse gesammelt wie zehntausend hungrige amster ihre Weizenkörner für den Wintervorrat. Gentherapie, Apoptose, MicroRA, Epigenetik, Sequenzierung überall gab es neue Entwicklungen, Erkenntnisse, Sichtweisen. Das konnten wir nicht ignorieren, nur um bei der magischen Zahl von 100 Seiten zu bleiben. Jawohl: Die Biochemie und Molekularbiologie hat in den letzten Jahren alle Grenzen gesprengt, auch die von Biochemie-light. Dennoch: sein Prinzip konzentrieren, illustrieren, simplifizieren hält Biochemie-light auch in der fünften Auflage durch. Jetzt gerade. Wir bedanken uns bei den Studenten der Medizin, Frederick Giesel, und Zahnmedizin, Martin Stannarius, für die Idee zu dem Buch. ord Michael Becker hat wertvolle Vorschläge zu Inhalt und Aufbau gemacht, so geht die chemische Einleitung auf seine Anregung zurück. Um die nachfolgenden Auflagen haben sich viele Kritiker verdient gemacht, so ans Bisswanger aus Tübingen, der uns in der Kinetik beraten hat, ornel Mülhardt aus Basel, Roland ütterer aus Würzburg, Michaela Wendeler und Thomas Kolter aus Bonn. Mit André Schrattenholz aus Mainz haben wir hilfreiche Diskussionen geführt. Auch aufmerksame Leser haben dafür gesorgt, dass wir Fehler ausmerzen und schwer Verständliches verdaulich machen konnten. So ans Kunze aus Göttingen, Alexander Schulze aus Kassel und Eva-Maria Wingender aus Antwerpen. Für diese Auflage haben uns Bettina Staiger aus Regensburg, Ella Klundt aus Freiburg und Michael Jelden die Augen geöffnet. Wir, längst text- und formelblind, hätten höchstens einen Bruchteil der Fehler gefunden, die diese Täubchen aus den Seiten lasen. Frieder Wiech lieferte wie immer die Zeichnungen. Last but not least: Anregungen, Kritik oder Verbesserungsvorschläge an nehmen wir gerne entgegen. Lob dagegen verbreiten Sie besser unter Ihren Studienkollegen. erbst 2013 Autoren und Verlag
4 Inhaltsverzeichnis Grundbegriffe Lipide und Zucker Lipide Monosaccharide Disaccharide Polysaccharide... 4 Zuckerderivate... 5 Glycoproteine... 6 Glycolipide... 6 Proteine... 7 Aminosäuren Proteinaufbau Proteinkonformation Proteinfunktionen Strukturproteine Enzyme Transportproteine Proteinanalytik hromatographie Polyacrylamidgelelektrophorese Aminosäuresequenz Aminosäurezusammensetzung Enzyme, ofaktoren und Kinetik Thermodynamische Grundlagen Klassifizierung von Enzymen Mechanismen und Regulation von Enzymen. 23 ATP, AD +, oenzym A, S-Adenosylmethionin. 24 Weitere ofaktoren, Vitamine Enzymkinetik Allosterie ucleinsäuren Grundlagen Desoxyribonucleinsäuren DA-Replikation DA-Reparatur DA-Marker Ribonucleinsäuren tra, rra, snra, mra Transkription Proteinbiosynthese Der genetische ode Translation emmer der Translation und Transkription.. 51 Micro-RA Viren Plasmide Transposons Telomere Methoden der Molekularbiologie Restriktionsnucleasen ucleinsäuren isolieren ucleinsäuren trennen DA-Sequenzieren ybridisieren, Southern-blotting Klonieren Gentherapie I Polymerase-Kettenreaktion (PR) Epigenetik Stoffwechsel Glycolyse und Gluconeogenese itratzyklus xidative Phosphorylierung Glycogen (Abbau, Synthese, Regulation) Pentosephosphatweg Lipidsynthese Fettsäuresynthese Regulation der Fettsäuresynthese Phospholipidsynthese holesterolsynthese Lipidabbau β-xidation holesterolabbau Lipoproteine Stoffwechsel von Purin- und Pyrimidinbasen. 91 Aminosäurebiosynthese Aminosäureabbau Porphyrinsynthese arnstoffzyklus Kompartimentierung Apoptose Der optische Test ormone ormonrezeptoren und G-Proteine Regulation des Blutglucosespiegels Insulinsynthese Diabetes mellitus ypothalamisch-hypophysäres System AT Vitamin D und alcitriol ormone der ebennierenrinde ormone des ebennierenrindenmarks Renin-Angiotensin-System Schilddrüsenhormone Endorphine Molekulare Physiologie Immunsystem Antikörper (= Immunglobuline) T-Zell vermittelte Immunität Monoklonale Antikörper ELISA und Western-Blot Reizleitung im ervensystem Phys. Grundlagen und Ionenkanäle eurotransmitter-rezeptoren Biochemie des Sehens Muskel: Kontraktion und Regulation Verdauung (Magen, Pankreas, Darm) Leber iere Blut Bindung von ämoglobin Regulation der 2 -Bindung von ämoglobin. 136 Puffersysteme des Blutes Blutgerinnung Wie entsteht Krebs? ii
5 Verzeichnis der Kapitelüberschriften hemische Grundbegriffe I 1 Lipide und Zucker Lipide dienen als Energiequelle, zum Bau von Zellmembranen und als ormone Monosaccharide sind Aldehyde oder Ketone mit mindestens zwei ydroxylgruppen Asymmetrische -Atome, optische Aktivität und Fischer-Projektion Disaccharide entstehen aus zwei Monosacchariden Polysaccharide dienen als Zucker speicher oder Strukturelement Zucker sind Bausteine von DA, RA und ofaktoren Glycoproteine sind Proteine mit ligosaccharidketten Glycolipide sind Derivate des eramids Proteine Proteine bestehen aus Aminosäuren In Proteinen sind Aminosäuren über Peptidbindungen verknüpft Wechselwirkungen zwischen Amino säuren bestimmen die Raumstruktur des Proteins Proteine erfüllen Funktionen Strukturproteine Enzyme katalysieren biochemische Reaktionen Transportproteine transportieren Stoffe Lösliche Transportproteine Transportproteine in Membranen Die Glucosetransporter: eine Proteinfamilie, die nicht nur Glucose transportiert Proteinanalytik Proteine trennt man chromatographisch Die SDS-Gelelektrophorese trennt Proteine nach Größe auf Mit dem Edman-Abbau lassen sich Aminosäuresequenzen bestimmen Die Aminosäure zusammen set zung gibt Art und Menge der Aminosäuren eines P roteins an Proteinbestimmung Enzyme, ofaktoren und Kinetik Enzyme lassen eine Reaktion schneller laufen, beeinflussen aber nicht das Reaktionsgleichgewicht Es gibt sechs Enzymklassen Mechanismen und Regulation von Enzymen Viele Enzyme brauchen ofaktoren ATP ist die Energieeinheit des Stoffwechsels AD + /AD wird bei Redoxreaktionen gebraucht oenzym A aktiviert arbonsäuren S-Adenosylmethionin spendet bei vielen Methylierungen die Methylgruppen Tetrahydrofolat überträgt 1 -Einheiten ofaktoren übertragen auch Aminogruppen und Vitamine sind oft Vorstufen von ofaktoren oder ormonen Enzymkinetik Michaelis-Menten-Kinetik emmung der Enzymaktivität Allosterie reguliert effizient Stoffwechselwege ucleinsäuren Grundlagen Desoxyribonucleinsäure (DA) Das Erbgut verdoppelt sich durch DA-Replikation Replikation bei Prokaryoten Replikation bei Eukaryoten DA-Reparatur verringert Mutationsschäden DA-Marker kennzeichnen Individualität und Abstammung aplogruppen Ribonucleinsäuren (RA) Es gibt fünf RAs: tra, rra, mra, snra, mira Die DA-abhängige RA-Synthese heißt Transkription Die Transkription wird bei Eukaryoten über regulative Sequenzen gesteuert Bei Prokaryoten regulieren Promotor und benachbarte Sequenzen die Transkription Proteinbiosynthese (Translation) Der genetische ode ist degeneriert Aminosäuren werden spezifisch mit ihren tras verknüpft Translation bei Prokaryoten Die Initiation braucht Proteinfaktoren, fmet-tra, mra, GTP und das Ribosom Die Elongation benötigt Elongationsfaktoren, GTP und Aminoacyl-tRA Das Stopcodon löst die Termination aus Bei Eukaryoten verläuft die Translation ähnlich wie bei Prokaryoten Viele Bakterien und Pilze synthetisieren emmer der Transkription und Translation Die Spezifität der Antibiotika schützt nicht immer vor ebenwirkungen MicroRAs (mira) regulieren Gene Viren, Plasmide und Transposons Viren sind unabhängige genetische Elemente Retroviren sind RA-Viren epatitis B-Viren sind DA-Viren ucleosid analoga behindern die Virusvermehrung Plasmide: extrachromosomale DA-Ringe iii
6 4.6.3 Transposons sind DA-Abschnitte, die ihren rt im Genom wechseln können Telomere und Telomerasen schützen hromosomenenden Methoden der Molekularbiologie Restriktionsnucleasen schneiden DA an bestimmten Stellen Wie man ucleinsäuren aus Zellen isoliert Die Elektrophorese trennt ucleinsäuregemische auf DA-Sequenzieren: Produktion genetischer Information DA-Sequenzieren nach Maxam-Gilbert DA-Sequenzieren nach Sanger Pyrosequenzieren bringt Licht in die Sequenz ybridisierung weist in ucleinsäuren bestimmte Sequenzen nach Der Southern-Blot überträgt DA- Fragmente auf eine Membran Durch Klonieren kann man Kopien eines Gens herstellen Expressionsvektoren verwandeln Bakterien in Proteinfabrikle Auch in Eukaryotenzellen lassen sich fremde Gene einführen und exprimieren Gentherapie: Praktische Anwendung der Gentechnik, die praktisch noch nicht funktioniert Polymerase-Kettenreaktion (PR) Epigenetik: der Einfluss der Umwelt auf das Genom Epigenetik bringt verschiedene rganismen hervor Stoffwechsel Glycolyse und Gluconeogenese Der itratzyklus produziert Reduktionsäquivalente und Vorstufen für Biosynthesen Die Pyruvat-Dehydrogenase verknüpft die Glycolyse mit dem itratzyklus und wird reguliert Die oxidative Phosphorylierung liefert ATP Die Atmungskette überträgt Elektronen von Reduktionsäquivalenten auf Die xidation der Reduktionsäquivalent e ist mit der Phosphorylierung von ADP gekoppelt Die ATP-Synthase ist ein ano-motor, der Protonenbewegung in Drehbewegung u msetzt und ATP erzeugt Glycogen speichert Glucose Der Pentosephosphatweg liefert ADP und wandelt Monosaccharide ineinander um Lipidsynthese Typische Verbindungen des Lipidstoffwechsels sind Thioester und ADP Fettsäuren werden aus 2 -Einheiten synthetisiert Die Fettsäuresynthese wird über die Acetyl-oA-arboxylase reguliert Phospholipide entstehen bei der U msetzung von Diglyceriden mit DP- Verbindungen holesterol entsteht aus Acetyl-oA und Acetoacetyl-oA Lipidabbau Fettsäuren werden durch b-xidation abgebaut Aus Acetyl-oA können Ketonkörper e ntstehen holesterol wird zu Gallensäuren abgebaut Lipide werden von Lipoproteinen t ransportiert Purin- und Pyrimidinbasen Biosynthese der Purin- und Pyrimidinbasen Abbau der Purin- und Pyrimidinbasen Biosynthese der Aminosäuren Aminosäureabbau Für das äm müssen aus Succinyl-oA und Glycin Porphyrine synthetisiert werden Der arnstoffzyklus entsorgt Ammoniak Stoffwechselprozesse laufen in bestimmten Zellkompartimenten ab Apoptose: Die Zelle begeht Selbstmord Mit optischen Tests lässt sich die Konzentration von Metaboliten bestimmen ormone ormonrezeptoren und G-Proteine vermitteln das ormonsignal ins Zellinnere Der Blutglucosespiegel wird hormonell r eguliert Insulin entsteht aus Präproinsulin Diabetes mellitus tritt in zwei Formen auf Das hypothalamisch-hypophysäre System: eine ormonhierarchie AT ist eines der Produkte des PM-Gens Aus Vitamin D entsteht das ormon alcitriol Die ebennieren rinde produziert Steroidhormone Die chromaffinen Zellen des ebennierenmarks erzeugen Adrenalin Das Renin-Angiotensinsystem reguliert B lutdruck sowie Wasser- und a + -Retention Schilddrüsenhormone entstehen aus T yrosin Endorphine aktivieren pioidrezeptoren Molekulare Physiologie Das Immunsystem Die spezifische Immunabwehr Die humorale Immunität basiert auf antikörper sezernierenden Zellen Antikörper bestehen aus vier Polypeptidketten iv
7 Ein Mensch besitzt Millionen v erschiedener Antikörper T-Zell-vermittelte Immunität (= zelluläre Immunität) Es gibt zwei Klassen von M-Proteinen Wie für B-Zellen gilt auch für T-Zellen das Prinzip der klonalen Selektion Monoklonale Antikörper sind identische Moleküle Mit Antikörpern kann man Krankheitserreger nachweisen Reizleitung im ervensystem Physikalische Grundlagen Der ervenimpuls entsteht durch sich öffnende und schließende Ionenkanäle Synapsen übertragen ervenimpulse von Zelle zu Zelle eurotransmitter-rezeptoren sind oder steuern Ionenkanäle Die Acetylcholinesterase spaltet A cetylcholin in Acetat und holin Sehen basiert auf der durch Licht aus gelösten Konformationsänderung von Rhodopsin Muskel Die Muskelkontraktion kommt durch Wechselwirkung zwischen Actin und Myosin zustande Die Muskelkontraktion wird über die a 2+ -Konzentration im Sarkoplasma reguliert Muskeln brauchen ATP Verdauung Im Magen wird die ahrung ange säuert und von Proteasen verdaut Das Pankreas gibt Vorstufen von Verdauungsenzymen in den Dünndarm ab Der Dünndarm resorbiert die Spaltprodukte Der Dünndarm nimmt a 2+, Phosphat, Eisen und Kupfer auf Leber Die Leber baut Plasmaproteine ab Die Leber bildet Galle Die Leber verarbeitet den vom Alaninzyklus angelieferten Stickstoff der Muskelaminosäuren Die Leber entgiftet lipophile Fremdstoffe Die Leber führt Fructose der Glycolyse zu. Macht das dick? iere Die iere reguliert Wasser und Elektrolythaushalt Die Resorption von a 2+, Phosphat, a + und Wasser aus dem Primärharn wird von ormonen reguliert Blut Zusammensetzung von Plasma ämoglobin bindet Die 2 -Bindung wird durch p und G ewebs- 2 reguliert Die 2 -Affinität von ämoglobin hängt von 2,3-Bisphosphoglycerat ab Drei Puffersysteme halten den Blut-p konstant Die Blutgerinnung wird durch eine Kaskade enzymatischer Reaktionen ausgelöst Wie entsteht Krebs? Genetische Theorie der Krebs ent - stehung Stoffwechseltheorie der Tumorgenese (Warburg-ypothese) Tafeln Tafel A: Die Aminosäuren der Proteine Tafel S: Stoffwechsel-Übersicht Tafel I: Antikörperbildung durch B-Zellen Tafel P: Proteinanalytik mit Massenspektro - metrie Proteomics Tafel D: DA-Arrays Tafel R: RA-Interferenz und Antisense- ligonucleotide Tafel Z: Übersicht über die Zelle, ihre rga - nellen und deren wichtigste Funktionen am Beispiel einer Leberzelle Glossar Stichwortverzeichnis v
8 Der Aufbau von Biochemie-light Biochemie-light bringt neben möglichst kurzen Texten möglichst einfache Illustrationen. Das Glossar erläutert die von den Praktikumsleitern gern gefragten Begriffe und wappnet Sie gegen die beliebten Fragen der Art: Erklären Sie mir doch mal, was Sie unter xy verstehen. Im Glossar oder im Stichwortverzeichnis können Sie auch nachschlagen, wenn Ihnen beim Lesen ein unbekannter Begriff aufstößt. Die Kapitelüberschriften fassen meistens den Inhalt eines Kapitels als Lehr- und Merksatz zusammen. Das Kapitelverzeichnis ist also die Essenz der Essenz der Biochemie und sein Studium soll es Ihnen ermöglichen, zu einem Thema wenigstens irgendetwas sagen zu können. ichts wirkt so vernichtend in einer Prüfung wie das Schweigen der Lämmer. Texte in Kleinschrift halten wir für nicht absolut essentiell, aber nützlich. Bei der vielleicht zu ausführlich behandelten Kinetik müssen Sie sich nicht grämen, wenn Sie nicht alles verstehen auch manch ein Praktikumsleiter kann die Michaelis-Menten-Gleichung nicht herleiten. Überhaupt: icht gleich verzweifeln, wenn mal etwas unklar bleibt. Einfach weiterlesen und überschlafen. Das Verständnis kommt oft am nächsten Morgen oder am übernächsten. Bei den Farben gilt: Rot steht meistens für DA, aber auch für Blut, äm etc. Blau steht meistens für Protein oder Aminosäuren, oft auch für wässrige Lösungen. Grün steht meistens für RA, gelegentlich auch für Monosaccharide. Magenta steht meistens für die Fettsäurereste der Phospholipide und damit für Zellmembranen. Gelb steht für Urin, Disulfidbrücken, Lipide. Für die Zeichen gilt: Schmalpfeil steht für einen Reaktionsschritt Breitpfeil steht für mehrere Reaktionsschritte + bei einem Pfeil steht für Aktivierung bei einem Pfeil steht für emmung P steht für Phosphatgruppe oder steht für Polypeptidkette und die Kreise für einzelne Aminosäurereste vi
9 Abkürzungen AE AP AT ADP AMP ATP bp BPG BSE camp DP cgmp oa TP DA EDTA ELISA ER FAD G G GABA GLUT GTP b DL RE IRE ITAM K M LD LDL M mra mira mm M mtda MW angiotensin converting enzyme Acyl-arrier-Proteinabschnitt Adrenocorticotropes ormon Adenosindiphosphat Adenosinmonophosphat Adenosintriphosphat Basenpaare 2,3-Bisphosphoglycerat Bovine spongiforme Enzephalopathie 3,5-cyclo-Adenosinmonophosphat ytidindiphosphat 3,5-cyclo-Guanosinmonophosphat oenzym A ytidintriphosphat Desoxyribonucleinsäure Ethylendiamintetraessigsäure enzyme-linked immunosorbent assay endoplasmatisches Reticulum Flavin-Adenin-Dinucleotid freie Enthalpie Änderung der freien Enthalpie γ-amino-buttersäure Glucose-Transporter Guanosintriphosphat ämoglobin high density lipoprotein hormone response element iron response element immunoreceptor tyrosine-based activation motif Michaelis-Konstante Lactatdehydrogenase low density lipoprotein molar (Konzentrationseinheit Mol/l) messenger RA MicroRA millimolar (Konzentrationseinheit mmol/l) major histocompatibility complex mitochondriale DA Molekulargewicht vii
10 AD + AD PAGE PR PD PT R RA RS SDS SP SR STR T TF UDP UMP UTP V VLDL ZS icotinamid-adenin-dinucleotid (oxidiert) icotinamid-adenin-dinucleotid (reduziert) polyacrylamide gel electrophoreses polymerase chain reaction Pyruvat-Dehydrogenase Phenylisothiocyanat Gaskonstante Ribonucleinsäure reactive oxygen species Sodium-Dodecylsulfat single nucleotide polymorphism sarkoplasmatisches Reticulum short tandem repeat absolute Temperatur Tetrahydrofolat Uridindiphosphat Uridinmonophosphat Uridintriphosphat Maximalgeschwindigkeit very low density lipoprotein Zentralnervensystem viii
11 hemische Grundbegriffe Die Seiten I und II wiederholen die wichtigsten Begriffe der hemie. Führen Sie sich die zu Gemüte! Anderenfalls werden Ihnen die Seiten von Biochemie-light vorkommen wie Scheunentore und Sie sich wie der chse, der davorsteht und nicht hinein kann. Zudem: In der mündlichen Prüfung nicht zu wissen, was ein Ester ist, bringt das Blut auch des gutmütigsten Prüfers zum Kochen. Alkohole besitzen eine ydroxylgruppe ( ) Beispiel: Ethanol 2 3 an einem Alkylrest. Alkylrest? Das ist ein Kohlenwasserstoffrest der Formel n 2n+1. ydroxylgruppe Alkylrest mit n = 2 Säuren können Protonen ( + -Ionen) abgeben. Sie dissoziieren (zerfallen) in wässriger Lösung in Proton und Säureanion; starke Säuren vollständig, schwache nur teilweise. Biochemisch wichtig sind Kohlensäure ( 2 3 ), Phosphorsäure ( 3 P 4 ) und arbonsäuren, die eine arboxylgruppe ( ) an einem Alkylrest tragen. Beispiel: Essigsäure 3 3 arboxylgruppe Alkylrest andere Darstellung Dissoziation: Ester entstehen, wenn eine Säure und ein Alkohol unter Wasserabspaltung eine chemische Verbindung eingehen. Säure Alkohol Ester Säureanhydride entstehen aus zwei Säuremolekülen unter Wasserabspaltung. Dabei müssen die Säuren nicht gleich sein. Eine arbonsäure kann auch mit Phosphorsäure ein gemischtes Säureanhydrid bilden. Säure Säure Säureanhydrid Ketone und Aldehyde enthalten eine arbonylgruppe ( ). Ketone besitzen ein sekundäres -Atom, Aldehyde ein primäres. Primär bedeutet mit einem weiteren -Atom verknüpft, sekundär mit zwei weiteren -Atomen verknüpft. Es gibt Verbindungen, die eine arbonyl- und eine arboxylgruppe enthalten, zum Beispiel die für die Biochemie wichtigen α-ketosäuren. Formel: Alkylrest 1 Alkylrest 2 Keton Beispiel: 3 3 Alkylrest 3 Aldehyd Acetaldehyd Alkylrest 3 α-ketosäure Brenztraubensäure Anion: Pyruvat Aceton Primäre Amine enthalten eine Aminogruppe ( 2 ) an einem Alkylrest. Amine sind basische Verbindungen, d. h. sie können Protonen binden. Die Aminogruppe ist wie die ydroxyl- oder arbonylgruppe eine funktionelle, d. h. eine reaktionsfähige Gruppe. Beispiel: Ethylamin Aminogruppe Alkylrest Protonierung: Bei der xidation werden einem Atom/Molekül Elektronen entzogen. Dies geschieht entweder durch Umsetzung mit Sauerstoff oder durch Entzug von Wasserstoff (Dehydrierung). Im Gegensatz dazu werden bei der Reduktion Elektronen bzw. Wasserstoffatome zugeführt (ydrierung). Im Beispiel rechts wird jeweils das rote -Atom oxidiert bzw. reduziert. xidation Reduktion Alkohol Aldehyd Säure I
12 Ein Mol ist eine Mengenangabe: Ein Mol entspricht dem Molekulargewicht (MW) einer Substanz in Gramm. Ein Mol enthält immer die gleiche Anzahl von Teilchen (Molekülen oder Atomen), nämlich 6, (Loschmidt sche Zahl). 1 Mol Glucose = 180 Gramm Glucose = 6, Moleküle 1 Mol Ethanol = 46 Gramm Ethanol = 6, Moleküle Die Molarität ist eine Konzentrationsangabe, bezeichnet also eine Stoffmenge pro Volumen. Eine 1 molare Lösung enthält ein Mol einer Substanz pro Liter (1 Mol = 1 M). Eine millimolare Lösung enthält ein tausendstel Mol pro Liter (1 mmol/l = 1 mm). Die Protonenkonzentration einer Lösung bestimmt ihren Säuregrad. Bei hoher Protonenkonzentration ist die Lösung sauer, bei niedriger alkalisch. Das Maß für die Säurestärke ist der p-wert. Der p- Wert ist der negative dekadische Logarithmus der + -Ionen-Konzentration. Eine Lösung mit einer + -Ionen-Konzentration von 10 2 Mol/l hat also einen p-wert von 2 und ist sauer. Reines Wasser hat einen p-wert von 7 und ist neutral. Säuren erniedrigen den p-wert, Basen erhöhen ihn. Puffer halten den p-wert einer Lösung konstant. Ein Puffer ist eine Lösung einer schwachen Säure und ihres Salzes (z. B. 2 3 und a 3, allgemein A und MeA). Die schwache Säure ist kaum dissoziiert, ihr Salz zerfällt jedoch vollständig in Metallion und Anion. Gibt man Protonen zu der Lösung, werden sie von den Anionen abgefangen. Es bildet sich die schwache Säure. Gibt man - Ionen zu, dann reagieren diese mit der Säure zu Wasser und dem Anion. Der p-wert der Lösung ändert sich in beiden Fällen kaum, sie puffert. Für eine chemische Reaktion im Gleichgewicht gilt das Massenwirkungsgesetz. Es gibt das Ver hältnis zwischen den molaren Konzentrationen der Reaktionspartner an (hier: [A], [B], []). Die Gleichgewichtskonstante K hängt von der Triebkraft der Reaktion ab, der freien Energie. Jede Reaktion hat also ihr eigenes K. Das Massenwirkungsgesetz gilt auch für die Dissoziation von Wasser in + und. In einer wässrigen Lösung ist die Konzentration von Wasser [ 2 ] in etwa konstant, nämlich 55,5 Mol/l (1 Mol 2 18 g). Daher ist auch das Produkt von [ + ] und [ ] konstant, es beträgt In reinem Wasser ist die Konzentration der Protonen gleich der Konzentration der ydroxylionen, nämlich Damit hat die Lösung einen p-wert von 7. Gibt man nun eine Säure dazu, so erhöht sich [ + ], denn die Säure gibt Protonen ab. ach dem Massenwirkungsgesetz muss das Produkt aus [ + ] und [ ] konstant bleiben, deshalb nimmt [ ] in entsprechendem Verhältnis ab. Eine 1 molare Glucoselösung enthält 180 Gramm Glucose pro Liter oder 0,18 Gramm Glucose pro Milliliter p log [ + ] p 1 p 7 p 14 sauer neutral basisch Pufferlösung der schwachen Säure A und ihres a + -Salzes in 2 : A a + A- A- a + A- Reaktion - a A + + A A- a + A- A A a + A- [ ] [ ] [ ] a + A Massenwirkungsgesetz [ ] [ ] [ ] [ ] [ ] [ ] (eckige Klammern bedeuten Konzentration in Mol/l) Aus dem Massenwirkungsgesetz ergibt sich die enderson-asselbalch-gleichung: [ + ] [A - ] [A - ] K p pk S S + log [A] [A] Massenwirkungsgesetz enderson-asselbalch- Gleichung Mit der enderson-asselbalch-gleichung lässt sich der p-wert berechnen, wenn das Verhältnis von [A ]/[A] und der pk S bekannt sind. Beispiel: Wie hoch ist der p-wert einer Lösung von 0,1 M Essigsäure und 1 M a-acetat? In einem Tabellenwerk finden Sie für Essigsäure und Acetat, dass pks = 4,8. Für den p gilt dann: p = 4,8 + log (1M/0,1M) = 4,8 + log 10 = 5,8 II
13 1 Lipide und Zucker 1.1 Lipide dienen als Energiequelle, zum Bau von Zellmembranen und als ormone Lipide bestehen zum großen Teil aus hydrophoben (wasserscheuen) Resten. Daher sind die meisten Lipide wasserunlöslich und membrangängig. Die wichtigsten Lipide sind die Triacylglyceride (Triglyceride), Phospholipide und holesterolderivate. Triglyceride sind Ester des Glycerins mit Fettsäuren Vorkommen: Depotfette im Unterhautgewebe. Zweck: Die Fettsäuren des Depotfetts bilden die Energiereserve des Körpers. Fettgewebe ist das größte Speicherorgan des rganismus: Triglyceride sind wasserunlöslich, deshalb osmotisch ungefährlich und können in größeren Mengen als Monomere gelagert werden. Die wasserlösliche Glucose dagegen, die ebenfalls der Energieerzeugung dient, kann nicht als Monomer gelagert werden. In Zellen, die viel Glucose enthalten, würde Wasser durch die Zellmembran einströmen, um den Konzentrationsunterschied auszugleichen. Die Zellen würden platzen. Phospholipide sind Ester des Glycerins mit zwei Fettsäuren und einem Phosphorsäureester Vorkommen: Sie bilden die Membranen von Zellen und Zellorganellen. Aufbau: Meist handelt es sich um Ester der Phosphorsäure mit Aminoalkoholen wie holin, Ethanolamin oder siehe rechts der Aminosäure Serin. Der Phosphorsäureester und damit auch das Phospholipid tragen Ladungen. Zweck: In wässriger Lösung bilden die Phospholipide Doppelschichten. Der hydrophile (wasserliebende) Teil des Phospholipids, der Phosphorsäureester, zeigt dabei zur wässrigen Umgebung. Die hydrophoben Fettsäuren sind ins Membraninnere gerichtet. Sie bilden eine Barriere für Ionen und hydrophile Moleküle wie Glucose. Die Doppelschicht kann Proteine an- und einlagern. Proteine, die die Doppelschicht durchspannen, heißen integrale Membranproteine. 2 2 Glycerin Fettsäure (meist Palmitin- oder Stearinsäure) Triglycerid Phospholipid (Phosphatidylserin) 2 P 3 2 Phosphorsäureester Ausschnitt aus der Zellmembran hydrophiler Kopf = Phosphorsäureester Sphingophospholipide Vorkommen: Gehirn und ervengewebe. Aufbau: Sphingophospholipide bestehen aus dem Aminoalkohol Sphingosin, einer Fettsäure, einem Phosphatrest (gelb) und (meistens) dem Aminoalkohol holin (blau). Die Fettsäure ist nicht als Ester, sondern über eine Amidbindung (grün) mit dem Sphingomyelin ver knüpft. hydrophobe Fettsäurereste integrales Membranprotein 2 Sphingosin P Sphingomyelin
14 holesterolderivate Vorkommen: Zellmembran, ebennierenrinde, Leber. Zweck: holesterol stabilisiert Zellmembranen. holesterol ist zudem Ausgangsmaterial vieler Synthesen: Aus holesterol werden Steroidhormone (Sexualhormone, Glucocorticoide, Mineralocorticoide) und Gallensalze gebildet. Letztere dienen der Fettemulgierung im Darm. Auch Vitamin D entsteht aus holesterol holesterol (räumliche Formel) wird in Zellmembranen eingelagert Das Sexualhormon Testosteron Das Sexualhormon Estradiol 2 = Das Glucocorticoid ortisol wirkt auf den Glucosestoffwechsel Monosaccharide sind Aldehyde oder Ketone mit mindestens zwei ydroxylgruppen Bei Monosacchariden (Einfachzuckern) trägt in der Regel jedes -Atom eine ydroxylgruppe, bis auf eines, das die Aldehyd- oder Ketogruppe (rot) trägt. Zucker mit Aldehydgruppe heißen Aldosen, mit Keto gruppe Ketosen. exosen besitzen sechs, Pentosen fünf -Atome. Pentosen und exosen können in einer offenkettigen und in einer ringförmigen Form existieren. Weil eine Aldehydgruppe leicht andere Verbindungen reduziert und dabei selber zur Säure oxidiert wird, nennt man die Aldehydgruppe das reduzierende Ende eines Zuckers. Die wichtigsten Monosaccharide sind die Pentose Ribose und die exosen Glucose, Fructose, Mannose und Galactose. 1.3 Asymmetrische -Atome, optische Aktivität und Fischer-Projektion Ein -Atom hat vier Valenzen, kann also bis zu vier Substituenten binden. Die vier Substituenten sind räumlich um das -Atom verteilt. Sie liegen nicht in der Papierebene, sondern in den Ecken einer Dreieckspyramide (Tetraeder). Die Substituenten können gleich sein oder verschieden. Ein -Atom mit vier verschiedenen Substituenten ist asymmetrisch. offenkettige Form Ribose (Aldose) Glucose (Aldose) Ringform (aworth-darstellung) Fructose (Ketose) Das zweite -Atom von Glucose ist asymmetrisch: es besitzt vier verschiedene Substituenten.
15 Alle Monosaccharide mit Ausnahme von Dihydroxyaceton besitzen ein oder mehrere asymme trische -Atome, die Aldohexosen z. B. vier. Asymmetrische -Atome können ihre Substituenten in zwei spiegelbildlichen Anordnungen (Konformationen) tragen. Diese Konformationen lassen sich wie linke und rechte and nicht durch Drehen zur Deckung bringen. Dies nennt man hiralität (= ändigkeit). Die spiegelbildlichen Molekülpaare heißen Enantiomere. Sie sind Stereoisomere. Zucker mit einem hiralitätszentrum, d. h. einem asymmetrischen -Atom, treten also in zwei verschiedenen räumlichen Konfigurationen als Stereoisomere auf. Zucker mit n asymmetrischen -Atomen kommen in 2 n Stereoisomeren vor. Stereoisomere sind optisch aktiv: sie drehen die Schwingungsebene von polarisiertem Licht entweder im Uhrzeigersinn (rechtsdrehend) oder dagegen (linksdrehend). Das Ausmaß der Drehung hängt von der Konzentration des optisch aktiven Stoffes ab. Der Effekt wird in der Medizintechnik zur Bestimmung von Zuckern in Körperflüssigkeiten benutzt. Der einfachste Zucker mit asymmetrischem -Atom ist Glycerinaldehyd. Er bildet zwei stereo isomere Formen: D- und L-Konfigura tion. Glycerinaldehyd wurde als Bezugssubstanz für die Konfiguration optisch aktiver Verbindungen gewählt. Dreht man den Tetraeder so, dass die Aldehydgruppe nach oben und die 2 -Gruppe nach hinten zeigt, dann liegen und jeweils auf den Enden der vorderen Kante. Ist die rechte Ecke mit besetzt, so hat man die D-Form, sitzt links, die L-Form. Die räumliche Darstellung als Tetraedermodell ist um ständ lich, sie wird deshalb vereinfacht zur Fischer- Projektion. Dafür wird die Kohlenwasserstoffkette be ginnend mit dem -Atom mit der höchsten xida tionsstufe untereinander geschrieben, die Substituenten jeweils nach links bzw. rechts. Vereinbarungsgemäß liegen horizontale Substituenten vor der Papier ebene, vertikale dahinter. Vom D- bzw. L-Glycerinaldehyd leiten sich die D- und L-Zucker ab. Bei ihnen zeigt das von der arbonylgruppe am weitesten entfernte asymmetrische - Atom die gleiche Konfiguration wie D- bzw. L-Glycerinaldehyd. Damit man bei Verbindungen mit mehreren hiralitätszentren die absolute Konfiguration an jedem ein zelnen asymmetrischen -Atom festlegen kann, wurde nach den erren ahn, Ingold, Prelog das IP-System entwickelt. Je höher die rdnungszahl des Atoms, mit dem der Substituent an das -Atom gebunden ist, desto höher seine Priorität, also > > >. Doppelbindungen zählen doppelt. Sind die Erstatome gleich, so wird auch noch das Zweitatom zur Bewertung mit herangezogen, also > 2 > 3. In der Tetraederdarstellung wird der Substituent mit der niedrigsten Priorität nach hinten gestellt. Die restlichen Substituenten können nun Spiegel Asymmetrisches -Atom (schwarz): spiegelbildliche Anordnung der Substituenten. Sie sitzen in den vier Ecken eines Tetraeders und lassen sich durch Drehen nicht zur Deckung bringen. Schwingungsebene parallel zum Blatt Räumliche Darstellung: 2 Fischer-Projektion: 2 2 D-Glycerinaldehyd (-Gruppe rechts) D-Glucose R-Glycerinaldehyd Zuckerlösung Schwingungsebene im Uhrzeigersinn gedreht 2 L-Glycerinaldehyd (-Gruppe links) L-Glucose 2 2 S-Glycerinaldehyd 3
16 entweder mit fallender Priorität im Uhrzeigersinn (R-Form) oder dagegen (S-Form) angeordnet sein. Die meisten biochemisch wichtigen Verbindungen sind chiral, so die Aminosäuren und viele Zucker. Der rganismus verwendet jedoch nur ein Enantiomer, z. B. D-Glucose oder L-Aminosäuren. Als Epimere bezeichnet man Zucker, die sich nur in der Konfiguration an einem asymmetrischen -Atom unterscheiden. Epimer sind z. B. D-Glucose und D-Mannose. Sie unterscheiden sich am asymmetrischen 2 (rot). Wie erwähnt, können Pentosen und ex osen in offenkettiger und ringförmiger Form existieren. Dabei reagiert die Aldehyd- bzw. Ketogruppe der offenkettigen Form mit einer ydroxylgruppe zum albacetal bzw. albketal. Durch Ringbildung entsteht ein neues asymmetrisches Zentrum am ehemaligen arbonyl-kohlenstoff ( 1 ). In Folge treten zwei neue Isomere des Zuckers auf, z. B. α-d-glucose und β-d-glucose. Diese Isomere heißen Anomere, ihre Umwandlung ineinander Mutarotation. 1.4 Disaccharide entstehen aus zwei Monosacchariden Der ehemalige arbonyl-kohlenstoff der ringförmigen Monosaccharide ist besonders re aktiv. Er kann mit alkoholischen Gruppen anderer Mono saccharide unter Wasserabspal tung reagieren. Es entstehen -glyco sidische Bindungen und Di-, Tri-, ligo- und Polysaccharide. Disaccharide sind Maltose (zweimal Glucos e), Saccharose (= Rohrzucker; Fructose und Glucose) und Lactose (= Milchzucker; Galactose und Fructose). Frauenmilch enthält ca. 7,5% Lactose. Sie wird im Darm in ihre Bausteine gespalten und die Galactose in Glucose umgewandelt. Bei der Galactosämie, einer erblichen Stoffwechselkrankheit, wird Galactose nur teilweise oder gar nicht umgesetzt. Also häuft sie sich im Körper an. Die Folgen sind Ikterus (Gelbsucht) und Trübung der Augenlinse. ligosaccharide bestehen aus drei oder mehr Monosacchariden, sie gehen nahtlos in die Polysaccharide über. 1.5 Polysaccharide dienen als Zucker speicher oder Strukturelement D oder L bzw. R oder S sagt nichts über die Drehrichtung aus! Es gibt D-Enantiomere, die polarisiertes Licht nach rechts drehen, und solche, die es nach links drehen! Das Gleiche gilt für Verbindungen mit L- bzw. R- oder S-Konfiguration D-Glucose D-Glucose a-d-glucose 1 β-d-galactose Disaccharid: Lactose D-Mannose α-d-glucose Ringbildung b-d-glucose Verknüpfung von Monosacchariden Das Polysaccharid Glycogen ist die Speicherform der Glucose. Die Leber ist der auptspeicher. Sie enthält zwischen 1% (unger) und 10% ihres Gewichtes an Glycogen. In geringerem Ausmaß wird Glycogen auch im Muskel gespeichert. Glycogen Leber
17 Glycogen besteht aus Ketten von α-1,4-glycosidisch verknüpften Glucose einheiten; α-1,6-bindungen füh ren Verzweigungen ein. Das Glycogen-Molekül ähnelt einem Strauch mit einem reduzierenden Anfang (die arbonylgrupp e) und vielen nicht reduzierenden Enden. Auch pflanzliche Stärke ist ein Glucosepolymer. Sie besteht aus einem linearen α-1,4-polymer, der Amylose, und dem verzweigten Amylopektin. Auf Glucosereste kommt eine (α-1,6) Verzweigung. Amylopektin ähnelt damit dem Glycogen. Die beiden Polymere unterscheiden sich aber im Verzweigungsgrad. Beim Glycogen kommt auf alle 12 Reste eine Verzweigung. Die für den Menschen unverdauliche ellulose ist ein Polysaccharid aus β-1,4- glycosidisch verbundenen Glucoseresten. Saure Mucopolysaccharide dienen als Füll- oder Schmiermittel. Diese gallertartigen linearen Polysaccharide bestehen meist aus zwei alternierenden Monosaccharideinheiten. Mindestens eine davon trägt eine saure Gruppe (z. B. arboxyloder Sulfonylrest). 2 2 Mucopolysaccharid Bestandteile yaluronsäure hondroitin 1 1,6 hondroitin-4-sulfat Dermatansulfat Glycogen (Ausschnitt) ,4 1,4 Glucuronsäure, -Acetylglucosamin Glucuronsäure, -Acetylgalactosamin Glucuronsäure, -Acetylgalactosamin-4-sulfat Iduronsäure, -Acetylgalactosamin-4-sulfat eparin Glucosamin-6-sulfat, Iduronsäure, Glucuronsäure-2-sulfat Keratansulfat Galactose, Galactose-6-sulfat Vorkommen Bei Aminozuckern ist eine ydroxylgruppe durch eine Aminogruppe ersetzt worden. Aminozucker sind Glucosamin und Galactosamin bzw. ihre acetylierten Derivate -Acetylglucosamin und -Acetylgalactosamin. Synovialflüssigkeit (Gelenke) ornea Knorpel aut Lunge ornea Glycogen 1.6 Zucker sind Bausteine von DA, RA und ofaktoren Aminogruppen ( 2 ) kann man mit Zuckern -glycosidisch verknüpfen (rot unterlegt). Auch hier reagiert das reaktive 1 des Monosaccharids. Purin- oder Pyrimidinbasen (s. 4.1) verbinden sich so mit Ribose oder Desoxyribose zu ucleosiden. ucleoside sind Bestandteil der DA, RA und enzymatischer ofaktoren wie AD, ATP, oenzym A (s. 3.4). Mit Phosphorsäure bilden die ydroxylgruppen der Zucker unter Wasserabspaltung Phosphorsäureester. Diese dienen im Stoffwechsel als energiereiche Zwischenstufen. Purinbase: Adenin 2 2 D-Ribose -glycosidische Verknüpfung Adenosin 2 P 2 P = P Glucosamin 2 Phosphorsäureester 2 und Aminozucker Glucose-6-phosphat 3 - R - = R -Acetyl- Glucosamin Acetylneuraminsäure = Sialinsäure 5
18 1.7 Glycoproteine sind Proteine mit ligosaccharidketten Die meist extrazellulären Proteine enthalten ligosaccharide, so Fibrinogen, Immunglobuline, thyroxinbindendes Protein. Die ligosaccharide sind entweder -glycosidisch an Serin- oder -glycosidisch an Asparaginreste gekoppelt. Serin und Asparagin sind Aminosäuren (Tafel A). Die ligosaccharide der Glycoproteine bestehen aus selteneren Monosacchariden (z. B. β-l-fucose), Aminozuckern oder Zuckersäuren, die arboxyl- oder Sulfonylreste tragen. Endständiger Baustein ist oft die negativ geladene Sialinsäure (= -Acetyl-euraminsäure). 2 = 3 o -glycosidisch gebundener ligosaccharidrest Glycoprotein 2 = 3 2 = Asparagin andere Aminosäuren Proteinteil 1.8 Glycolipide sind Derivate des eramids eramid besteht aus einer Fettsäure und Sphingosin (gelb). Letzteres trägt zwei ydroxylgruppen, eine davon kann Zucker binden. Bei den erebrosiden ist das eramid am Sphingosin mit Glucose oder Galactose verknüpft. Bei Gangliosiden hängen längere Zuckerketten mit Sialinsäureresten am Sphingosin des eramids. In der grauen Substanz des Gehirns machen Ganglioside 6% der Lipide aus. Bei der Erbkrankheit Tay-Sachs fehlt das Enzym b--acetylhexosaminidase. Daher können terminale, d. h. am Ende der Zuckerkette des Gangliosids sitzende -Acetylgalacto saminreste nicht entfernt werden. Dies verhindert den sukzessiven Abbau der Zuckerkette und damit der Ganglioside. Die Folge: Ganglioside reichern sich in den Lysosomen der ervenzellen an. Die Zellen blähen sich auf und sterben ab (ekrose s. 5.15). Gangliosid Kette von exosen eramidrest eramid; gelb unterlegt: Sphingosin terminaler -Acetylgalactosaminrest b--acetylhexosaminidase fehlende b--acetylhexosaminidase Ganglioside reichern sich an Tay-Sachs-Krankheit 2 Anknüpfpunkt für Zuckerreste -Acetylgalactosamin weiterer sukzessiver Abbau von exoseresten Glycolipide sitzen in der Außenseite der Plasmamembran; Plasmamembranen sind also bezüglich ihrer Lipide unsymmetrisch aufgebaut. Glycolipide lagern sich in die äußere Schicht der Zellmembran ein 6 Wie die Glycoproteine, so spielen auch die Glycolipide eine Rolle bei der Gewebs-, rgan- und Blutgruppenspezifität. Auch an der Zell-Zellerkennung sind Glycolipide beteiligt. Krebszellen präsentieren auf ihrer berfläche charakteristische, von normalen Zellen abweichende Glycolipide. Zellinneres
19 2 Proteine 2.1 Proteine bestehen aus Aminosäuren Aminosäuren besitzen an ihrem α--atom einen Amino- (grün) und einen arboxylrest (rot). Außerdem trägt das α--atom ein Wasserstoffatom und einen Rest R. In diesem Rest R, der Seitenkette, unterscheiden sich die Aminosäuren voneinander. Eine Übersicht über die 20 in Proteinen vorkommenden Aminosäuren finden Sie auf Tafel A. allgemeiner Aufbau der Aminosäuren 3 + R α--atom Beispiel: Die Aminosäure Alanin Das α--atom einer Aminosäure trägt vier verschiedene Substituenten (Ausnahme: Glycin). Das α--atom ist damit ein chirales Zentrum (oder asymmetrisch (s. 1. 3)). Es gibt also zwei spiegelbildliche Isomere: die L- und die D- Aminosäuren. Diese Isomere nennt man Enantiomere. In Proteinen kommen nur die L-Aminosäuren vor. 3 + R L-Aminosäure R + 3 D-Aminosäure Aminosäuren besitzen mindestens zwei ionisierbare Gruppen, die Aminogruppe (rot) und die arboxylgruppe (grün). Aminosäuren sind also Zwitterionen. Sie können, abhängig vom p-wert der Umgebung, eine positive oder eine negative Ladung annehmen. Manche Aminosäuren wie Glutamat oder Lysin besitzen sogar drei ionisierbare Gruppen R - + R - + Ladung von Alanin in Abhängigkeit vom p p Titrationskurve von Alanin Zugegebene Menge an -Ionen 3 + R In Proteinen sind Aminosäuren über Peptidbindungen verknüpft Durch Wasserabspaltung zwischen der arboxyl- und der Aminogruppe zweier Aminosäuren entsteht die Peptidbindung (= Amidbindung). Peptide und Proteine besitzen einen Aminoterminus (grün) und einen arboxyterminus (rot). Kurz: - bzw. -Terminus. Werden zwei Aminosäuren miteinander verknüpft, bildet sich ein Dipeptid, bei dreien ein Tripeptid etc. Ab 50 Aminosäuren spricht man von Proteinen (= Polypeptide). Die Eigenschaften der Polypeptide werden von den Eigenschaften der Aminosäurereste bestimmt. Die am Aufbau der Proteine beteiligten Aminosäuren (Tafel A) nennt man proteinogen. Die meisten kann der Mensch selber synthetisieren (s. 5.10), einige müssen mit der ahrung aufgenommen werden. Dies sind die essenziellen Aminosäuren R1 R1 R2 2 R R 1 R 2 R 3 R 4 R 5 R 6 exapeptid essenzielle Aminosäuren: Valin (Val), Leucin (Leu), Isoleucin (Ile), Methionin (Met), Threonin (Thr), Lysin (Lys), istidin (is), Phenylalanin (Phe), Tyrosin (Tyr) 7
20 Auch ystein ist eine Aminosäure. Sie enthält eine S- Gruppe. Zwischen den ysteinresten einer Polypeptidkett e können daher Disulfidbrücken geknüpft werden. Diese können sich sowohl intra- (innerhalb einer Peptidkette) als auch intermolekular (zwischen zwei Peptidketten) bilden. Intramolekulare Disulfidbrücken stabilisieren das Protein. Sie können reduktiv oder oxidativ gespalten werden. Dabei geht meist die Aktivität des Proteins/Peptids verloren. Manche Aminosäuren besitzen positiv oder negativ geladene Reste (Glu:, Lys: 3 +). Deshalb tragen die meisten Proteine Ladungen. Die ettoladung eines Proteins ist die Summe der Ladungen der Aminosäureseitenketten und von - und -Terminus. Sie hängt vom p-wert der umgebenden Lösung ab (s. 2.1). at ein Protein beim physiologischen p von 7,38 eine positive ettoladung, nennt man es basisch, hat es eine negative ettoladung, heißt es sauer. Der isoelektrische Punkt eines Proteins ist der p-wert, bei dem seine ettoladung gleich 0 ist. S intramolekulare Disulfidbrücke im Peptidhormon Vasopressin ys-tyr-phe-gln-asn-ys-pro-arg-gly- 2 S Proteine tragen Ladungen; hier: saures Protein, ettoladung = Wechselwirkungen zwischen Amino säuren bestimmen die Raumstruktur des Proteins Die räumliche Struktur eines Proteins, seine Konformation, bildet die Grundlage seiner Funktion. Sie wird bestimmt von den räumlichen Eigenheiten der Peptidbindung, der Primärstruktur (s. u.) und der Umgebung (Lösungsmittel, p). Unter Primärstruktur versteht man die Reihenfolge der Aminosäuren in der Polypeptidkette, ihre Sequenz. Man schreibt die Sequenz von der -terminalen Aminosäure (links) zur -terminalen Aminosäure (rechts). Die Peptidkette ist kein regelloser Knäuel, sondern faltet sich zu einer charakteristischen räumlichen Anordnung. Diese Faltung wird durch Wasserstoffbrücken stabilisiert. Bei der Wasserstoffbrücke teilen sich zwei Atome, ein - Donor und ein -Akzeptor, ein -Atom. Das -Atom bildet zu beiden eine Bindung aus. -Donor kann der Stickstoff einer Amino- oder der Sauerstoff einer ydroxylgruppe sein. -Akzeptoren sind oft arbonyl-sauerstoffatome. Die Bindung ist am stärksten, wenn Donor, -Atom und Akzeptor auf einer Linie liegen. Eine Wasserstoffbrücke ist also gerichtet. Ihre Bindungsenergie liegt bei 40 kj/mol und beträgt somit etwa 1/10 einer kovalenten Bindung. rote Pfeile: große Rotationsfreiheit R 1 R 2 Die vier Atome der Peptidbindung liegen in einer Ebene (blau), sie können nicht um die --Bindung rotieren Zwischen arbonyl-sauerstoff und Stickstoff der Aminogruppe bildet sich eine Wasserstoffbrücke: Akzeptor Donor Die Sekundärstruktur beschreibt die räumliche Anordnung nahe benachbarter Aminosäurereste. Sie ordnen sich bevorzugt als β-faltblatt oder als α-elix. Faltblatt und elix werden durch Wasserstoffbrücken stabilisiert. Beim β-faltblatt bilden sich Wasserstoffbrücken zwischen benachbarten Ketten. Die Atome der Peptidbindung liegen in den Ebenen des Faltblatts, die Reste ragen an den Knickstellen nach oben oder unten heraus. Man unterscheidet antiparalleles Faltblatt (eine der benachbarten Ketten verläuft vom - zum -Terminus, die andere umgekehrt) und paralleles Faltblatt (beide -Terminus -Terminus R β-faltblatt (antiparallele Anordnung) R R R R R -Terminus -Terminus 8
COOH. Die Aminosäuren tragen laborübliche Abkürzungen, so stehen z. B. Gly für Glycin oder Phe für Phenylalanin.
 Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Aminosäuren - Proteine
 Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Foliensatz; Arbeitsblatt; Internet. Je nach chemischem Wissen können die Proteine noch detaillierter besprochen werden.
 03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Organische Chemie I Chemie am 16.11.2012. Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2
 Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Chemie Zusammenfassung KA 2
 Chemie Zusammenfassung KA 2 Wärmemenge Q bei einer Reaktion Chemische Reaktionen haben eine Gemeinsamkeit: Bei der Reaktion wird entweder Energie/Wärme frei (exotherm). Oder es wird Wärme/Energie aufgenommen
Chemie Zusammenfassung KA 2 Wärmemenge Q bei einer Reaktion Chemische Reaktionen haben eine Gemeinsamkeit: Bei der Reaktion wird entweder Energie/Wärme frei (exotherm). Oder es wird Wärme/Energie aufgenommen
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6
 Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
c C 2 K = c A 2 c B 2mol /l 2 0,5mol /l 2 4 mol /l K =4l /mol
 Berechnungen zum Massenwirkungsgesetz 1/13 Jakob 2010 Fall 1a: Gegeben: Gleichgewichtskonzentrationen aller Stoffe; Gesucht: Gleichgewichtskonstante Die Reaktion 2A + B 2C befindet sich im Gleichgewicht.
Berechnungen zum Massenwirkungsgesetz 1/13 Jakob 2010 Fall 1a: Gegeben: Gleichgewichtskonzentrationen aller Stoffe; Gesucht: Gleichgewichtskonstante Die Reaktion 2A + B 2C befindet sich im Gleichgewicht.
Auswahlverfahren Medizin Prüfungsgebiet Chemie. 6.Termin Organische Chemie Naturstoffe
 Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Elektrolyte. (aus: Goldenberg, SOL)
 Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
b) Synthese - der Nucleoside nach Vorbrüggen (am Beispiel eines RNA-Bausteins)
 b) Synthese - der ucleoside nach Vorbrüggen (am Beispiel eines RA-Bausteins) Ac TMSTf Me 3 Si - Tf Ac Ac Ac Ac achbargruppeneffekt Ac - Tf TMS TMSCl TMS- freies Elektronenpaar am Stickstoffatom jetzt nucleophil
b) Synthese - der ucleoside nach Vorbrüggen (am Beispiel eines RA-Bausteins) Ac TMSTf Me 3 Si - Tf Ac Ac Ac Ac achbargruppeneffekt Ac - Tf TMS TMSCl TMS- freies Elektronenpaar am Stickstoffatom jetzt nucleophil
Material zur Vorbereitung der Prüfung im Fach Chemie
 Material zur Vorbereitung der Prüfung im Fach Chemie 1 Empfohlene Literatur Duden Basiswissen Schule: Abitur Chemie Schulbücher für die Sekundarstufe II: - Chemie im Kontext, CVK Verlag - Elemente Chemie
Material zur Vorbereitung der Prüfung im Fach Chemie 1 Empfohlene Literatur Duden Basiswissen Schule: Abitur Chemie Schulbücher für die Sekundarstufe II: - Chemie im Kontext, CVK Verlag - Elemente Chemie
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht
 8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
1 Mathematische Grundlagen
 Mathematische Grundlagen - 1-1 Mathematische Grundlagen Der Begriff der Menge ist einer der grundlegenden Begriffe in der Mathematik. Mengen dienen dazu, Dinge oder Objekte zu einer Einheit zusammenzufassen.
Mathematische Grundlagen - 1-1 Mathematische Grundlagen Der Begriff der Menge ist einer der grundlegenden Begriffe in der Mathematik. Mengen dienen dazu, Dinge oder Objekte zu einer Einheit zusammenzufassen.
Primzahlen und RSA-Verschlüsselung
 Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
Primzahlen und RSA-Verschlüsselung Michael Fütterer und Jonathan Zachhuber 1 Einiges zu Primzahlen Ein paar Definitionen: Wir bezeichnen mit Z die Menge der positiven und negativen ganzen Zahlen, also
Wird vom Korrektor ausgefüllt: Aufgabe 1 2 3 4 5 6 7 8 9 10 11 12 Punkte
 Klausur zur Vorlesung Grundlagen der Chemie für Mediziner und Biologen & Chemie-Praktikum für Molekulare Medizin und Biologie Gehalten im Wintersemester 2008/2009 Bitte diese 3 Felder ausfüllem: Name Matrikelnummer
Klausur zur Vorlesung Grundlagen der Chemie für Mediziner und Biologen & Chemie-Praktikum für Molekulare Medizin und Biologie Gehalten im Wintersemester 2008/2009 Bitte diese 3 Felder ausfüllem: Name Matrikelnummer
Lösungsblatt zu Aufbau von Aminosäuren
 Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
ONLINE-AKADEMIE. "Diplomierter NLP Anwender für Schule und Unterricht" Ziele
 ONLINE-AKADEMIE Ziele Wenn man von Menschen hört, die etwas Großartiges in ihrem Leben geleistet haben, erfahren wir oft, dass diese ihr Ziel über Jahre verfolgt haben oder diesen Wunsch schon bereits
ONLINE-AKADEMIE Ziele Wenn man von Menschen hört, die etwas Großartiges in ihrem Leben geleistet haben, erfahren wir oft, dass diese ihr Ziel über Jahre verfolgt haben oder diesen Wunsch schon bereits
Grundideen der Gentechnik
 Grundideen der Gentechnik Die Gentechnik kombiniert Biotechnik und Züchtung. Wie in der Züchtung wird die Erbinformation eines Lebewesen verändert. Dabei nutzte man in den Anfängen der Gentechnik vor allem
Grundideen der Gentechnik Die Gentechnik kombiniert Biotechnik und Züchtung. Wie in der Züchtung wird die Erbinformation eines Lebewesen verändert. Dabei nutzte man in den Anfängen der Gentechnik vor allem
Anleitung über den Umgang mit Schildern
 Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Parotis Pankreas. Dünndarm Bürstensaum. Amylose Amylopektin Glykogen. Maltose. Glucose. Isomaltose. Saccharose. Fructose. Lactose. Galaktose.
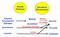 Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Versuch 8. Plasmid - Isolierung
 Versuch 8 Plasmid - Isolierung Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X C. Weindel & M. Schwarz Wird benotet?: Einleitung Ein Plasmid
Versuch 8 Plasmid - Isolierung Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X C. Weindel & M. Schwarz Wird benotet?: Einleitung Ein Plasmid
ORGANISCHE CHEMIE-ÜBUNGEN für Studierende mit Chemie als Nebenfach
 Prof. Dr. Th. K. Lindhorst RGAISCE CEMIE-ÜBUGE für Studierende mit Chemie als ebenfach 1. a) Alanin ist 2-Aminopropansäure. Wählen Sie für die Darstellung der beiden enantiomeren Formen von Alanin eine
Prof. Dr. Th. K. Lindhorst RGAISCE CEMIE-ÜBUGE für Studierende mit Chemie als ebenfach 1. a) Alanin ist 2-Aminopropansäure. Wählen Sie für die Darstellung der beiden enantiomeren Formen von Alanin eine
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Lerntext Pflanzen 1. Was sind Pflanzen?
 Was sind Pflanzen? Lerntext Pflanzen 1 Pleurotus_ostreatus Ausschnitt eines Photos von Tobi Kellner, das er unter der Lizenz CC BY-SA 3.0 zur Verfügung stellte Der Körper eines Pilzes ist ein Fadengeflecht
Was sind Pflanzen? Lerntext Pflanzen 1 Pleurotus_ostreatus Ausschnitt eines Photos von Tobi Kellner, das er unter der Lizenz CC BY-SA 3.0 zur Verfügung stellte Der Körper eines Pilzes ist ein Fadengeflecht
50. Mathematik-Olympiade 2. Stufe (Regionalrunde) Klasse 11 13. 501322 Lösung 10 Punkte
 50. Mathematik-Olympiade. Stufe (Regionalrunde) Klasse 3 Lösungen c 00 Aufgabenausschuss des Mathematik-Olympiaden e.v. www.mathematik-olympiaden.de. Alle Rechte vorbehalten. 503 Lösung 0 Punkte Es seien
50. Mathematik-Olympiade. Stufe (Regionalrunde) Klasse 3 Lösungen c 00 Aufgabenausschuss des Mathematik-Olympiaden e.v. www.mathematik-olympiaden.de. Alle Rechte vorbehalten. 503 Lösung 0 Punkte Es seien
Spektroskopie. im IR- und UV/VIS-Bereich. Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) http://www.analytik.ethz.
 Spektroskopie im IR- und UV/VIS-Bereich Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Enantiomere sind Stereoisomere,
Spektroskopie im IR- und UV/VIS-Bereich Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Enantiomere sind Stereoisomere,
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Professionelle Seminare im Bereich MS-Office
 Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Thermodynamik. Basics. Dietmar Pflumm: KSR/MSE. April 2008
 Thermodynamik Basics Dietmar Pflumm: KSR/MSE Thermodynamik Definition Die Thermodynamik... ist eine allgemeine Energielehre als Teilgebiet der Chemie befasst sie sich mit den Gesetzmässigkeiten der Umwandlungsvorgänge
Thermodynamik Basics Dietmar Pflumm: KSR/MSE Thermodynamik Definition Die Thermodynamik... ist eine allgemeine Energielehre als Teilgebiet der Chemie befasst sie sich mit den Gesetzmässigkeiten der Umwandlungsvorgänge
Chemische Reaktionen
 Ein paar Worte zuvor 7 Stoffe und ihre Eigenschaften 1 Reine Stoffe und Gemische 10 2 Aggregatzustände, Dichte, Löslichkeit, Brennbarkeit und Leitfähigkeit 12 3 Trennverfahren 19 Auf einen Blick: Stoffe
Ein paar Worte zuvor 7 Stoffe und ihre Eigenschaften 1 Reine Stoffe und Gemische 10 2 Aggregatzustände, Dichte, Löslichkeit, Brennbarkeit und Leitfähigkeit 12 3 Trennverfahren 19 Auf einen Blick: Stoffe
Zeichen bei Zahlen entschlüsseln
 Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
Zeichen bei Zahlen entschlüsseln In diesem Kapitel... Verwendung des Zahlenstrahls Absolut richtige Bestimmung von absoluten Werten Operationen bei Zahlen mit Vorzeichen: Addieren, Subtrahieren, Multiplizieren
ORGANISCHE CHEMIE. Aminosäuren und Proteine
 RGAISE EMIE Aminosäuren und Proteine Aminosäuren (AS) R 2 arbonsäuren mit einer Aminogruppe Die (etwa) 20 proteinogenen Aminosäuren sind alle α-aminosäuren (Aminogruppe an -2), unterscheiden sich durch
RGAISE EMIE Aminosäuren und Proteine Aminosäuren (AS) R 2 arbonsäuren mit einer Aminogruppe Die (etwa) 20 proteinogenen Aminosäuren sind alle α-aminosäuren (Aminogruppe an -2), unterscheiden sich durch
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Wortschema Reaktionsschema Beispiel 1: Kupfer und Schwefel Vorzahlen
 6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Umgang mit Schaubildern am Beispiel Deutschland surft
 -1- Umgang mit Schaubildern am Beispiel Deutschland surft Im Folgenden wird am Beispiel des Schaubildes Deutschland surft eine Lesestrategie vorgestellt. Die Checkliste zur Vorgehensweise kann im Unterricht
-1- Umgang mit Schaubildern am Beispiel Deutschland surft Im Folgenden wird am Beispiel des Schaubildes Deutschland surft eine Lesestrategie vorgestellt. Die Checkliste zur Vorgehensweise kann im Unterricht
IV. Übungsaufgaben für die Jahrgangstufe 9 & 10
 IV. Übungsaufgaben für die Jahrgangstufe 9 & 10 Von der Erbanlage zum Erbmerkmal: 34) Welche Aufgaben haben Chromosomen? 35) Zeichne und benenne die Teile eines Chromosoms, wie sie im Lichtmikroskop während
IV. Übungsaufgaben für die Jahrgangstufe 9 & 10 Von der Erbanlage zum Erbmerkmal: 34) Welche Aufgaben haben Chromosomen? 35) Zeichne und benenne die Teile eines Chromosoms, wie sie im Lichtmikroskop während
Endstoffe (Produkte) Aus dem Reaktionsgemisch entweichendes Gas, z. B. 2 Welche Informationen kann man einer Reaktionsgleichung entnehmen?
 Reaktionsgleichungen Reaktionsgleichungen Blatt 1/5 1 Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen, also einen chemischen Prozeß. Auf der einen Seite steht,
Reaktionsgleichungen Reaktionsgleichungen Blatt 1/5 1 Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen, also einen chemischen Prozeß. Auf der einen Seite steht,
Zwischenablage (Bilder, Texte,...)
 Zwischenablage was ist das? Informationen über. die Bedeutung der Windows-Zwischenablage Kopieren und Einfügen mit der Zwischenablage Vermeiden von Fehlern beim Arbeiten mit der Zwischenablage Bei diesen
Zwischenablage was ist das? Informationen über. die Bedeutung der Windows-Zwischenablage Kopieren und Einfügen mit der Zwischenablage Vermeiden von Fehlern beim Arbeiten mit der Zwischenablage Bei diesen
Erstellen einer Collage. Zuerst ein leeres Dokument erzeugen, auf dem alle anderen Bilder zusammengefügt werden sollen (über [Datei] > [Neu])
![Erstellen einer Collage. Zuerst ein leeres Dokument erzeugen, auf dem alle anderen Bilder zusammengefügt werden sollen (über [Datei] > [Neu]) Erstellen einer Collage. Zuerst ein leeres Dokument erzeugen, auf dem alle anderen Bilder zusammengefügt werden sollen (über [Datei] > [Neu])](/thumbs/29/13170670.jpg) 3.7 Erstellen einer Collage Zuerst ein leeres Dokument erzeugen, auf dem alle anderen Bilder zusammengefügt werden sollen (über [Datei] > [Neu]) Dann Größe des Dokuments festlegen beispielsweise A4 (weitere
3.7 Erstellen einer Collage Zuerst ein leeres Dokument erzeugen, auf dem alle anderen Bilder zusammengefügt werden sollen (über [Datei] > [Neu]) Dann Größe des Dokuments festlegen beispielsweise A4 (weitere
Katalysatoren - Chemische Partnervermittlung im virtuellen Labor
 Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
1.6 ph-werte. Einführung Chemie Seite 19
 Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Text: Octapharma GmbH Illustrationen: Günter Hengsberg Layout: nonmodo, Köln
 Unser Immunsystem Text: Octapharma GmbH Illustrationen: Günter Hengsberg Layout: nonmodo, Köln Bakterien und Viren können uns krank machen. Wir bekommen dann Husten, Schnupfen oder Durchfall. Unser Körper
Unser Immunsystem Text: Octapharma GmbH Illustrationen: Günter Hengsberg Layout: nonmodo, Köln Bakterien und Viren können uns krank machen. Wir bekommen dann Husten, Schnupfen oder Durchfall. Unser Körper
Aliphatische Aminosäuren. Aromatische Aminosäuren
 Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Woche 1: Was ist NLP? Die Geschichte des NLP.
 Woche 1: Was ist NLP? Die Geschichte des NLP. Liebe(r) Kursteilnehmer(in)! Im ersten Theorieteil der heutigen Woche beschäftigen wir uns mit der Entstehungsgeschichte des NLP. Zuerst aber eine Frage: Wissen
Woche 1: Was ist NLP? Die Geschichte des NLP. Liebe(r) Kursteilnehmer(in)! Im ersten Theorieteil der heutigen Woche beschäftigen wir uns mit der Entstehungsgeschichte des NLP. Zuerst aber eine Frage: Wissen
Bekommen durch Ansteckung. H Human Beim Menschen. Acquired I D. Schwäche des Immunsystems. Schwäche des Immunsystems.
 Test 3.1.1 HIV / Aids: Was ist das? H Human Beim Menschen A Acquired Bekommen durch Ansteckung I Immunodeficiency Schwäche des Immunsystems I D Immune Deficiency Schwäche des Immunsystems V Virus Virus
Test 3.1.1 HIV / Aids: Was ist das? H Human Beim Menschen A Acquired Bekommen durch Ansteckung I Immunodeficiency Schwäche des Immunsystems I D Immune Deficiency Schwäche des Immunsystems V Virus Virus
Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2
 Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2 1. Wie viel mol Eisen sind in 12 x 10 23 Molekülen enthalten? ca. 2 Mol 2. Welches Volumen Litern ergibt sich wenn ich 3 mol
Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2 1. Wie viel mol Eisen sind in 12 x 10 23 Molekülen enthalten? ca. 2 Mol 2. Welches Volumen Litern ergibt sich wenn ich 3 mol
Vergleichsarbeiten in 3. Grundschulklassen. Mathematik. Aufgabenheft 1
 Vergleichsarbeiten in 3. Grundschulklassen Mathematik Aufgabenheft 1 Name: Klasse: Herausgeber: Projekt VERA (Vergleichsarbeiten in 3. Grundschulklassen) Universität Koblenz-Landau Campus Landau Fortstraße
Vergleichsarbeiten in 3. Grundschulklassen Mathematik Aufgabenheft 1 Name: Klasse: Herausgeber: Projekt VERA (Vergleichsarbeiten in 3. Grundschulklassen) Universität Koblenz-Landau Campus Landau Fortstraße
Kohlenhydrate. Diese Abbildung zeigt Strukturformeln von Zellulose und Stärke.
 Lerntext Ernährung Bisher haben sich fast alle Empfehlungen der Ernährungswissenschaftler als falsch erwiesen. Gültig blieben zwei Regeln, die Menschen schon lange vor den Wissenschaftlern kannten. Man
Lerntext Ernährung Bisher haben sich fast alle Empfehlungen der Ernährungswissenschaftler als falsch erwiesen. Gültig blieben zwei Regeln, die Menschen schon lange vor den Wissenschaftlern kannten. Man
7. Tag: Säuren und Basen
 7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik
 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
Alle Schlüssel-Karten (blaue Rückseite) werden den Schlüssel-Farben nach sortiert und in vier getrennte Stapel mit der Bildseite nach oben gelegt.
 Gentlemen", bitte zur Kasse! Ravensburger Spiele Nr. 01 264 0 Autoren: Wolfgang Kramer und Jürgen P. K. Grunau Grafik: Erhard Dietl Ein Gaunerspiel für 3-6 Gentlemen" ab 10 Jahren Inhalt: 35 Tresor-Karten
Gentlemen", bitte zur Kasse! Ravensburger Spiele Nr. 01 264 0 Autoren: Wolfgang Kramer und Jürgen P. K. Grunau Grafik: Erhard Dietl Ein Gaunerspiel für 3-6 Gentlemen" ab 10 Jahren Inhalt: 35 Tresor-Karten
Handbuch Fischertechnik-Einzelteiltabelle V3.7.3
 Handbuch Fischertechnik-Einzelteiltabelle V3.7.3 von Markus Mack Stand: Samstag, 17. April 2004 Inhaltsverzeichnis 1. Systemvorraussetzungen...3 2. Installation und Start...3 3. Anpassen der Tabelle...3
Handbuch Fischertechnik-Einzelteiltabelle V3.7.3 von Markus Mack Stand: Samstag, 17. April 2004 Inhaltsverzeichnis 1. Systemvorraussetzungen...3 2. Installation und Start...3 3. Anpassen der Tabelle...3
Übung 11 Genregulation bei Prokaryoten
 Übung 11 Genregulation bei Prokaryoten Konzepte: Differentielle Genexpression Positive Genregulation Negative Genregulation cis-/trans-regulation 1. Auf welchen Ebenen kann Genregulation stattfinden? Definition
Übung 11 Genregulation bei Prokaryoten Konzepte: Differentielle Genexpression Positive Genregulation Negative Genregulation cis-/trans-regulation 1. Auf welchen Ebenen kann Genregulation stattfinden? Definition
VORANGEGANGENE MODELLE
 VORANGEGANGENE MODELLE UNSER THEMA HEUTE Ziel dieses Papers: - Nähere Charakterisierung der AuxREs - Analyse eines zu den AuxREs gehörenden Transkriptionsfaktors WAS BEREITS BEKANNT WAR: - Auxin moduliert
VORANGEGANGENE MODELLE UNSER THEMA HEUTE Ziel dieses Papers: - Nähere Charakterisierung der AuxREs - Analyse eines zu den AuxREs gehörenden Transkriptionsfaktors WAS BEREITS BEKANNT WAR: - Auxin moduliert
OECD Programme for International Student Assessment PISA 2000. Lösungen der Beispielaufgaben aus dem Mathematiktest. Deutschland
 OECD Programme for International Student Assessment Deutschland PISA 2000 Lösungen der Beispielaufgaben aus dem Mathematiktest Beispielaufgaben PISA-Hauptstudie 2000 Seite 3 UNIT ÄPFEL Beispielaufgaben
OECD Programme for International Student Assessment Deutschland PISA 2000 Lösungen der Beispielaufgaben aus dem Mathematiktest Beispielaufgaben PISA-Hauptstudie 2000 Seite 3 UNIT ÄPFEL Beispielaufgaben
Welche Lagen können zwei Geraden (im Raum) zueinander haben? Welche Lagen kann eine Gerade bezüglich einer Ebene im Raum einnehmen?
 Welche Lagen können zwei Geraden (im Raum) zueinander haben? Welche Lagen können zwei Ebenen (im Raum) zueinander haben? Welche Lagen kann eine Gerade bezüglich einer Ebene im Raum einnehmen? Wie heiÿt
Welche Lagen können zwei Geraden (im Raum) zueinander haben? Welche Lagen können zwei Ebenen (im Raum) zueinander haben? Welche Lagen kann eine Gerade bezüglich einer Ebene im Raum einnehmen? Wie heiÿt
2.8 Grenzflächeneffekte
 - 86-2.8 Grenzflächeneffekte 2.8.1 Oberflächenspannung An Grenzflächen treten besondere Effekte auf, welche im Volumen nicht beobachtbar sind. Die molekulare Grundlage dafür sind Kohäsionskräfte, d.h.
- 86-2.8 Grenzflächeneffekte 2.8.1 Oberflächenspannung An Grenzflächen treten besondere Effekte auf, welche im Volumen nicht beobachtbar sind. Die molekulare Grundlage dafür sind Kohäsionskräfte, d.h.
Informationsblatt Induktionsbeweis
 Sommer 015 Informationsblatt Induktionsbeweis 31. März 015 Motivation Die vollständige Induktion ist ein wichtiges Beweisverfahren in der Informatik. Sie wird häufig dazu gebraucht, um mathematische Formeln
Sommer 015 Informationsblatt Induktionsbeweis 31. März 015 Motivation Die vollständige Induktion ist ein wichtiges Beweisverfahren in der Informatik. Sie wird häufig dazu gebraucht, um mathematische Formeln
Kreativ visualisieren
 Kreativ visualisieren Haben Sie schon einmal etwas von sogenannten»sich selbst erfüllenden Prophezeiungen«gehört? Damit ist gemeint, dass ein Ereignis mit hoher Wahrscheinlichkeit eintritt, wenn wir uns
Kreativ visualisieren Haben Sie schon einmal etwas von sogenannten»sich selbst erfüllenden Prophezeiungen«gehört? Damit ist gemeint, dass ein Ereignis mit hoher Wahrscheinlichkeit eintritt, wenn wir uns
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Grundlagen. Maximilian Ernestus Waldorfschule Saarbrücken
 Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Musterlösung - Übung 5 Vorlesung Bio-Engineering Sommersemester 2008
 Aufgabe 1: Prinzipieller Ablauf der Proteinbiosynthese a) Erklären Sie folgende Begriffe möglichst in Ihren eigenen Worten (1 kurzer Satz): Gen Nukleotid RNA-Polymerase Promotor Codon Anti-Codon Stop-Codon
Aufgabe 1: Prinzipieller Ablauf der Proteinbiosynthese a) Erklären Sie folgende Begriffe möglichst in Ihren eigenen Worten (1 kurzer Satz): Gen Nukleotid RNA-Polymerase Promotor Codon Anti-Codon Stop-Codon
Modellbildungssysteme: Pädagogische und didaktische Ziele
 Modellbildungssysteme: Pädagogische und didaktische Ziele Was hat Modellbildung mit der Schule zu tun? Der Bildungsplan 1994 formuliert: "Die schnelle Zunahme des Wissens, die hohe Differenzierung und
Modellbildungssysteme: Pädagogische und didaktische Ziele Was hat Modellbildung mit der Schule zu tun? Der Bildungsplan 1994 formuliert: "Die schnelle Zunahme des Wissens, die hohe Differenzierung und
Alle gehören dazu. Vorwort
 Alle gehören dazu Alle sollen zusammen Sport machen können. In diesem Text steht: Wie wir dafür sorgen wollen. Wir sind: Der Deutsche Olympische Sport-Bund und die Deutsche Sport-Jugend. Zu uns gehören
Alle gehören dazu Alle sollen zusammen Sport machen können. In diesem Text steht: Wie wir dafür sorgen wollen. Wir sind: Der Deutsche Olympische Sport-Bund und die Deutsche Sport-Jugend. Zu uns gehören
Kohlenhydrate und ihre Funktionen
 Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
mentor Grundwissen Chemie. 5. bis 10. Klasse Usedom
 mentor Grundwissen mentor Grundwissen Chemie. 5. bis 10. Klasse Alle wichtigen Themen von Andreas Usedom 1. Auflage mentor Grundwissen Chemie. 5. bis 10. Klasse Usedom schnell und portofrei erhältlich
mentor Grundwissen mentor Grundwissen Chemie. 5. bis 10. Klasse Alle wichtigen Themen von Andreas Usedom 1. Auflage mentor Grundwissen Chemie. 5. bis 10. Klasse Usedom schnell und portofrei erhältlich
Einführung. KLASSE: 9TE NAME: Vorname: Datum: LTAM Naturwissenschaften 9e Chemische Gleichungen 1 -
 Einführung Ein Gärtner bestellt beim Großhändler Blumen. Dort werden Tulpen in Dreier-Sträußen und Vergissmeinnichtchen in Zweier-Sträußen angeboten. Für Valentinstag, möchte der Gärtner ein Sonderangebot
Einführung Ein Gärtner bestellt beim Großhändler Blumen. Dort werden Tulpen in Dreier-Sträußen und Vergissmeinnichtchen in Zweier-Sträußen angeboten. Für Valentinstag, möchte der Gärtner ein Sonderangebot
Kulturelle Evolution 12
 3.3 Kulturelle Evolution Kulturelle Evolution Kulturelle Evolution 12 Seit die Menschen Erfindungen machen wie z.b. das Rad oder den Pflug, haben sie sich im Körperbau kaum mehr verändert. Dafür war einfach
3.3 Kulturelle Evolution Kulturelle Evolution Kulturelle Evolution 12 Seit die Menschen Erfindungen machen wie z.b. das Rad oder den Pflug, haben sie sich im Körperbau kaum mehr verändert. Dafür war einfach
Abgestufte Lernhilfen
 Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Referat : Aufbau v. Proteinen u. ihre Raumstruktur
 Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
2 Physikalische Eigenschaften von Fettsäuren: Löslichkeit, Dissoziationsverhalten, Phasenzustände
 2 Physikalische Eigenschaften von Fettsäuren: Löslichkeit, Dissoziationsverhalten, Phasenzustände Als Fettsäuren wird die Gruppe aliphatischer Monocarbonsäuren bezeichnet. Der Name Fettsäuren geht darauf
2 Physikalische Eigenschaften von Fettsäuren: Löslichkeit, Dissoziationsverhalten, Phasenzustände Als Fettsäuren wird die Gruppe aliphatischer Monocarbonsäuren bezeichnet. Der Name Fettsäuren geht darauf
Daten sammeln, darstellen, auswerten
 Vertiefen 1 Daten sammeln, darstellen, auswerten zu Aufgabe 1 Schulbuch, Seite 22 1 Haustiere zählen In der Tabelle rechts stehen die Haustiere der Kinder aus der Klasse 5b. a) Wie oft wurden die Haustiere
Vertiefen 1 Daten sammeln, darstellen, auswerten zu Aufgabe 1 Schulbuch, Seite 22 1 Haustiere zählen In der Tabelle rechts stehen die Haustiere der Kinder aus der Klasse 5b. a) Wie oft wurden die Haustiere
Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU
 Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU 2 DIE MEDIZINISCH-PSYCHOLOGISCHE UNTERSUCHUNG (MPU) IST HOCH ANGESEHEN Das Image der Medizinisch-Psychologischen Untersuchung (MPU) ist zwiespältig: Das ist
Verband der TÜV e. V. STUDIE ZUM IMAGE DER MPU 2 DIE MEDIZINISCH-PSYCHOLOGISCHE UNTERSUCHUNG (MPU) IST HOCH ANGESEHEN Das Image der Medizinisch-Psychologischen Untersuchung (MPU) ist zwiespältig: Das ist
Dissoziation, ph-wert und Puffer
 Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Metabolisierung des Aminosäure-Kohlestoffgerüstes
 Metabolisierung des Aminosäure-Kohlestoffgerüstes Abbau zu 7 wichtigen Molekülen: Pyruvat, Acetyl-CoA, Acetoacetyl-CoA, -Ketoglutarat, Succinyl-CoA, Fumarat, Oxalacetat >> also zu 4 Intermediaten des Citratzyklus,
Metabolisierung des Aminosäure-Kohlestoffgerüstes Abbau zu 7 wichtigen Molekülen: Pyruvat, Acetyl-CoA, Acetoacetyl-CoA, -Ketoglutarat, Succinyl-CoA, Fumarat, Oxalacetat >> also zu 4 Intermediaten des Citratzyklus,
Strom in unserem Alltag
 Strom in unserem Alltag Kannst du dir ein Leben ohne Strom vorstellen? Wir verbrauchen jeden Tag eine Menge Energie: Noch vor dem Aufstehen klingelt der Radiowecker, dann schalten wir das Licht ein, wir
Strom in unserem Alltag Kannst du dir ein Leben ohne Strom vorstellen? Wir verbrauchen jeden Tag eine Menge Energie: Noch vor dem Aufstehen klingelt der Radiowecker, dann schalten wir das Licht ein, wir
DAVID: und David vom Deutschlandlabor. Wir beantworten Fragen zu Deutschland und den Deutschen.
 Manuskript Die Deutschen sind bekannt dafür, dass sie ihre Autos lieben. Doch wie sehr lieben sie ihre Autos wirklich, und hat wirklich jeder in Deutschland ein eigenes Auto? David und Nina fragen nach.
Manuskript Die Deutschen sind bekannt dafür, dass sie ihre Autos lieben. Doch wie sehr lieben sie ihre Autos wirklich, und hat wirklich jeder in Deutschland ein eigenes Auto? David und Nina fragen nach.
Kapiteltest 1.1. Kapiteltest 1.2
 Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Grundlagen der Theoretischen Informatik, SoSe 2008
 1. Aufgabenblatt zur Vorlesung Grundlagen der Theoretischen Informatik, SoSe 2008 (Dr. Frank Hoffmann) Lösung von Manuel Jain und Benjamin Bortfeldt Aufgabe 2 Zustandsdiagramme (6 Punkte, wird korrigiert)
1. Aufgabenblatt zur Vorlesung Grundlagen der Theoretischen Informatik, SoSe 2008 (Dr. Frank Hoffmann) Lösung von Manuel Jain und Benjamin Bortfeldt Aufgabe 2 Zustandsdiagramme (6 Punkte, wird korrigiert)
Geld Verdienen im Internet leicht gemacht
 Geld Verdienen im Internet leicht gemacht Hallo, Sie haben sich dieses E-book wahrscheinlich herunter geladen, weil Sie gerne lernen würden wie sie im Internet Geld verdienen können, oder? Denn genau das
Geld Verdienen im Internet leicht gemacht Hallo, Sie haben sich dieses E-book wahrscheinlich herunter geladen, weil Sie gerne lernen würden wie sie im Internet Geld verdienen können, oder? Denn genau das
Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m(h) = 1 u
 Analytische Chemie Stöchiometrie Absolute Atommasse Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m() = 1 u Stoffmenge n Die Stoffmenge
Analytische Chemie Stöchiometrie Absolute Atommasse Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m() = 1 u Stoffmenge n Die Stoffmenge
Arbeitspunkt einer Diode
 Arbeitspunkt einer Diode Liegt eine Diode mit einem Widerstand R in Reihe an einer Spannung U 0, so müssen sich die beiden diese Spannung teilen. Vom Widerstand wissen wir, dass er bei einer Spannung von
Arbeitspunkt einer Diode Liegt eine Diode mit einem Widerstand R in Reihe an einer Spannung U 0, so müssen sich die beiden diese Spannung teilen. Vom Widerstand wissen wir, dass er bei einer Spannung von
Mind Mapping am PC. für Präsentationen, Vorträge, Selbstmanagement. von Isolde Kommer, Helmut Reinke. 1. Auflage. Hanser München 1999
 Mind Mapping am PC für Präsentationen, Vorträge, Selbstmanagement von Isolde Kommer, Helmut Reinke 1. Auflage Hanser München 1999 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 21222 0 schnell
Mind Mapping am PC für Präsentationen, Vorträge, Selbstmanagement von Isolde Kommer, Helmut Reinke 1. Auflage Hanser München 1999 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 21222 0 schnell
Konzepte der Informatik
 Konzepte der Informatik Vorkurs Informatik zum WS 2011/2012 26.09. - 30.09.2011 17.10. - 21.10.2011 Dr. Werner Struckmann / Christoph Peltz Stark angelehnt an Kapitel 1 aus "Abenteuer Informatik" von Jens
Konzepte der Informatik Vorkurs Informatik zum WS 2011/2012 26.09. - 30.09.2011 17.10. - 21.10.2011 Dr. Werner Struckmann / Christoph Peltz Stark angelehnt an Kapitel 1 aus "Abenteuer Informatik" von Jens
Übung 8. 1. Zellkommunikation. Vorlesung Bio-Engineering Sommersemester 2008. Kapitel 4. 4
 Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 05. 05. 08
Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 05. 05. 08
Info zum Zusammenhang von Auflösung und Genauigkeit
 Da es oft Nachfragen und Verständnisprobleme mit den oben genannten Begriffen gibt, möchten wir hier versuchen etwas Licht ins Dunkel zu bringen. Nehmen wir mal an, Sie haben ein Stück Wasserrohr mit der
Da es oft Nachfragen und Verständnisprobleme mit den oben genannten Begriffen gibt, möchten wir hier versuchen etwas Licht ins Dunkel zu bringen. Nehmen wir mal an, Sie haben ein Stück Wasserrohr mit der
Die Gleichung A x = a hat für A 0 die eindeutig bestimmte Lösung. Für A=0 und a 0 existiert keine Lösung.
 Lineare Gleichungen mit einer Unbekannten Die Grundform der linearen Gleichung mit einer Unbekannten x lautet A x = a Dabei sind A, a reelle Zahlen. Die Gleichung lösen heißt, alle reellen Zahlen anzugeben,
Lineare Gleichungen mit einer Unbekannten Die Grundform der linearen Gleichung mit einer Unbekannten x lautet A x = a Dabei sind A, a reelle Zahlen. Die Gleichung lösen heißt, alle reellen Zahlen anzugeben,
Wachstum 2. Michael Dröttboom 1 LernWerkstatt-Selm.de
 1. Herr Meier bekommt nach 3 Jahren Geldanlage 25.000. Er hatte 22.500 angelegt. Wie hoch war der Zinssatz? 2. Herr Meiers Vorfahren haben bei der Gründung Roms (753. V. Chr.) 1 Sesterze auf die Bank gebracht
1. Herr Meier bekommt nach 3 Jahren Geldanlage 25.000. Er hatte 22.500 angelegt. Wie hoch war der Zinssatz? 2. Herr Meiers Vorfahren haben bei der Gründung Roms (753. V. Chr.) 1 Sesterze auf die Bank gebracht
1 topologisches Sortieren
 Wolfgang Hönig / Andreas Ecke WS 09/0 topologisches Sortieren. Überblick. Solange noch Knoten vorhanden: a) Suche Knoten v, zu dem keine Kante führt (Falls nicht vorhanden keine topologische Sortierung
Wolfgang Hönig / Andreas Ecke WS 09/0 topologisches Sortieren. Überblick. Solange noch Knoten vorhanden: a) Suche Knoten v, zu dem keine Kante führt (Falls nicht vorhanden keine topologische Sortierung
BROTTEIG. Um Brotteig zu machen, mischt ein Bäcker Mehl, Wasser, Salz und Hefe. Nach dem
 UNIT BROTTEIG BROTTEIG Um Brotteig zu machen, mischt ein Bäcker Mehl, Wasser, Salz und Hefe. Nach dem Mischen wird der Teig für mehrere Stunden in einen Behälter gegeben, um den Gärungsprozess zu ermöglichen.
UNIT BROTTEIG BROTTEIG Um Brotteig zu machen, mischt ein Bäcker Mehl, Wasser, Salz und Hefe. Nach dem Mischen wird der Teig für mehrere Stunden in einen Behälter gegeben, um den Gärungsprozess zu ermöglichen.
4. Wässrige Lösungen schwacher Säuren und Basen
 4. Wässrige Lösungen schwacher Säuren und Basen Ziel dieses Kapitels ist es, das Vorgehenskonzept zur Berechnung von ph-werten weiter zu entwickeln und ph-werte von wässrigen Lösungen einprotoniger, schwacher
4. Wässrige Lösungen schwacher Säuren und Basen Ziel dieses Kapitels ist es, das Vorgehenskonzept zur Berechnung von ph-werten weiter zu entwickeln und ph-werte von wässrigen Lösungen einprotoniger, schwacher
Lösungen zu den Übungsaufgaben zur Thematik Säure/Base (Zwei allgemeine Hinweise: aus Zeitgründen habe ich auf das Kursivsetzen bestimmter Zeichen
 Lösungen zu den Übungsaufgaben zur Thematik Säure/Base (Zwei allgemeine Hinweise: aus Zeitgründen habe ich auf das Kursivsetzen bestimmter Zeichen verzichtet; Reaktionsgleichungen sollten den üblichen
Lösungen zu den Übungsaufgaben zur Thematik Säure/Base (Zwei allgemeine Hinweise: aus Zeitgründen habe ich auf das Kursivsetzen bestimmter Zeichen verzichtet; Reaktionsgleichungen sollten den üblichen
AUFGABENSAMMLUNG Lösungen. Variabilität von Antikörpern 1
 Variabilität von Antikörpern 1 Rezeptoren bzw. Antikörper eines noch undifferenzierten B-Lymphocyten: a) Schreiben Sie die Anzahl der variablen Exons je Chromosom auf. b) Berechnen Sie die mögliche Anzahl
Variabilität von Antikörpern 1 Rezeptoren bzw. Antikörper eines noch undifferenzierten B-Lymphocyten: a) Schreiben Sie die Anzahl der variablen Exons je Chromosom auf. b) Berechnen Sie die mögliche Anzahl
