Neuartige Therapien für MS, Teil 1: Wissenschaftliche Grundlagen und Auswirkungen oraler MS-Therapien.
|
|
|
- Elvira Hafner
- vor 8 Jahren
- Abrufe
Transkript
1 Neuartige Therapien für MS, Teil 1: Wissenschaftliche Grundlagen und Auswirkungen oraler MS-Therapien Gefördert durch einen unabhängigen Fortbildungszuschuss von Biogen Idec
2 Neuartige Therapien für MS, Teil 1: Wissenschaftliche Grundlagen und Auswirkungen oraler MS-Therapien Zielgruppe Diese Schulung ist für ein ein weltweites Publikum von Neurologen und Hausärzten gedacht. Ziel Das Ziel dieser Schulung ist die Überprüfung der jüngsten klinischen Daten und Profile der neuen krankheitsmodifizierenden Therapien für multiple Sklerose (MS) im Hinblick auf Schubrate, Fortschreiten der Krankheit, Neurodegeneration, Wirkungsmechanismen sowie Wirksamkeits- und Sicherheitsprofile. Lernziele Die Teilnehmerinnen und Teilnehmer sollen nach dem Abschluss der Schulung in der Lage sein: 1. Die Wirkungsmechanismen von MS-Therapien zu vergleichen und gegenüberzustellen 2. Die neuesten klinischen Daten zu neuartigen krankheitsmodifizierenden Therapien hinsichtlich Wirksamkeit, Sicherheit und Verträglichkeit zu diskutieren 3. Die Daten von injizierbaren und oralen MS-Wirkstoffen zu vergleichen und gegenüberzustellen 4. Bei der Wahl eines Medikaments für den einzelnen Patienten Nutzen und Risiken injizierbarer und oraler Wirkstoffe zu beurteilen Herausgeberinformationen und Offenlegungserklärungen Ron Schaumburg, MA Wissenschaftlicher Leiter, Medscape, LLC Offenlegung: Ron Schaumburg, MA, hat keine relevanten finanziellen Verbindungen offengelegt. Andrew N. Wilner, MD Neurohospitalist, Abteilung für Neurologie, Lawrence and Memorial Hospital, New London, Connecticut Offenlegung: Andrew N. Wilner, MD, hat keine relevanten finanziellen Verbindungen offengelegt Informationen über Autoren/Fakultätsmitglieder und Offenlegungserklärungen Dr. med. Mathias Buttmann, Oberarzt für Neurologie, Leiter der MS-Spezialambulanz, stellvertretender Leiter der klinischen Forschungsgruppe für multiple Sklerose an der Neurologischen Klinik und Poliklinik des Universitätsklinikums Würzburg in Deutschland Dr. Mathias Buttmann hat folgende relevante finanzielle Beziehungen offengelegt: Hat als Berater und Gutachter agiert für: Bayer HealthCare Pharmaceuticals; Biogen Idec, Inc.; Genzyme Corporation; Merck Serono; Novartis Pharmaceuticals Corporation; Ocatapharma Hat finanzielle Mittel erhalten von: Merck Serono; Novartis Pharmaceuticals Dr. Buttmann beabsichtigt, den nicht-zugelassenen Gebrauch von Arzneimitteln, mechanischen Geräten, Biologika oder Diagnostika zu diskutieren, die von der FDA in den Vereingten Staaten zugelassen sind. Dr. Buttmann beabsichtigt, in der Prüfung befindliche Arzneimittel, mechanische Geräte, Biologika oder Diagnostika zu diskutieren, die von der FDA in den Vereinigten Staaten nicht zugelassen sind. Pg.2
3 Einleitung Die multiple Sklerose (MS) ist eine durch die Kombination aus genetischer Anfälligkeit und Umwelteinflüssen verursachte chronisch entzündliche demyelinisierende Erkrankung des Gehirns und des Rückenmarks. [1,2] Ein T-Zell-vermittelter Autoimmunangriff auf Myelinbestandteile ist möglicherweise der zentrale Aspekt ihrer Pathogenese, obwohl bislang die Existenz eines der Mehrheit der Patienten gemeinsamen MS-spezifischen Autoantigens nicht bestätigt werden konnte. [2] Die multiple Sklerose betrifft etwa Menschen in den Vereinigten Staaten und über in Europa. Die geschätzte weltweite Prävalenz beträgt 2,3 Millionen. [3,4] Die Krankheit tritt bei Frauen mindestens doppelt so häufig auf wie bei Männern und wird in den meisten Fällen im Alter von 20 bis 40 Jahren diagnostiziert. Obwohl der ursprüngliche klinische Verlauf typischerweise schubförmig remittierend (RRMS) ist, treten ungefähr zwei Drittel der RRMS-Patienten, die nicht mit modernen krankheitsmodifizierenden Therapien (DMT) behandelt wurden, letztlich in eine sekundäre progrediente Phase (SPMS) ein, die von einer stetigen Zunahme der Behinderung gekennzeichnet ist. [5,6] Bei 10 bis 15 % aller MS-Patienten zeigt die Erkrankung einen primär progredienten Verlauf (PPMS). Fünfzehn Jahre nach Ausbruch der Krankheit benötigen 50 % der unbehandelten Patienten Hilfe beim Gehen. [7] Beobachtungsstudien aus verschiedenen Ländern deuten in den letzten Jahren auf einen allgemein gutartigeren klinischen Verlauf hin. Teilweise könnte dies auf die Verfügbarkeit moderner DMT für Patienten mit RRMS zurückzuführen sein. [8] Aktuelle DMT zielen in erster Linie darauf ab, Schübe und neue permanente Behinderungen sowie die mittels Magnetresonanztomografie (MRT) nachgewiesene Krankheitsaktivität zu verhindern. Diese Wirkstoffe können entweder als Injektion, Infusion oder oral verabreicht werden. Für Patienten mit PPMS gibt es leider noch keine zugelassenen DMT. Akute Schübe werden mit hochdosierten intravenösen Kortikosteroiden über 3 bis 5 Tage als Standardtherapie behandelt. Symptomatische Medikamente zur Verbesserung der Gehfähigkeit oder zur Linderung von Symptomen wie Spastizität und Ermüdung bieten Patienten mit einem chronisch progredienten Krankheitsverlauf pharmakologische Behandlungsmöglichkeiten. Die jüngst erfolgte Einführung dreier oraler DMT hat die Zahl der therapeutischen Möglichkeiten für Menschen mit RRMS beträchtlich erhöht. Andere Behandlungsmöglichkeiten wie neue monoklonale Antikörper zeichnen sich bereits ab. [9] Injektionstherapie Mit der Zulassung von injizierbaren Interferon-β-1b-, gefolgt von Interferon β-1a-präparaten und Glatirameracetat (GA) durch die amerikanische Arzneimittelbehörde Food and Drug Administration (FDA) im Jahr 1993 war erstmals eine moderne wirksame Behandlung von RRMS verfügbar. [10] Diese Arzneimittel sind mittlerweile in den meisten Ländern zugelassen. Manche Interferon-β-Präparate sind zudem in manchen Ländern für Patienten mit SPMS und überlagerten Schüben zugelassen. [11] Aus zweijährigen wegweisenden klinischen Studien ging hervor, dass diese parenteralen Behandlungen die Häufigkeit schubförmig remittierender Episoden im Vergleich mit Placebo um etwa 30 % senkten und die meisten das Risiko einer neuen permanenten Behinderung moderat reduzierten. [12] Die Einhaltung des injizierbaren Behandlungsregimes könnte allerdings aufgrund kutaner Nebenwirkungen wie Schmerzen, Entzündungen, Verhärtungen und Lipoathrophie sowie nachteiliger systemischer Wirkungen wie grippeähnlicher Symptome, Leberfunktionsstörungen und Zytopenien beeinträchtigt sein. [13,14] Injizierbare Therapien sind die am häufigsten verschriebenen Behandlungen bei MS. Allerdings haben ihre mäßige Wirksamkeit in Kombination mit ihrem zwar meist benignen, aber doch suboptimalen und die Therapietreue beeinträchtigendem Nebenwirkungsprofil zu weiteren Forschungen in Richtung effektiverer und besser verträglicher Therapien geführt. [15,16] Infusionstherapie Zu den derzeit von der FDA und der Europäischen Arzneimittelagentur (EMA) zugelassenen Infusionstherapien für MS gehören Natalizumab und Mitoxantron. Alemtuzumab erhielt in Europa die Zulassung im September 2013, doch die FDA verweigerte die Zulassung für die Vereinigten Staaten im Dezember Alle drei Wirkstoffe sind hochwirksam, wenn es um die Senkung der Schubrate geht, doch insgesamt sind sie, aufgrund der potenziell schwerwiegenden Nebenwirkungen, auf die Anwendung als Zweit- oder Drittlinientherapie beschränkt. Natalizumab war mit Stand Januar 2014 bei 1 von 290 behandelten Patienten mit progressiver multifokaler Leukenzephalopathie (PML) assoziiert, [17] während Mitoxantron bei 12 % zu systolischer Dysfunktion, bei 0,4 % zu kongestiver Herzinsuffizienz und bei 0,8 % zu sekundärer akuter Leukämie führte. [18] Auf die Behandlung mit Alemtuzumab können lebensbedrohende, aber behandelbare Autoimmun-Nebenwirkungen folgen wie Immunthrombozytopenie bei 1 % und das Goodpasture-Syndrom bei 0,3 %. Überdies trat bei etwa einem Drittel der Patienten innerhalb von 3 Jahren nach der Infusionsbehandlung eine autoimmune Funktionsstörung der Schilddrüse auf. In manchen Fällen können diese Komplikationen erst Jahre nach der letzten Infusion auftreten. [19] Pg.3
4 Neuartige Therapien für MS, Teil 1: Wissenschaftliche Grundlagen und Auswirkungen oraler MS-Therapien Orale Therapien Seit 2010 sind 3 orale Therapien verfügbar. Jede verfügt über einen eigenen Wirkmechanismus und ein einzigartiges Nebenwirkungsprofil. Diese neuen Medikamente und weitere noch in Entwicklung befindliche orale Therapien werden im Folgenden genauer betrachtet. Fingolimod Vorgeschichte. Fingolimod leitet sich von Myriocin/ISP-1, einem Metaboliten des entomopathogenen Pilzes Isaria sinclairii ab. [15] Ursprünglich als Immunsuppressivum zur Vermeidung der Abstoßung von Nierentransplantaten untersucht, zeigte sich in klinischen Phase-3-Studien, dass die Substanz die Wirkung von Cyclosporin nicht verstärkt. [15] Weitere Untersuchungen ergaben, dass Fingolimod nach Phosphorylierung in vivo und damit dem Übergang in seinen aktiven Zustand an G-Protein-gekoppelte Sphingosin-1-Phosphat -S1P-)Rezeptoren bindet. Fingolimod senkt die Zahl der peripheren Lymphozyten, einschließlich der CD4+ T-Zellen, der CD8+ T-Zellen und der B-Zellen. [20] Die Wirkungen auf Zellmigration und Zelltransport wiesen darauf hin, dass Fingolimod therapeutische Anwendung bei Autoimmunerkrankungen wie MS finden könnte. [20] Wirkungsmechanismus. Fingolimod bindet an 4 von 5 S1P-Rezeptoren (S1P1, 3, 4 und 5) und verfügt über mindestens zwei Wirkungsmechanismen, die MS-Patienten zugutekommen können. Im Rahmen des ersten Mechanismus fungiert Fingolimod funktionell als Antagonist zu den S1P1-Lymphozytenrezeptoren, wodurch es zur Retention Chemokinrezeptor7-(CCR7-)positiver naiver und früher zentraler Gedächtnis-T-Zellen in den Lymphknoten kommt, was deren Infiltration des Zentralnervensystems (ZNS) verhindert, wo diese entzündliche Schäden verursachen könnten. Im Gegensatz dazu bleiben die für die Abwehr fremder Antigene und Krebszellen erforderlichen CCR7-negativen späten Effektorzellen und Effektor-Gedächtnis-T-Zellen von Fingolimod vergleichsweise unbeeinflusst. [20] Hinsichtlich des zweiten Mechanismus könnte Fingolimod, das die Blut-Hirn-Schranke effizient überwindet, direkt auf Astrozyten, Oligodendrozyten, Neuronen, Mikroglia und dendritische Zellen wirken, die ebenfalls S1P-Rezeptoren exprimieren. Diese direkten Effekte im ZNS könnten neuroprotektiver Natur sein, die Erhaltung von Myelin fördern und die Neurodegeneration verhindern, wie im Tiermodell gezeigt wurde. [21] Klinische Phase-3-Studien. Eine randomisierte, doppelblinde, Placebo-kontrollierte Phase-3-Studie zu oralem Fingolimod bei 1272 Patienten mit RRMS (FREEDOMS) ergab über einen Zeitraum von 2 Jahren eine jährliche Schubrate von 0,40 unter Placebo, 0,18 unter Fingolimod 0,5 mg/tag und 0,16 unter Fingolimod 1,25 mg/tag. Beide Fingolimod-Dosen erzielten eine relative Senkung von 54 % beziehungsweise 60 % (p <0,001 für beide Dosen gegenüber Placebo). [22] Der zweite primäre Endpunkt die nach 3 Monaten bestätigte Behinderungsprogression nach zweijähriger Therapie wurde bei 24,1 % der mit Placebo behandelten Patienten, bei 17,7 % der mit Fingolimod 0,5 mg/tag und bei 16,6 % der mit Fingolimod 1,25 mg/tag behandelten Patienten festgestellt, wodurch sich relative Senkungen der Hazard Ratio (HR) von 30 % beziehungsweise 32 % bei beiden Fingolimod- Gruppen gegenüber dem Placebo ergaben (p=0,02 für beide Fingolimod-Dosen gegenüber Placebo). Beide Dosen von Fingolimod waren dem Placebo nach 24 Monaten hinsichtlich aller MRT-Werte (p<0,001 bis p =0,03) und auch bei den Werten für Hirnatrophie (p <0,001 für beide Fingolimod-Dosen gegenüber Placebo) überlegen. Im Hinblick auf die Präsenz Gadoliniumanreichender Läsionen im MRT gab es zu Beginn in der FREEDOMS-Studie kein Missverhältnis. Zu den Nebenwirkungen zählten Bradykardie und AV-Leitungsblock zum Zeitpunkt der ersten Dosis, erhöhte Leberenzyme, Hypertonie und Makulaödem. In einer zweiten, vornehmlich in den Vereinigten Staaten durchgeführten randomisierten, doppelblinden, Phase-3-Studie (FREEDOMS II), deren Ergebnisse im Jahr 2012 auf medizinischen Konferenzen präsentiert wurden, wurden Fingolimod-Dosen von 0,5 oder 1,25 mg/tag im Vergleich zu Placebo bei 1083 Patienten mit RRMS untersucht. [23] Nach 2 Jahren betrug die jährliche Schubrate unter Placebo 0,40, unter Fingolimod 0,5 mg/tag lag sie bei 0,21 und unter Fingolimod 1,25 mg/tag bei 0,20 (p<0,001 für beide Dosen gegenüber Placebo). Anders als bei FREEDOMS I wurde bei keiner Dosis eine signifikante Senkung der bestätigten Behinderungsprogression verzeichnet. Dennoch ergab sich im MRT gegenüber dem Placebo eine signifikante Verringerung der Veränderungen des Hirnvolumens, der Entzündungsaktivität sowie der Krankheitslast. [24] Zu den in der Fingolimod-Gruppe häufiger als in der Placebo-Gruppe auftretenden Nebenwirkungen zählten Basalzellkarzinome, Herpes-Zoster-Infektionen, Hypertonie, Lymphopenie, Leukopenie, erhöhte Alanin-Aminotransferase-Werte, symptomatische Bradykardie und AV-Block zweiten Grades. Pg.4
5 In der randomisierten, doppelblinden, 12-monatigen Phase-3-Parallelgruppenstudie TRANSFORMS mit 1292 Patienten mit RRMS wurde Fingolimod in den Dosen 0,5 mg/tag und 1,25 mg/tag mit wöchentlichen intramuskulären Injektionen von Interferon-β-1a (30 μg) im Double-Dummy-Design verglichen. [25] Die jährliche Schubrate betrug 0,33 in der Interferon-Gruppe, 0,16 in der mit Fingolimod 0,5 mg/tag behandelten Gruppe und 0,20 in der mit Fingolimod 1,25 mg/tag behandelten Gruppe (p<0,001 für beide Fingolimod-Dosen). Hinsichtlich der Behinderungsprogression gab es in dieser einjährigen Studie keine signifikanten Unterschiede zwischen den Gruppen. Die Anzahl neuer oder vergrößerter T2-Läsionen, Gadolinium-(Gd-)anreichernder T1- Läsionen und das Ausmaß der Hirnatrophie fielen in beiden Fingolimod-Gruppen signifikant niedriger aus als in der mit Interferon-β-1a behandelten Gruppe. In der mit der höheren Fingolimod-Dosis behandelten Gruppe gab es 2 Todesfälle infolge primärer disseminierter Varicella-Zoster-Infektion bzw. Herpes-Simplex-Virusenzephalitis. Im Übrigen waren die Nebenwirkungen ähnlich der in der FREEDOMS-II-Studie. Aktuelle Forschung. Zu dem laufenden klinischen Fingolimod-Forschungsprogramm zählen eine multizentrische, doppelblinde, Placebo-kontrollierte Studie mit Patienten mit PPMS, deren primärer Abschluss für September 2014 erwartet wird (INFORMS) sowie auch Studien zu optischer Neuritis, amyothropher Lateralsklerose, Rett-Syndrom und anderen Indikationen. Darüber hinaus sind mehrere Beobachtungsstudien zur Sicherheit bei MS-Patienten im Gange, einschließlich eines weltweiten S chwangerschaftsregisters. [26] Indikationen. Zum Zeitpunkt der Abfassung dieses Artikels (April 2014) ist Fingolimod 0,5 mg als einmal täglich einzunehmendes Medikament der Erstlinientherapie von Patienten mit schubförmigen oder schubförmig remittierenden Formen der MS in folgenden Ländern zugelassen (in der Reihenfolge der Zulassung): in Russland, den Vereinigten Staaten, den Vereinigten Arabischen Emiraten (alle drei im Jahr 2010), in der Schweiz, Australien und in über 30 weiteren Ländern. In Kanada und der Europäischen Union wurde Fingolimod im Jahr 2011 nur für Patienten mit hochaktiver RRMS zugelassen. Diese Entscheidung wurde auch in einigen anderen Ländern getroffen. Mit Januar 2014 umfasst die klinische Forschung über Patienten und über Patientenjahre. [27] Kontraindikationen. Fingolimod sollte bei folgenden Indikationen nicht verabreicht werden: bei kurz zurückliegendem Myokardinfarkt, instabiler Angina, Schlaganfall, transitorischer ischämischer Attacke, dekompensierter Herzinsuffizienz mit erforderlichem Krankenhausaufenthalt, Herzinsuffizienz Klasse III/IV, im Falle einer Vorgeschichte oder bei Vorliegen eines atrioventrikulären Blocks II. oder III. Grades Typ Mobitz II, Sick-Sinus-Syndrom (außer der Patient hat einen Herzschrittmacher), QTc-Intervall 500 ms im Vergleich zur Baseline oder bei einer Behandlung mit Antiarrhythmika der Klassen Ia oder III. [28] Da Daten aus Tierversuchen auf ein Teratogenitätsrisiko hinweisen (FDA-Kategorie C), können Frauen im gebärfähigen Alter zwar Fingolimod verschrieben bekommen, sollten aber während der Behandlung und noch 2 Monate nach Abschluss der Behandlung eine wirksame Empfängnisverhütungsmethode anwenden. [29] Teriflunomid Vorgeschichte. Das zweite orale Medikament für RRMS, das von der FDA zugelassen wurde, war Teriflunomid im Jahr Dabei handelt es sich um einen aktiven Metaboliten von Leflunomid, einem Medikament der Zweitlinientherapie nach Methotrexat bei rheumatoider Arthritis. [30] Leflunomid wurde ursprünglich im Rahmen groß angelegter Wirkstoffforschungsprogramme entdeckt, die auf die Identifizierung von Pestiziden für die Landwirtschaft abzielten. Doch bald erkannte man die entzündungshemmenden Eigenschaften der Substanz. [31] In der Europäischen Union ist Leflunomid für die Behandlung von rheumatoider Arthritis seit 1999 und für Psoriasis seit 2004 zugelassen, wobei sich die klinische Forschung auf über 2 Millionen Patientenjahre stützt. Leflunomid kann zu schweren Leberfunktionsstörungen als Nebenwirkung führen und war im Tierversuch teratogen [30], obwohl sich beim Menschen noch keine teratogenen Effekte zeigten. [31] Wirkungsmechanismus. Teriflunomid hemmt die Dihydroorotat-Dehydrogenase, das geschwindigkeitsbestimmende Enzym in der Neusynthese von mitochondrialem Pyrimidin. [31] Teriflunomid zielt auf Lymphoblasten ab, die einen hohen Bedarf an Pyrimidin haben, hat aber keine Wirkung auf ruhende Lymphozyten und homöostatisch proliferierende Lymphozyten, die über einen eigenen Salvage-Pathway ausreichend mit Pyrimidin versorgt werden. [31] In höheren Konzentrationen hemmt Teriflunomid in vitro zudem Tyrosinkinasen und Cyclooxygenase 2, was zu veränderter Zytokin- und Adhäsionsmolekülexpression führt, die in vivo therapeutisch relevant sein könnte. [31] Pg.5
6 Neuartige Therapien für MS, Teil 1: Wissenschaftliche Grundlagen und Auswirkungen oraler MS-Therapien Klinische Phase-3-Studien. Eine randomisierte, doppelblinde, Placebo-kontrollierte Phase-3-Studie zu Teriflunomid (TEMSO) mit.088 Patienten mit RRMS ergab über einen Zeitraum von 2 Jahren eine jährliche Schubrate von 0,54 für Placebo gegenüber 0,37 für Teriflunomid 7 mg/tag und 0,37 für Teriflunomid 14 mg/tag. Dies ergibt eine relative Risikosenkung von 31,2 % beziehungsweise 31,5 % für beide Teriflunomid-Dosen im Vergleich zu Placebo (p<0,001 für beide Teriflunomid-Dosen). [32] Die über 12 Wochen bestätigte Behinderungsprogression zeigte lediglich einen statistischen Trend in Richtung einer möglichen Senkung mit Teriflunomid 7 mg/tag (21,7 % der Patienten) im Vergleich zu Placebo (27,3 %) (p=0,08), doch mit der Teriflunomid-Dosis von 14 mg/tag war sie gegenüber dem Placebo signifikant niedriger (20,2 %, p=0,03). Im Vergleich zu Placebo waren die Veränderungen des gesamten T-2-Läsionsvolumens im MRT nach 108 Wochen mit der einmal täglichen 7-mg -Dosis um 39,4 % (p=0,03) und mit der einmal täglichen 14-mg-Dosis um 67,4 % (p=0,003) geringer. [33] Gd-anreichernde T1-Läsionen waren mit beiden Teriflunomid-Dosen gegenüber Placebo signifikant reduziert (p<0,001 für beide Dosen), während die Hirnatrophie durch Teriflunomid nicht signifikant beeinflusst wurde (p=0,19 mit 7 mg und P =0,35 mit 14 mg gegenüber Placebo). Zu den Nebenwirkungen zählten Durchfall, Übelkeit, Haarausfall, was nur selten zu einer Unterbrechung der Behandlung führte, sowie leicht erhöhte Alanin-Aminotransferase-Werte. Es trat jedoch kein Fall einer schweren Leberfunktionsstörung auf. Eine weitere randomisierte, doppelblinde, Placebo-kontrollierte Phase-3-Studie (TOWER) ergab bei 1169 Patienten mit schubförmiger MS geringere jährliche Schubraten bei der Behandlung mit Teriflunomid 7 mg/tag (0,39, p=0,0183) und Teriflunomid 14 mg/tag (0,32, p=0,001) im Vergleich zu Placebo (0,50). [5] Ähnlich wie bei den Ergebnissen der TEMSO-Studie senkte Teriflunomid 14 mg/tag das Risiko einer nachhaltigen Akkumulation von Behinderungen signifikant (relative HR-Senkung 32 %, p=0,0442), wohingegen sich die Ergebnisse der einmal täglichen 7 mg -Dosis nicht vom Placebo unterschieden. MRT- Endpunkte waren in der TOWER-Studie nicht vorgesehen. Die häufigsten Nebenwirkungen waren jenen der TEMSO-Studie ähnlich. TOPIC war eine Placebo-kontrollierte, 2-jährige Phase-3-Studie mit 618 Patienten, die eine erste auf MS (klinisch isoliertes Syndrom) hindeutende klinische Episode aufwiesen. [34] Sowohl Teriflunomid 7 mg/tag als auch 14 mg/tag reduzierten das Risiko der Entwicklung einer klinisch definierten MS signifikant: Placebo (35,9 %), Teriflunomid 7 mg/tag (27,6 %, p=0,0271), Teriflunomid 14 mg/tag (24 %, p=0,0087). Das Medikament senkte in beiden Behandlungsdosen signifikant das Risiko eines neuen Schubs und neuer T2-Läsionen im MRT. Insgesamt bestätigte das Nebenwirkungsprofil dieser Studie die diesbezüglichen Ergebnisse der TEMSO- und TOWER-Studie. In der für die Auswerter verblindeten Phase-3-Vergleichsstudie TENERE, an der 324 Patienten mit schubförmiger MS teilnahmen, gab es zwischen Teriflunomid 14 mg/tag (0,26) and Interferon-β-1a (44 μg) (0,22, P =0,6) keine signifikanten Unterschiede hinsichtlich dem sekundären Endpunkt der jährlichen Schubrate. Allerdings lag die jährliche Schubrate bei Patienten, die mit Teriflunomid 7 mg/tag (0,41) behandelt wurden, signifikant höher als bei Patienten, die Interferon-β-1a (p=0,03) erhielten. [35] Hinsichtlich des primären zusammengesetzten Endpunkts, der Zeit bis zum Behandlungsversagen definiert als erstes Auftreten eines bestätigten Schubs oder des dauerhaften Behandlungsabbruchs aus anderen Gründen zeigten sich zwischen den 3 Behandlungsgruppen keine Unterschiede. Aktuelle Forschung. Die laufende klinische Forschung hinsichtlich Teriflunomid konzentriert sich weiterhin auf MS mit Studien zur Pharmakokinetik, Wirksamkeit und Sicherheit, Auswirkungen auf Immunzellen, Gehirnpathologie und andere Untersuchungen (clinicaltrials.gov). Überdies sind Beobachtungsstudien zur Sicherheit im Gange und ab Juni 2014 wird mit der Datensammlung für ein von der EMA gefordertes internationales Schwangerschaftsregister begonnen. [36] Indikationen. Teriflunomid ist von der FDA für die einmal tägliche Einnahme zur Behandlung der schubförmigen multiplen Sklerose zugelassen. In der Europäischen Union ist Teriflunomid zur Behandlung von Erwachsenen mit RRMS zugelassen. Zu den weiteren Ländern mit einer bestehenden Zulassung zählen Argentinien, Australien, Kolumbien, Kanada, Mexiko, Venezuela und Südkorea. Bis April 2014 sind über MS-Patienten mit dem Medikament behandelt worden. [37] Pg.6
7 Kontraindikationen. Aufgrund der Erfahrungen mit der Muttersubstanz Leflunomid gilt für Teriflunomid eine Black-Box-Warnung der FDA hinsichtlich Leberversagen. [38] Bislang wurden keine Fälle eines schweren Leberversagens im Zuge der Behandlung mit Teriflunomid gemeldet. Dennoch ist es bei Patienten mit bestehenden schweren Leberfunktionsstörungen kontraindiziert. Auch im Hinblick auf seine Teratogenität besteht für Teriflunomid eine Black-Box-Warnung, weswegen es in der Schwangerschaft kontraindiziert ist (FDA-Warnung der Kategorie X). 38] Das Medikament erwies sich bei Tieren als teratogen. Die sehr begrenzten Erfahrungswerte beim Menschen haben bislang noch kein teratogenes Potenzial gezeigt. Teriflunomid hat eine lange Halbwertszeit von ungefähr 2 Wochen, wobei die messbaren Serumspiegel von Teriflunomid bis zu 2 Jahre nach dem Ende der Behandlung nachweisbar sein können. Daher sollten Frauen, die während der Behandlung mit Teriflunomid schwanger werden, das Medikament unverzüglich absetzen, ärztliche Beratung suchen und sich einer beschleunigten Elimination mittels Colestyramin oder Aktivkohle unterziehen, um eine bestätigte Teriflunomid-Plasmakonzentration von unter 0,02 µg/ml zu erreichen. [38] Dimethylfumarat (DMF) Vorgeschichte. DMF ist ein auch als BG-12 bekannter Fumarsäureester, der im Jahr 2013 erstmals als orales Medikament zur Behandlung von RRMS zugelassen wurde. Fumarsäureester werden seit 1959 in der Behandlung der Psoriasis eingesetzt und sind die am häufigsten angewandte Behandlung für schwere Psoriasis in Deutschland, wo sie für diese Indikation formal im Jahr 1994 zugelassen wurden. [39] Anders als die in Deutschland verwendete Kombination aus Fumarsäureestern, ist DMF ein einzelnes Fumaratderivat. [39] DMF unterliegt einem raschen First-Pass-Effekt und wird dabei zum ebenfalls pharmakologisch aktiven Monomethylfumarat umgewandelt. [40] DMF fand in der Vergangenheit Anwendung als Biozid in Schuhen und Möbeln, wurde von der Europäischen Union allerdings aufgrund seines hohen Potenzials, auch in geringen Konzentrationen eine Kontaktdermatitis auszulösen, verboten. [41] Wirkungsmechanismus. DMF aktiviert den Nrf-2-ARE-Signalweg (nuclear 1 factor (erythroid-derived 2)-like 2 antioxidant response pathway), der theoretisch Neuroinflammation, Neurodegeneration und toxischen oxidativen Stress bekämpft. [42] Zusätzlich hemmt DMF den NF- K B-Signalweg (nuclear factor K B ) und blockiert daher durch den Tumornekrosefaktor α induzierte zelluläre Funktionen, einschließlich dessen proinflammatorische Wirkungen. [39] Klinische Phase-3-Studien. In einer randomisierten, doppelblinden, Placebo-kontrollierten Phase-3-Studie (DEFINE) mit 1237 Patienten mit RRMS lag der Anteil der Patienten, die während der 2 Jahre dauernden Studie einen erneuten Schub erlitten der primäre Endpunkt der Studie bei DMF 240 mg zweimal täglich (27 %) und DMF 240 mg dreimal täglich (26 %) signifikant niedriger als bei der Placebo-Gruppe (46 %, p<0,001 für jede Dosis). [42] Die jährliche Schubrate in zwei Jahren betrug 0,36 unter Placebo, 0,17 unter DMF 240 mg zweimal täglich und 0,19 unter DMF 240 mg dreimal täglich, was einer relativen Senkung unter DMF von 53 % beziehungsweise 48 % entspricht (p<0,001 für jede Dosis). Zu beachten ist allerdings, dass zu Studienbeginn ein starkes Ungleichgewicht hinsichtlich der Existenz von Gd-anreichernden MRT-Läsionen zuungunsten jener Patienten vorlag, die mit Placebo behandelt wurden. Von den Patienten, die einer MRT unterzogen wurden (Placebo, n=180; DMF zweimal täglich, n=176), wiesen zu Studienbeginn im Placebo-Arm 30 % mehr Patienten Gd-anreichernde Läsionen im MRT auf. Die Präsenz derartiger Läsionen ist ein etablierter Prädiktor für die zukünftige Schubaktivität. Zudem und im Gegensatz zu vorangegangenen RRMS-Studien war in den 12 Monaten vor dieser Studie keine klinische Schubaktivität erforderlich, um in die DEFINE-Studie aufgenommen zu werden. Daher darf fairerweise davon ausgegangen werden, dass in der DEFINE-Studie Patienten, die mit Placebo behandelt wurden, im Vergleich zu den mit DMF behandelten zu Studienbeginn eine höhere entzündliche Krankheitsaktivität aufwiesen, wodurch die Ergebnisse möglicherweise zugunsten von DMF verzerrt wurden. Beide DMF-Dosen senkten die bestätigte Behinderungsprogression nach 12 Wochen, die in der Placebo-Gruppe bei 27 % lag. In der Gruppe, die zweimal täglich DMF erhielt, lad diese bei 16 % (p=0,005) und bei 18 % in der Gruppe, die dreimal täglich DMF erhielt (p=0,01). Dies entspricht einer relativen HR-Senkung von 38 % beziehungsweise 34 %. Im Gegensatz dazu zeigte sich bei keiner der beiden DMF-Dosen im Vergleich zu Placebo ein signifikanter Effekt auf die bestätigte Behinderungsprogression nach 24 Wochen. Die Zahl der Gd-anreichernden Läsionen sowie der neuen oder sich vergrößernden T2-gewichteten hyperintensen Läsionen wurde im Vergleich zu Placebo mit beiden DMF-Dosierungen gesenkt (p<0,001 für jede Dosis). Zu beachten ist allerdings, dass die Zahl der kontrastmittelaufnehmenden Läsionen zu Studienbeginn in der Placebo-Gruppe um 30 % höher lag, was möglicherweise zu einer Überschätzung des DMF-Behandlungseffekts führte. Im Hinblick auf Hirnatrophie wurde über die 2 Jahre ein uneinheitlicher Effekt beobachtet; zu einer signifikanten Senkung führte lediglich die niedrigere Dosis (p= 0,02), nicht jedoch die höhere. [43] In einer gesundheitsbezogenen Einschätzung der Lebensqualität schnitt DMF hinsichtlich des Summenwerts aller physischen Komponenten des Short-Form-36-Gesundheitsfragebogens (SF-36) gegenüber Placebo besser ab (p<0,001 für jede Dosis). [44] Pg.7
8 Neuartige Therapien für MS, Teil 1: Wissenschaftliche Grundlagen und Auswirkungen oraler MS-Therapien Zu den in der DEFINE-Studie aufgetretenen Nebenwirkungen zählten Flush, Durchfall, Übelkeit, Oberbauchschmerzen, v erminderte Lymphozytenzahl, erhöhte Leber-Aminotransferase-Werte und Proteinurie. Flush und gastrointestinale Symptome verringerten sich in den ersten Monaten der Behandlung. Doch obwohl die Inzidenz gastrointestinaler Symptome und der Flush-Symptomatik über mehrere Behandlungsphasen abnahm, sank die Prävalenz dieser Nebenwirkungen nicht so stark. [41] Die Gesamtprävalenz der Flush-Symptomatik lag im ersten Monat bei 31 %; im zweiten Monat sank der Wert auf 24 %, während er in den darauffolgenden Monaten nur leicht, wenn überhaupt, abnahm. Bei drei ernsthaften Flush-Ereignissen mussten die betroffenen Patienten hospitalisiert und mit intravenösen Kortikosteroiden behandelt werden. Die Gesamtprävalenz gastrointestinaler Symptome bei Patienten, die mit DMF zweimal täglich behandelt worden waren, lag im ersten Monat bei 22 %, im zweiten Monat bei 17 % und bei 6 bis 12 % in den darauffolgenden Monaten. Während die Gesamtzahl der Patienten, die die Behandlung beendeten, zwischen der Placebo- und den DMF-Gruppen vergleichbar war, brachen Patienten, die DMF erhielten, die Behandlung dreimal öfter aufgrund von Flush oder gastrointestinaler Symptome ab. Patienten, die mit Placebo behandelt wurden, beendeten die Behandlung eher aufgrund des Fortschreitens der Erkrankung. Die Inzidenz von Flush und der damit verbundenen Symptome war in der DMF-Gruppe fünfmal höher als bei Patienten, die mit Placebo oder GA behandelt worden waren. Aufgrund der teilweise vorübergehenden Natur dieser Nebenwirkungen ist die Aufklärung der Patienten und eine engmaschige Überwachung vor allem in den ersten Wochen der Behandlung von Bedeutung, um entsprechende Therapietreue sicherzustellen. In einer weiteren randomisierten, Placebo-kontrollierten Phase-3-Studie (CONFIRM) erhielten 1430 Patienten mit RRMS entweder DMF 240 mg zweimal täglich, DMF 240 mg dreimal täglich, Placebo oder tägliche subkutane GA-Injektionen (20 mg) als aktive Vergleichssubstanz gegenüber Placebo. [45] Die Studie war nicht konzipiert, um die Überlegenheit oder Nichtunterlegenheit von DMF gegenüber GA zu untersuchen. Die jährliche Schubrate betrug in der Placebo-Gruppe 0,40 und war in allen 3 aktiven Gruppen niedriger: DMF 240 mg zweimal täglich (0,22, p<0,001), DMF 240 mg dreimal täglich (0,20, p<0,001), and GA (0,29, p=0,01). Im Hinblick auf die Verteilung von Gd-anreichernden Läsionen im MRT zu Studienbeginn gab es bei der CONFIRM-Studie kein Ungleichgewicht. Die Gabe von DMF zweimal täglich senkte die Schubrate um 44 % gegenüber Placebo. Untersuchungen von Teilgruppen sowohl in der DEFINE- als auch der CONFIRM-Studie zeigten, dass DMF bei jenen Patienten eine geringere Wirkung auf die Schübe hatte, die zu Studienbeginn höhere EDSS-Scores aufwiesen, sowie bei Patienten, die zuvor bereits behandelt worden waren, und bei Patienten, die zumindest 40 Jahre alt waren. Dennoch wurde eine konsistente Senkung der Schubraten bei dem begrenzten Anteil von Patienten mit vormals hoher Krankheitsaktivität nachgewiesen. Keine der aktiven Behandlungen erreichte bei der möglichen relativen Risikosenkung der bestätigten Behinderungsprogression nach 12 Wochen einen statistisch signifikanten Wert: DMF zweimal täglich (-21 %, p=0,25), DMF dreimal täglich (-24 %, p=0,20) oder GA (-7 %, p=0,70). Alle 3 aktiven Behandlungen senkten die Zahl der neuen oder sich vergrößernden T2-gewichteten hyperintensen Läsionen im MRT im Vergleich zu Placebo (p<0,001 für alle) ebenso wie der neuen T1-gewichteten hypointensen Läsionen (p<0,001 für jede DMF-Dosis und p=0,002 für GA). Im Gegensatz dazu war der Wert für Hirnatrophie über den weder in der CONFIRM- noch in der DEFINE-Studie berichtet wird im Vergleich zu Placebo in keinem der 3 aktiven Behandlungsarme signifikant niedriger. [46] Die Nebenwirkungen gestalteten sich ähnlich wie in der DEFINE-Studie. Die mit Placebo behandelten Patienten wiesen tendenziell schlechtere Scores in den SF-36-Subskalen auf, während sich Patienten, die mit DMF oder GA behandelt wurden, insgesamt verbesserten oder stabil blieben. [47] Aktuelle Forschung. Die aktuelle klinische Forschung konzentriert sich primär auf Pharmakokinetik, spezielle Populationen, Verträglichkeit und den Einsatz von DMF bei RRMS und Psoriasis. Überdies laufen zurzeit Beobachtungsstudien zur Sicherheit sowie die Etablierung eines weltweiten Schwangerschafts-Expositionsregisters. Indikationen. DMF ist von der FDA und in Australien für die Behandlung von schubförmiger MS bei Erwachsenen zugelassen. In der Europäischen Union und in Kanada ist DMF für die Behandlung von Patienten mit RRMS zugelassen. In Europa wurde das Medikament mit Stand vom März 2014 nur in Deutschland vermarktet. Bis September 2013 wurden weltweit ungefähr Patienten mit DMF behandelt. Darin eingeschlossen sind Patienten im Umfeld der Anwendungsbeobachtung, in klinischen Studien und kostenlosen Medikamentenprogrammen. [48] Kann Fumarsäure PML verursachen? Zum Zeitpunkt der Abfassung dieses Artikels liegen 4 Fälle von PML bei Patienten mit Psoriasis vor, die in Verbindung mit Fumarsäure enthaltenden Produkten stehen. Mindestens drei dieser Patienten hatten bereits länger an schwerer Lymphopenie gelitten, bevor sie PML entwickelten. Bislang gibt es keine Berichte über PML-Fälle bei MS- Patienten, die mit DMF behandelt wurden. Die Verringerung der Lymphozytenzahl in Phase 3 der DEFINE- und CONFIRM- Studien zeigte einen Plateauwert bis Woche 96. [42,45] Angesichts dieser Daten ist es möglicherweise ratsam, die Lymphozytenzahl bei MS-Patienten, die mit DMF behandelt werden, sorgfältig und fortgesetzt zu überwachen, um PML-gefährdete Patienten frühzeitig zu identifizieren. Pg.8
9 Kontraindikationen. Für DMF werden in der Packungsbeilage keine absoluten Kontraindikationen angeführt, allerdings ist es sinnvoll, dieses Medikament nicht Patienten mit schweren Infektionen zu verschreiben. [53] Da DMF Lymphopenie verursachen kann, sollte, wie in der Verschreibungsinformation dargelegt, vor der Behandlung ein komplettes Blutbild angefertigt und regelmäßig wiederholt werden. Sollte sich während der Behandlung eine schwere Lymphopenie einstellen, tritt diese wahrscheinlich in den ersten Monaten der Therapie auf. Bei Menschen bestehen keine bekannten teratogenen Wirkungen, während derartige Nebenwirkungen im Tiermodell beobachtet wurden (Kategorie C). Weitere in Phase 3 und Phase 2 geprüfte orale Wirkstoffe Azathioprin. Das Purinnukleosid-Analogon Azathioprin wurde in Deutschland im Jahr 2000 als Zweitlinienmedikament zur Behandlung von RRMS zwar zugelassen, jedoch nie einer gründlichen Prüfung gemäß aktuellen Standards unterzogen. In den Vereinigten Staaten ist Azathioprin zur Verhinderung von Abstoßungsreaktionen bei Homotransplantationen von Nieren sowie für das Management der aktiven rheumatoiden Arthritis zugelassen. [54] Cladribin. Die intrazelluläre Ansammlung des aktiven Metaboliten von Cladribin, 2-Chlor-Desoxyadenosintriphosphat, unterbricht den zellulären Metabolismus, hemmt die DNA-Synthese und -Reparatur und führt zu Apoptose. [55] Seine Affinität für Lymphozyten führt zur raschen Abnahme von CD4+ und CD8+ T-Zellen und von CD19+ B-Zellen, wobei andere Immunzellen vergleichsweise unbeeinflusst bleiben. Zudem senkt Cladribin proinflammatorische Zytokine, Chemokine, die Adhäsionsmolekülexpression und mononukleäre Zellmigration. [55] Im Rahmen einer randomisierten, doppelblinden, Placebo-kontrollierten Phase-3-Studie (CLARITY) zur Beurteilung von 2 Cladribin-Dosen (3,5 mg/kg oder 5,25 mg/kg) bei 1326 Patienten mit RRMS zeigte sich eine signifikante Senkung der Schubraten, des Risikos der Behinderungsprogression und der durch MRT nachgewiesenen Krankheitsaktivität. [55] Zu den nennenswerten Nebenwirkungen zählten Lymphopenie (21,6 % in der Niedrigdosis-Gruppe und 31,5 % in der Hochdosis-Gruppe) sowie Herpes Zoster (8 Patienten in der Niedrigdosis-Gruppe und 12 Patienten in der Hochdosis-Gruppe gegenüber keinem Patienten in der Placebo-Gruppe). In einer randomisierten, doppelblinden Phase-3-Studie (ORACLE) verzögerte oral verabreichtes Cladribin die Diagnose von MS bei Patienten mit einem ersten klinischen demyelinisierenden Ereignis signifikant. [56] Obwohl ursprünglich in Russland und Australien zugelassen, verweigerten FDA und EMA Cladribin die Zulassung aufgrund von Bedenken hinsichtlich zunehmender opportunistischer Infektionen und Malignitäten. [56] Im Anschluss daran brach der Sponsor die Entwicklung von Cladribin ab. Laquinimod. Laquinimod ist ein orales Chinolin-3-Carboxamid-Derivat von Roquinimex, das bereits zuvor in Phase-3-Studien als Therapie für MS untersucht wurde, jedoch aufgrund schwerer, immunvermittelter unerwünschter Ereignisse wie Serositis, Perikarditis und Myokardinfarkt zurückgezogen wurde. [16,57] Laquinimod wurde in der Hoffnung entwickelt, ein besseres Sicherheitsprofil aufzuweisen als Roquinimex. Es wurde festgestellt, dass Laquinimod die Infiltration von Entzündungszellen in das ZNS reduziert, die Demyelinisierung verringert und Verlust des Axons verhindert. Obwohl der genaue Wirkungsmechanismus, einschließlich des molekularen Zieles, unbekannt ist, beschränkt Laquinimod die Lymphozytenmigration in das ZNS und reguliert die proinflammatorischen Reaktionen der Astrozyten herunter. [16] Seine Fähigkeit, die Hirnatrophie einzuschränken, deutet auf einen möglichen neuroprotektiven Effekt hin. Im Rahmen einer randomisierten, doppelblinden Phase-3-Studie (ALLEGRO) wurde 1106 Patienten mit RRMS zwei Jahre lang ein Placebo oder Laquinimod 0,6 mg/tag oral verabreicht. [57] In der Laquinimod-Gruppe lag die jährliche Schubrate bei 0,30 im Vergleich zu 0,39 in der Placebo-Gruppe (p=0,002 nach Bereinigung um Baseline-Variablen), was einer relativen HR-Reduktion von 23 % entspricht. Die Laquinimod-Gruppe wies auch ein reduziertes Risiko einer bestätigten Behinderungsprogression nach 3 Monaten auf (11,1 %), während dieser Wert in der Placebo-Gruppe bei 15,7 % lag (p=0,01 nach Bereinigung um Baseline- Variablen). Hinsichtlich der MRT-Parameter war die kumulative Zahl Gd-anreichernder Läsionen und neuer oder sich vergrößernder Läsionen in T2-gewichteten Aufnahmen bei der Laquinimod-Gruppe niedriger als in der Placebo-Gruppe (p<0,001 für beide nach Bereinigung). Darüber hinaus war die Hirnatrophie bei Patienten, die Laquinimod erhielten, weniger ausgeprägt (p<0,001 nach Bereinigung). Nicht bereinigte Analysen wurden in der ALLEGRO-Studie nicht angegeben. [57,58] 24 Patienten (5 %) die mit Laquinimod behandelt wurden, wiesen vorübergehend Alanin-Aminotransferase-Werte auf, die dreimal so hoch waren als der obere Grenzwert des Normalbereichs (ULN). In der Placebo-Gruppe war dies bei 8 Patienten (2 %) der Fall. Werte, die fünfmal höher lagen als ULN, waren auf beide Gruppen gleich verteilt. Zu den unerwünschten Ereignissen, die mindestens bei 2 Laquinimod-Patienten und häufiger als in der Placebo-Gruppe auftraten, zählten Durchfall, Übelkeit, Bauchschmerzen, Infektionen der Harnwege, Sinusitis, Blinddarmentzündung (5 Laquinimod-Patienten und 1 Placebo-Patient), Husten, Rückenschmerzen, Gelenkschmerzen und Schlaflosigkeit. Pg.9
10 Neuartige Therapien für MS, Teil 1: Wissenschaftliche Grundlagen und Auswirkungen oraler MS-Therapien In eine randomisierte, doppelblinde, Placebo-kontrollierte Phase-3-Studie (BRAVO) zur Beurteilung von Laquinimod 0,6 mg/tag mit 1331 Patienten mit RRMS wurde für den deskriptiven Vergleich noch ein dritter, für den Auswerter verblindeter Studienarm aufgenommen, in dem Patienten Interferon-β-1a (30 μg einmal wöchentlich) intramuskulär verabreicht wurde. [59] Die auf der ECTRIMS/ACTRIMS-Konferenz im Jahr 2011 brandaktuell präsentierten, nicht bereinigten Daten der BRAVO-Studie zeigten hinsichtlich des Unterschiedes in der jährlichen Schubrate dem primären Endpunkt zwischen Laquinimod und Placebo nur einen statistischen Trend (relative Senkung durch Laquinimod -18 %, p= 0,075). [60] Nach der Korrektur von Ungleichheiten zwischen den Behandlungsgruppen zu Studienbeginn hinsichtlich der Zahl von T-2-Läsionen und der Prozentzahl der Patienten mit Gd-anreichernden Läsionen zeigte eine bereinigte Analyse allerdings, dass Laquinimod die jährliche Schubrate signifikant auf 0,29 verringerte, während dieser Wert für Placebo bei 0,37 (p=0,026) lag. In der Placebo-Gruppe wiesen zu Studienbeginn 16 % weniger Patienten Gd-anreichernde MRT-Läsionen auf als in der Laquinimod-Gruppe. Ebenso zeigte sich mit Laquinimod eine nur grenzwertige Signifikanz im Hinblick auf die Senkung der Behinderungsprogression. Lediglich 13 % der Placebo-Patienten wiesen eine bestätigte Progression gegenüber 10 % der Laquinimod-Patienten (HR-Senkung -31 %, p=0,063) auf. Im Vergleich mit Placebo war die Hirnatrophie im MRT mit -28 % signifikant reduziert (p<0,001). Die Nebenwirkungen waren ähnlich wie in der ALLEGRO-Studie. Lebensbedrohende Malignitäten oder opportunistische Infektionen traten nicht auf. [16] Interferon-β-1a senkte die jährliche Schubrate signifikant auf 0,27 gegenüber 0,37 für Placebo (p=0,002). Interferon-β-1a wies hinsichtlich des Risikos der Behinderungsprogression oder der Hirnatrophie im Vergleich zu Placebo keinen signifikanten Effekt auf. Eine dritte Phase-3- Studie, CONCERTO, wird zurzeit durchgeführt. In dieser Studie werden ungefähr 1800 Patienten bis zu 24 Monate untersucht. Ein Studienarm sieht die Behandlung mit Laquinimod 1,2 mg/tag vor, ein zweiter mit Laquinimod 0,6 mg/tag, ein weiterer den Vergleich mit Placebo vor. Die ARPEGGIO-Studie, eine Phase-2-Studie mit 500 Patienten mit PPMS, befindet sich derzeit in der Planungsphase. In Phase 2 geprüfte Wirkstoffe Gegenwärtig befinden sich neuartige S1P-Rezeptoragonisten mit höherer Rezeptor-Subtyp-Selektivität als Fingolimod in der Entwicklung. Zu diesen Wirkstoffen der nächsten Generation zählen Siponimod, Ponesimod, KRP-203, ONO-4641, RPC1063, CS-0777 und GSK [61] Siponimod zielt selektiv auf S1P1 und S1P5 ab, hat jedoch keinen Einfluss auf S1P2, -3 und -4. Dieses Profil könnte besonders vorteilhaft sein, da S1P1 und S1P5 an Astrogliose, dem Zellüberleben, der Prozessmodellierung bei Oligodendrozyten und der T-Zellen-Migration in das ZNS beteiligt sind. Die Wirksamkeit und Sicherheit von Siponimod bei SPMS wird derzeit im Rahmen der Phase-3-Studie EXPAND untersucht. [61] ONO-4641 ist ebenfalls ein selektiver S1P1- und S1P5-Agonist. In einer Phase-2-Studie zu RRMS (DreaMS) senkte ONO-4641 die Zahl der Hirnläsionen im MRT. [61] Um festzustellen, ob selektive S1P-Agonisten einen Sicherheitsvorteil gegenüber Fingolimod bieten, bedarf es weiterer klinischer Studien. [62] Zudem zeigte sich Firategrast, ein oraler Integrin-α-4-Inhibitor, in einer randomisierten, doppelblinden, Placebo-kontrollierten Phase-2-Studie mit Patienten mit RRMS vielversprechend, doch bislang hat keine Phase-3-Studie dazu begonnen. [63] Die Auswirkungen neuer oraler Wirkstoffe auf die Behandlung von MS Mit den drei neuen oralen DMT Fingolimod, Teriflunomid und DMF wurden die Behandlungsoptionen für Menschen mit RRMS beträchtlich erweitert. Die relativen Vorteile und Risiken dieser Wirkstoffe müssen bei der Auswahl einer Behandlung für den individuellen Patienten berücksichtigt werden. Pg.10
11 Wirksamkeit. Obwohl nur wenige direkte Vergleiche zwischen den oralen Wirkstoffen und den parenteralen DMT für MS vorliegen, können die Daten aus den Studien hinsichtlich der Wirksamkeit aufschlussreich sein. Im Rahmen der einjährigen Parallelgruppenstudie TRANSFORMS im Double-Dummy-Design wiesen mit Fingolimod behandelte RRMS-Patienten signifikant niedrigere jährliche Schubraten und weniger Hirnatrophie auf als Patienten, die mit intramuskulär verabreichtem Interferon-β-1a behandelt wurden. [25] Die CONFIRM-Studie war zwar nicht dazu angelegt, die Wirksamkeit von DMF und GA direkt zu vergleichen, doch schienen eine Reihe von Parametern einen Vorteil von DMF zu ergeben, obwohl sich DMF hinsichtlich einer Reihe von Schlüsselaspekten nicht vorteilhafter präsentierte als das Placebo. [44] In der dem Bewerter gegenüber verblindeten TENERE-Studie erwies sich Teriflunomid 14 mg/tag hinsichtlich der jährlichen Schubrate und der Zeit bis zum Behandlungsversagen als mit Interferon-β-1a vergleichbar, während die Schubrate bei Patienten, die mit Teriflunomid 7 mg/tag behandelt wurden, signifikant höher war. [35] Obwohl Laquinimod die jährliche Schubrate im Vergleich zu Placebo nicht signifikant verringerte, zeigte es im Rahmen der BRAVO-Studie einen signifikanten Behandlungseffekt im Hinblick auf Hirnatrophie. Umgekehrt verringerte intramuskulär verabreichtes Interferon-β-1a zwar die Schubrate im Vergleich zu Placebo signifikant, jedoch nicht das Ausmaß der Hirnatrophie. Mit dieser Studie sollte nicht die Überlegenheit oder Nichtunterlegenheit von Laquinimod gegenüber Interferon β-1a geprüft werden. Um die relative Wirksamkeit oraler und injizierbarer Medikamente deutlich einzuordnen, bedarf es weiterer vergleichender Daten. Sicherheit und Verträglichkeit. Obwohl injizierbare Interferone und GA eine umfangreiche Erfolgsbilanz hinsichtlich ihrer Sicherheit vorweisen können, wird ihr mäßiger therapeutischer Nutzen möglicherweise durch mangelnde Therapietreue beeinträchtigt. Einmal täglich einzunehmende orale Wirkstoffe (wie Fingolimod, Teriflunomid) oder zweimal täglich einzunehmende Medikamente (DMF) verfügen über das theoretische Potenzial, die Therapietreue zu verbessern, weil die Unannehmlichkeiten häufiger Injektionen entfallen. Doch Fragen der Verträglichkeit entstehen möglicherweise auch bei oral einzunehmenden Medikamenten. So treten beispielsweise bei Einnahme von Fingolimod Herpes-Zoster-Infektionen auf, bei DMF gastrointestinale Beschwerden und im Fall von Teriflunomid kommt es zu Haarausfall. Zudem können bei jedem der oralen Wirkstoffe potenziell schwerwiegende systemische Nebenwirkungen auftreten. Langfristige Erfahrungen in der Praxis sind begrenzt, obwohl alle oralen Medikamente in mindestens zwei klinischen Phase-3-Studien untersucht wurden. Auch die Teratogenität der Wirkstoffe sorgt für Bedenken, da sich viele MS-Patientinnen im gebärfähigen Alter befinden. Fingolimod und DMF sind hinsichtlich Schwangerschaft in der FDA-Kategorie C eingestuft, Teriflunomid in Kategorie X. Die bislang sehr begrenzten Erfahrungswerte wiesen kein teratogenes Potenzial dieser Medikamente beim Menschen auf. Interferon β war beim Menschen mit einem geringeren durchschnittlichem Geburtsgewicht, kürzerer mittlerer Geburtsdauer und Frühgeburten assoziiert und ist in der FDA-Kategorie C eingestuft. GA, für das im Vergleich zu Interferon β weniger Daten hinsichtlich der diesbezüglichen Auswirkungen auf den Menschen öffentlich verfügbar sind, ist in Kategorie B eingestuft. [64] Keine teratogenen Effekte bei Tieren oder Menschen wurden bislang für GA beschrieben, für das Erfahrungswerte aus über 2 Millionen MS- Patientenjahren vorliegen (Teva Pharmaceuticals, persönliche Kommunikation, März 2014). Schlussfolgerungen Die neuen oralen Wirkstoffe für MS bieten eine höchst willkommene Ergänzung zum etablierten Rüstzeug parenteraler DMT. Sowohl ältere als auch neuere Präparate haben Vor- und Nachteile. Da es uns an langfristigen Sicherheitsdaten für diese neuen oralen Wirkstoffe fehlt, ist es ratsam, die klinischen Erfahrungen hinsichtlich Wirksamkeit und unerwünschter Ereignisse zu verfolgen, wenn die Anwendung dieser Medikamente bei unseren Patienten erwogen wird. So viele Patienten wie möglich sollten in prospektive Sicherheits-Beobachtungsregister aufgenommen werden. Angesichts der steigenden Zahl an verfügbaren Behandlungsmöglichkeiten ist die Ermittlung von prädiktiven Biomarkern, die zu einer Individualisierung der Behandlungsentscheidungen beitragen könnten, eine der vordringlichsten noch zu erfüllenden Voraussetzungen im Bereich des Managements der MS. Persönliche Widmung. Der Autor möchte diesen Artikel einem Familienmitglied widmen, das an RRMS erkrankt ist und dem es nach dramatischen Anfängen in den letzten 15 Jahren mit einem injizierbaren Erstlinienwirkstoff gut gegangen ist. Pg.11
12 Neuartige Therapien für MS, Teil 1: Wissenschaftliche Grundlagen und Auswirkungen oraler MS-Therapien LITERATUR 1. Compston A, Coles A. Multiple sclerosis. Lancet. 2008;372: Nylander A, Hafler DH. Multiple sclerosis. J Clin Invest. 2012;122: National MS Society. MS prevalence. About-the-Society/MS-Prevalence. Accessed March 24, World Health Organization. Mental health. Atlas: Multiple Sclerosis Resources in the World neurology/atlas_multiple_sclerosis_resources_2008/en/. Accessed March 24, Confavreux C, O Connor P, Comi G, et al. Oral teriflunomide for patients with relapsing multiple sclerosis (TOWER): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Neurol. 2014;13: Confavreux C, Vukusic S. Age at disability milestones in multiple sclerosis. Brain. 2006;129: Noseworthy JH, Lucchinetti C, Rodriguez M, Weinshenker BG. Multiple sclerosis. New Engl J Med. 2000;343: Kister I, Chamot E, Cutter G, et al. Increasing age at disability milestones among MS patients in the MSBase Registry. J Neurol Sci. 2012;318: Deiss A, Brecht I, Haarmann A, Buttmann M. Treating multiple sclerosis with monoclonal antibodies: a 2013 update. Expert Rev Neurother. 2013;13: Buttmann M, Rieckmann P. Interferon-beta1b in multiple sclerosis. Expert Rev Neurother. 2007;7: La Mantia L, Vacchi L, Di Pietrantonj C, et al. Interferon beta for secondary progressive multiple sclerosis. Cochrane Database Syst Rev. 2012;1:CD Goodin DS. The use of interferon beta and glatiramer acetate in multiple sclerosis. Semin Neurol. 2013;33: Galetta SL, Markowitz C. US FDA-approved disease-modifying treatments for multiple sclerosis: review of adverse effect profiles. CNS Drugs. 2005;19: Balak DM, Hengstman GJ, Çakmak A, et al. Cutaneous adverse events associated with disease-modifying treatment in multiple sclerosis: a systematic review. Mult Scler. 2012;18: Chun J, Brinkmann V. A mechanistically novel, first oral therapy for multiple sclerosis: the development of fingolimod (FTY720, Gilenya). Discov Med. 2011;12: Haggiag S, Ruggiere S, Gasperini C, et al. Efficacy and safety of laquinimod in multiple sclerosis. Ther Adv Neurol Disorders. 2013;6: Biogen Idec, Inc. Data on file. Accessed March 7, Marriott JJ, Miyasaki JM, Gronseth G, et al. Evidence Report: The efficacy and safety of mitoxantrone (Novantrone) in the treatment of multiple sclerosis: report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Neurology. 2010;74: Costelloe L, Jones J, Coles A. Secondary autoimmune diseases following alemtuzumab therapy for multiple sclerosis. Expert Rev Neurother. 2012;12: Brinkmann V, Billich A, Baumruker T, et al. Fingolimod (FTY720): discovery and development of an oral drug to treat multiple sclerosis. Nature Reviews Drug Discovery. 2010;9: Groves A, Kihara Y, Chun J. Fingolimod: direct CNS effects of sphingosine 1-phosphate (S1P) receptor modulation and implications in multiple sclerosis therapy. J Neurol Sci. 2013;328: Kappos L, Radue EW, O Connor P, et al. A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis. New Engl J Med. 2010;362: Calabresi PA, Goodin D, Jeffery D. Efficacy and safety of fingolimod versus placebo: primary outcomes from the phase 3 FREEDOMS II study in patients with relapsing-remitting multiple sclerosis. Poster presented at: 28th Annual Meeting of the European Committee for Treatment and Research in Multiple Sclerosis; October 10-13, 2012; Lyon, France. Poster Radue EW, Goodin D, Jeffery D, et al. Fingolimod reduces magnetic resonance imaging inflammatory lesion activity versus placebo in patients with relapsing-remitting multiple sclerosis: results from the phase 3 FREEDOMS II study. Poster presented at: 28th Annual Meeting of the European Committee for Treatment and Research in Multiple Sclerosis; October 10-13, 2012; Lyon, France. Poster Cohen JA, Barkhof F, Comi G, et al. Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis. New Engl J Med. 2010;362: Gilenya Pregnancy Registry. Accessed on March 24, Novartis Pharma GmbH. Personal communication. 28. Gilenya [package insert]. East Hanover, NJ: Novartis Pharmaceuticals Corporation; Karlsson G, Francis G, Koren G, et al. Pregnancy outcomes in the clinical development program of fingolimod in multiple sclerosis. Neurology. 2014;82: Behrens F, Koehm M, Burkhardt H. Update 2011: leflunomide in rheumatoid arthritis-strengths and weaknesses. Curr Opin Rheumatol. 2011;23: Claussen MC, Korn T. Immune mechanisms of new therapeutic strategies in MS-teriflunomide. Clin Immunol. 2012;142: Østensen M, Förger F. How safe are anti-rheumatic drugs during pregnancy? Curr Opin Pharmacol. 2013;13: O Connor P, Wolinsky JS, Confavreux C, et al. Randomized trial of oral teriflunomide for relapsing multiple sclerosis. New Engl J Med. 2011;365: Wolinsky JS, Naravana PA, Nelson F, et al. Magnetic resonance imaging outcomes from a phase III trial of teriflunomide. Mult Scler. 2013;19: Miller A, Wolinsky J, Kappos L, et al. TOPIC main outcomes: efficacy and safety of once-daily oral teriflunomide in patients with clinically isolated syndrome. Presented at: 29th Annual Meeting of the European Committee for Treatment and Research in Multiple Sclerosis; October 2-5, 2013; Copenhagen, Denmark. Oral presentation Vermersch P, Czlonkowska A, Grimaldi LME, et al. Teriflunomide versus subcutaneous interferon beta-1a in patients with relapsing multiple sclerosis: a randomised, controlled phase 3 trial. Mult Scler [Epub ahead of print] 36. European Network of Centres for Pharmacoepidemiology and Pharmaco vigilance. Study identification: an international pregnancy exposure registry of women with multiple sclerosis (MS) exposed to teriflunomide. Accessed on March 24, Genzyme Sanofi. Personal communication. 38. Aubagio [package insert]. Cambridge, MA: Genzyme Corporation; Mrowietz U, Asadullah K. Dimethylfumarate for psoriasis: more than a dietary curiosity. Trends Mol Med. 2005;11: Albrecht P, Bouchachia I, Goebels N, et al. Effects of dimethyl fumarate on neuroprotection and immunomodulation. J Neuroinflammation. 2012;9: BLC Leather Technology Centre Ltd. Dimethyl fumarate -- the background. Leather Magazine. 18 November documents/dmfbackground.pdf. Accessed April 1, Pg.12
13 42. Gold R, Kappos L, Arnold DL, et al. Placebo-controlled phase 3 study of oral BG-12 for relapsing multiple sclerosis. New Engl J Med. 2012;367: Arnold DL, Gold R, Kappos L, et al. Effect of BG-12 on brain atrophy and lesions volume: MRI results from the DEFINE study during first and second year of treatment. Paper presented at: 64th American Academy of Neurology Annual Meeting; April 21-28, 2011; New Orleans, LA. Abstract IN Kappos L, Gold R, Arnold DL, et al. Quality of life outcomes with BG-12 (dimethyl fumarate) in patients with relapsing-remitting multiple sclerosis: The DEFINE study. Mult Scler J. 2014;20: Fox RJ, Miller DH, Phillips JT, et al. Placebo-controlled phase 3 study of oral BG-12 or glatiramer in multiple sclerosis. New Engl J Med. 2012;367: Arnold D, Gold R, Kappos L, et al. Effect of BG-12 on brain atrophy and lesions volume: MRI results from the DEFINE study during first and second year of treatment. Paper presented at: 64th American Academy of Neurology Annual Meeting; April 21-28, 2011; New Orleans, LA. Abstract S Kita M, Fox RJ, Phillips JT, et al. Effects of BG-12 (dimethyl fumarate) on health-related quality of life in patients with relapsing-remitting multiple sclerosis: findings from the CONFIRM study. Mult Scler J. 2014;20: Biogen Idec, Inc. Personal communication. 49. Sweetser MT, Dawson KT, Bozic C. Manufacturer s response to case reports of PML. New Engl J Med. 2013;368: Buttmann M, Stoll G. Case reports of PML in patients treated for psoriasis. New Engl J Med. 2013;369: Ermis U, Weis J, Schulz JB. PML in a patient treated with fumaric acid. New Engl J Med. 2013;368: van Oosten BW, Killestein J, Wattjes MP. Case reports of PML in patients treated for psoriasis. N Engl J Med. 2013;369: Tecfidera [package insert]. Cambridge, MA: Biogen Idec, Inc; Imuran [package insert]. San Diego, CA; Prometheus Laboratories; May Giovannoni G, Comi G, Cook S, et al. A placebo-controlled trial of oral cladribine for relapsing multiple sclerosis. New Engl J Med. 2010;362: Leist TP, Comi G, Cree BAC, et al. Effect of oral cladribine on time to conversion to clinically definite multiple sclerosis in patients with a first demyelinating event (ORACLE MS): a phase 3 randomised trial. Lancet Neurol [Epub ahead of print] 57. Comi G, Jeffery D, Kappos L, et al. Placebo-controlled trial of oral laquinimod for multiple sclerosis. New Engl J Med. 2012;366: Filippi M, Rocca MA, Pagani E, et al. Placebo-controlled trial of oral laquinimod in multiple sclerosis: MRI evidence of an effect on brain tissue damage. J Neurol Neurosurg Psychiatry [Epub ahead of print] 59. Vollmer TL, Sorensen PS, Selmaj K, et al. A randomized placebo-controlled phase III trial of oral laquinimod for multiple sclerosis. J Neurol [Epub ahead of print] 60. Vollmer TL, Soelberg Sorensen P, Arnold DL on behalf of the BRAVO Study Goup. A placebo-controlled and active comparator phase III trial (BRAVO) for relapsing-remitting multiple sclerosis. Paper presented at: 5th Joint Triennial Congress of the European and Americas Committees for Treatment and Research in Multiple Sclerosis; October 19-22; Amsterdam, The Netherlands. Late-breaking news abstract Bigaud M, Guerini D, Billich A, et al. Second generation S1P pathway modulators: research strategies and clinical developments. Biochimica et Biophysica Acta [Epub ahead of print] 62. Roberts E, Guerrero M, Urbano M, Rosen H. Sphingosine 1-phosphate receptor agonists: a patent review ( ). Expert Opin Ther Patents. 2013;23: Miller DH, Weber T, Grove R, et al. Firategrast for relapsing remitting multiple sclerosis: a phase 2, randomised, double-blind, placebocontrolled trial. Lancet Neurol. 2012;11: Lu E, Wang BW, Guimond C, et al. Disease-modifying drugs for multiple sclerosis in pregnancy: a systematic review. Neurology. 2012;79: Pg.13
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva
 Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
Europäische Arzneimittelbehörde empfiehlt Aussetzung der Marktzulassung für Raptiva Darmstadt (19. Februar 2009) Die Merck KGaA hat heute bekannt gegeben, dass die europäische Arzneimittelbehörde EMEA
Willkommen zum 4. Lüdenscheider Tag der MS
 Willkommen zum 4. Lüdenscheider Tag der MS Update 2012 Therapieoptionen bei MS Referent: Dr. med. Sebastian Schimrigk Lüdenscheid, den 11. Februar 2012 Was sind die Behandlungsziele? 1. Ordnung: Verhinderung
Willkommen zum 4. Lüdenscheider Tag der MS Update 2012 Therapieoptionen bei MS Referent: Dr. med. Sebastian Schimrigk Lüdenscheid, den 11. Februar 2012 Was sind die Behandlungsziele? 1. Ordnung: Verhinderung
MS Basistherapie: Noch aktuell? Was sagen die Langzeitstudien über 20 Jahre? Ms katte Pat FB 2014 1
 MS Basistherapie: Noch aktuell? Was sagen die Langzeitstudien über 20 Jahre? Ms katte Pat FB 2014 1 Die MS-Therapie auf einen Blick Therapieswitsch Mitoxantron * Tysabri (Natalizumab) Gilenya (Fingolimod)
MS Basistherapie: Noch aktuell? Was sagen die Langzeitstudien über 20 Jahre? Ms katte Pat FB 2014 1 Die MS-Therapie auf einen Blick Therapieswitsch Mitoxantron * Tysabri (Natalizumab) Gilenya (Fingolimod)
DGN 2010 Weiter auf Erfolgskurs AVONEX, die verlässliche Basistherapie bei Multipler Sklerose
 DGN 2010 Weiter auf Erfolgskurs AVONEX, die verlässliche Basistherapie bei Multipler Sklerose Mannheim (23. September 2010) - Die MS-Forschung ist derzeit geprägt von zahlreichen Neuentwicklungen. Bewährten
DGN 2010 Weiter auf Erfolgskurs AVONEX, die verlässliche Basistherapie bei Multipler Sklerose Mannheim (23. September 2010) - Die MS-Forschung ist derzeit geprägt von zahlreichen Neuentwicklungen. Bewährten
MS 10 Fragen und Antworten
 Hintergrundinformation MS 10 Fragen und Antworten Was ist MS? Multiple Sklerose (MS) ist eine chronische Erkrankung des Zentralen Nervensystems (ZNS), d.h. des Gehirns und des Rückenmarks. Bei der MS handelt
Hintergrundinformation MS 10 Fragen und Antworten Was ist MS? Multiple Sklerose (MS) ist eine chronische Erkrankung des Zentralen Nervensystems (ZNS), d.h. des Gehirns und des Rückenmarks. Bei der MS handelt
Patienteninformationsbroschüre Valproat
 Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Patienteninformationsbroschüre Valproat Informationen für Patientinnen Die Informationen in dieser Broschüre sind für Frauen bestimmt, denen Valproat verschrieben wird und die schwanger werden können (Frauen
Neue diagnostische Kriterien. Warum früh diagnostizieren? Wie sicher! - diagnostizieren?
 Neue diagnostische Kriterien Warum früh diagnostizieren? Wie sicher! - diagnostizieren? MS-Forum Buchholz 14.Juni 2008 Warum Früh? chronische Erkrankung bleibende Behinderungen Berufsunfähigkeit Psychische
Neue diagnostische Kriterien Warum früh diagnostizieren? Wie sicher! - diagnostizieren? MS-Forum Buchholz 14.Juni 2008 Warum Früh? chronische Erkrankung bleibende Behinderungen Berufsunfähigkeit Psychische
Was kann man erwarten?
 Neue Therapien der Multiplen Sklerose Was kann man erwarten? Prim. Univ.-Doz. Dr. Christian Eggers Neurologie mit Stroke Unit Krankenhaus der Barmherzigen Brüder Linz Derzeitige Medikamente in der Behandlung
Neue Therapien der Multiplen Sklerose Was kann man erwarten? Prim. Univ.-Doz. Dr. Christian Eggers Neurologie mit Stroke Unit Krankenhaus der Barmherzigen Brüder Linz Derzeitige Medikamente in der Behandlung
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU - Kombination mit Sulfonylharnstoff n
 Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
Indikationserweiterungen für JANUVIA (Sitagliptin, MSD) in der EU Kombination mit Sulfonylharnstoff nun ebenfalls zugelassen Haar (März 2008) - Die europäische Arzneimittelbehörde EMEA hat JANUVIA für
MS-Versorgung eine Herausforderung für die Pharmaindustrie? Birgit Fischer, 24. Juni 2014
 MS-Versorgung eine Herausforderung für die Pharmaindustrie? Birgit Fischer, 24. Juni 2014 Patientenwünsche Quelle: http://www.dmsg.de/wunschwand/ Seite 2 MS-Therapie, aktueller Stand ca. 120.000 Patientinnen
MS-Versorgung eine Herausforderung für die Pharmaindustrie? Birgit Fischer, 24. Juni 2014 Patientenwünsche Quelle: http://www.dmsg.de/wunschwand/ Seite 2 MS-Therapie, aktueller Stand ca. 120.000 Patientinnen
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar?
 Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Dr. med. Jutta Scheiderbauer Seit den 1990er Jahren hat sich etabliert, die schubförmige Multiple Sklerose (MS) mit
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Dr. med. Jutta Scheiderbauer Seit den 1990er Jahren hat sich etabliert, die schubförmige Multiple Sklerose (MS) mit
Intraoperative Strahlentherapie bei Brustkrebs
 Intraoperative Strahlentherapie bei Brustkrebs Uniklinik Köln 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt wird, ist erst einmal die Sorge groß. Beruhigend zu wissen, dass es
Intraoperative Strahlentherapie bei Brustkrebs Uniklinik Köln 1 Kein Grund für Verzweiflung Wenn die Diagnose Brustkrebs festgestellt wird, ist erst einmal die Sorge groß. Beruhigend zu wissen, dass es
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar?
 Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Themen: Übersicht der MS-Immuntherapeutika Off label Medikamente Welche Medikamtente bei welcher Patientensituation?
Welche Immuntherapeutika sind momentan bei schubförmiger Multipler Sklerose verfügbar? Themen: Übersicht der MS-Immuntherapeutika Off label Medikamente Welche Medikamtente bei welcher Patientensituation?
Neue Therapien in der MS
 Neue Therapien in der MS Prof. Dr. Heinz Wiendl Direktor Klinik für Allg. Neurologie Westfälische Wilhelms-Universität Münster Diese Veranstaltung wurde unterstützt von: -Biogen Idec -TEVA Pharma MS: Therapiesituationen
Neue Therapien in der MS Prof. Dr. Heinz Wiendl Direktor Klinik für Allg. Neurologie Westfälische Wilhelms-Universität Münster Diese Veranstaltung wurde unterstützt von: -Biogen Idec -TEVA Pharma MS: Therapiesituationen
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen
 Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
Sumatriptan Antrag auf Freistellung von der Verschreibungspflicht mit Beschränkungen Sachverständigen-Ausschuss für Verschreibungspflicht 62. Sitzung am 13.01.2009 im Bundesinstitut für Arzneimittel- und
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
Diabetes. Zulassungserweiterung: Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Mens
 Zulassungserweiterung Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Menschen mit Typ 2 Diabetes Mainz (16. November 2011) Die Europäische Kommission hat die Zulassung des modernen
Zulassungserweiterung Levemir (Insulin detemir) als Add-on Therapie zu Victoza (Liraglutid) bei Menschen mit Typ 2 Diabetes Mainz (16. November 2011) Die Europäische Kommission hat die Zulassung des modernen
MS und Impfungen. DAS KLEINE IMPF-1x1. DAS KLEINE IMPF-1x1. Christian Lampl. Abteilung für Allgemeine Neurologie und Schmerzmedizin
 MS und Impfungen Christian Lampl Abteilung für Allgemeine Neurologie und Schmerzmedizin DAS KLEINE IMPF-1x1 Impfungen stellen sehr wirksame und wichtige präventivmedizinische Maßnahmen dar. Das unmittelbare
MS und Impfungen Christian Lampl Abteilung für Allgemeine Neurologie und Schmerzmedizin DAS KLEINE IMPF-1x1 Impfungen stellen sehr wirksame und wichtige präventivmedizinische Maßnahmen dar. Das unmittelbare
Osteoporose. Ein echtes Volksleiden. Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen
 Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Osteoporose Osteoporose 9 Osteoporose Ein echtes Volksleiden Schon jetzt zählen die Osteoporose und die damit verbundene erhöhte Brüchigkeit der Knochen in den entwickelten Ländern zu den häufigsten Erkrankungen
Aktuelles zur Therapie der MS
 KLINIKEN LANDKREIS SIGMARINGEN GmbH AKADEMISCHES LEHRKRANKENHAUS DER UNIVERSITÄT TÜBINGEN Aktuelles zur Therapie der MS PD Dr. med. Oliver Neuhaus Chefarzt Abteilung Neurologie Was ist Multiple Sklerose?
KLINIKEN LANDKREIS SIGMARINGEN GmbH AKADEMISCHES LEHRKRANKENHAUS DER UNIVERSITÄT TÜBINGEN Aktuelles zur Therapie der MS PD Dr. med. Oliver Neuhaus Chefarzt Abteilung Neurologie Was ist Multiple Sklerose?
Vorteile der 1x wöchentlichen MS-Basistherapie
 Der Patient im Fokus Vorteile der 1x wöchentlichen MS-Basistherapie Nürnberg (4. Dezember 2012) - In der Behandlung von Patienten mit Multipler Sklerose (MS) ist Interferon beta-1a i.m. (Avonex ) als effektives
Der Patient im Fokus Vorteile der 1x wöchentlichen MS-Basistherapie Nürnberg (4. Dezember 2012) - In der Behandlung von Patienten mit Multipler Sklerose (MS) ist Interferon beta-1a i.m. (Avonex ) als effektives
Behandlung der Multiplen Sklerose durch Inhibition von Adhäsionsmolek. sionsmolekülen len. Dr. Martin Berghoff
 Behandlung der Multiplen Sklerose durch Inhibition von Adhäsionsmolek sionsmolekülen len Dr. Martin Berghoff Immunmodulierende Basistherapie (1) Interferon-β (IFN-β)1b (Betaferon) und 1a (Rebif / Avonex)
Behandlung der Multiplen Sklerose durch Inhibition von Adhäsionsmolek sionsmolekülen len Dr. Martin Berghoff Immunmodulierende Basistherapie (1) Interferon-β (IFN-β)1b (Betaferon) und 1a (Rebif / Avonex)
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
Medikament zur Behandlung der Muskeldystrophie Duchenne jetzt in Deutschland VERFÜGBAR:
 München, den 08.01.2015 Medikament zur Behandlung der Muskeldystrophie Duchenne jetzt in Deutschland VERFÜGBAR: TRANSLARNA TM mit dem Wirkstoff Ataluren Liebe Patienten, liebe Eltern, In einem Schreiben
München, den 08.01.2015 Medikament zur Behandlung der Muskeldystrophie Duchenne jetzt in Deutschland VERFÜGBAR: TRANSLARNA TM mit dem Wirkstoff Ataluren Liebe Patienten, liebe Eltern, In einem Schreiben
10.000 10.000. an Masern erkrankt. an Mumps erkrankt. mit Röteln infiziert
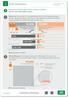 Nutzen: Bei Viruskontakt ist mein geimpftes Kind auch künftig besser gegen Masern, Mumps und Röteln geschützt. Je mehr Menschen geimpft sind, desto unwahrscheinlicher werden Kontakte mit dem Virus. ohne
Nutzen: Bei Viruskontakt ist mein geimpftes Kind auch künftig besser gegen Masern, Mumps und Röteln geschützt. Je mehr Menschen geimpft sind, desto unwahrscheinlicher werden Kontakte mit dem Virus. ohne
BAnz AT 20.11.2014 B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Greater occipital nerve block using local anaesthetics alone or with triamcinolone for transformed migraine: a randomised comparative study
 Greater occipital nerve block using local anaesthetics alone or with triamcinolone for transformed migraine: a randomised comparative study A. Ashkenazi, R. Matro, J.W. Shaw, M.A. Abbas, S.D. Silberstein
Greater occipital nerve block using local anaesthetics alone or with triamcinolone for transformed migraine: a randomised comparative study A. Ashkenazi, R. Matro, J.W. Shaw, M.A. Abbas, S.D. Silberstein
Vor- und Nachteile der Kastration
 Vor- und Nachteile der Kastration Was versteht man unter Kastration? Unter Kastration versteht man die chirugische Entfernung der Keimdrüsen. Bei der Hündin handelt es sich dabei um die Eierstöcke, beim
Vor- und Nachteile der Kastration Was versteht man unter Kastration? Unter Kastration versteht man die chirugische Entfernung der Keimdrüsen. Bei der Hündin handelt es sich dabei um die Eierstöcke, beim
Zulassungserweiterung für den adjuvanten Einsatz von Trastuzumab
 Patientinnen mit frühem HER2-positivem Mammakarzinom individuell behandeln Zulassungserweiterung für den adjuvanten Einsatz von Trastuzumab Grenzach-Wyhlen (25. Mai 2011) - Der Einsatz des monoklonalen
Patientinnen mit frühem HER2-positivem Mammakarzinom individuell behandeln Zulassungserweiterung für den adjuvanten Einsatz von Trastuzumab Grenzach-Wyhlen (25. Mai 2011) - Der Einsatz des monoklonalen
IMMUNTHERAPIE 2017 JETZT AUCH BEI CHRONISCHER MS? Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg
 IMMUNTHERAPIE JETZT AUCH BEI CHRONISCHER MS? Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg MS Therapie H. Houston Merritt The surest way to lose a reputation in neurology is
IMMUNTHERAPIE JETZT AUCH BEI CHRONISCHER MS? Brigitte Wildemann, Neurologische Klinik Universitätsklinikum Heidelberg MS Therapie H. Houston Merritt The surest way to lose a reputation in neurology is
DMSG Kontaktstelle Winsen. Neurologische Abteilung Buchholz
 DMSG Kontaktstelle Winsen Neurologische Abteilung Buchholz 2. Buchholzer MS - Forum Vergleich immunmodulierender Therapien bei der Multiplen Sklerose Ebenen der Behandlung der MS Akute Behandlung der Schübe
DMSG Kontaktstelle Winsen Neurologische Abteilung Buchholz 2. Buchholzer MS - Forum Vergleich immunmodulierender Therapien bei der Multiplen Sklerose Ebenen der Behandlung der MS Akute Behandlung der Schübe
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Viscosan - Augentropfen Wirkstoff: Hypromellose
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Viscosan - Augentropfen Wirkstoff: Hypromellose Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
10 Antworten zum Thema Generika
 10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
10 Antworten zum Thema Generika Die mit dem Regenbogen Liebe Leserin, Lieber Leser Immer mehr Schweizerinnen und Schweizer leiden unter den jährlich steigenden Gesundheitskosten und Krankenkassenprämien.
Multiple Sklerose Aktuelle Behandlungskonzepte. Matthias Bußmeyer Klinik für Neurologie und klinische Neurophysiologie 26.01.2013
 Multiple Sklerose Aktuelle Behandlungskonzepte Matthias Bußmeyer Klinik für Neurologie und klinische Neurophysiologie 26.01.2013 1 Säulen der MS-Therapie Therapie der Multiplen Sklerose Schubtherapie Krankheitsmodifizierende
Multiple Sklerose Aktuelle Behandlungskonzepte Matthias Bußmeyer Klinik für Neurologie und klinische Neurophysiologie 26.01.2013 1 Säulen der MS-Therapie Therapie der Multiplen Sklerose Schubtherapie Krankheitsmodifizierende
Sklerose verlangsamen
 Weniger Schübe, mehr Lebensqualität Frühe Basistherapie kann Krankheitsverlauf der Multiplen Sklerose verlangsamen Hamburg (12. September 2008) - Die Frühtherapie der Multiplen Sklerose war eines der relevanten
Weniger Schübe, mehr Lebensqualität Frühe Basistherapie kann Krankheitsverlauf der Multiplen Sklerose verlangsamen Hamburg (12. September 2008) - Die Frühtherapie der Multiplen Sklerose war eines der relevanten
Trockenes Auge. Haben Sie Trockene Augen?
 Trockenes Auge Jeder 3 bis 5 Patient, der den Augenarzt besucht, an der Krankheit Trockenes Auge leidet. Ein Trockenes Auge entsteht, wenn der Körper zu wenig Tränenflüssigkeit produziert oder die Zusammensetzung
Trockenes Auge Jeder 3 bis 5 Patient, der den Augenarzt besucht, an der Krankheit Trockenes Auge leidet. Ein Trockenes Auge entsteht, wenn der Körper zu wenig Tränenflüssigkeit produziert oder die Zusammensetzung
MS- Multiple Sklerose:
 MS- Multiple Sklerose: Die medizinisch bedeutsamste Funktion von Insulin ist die Senkung des Blutzuckerspiegels. ~ 1 ~ Gliederung: MS- Multiple Sklerose: 1. Was ist Multiple Sklerose? 2. Symptome 3. Der
MS- Multiple Sklerose: Die medizinisch bedeutsamste Funktion von Insulin ist die Senkung des Blutzuckerspiegels. ~ 1 ~ Gliederung: MS- Multiple Sklerose: 1. Was ist Multiple Sklerose? 2. Symptome 3. Der
Kritische Lebensereignisse und Gesundheit im Alter
 Christian Deindl, Universität zu Köln Kritische Lebensereignisse und Gesundheit im Alter DGS Trier, Oktober 2014 Hintergrund Die Geburt eines Kindes Arbeitslosigkeit Auszug aus dem Elternhaus Haben Auswirkungen
Christian Deindl, Universität zu Köln Kritische Lebensereignisse und Gesundheit im Alter DGS Trier, Oktober 2014 Hintergrund Die Geburt eines Kindes Arbeitslosigkeit Auszug aus dem Elternhaus Haben Auswirkungen
Patientenleitfaden für das Gespräch mit dem Arzt. Liebe Patientin, lieber Patient!
 Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
allensbacher berichte
 allensbacher berichte Institut für Demoskopie Allensbach 2006 / Nr. 8 ALTERSVORSORGE THEMA NUMMER 1 Allensbach am Bodensee, Mitte Mai 2006. - Das Thema Altersvorsorge beschäftigt die Bevölkerung immer
allensbacher berichte Institut für Demoskopie Allensbach 2006 / Nr. 8 ALTERSVORSORGE THEMA NUMMER 1 Allensbach am Bodensee, Mitte Mai 2006. - Das Thema Altersvorsorge beschäftigt die Bevölkerung immer
Fremdwährungsanteil bei Tilgungsträgerkrediten bei 86 % eine Analyse der Fremdwährungskreditstatistik 1
 Fremdwährungsanteil bei strägerkrediten bei 86 % eine Analyse der Fremdwährungskreditstatistik 1 Christian Sellner 2 Im europäischen Vergleich ist das Volumen der Fremdwährungskredite in Österreich sehr
Fremdwährungsanteil bei strägerkrediten bei 86 % eine Analyse der Fremdwährungskreditstatistik 1 Christian Sellner 2 Im europäischen Vergleich ist das Volumen der Fremdwährungskredite in Österreich sehr
Angaben zu internationalen/kulturellen Unterschieden beim Placeboeffekt
 1 Angaben zu internationalen/kulturellen Unterschieden beim Placeboeffekt Placebo-Heilungsrate von Magengeschwüren: 7 % in Brasilien und 59 % in Deutschland (Moermann 2000) Placebo-Ansprechrate bei Migräne:
1 Angaben zu internationalen/kulturellen Unterschieden beim Placeboeffekt Placebo-Heilungsrate von Magengeschwüren: 7 % in Brasilien und 59 % in Deutschland (Moermann 2000) Placebo-Ansprechrate bei Migräne:
Antikoagulation 2012: alles anders?
 Antikoagulation 2012: alles anders? Ärztekongress Arosa 24. März 2012 (Etzel Gysling) Neue Antikoagulantien Wo und wofür sind sie aktuell zugelassen? Seit 2011 sind neue Studienresultate und eine neue
Antikoagulation 2012: alles anders? Ärztekongress Arosa 24. März 2012 (Etzel Gysling) Neue Antikoagulantien Wo und wofür sind sie aktuell zugelassen? Seit 2011 sind neue Studienresultate und eine neue
3.9 Brustdrüse der Frau
 ICD-10 C50 Ergebnisse zur 77 3.9 Brustdrüse der Frau Kernaussagen Inzidenz und Mortalität: Die altersstandardisierte Inzidenz von Krebserkrankungen der weiblichen Brustdrüse (Mammakarzinom) ist seit den
ICD-10 C50 Ergebnisse zur 77 3.9 Brustdrüse der Frau Kernaussagen Inzidenz und Mortalität: Die altersstandardisierte Inzidenz von Krebserkrankungen der weiblichen Brustdrüse (Mammakarzinom) ist seit den
Wenn Ihnen etwas auf den Magen schlägt, dann schlagen Sie zurück! Aber fragen Sie vorher besser Ihren Apotheker!
 Wenn Ihnen etwas auf den Magen schlägt, dann schlagen Sie zurück! Aber fragen Sie vorher besser Ihren Apotheker! Selbstmedikation Selbstmedikation ist ein weltweiter Trend Selbstmedikation ist praktisch
Wenn Ihnen etwas auf den Magen schlägt, dann schlagen Sie zurück! Aber fragen Sie vorher besser Ihren Apotheker! Selbstmedikation Selbstmedikation ist ein weltweiter Trend Selbstmedikation ist praktisch
Orale MS Therapien. Ralf Gold Neurologische Klinik St. Josef Hospital, Klinikum der Ruhr-Universität Bochum
 rale MS Therapien Ralf Gold Neurologische Klinik St. Josef Hospital, Klinikum der Ruhr-Universität Bochum Was entwickelt sich in der Pipeline? Neue MS Therapie wird riskant..! rale Therapeutika: welche
rale MS Therapien Ralf Gold Neurologische Klinik St. Josef Hospital, Klinikum der Ruhr-Universität Bochum Was entwickelt sich in der Pipeline? Neue MS Therapie wird riskant..! rale Therapeutika: welche
Die Sicht der EMEA. für Zulassungs-, Therapie- und. Berlin-Brandenburgische Akademie der
 Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Nachgefragt! - Welche Perspektive haben Menschen nach einem schweren Schlaganfall?
 Nachgefragt! - Welche Perspektive haben Menschen nach einem schweren Schlaganfall? Ergebnisse einer Nachbefragung von Patienten ein Jahr nach der Frührehabilitation Die Neurologische Frührehabilitation
Nachgefragt! - Welche Perspektive haben Menschen nach einem schweren Schlaganfall? Ergebnisse einer Nachbefragung von Patienten ein Jahr nach der Frührehabilitation Die Neurologische Frührehabilitation
INFORMATIONEN FÜR TYP-2-DIABETIKER. Warum der HbA 1c -Wert für Sie als Typ-2-Diabetiker so wichtig ist!
 INFORMATIONEN FÜR TYP-2-DIABETIKER Warum der HbA 1c -Wert für Sie als Typ-2-Diabetiker so wichtig ist! Liebe Leserin, lieber Leser, Wer kennt das nicht: Kurz vor dem nächsten Arztbesuch hält man sich besonders
INFORMATIONEN FÜR TYP-2-DIABETIKER Warum der HbA 1c -Wert für Sie als Typ-2-Diabetiker so wichtig ist! Liebe Leserin, lieber Leser, Wer kennt das nicht: Kurz vor dem nächsten Arztbesuch hält man sich besonders
Screening Das Programm. zur Früherkennung von Brustkrebs
 Mammographie Screening Das Programm zur Früherkennung von Brustkrebs das Mammographie Screening Programm Wenn Sie zwischen 50 und 69 Jahre alt sind, haben Sie alle zwei Jahre Anspruch auf eine Mammographie-Untersuchung
Mammographie Screening Das Programm zur Früherkennung von Brustkrebs das Mammographie Screening Programm Wenn Sie zwischen 50 und 69 Jahre alt sind, haben Sie alle zwei Jahre Anspruch auf eine Mammographie-Untersuchung
» Ihre Bedürfnisse stehen im Mittelpunkt» Alle Fachdisziplinen in einem Haus» Medizinische Diagnostik & Therapie wissenschaftlich fundiert
 » Ihre Bedürfnisse stehen im Mittelpunkt» Alle Fachdisziplinen in einem Haus» Medizinische Diagnostik & Therapie wissenschaftlich fundiert » PAN Prevention Center Prof. Dr. med. C. A. Schneider Ärztlicher
» Ihre Bedürfnisse stehen im Mittelpunkt» Alle Fachdisziplinen in einem Haus» Medizinische Diagnostik & Therapie wissenschaftlich fundiert » PAN Prevention Center Prof. Dr. med. C. A. Schneider Ärztlicher
Hautkrebsscreening. 49 Prozent meinen, Hautkrebs sei kein Thema, das sie besorgt. Thema Hautkrebs. Ist Hautkrebs für Sie ein Thema, das Sie besorgt?
 Hautkrebsscreening Datenbasis: 1.004 gesetzlich Krankenversicherte ab 1 Jahren Erhebungszeitraum:. bis 4. April 01 statistische Fehlertoleranz: +/- Prozentpunkte Auftraggeber: DDG Hautkrebs ist ein Thema,
Hautkrebsscreening Datenbasis: 1.004 gesetzlich Krankenversicherte ab 1 Jahren Erhebungszeitraum:. bis 4. April 01 statistische Fehlertoleranz: +/- Prozentpunkte Auftraggeber: DDG Hautkrebs ist ein Thema,
Die Post hat eine Umfrage gemacht
 Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
Die Post hat eine Umfrage gemacht Bei der Umfrage ging es um das Thema: Inklusion Die Post hat Menschen mit Behinderung und Menschen ohne Behinderung gefragt: Wie zufrieden sie in dieser Gesellschaft sind.
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Legalon SIL - Trockensubstanz zur Infusionsbereitung
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Legalon SIL - Trockensubstanz zur Infusionsbereitung Wirkstoff: Silibinin-C-2,3-bis(hydrogensuccinat), Dinatriumsalz Lesen Sie die gesamte
Leseauszug DGQ-Band 14-26
 Leseauszug DGQ-Band 14-26 Einleitung Dieser Band liefert einen Ansatz zur Einführung von Prozessmanagement in kleinen und mittleren Organisationen (KMO) 1. Die Erfolgskriterien für eine Einführung werden
Leseauszug DGQ-Band 14-26 Einleitung Dieser Band liefert einen Ansatz zur Einführung von Prozessmanagement in kleinen und mittleren Organisationen (KMO) 1. Die Erfolgskriterien für eine Einführung werden
Minimale Resterkrankung, Hochdurchsatz-Sequenzierung und Prognose beim multiplen Myelom
 Minimale Resterkrankung, Hochdurchsatz-Sequenzierung und Prognose beim multiplen Myelom Von Navneet Ramesh und Maike Haehle, übersetzt von Sabine Schock Vom 8. Apr 2014 7:41 Uhr; aktualisiert am 8. Apr
Minimale Resterkrankung, Hochdurchsatz-Sequenzierung und Prognose beim multiplen Myelom Von Navneet Ramesh und Maike Haehle, übersetzt von Sabine Schock Vom 8. Apr 2014 7:41 Uhr; aktualisiert am 8. Apr
Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn
 An die Redaktionen von Presse, Funk und Fernsehen 32 02. 09. 2002 Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn Das aktive Sparen ist nach wie vor die wichtigste Einflussgröße
An die Redaktionen von Presse, Funk und Fernsehen 32 02. 09. 2002 Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn Das aktive Sparen ist nach wie vor die wichtigste Einflussgröße
Cytomegalie & Co. Häufige Virusinfektionen in der Schwangerschaft. Deutsches Grünes Kreuz e.v.
 Cytomegalie & Co Häufige Virusinfektionen in der Schwangerschaft Schwangerschaft Eine ganz besondere Zeit der Vorfreude Verantwortung Sorge Die werdenden Eltern möchten alles richtig machen für das Wohl
Cytomegalie & Co Häufige Virusinfektionen in der Schwangerschaft Schwangerschaft Eine ganz besondere Zeit der Vorfreude Verantwortung Sorge Die werdenden Eltern möchten alles richtig machen für das Wohl
Genetisch... Unterschied. DNA zu... 99,9% identisch
 Genetisch... Unterschied DNA zu... 99,9% identisch Alle Menschen unterscheiden sich aus genetischer Sicht nur um 0,1% Die übrigen 99,9% sind exakt gleich, egal ob miteinander verwandt oder nicht. Diese
Genetisch... Unterschied DNA zu... 99,9% identisch Alle Menschen unterscheiden sich aus genetischer Sicht nur um 0,1% Die übrigen 99,9% sind exakt gleich, egal ob miteinander verwandt oder nicht. Diese
Sicherheitsrundgänge mit Führungskräften, Sicherheitsklima und Risikoreduktion
 Sicherheitsrundgänge mit Führungskräften, Sicherheitsklima und Risikoreduktion René Schwendimann, PhD, RN Internationaler Kongress - Patientensicherheit - avanti! Stiftung für Patientensicherheit Schweiz
Sicherheitsrundgänge mit Führungskräften, Sicherheitsklima und Risikoreduktion René Schwendimann, PhD, RN Internationaler Kongress - Patientensicherheit - avanti! Stiftung für Patientensicherheit Schweiz
Stammzellen-Konzepte.com
 Arthrose bei Hunden mit Stammzellen behandeln 6 Gründe, die bei Hunde-Arthrose für eine Stammzellen-Therapie sprechen. Tierarzt finden auf Hunde-Arthrose mit Stammzellentherapie erfolgreich behandeln:
Arthrose bei Hunden mit Stammzellen behandeln 6 Gründe, die bei Hunde-Arthrose für eine Stammzellen-Therapie sprechen. Tierarzt finden auf Hunde-Arthrose mit Stammzellentherapie erfolgreich behandeln:
Labortests für Ihre Gesundheit. Therapie nach Maß 26
 Labortests für Ihre Gesundheit Therapie nach Maß 26 01IPF Labortests für Ihre Gesundheit Therapie nach Maß Die individuelle Dosis finden Jeder Mensch ist einzigartig. Keiner gleicht dem anderen nicht nur
Labortests für Ihre Gesundheit Therapie nach Maß 26 01IPF Labortests für Ihre Gesundheit Therapie nach Maß Die individuelle Dosis finden Jeder Mensch ist einzigartig. Keiner gleicht dem anderen nicht nur
Moderne MRT-Bildauswertung mit appmri Hippocampus Volume Analyser.
 APPMRI HIPPOCAMPUS VOLUME Moderne MRT-Bildauswertung mit appmri Hippocampus Volume Analyser. Quantitative und zuverlässige Informationen zur Unterstützung bei der Diagnose von Alzheimer Unser Schwerpunkt
APPMRI HIPPOCAMPUS VOLUME Moderne MRT-Bildauswertung mit appmri Hippocampus Volume Analyser. Quantitative und zuverlässige Informationen zur Unterstützung bei der Diagnose von Alzheimer Unser Schwerpunkt
Fragebogen: Abschlussbefragung
 Fragebogen: Abschlussbefragung Vielen Dank, dass Sie die Ameise - Schulung durchgeführt haben. Abschließend möchten wir Ihnen noch einige Fragen zu Ihrer subjektiven Einschätzung unseres Simulationssystems,
Fragebogen: Abschlussbefragung Vielen Dank, dass Sie die Ameise - Schulung durchgeführt haben. Abschließend möchten wir Ihnen noch einige Fragen zu Ihrer subjektiven Einschätzung unseres Simulationssystems,
SCHÖNE ZÄHNE. Lebensqualität mit Zahnimplantaten 1
 SCHÖNE ZÄHNE Lebensqualität mit Zahnimplantaten 1 1 Lebensqualität mit Zahnimplantaten bezieht sich auf eine höhere Lebensqualität mit einem Zahnimplantat im Vergleich zu keiner Behandlung. Awad M.A et
SCHÖNE ZÄHNE Lebensqualität mit Zahnimplantaten 1 1 Lebensqualität mit Zahnimplantaten bezieht sich auf eine höhere Lebensqualität mit einem Zahnimplantat im Vergleich zu keiner Behandlung. Awad M.A et
Informationen zum Thema Europäische Krankenversicherungskarte
 Gesundheitskarte AKTUELL Informationen zum Thema Europäische Krankenversicherungskarte Von Anfang an ist die Rückseite der elektronischen Gesundheitskarte für die Aufnahme der Europäischen Krankenversicherungskarte
Gesundheitskarte AKTUELL Informationen zum Thema Europäische Krankenversicherungskarte Von Anfang an ist die Rückseite der elektronischen Gesundheitskarte für die Aufnahme der Europäischen Krankenversicherungskarte
Eine Autoimmunerkrankung kommt selten allein was tun wenn Diabetes und Co zusammentreffen. Dr.oec.troph. Astrid Tombek
 Eine Autoimmunerkrankung kommt selten allein was tun wenn Diabetes und Co zusammentreffen Dr.oec.troph. Astrid Tombek Pathophysiologie Autoimmunerkrankungen Def.: ein Überbegriff für Krankheiten, deren
Eine Autoimmunerkrankung kommt selten allein was tun wenn Diabetes und Co zusammentreffen Dr.oec.troph. Astrid Tombek Pathophysiologie Autoimmunerkrankungen Def.: ein Überbegriff für Krankheiten, deren
Diabetische Netzhauterkrankung
 Diabetes und Auge Diabetische Netzhauterkrankung Die diabetische Retinopathie ist die häufigste Erblindungsursache in der Bevölkerung zwischen dem 30. und 65. Lebensjahren in der westlichen Welt. Das Auftreten
Diabetes und Auge Diabetische Netzhauterkrankung Die diabetische Retinopathie ist die häufigste Erblindungsursache in der Bevölkerung zwischen dem 30. und 65. Lebensjahren in der westlichen Welt. Das Auftreten
Tutorial: Homogenitätstest
 Tutorial: Homogenitätstest Eine Bank möchte die Kreditwürdigkeit potenzieller Kreditnehmer abschätzen. Einerseits lebt die Bank ja von der Vergabe von Krediten, andererseits verursachen Problemkredite
Tutorial: Homogenitätstest Eine Bank möchte die Kreditwürdigkeit potenzieller Kreditnehmer abschätzen. Einerseits lebt die Bank ja von der Vergabe von Krediten, andererseits verursachen Problemkredite
Sandoz Pharmaceuticals AG
 Die Pille danach. Was ist eine Notfallverhütung oder die sogenannte «Pille danach»? 1 Wann wird NorLevo Uno eingenommen? 2 Bei der «Pille danach» handelt es sich um eine Notfallverhütung, die eine unerwünschte
Die Pille danach. Was ist eine Notfallverhütung oder die sogenannte «Pille danach»? 1 Wann wird NorLevo Uno eingenommen? 2 Bei der «Pille danach» handelt es sich um eine Notfallverhütung, die eine unerwünschte
1. Pharmaindustrie allgemein. 2. Das Pharmaunternehmen GlaxoSmithKline. Autoren: Anke Jakubzik Tobias Bräutigam
 Unternehmen als internationale Akteure 1. Pharmaindustrie allgemein 2. Das Pharmaunternehmen GlaxoSmithKline Autoren: Anke Jakubzik Tobias Bräutigam Pharmaindustrie allgemein! ein Teil der chemischen Industrie,
Unternehmen als internationale Akteure 1. Pharmaindustrie allgemein 2. Das Pharmaunternehmen GlaxoSmithKline Autoren: Anke Jakubzik Tobias Bräutigam Pharmaindustrie allgemein! ein Teil der chemischen Industrie,
Verbesserung der Validität der Messung der Tiefe approximaler Karies auf Röntgenbildern durch digitale Bearbeitung
 Sophia Viktoria Adzoa Seneadza Dr. med. dent. Verbesserung der Validität der Messung der Tiefe approximaler Karies auf Röntgenbildern durch digitale Bearbeitung Geboren am 08.03.1971 in Heidelberg Staatsexamen
Sophia Viktoria Adzoa Seneadza Dr. med. dent. Verbesserung der Validität der Messung der Tiefe approximaler Karies auf Röntgenbildern durch digitale Bearbeitung Geboren am 08.03.1971 in Heidelberg Staatsexamen
Entwicklung des Kreditvolumens an Nichtbanken im Euroraum
 Entwicklung des Kreditvolumens an Nichtbanken im Die durchschnittliche Jahreswachstumsrate des Kreditvolumens an Nichtbanken im lag im Jahr 27 noch deutlich über 1 % und fiel in der Folge bis auf,8 % im
Entwicklung des Kreditvolumens an Nichtbanken im Die durchschnittliche Jahreswachstumsrate des Kreditvolumens an Nichtbanken im lag im Jahr 27 noch deutlich über 1 % und fiel in der Folge bis auf,8 % im
Auswertung des Fragebogens zum CO2-Fußabdruck
 Auswertung des Fragebogens zum CO2-Fußabdruck Um Ähnlichkeiten und Unterschiede im CO2-Verbrauch zwischen unseren Ländern zu untersuchen, haben wir eine Online-Umfrage zum CO2- Fußabdruck durchgeführt.
Auswertung des Fragebogens zum CO2-Fußabdruck Um Ähnlichkeiten und Unterschiede im CO2-Verbrauch zwischen unseren Ländern zu untersuchen, haben wir eine Online-Umfrage zum CO2- Fußabdruck durchgeführt.
Weltweite Wanderschaft
 Endversion nach dem capito Qualitäts-Standard für Leicht Lesen Weltweite Wanderschaft Migration bedeutet Wanderung über große Entfernungen hinweg, vor allem von einem Wohnort zum anderen. Sehr oft ist
Endversion nach dem capito Qualitäts-Standard für Leicht Lesen Weltweite Wanderschaft Migration bedeutet Wanderung über große Entfernungen hinweg, vor allem von einem Wohnort zum anderen. Sehr oft ist
WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE
 WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE Nabelschnurblut ist wertvoll! Wenn sich Eltern dafür entscheiden, das Nabelschnurblut ihres Kindes aufzubewahren, können sie damit dem Kind selbst,
WEGWEISER ZUR EINLAGERUNG VON NABELSCHNURBLUT UND -GEWEBE Nabelschnurblut ist wertvoll! Wenn sich Eltern dafür entscheiden, das Nabelschnurblut ihres Kindes aufzubewahren, können sie damit dem Kind selbst,
Osteoporose, Spondylarthropathien
 KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Osteoporose, Spondylarthropathien Dr. med. Nadine Schneider Teriparatid oder Alendronat bei Glukokortikoidinduzierter Osteoporose? (Saag et al. NEJM 2007; 357:2028-39)
KLINIK UND POLIKLINIK FÜR INNERE MEDIZIN I Osteoporose, Spondylarthropathien Dr. med. Nadine Schneider Teriparatid oder Alendronat bei Glukokortikoidinduzierter Osteoporose? (Saag et al. NEJM 2007; 357:2028-39)
Merck beantragt Zulassung in den USA für Cladribin-Tabletten als mögliche orale Kurzzeitbehandlung der Multiplen Sklerose
 Merck beantragt Zulassung in den USA für Cladribin-Tabletten als mögliche orale Kurzzeitbehandlung der Multiplen Sklerose Darmstadt (30. September 2009) - Die Merck KGaA hat heute bekannt gegeben, dass
Merck beantragt Zulassung in den USA für Cladribin-Tabletten als mögliche orale Kurzzeitbehandlung der Multiplen Sklerose Darmstadt (30. September 2009) - Die Merck KGaA hat heute bekannt gegeben, dass
Die HIT ist keine Allergie! Da die von ihr ausgelösten. Krankheitsbild. Was ist eine Histamin- Intoleranz?
 Was ist eine Histamin- Intoleranz? Die Histamin-Intoleranz ist eine Pseudoallergie. Die HIT ist keine Allergie! Da die von ihr ausgelösten Gesundheitsstörungen jedoch von allergiebedingten Beschwerden
Was ist eine Histamin- Intoleranz? Die Histamin-Intoleranz ist eine Pseudoallergie. Die HIT ist keine Allergie! Da die von ihr ausgelösten Gesundheitsstörungen jedoch von allergiebedingten Beschwerden
HAFTUNG AUS FEHLERHAFTEN GUTACHTEN
 HAFTUNG AUS FEHLERHAFTEN GUTACHTEN Fortbildungsveranstaltung des Bundesverbandes unabhängiger Pflegesachverständiger, 22.02.2014, Lübeck Dr. Roland Uphoff, M.mel. Fachanwalt für Medizinrecht 839a BGB Haftung
HAFTUNG AUS FEHLERHAFTEN GUTACHTEN Fortbildungsveranstaltung des Bundesverbandes unabhängiger Pflegesachverständiger, 22.02.2014, Lübeck Dr. Roland Uphoff, M.mel. Fachanwalt für Medizinrecht 839a BGB Haftung
Die Online-Meetings bei den Anonymen Alkoholikern. zum Thema. Online - Meetings. Eine neue Form der Selbsthilfe?
 Die Online-Meetings bei den Anonymen Alkoholikern zum Thema Online - Meetings Eine neue Form der Selbsthilfe? Informationsverhalten von jungen Menschen (Quelle: FAZ.NET vom 2.7.2010). Erfahrungen können
Die Online-Meetings bei den Anonymen Alkoholikern zum Thema Online - Meetings Eine neue Form der Selbsthilfe? Informationsverhalten von jungen Menschen (Quelle: FAZ.NET vom 2.7.2010). Erfahrungen können
Bericht über die Untersuchung zur Erblichkeit von Herzerkrankungen beim PON
 1 Bericht über die Untersuchung zur Erblichkeit von Herzerkrankungen beim PON Einleitung Bei der Rasse PON wurden im APH in der letzten Zeit auffällig viele Herzkrankheiten und Herzveränderungen unterschiedlicher
1 Bericht über die Untersuchung zur Erblichkeit von Herzerkrankungen beim PON Einleitung Bei der Rasse PON wurden im APH in der letzten Zeit auffällig viele Herzkrankheiten und Herzveränderungen unterschiedlicher
Bevölkerung mit Migrationshintergrund an der Gesamtbevölkerung 2012
 Statistische Übersicht inkl. dem Vergleich zwischen und zur (Aus-)Bildungssituation von jungen Menschen mit und ohne Migrationshintergrund 1 in den Bundesländern nach dem Mikrozensus Erstellt im Rahmen
Statistische Übersicht inkl. dem Vergleich zwischen und zur (Aus-)Bildungssituation von jungen Menschen mit und ohne Migrationshintergrund 1 in den Bundesländern nach dem Mikrozensus Erstellt im Rahmen
Patientenverfügung. Was versteht man genau unter einer Patientenverfügung? Meine persönliche Patientenverfügung
 Patientenverfügung Erarbeitet vom Klinischen Ethikkomitee im Klinikum Herford. Im Komitee sind sowohl Ärzte als auch Mitarbeitende der Pflegedienste, Theologen und ein Jurist vertreten. Der Text entspricht
Patientenverfügung Erarbeitet vom Klinischen Ethikkomitee im Klinikum Herford. Im Komitee sind sowohl Ärzte als auch Mitarbeitende der Pflegedienste, Theologen und ein Jurist vertreten. Der Text entspricht
RSV. RSV kennen. Das Virus, das Eltern kennen sollten. Informationen. Kinder schützen
 RSV kennen Kinder schützen RSV Das Virus, das Eltern kennen sollten. Informationen zu einem wenig bekannten Virus sowie praktische Ratschläge, wie Sie das Risiko einer RSV-Infektion verringern können.
RSV kennen Kinder schützen RSV Das Virus, das Eltern kennen sollten. Informationen zu einem wenig bekannten Virus sowie praktische Ratschläge, wie Sie das Risiko einer RSV-Infektion verringern können.
KOPIE. Diabetes in Kürze. «Schritt um Schritt zu mehr Gesundheit!»
 Diabetes in Kürze «Schritt um Schritt zu mehr Gesundheit!» Schweizerische Diabetes-Gesellschaft Association Suisse du Diabète Associazione Svizzera per il Diabete Was ist Diabetes? Es gibt 2 Typen von
Diabetes in Kürze «Schritt um Schritt zu mehr Gesundheit!» Schweizerische Diabetes-Gesellschaft Association Suisse du Diabète Associazione Svizzera per il Diabete Was ist Diabetes? Es gibt 2 Typen von
Europäischer Fonds für Regionale Entwicklung: EFRE im Bundes-Land Brandenburg vom Jahr 2014 bis für das Jahr 2020 in Leichter Sprache
 Für Ihre Zukunft! Europäischer Fonds für Regionale Entwicklung: EFRE im Bundes-Land Brandenburg vom Jahr 2014 bis für das Jahr 2020 in Leichter Sprache 1 Europäischer Fonds für Regionale Entwicklung: EFRE
Für Ihre Zukunft! Europäischer Fonds für Regionale Entwicklung: EFRE im Bundes-Land Brandenburg vom Jahr 2014 bis für das Jahr 2020 in Leichter Sprache 1 Europäischer Fonds für Regionale Entwicklung: EFRE
Erfolg und Vermögensrückgänge angefertigt im Rahmen der Lehrveranstaltung Nachrichtentechnik von: Eric Hansen, eric-hansen@gmx.de am: 07.09.
 Abstract zum Thema Handelssysteme Erfolg und Vermögensrückgänge angefertigt im Rahmen der Lehrveranstaltung Nachrichtentechnik von: Eric Hansen, eric-hansen@gmx.de am: 07.09.01 Einleitung: Handelssysteme
Abstract zum Thema Handelssysteme Erfolg und Vermögensrückgänge angefertigt im Rahmen der Lehrveranstaltung Nachrichtentechnik von: Eric Hansen, eric-hansen@gmx.de am: 07.09.01 Einleitung: Handelssysteme
Implantate Anwendung in unserer Praxis
 PRAXIS DR. MED. DENT. SIEGFRIED MASLO, AUF DEM KLÜTERORT 20, 27798 HUDE Anwendung in unserer Praxis 20, 27798 Hude Seite 1 Lust auf schöne und natürliche Zähne? kommen der natürlichen Optik am nächsten.
PRAXIS DR. MED. DENT. SIEGFRIED MASLO, AUF DEM KLÜTERORT 20, 27798 HUDE Anwendung in unserer Praxis 20, 27798 Hude Seite 1 Lust auf schöne und natürliche Zähne? kommen der natürlichen Optik am nächsten.
Ziele der Hepatitis C-Therapie
 Behandlung der Hepatitis C Zur Behandlung der Hepatitis C stehen heute neben pegyliertem Interferon alfa (PEG-INF) und Ribavirin auch Proteaseinhibitoren (direkt antiviral wirksame Substanzen) zur Verfügung.
Behandlung der Hepatitis C Zur Behandlung der Hepatitis C stehen heute neben pegyliertem Interferon alfa (PEG-INF) und Ribavirin auch Proteaseinhibitoren (direkt antiviral wirksame Substanzen) zur Verfügung.
geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Gehen wir einmal davon aus, dass die von uns angenommenen
 geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Vollständigkeit halber aufgeführt. Gehen wir einmal davon aus, dass die von uns angenommenen 70% im Beispiel exakt berechnet sind. Was würde
geben. Die Wahrscheinlichkeit von 100% ist hier demnach nur der Vollständigkeit halber aufgeführt. Gehen wir einmal davon aus, dass die von uns angenommenen 70% im Beispiel exakt berechnet sind. Was würde
