1 Skelettformeln zeichnen
|
|
|
- Jürgen Siegel
- vor 7 Jahren
- Abrufe
Transkript
1 19 1 Skelettformeln zeichnen In diesem Kapitel lernen Sie die wichtigste Kurzschrift der Organischen Chemie kennen erspart Ihnen das Periodensystem die Zählerei lernen Sie charakteristische Strukturen kennen, die Ihnen das Leben noch weiter vereinfachen Um Ihren Kurs über Organische Chemie zubestehen, müssen Sie zunächst lernen, die Zeichnungen zuinterpretieren, die inder Organischen Chemie üblich sind. Wenn Sie die Darstellung eines Moleküls sehen, ist esunabdingbar, dass Sie sämtliche darin enthaltenen Informationen entschlüsseln können. Ohne diese Fähigkeit ist es nahezu unmöglich, auch nur die einfachsten Reaktionen und Zusammenhänge zu verstehen. Moleküle können auf verschiedene Art und Weise gezeichnet werden. Unten sehen Sie zum Beispiel drei dieser Möglichkeiten, ein und dasselbe Molekül zu Papier zu bringen: Zweifellos lässt sich die rechte Struktur (Skelettformel) am schnellsten zeichnen, überschauen und in Informationen übersetzen. Wenn Sie eine beliebige Seite inder zweiten Hälfte dieses Buches aufschlagen, werden Sie feststellen, dass nahezu jede Seite mit solchen Skelettformeln übersät ist. Die meisten Studenten werden rasch mit diesen Formeln vertraut und sind sich dabei dennoch nicht bewusst, wie absolut wichtig es ist, diese Darstellungen flüssig lesen zukönnen. Dieses Kapitel soll Ihnen dabei helfen, Ihre Fähigkeiten im schnellen und flüssigen Lesen dieser Abbildungen zuentwickeln. Skelettformelnlesen Skelettformeln zeigen das Kohlenstoffgerüst (die Verbindungen aller Kohlenstoffatome, die das Rückgrat oder Skelett des Moleküls bilden) mit allen an-
2 20 1 Skelettformeln zeichnen hängenden funktionellen Gruppen wie zum Beispiel -OH oder -Br. Einfache Bindungslinien werden dabei in Zickzackform gezeichnet, wobei jede Ecke zwischen zwei Linien und jeder Endpunkt einer Linie ein Kohlenstoffatom markiert. Die folgende Verbindung besteht zum Beispiel aus 7Kohlenstoffatomen: Dabei wird häufig vergessen, dass auch die Enden jeder Linie für jeweils ein Kohlenstoffatom stehen. Das folgende Molekül hat zum Beispiel 6Kohlenstoffatome (vergewissern Sie sich, dass Sie alle zählen können): Doppelbindungen werden durch zwei parallele Linien dargestellt, Dreifachbindungen entsprechend durch drei parallele Linien: Vergewissern Sie sich beim Zeichnen von Dreifachbindungen, dass Sie sie in einer geraden Linie und nicht im Zickzack zeichnen, da Dreifachbindungen linear sind (mehr zu diesem Thema finden Sie im Kapitel über Geometrie). Das erscheint auf den ersten Blick recht verwirrend, da es Ihnen soein wenig erschwert wird, die Anzahl der Kohlenstoffatome ineiner Dreifachbindung zu überblicken. Schauen wir uns die Sache also einmal näher an: Häufig sieht man eine kleine Lücke auf jeder Seite einer Dreifachbindung, etwa so: Die beiden obigen Zeichnungen werden häufig verwendet. Sie sollten Ihre Augen schulen, Dreifachbindungen injeder dieser beiden Darstellungsweisen zuerkennen. Lassen Sie sich von Dreifachbindungen nicht verwirren.
3 Skelettformeln lesen 21 Die beiden Kohlenstoffatome einer Dreifachbindung und die anjeder Seite daran anschließenden Kohlenstoffatome werden als gerade Linie dargestellt. Alle anderen Bindungen jedoch werden inzickzackform gezeichnet: BEISPIEL Zählen Sie die Kohlenstoffatome injeder der folgenden Darstellungen: Lösung Die erste Verbindung hat sechs Kohlenstoffatome, die zweite Verbindung hat 5Kohlenstoffatome. Aufgaben Zählen Sie die Kohlenstoffatome injeder der folgenden Zeichnungen
4 22 1 Skelettformeln zeichnen Da wir jetzt wissen, wie man Kohlenstoffatome zählt, müssen wir nun lernen, wie man die Anzahl der Wasserstoffatome in der Skelettformel eines Moleküls bestimmt. Da die meisten Wasserstoffatome nicht dargestellt werden, lassen sich Skelettformeln sehr rasch zeichnen. Wasserstoffatome, die anandere Atome als Kohlenstoffatome gebunden sind (wie beispielsweise Stickstoff oder Sauerstoff) müssen jedoch immer dargestellt werden: Wasserstoffatome, die ankohlenstoffatome gebunden sind, werden meist nicht dargestellt. Mit der folgenden Regel können Sie die Anzahl der Wasserstoffatome pro Kohlenstoffatom bestimmen: neutrale Kohlenstoffatome gehen
5 Skelettformeln lesen 23 insgesamt vier Bindungen ein. Inder folgenden Abbildung sehen Sie, dass das hervorgehobene Kohlestoffatom nur zwei Bindungslinien besitzt: Das legt nahe, dass noch zwei weitere Bindungen existieren, die zujeweils einem Wasserstoffatom führen (damit der Kohlenstoff insgesamt vier Bindungen eingeht). Dadurch können wir uns das Zeichnen der Wasserstoffatome und somit viel Zeit beim Darstellen von Molekülen sparen. Es wird einfach davon ausgegangen, dass eine Durchschnittsperson in der Lage ist, bis vier zuzählen und dadurch die Anzahl der Wasserstoffatome ineinem Molekül bestimmen kann, auch wenn nicht alle ausdrücklich dargestellt sind. Sie müssen also nur die Bindungslinien zählen, die von jedem Kohlenstoffatom abgehen und dann genügend Wasserstoffatome hinzu addieren, um die vier Bindungen des Kohlenstoffatoms zuvervollständigen. Wenn Sie das viele Male geübt haben, werden Sie den Punkt erreichen, andem Sie nicht einmal mehr zählen müssen. Sie werden einfach so versiert im Betrachten dieser Zeichnungen sein, dass Sie die Anzahl Wasserstoffatome sofort»überblicken«. Wenden wir uns jetzt ein paar Übungen zu, die Ihnen helfen, diesen Punkt zu erreichen. BEISPIEL Das folgende Molekül hat neun Kohlenstoffatome. Bestimmen Sie die Anzahl der Wasserstoffatome, die an jedes einzelne Kohlenstoffatom gebunden sind.
6 24 1 Skelettformeln zeichnen Aufgaben Bestimmen Sie bei jedem der folgenden Moleküle die Anzahl der Wasserstoffatome, die anjedes einzelne Kohlenstoffatom gebunden sind. Die erste Aufgabe wurde bereits für Sie gelöst (die Zahlen stehen für die jeweilige Anzahl der Wasserstoffatome pro Kohlenstoffatom)
7 Skelettformeln zeichnen 25 Jetzt verstehen Sie bestimmt, warum sich soviel Zeit sparen lässt, wenn Moleküle in der Skelettformel gezeichnet werden. Natürlich geht es schneller, wenn nicht jedes einzelne Cund Hdargestellt werden muss. Aber diese Zeichnungen haben einen noch größeren Vorteil: Sie sind nicht nur leichter darzustellen sondern auch leichter zu lesen. Betrachten Sie dazu die folgende Reaktion als Beispiel: In dieser Form ist es etwas schwierig zuerkennen, was genau bei dieser Reaktion passiert. Wahrscheinlich müssen Sie erst ein Weilchen darauf starren, um die Veränderungen nachvollziehen zu können. Wenn wir diese Reaktion jedoch mithilfe von Skelettformeln darstellen, wird die Reaktion sofort viel leichter lesbar: Sobald Sie die Reaktion sehen, wissen Sie sofort, was passiert: Eine Doppelbindung wird in eine Einfachbindung verwandelt, indem andie Kohlenstoffe der Doppelbindung zwei Wasserstoffatome hinzugefügt (»addiert«) werden. Sobald Sie mit dem Lesen dieser Darstellungen einmal vertraut sind, werden Sie die Veränderungen im Verlauf einer Reaktion viel schneller erkennen. Skelettformelnzeichnen Da Sie jetzt wissen, wie Skelettformeln zu lesen sind, müssen Sie nun noch lernen, wie man sie selber zeichnet. Nehmen wir dazu das folgende Molekül als Beispiel:
8 26 1 Skelettformeln zeichnen Um dieses Molekül in der Skelettformel darzustellen, müssen Sie sich zunächst auf das Kohlenstoffgerüst konzentrieren und dann alle anderen Atome außer Cund Heinzeichnen. Sämtliche Atome, die nicht Coder H sind, müssen dargestellt werden. Das obige Beispiel würde dann so aussehen: Die folgenden Hinweise werden Ihnen beim Lösen weiterer Aufgaben helfen. Tipp Denken Sie daran, dass Kohlenstoffatome in einer geraden Kette, die über Einfachbindungen miteinander verbunden sind, in Zickzackform dargestellt werden: 1. Versuchen Sie beim Zeichnen einer Doppelbindung die anderen Bindungen so weit wie möglich von dieser entfernt zuplatzieren: 2. Beim Zeichnen von Zickzacklinien ist es egal, von welcher Seite Sie beginnen und inwelche Richtung die Kette fortgesetzt wird: AUFGABEN Zeichnen Sie die Skelettformel für jede der folgenden Verbindungen in den daneben stehenden Kasten.
9 Fehler vermeiden Fehler vermeiden Warnung 1. Zeichnen Sie niemals ein Kohlenstoffatom mit mehr als vier Bindungen. Das ist ein großer Fehler. Kohlenstoffatome besitzen nur vier Orbitale; daher können Kohlenstoffatome nur vier Bindungen ausbilden (Bindungen entstehen, wenn Orbitale eines Atoms mit Orbitalen
10 28 1 Skelettformeln zeichnen eines anderen Atoms überlappen). Dies gilt für alle Elemente der zweiten Reihe des Periodensystems (der»zweiten Periode«). ImKapitel über das Zeichnen von Resonanzstrukturen werden wir auf dieses Thema ausführlicher eingehen. 2. Beim Zeichnen eines Moleküls sollten Sie entweder alle C- und H-Atome darstellen oder aber die Skelettformel verwenden, in der Cund Hnicht eingezeichnet werden. Sie dürfen jedoch nicht die C-Atome zeichnen und gleichzeitig die H-Atome weglassen: Diese Zeichnung ist nicht korrekt. Lassen Sie also (bevorzugt) entweder die C s weg oder fügen Sie die H smit ein. 3. Wenn Sie jedes Kohlenstoffatom in einer Zickzacklinie zeichnen, richten Sie alle Bindungsarme so weit voneinander entfernt wie möglich aus: Weitere Übungen Schauen Sie sich jetzt die folgende Reaktion anund versuchen Sie nachzuvollziehen, welche Veränderungen dabei stattfinden: Dabei ist es zunächst einmal egal, wie es zu diesen Veränderungen kommt. Das werden Sie später verstehen, wenn Sie Reaktionsmechanismen kennenlernen. Konzentrieren Sie sich also fürs Erste ganz auf die Erklärung, was eigentlich geschieht. Für den Fall des obigen Beispiels können wir sagen, dass
11 Weitere Übungen 29 zwei Wasserstoffatome an das Molekül addiert werden (eines an jedes Ende der Doppelbindung). Betrachten Sie ein anderes Beispiel: In diesem Beispiel eliminieren wir ein Hund ein Br, um eine Doppelbindung zu erzeugen. Wenn Sie nicht sofort erkennen können, dass ein Hentfernt wurde, müssen Sie die Gesamtzahl der Wasserstoffatome imausgangsmolekül ermitteln und diese mit der Anzahl der H-Atome im Reaktionsprodukt vergleichen: Betrachten Sie nun noch ein Beispiel: In diesem Beispiel substituieren (ersetzen) wir ein Brom- durch ein Chloratom. Aufgaben Geben Sie für jede der folgenden Reaktionen die entsprechende Veränderung deutlich an. Injedem Fall sollte Ihre Antwort wie einer der folgenden Sätze klingen: XY wird/werden addiert., XY wird/werden eliminiert. oder XY wird/werden substituiert. 1.23
12 30 1 Skelettformeln zeichnen
13 Formalladungen identifizieren 31 Formalladungen identifizieren Formalladungen sind Ladungen (entweder positive oder negative), die wir häufig in unseren Zeichnungen auftauchen lassen müssen. Sie sind von besonderer Bedeutung. Wenn Sie eine Formalladung weglassen, obwohl sie erforderlich wäre, wird Ihre Zeichnung dadurch unvollständig (und falsch). Sie müssen also lernen, wie Sie Formalladungen identifizieren und einzeichnen können. Wenn Sie das nicht beherrschen, werden Sie nicht in der Lage sein, eine Resonanzstruktur zu zeichnen(diewir unsimnächsten Kapitelanschauen) unddannwirdesfür Sie auchextremschwer,diesenkurszubestehen. Eine Formalladung ist eine Ladung aneinem Atom, das nicht die volle Anzahl seiner Valenzelektronen besitzt. Bei der Bestimmung der Formalladung eines Atoms müssen wir zuerst die Anzahl der Valenzelektronen kennen, die das Atom haben müsste. Wir können diese Zahl im Periodensystem der Elemente ablesen, dadie Nummer jeder Spalte im Periodensystem (die»gruppe«) der Anzahl der Valenzelektronen der jeweiligen Elemente entspricht (Valenzelektronen sind Elektronen der Valenzschale, also der äußersten Elektronenschale um ein Atom wahrscheinlich haben Sie das bereits im Chemieunterricht in der Schule gelernt). Kohlenstoff befindet sich zum Beispiel inspalte 4A (der vierten»hauptgruppe«) und besitzt daher 4Valenzelektronen. Jetzt wissen Sie, wie Sie herausfinden können, wie viele Valenzelektronen ein Atom haben sollte. Als Nächstes fragen wir uns, wie viele Elektronen das Atom denn tatsächlich in der Zeichnung besitzt. Aber wie können wir diese Anzahl bestimmen? Lassen Sie uns dazuein Beispiel anschauen. Betrachten Sie das zentralekohlenstoffatom in der folgenden Verbindung: Denken Sie daran, dass jede Bindungslinie zwei Elektronen repräsentiert, die sich jeweils zwei Atome teilen. Als erstes entfernen Sie nun jede Bindungslinie und ersetzen sie stattdessen durch zwei Punkte, die für die Elektronen des einen und des anderen Atoms stehen:
14 32 1 Skelettformeln zeichnen Bestimmen Sie nun die Anzahl der Elektronen, die das zentrale Kohlenstoffatom unmittelbar umgeben: Da gibt es also vier Elektronen. Diese Zahl entspricht der Elektronenzahl, die dasatomtatsächlich besitzt. Jetztsindwir in derlage, dietheoretische Anzahl allermöglichenelektronen (indiesemfallvier) mit deranzahl dertatsächlich vorhandenen Elektronen (in diesem Fall ebenfalls vier) zuvergleichen. Das diese beiden Zahlen gleich groß sind, trägt das Atom keine Formalladung (0). Daswirdauf diemeisten Atome in denverbindungenzutreffen, diesie in diesem Kurs zeichnen werden. Manchmal aber wird esdoch eine Differenz zwischen der theoretisch möglichen und der tatsächlich vorhandenen Elektronenzahl geben. In diesen Fällen kommt eine Formalladung insspiel.schauen wiruns alsoein Atom an,das eine Formalladung trägt. Betrachten Sie dazu das Sauerstoffatom in der folgenden Verbindung: Lassen Sie uns damit anfangen, die Anzahl der Valenzelektronen zu bestimmen, die ein Sauerstoffatom theoretisch haben kann. Sauerstoff befindet sich im Periodensystem inspalte 6A (der sechsten Hauptgruppe), also darf Sauerstoff sechs Valenzelektronen haben. Als Nächstes schauen wir uns das Sauerstoffatom in der obigen Verbindung an und fragen uns, wie viele Valenzelektronen es tatsächlich besitzt. Also zeichnen wir die Verbindung neu, indem wir die C-O-Bindung formal aufspalten: Zusätzlich zudem Elektron, das das Sauerstoffatom durch die C-O-Bindung erhält, besitzt das Sauerstoffatom auch drei freie Elektronenpaare. Ein freies Elektronenpaar liegt dann vor, wenn zwei Elektronen am gleichen Atom nicht für eine Bindung genutzt werden. Freie Elektronenpaare werden in Form zweier nebeneinander liegender Punkte aneinem Atom dargestellt
15 Formalladungen identifizieren 33 und wie Sie sehen, hat das obige Sauerstoffatom drei dieser freien Elektronenpaare. (Denken Sie daran, dass jedes freie Elektronenpaar zwei Elektronen enthält!) Wir sehen also, dass das Sauerstoffatom tatsächlich sieben Elektronen besitzt, also ein Elektron mehr, als es haben sollte. Aus diesem Grund trägt das Atom eine negative Ladung: BEISPIEL Betrachten Sie das Stickstoffatom in der folgenden Verbindung und ermitteln Sie, obeseine Formalladung trägt: Lösung Stickstoff steht im Periodensystem inspalte 5A(der 5.Hauptgruppe) und darf demnach 5Valenzelektronen besitzen. Nun zählen wir, wie viele Elektronen es tatsächlich aufweist: Es hat nur vier. Das ist ein Elektron weniger als theoretisch möglich. Aus diesem Grund trägt das Stickstoffatom eine positive Ladung: Aufgaben Bestimmen Sie für jede der folgenden Strukturen, ob das Stickstoff- oder Sauerstoffatom eine Formalladung trägt. Zeichnen Sie die Ladung ein, wenn es eine gibt.
16 34 1 Skelettformeln zeichnen Das bringt uns zum wichtigsten Atom überhaupt: Kohlenstoff. Wir wissen nun, dass Kohlenstoff immer vier Bindungen eingeht. Deswegen können wir beim Zeichnen von Skelettformeln die Wasserstoffatome ignorieren, daeinfach davon ausgegangen wird, dass wir wissen, wie man bis vier zählt, und entsprechend bestimmen können, wie viele Wasserstoffatome wohl vorhanden sind. Bisher haben wir indiesem Zusammenhang stets nur von Kohlenstoffatomen ohne Formalladung gesprochen (die meisten Kohlenstoffatome in den meisten Verbindungen tragen keine Formalladungen). Aber dawir
17 Formalladungen identifizieren 35 jetzt wissen, was eine Formalladung ist, können wir nun herausfinden, was passiert, wenn Kohlenstoff doch einmal eine Formalladung trägt. Wenn ein Kohlenstoffatom eine Formalladung trägt, können wir nicht mehr davon ausgehen, dass es vier Bindungen eingehen kann. Tatsächlich besitzt es dann nur noch drei Bindungsarme. Lassen Sie uns herausfinden, warum das soist. Schauen wir uns zunächst C + und dann C - an. Wenn Kohlenstoff eine positive Formalladung trägt, besitzt esnur drei Elektronen (eigentlich sollte es vier besitzen, da es in Gruppe 4A des Periodensystems steht). Da es nur drei Elektronen besitzt, kann es auch nur drei Bindungen eingehen. So einfach ist das. Ein Kohlenstoffatom mit einer positiven Formalladung hat also nur drei Bindungsarme. Daran sollten Sie stets denken, wenn Sie die Wasserstoffatome zählen: Schauen wirnun,was geschieht,wennein Kohlenstoffatom eine negative Formalladung trägt. Die negative Formalladung entsteht durch ein zusätzliches Elektron zu denviertheoretischmöglichen Elektronen, diekohlenstoffhaben darf. Esbesitzt dann also fünf Elektronen. Zwei dieser Elektronen bilden ein freies Elektronenpaar,die anderen drei ElektronengehenBindungenein: Das freie Elektronenpaar entsteht, da nicht mit allen fünf Elektronen Bindungen gebildet werden können. Kohlenstoff kann niemals fünf Bindungen eingehen. Warum nicht? Elektronen existieren inaufenthaltsräumen, die man als Orbitale bezeichnet. Diese Orbitale können entweder mit den Orbitalen eines anderen Atoms überlappen und dabei Bindungen bilden, oder sie können zwei Elektronen (ein freies Elektronenpaar) beherbergen. Kohlenstoff besitzt nur vier Orbitale, also besteht keine Möglichkeit, dass esjefünf Bindungen ausbilden kann es besitzt einfach keine fünf Orbitale, die zur Bildung von fünf Bindungen nun einmal nötig sind. Aus diesem Grund besitzt ein Kohlenstoffatom mit einer negativen Formalladung ein freies Elektronenpaar (wenn Sie sich die obige Verbindung anschauen, kommen Sie entspre-
18 36 1 Skelettformeln zeichnen chend auf vier Orbitale eines für das freie Elektronenpaar und drei weitere für die Bindungen). Aus diesem Grund kann ein Kohlenstoffatom mit einer negativen Ladung auch nur drei Bindungen eingehen (genau wie ein positiv geladener Kohlenstoff). Beim Zählen der Wasserstoffatome sollten Sie dies im Hinterkopf behalten: Freie Elektronenpaare aufspüren, die nicht eingezeichnet sind Anhand der obigen Fälle (Sauerstoff, Stickstoff, Kohlenstoff) verstehen Sie nun, dass es wichtig ist, die Anzahl der freien Elektronenpaare zu kennen, um die Formalladung eines Atoms zu bestimmen. Schauen wir uns nun das folgende Beispiel mit einem Stickstoffatom an: Wären die freien Elektronenpaare eingezeichnet, wären wir in der Lage, die Ladung zu bestimmen (zwei Elektronenpaare würden eine negative Ladung bedeuten, ein Elektronenpaar würde zu einer positiven Ladung führen). Umgekehrt könnten wir bei eingezeichneter Formalladung die Anzahl der freien Elektronenpaare bestimmen (eine negative Ladung würde auf zwei Elektronenpaare hinweisen, eine positive Ladung würde ein freies Elektronenpaar bedeuten). Sowird klar, dass in Strukturen entweder freie Elektronenpaare oder Formalladungen eingetragen sein müssen. Sie sollten essich zur Gewohnheit machen, immer nur die Formalladungen einzutragen und die freien Elektronenpaare wegzulassen. Das ist nicht nur viel einfacher darzustellen, da Sie meist nicht mehr als eine Ladung pro Zeichnung eintragen müssen (wenn überhaupt), sondern spart auch Zeit, dasie nicht mühsam jedes einzelne freie Elektronenpaar anjedem Atom einzuzeichnen brauchen. Nachdem wir jetzt bestimmt haben, dass Formalladungen immer eingezeichnet werden müssen und freie Elektronenpaare weggelassen werden können,
19 Freie Elektronenpaare aufspüren, die nicht eingezeichnet sind 37 müssen wir nun üben, die freien Elektronenpaare auch dann zu erkennen, wenn Sie nicht eingezeichnet sind. Das ist nicht viel anders, als Sie darauf zu trainieren, immer alle Wasserstoffatome in einer Skelettformel wahrzunehmen, auch wenn sie nicht ausdrücklich angegeben sind. Wenn Sie zählen können, dann können Sie auch herausfinden, wie viele freie Elektronenpaare sich an einem Atom befinden, auch wenn sie dort nicht eingezeichnet sind. Schauen wir uns dazu ein Beispiel an: In diesem Fall betrachten wir ein Sauerstoffatom.Sauerstoff befindet sich im Periodensystem in der sechsten Hauptgruppe (Spalte 6A) und kann demnach 6 Elektronen besitzen. Nun müssen wirdie Formalladung betrachten. DiesesSauerstoffatom trägt eine negative Ladung, esbesitzt also ein überzähliges Elektron. Daher muss dieses Sauerstoffatom = 7 Elektronen besitzen.jetzt können wir herausfinden,wie vielefreie Elektronenpaare vorhanden sind. Vom Sauerstoff geht eine Bindung aus, das heißt, ernutzt eins seiner sieben Elektronen, um einen Bindung einzugehen. Die anderen sechs müssen daher freie Elektronenpaare sein. Da jedes freie Elektronenpaar aus zwei Elektronen besteht, müssen drei freie Elektronenpaare vorliegen: Lassen Sie uns den Prozess noch einmal überblicken: 1. Bestimmen Sie die Anzahl der Elektronen, die das Atom laut Periodensystem theoretisch haben sollte. 2. Betrachten Sie die Formalladung. Eine negative Ladung entsteht durch ein überzähliges Elektron, eine positive Ladung durch ein fehlendes Elektron. 3. Nun kennen Sie die Anzahl der Elektronen, die das Atom tatsächlich besitzt. Bestimmen Sie anhand dieser Zahl die Anzahl der freien Elektronenpaare. Jetzt müssen wir uns mit den häufigsten Strukturen vertraut machen. Obwohl es natürlich wichtig ist, durch Abzählen die Anzahl freier Elektronenpaare bestimmen zu können, ist es eigentlich viel wichtiger, den Punkt zu erreichen, andem Sie keine Zeit mehr mit Zählen verschwenden müssen. Sie müssen also mit den Strukturen vertraut werden, denen Sie am häufigsten begegnen. Lassen Sie uns das Ganze methodisch angehen.
20 38 1 Skelettformeln zeichnen Wenn Sauerstoff keine Formalladung trägt, hat eszwei Bindungen und zwei freie Elektronenpaare: Wenn Sauerstoff eine negative Ladung trägt, muss ereine Bindung und drei freie Elektronenpaare besitzen: Wenn Sauerstoff eine positive Ladung trägt, muss er drei Bindungen und ein freies Elektronenpaar besitzen:
21 Freie Elektronenpaare aufspüren, die nicht eingezeichnet sind 39 BEISPIEL Zeichnen Sie alle freien Elektronenpaare indie folgende Struktur ein: Lösung Das Sauerstoffatom trägt eine positive Formalladung und ist andrei Bindungen beteiligt. Früher oder später sollten Sie den Punkt erreichen, an dem Sie sofort erkennen, dass dies auf ein einzelnes freies Elektronenpaar hinweist: Bis Sie diesen Punkt erreicht haben, sollten Sie die Aufgabe durch Zählen lösen. Sauerstoff sollte eigentlich immer sechs Elektronen haben. Dieses Sauerstoffatom trägt eine positive Formalladung, also besitzt es ein Elektron weniger. Das heißt, der Sauerstoff besitzt 6 1=5Elektronen. Jetzt können wir die Anzahl der freien Elektronenpaare bestimmen. Das Sauerstoffatom hat drei Bindungen, das heißt, dass esdrei seiner fünf Elektronen für Bindungen einsetzt. Die restlichen zwei müssen daher als freies Elektronenpaar vorliegen. Also gibt es nur ein einziges Elektronenpaar. Aufgaben Gehen Sie die obigen Beispiele noch einmal durch und wenden Sie sich dann den folgenden Aufgaben zu. Zeichnen Sie in jede der unten stehenden Strukturen die freien Elektronenpaare ein. Versuchen Sie zuerkennen, wie viele freie Elektronenpaare vorliegen, ohne die Elektronen vorher durchzuzählen. Erst dann zählen Sie nach, um zu sehen, ob Sie mit Ihrer Antwort richtig lagen
22 40 1 Skelettformeln zeichnen Jetzt schauen wir uns die häufigsten Fälle für Stickstoffatome an. Wenn Stickstoff keine Formalladung trägt, ist esdrei Bindungen eingegangen und hat ein freies Elektronenpaar: Wenn Stickstoff eine negative Ladung trägt, muss es zwei Bindungen und zwei freie Elektronenpaare besitzen:
23 Freie Elektronenpaare aufspüren, die nicht eingezeichnet sind 41 Wenn Stickstoff eine positive Formalladung trägt, muss esvier Bindungen und kein freies Elektronenpaar besitzen: BEISPIEL Zeichnen Sie alle freien Elektronenpaare indie folgende Struktur ein: Das zentrale Stickstoffatom hat eine positive Formalladung und vier Bindungen. Schon bald sollten Sie den Punkt erreichen, an dem Sie sofort erkennen, dass dieses Stickstoffatom kein einziges freies Elektronenpaar besitzt. Die beiden anderen Stickstoffatome haben je eine negative Formalladung und zwei Bindungen. In diesen Fällen sollten Sie erkennen, dass diese Stickstoffatome jeweils zwei freie Elektronenpaare besitzen: Bis Sie diese Zusammenhänge erkennen, sollten Sie die Lösung durch Zählen bestimmen. Stickstoff kann 5Elektronen aufweisen. Der Stickstoff in der Mitte trägt eine positive Ladung, also fehlt ihm ein Elektron. Oder anders ausgedrückt: dieser Stickstoff hat 5-1=4Elektronen. Jetzt können wir herausfinden, wie viele freie Elektronenpaare vorliegen. Da vier Bindungen vorhanden sind, verwendet der Stickstoff all seine Elektronen für Bindungen. Also hat dieser Stickstoff kein freies Elektronenpaar. Die beiden anderen Stickstoffatome tragen jeweils eine negative Formalladung. Das heißt, beide verfügen über ein zusätzliches Elektron, also 5 +1=6Elektronen. Jedes der beiden Stickstoffatome hat zwei Bindungen, das heißt, jedes Atom hat vier Elektronen übrig, die sich inform zweier Elektronenpaare organisieren können.
24 42 1 Skelettformeln zeichnen Aufgaben Gehen Sie die obigen Zustände für Stickstoff noch einmal durch und widmen Sie sich dann den folgenden Aufgaben. Zeichnen Sie in jede der unten stehenden Strukturen die freien Elektronenpaare ein. Versuchen Sie zu erkennen, wie viele freie Elektronenpaare vorhanden sind, ohne die Elektronen zu zählen. Zählen Sie dann nach, um zu sehen, ob Sie mit Ihrer Antwort richtig lagen
1.4. Die Darstellung von Strukturen
 1 Elektronenstruktur und Bindung Säuren und Basen 3D-Moleküle: Li, 2, F zieht positive Ladungen an rot orange gelb grün blau zieht negative Ladungen an stärkstes negatives elektrostatisches Potenzial stärkstes
1 Elektronenstruktur und Bindung Säuren und Basen 3D-Moleküle: Li, 2, F zieht positive Ladungen an rot orange gelb grün blau zieht negative Ladungen an stärkstes negatives elektrostatisches Potenzial stärkstes
Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3
 Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3 Teil 1: Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben p-orbitale? Skizzieren
Übungen zur VL Chemie für Biologen und Humanbiologen 18.11.2011 Lösung Übung 3 Teil 1: Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben p-orbitale? Skizzieren
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
Übungen zur VL Chemie für Biologen und Humanbiologen Diese Aufgaben werden in der Übung besprochen.
 Übungen zur VL Chemie für Biologen und umanbiologen 03.10.2010 Diese Aufgaben werden in der Übung besprochen. Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben
Übungen zur VL Chemie für Biologen und umanbiologen 03.10.2010 Diese Aufgaben werden in der Übung besprochen. Die Geometrie organischer Verbindungen 1. Welche Form hat ein s-orbital? Welche Form haben
Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen
 Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu?
Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu?
Auf der rechten Seite sind Beispiele für kovalente Bindungen.
 Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
2. Verhalten der Elemente bei einer Reaktion: Warum funkt s bei unterschiedlichen
 1. Atombau und Periodensystem 1a) Nach welchem Gesichtspunkt sind die Elemente im Periodensystem von 1- ca. 103 angeordnet? 1b) Nach welchem Gesichtspunkt ist ein Element einer PERIODE zugeordnet? 1c)
1. Atombau und Periodensystem 1a) Nach welchem Gesichtspunkt sind die Elemente im Periodensystem von 1- ca. 103 angeordnet? 1b) Nach welchem Gesichtspunkt ist ein Element einer PERIODE zugeordnet? 1c)
Welche Arten von Formeln stehen dem Chemiker zur Verfügung?
 Welche Arten von Formeln stehen dem Chemiker zur Verfügung? 1. Summenformeln 2. Valenzstrichformeln (Lewis-Strichformeln) 3. Strukturformeln Summenformel: Die Summenformel dient dazu Art und Anzahl der
Welche Arten von Formeln stehen dem Chemiker zur Verfügung? 1. Summenformeln 2. Valenzstrichformeln (Lewis-Strichformeln) 3. Strukturformeln Summenformel: Die Summenformel dient dazu Art und Anzahl der
Lineare Funktionen. Die generelle Form der Funktion lautet dabei:
 Lineare Funktionen Das Thema lineare Funktionen begleitet euch in der Regel von der 7. Klasse an und wird stufenweise erlernt. Meist beginnt es mit einfachem Zeichnen oder Ablesen einer linearen Funktion
Lineare Funktionen Das Thema lineare Funktionen begleitet euch in der Regel von der 7. Klasse an und wird stufenweise erlernt. Meist beginnt es mit einfachem Zeichnen oder Ablesen einer linearen Funktion
Zeichnen von Valenzstrichformeln
 Zeichnen von Valenzstrichformeln ür anorganische Salze werden keine Valenzstrichformeln gezeichnet, da hier eine ionische Bindung vorliegt. Die Elektronen werden vollständig übertragen und die Ionen bilden
Zeichnen von Valenzstrichformeln ür anorganische Salze werden keine Valenzstrichformeln gezeichnet, da hier eine ionische Bindung vorliegt. Die Elektronen werden vollständig übertragen und die Ionen bilden
Lineare Funktionen. y = m x + n
 Lineare Funktionen Das Thema lineare Funktionen begleitet euch in der Regel von der 7. Klasse an und wird stufenweise erlernt. Meist beginnt es mit einfachem Zeichnen oder Ablesen einer linearen Funktion
Lineare Funktionen Das Thema lineare Funktionen begleitet euch in der Regel von der 7. Klasse an und wird stufenweise erlernt. Meist beginnt es mit einfachem Zeichnen oder Ablesen einer linearen Funktion
Die Anzahl der Protonen und Neutronen entspricht der Atommassenzahl.
 Atom Der Begriff Atom leitet sich von atomos her, was unteilbar heisst. Diese Definition ist alt, da man heutzutage fähig ist, Atome zu teilen. Atommassenzahl Die Anzahl der Protonen und Neutronen entspricht
Atom Der Begriff Atom leitet sich von atomos her, was unteilbar heisst. Diese Definition ist alt, da man heutzutage fähig ist, Atome zu teilen. Atommassenzahl Die Anzahl der Protonen und Neutronen entspricht
1. Bedeutung der Oxidationszahlen
 1. Bedeutung der Oxidationszahlen Unterschiedliche Atome geben eine unterschiedliche Zahl an Elektronen ab: Dann hat das Atom eine positive Oxidationsstufe; das Atom ist mit weniger Elektronen als Protonen
1. Bedeutung der Oxidationszahlen Unterschiedliche Atome geben eine unterschiedliche Zahl an Elektronen ab: Dann hat das Atom eine positive Oxidationsstufe; das Atom ist mit weniger Elektronen als Protonen
Elektronenkonfiguration
 Um die chemischen Eigenschaften von Elementen zu verstehen, muss man deren Elektronenkonfiguration kennen. Als Elektronenkonfiguration bezeichnet man die Verteilung der Elektronen auf Schalen um den Kern
Um die chemischen Eigenschaften von Elementen zu verstehen, muss man deren Elektronenkonfiguration kennen. Als Elektronenkonfiguration bezeichnet man die Verteilung der Elektronen auf Schalen um den Kern
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Das Tetraeder-Bällchen/Oktaeder-Bällchen
 H-Atome: klein, weiß Edelgas-Atome: He, Ne, Ar, Kr, Xe, Rn: verschiedene Lila-Töne Metalle: Natrium, Calcium: eher Dunkelblau-Töne Nichtmetalle: C N O F P S Cl grau (kopiert) hellblau rot hellgelb orange
H-Atome: klein, weiß Edelgas-Atome: He, Ne, Ar, Kr, Xe, Rn: verschiedene Lila-Töne Metalle: Natrium, Calcium: eher Dunkelblau-Töne Nichtmetalle: C N O F P S Cl grau (kopiert) hellblau rot hellgelb orange
1.1 Darstellung organischer Verbindungen
 1 Lösung 1 AC/OC I, HS 2017 1.1 Darstellung organischer Verbindungen Organische Verbindungen können auf verschiedene Weise dargestellt werden. Ergänzen Sie die untenstehenden Beispiele von Harnstoff, Ethylenglykol
1 Lösung 1 AC/OC I, HS 2017 1.1 Darstellung organischer Verbindungen Organische Verbindungen können auf verschiedene Weise dargestellt werden. Ergänzen Sie die untenstehenden Beispiele von Harnstoff, Ethylenglykol
Übungsaufgaben zum Atomaufbau und Periodensystem
 Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten
Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten
MAGNESIUM. 1. Bei Verbrennungsreaktionen entstehen in der Regel (kreuze richtig an):
 MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
Einheiten und Einheitenrechnungen
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig?
 1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
Nucleophile Substitution: S N 2-Reaktion
 Nucleophile Substitution: S N 2-Reaktion Diese teilweise Verschiebung von Elektronendichte und die damit einhergehende Polarisierung kann z.b. durch den griechischen Buchstaben und das hochgestellte entsprechende
Nucleophile Substitution: S N 2-Reaktion Diese teilweise Verschiebung von Elektronendichte und die damit einhergehende Polarisierung kann z.b. durch den griechischen Buchstaben und das hochgestellte entsprechende
Pentan enthält 12 Atome Wasserstoff, ein Wassermolekül 2 Atome. Es entstehen also 6 Moleküle Wasser:
 VERTIEFUNG Aufstellen und Einrichten von Gleichungen Reaktionsgleichungen fassen eine chemische Reaktion knapp zusammen. Es werden die Edukte (Ausgangsstoffe) angegeben, die in der chemischen Reaktion
VERTIEFUNG Aufstellen und Einrichten von Gleichungen Reaktionsgleichungen fassen eine chemische Reaktion knapp zusammen. Es werden die Edukte (Ausgangsstoffe) angegeben, die in der chemischen Reaktion
3. Übung Allgemeine Chemie AC01
 Allgemeine und Anorganische Chemie Aufgabe 1: 3. Übung Allgemeine Chemie AC01 Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten im Kern immer die
Allgemeine und Anorganische Chemie Aufgabe 1: 3. Übung Allgemeine Chemie AC01 Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten im Kern immer die
Chemische Bindungen Atombindung
 Atombindung Das Lewis Modell der kovalenten Bindung Die Entstehung von Molekülen beruht auf der Bildung von gemeinsamen, bindenden Elektronenpaaren in dem Bestreben der Atome, eine energetisch stabile
Atombindung Das Lewis Modell der kovalenten Bindung Die Entstehung von Molekülen beruht auf der Bildung von gemeinsamen, bindenden Elektronenpaaren in dem Bestreben der Atome, eine energetisch stabile
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
CHEMIE KAPITEL 1 AUFBAU DER MATERIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2014 / 2015
 CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Valenzelektronen und Atomeigenschaften Valenzelektronen (Außenelektronen) bestimmen
CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Valenzelektronen und Atomeigenschaften Valenzelektronen (Außenelektronen) bestimmen
Lernmaterial Lernfeld 1 Grundlagen Physik und Chemie. Chemische Grundlagen, Bindungsarten. Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms
 Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
0.6 Einfache Modelle der chemischen Bindung
 0.6 Einfache Modelle der chemischen Bindung Ionenbindung Ionenbindungen entstehen durch Reaktion von ausgeprägt metallischen Elementen (Alkalimetalle und Erdalkalimetalle mit geringer Ionisierungsenergie)
0.6 Einfache Modelle der chemischen Bindung Ionenbindung Ionenbindungen entstehen durch Reaktion von ausgeprägt metallischen Elementen (Alkalimetalle und Erdalkalimetalle mit geringer Ionisierungsenergie)
Die chemische Bindung: Erklärt was die Atome in den Atomverbänden zusammenhält. A. Soi
 Die chemische Bindung: Erklärt was die Atome in den Atomverbänden zusammenhält. A. Soi 2017 18 187 Tip II: Wie gelange ich von der Molekülformel zur Lewis Formel? Das Bauprinzip von Molekülen. i) Ein Zentralatom,
Die chemische Bindung: Erklärt was die Atome in den Atomverbänden zusammenhält. A. Soi 2017 18 187 Tip II: Wie gelange ich von der Molekülformel zur Lewis Formel? Das Bauprinzip von Molekülen. i) Ein Zentralatom,
Grundlagen der Chemie Die Atombindung Kovalente Bindungen
 Die Atombindung Kovalente Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Kovalente Bindungen In einem
Die Atombindung Kovalente Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Kovalente Bindungen In einem
Unser Wissen über Atom- und Molekülorbitale wenden wir nun an, um zweiatomige Moleküle der Elemente der 2. Periode zu bilden.
 Additum 6.1 Übersicht und Lernziele Thema Unser Wissen über Atom- und orbitale wenden wir nun an, um zweiatomige e der Elemente der 2. Periode zu bilden. Lernziele 1. Es ist Ihnen möglich, nach dem Studium
Additum 6.1 Übersicht und Lernziele Thema Unser Wissen über Atom- und orbitale wenden wir nun an, um zweiatomige e der Elemente der 2. Periode zu bilden. Lernziele 1. Es ist Ihnen möglich, nach dem Studium
Ionenbindungen. Chemie. Library
 Chemie Ionenbindungen Library IONENBINDUNGEN Begriffserklärung 1 Formeltabelle 1 Ladungsermittlung 2 Formale Ladung 3 Hydrogen-Ionen 3 Verhältnisformeln 4 Nomenklatur 4 Gitterenthalpie 4 Eigenschaften
Chemie Ionenbindungen Library IONENBINDUNGEN Begriffserklärung 1 Formeltabelle 1 Ladungsermittlung 2 Formale Ladung 3 Hydrogen-Ionen 3 Verhältnisformeln 4 Nomenklatur 4 Gitterenthalpie 4 Eigenschaften
Lineare Gleichungssysteme mit 2 Variablen
 Lineare Gleichungssysteme mit 2 Variablen Lineare Gleichungssysteme mit 2 Variablen Einzelne lineare Gleichungen mit zwei Variablen Bis jetzt haben wir nur lineare Gleichungen mit einer Unbekannten (x)
Lineare Gleichungssysteme mit 2 Variablen Lineare Gleichungssysteme mit 2 Variablen Einzelne lineare Gleichungen mit zwei Variablen Bis jetzt haben wir nur lineare Gleichungen mit einer Unbekannten (x)
Atome und Periodensystem
 Kapitel 1 Atome und Periodensystem Lernziele Aufbau und Bestandteile der Atome Isotope Periodensystem der chemischen Elemente Atomaufbau und Isotope Nach dem Atommodell von Rutherford besteht das Atom
Kapitel 1 Atome und Periodensystem Lernziele Aufbau und Bestandteile der Atome Isotope Periodensystem der chemischen Elemente Atomaufbau und Isotope Nach dem Atommodell von Rutherford besteht das Atom
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Grundlagen. Maximilian Ernestus Waldorfschule Saarbrücken
 Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Anleitung für ChemSketch
 Anleitung für ChemSketch Bildschirmerklärung: Die beiden wichtigsten Bereiche sind die Seitenleiste und die Kopfleiste. An der Seitenleiste sind die häufigsten Elemente aufgelistet, ebenso wie der Button
Anleitung für ChemSketch Bildschirmerklärung: Die beiden wichtigsten Bereiche sind die Seitenleiste und die Kopfleiste. An der Seitenleiste sind die häufigsten Elemente aufgelistet, ebenso wie der Button
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Endstoffe (Produkte) Aus dem Reaktionsgemisch entweichendes Gas, z. B. 2 Welche Informationen kann man einer Reaktionsgleichung entnehmen?
 Reaktionsgleichungen Reaktionsgleichungen Blatt 1/5 1 Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen, also einen chemischen Prozeß. Auf der einen Seite steht,
Reaktionsgleichungen Reaktionsgleichungen Blatt 1/5 1 Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen, also einen chemischen Prozeß. Auf der einen Seite steht,
Vollhardt, 3. Aufl., S. 6/7, 4. Aufl., S. 7-9; Hart, S. 4-10; Buddrus, S. 2-4
 Vorlesung 3 Bindungen in rganischen Molekülen IonenbindungKovalente Bindung Vollhardt, 3 Aufl, S 6/7, 4 Aufl, S 79; art, S 410; Buddrus, S 24 Regeln zur Erstellung von Lewisormeln Vollhardt, 3 Aufl, S
Vorlesung 3 Bindungen in rganischen Molekülen IonenbindungKovalente Bindung Vollhardt, 3 Aufl, S 6/7, 4 Aufl, S 79; art, S 410; Buddrus, S 24 Regeln zur Erstellung von Lewisormeln Vollhardt, 3 Aufl, S
Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen
 Wiederholung der letzten Vorlesungsstunde: Thema: Das wellenmechanische h Atommodell (Orbitalmodell) ll) Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen beschrieben werden, Hauptquantenzahl
Wiederholung der letzten Vorlesungsstunde: Thema: Das wellenmechanische h Atommodell (Orbitalmodell) ll) Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen beschrieben werden, Hauptquantenzahl
Chemie Zusammenfassung III
 Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten.
![Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten. Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten.](/thumbs/95/126174167.jpg) Hewlett-Packard Company [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten Johanika [Datum] Walter Whites Chemie Quiz Fragen 1. Aus wie vielen Atomen besteht
Hewlett-Packard Company [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten Johanika [Datum] Walter Whites Chemie Quiz Fragen 1. Aus wie vielen Atomen besteht
11. Kernphysik. [55] Ianus Münze
![11. Kernphysik. [55] Ianus Münze 11. Kernphysik. [55] Ianus Münze](/thumbs/52/29657300.jpg) 11. Kernphysik Der griechische Gott Ianus ist einer der ältesten römischen Gottheiten. Er gehört zur rein römischen Mythologie, das heißt es gibt in der griechischen Götterwelt keine vergleichbare Gestalt.
11. Kernphysik Der griechische Gott Ianus ist einer der ältesten römischen Gottheiten. Er gehört zur rein römischen Mythologie, das heißt es gibt in der griechischen Götterwelt keine vergleichbare Gestalt.
Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch
 Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch Verbindungen untersuchen, ihre Zusammensetzung verstehen und
Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch Verbindungen untersuchen, ihre Zusammensetzung verstehen und
Kovalenzbindungen und zwischenmolekulare Kräfte
 Chemie Kovalenzbindungen und zwischenmolekulare Kräfte Zusammenfassungen Prüfung Donnerstag, 11. Mai 2017 _ Kovalenzbindungen 1 _ Elektronenpaar-Abstossungsmodell 2 _ Polare und apolare Bindungen 3 _ Dipolmoleküle
Chemie Kovalenzbindungen und zwischenmolekulare Kräfte Zusammenfassungen Prüfung Donnerstag, 11. Mai 2017 _ Kovalenzbindungen 1 _ Elektronenpaar-Abstossungsmodell 2 _ Polare und apolare Bindungen 3 _ Dipolmoleküle
2.3 Klebstoffe 4.1 Chemie und Kunststoffgrundlagen 2
 2.3 Klebstoffe 4.1 Chemie und Kunststoffgrundlagen 2 Kunststoffe (Klebstoffe) werden in drei Gruppen eingeteilt: 2.3 Klebstoffe 4.1 Chemie und Kunststoffgrundlagen Um den richtigen Klebstoff auszuwählen,
2.3 Klebstoffe 4.1 Chemie und Kunststoffgrundlagen 2 Kunststoffe (Klebstoffe) werden in drei Gruppen eingeteilt: 2.3 Klebstoffe 4.1 Chemie und Kunststoffgrundlagen Um den richtigen Klebstoff auszuwählen,
4 Die Atombindung im Wasserstoff-Molekül
 4.1 Übersicht und Lernziele Thema Bis jetzt haben wir nur von Atomen gesprochen. In der Chemie beschäftigen wir uns aber normalerweise mit Molekülen oder Ionen. Wir wollen deshalb in diesem Kapitel auf
4.1 Übersicht und Lernziele Thema Bis jetzt haben wir nur von Atomen gesprochen. In der Chemie beschäftigen wir uns aber normalerweise mit Molekülen oder Ionen. Wir wollen deshalb in diesem Kapitel auf
Repetitionen Chemie und Werkstoffkunde
 BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 2 Begriffe der Chemie und Werkstoffkunde Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 2 Begriffe der Chemie und Werkstoffkunde Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
Repetitionen Chemie und Werkstoffkunde
 BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 2 Begriffe der Chemie und Werkstoffkunde Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 2 Begriffe der Chemie und Werkstoffkunde Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1,
Aufgabe 1: Grundwissen zum Atomaufbau und physikalischen Größen
 Probearbeit Physik Aufgabe 1: Grundwissen zum Atomaufbau und physikalischen Größen [14 Punkte] Hinweis: Nutze zur Bearbeitung dieser Aufgabe das beigefügte Periodensystem der Elemente (PDE). (a) Bestimme
Probearbeit Physik Aufgabe 1: Grundwissen zum Atomaufbau und physikalischen Größen [14 Punkte] Hinweis: Nutze zur Bearbeitung dieser Aufgabe das beigefügte Periodensystem der Elemente (PDE). (a) Bestimme
Lösungen der Kontrollaufgaben
 Lösungen der Kontrollaufgaben Lösungen zu den Kontrollaufgaben 1.1 1.) 1000 2.) Glas und PVC ziehen einander an. - Begründung: Da offenbar Hartgummi und PVC gleichartig geladen sind (Abstossung), Glas
Lösungen der Kontrollaufgaben Lösungen zu den Kontrollaufgaben 1.1 1.) 1000 2.) Glas und PVC ziehen einander an. - Begründung: Da offenbar Hartgummi und PVC gleichartig geladen sind (Abstossung), Glas
CHEMIE KAPITEL 1 AUFBAU DER MATERIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2014 / 2015
 CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Atombau und Elementarteilchen Folie 3 Atommasse und Stoffmenge Stoffmenge [mol]: 12,000
CHEMIE KAPITEL 1 AUFBAU DER MATERIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2014 / 2015 Folie 2 Atombau und Elementarteilchen Folie 3 Atommasse und Stoffmenge Stoffmenge [mol]: 12,000
Kantengraphen und Planare Graphen. Seminararbeit
 Kantengraphen und Planare Graphen Seminararbeit in Mathematisches Seminar für LAK 621.378 SS 2018 vorgelegt von Anna Maria Gärtner bei: Baur, Karin, Univ.-Prof. Dr.phil. Graz, 2018 Inhaltsverzeichnis 1
Kantengraphen und Planare Graphen Seminararbeit in Mathematisches Seminar für LAK 621.378 SS 2018 vorgelegt von Anna Maria Gärtner bei: Baur, Karin, Univ.-Prof. Dr.phil. Graz, 2018 Inhaltsverzeichnis 1
VERTIEFUNG. Die Funktionsweise einer Brennstoffzelle
 Die Funktionsweise einer Brennstoffzelle VERTIEFUNG Die folgenden Abbildungen sollen dir helfen, die Vorgänge zu verstehen, die in der Brennstoffzelle ablaufen. Arbeitsauftrag: Beschreibe jeweils die dargestellten
Die Funktionsweise einer Brennstoffzelle VERTIEFUNG Die folgenden Abbildungen sollen dir helfen, die Vorgänge zu verstehen, die in der Brennstoffzelle ablaufen. Arbeitsauftrag: Beschreibe jeweils die dargestellten
Grundwissenkarten Hans-Carossa-Gymnasium. 9. Klasse. Chemie SG
 Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
08.12.2013. Wichtige Stoffgruppen. Stoffgruppe. Atomverband. Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Metall Metall:
 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter) - Salze Nichtmetall Nichtmetall:
1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter) - Salze Nichtmetall Nichtmetall:
Bundesrealgymnasium Imst. Chemie Klasse 8. Kohlenstoffchemie
 Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Vorlesung Chemie für Biologen: Klausur 1 WS Sa
 1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
4.2 Kovalente Bindung. Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916)
 4.2 Kovalente Bindung Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916) Treten Atome von Nichtmetallen miteinander in Wechselwirkung, kommt es nicht zu einer Übertragung von Elektronen. Nichtmetallatome
4.2 Kovalente Bindung Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916) Treten Atome von Nichtmetallen miteinander in Wechselwirkung, kommt es nicht zu einer Übertragung von Elektronen. Nichtmetallatome
Aufgabe 1:Grundwissen zum Atomaufbau und physikalischen Größen
 Probearbeit Physik Aufgabe 1:Grundwissen zum Atomaufbau und physikalischen Größen [14 Punkte] Hinweis:Nutze zur Bearbeitung dieser Aufgabe das beigefügte Periodensystem der Elemente (PDE). (a) Bestimme
Probearbeit Physik Aufgabe 1:Grundwissen zum Atomaufbau und physikalischen Größen [14 Punkte] Hinweis:Nutze zur Bearbeitung dieser Aufgabe das beigefügte Periodensystem der Elemente (PDE). (a) Bestimme
Atomphysik Klasse 9. Aufgabe: Fülle die freien Felder aus!
 1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
1 Aufbau der Materie. 1.1 Anfänge und Kernhüllenmodell. Bauchemie / Bauphysik II Modul M-T 6
 1 Aufbau der Materie 1.1 Anfänge und Kernhüllenmodell 400 J. v. Chr. suchte Demokrit als erster die kleinsten Teile der Materie. Und weil auch er diese damals nicht sehen konnte, entwickelte er eine Modellvorstellung
1 Aufbau der Materie 1.1 Anfänge und Kernhüllenmodell 400 J. v. Chr. suchte Demokrit als erster die kleinsten Teile der Materie. Und weil auch er diese damals nicht sehen konnte, entwickelte er eine Modellvorstellung
Eine Einführung in die Organische Chemie
 Kapitel 10 Eine Einführung in die Organische Chemie Abb. 10.1: Das erste e Molekül. Seit der Begründung der Naturwissenschaft Chemie haben die Stoffe der belebten Natur, von Organismen, einen besonderen
Kapitel 10 Eine Einführung in die Organische Chemie Abb. 10.1: Das erste e Molekül. Seit der Begründung der Naturwissenschaft Chemie haben die Stoffe der belebten Natur, von Organismen, einen besonderen
Aufstellen von Valenzstrichformeln
 Anleitung: n - Descartes-Gymnasium Neuburg Autor: M. Helldobler Seite 1 Aufstellen von n 1. Grundlagen zum Aufstellen von n Verwendete Abkürzungen: VE = Valenzelektron(en) VSF = (n) VEP = Valenzelektronenpaar(e)
Anleitung: n - Descartes-Gymnasium Neuburg Autor: M. Helldobler Seite 1 Aufstellen von n 1. Grundlagen zum Aufstellen von n Verwendete Abkürzungen: VE = Valenzelektron(en) VSF = (n) VEP = Valenzelektronenpaar(e)
Beilage 2: Interview: Klug Hans-Peter
 1.Seite von Beilage 2 Beilage 2: Interview: Klug Hans-Peter naja Wie geht s dir mit Chemie? Gut Lieblingsgegenstand: Turnen Periodensystem ist doch eher trocken und schwer zu verstehen: Wie geht es dir
1.Seite von Beilage 2 Beilage 2: Interview: Klug Hans-Peter naja Wie geht s dir mit Chemie? Gut Lieblingsgegenstand: Turnen Periodensystem ist doch eher trocken und schwer zu verstehen: Wie geht es dir
Organische Chemie. Kapitel 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Organische Verbindungen enthalten Kohlenstoff
 rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
Übungen zur Vorlesung Physikalische Chemie II Lösungsvorschlag zu Blatt 5
 Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 30.07.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel CH 2 O ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 30.07.2018 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel CH 2 O ein, die die folgenden Eigenschaften
Schweizerische Maturitätsprüfung Gruppe / Kandidat/in Nr:... Winter 2010, Zürich Name/Vorname:...
 Gruppe / Kandidat/in Nr:... Name/Vorname:... Grundlagenfach Bereich Teil: NATURWISSENSCHAFTEN Chemie Verfasser: Richtzeit: Hilfsmittel: Hinweise: R. Guenin, J. Lipscher, S. Steiner 80 Minuten (von total
Gruppe / Kandidat/in Nr:... Name/Vorname:... Grundlagenfach Bereich Teil: NATURWISSENSCHAFTEN Chemie Verfasser: Richtzeit: Hilfsmittel: Hinweise: R. Guenin, J. Lipscher, S. Steiner 80 Minuten (von total
Grundwissen C8 NTG. 1. Stoffe und Reaktionen. Reinstoff
 Grundwissen C8 NTG 1. Stoffe und Reaktionen Reinstoff Stoffgemisch - besitzt unter bestimmten Bedingungen (z.b. Temperatur, Druck ) kennzeichnende Eigenschaften, z.b. Farbe, Geruch, Geschmack, Dichte,
Grundwissen C8 NTG 1. Stoffe und Reaktionen Reinstoff Stoffgemisch - besitzt unter bestimmten Bedingungen (z.b. Temperatur, Druck ) kennzeichnende Eigenschaften, z.b. Farbe, Geruch, Geschmack, Dichte,
Aktuelle Beispiele aus der Forschung
 Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 3 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Zum Nachlesen/Vertiefen des Vorlesungsstoffs von heute siehe Maitland
1 Lösung 3 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Zum Nachlesen/Vertiefen des Vorlesungsstoffs von heute siehe Maitland
Stoffplan GLF Chemie 4Mb
 Organische Chemie Stoffplan GLF Chemie 4Mb Theorie: Organische Chemie: -Kohlenwasserstoffe -Aromatische Kohlenwasserstoffe: z.b. Benzol -Organische Sauerstoffverbindungen: z.b. Ethanol -Von der Organik
Organische Chemie Stoffplan GLF Chemie 4Mb Theorie: Organische Chemie: -Kohlenwasserstoffe -Aromatische Kohlenwasserstoffe: z.b. Benzol -Organische Sauerstoffverbindungen: z.b. Ethanol -Von der Organik
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
2 Die Atombindung im Wasserstoff-Molekül
 2.1 Lernziele 1. Sie wissen, wie eine chemische Bindung zwischen zwei Wasserstoff-Atomen zustande kommt. 2. Sie können den bindenden vom antibindenden Zustand unterscheiden. 3. Sie wissen, weshalb das
2.1 Lernziele 1. Sie wissen, wie eine chemische Bindung zwischen zwei Wasserstoff-Atomen zustande kommt. 2. Sie können den bindenden vom antibindenden Zustand unterscheiden. 3. Sie wissen, weshalb das
Basisprüfung Allgemeine Chemie (Teil OC) Montag, 3. September 2007
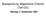 Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
5 Mehrelektronensysteme
 5.1 Übersicht und Lernziele Thema Im ersten Teil dieses Kapitels behandeln wir Atome, die mehr als ein Elektron besitzen. Anschliessend betrachten wir im zweiten Teil die Bildung von Bindungen zwischen
5.1 Übersicht und Lernziele Thema Im ersten Teil dieses Kapitels behandeln wir Atome, die mehr als ein Elektron besitzen. Anschliessend betrachten wir im zweiten Teil die Bildung von Bindungen zwischen
Mathematik: Mag. Schmid Wolfgang Arbeitsblatt Semester ARBEITSBLATT 13 EBENE KOORDINATENGEOMETRIE DER ORTSVEKTOR
 ARBEITSBLATT 13 EBENE KOORDINATENGEOMETRIE DER ORTSVEKTOR Bei sehr vielen mathematischen Aufgabenstellungen ist nicht nur die Länge von bestimmten Strecken oder der Umfang interessant, sondern auch die
ARBEITSBLATT 13 EBENE KOORDINATENGEOMETRIE DER ORTSVEKTOR Bei sehr vielen mathematischen Aufgabenstellungen ist nicht nur die Länge von bestimmten Strecken oder der Umfang interessant, sondern auch die
2. Elektroneneffekte in den organischen Molekülen
 2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
Organik-Beispiel. Inhaltsverzeichnis
 Inhaltsverzeichnis I. Säure-Basen-Gleichungen... 2 a) Nach Arrhenius:... 2 b) Nach Broensted:... 2 c) Nach Lewis:... 2 II. H 2 O + HCl?... 4 a) Was ist in der Reaktion passiert? Welche Produkte entstehen?...
Inhaltsverzeichnis I. Säure-Basen-Gleichungen... 2 a) Nach Arrhenius:... 2 b) Nach Broensted:... 2 c) Nach Lewis:... 2 II. H 2 O + HCl?... 4 a) Was ist in der Reaktion passiert? Welche Produkte entstehen?...
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Hybridorbitale und ihre Bedeutung
 Hybridorbitale und ihre Bedeutung Roland Heynkes 27.4.2005, Aachen Die Chemie wird kaum von den Atomkernen und den inneren Elektronenschalen, sondern hauptsächlich von der jeweils äußersten Elektronenschale
Hybridorbitale und ihre Bedeutung Roland Heynkes 27.4.2005, Aachen Die Chemie wird kaum von den Atomkernen und den inneren Elektronenschalen, sondern hauptsächlich von der jeweils äußersten Elektronenschale
Grundwissenskatalog Chemie G8 8. Klasse nt
 Grundwissenskatalog Chemie G8 8. Klasse nt 1. Wissenschaft Chemie: Chemie ist die Lehre von den Stoffen. Chemischer Vorgang: Stoffänderung Physikalischer Vorgang: Zustandsänderung 2. Unterteilung Stoffe:
Grundwissenskatalog Chemie G8 8. Klasse nt 1. Wissenschaft Chemie: Chemie ist die Lehre von den Stoffen. Chemischer Vorgang: Stoffänderung Physikalischer Vorgang: Zustandsänderung 2. Unterteilung Stoffe:
Repetitionen Chemie und Werkstoffkunde
 BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 1 Einteilung der Stoffe Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1, 8772 Nidfurn 055-654
BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 1 Einteilung der Stoffe Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1, 8772 Nidfurn 055-654
1 Struktur und Bindung organischer Moleküle
 1 Struktur und Bindung organischer Moleküle 20. (sowie 21 und 25, s. unten) (a) (b) Die Dreifachbindung ist fur die Ausbildung der Oktette an C und N erforderlich. (c) d + d H:O :Cl: (d) Man beachte, dass
1 Struktur und Bindung organischer Moleküle 20. (sowie 21 und 25, s. unten) (a) (b) Die Dreifachbindung ist fur die Ausbildung der Oktette an C und N erforderlich. (c) d + d H:O :Cl: (d) Man beachte, dass
Zuusammenfassung Klasssenarbeit Chemie
 Zuusammenfassung Klasssenarbeit Chemie Moritz F. Kuntze 10. November 2016 1 Inhaltsverzeichnis 1 Wertigkeit 3 1.1 Bestimmung der Wertigkeit......................... 3 1.2 Nutzen der Wertigkeit............................
Zuusammenfassung Klasssenarbeit Chemie Moritz F. Kuntze 10. November 2016 1 Inhaltsverzeichnis 1 Wertigkeit 3 1.1 Bestimmung der Wertigkeit......................... 3 1.2 Nutzen der Wertigkeit............................
Inhalt: Die vorliegenden Folienvorlagen enthalten folgende Elemente:
 Inhalt: Punkte im Koordinatensstem Funktionen und ihre Schaubilder Punktprobe und Koordinaten berechnen Proportionale Funktionen 5 Steigung und Steigungsdreieck 6 Die Funktion = m + b 7 Funktionsgleichungen
Inhalt: Punkte im Koordinatensstem Funktionen und ihre Schaubilder Punktprobe und Koordinaten berechnen Proportionale Funktionen 5 Steigung und Steigungsdreieck 6 Die Funktion = m + b 7 Funktionsgleichungen
Tutorium zum Strukturformeleditor Stand:
 Tutorium zum Strukturformeleditor Stand: 24.2.2015 Das folgende Beispiel ist konzipiert für die nicht registrierte Version des Programms. Durch eine Registrierung kann der Zeichenbereich vergrößert werden
Tutorium zum Strukturformeleditor Stand: 24.2.2015 Das folgende Beispiel ist konzipiert für die nicht registrierte Version des Programms. Durch eine Registrierung kann der Zeichenbereich vergrößert werden
[ ] 1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe + - Moleküle aus gleichen Atomen. Ionen. Moleküle aus verschiedenen Atomen
![[ ] 1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe + - Moleküle aus gleichen Atomen. Ionen. Moleküle aus verschiedenen Atomen [ ] 1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe + - Moleküle aus gleichen Atomen. Ionen. Moleküle aus verschiedenen Atomen](/thumbs/68/58264490.jpg) 1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe Gemische Reinstoffe Elemente Verbindungen gleiche Atome Moleküle aus gleichen Atomen Moleküle aus verschiedenen Atomen Ionen + Kation Anion z.b.
1. Stoffe und Reaktionen (Kartei 8.8, 8.10 und 8.13) Stoffe Gemische Reinstoffe Elemente Verbindungen gleiche Atome Moleküle aus gleichen Atomen Moleküle aus verschiedenen Atomen Ionen + Kation Anion z.b.
