Arbeitsheft Organische Redoxreaktionen Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse:
|
|
|
- Jürgen Bergmann
- vor 7 Jahren
- Abrufe
Transkript
1 Arbeitsheft Organishe Reoxreaktionen Inhalt Jakob Inhaltsverzeihnis: Seite: Vorkenntnisse: Bestimmung er OZ bei organishen Molekülen Arbeitsheft Reoxreaktionen Verbrennung von Kohlenwasserstoffen. Oxiation von Methan mit Sauerstoff. Oxiation von Ethin mit Sauerstoff 4 Nahweis von Alkenen. Oxiation von Ethen mit Permanganationen in alkalisher Lösung 5 4 Strukturaufklärung bei Alkoholen 4. Oxiation von Natrium mit Ethanol 6 5 Nahweis von Alkoholen un Alehyen 5. Oxiation von Ethanol mit Dihromationen in saurer Lösung 7 5. Oxiation von Ethanol mit festem Kupfer(II)oxi 8 5. Oxiation von Ethanal mit Kufper(II)ionen in alkalisher Lösung Oxiation von Ethanal mit Silber(I)ionen in alkalisher Lösung 0 6 Tabelle zu en Alkohol- un Alehynahweisen 7 Elektronenrukreihe zu en Alkohol- un Alehynahweisen Verknüpfung mit aneren Themenbereihen: Energieumsatz bei Reoxreaktionen (=> vgl. Arbeitsheft Stoffwehsel) Nahweis von Funktionellen Gruppen un Strukturaufklärung Versuhsübershrift nah em Shema: Oxiation es Rem mit em Oxm Versuhsurhführung (D) mit beshrifteter Skizze Beobahtung (B) un Folgerung (F) Versuhsbeshreibung Reaktionsgleihung (Gl) mit en Teilgleihungen evtl. Merksatz
2 Arbeitsheft Organishe Reoxreaktionen Bestimmung er OZ bei organishen Molekülen Jakob Bestimmung er OZ bei organishen Molekülen (Benutze ie Regeln aus em Arbeitsheft Elektronenübergänge) Beahte bei er formalen Binungsspaltung, ass ie C-H Binung shwah polar ist, obwohl sie im Kapitel zwishenmolekulare Kräfte vereinfaht als unpolar gilt! A B C D E F Molekül Name C-Atom Nr. A B C D E F OZ Funktionelle Gruppe
3 Arbeitsheft Organishe Reoxreaktionen Verbrennung von Kohlenwasserstoffen Jakob B: Oxiation von mit F: Versuhsbeshreibung Am Bunsenbrenner wir as vor allem aus Methan bestehene Gasgemish Ergas entzünet. Bei ausreihener Sauerstoffzufuhr ist ie sehr heiße Flamme farblos bis shwah bläulih. Hält man ein kühles Glasrohr über ie Flamme, so beobahtet man ie Konensation einer niht brennbaren, farblosen Flüssigkeit. Fängt man as ebenfalls entstehene farblose Gas auf un leitet es in Caliumhyroxi-Lösung (= Kalkwasser ), so bilet sih ein weißer Nieershlag von Caliumarbonat (= Kalk ). Re.: Rem + + Oxm Oxm Rem Der Laungs- un Stoffmengenausgleih wir vereinfaht wie in sauren Lösungen vorgenommen. Für ie Gesamtgleihung ist er Laungs- un Stoffmengenausgleih hier niht von Beeutung. Kohlenwasserstoffe verbrennen unter. Sie können aher als ienen. Je länger ie Kette es Kohlenstoffgerüsts ist, esto heller leuhtet ie Flamme un esto mehr rußt ie Flamme, a ann niht vollstänig reagiert.
4 Arbeitsheft Organishe Reoxreaktionen Verbrennung von Kohlenwasserstoffen Jakob 4 B: Oxiation von mit F: Versuhsbeshreibung Der Bunsenbrenner wir an eine Gasflashe mit Ethin (= Aetylen ) angeshlossen un entzünet. Bei ausreihener Sauerstoffzufuhr ist ie sehr heiße Flamme farblos bis shwah bläulih. Hält man ein kühles Glasrohr über ie Flamme, so beobahtet man ie Konensation einer niht brennbaren, farblosen Flüssigkeit. Fängt man as ebenfalls entstehene farblose Gas auf un leitet es in Caliumhyroxi-Lösung (= Kalkwasser ), so bilet sih ein weißer Nieershlag von Caliumarbonat (= Kalk ). Re.: Rem + + Oxm Oxm Rem Der Laungs- un Stoffmengenausgleih wir vereinfaht wie in sauren Lösungen vorgenommen. Für ie Gesamtgleihung ist er Laungs- un Stoffmengenausgleih hier niht von Beeutung. Ethin verbrennt wie Wasserstoff mit einer sehr Flamme. Es wir aher zum Aetylen- eingesetzt. Bei Sauerstoffmangel leuhtet ie Flamme aber nur beim mit, a bei em aneren Gas kein entstehen kann.
5 Arbeitsheft Organishe Reoxreaktionen Nahweis von Alkenen Jakob 5 B: Oxiation von mit F: / Versuhsbeshreibung Das farblose Gas Ethen wir in eine violette alkalishe Kaliumpermanganat- Lösung geleitet. Die Lösung entfärbt sih un es entsteht ein brauner Feststoff von Mangan(IV)oxi (= Braunstein ). Es entsteht zunähst eine sogenannte Dihyroxy-Verbinung (Abb. ), ie ann bei rastisheren Reaktionbeingungen weiter oxiiert weren kann bis zu zwei Molekülen Kohlenstoffioxi. Re.: Rem Oxm Oxm Rem Abb. :, Ethaniol Die Reaktion von Alkenen wir auh genannt. Permanganationen sin in Lösung nur. Sie reagieren aher nur mit shwahen Reuktionsmitteln wie eben en Alkenen, niht jeoh mit aneren Stoffklassen. Alternativ kann man en Versuh auh mit Cylohexen ausführen beahte ie ann veränerte OZ! Die Differenz er OZ ist aber auh bei iesem Alternativversuh natürlih gleih er beim oben beshriebenen.
6 Arbeitsheft Organishe Reoxreaktionen 4 Strukturaufklärung von Alkoholen Jakob 6 B: Oxiation von mit F: / Versuhsbeshreibung Etwas wasserfreies, farbloses Ethanol wir in eine Glaswanne gegeben un ein kleines Stük Natrium wir auf ie Oberflähe er Flüssigkeit gelegt. An er Kontaktflähe zwishen Natriumstükhen un Ethanol entstehen kleine farblose Gasbläshen, ie as Metall wie ein Luftkissenboot auf er Oberflähe hin un hersausen lassen. Das Natriumstükhen sheint sih abei aufzulösen. Fängt man as entstehene Gas auf un lässt es mit Re.: reagieren, so ist ie Rem Oxm Oxm Rem positiv. Dieser Versuh zeigt ie enge Die Funktionelle Gruppe er Alkohole ist ie Diese besitzt ein Wasserstoffatom. Daher kann sie ähnlihe wie mit sehr starken wie en Alkalimetallen reagieren. Verwantshaft er Alkohole mit em Molekül. Mit einem flüssigen Ether funktioniert er Versuh niht!
7 Arbeitsheft Organishe Reoxreaktionen 5 Nahweis von Alkoholen un Alehyen Jakob 7 Oxiation von mit B: Versuhsbeshreibung Zu etwas Ethanol wir orangefarbene saure Kaliumihromat-Lösung gegeben. Die Lösung änert ihre Farbe von orange nah grün. Oben am Reagenzglas ist er Geruh von Essigsäure wahrnehmbar. F: Re.: Rem Oxm Oxm Rem Primäre Alkohole weren zunähst zum oxiiert. Da iese stärkere weiteroxiiert zur sin, als Alkohole, weren sie sofort. Die Oxiation mit Dihromationen ist somit kein eineutiger Nahweis für Alkohole, a Dihromationen in saurer Lösung zu starke sin.
8 Arbeitsheft Organishe Reoxreaktionen 5 Nahweis von Alkoholen un Alehyen Jakob 8 B: Oxiation von mit Versuhsbeshreibung Zur Vorbereitung wir zunähst ein Stük Kupferbleh mit er nihtleuhtenen Bunsenbrennerflamme an er Luft solange erhitzt, bis sih ein shwarzer Feststoff auf er Oberflähe bilet. Es hanelt sih abei niht um Kohlenstoff, sonern um shwarzes Kupfer(II)oxi. F: Re.: Rem + + Oxm Oxm Rem + Beim eigentlihen Versuh füllt man Ethanol in ein Beherglas un tauht ann as vorbereitete Stük Kupferbleh mit em Kupfer(II)oxi-Überzug in as Ethanol. Man beobahtet eine Entfärbung am Kupferbleh, seine Oberflähe ist nah em Eintauhen also wieer rötlih metallish glänzen. Über em Beherglas ist er Geruh von Essigsäure wahrnehmbar. Primäre Alkohole weren zunähst zum oxiiert. Da iese stärkere sin, als Alkohole, weren sie sofort weiteroxiiert zur. Die Oxiation mit festem Kupfer(II)oxi ist somit kein eineutiger Nahweis für Alkohole, a Kupfer(II)ionen als Feststoff zu starke sin. Der Laungs- un Stoffmengenausgleih wir hier vereinfaht wie in sauren Lösungen vorgenommen. Falls sih vorher etwas Kupfer(II)oxi löst, wäre auh alkalish sinnvoll, a aber eine Säure entsteht, eben auh sauer.
9 Arbeitsheft Organishe Reoxreaktionen 5 Nahweis von Alkoholen un Alehyen Jakob 9 Oxiation von mit B: F: Re.: Rem Oxm Oxm Rem Versuhsbeshreibung Zur Vorbereitung wir nähst zu einer hellblauen Kupfer(II)sulfat-Lösung (= Fehling-Lösung I ) etwas farblose Kaliumtartrat-Natriumhyroxi-Lösung (= Fehling-Lösung II ) gegeben. Die Farbe änert sih nah Tiefblau, a löslihe Kupfer(II)tartratkomplexionen entstehen. Die Zugabe er Tartrationen ient nur azu, ass in er alkalishen Lösung kein shwerlöslihes weißes Kupfer(II)hyroxi aus er Lösung als Feststoff ausfällt. Beim eigentlihen Versuh füllt man as farblose Ethanal (= Aetalehy) in ein Reagenzglas un gibt as tiefblaue Gemish er Fehling I + II Lösung azu. Nun wir as Reagenzglas über em Bunsenbrenner erhitzt, bis sih ein braunroter Feststoff bilet, as rote Kupfer(I)oxi. Oben am Reagenzglas ist er Geruh von Essigsäure wahrnehmbar. Alehye weren zur oxiiert. Kupfer(II)ionen sin in Lösung, sie können aher bei er für en Nahweis von Alehyen, ie relativ starke sin, eingesetzt weren.
10 Arbeitsheft Organishe Reoxreaktionen 5 Nahweis von Alkoholen un Alehyen Jakob 0 Oxiation von mit B: F: Re.: Rem Oxm Oxm Rem Alehye weren zur oxiiert. Silber(I)ionen sin in Lösung Versuhsbeshreibung Zur Vorbereitung wir nähst zu einer farblosen Silber(I)nitrat-Lösung etwas farblose Ammoniak- Natriumhyroxi-Lösung gegeben. Die Lösung bleibt farblos, a löslihe farblose Silber(I)ammoniakkomplexionen entstehen. Die Zugabe von Ammoniak ient nur azu, ass in er alkalishen Lösung kein shwerlöslihes weißes Silber(I)hyroxi aus er Lösung als Feststoff ausfällt. Beim eigentlihen Versuh füllt man as farblose Ethanal (= Aetalehy) in einen gläsernen Runkolben un gibt as farblose Gemish er vorbereiteten Lösung (= Tollens-Lösung ) azu. Nun wir er Runkolben über em Bunsenbrenner unter Drehen gleihmäßig erhitzt, bis sih ein silbriger Feststoff bilet. Da sih er Feststoff an er Glasinnenwan absheiet, entsteht ein Silberspiegel. Oben am Reagenzglas ist er Geruh von Essigsäure wahrnehmbar., sie können aher bei er für en Nahweis von Alehyen, ie relativ starke sin, eingesetzt weren.
11 Arbeitsheft Organishe Reoxreaktionen 6 Tabelle zu en Alkohol- un Alehynahweisen Jakob 6 Tabelle zu en Alkohol- un Alehynahweisen (Ergänze ie allgemeinen Enstoffe un ie Farbe nah Ablauf er Reaktion) Rem primärer Alkohol Oxm saure Kaliumihromat- Lösung festes Kupfer(II)oxi alkalishe Kupfer(II)sulfat-Lösung alkalishe Silber(I)nitrat-Lösung sekunärer Alkohol tertiärer Alkohol Alehy Keton
12 Arbeitsheft Organishe Reoxreaktionen 7 Elektronenrukreihe zu en Alkohol- un Alehynahweisen Jakob 7 Elektronenrukreihe zu en Alkohol- un Alehynahweisen Rem Oxm Alehye sin stärkere als Alkohole. Alehye können aher nur mit er oer er nahgewiesen weren. Die stärkeren festes Kupfer(II)oxi un alkalishe Kaliumihromat-Lösung sin niht als -Nahweis geeignet, weil sie auh mit un Alkoholen reagieren. Alkalishe Kaliumpermanganat-Lösung reagiert weer mit Alehyen noh Alkoholen. sin aher noh shwähere. Dies ermögliht ie.
Versuchsüberschrift nach dem Schema: Protonierung der Base mit der Säure
 Arbeitsheft Säuren und Basen Inhalt Jakob 1 Inhaltsverzeihnis: Seite: 1 Definition für wässrige Lösungen (Arrhenius) 1.1 Wasser Chlorwasserstoff 2 1.2 Ammoniak Wasser 3 2 Allgemeine Definition (Brönsted)
Arbeitsheft Säuren und Basen Inhalt Jakob 1 Inhaltsverzeihnis: Seite: 1 Definition für wässrige Lösungen (Arrhenius) 1.1 Wasser Chlorwasserstoff 2 1.2 Ammoniak Wasser 3 2 Allgemeine Definition (Brönsted)
Versuchsüberschrift nach dem Schema: Oxidation des Redm mit dem Oxm
 Arbeitsheft Reoxreaktionen Inhalt Jakob 1 Inhaltsverzeihnis: Versuh-Nr.: Seite: 1 Einfahe Elektronenrukreihe 1.1 Oxiation von Zink Brom Versuh 1 2 1.2 Oxiation von Ioiionen Brom Versuh 2 3 1.3 Oxiation
Arbeitsheft Reoxreaktionen Inhalt Jakob 1 Inhaltsverzeihnis: Versuh-Nr.: Seite: 1 Einfahe Elektronenrukreihe 1.1 Oxiation von Zink Brom Versuh 1 2 1.2 Oxiation von Ioiionen Brom Versuh 2 3 1.3 Oxiation
Arbeitsheft Ionische Reaktionsmechanismen Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse:
 Arbeitsheft Ionische Reaktionsmechanismen Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse: 1 Laung, Teillaung, Oxiationszahl, Formale Laung 2 Atombinung, Nichtmetalle, Valenzelektronen, Binene
Arbeitsheft Ionische Reaktionsmechanismen Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse: 1 Laung, Teillaung, Oxiationszahl, Formale Laung 2 Atombinung, Nichtmetalle, Valenzelektronen, Binene
Zum Begriff der Paare: ab ordinalem Messniveau
 Zum Begriff er Paare: ab orinalem Messniveau Begriffsefinition von Paaren: gleihe bzw. untershielihe Rangornung zwishen Untersuhungsobjekten (z. B. Personen) Paare können konkorant oer iskorant sein 1)
Zum Begriff er Paare: ab orinalem Messniveau Begriffsefinition von Paaren: gleihe bzw. untershielihe Rangornung zwishen Untersuhungsobjekten (z. B. Personen) Paare können konkorant oer iskorant sein 1)
Grundwissen Chemie 10. Klasse NTG
 Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Mathematische Modelle und numerische Methoden in der Biologie
 Institut für Angewante un Numerishe Mathematik Prof. Dr. Tobias Jahnke, Dipl.-Biol. Mihael Kreim Mathematishe Moelle un numerishe Methoen in er Biologie Sommersemester 2012 3. Übungsblatt Gruppenübung
Institut für Angewante un Numerishe Mathematik Prof. Dr. Tobias Jahnke, Dipl.-Biol. Mihael Kreim Mathematishe Moelle un numerishe Methoen in er Biologie Sommersemester 2012 3. Übungsblatt Gruppenübung
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Barocker Kontrapunkt Invention: idealtypische ( akademische ) Form
 Hans Peter Reutter: Invention 1 Baroker Kontrapunkt Invention: iealtypishe ( akaemishe ) Form Bis zum Ene er Barokzeit sin ie Bezeihnungen für polyphone Formen eigentlih ziemlih austaushbar: Fuge, Rierar,
Hans Peter Reutter: Invention 1 Baroker Kontrapunkt Invention: iealtypishe ( akaemishe ) Form Bis zum Ene er Barokzeit sin ie Bezeihnungen für polyphone Formen eigentlih ziemlih austaushbar: Fuge, Rierar,
EINE KERZE INTERPRETATIONEN BEOBACHTUNGEN FLAMME REAKTIONEN WACHS DOCHT GASE. Reaktionsgleichungen Prozesse. Theorien
 Reaktionsgleichungen Prozesse INTERPRETATIONEN BEOBACHTUNGEN Theorien Licht Produkte Reaktionsgleichungen Thermodynamik Geschwindigkeit REAKTIONEN EINE KERZE FLAMME Farbe Form Bewegung Einflüsse WACHS
Reaktionsgleichungen Prozesse INTERPRETATIONEN BEOBACHTUNGEN Theorien Licht Produkte Reaktionsgleichungen Thermodynamik Geschwindigkeit REAKTIONEN EINE KERZE FLAMME Farbe Form Bewegung Einflüsse WACHS
Entscheide bei jeder Aussage, ob es eine reine Beobachtung ist oder nicht, und kreuze an!
 Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
1 Stoffklasse Alkane : C n H 2n+2 Namensendung an
 rganische hemie LÖSUNGEN Seite 1 von 11 1 Stoffklasse Alkane : n 2n+2 Namensendung an Zahl der -Atome Name Molekülformel Lewisformel Keilstrichformel Skelettformel 1 Methan 4 Sinnlos 2 Ethan 2 6 3 Propan
rganische hemie LÖSUNGEN Seite 1 von 11 1 Stoffklasse Alkane : n 2n+2 Namensendung an Zahl der -Atome Name Molekülformel Lewisformel Keilstrichformel Skelettformel 1 Methan 4 Sinnlos 2 Ethan 2 6 3 Propan
Physikaufgabe 95. Lösung: Integriert man die spektrale Energiedichte der Hohlraumstrahlung. d, dx, x c
 Home Startseite Impressum Kontakt Gästebuh Aufgabe: Behaneln Sie as All als Shwarzen Körper berehnen Sie seine asse un araus en aius un as Alter es niversums un ie Größe er Vakuumpolarisation. Lösung:
Home Startseite Impressum Kontakt Gästebuh Aufgabe: Behaneln Sie as All als Shwarzen Körper berehnen Sie seine asse un araus en aius un as Alter es niversums un ie Größe er Vakuumpolarisation. Lösung:
Summenformel Elektronenstrichformel Name Siedepunkt
 Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Das Chemische Gleichgewicht Massenwirkungsgesetz
 Das Chemishe Gleihgewiht Massenwirkungsgesetz Reversible Reaktionen: Beisiel : (Bodenstein 899 Edukt (Reaktanden Produkt H + I HIH Beobahtung: Die Reaktion verläuft unvollständig! ndig! D.h. niht alle
Das Chemishe Gleihgewiht Massenwirkungsgesetz Reversible Reaktionen: Beisiel : (Bodenstein 899 Edukt (Reaktanden Produkt H + I HIH Beobahtung: Die Reaktion verläuft unvollständig! ndig! D.h. niht alle
Schulcurriculum des Faches Chemie. für die Klassenstufen 8 10
 Schulcurriculum des Faches Chemie für die Klassenstufen 8 10 Chemie - Klasse 8 Was ist Chemie? Richtig experimentieren und Entsorgen Naturwissenschaftliche Arbeitsweise Rotkraut oder Blaukraut? Richtig
Schulcurriculum des Faches Chemie für die Klassenstufen 8 10 Chemie - Klasse 8 Was ist Chemie? Richtig experimentieren und Entsorgen Naturwissenschaftliche Arbeitsweise Rotkraut oder Blaukraut? Richtig
1 Lehrerversuch Alkalimetalle in Wasser
 1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
Echt ätzend! - Was ist und wie wirkt Abflussreiniger?
 Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
STOFFE U N D STOFFTRENNUNG
 Inhalt WAS IST CHEMIE? 10 STOFFE U N D STOFFTRENNUNG 22 Chemie erlebt Chem ie-chancen und Gefahren...12 Umgang mit Chemikalien... 14 Chemie erlebt Chemie is t... 16 Methode Regeln beim Experimentieren...17
Inhalt WAS IST CHEMIE? 10 STOFFE U N D STOFFTRENNUNG 22 Chemie erlebt Chem ie-chancen und Gefahren...12 Umgang mit Chemikalien... 14 Chemie erlebt Chemie is t... 16 Methode Regeln beim Experimentieren...17
Steckbrief von Sauerstoff, O 2
 Steckbrief von Sauerstoff, O 2 farblos, d.h. unsichtbar, nur in sehr dicken Schichten himmelblau geruch- und geschmacklos - Etwas schwerer als Luft - notwendig für die Verbrennung, brennt aber nicht selbst
Steckbrief von Sauerstoff, O 2 farblos, d.h. unsichtbar, nur in sehr dicken Schichten himmelblau geruch- und geschmacklos - Etwas schwerer als Luft - notwendig für die Verbrennung, brennt aber nicht selbst
Organische Moleküle. Verschiedene Ansichten des Methans
 Organische Räumlicher Bau, Elektronendichteverteilungen Verschiedene Ansichten des Methans Ansicht des Methans mit seiner Elektronenhülle (Solid-Darstellung) Ansicht des Methans mit seiner Elektronenhülle
Organische Räumlicher Bau, Elektronendichteverteilungen Verschiedene Ansichten des Methans Ansicht des Methans mit seiner Elektronenhülle (Solid-Darstellung) Ansicht des Methans mit seiner Elektronenhülle
Summenformel. Strukturformel. Halbstrukturformel. Fossile Energieträger. ( 10. Klasse NTG 1 / 47 ) ( 10. Klasse NTG 2 / 47 ) ( 10. Klasse NTG 3 / 47 )
 Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Geschwister-Scholl-Gymnasium Schulcurriculum Stuttgart-Sillenbuch. Gesamt Chemie
 Chemie - Klasse 8 Thema / Inhalt Thema / Inhalt Was ist Chemie? Richtig experimentieren und entsorgen Naturwissenschaftliche Arbeitsweise Rotkraut oder Blaukraut? Richtig protokollieren Stoffeigenschaften:
Chemie - Klasse 8 Thema / Inhalt Thema / Inhalt Was ist Chemie? Richtig experimentieren und entsorgen Naturwissenschaftliche Arbeitsweise Rotkraut oder Blaukraut? Richtig protokollieren Stoffeigenschaften:
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Verbindungen mit Sauerstoff heißen
 Welche der flgenden Aussagen trifft für Sauerstff Sauerstff ist durchsichtig. etwa 10% Sauerstff ist brennbar. etwa 15% Sauerstff ist ein Gas. etwa 20% Sauerstff fördert die Verbrennung. etwa 25% Verbindungen
Welche der flgenden Aussagen trifft für Sauerstff Sauerstff ist durchsichtig. etwa 10% Sauerstff ist brennbar. etwa 15% Sauerstff ist ein Gas. etwa 20% Sauerstff fördert die Verbrennung. etwa 25% Verbindungen
Untersuche die Kerzenflamme sowie die Vorgänge, die beim Verbrennen des Kerzenwachses ablaufen.
 Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P7154200) 2.10 Die Kerzenflamme Experiment von: Seb Gedruckt: 24.03.2014 11:14:37 intertess (Version 13.12 B214, Export 2000)
Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P7154200) 2.10 Die Kerzenflamme Experiment von: Seb Gedruckt: 24.03.2014 11:14:37 intertess (Version 13.12 B214, Export 2000)
5.2 Schiffsche und Fehlingsche Probe. Aufgabe. Wie lassen sich Alkanale von Alkanolen unterscheiden?
 Naturwissenschaften - Chemie - Organische Chemie - 5 Carbonylverbindungen (P772400) 5.2 Schiffsche und Fehlingsche Probe Experiment von: Anouch Gedruckt: 25.02.204 4:00:42 intertess (Version 3.2 B24, Export
Naturwissenschaften - Chemie - Organische Chemie - 5 Carbonylverbindungen (P772400) 5.2 Schiffsche und Fehlingsche Probe Experiment von: Anouch Gedruckt: 25.02.204 4:00:42 intertess (Version 3.2 B24, Export
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Anhand welcher Eigenschaften lässt sich Wasserstoff identifizieren?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75500) 5.2 Nachweis von Wasserstoff Experiment von: Phywe Gedruckt:.0.203 3:02:34 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75500) 5.2 Nachweis von Wasserstoff Experiment von: Phywe Gedruckt:.0.203 3:02:34 intertess (Version 3.06 B200, Export 2000) Aufgabe
2.9 Aufbau und Funktion eines Bunsenbrenners. Aufgabe. Wie ist der Bunsenbrenner aufgebaut?
 Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P75400) 2.9 Aufbau und Funktion eines Bunsenbrenners Experiment von: Seb Gedruckt: 24.03.204 ::49 intertess (Version 3.2 B24,
Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P75400) 2.9 Aufbau und Funktion eines Bunsenbrenners Experiment von: Seb Gedruckt: 24.03.204 ::49 intertess (Version 3.2 B24,
1. Wer sich über Erdgas informieren will, findet im Internet viele Informationen dazu, zum Beispiel diese:
 Autos, die mit Erdgas fahren Seit mehr als 15 Jahren werden Erdgasautos in Serie gefertigt. Das Erdgas wird in Tanks mitgeführt und steht unter einem Druck von 200 bar. Mittlerweile gibt es in Österreich
Autos, die mit Erdgas fahren Seit mehr als 15 Jahren werden Erdgasautos in Serie gefertigt. Das Erdgas wird in Tanks mitgeführt und steht unter einem Druck von 200 bar. Mittlerweile gibt es in Österreich
Untersuche an einigen Beispielen, welche Grundstoffe am Aufbau unserer Nahrung beteiligt sind.
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802200) 4. Nahrungsmittel und Nährstoffe Experiment von: Phywe Gedruckt: 07.0.203 5:36:8 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802200) 4. Nahrungsmittel und Nährstoffe Experiment von: Phywe Gedruckt: 07.0.203 5:36:8 intertess (Version
Arbeitsheft Elektronenpaarbindung in molekularen Stoffen Jakob 1
 Arbeitsheft Elektronenpaarbindung in molekularen Stoffen Jakob 1 Inhaltsverzeichnis: 1 Die Bildung von Wasser 1.1 Atombindungsmodell für das Wasserstoff-Molekül 2 1.2 Vereinfacht: Aus einzelnen Atomen
Arbeitsheft Elektronenpaarbindung in molekularen Stoffen Jakob 1 Inhaltsverzeichnis: 1 Die Bildung von Wasser 1.1 Atombindungsmodell für das Wasserstoff-Molekül 2 1.2 Vereinfacht: Aus einzelnen Atomen
Schulversuch-Protokoll Jan gr. Austing
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
Was versteht man unter "ungesättigten" Kohlenwasserstoffen?
 Naturwissenschaften - Chemie - Organische Chemie - 2 Kohlenwasserstoffe (P77000) 2.4 Ethendarstellung Experiment von: PHYWE Gedruckt: 0.02.206 :0:32 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 2 Kohlenwasserstoffe (P77000) 2.4 Ethendarstellung Experiment von: PHYWE Gedruckt: 0.02.206 :0:32 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
ph-wert Berechnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation c(h 3 O + ) = c(säure)
 ph-wert Berehnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation (H 3 O + ) = (Säure) ph lg H 3 O Beispiel H 2 SO 4 (H 2 SO 4 ) = 0,1 mol/l (H 3 O + ) = 0,2 mol/l ph = -lg 0,2 = -(-0,699)
ph-wert Berehnung starke Säuren z.b. HCl, HNO 3, H 2 SO 4 vollständige Dissoziation (H 3 O + ) = (Säure) ph lg H 3 O Beispiel H 2 SO 4 (H 2 SO 4 ) = 0,1 mol/l (H 3 O + ) = 0,2 mol/l ph = -lg 0,2 = -(-0,699)
Schulversuchspraktikum. Michaela Micke. Sommersemester Klassenstufen 9 & 10. Chemie der Kohlenwasserstoffe. Methan & Erdgas
 Schulversuchspraktikum Michaela Micke Sommersemester 2012 Klassenstufen 9 & 10 Chemie der Kohlenwasserstoffe Methan & Erdgas 1 Konzept und Ziele 1 Auf einen Blick: Die vorliegende Unterrichtseinheit für
Schulversuchspraktikum Michaela Micke Sommersemester 2012 Klassenstufen 9 & 10 Chemie der Kohlenwasserstoffe Methan & Erdgas 1 Konzept und Ziele 1 Auf einen Blick: Die vorliegende Unterrichtseinheit für
Die Kerzenflamme (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer. Brennstoffe. Wir Unterscheiden grundsätzlich Brennstoffe in:
 Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
1.6 Wirkung von Säuren auf Metalle. Aufgabe. Wie wirken Säuren auf Metalle? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P757500).6 Wirkung von Säuren auf Metalle Experiment von: Phywe Gedruckt: 5.0.203 :39:04 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P757500).6 Wirkung von Säuren auf Metalle Experiment von: Phywe Gedruckt: 5.0.203 :39:04 intertess (Version 3.06 B200, Export 2000) Aufgabe
3.1. Prüfungsaufgaben zur Elektrostatik
 3.. Prüfungsaufgaben zur Elektrostatik ufgabe a: Fellinien Zeichne ie Fellinien für zwei verschoben parallel angeornete gleichnamig gelaenen Platten: Lösung: ufgabe b: Fellinien Zeichne ie Fellinien für
3.. Prüfungsaufgaben zur Elektrostatik ufgabe a: Fellinien Zeichne ie Fellinien für zwei verschoben parallel angeornete gleichnamig gelaenen Platten: Lösung: ufgabe b: Fellinien Zeichne ie Fellinien für
1.1.8 Radialsymmetrisches elektrisches Feld, Coulomb-Gesetz; Kapazität des Kugelkondensators
 8 Raialsymmetrisches elektrisches Fel, Coulomb-Gesetz; Kapazität es Kugelkonensators Die Felstärke im raialen Fel - as Coulombsche Gesetz Am Ene es letzten Kapitels wure ie Grungleichung es elektrischen
8 Raialsymmetrisches elektrisches Fel, Coulomb-Gesetz; Kapazität es Kugelkonensators Die Felstärke im raialen Fel - as Coulombsche Gesetz Am Ene es letzten Kapitels wure ie Grungleichung es elektrischen
Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )
![Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 ) Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )](/thumbs/74/69784240.jpg) 1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
2.8 Laugenbildung durch Reaktion von Metalloxiden mit Wasser. Aufgabe. Woraus lassen sich Laugen herstellen? (2)
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P759200) 2.8 Laugenbildung durch Reaktion von Metalloxiden mit Wasser Experiment von: Phywe Gedruckt: 5.0.203 2:6:25 intertess (Version 3.06
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P759200) 2.8 Laugenbildung durch Reaktion von Metalloxiden mit Wasser Experiment von: Phywe Gedruckt: 5.0.203 2:6:25 intertess (Version 3.06
Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser"
 Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser" a) Identifizierung des entstehenden Gases: Chemikalien: Geräte: Lithium [C] [F], Natrium [C] [F] (jeweils in Benzin mit Siedebereich 90-110
Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser" a) Identifizierung des entstehenden Gases: Chemikalien: Geräte: Lithium [C] [F], Natrium [C] [F] (jeweils in Benzin mit Siedebereich 90-110
Anhand welcher Eigenschaften lässt sich Sauerstoff identifizieren?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75400) 5. Nachweis von Sauerstoff Experiment von: Phywe Gedruckt:.0.203 3:00:4 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75400) 5. Nachweis von Sauerstoff Experiment von: Phywe Gedruckt:.0.203 3:00:4 intertess (Version 3.06 B200, Export 2000) Aufgabe
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Grundpraktikum für Biologen 2016
 Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
Grundpraktikum für Biologen 2016 31.03.2016 Übersicht # 2 Kovalente Bindung Freies Elektronenpaar Einzelnes Elektron Oktett erfüllt Einzelne Chloratome haben einen Elektronenmangel Reaktion zu Cl 2 erfüllt
HTL Kapfenberg pc_reifeprüfungsaufgaben_ma_11_bsp.31.mcd Seite 1 von 7
 HTL Kapfenberg p_reifeprüfungsaufgaben_ma Bsp.3.m Seie von 7 Angaben zu Aufgabe 3: Ein shwingfähiges mehanishes Sysem is mi einem geshwinigeisproporionalem Dämpfer ausgesae. Folgene in iesem Zusammenhang
HTL Kapfenberg p_reifeprüfungsaufgaben_ma Bsp.3.m Seie von 7 Angaben zu Aufgabe 3: Ein shwingfähiges mehanishes Sysem is mi einem geshwinigeisproporionalem Dämpfer ausgesae. Folgene in iesem Zusammenhang
Welche Eigenschaften besitzen Calcium- und Magnesiumlaugen?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P758900) 2.5 Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) Experiment von: Phywe Gedruckt: 5.0.203 2:3:05 intertess
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P758900) 2.5 Herstellung und Eigenschaften von Kalkwasser (Magnesiumhydroxidlösung) Experiment von: Phywe Gedruckt: 5.0.203 2:3:05 intertess
REDOXPROZESSE. Die Redoxreaktion setzt sich aus einer Oxidation und einer Reduktion zusammen. [1, 2]
![REDOXPROZESSE. Die Redoxreaktion setzt sich aus einer Oxidation und einer Reduktion zusammen. [1, 2] REDOXPROZESSE. Die Redoxreaktion setzt sich aus einer Oxidation und einer Reduktion zusammen. [1, 2]](/thumbs/29/13620695.jpg) Universität Regensburg Institut für Anorganische Chemie: Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge im Wintersemester 2012/13 23.11.2012 Dozentin: Dr. M. Andratschke Referentinnen: Stefanie
Universität Regensburg Institut für Anorganische Chemie: Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge im Wintersemester 2012/13 23.11.2012 Dozentin: Dr. M. Andratschke Referentinnen: Stefanie
3.11 Zerlegung von Wasser durch Reduktionsmittel. Aufgabe. Aus welchen Elementen besteht Wasser?
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P755500) 3. Zerlegung von Wasser durch Reduktionsmittel Experiment von: Seb Gedruckt: 24.03.204 :42:33
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P755500) 3. Zerlegung von Wasser durch Reduktionsmittel Experiment von: Seb Gedruckt: 24.03.204 :42:33
Die chemische Reaktion
 Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Aus den beiden Ausgangsstoffen (Edukten) entsteht ein neuer Stoff (Produkt) mit eigenen,
Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Aus den beiden Ausgangsstoffen (Edukten) entsteht ein neuer Stoff (Produkt) mit eigenen,
Logik / Kombinatorik - Hinweise zur Lösungsfindung
 Logik / Kombinatorik Hinweise zur Lösungsfinung Aufgabe 1) Günstige Bezeichnungen einführen; Tabelle anfertigen un ie unmittelbaren Folgerungen aus bis eintragen (siehe linke Tabelle). Da ies noch nicht
Logik / Kombinatorik Hinweise zur Lösungsfinung Aufgabe 1) Günstige Bezeichnungen einführen; Tabelle anfertigen un ie unmittelbaren Folgerungen aus bis eintragen (siehe linke Tabelle). Da ies noch nicht
,Prinzip: Versuchsaufbau - Variante I: Materialliste:
 Computer im Chemieunterricht Gaschromatographische Identifizierung Chromatogr.,Prinzip: Einige Kohlenwasserstoffe werden aus Carbiden im Minigasentwickler hergestellt. Weitere Kohlenwasserstoffe lassen
Computer im Chemieunterricht Gaschromatographische Identifizierung Chromatogr.,Prinzip: Einige Kohlenwasserstoffe werden aus Carbiden im Minigasentwickler hergestellt. Weitere Kohlenwasserstoffe lassen
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 1999/ Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 1999/ Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
7.5 Relativistische Bewegungsgleichung
 7.5. RELATIVISTISCHE BEWEGUNGSGLEICHUNG 7 7.5 Relativistishe Bewegungsgleihung Das Ziel ieses Abshnittes ist es, ie Bewegungsgleihung er Klassishen Mehanik an ie relativistishe Kinematik anzupassen. Ausgangspunkt
7.5. RELATIVISTISCHE BEWEGUNGSGLEICHUNG 7 7.5 Relativistishe Bewegungsgleihung Das Ziel ieses Abshnittes ist es, ie Bewegungsgleihung er Klassishen Mehanik an ie relativistishe Kinematik anzupassen. Ausgangspunkt
Schweizerische Maturitätsprüfung Gruppe / Kandidat/in Nr:... Winter 2010, Zürich Name/Vorname:...
 Gruppe / Kandidat/in Nr:... Name/Vorname:... Grundlagenfach Bereich Teil: NATURWISSENSCHAFTEN Chemie Verfasser: Richtzeit: Hilfsmittel: Hinweise: R. Guenin, J. Lipscher, S. Steiner 80 Minuten (von total
Gruppe / Kandidat/in Nr:... Name/Vorname:... Grundlagenfach Bereich Teil: NATURWISSENSCHAFTEN Chemie Verfasser: Richtzeit: Hilfsmittel: Hinweise: R. Guenin, J. Lipscher, S. Steiner 80 Minuten (von total
Lösungen für Klausur A
 Lösungen für Klausur A Aufgabe Skizze es Zelts im Querschnitt: h. (a) Aus sin folgt cos un aher h tan, also h. (b) Aus 9 4 4 folgt urch Wurzelziehen. Einsetzen von m in ie Beziehung aus (a) liefert h 6
Lösungen für Klausur A Aufgabe Skizze es Zelts im Querschnitt: h. (a) Aus sin folgt cos un aher h tan, also h. (b) Aus 9 4 4 folgt urch Wurzelziehen. Einsetzen von m in ie Beziehung aus (a) liefert h 6
Nachweis von Arsen mittels der Marshschen Probe
 Illumina-Chemie.de - Artikel Analytik Nachweis von Arsen mittels der Marshschen Probe Dieser Nachweis dient zum Nachweis von Arsen. Analog dazu können mit diesem Verfahren aber auch Antimon und Germanium
Illumina-Chemie.de - Artikel Analytik Nachweis von Arsen mittels der Marshschen Probe Dieser Nachweis dient zum Nachweis von Arsen. Analog dazu können mit diesem Verfahren aber auch Antimon und Germanium
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Hinweise zum möglichst effizienten Lernen mit Hilfe der Chemie-Arbeitshefte. 1 Vorbemerkungen. 1.1 Anforderungsniveaus
 g9_12_c_lernhinw.pdf 1/5 Hinweise zum möglichst effizienten Lernen mit Hilfe der Chemie-e Inhalt 1 Vorbemerkungen 1.1 Anforderungsniveaus (Vgl. Hinweise zur Biologie: g9_12_b_lernhinw.pdf) 1.2 Zum Aufbau
g9_12_c_lernhinw.pdf 1/5 Hinweise zum möglichst effizienten Lernen mit Hilfe der Chemie-e Inhalt 1 Vorbemerkungen 1.1 Anforderungsniveaus (Vgl. Hinweise zur Biologie: g9_12_b_lernhinw.pdf) 1.2 Zum Aufbau
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Hegel-Gymnasium Stuttgart-Vaihingen. Klasse 8
 24.September 2011 Hegel-Gymnasium Stuttgart-Vaihingen Curriculum Chemie Klasse 8 bis 10 Klasse 8 Kern- und Teilkompetenzen Kerncurriculum / Bildungsstandards / Teil der zentralen Jahrgangsarbeiten (ca.
24.September 2011 Hegel-Gymnasium Stuttgart-Vaihingen Curriculum Chemie Klasse 8 bis 10 Klasse 8 Kern- und Teilkompetenzen Kerncurriculum / Bildungsstandards / Teil der zentralen Jahrgangsarbeiten (ca.
Gruppentheorie und ihre Anwendungen in der Physik Ü5
 Frank Essenberger, Max Hoffmann 8. Juni 2007 Gruppentheorie un ihre Anwenungen in er Physik Ü5 Aufgabe 8 a) Als erstes müssen ie Gruppen bestimmt weren. Das Element E einer Gruppe G bilet immer einen Klasse
Frank Essenberger, Max Hoffmann 8. Juni 2007 Gruppentheorie un ihre Anwenungen in er Physik Ü5 Aufgabe 8 a) Als erstes müssen ie Gruppen bestimmt weren. Das Element E einer Gruppe G bilet immer einen Klasse
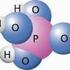
man sagt : Phosphor + Sauerstoff reagieren Tetraphosphorzu dekaoxid
 Die Luft 1.Versuch Wir entzünden eine Kerze und stülpen ein Becherglas darüber. Beobachtung : Nach kurzer Zeit erlischt die Flamme. Feststellung : Für die Verbrennung in unserer Umwelt ist Luft notwendig.
Die Luft 1.Versuch Wir entzünden eine Kerze und stülpen ein Becherglas darüber. Beobachtung : Nach kurzer Zeit erlischt die Flamme. Feststellung : Für die Verbrennung in unserer Umwelt ist Luft notwendig.
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Stationenlernen Chemie im Paket. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stationenlernen Chemie im Paket Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 59149 Stationenlernen:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stationenlernen Chemie im Paket Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 59149 Stationenlernen:
Vom Alkohol zum Alken
 1 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufe 9 & 10 Vom Alkohol zum Alken 2 Auf einem Blick: Diese Unterrichtseinheit für die Klasse 9 & 10 enthält Lehrerversuche und 1 Schülerversuch
1 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufe 9 & 10 Vom Alkohol zum Alken 2 Auf einem Blick: Diese Unterrichtseinheit für die Klasse 9 & 10 enthält Lehrerversuche und 1 Schülerversuch
FACHHOCHSCHULE HEILBRONN Hochschule für Technik und Wirtschaft Fachbereich Feinwerktechnik Prof. Dr.-Ing. J. Wild
 FACHHOCHSCHULE HEILBRONN Hohshule für Tehnik un Wirtshaft Fahereih Feinwerktehnik Prof. Dr.-Ing. J. Wil Leistungsnahweis im SS 1996 zum Diplomzeugnis Prüfungsfah: 3382 Getrieelehre 2 FT5 Zeit: 120 min
FACHHOCHSCHULE HEILBRONN Hohshule für Tehnik un Wirtshaft Fahereih Feinwerktehnik Prof. Dr.-Ing. J. Wil Leistungsnahweis im SS 1996 zum Diplomzeugnis Prüfungsfah: 3382 Getrieelehre 2 FT5 Zeit: 120 min
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Ruolf Feile Dipl. Phys. Markus Domschke Sommersemester 00 4. 8. Juni 00 Physik für Bauingenieure Übungsblatt 9 Gruppenübungen. Konensator Zwei quaratische Metallplatten mit
Fachbereich Physik Prof. Dr. Ruolf Feile Dipl. Phys. Markus Domschke Sommersemester 00 4. 8. Juni 00 Physik für Bauingenieure Übungsblatt 9 Gruppenübungen. Konensator Zwei quaratische Metallplatten mit
MS Michelson-Interferometer
 MS Michelson-Interferometer Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grunlagen 2 1.1 Aufbau.................................... 2 1.2 Interferenzmuster...............................
MS Michelson-Interferometer Blockpraktikum Herbst 2007 (Gruppe 2b) 24. Oktober 2007 Inhaltsverzeichnis 1 Grunlagen 2 1.1 Aufbau.................................... 2 1.2 Interferenzmuster...............................
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 2004/2005 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 2004/2005 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
 Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Die chemische Reaktion
 Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Beobachtung : Der gelbe Schwefel verbrennt mit blauer Flamme. Dabei wird Wärme frei und
Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Beobachtung : Der gelbe Schwefel verbrennt mit blauer Flamme. Dabei wird Wärme frei und
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
1. Probeklausur. φ = 2x 2 y(z 1).
 Übungen zur T: Theoretische Mechanik, SoSe04 Prof. Dr. Dieter Lüst Theresienstr. 37, Zi. 45. Probeklausur Dr. Reinke Sven Isermann Reinke.Isermann@lmu.e Übung.: Gegeben sei ie Funktion φ = x y z. a Berechnen
Übungen zur T: Theoretische Mechanik, SoSe04 Prof. Dr. Dieter Lüst Theresienstr. 37, Zi. 45. Probeklausur Dr. Reinke Sven Isermann Reinke.Isermann@lmu.e Übung.: Gegeben sei ie Funktion φ = x y z. a Berechnen
Redoxreaktionen. Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden
 Nach Lavoisier: : Redoxreaktionen Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden Aufnahme von Sauerstoff zb.: Verbrennen von Magnesium : Abgabe von Sauerstoff
Nach Lavoisier: : Redoxreaktionen Redoxreaktionen: Reaktionen bei denen Elektronen zwischen den Komponenten übertragen werden Aufnahme von Sauerstoff zb.: Verbrennen von Magnesium : Abgabe von Sauerstoff
Lösungen Kap. 4 Die chemische Reaktion
 Elemente Grundlagen der Chemie für Schweizer Maturitätsschulen Klett und Balmer Verlag Zug 2007 Verwendung für den Gebrauch in der eigenen Klasse gestattet Lösungen Kap. 4 Die chemische Reaktion Lösungen
Elemente Grundlagen der Chemie für Schweizer Maturitätsschulen Klett und Balmer Verlag Zug 2007 Verwendung für den Gebrauch in der eigenen Klasse gestattet Lösungen Kap. 4 Die chemische Reaktion Lösungen
Chemische Reaktionen. Wir erzeugen Wasser
 hemische Reaktionen + Natrium + -> hlor -> Natriumchlorid = Kochsalz Wir erzeugen Wasser Die kleinsten Teilchen des Sauerstoffes und des Wasserstoffes waren im roten Ballon bereits gut durchmischt. Daher
hemische Reaktionen + Natrium + -> hlor -> Natriumchlorid = Kochsalz Wir erzeugen Wasser Die kleinsten Teilchen des Sauerstoffes und des Wasserstoffes waren im roten Ballon bereits gut durchmischt. Daher
Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur
 Versuchsanweisung: Eigenschaften von Alkoholen, die ydroxylgruppe als funktionelle Gruppe Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur Organische Substanzen bestehen zum
Versuchsanweisung: Eigenschaften von Alkoholen, die ydroxylgruppe als funktionelle Gruppe Eigenschaften von Alkanolen (Alkohole) und deren Erklärung aus der Struktur Organische Substanzen bestehen zum
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1
 Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1 Brownsche Bewegung Beobachte die Bewegung von Rauchteilchen unter dem Miskroskop. Wie kann man die vom schottischen Botaniker
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1 Brownsche Bewegung Beobachte die Bewegung von Rauchteilchen unter dem Miskroskop. Wie kann man die vom schottischen Botaniker
Stöchiometrie. Unterrichtsideen für ein trockenes Thema. Schweizerische Chemische Gesellschaft, 22. Aug Workshop C2
 Schweizerische Chemische Gesellschaft, 22. Aug. 2017 Workshop C2 Stöchiometrie Unterrichtsideen für ein trockenes Thema an Amadeus Bärtsch, Fachdidaktik ETH Zürich www.fdchemie.pbworks.com Vorwort Ideen
Schweizerische Chemische Gesellschaft, 22. Aug. 2017 Workshop C2 Stöchiometrie Unterrichtsideen für ein trockenes Thema an Amadeus Bärtsch, Fachdidaktik ETH Zürich www.fdchemie.pbworks.com Vorwort Ideen
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Protokoll Tag 3. C. Kationennachweise. C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4
 Protokoll Tag 3 C. Kationennachweise C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4 V16 Nachweis von Na +, K +, Ca 2+, Sr 2+ und Ba 2+ durch Flammenfärbung Bei der Flammenprobe geht es
Protokoll Tag 3 C. Kationennachweise C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4 V16 Nachweis von Na +, K +, Ca 2+, Sr 2+ und Ba 2+ durch Flammenfärbung Bei der Flammenprobe geht es
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Auswertung der Lernbegleitbögen zu Beginn der Unterrichtseinheit
 Fragestellung des Lernbegleitbogens Du hast bereits verschiedene Oxidationsreaktionen (hier als Reaktionen von Stoffen mit Sauerstoff) kennen gelernt. Auffällig ist, dass sich Oxidationsreaktionen deutlich
Fragestellung des Lernbegleitbogens Du hast bereits verschiedene Oxidationsreaktionen (hier als Reaktionen von Stoffen mit Sauerstoff) kennen gelernt. Auffällig ist, dass sich Oxidationsreaktionen deutlich
Licht und Farbe - Dank Chemie!
 Licht und Farbe - Dank Chemie! Folie 1 Was verstehen wir eigentlich unter Licht? Licht nehmen wir mit unseren Augen wahr Helligkeit: Farbe: Schwarz - Grau - Weiß Blau - Grün - Rot UV-Strahlung Blau Türkis
Licht und Farbe - Dank Chemie! Folie 1 Was verstehen wir eigentlich unter Licht? Licht nehmen wir mit unseren Augen wahr Helligkeit: Farbe: Schwarz - Grau - Weiß Blau - Grün - Rot UV-Strahlung Blau Türkis
4.4 Borax-Probe. Aufgabe. Wie lässt sich Methanol von Ethanol unterscheiden? (1) Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77900) 4.4 Borax-Probe Experiment von: Anouch Gedruckt: 25.02.204 3:45:2 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wie lässt
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77900) 4.4 Borax-Probe Experiment von: Anouch Gedruckt: 25.02.204 3:45:2 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wie lässt
REDOX-REAKTIONEN Donator-Akzeptor-Konzept! So geht s: schrittweises Aufstellen von Redoxgleichungen Chemie heute
 REDOXREAKTIONEN In den letzten Wochen haben wir uns mit SäureBaseReaktionen und Redoxreaktionen beschäftigt. Viele Phänomene in uns und um uns herum sind solche Redoxreaktionen. Nun müssen wir unseren
REDOXREAKTIONEN In den letzten Wochen haben wir uns mit SäureBaseReaktionen und Redoxreaktionen beschäftigt. Viele Phänomene in uns und um uns herum sind solche Redoxreaktionen. Nun müssen wir unseren
Chemie: Nachweisreaktionen
 Chemie: Nachweisreaktionen 1. Nachweis von Elementen und Verbindungen a) Nachweis von Wasserstoff Wasserstoff H2 Nachweis: Knallgasprobe Durchführung: verschlossenes Reagenzglas wird waagerecht mit der
Chemie: Nachweisreaktionen 1. Nachweis von Elementen und Verbindungen a) Nachweis von Wasserstoff Wasserstoff H2 Nachweis: Knallgasprobe Durchführung: verschlossenes Reagenzglas wird waagerecht mit der
19. Ladungstransport über Wasserstoffbrückenbindungen. 1. Aufgabe
 19. Ladungstransport über Wasserstoffbrükenbindungen 1 19. Ladungstransport über Wasserstoffbrükenbindungen 1. Aufgabe Untersuhung der spezifishen Leitfähigkeit von Cl- bzw. KCl-haltigen Methanol/Wasser
19. Ladungstransport über Wasserstoffbrükenbindungen 1 19. Ladungstransport über Wasserstoffbrükenbindungen 1. Aufgabe Untersuhung der spezifishen Leitfähigkeit von Cl- bzw. KCl-haltigen Methanol/Wasser
Klasse 8 / 9 / 10 Blatt 1
 Klasse 8 / 9 / 0 Blatt Abkürzungen: n: () Stoffe und ihre Eigenschaften () Stoffe und ihre Teilchen () Chemische Reaktionen () Ordnungsprinzipien () Arbeitsweise () Umwelt und Gesellschaft en: (M) Methodenkompetenz
Klasse 8 / 9 / 0 Blatt Abkürzungen: n: () Stoffe und ihre Eigenschaften () Stoffe und ihre Teilchen () Chemische Reaktionen () Ordnungsprinzipien () Arbeitsweise () Umwelt und Gesellschaft en: (M) Methodenkompetenz
Klausur 4 Kurs 12Ph2 Physik-e
 007-06-1 Kausur 4 Kurs 1Ph Physik-e Lösung Version 007-07-03 1 Eräutern Sie, warum bei er Wehsespannung ie Sheitespannung immer größer as ie effektive Spannung ist un berehnen Sie ie Sheitespannung für
007-06-1 Kausur 4 Kurs 1Ph Physik-e Lösung Version 007-07-03 1 Eräutern Sie, warum bei er Wehsespannung ie Sheitespannung immer größer as ie effektive Spannung ist un berehnen Sie ie Sheitespannung für
a) b) Abb. 1: Buchstaben
 Hans Walser, [20171019] Magische Quarate ungeraer Seitenlänge nregung: uler (1782) 1 Worum geht es? Zu einer gegebenen ungeraen Zahl u wir ein magisches Quarat mit er Seitenlänge u konstruiert. 2 as Vorgehen
Hans Walser, [20171019] Magische Quarate ungeraer Seitenlänge nregung: uler (1782) 1 Worum geht es? Zu einer gegebenen ungeraen Zahl u wir ein magisches Quarat mit er Seitenlänge u konstruiert. 2 as Vorgehen
Herstellen gasförmiger Kohlenwasserstoffe Gaschromatografische Identifizierung. Präparategläschen mit Kappe und Septum Kanüle 0,6 mm
 Prinzip Einige Kohlenwasserstoffe werden aus Carbiden im Minigasentwickler hergestellt. Weitere Kohlenwasserstoffe lassen sich mit Hilfe des Perlkatalysators, der normalerweise bei Crackversuchen eingesetzt
Prinzip Einige Kohlenwasserstoffe werden aus Carbiden im Minigasentwickler hergestellt. Weitere Kohlenwasserstoffe lassen sich mit Hilfe des Perlkatalysators, der normalerweise bei Crackversuchen eingesetzt
Mathematik III. Vorlesung 87. Die äußere Ableitung
 Prof. Dr. H. Brenner Osnabrück WS 2010/2011 Mathematik III Vorlesung 87 Die äußere Ableitung In ieser Vorlesung weren wir ein neuartiges mathematisches Objekt kennenlernen, ie sogenannte äußere Ableitung.
Prof. Dr. H. Brenner Osnabrück WS 2010/2011 Mathematik III Vorlesung 87 Die äußere Ableitung In ieser Vorlesung weren wir ein neuartiges mathematisches Objekt kennenlernen, ie sogenannte äußere Ableitung.
