Methodenerstellung und Validierung von Käse
|
|
|
- Gerda Heike Bach
- vor 7 Jahren
- Abrufe
Transkript
1 Eiweißbestimmung mit Sprint Methodenerstellung und Validierung von Käse von Mag. Agnes Wolf
2 Inhaltsverzeichnis 1 Zielsetzung Käse 4 2 Methoden Bestimmung des Eiweißgehaltes in Fleisch- und Fleischerzeugnissen: 5 Kurzbeschreibung Chemikalien Geräte und Hilfsmittel Probenahme und Probenvorbereitung Auswertung 7 Berechnung Literatur Bestimmung des Eiweißgehaltes mit dem Sprint 8 3 Ergebnisse: Eiweißbestimmung anhand der Kjeldahl-Methode: Optimierung der Einwaage: Erstellen der Referenzgerade durch Aufnehmen von 4 Referenzen zur Vergleich Eiweißbestimmung Kjeldahl mit Sprint: 11 4 Rohdaten: Eiweißbestimmung anhand der Kjeldahl-Methode: Erstellen der Referenzgerade durch Aufnehmen von 4 Referenzen zur Eiweißbestimmung durch Sprint: 14 Mai 2009 Seite 2 von 14
3 1 Zielsetzung Im Rahmen dieses Projekts wird ein neues Verfahren zur Bestimmung des Proteingehalts angestrebt. Im Sprint wird für die Bestimmung des Proteingehaltes ein biochemische Methode genutzt (siehe unter Methoden). Es wird zunächst versucht die Proteinbestimmung von Brühwürsten zu optimieren und die Ergebnisse dieser Bestimmung mit jener der Standardmethode Kjeldahl zu vergleichen. Käse Validierung geg. Kjeldahl Methodenerstellung Parameter: 1. Einwaage 2. Homogenisierungszeit 3. Toleranzen ermitteln 4. Unterschiedlichkeit der Proben Zusammenfassung des Einzelprojekts Darstellung 1: Zusammenfassung der Arbeitsschritte anhand eines Flußdiagramms. Mai 2009 Seite 3 von 14
4 1.1 Käse. Es wurden folgende Käsesorten verwendet: Käsesorten Probennummer Tilsiter 1 Holländer 2 Toastkäse 3 Schafskäse 4 Tabelle 1.1 Verwendete Käsesorten Mai 2009 Seite 4 von 14
5 2 Methoden Die unten beschriebene Methode wurde nach LMBG 35 modifiziert. 2.1 Bestimmung des Eiweißgehaltes in Fleisch- und Fleischerzeugnissen: Unter dem Rohproteingehalt wird der nach dem hier beschriebenen Verfahren nach Kjeldahl ermittelte Stickstoffgehalt multipliziert mit dem Faktor 6,25 verstanden. Er wird in g/100g der Probe angegeben. Kurzbeschreibung Der organisch gebundene Stickstoff wird mit konzentrierter Schwefelsäure unter Zusatz eines Katalysatorgemisches oxidativ aufgeschlossen. Aus dem entstandenen Ammoniumsulfat wird der durch NaOH-Zusatz freigesetzte Ammoniak mit Hilfe einer Wasserdampfdestillation in eine borsäurehältige Vorlage übergetrieben und mit Salzsäure-Maßlösung titrimetrisch bestimmt Chemikalien Soweit nicht anders angegeben, sind analysenreine Chemikalien zu verwenden. Unter Lösung ist immer eine wässrige Lösung zu verstehen. Das Wasser muss entweder destilliert oder von entsprechender Reinheit sein. Selen- und quecksilberfreier Titandioxid-Katalysator (Kjeldahl Tabletten) Eine Tablette (5 g) bestehet aus 1,8% Titandioxid, 2,8% Kupfersulfat (wasserfrei) und 95,4% Kaliumsulfat, Merck Schwefelsäure (Massenanteil: w = etwa 98%) geeignet zur Stickstoffbestimmung, Merck Natriumhydroxid-Lösung stickstofffrei (Massenkonzentration: = mind. 32 g/100 ml, Merck) gesättigte Lösung von Borsäure (reinst), Merck Mischindikator von Merck (Nr ) Salzsäure-Maßlösung (Stoffmengenkonzentration: c=0,1 mol/l; 0,1N), Merck Geräte und Hilfsmittel Wägeschiffchen aus stickstofffreiem Pergamentpapier oder anderem zur Stickstoffbestimmung geeignetem Material, Schleicher und Schüll Kjeldahl-Aufschlußkolben Mai 2009 Seite 5 von 14
6 entsprechend der verwendeten Apparatur, Büchi Intensivheizgerät Heizblock, Digestion Unit K-435, Büchi Apparatur für die Stickstoffbestimmung Büchi, Destillation Unit 324, Fa. Büchi Bürette Brand, 50ml 500 ml Standkolben Präzisionswaage AB204-S/M von Mettler-Toledo Probenahme und Probenvorbereitung Die Fleisch- und Fleischerzeugnisproben werden mechanisch homogenisiert Durchführung Beim Arbeiten mit konzentrierter Schwefelsäure müssen Labormantel, Handschuhe und Schutzbrille getragen werden Vorbereitung der Probe Vor der Analyse soll die Probe Zimmertemperatur haben. Ein vorheriges Durchrühren von Hand ist erforderlich Bestimmung In ein Wägeschiffchen werden etwa 2 g der gut homogenisierten Probe auf 1 mg genau eingewogen. Das Schiffchen wird in einen Kjeldahl-Aufschlußkolben gegeben. Dann werden 20 ml Schwefelsäure und eine Kjeldahltablette zugesetzt und zur Oberflächenvergrößerung kräftig geschüttelt. Anschliessend wird der Kolbeninhalt zunächst vorsichtig (Stufe 5-6), dann kräftiger auf 400 bis 410 C erhitzt. (Anmerkung: ist erreichbar mit Stufe 8 bis 10.) Der Aufschluss ist beendet, wenn die Lösung klar und grün geworden ist. Nachdem der Kolbeninhalt auf 50 bis 60 C abgekühlt ist, wird der Kolben in die Kjeldahlapparatur eingesetzt. In einen 500ml Standkolben werden 2 Tropfen Indikator gegeben. Der so beschickte Kolben wird unter den Kühlerauslauf der Apparatur für die Stickstoffbestimmung gestellt. Die Destillation wird mit der Methode 4 durchgeführt. Zunächst wird die Probe mit 50 ml Wasser verdünnt, weiters werden in den Titrierkolben 60ml Borsäure vorgelegt, wobei darauf zu achten ist, dass der Auslauf in die Borsäure eintaucht. Anschließend wird die verdünnte Probenlösung mit Natronlauge im Überschuss (etwa 90 ml) versetzt. Nach der Durchmischung muss ein deutlicher Überschuss an Natronlauge, erkennbar Mai 2009 Seite 6 von 14
7 an der Farbkonstanz der Lösung, vorhanden sein. Der durch die NaOH freigesetze Ammoniak wird mittels Wasserdampf überdestilliert und in der borsäurehältigen Vorlage aufgefangen. Auf Kühlung ist zu achten, da sich die Vorlage bei der Destillation nicht erwärmen darf. Nach 5 Minuten ist die Destillation beendet und die Probe kann nach Ertönen eines akustischen Signals aus der Apparatur entnommen werden. Nach Abspülen des Kühlerauslaufs mit Wasser in die Vorlage wird mit Salzsäure (0,1 mol/l entspricht 0,1 N) bis zum Farbumschlag über grün nach rosa titriert Auswertung Berechnung Der Gesamtstickstoffgehalt in % (entspricht g/100g Probe) wird nach folgender Gleichung berechnet: % Stickstoff = (V * 0, * 100) / m V m Verbrauch an 0,1N HCl in ml Probeneinwaage in g Das Ergebnis wird auf zwei Stellen nach dem Komma gerundet angegeben. Der Rohproteingehalt in % wird nach folgender Gleichung berechnet: % Eiweiss = % Stickstoff * 6,25 Das Ergebnis wird auf zwei Stellen nach dem Komma gerundet angegeben Literatur 1.Amtliche Methodensammlung von Untersuchungsverfahren nach Paragraph 35 LMBG, Herausgeber: Bundesgesundheitsamt, Beuth-Verlag, Loseblattsammlung, L Mai 2009 Seite 7 von 14
8 2.2 Bestimmung des Eiweißgehaltes mit dem Sprint 1. Erstellen einer neuen Methode: vom Hauptmenü ausgehend Service mode aktivieren in Edit/Create Method entsprechenden Ordner auswählen (ANALYTICUM) Neue Methodenamen über Tastatur eingeben, Buchstaben mit Enter aktivieren; Methodennamen akzeptieren Entsprechende Parameter (entsprechend Material) eingeben: Material Solid Homogenize Speed Homogenize Time 90 Filter high normal Delay time 0 Settling time 90 Min Weight 0,7 Max Weight 0,8 Min Protein 16 Max Protein 30 Bias 0 mit ADD (auf der rechten Seite) entsprechende Referenzen eingeben (üblich 2 bis 3 Standards mit unterschiedlichen Eiweißgehalt!) mit ADD (unterhalb) - Aufnehmen von Messungen der Referenzproben (üblich sind 3 Wiederholungen!) 2. Messung des Proteingehaltes Filter einlegen Probenbecher auf die externe Waage stellen Tarieren des Probenbechers Entsprechendes Probenvolumen hineingeben (Vorsicht: Probenmaterial darf nicht am Rand des Bechers kleben falsche Messung!) Weiters WICHTIG: für einen erwarteten Proteingehalt von 12 % sollten nicht mehr als 1 Gramm eingewogen werden!! Eine Eiweißbestimmung dauert in etwa 3 Minuten; Die Speicherung erfolgt automatisch Mai 2009 Seite 8 von14
9 3 Ergebnisse: 3.1 Eiweißbestimmung anhand der Kjeldahl-Methode: Die Durchführung erfolgte wie unter Methoden beschrieben. Käse Eiweißgehalt in % MW [%] StabW Toastkäse 16,02 ± 0,13 Schafskäse 20,41 ± 0,11 Tilsiter 29,59 ± 0,21 Holländer 29,94 ± 0,15 Tabelle 3.1 Mittelwert und Standardabweichung der Eiweißbestimmung nach der Kjeldahlmethode. Eiweißbestimmung nach Kjeldahl 35,00% 30,00% 25,00% 20,00% 15,00% 10,00% 5,00% 0,00% Toastkäse Schafskäse Tilsiter Holländer Eiweiß [%] Käseprodukte Diagramm 2: Eiweißbestimmung der verschiedenen Käsesorten. Mai 2009 Seite 9 von14
10 3.2 Optimierung der Einwaage: Als optimale Einwaage wurde zunächst 0,7 bis 0,9 Gramm angenommen. Es stellte sich im Rahmen der Messungen eine optimale Einwaage von 0,7 bis 0,8 Gramm dar. 3.3 Erstellen der Referenzgerade durch Aufnehmen von 4 Referenzen zur Eiweißbestimmung mit Sprint: Für die Kalibrierung wurden 4 Referenzproben verwendet. Es wurden bei jeder Probe 3 Messungen durchgeführt. Weiters konnte durch Auswahl bestimmter Werte (Signal/Masse) ein r 2 von 0,9991 erzielt werden. Wurstart Probennummer Eiweiß [%] MW Toastkäse 1 16,02% 0,8024 Schafskäse 2 20,41% 0,8971 Tilsiter 3 29,57% 1,2140 Holländer 4 29,94% 1,2440 Tabelle 3.6.1: Mittelwert der erhaltenen Signale um Kalibrierung zu erstellen. Kalibrierung: Eiweiß [%] 28,00% 25,00% 22,00% 19,00% 16,00% 0,8 0,9 1 1,1 1,2 1,3 Signal [S/M] Reihe1 Trendlinie Diagramm 4: Kalibrierung für die Eiweißbestimmung. Mai 2009 Seite 10 von14
11 3.4 Vergleich Eiweißbestimmung Kjeldahl mit Sprint: Käseart Kjeldahl Eiweiß MW [%] StabW Sprint Eiweiß MW [%] StabW Toastkäse 16,02 ± 0,13 16,13 ± 0,01 Schafskäse 20,41 ± 0,11 20,60 ± 0,19 Tilsiter 29,59 ± 0,21 29,36 ± 0,04 Sorte 4 29,94 ± 0,15 29,83 ± 0,14 Tabelle 3.7.1: Vergleich der Mittelwerte der Eiweißbestimmung Sprint mit Kjeldahl. Wie aus der Tabelle ersichtlich, konnten vergleichbare Werte erzielt werden. Mai 2009 Seite 11 von14
12 4 Rohdaten: 4.1 Eiweißbestimmung anhand der Kjeldahl-Methode: Käseart Probennummer Messung Eiweißgehalt [%] Toastkäse Probe , ,89 MW [%] 16,02 s [%] ± 0,13 Tilsiter Probe ,8 2 29,37 MW [%] 29,59 s [%] ± 0,21 Schafskäse Probe , ,57 MW [%] 20,41 s [%] ± 0,11 Holländer Probe , ,08 MW [%] 29,94 s [%] ± 0,15 Tabelle 4.1: In dieser Tabelle sind die Rohdaten der Eiweißbestimmung durch die Kjeldahl-Methode angeführt. Mai 2009 Seite 12 von14
13 4.2 Erstellen der Referenzgerade durch Aufnehmen von 4 Referenzen zur Eiweißbestimmung mit Sprint: Erstellen der Referenzwerte: Käseart Probennummer Eiweiß[%] Signal/Masse Einwaage Schafskäse Probe 4 20,41% *0,8852 0,6992 *0,9090 0,7148 Toastkäse Probe3 16,02% *0,7897 0,7586 *0,8012 0,7658 *0,8163 0,7851 Tilsiter Probe1 29,59% *1,2176 0,7292 *1,2134 0,7372 *1,2103 0,7299 Holländer Probe 2 26,94% *1,2686 0,7709 *1,2214 0,7122 *1,2413 0,7352 Tabelle 4.2: Erstellung der Referenzwerte für die Eiweißbestimmung Mai 2009 Seite 13 von14
14 4.3 Eiweißbestimmung durch Sprint: Käseart Probennummer Messung Eiweißgehalt [%] Toastkäse Probe , , ,12 MW [%] 16,13 s [%] ± 0,01 Schafskäse Probe , , ,46 MW [%] 20,60 s [%] ± 0,19 Tilsiter Probe , , ,39 MW [%] 29,36 s [%] ± 0,16 Holländer Probe , , ,63 MW [%] 29,83 s [%] ± 0,14 Tabelle 4.3: In dieser Tabelle sind die Rohdaten der Eiweißbestimmung durch Sprint angeführt. Mai 2009 Seite 14 von14
Methodenerstellung und Validierung von Sojaprodukten
 Eiweißbestimmung mit Sprint Methodenerstellung und Validierung von Sojaprodukten von Mag. Agnes Wolf Inhaltsverzeichnis 1 Zielsetzung 3 1.1 Sojaprodukte 4 2 Methoden 5 2.1 Bestimmung des Eiweißgehaltes
Eiweißbestimmung mit Sprint Methodenerstellung und Validierung von Sojaprodukten von Mag. Agnes Wolf Inhaltsverzeichnis 1 Zielsetzung 3 1.1 Sojaprodukte 4 2 Methoden 5 2.1 Bestimmung des Eiweißgehaltes
Methodenerstellung und Validierung von Rohwürsten
 Eiweißbestimmung mit Sprint Methodenerstellung und Validierung von Rohwürsten von Mag. Agnes Wolf Homogenisierung mit CryoMill! Rohwurst Inhaltsverzeichnis 1 Zielsetzung 3 1.1 Rohwürste 4 2 Methoden 5
Eiweißbestimmung mit Sprint Methodenerstellung und Validierung von Rohwürsten von Mag. Agnes Wolf Homogenisierung mit CryoMill! Rohwurst Inhaltsverzeichnis 1 Zielsetzung 3 1.1 Rohwürste 4 2 Methoden 5
Methodenerstellung und Validierung von Kochwürsten
 Eiweißbestimmung mit Sprint Methodenerstellung und Validierung von Kochwürsten von Agnes Wolf Brühwurst Inhaltsverzeichnis 1 Zielsetzung 3 1.1 Brühwürste 4 2 Methoden 5 2.1 Bestimmung des Eiweißgehaltes
Eiweißbestimmung mit Sprint Methodenerstellung und Validierung von Kochwürsten von Agnes Wolf Brühwurst Inhaltsverzeichnis 1 Zielsetzung 3 1.1 Brühwürste 4 2 Methoden 5 2.1 Bestimmung des Eiweißgehaltes
PROTEINBESTIMMUNG MIT ITAG SPRINT EINE NEUE RASCHE BESTIMMUNG DES EIWEISSGEHALTES IN VERSCHIEDENEN LEBENSMITTELN. A. Wolf 1, M.
 PROTEINBESTIMMUNG MIT ITAG SPRINT EINE NEUE RASCHE BESTIMMUNG DES EIWEISSGEHALTES IN VERSCHIEDENEN LEBENSMITTELN A. Wolf 1, M. Lang 1 1 Analyticum-Labor für Lebensmitteluntersuchung, Parkring 1 A-874 Grambach,
PROTEINBESTIMMUNG MIT ITAG SPRINT EINE NEUE RASCHE BESTIMMUNG DES EIWEISSGEHALTES IN VERSCHIEDENEN LEBENSMITTELN A. Wolf 1, M. Lang 1 1 Analyticum-Labor für Lebensmitteluntersuchung, Parkring 1 A-874 Grambach,
NEU KJELDAHL CHEMIKALIEN UND KOLBEN FÜR DIE STICKSTOFFBESTIMMUNG
 NEU KJELDAHL CHEMIKALIEN UND KLBEN FÜR DIE STICKSTFFBESTIMMUNG KJELDAHL-KLBEN Die birnenförmigen Kolben mit langem Hals kommen vorwiegend bei der Bestimmung von organisch gebundenem Stickstoff zum Einsatz.
NEU KJELDAHL CHEMIKALIEN UND KLBEN FÜR DIE STICKSTFFBESTIMMUNG KJELDAHL-KLBEN Die birnenförmigen Kolben mit langem Hals kommen vorwiegend bei der Bestimmung von organisch gebundenem Stickstoff zum Einsatz.
Bestimmung des Stickstoffgehalts von Erde
 Bestimmung des Stickstoffgehalts von Erde Schülerversuch, ca. 25 Minuten Experiment Teil 1 Material und Chemikalien: Ofentrockene Erde Kaliumchloridlösung (c = 2 mol/l) Flasche (250 ml) Trichter Filterpapier
Bestimmung des Stickstoffgehalts von Erde Schülerversuch, ca. 25 Minuten Experiment Teil 1 Material und Chemikalien: Ofentrockene Erde Kaliumchloridlösung (c = 2 mol/l) Flasche (250 ml) Trichter Filterpapier
3 Kjeldahl-Kolben, 500 ml Weithals-Erlenmeyerkolben, 10 ml Vollpipette,
 Instrumentelle Bestimmungsverfahren 227 Versuch 451: Bestimmung von Stickstoff Arbeitsanleitung Geräteliste: KJELDAHL-Apparatur, 3 Kjeldahl-Kolben, 500 ml Weithals-Erlenmeyerkolben, 20 ml Vollpipette,
Instrumentelle Bestimmungsverfahren 227 Versuch 451: Bestimmung von Stickstoff Arbeitsanleitung Geräteliste: KJELDAHL-Apparatur, 3 Kjeldahl-Kolben, 500 ml Weithals-Erlenmeyerkolben, 20 ml Vollpipette,
Application Bulletin
 Application Bulletin Von Interesse für: Allgemein analytische Laboratorien; Lebensmittel A D 1, 2, 3, 4, 7, 8, 11 Umweltschutz; Dünger Bestimmung von Ammonium oder Kjeldahl- Stickstoff Zusammenfassung
Application Bulletin Von Interesse für: Allgemein analytische Laboratorien; Lebensmittel A D 1, 2, 3, 4, 7, 8, 11 Umweltschutz; Dünger Bestimmung von Ammonium oder Kjeldahl- Stickstoff Zusammenfassung
Lebensmittelverfahrenstechnik
 Fachhochschule Trier, Fachbereich BLV Studiengang Lebensmitteltechnik Lebensmittelverfahrenstechnik - Laborübung - 3. Semester Name:...... Datum:... Versuch: Bestimmung des Feuchtigkeitsgehalts in Getreidemehl
Fachhochschule Trier, Fachbereich BLV Studiengang Lebensmitteltechnik Lebensmittelverfahrenstechnik - Laborübung - 3. Semester Name:...... Datum:... Versuch: Bestimmung des Feuchtigkeitsgehalts in Getreidemehl
Bestimmung des Lactosegehalts in der Milch
 Bestimmung des Lactosegehalts in der Milch Prinzip: Die geklärte Zuckerlösung, welche reduzierende Zucker (z.b. Lactose oder Glucose) enthält, wird mit Kupfer(II)-Lösung versetzt. Cu 2+ -Ionen werden teilweise
Bestimmung des Lactosegehalts in der Milch Prinzip: Die geklärte Zuckerlösung, welche reduzierende Zucker (z.b. Lactose oder Glucose) enthält, wird mit Kupfer(II)-Lösung versetzt. Cu 2+ -Ionen werden teilweise
Abhängigkeit der Reaktionsgeschwindigkeit (RG) von der Konzentration: Kalk (CaCO 3 ) + Salzsäure (HCl)
 Abhängigkeit der Reaktionsgeschwindigkeit Abhängigkeit der Reaktionsgeschwindigkeit (RG) von der Konzentration: Kalk (CaCO 3 ) + Salzsäure (HCl) Beim Lösen von Kalk in Salzsäure bildet sich ein gut wasserlösliches
Abhängigkeit der Reaktionsgeschwindigkeit Abhängigkeit der Reaktionsgeschwindigkeit (RG) von der Konzentration: Kalk (CaCO 3 ) + Salzsäure (HCl) Beim Lösen von Kalk in Salzsäure bildet sich ein gut wasserlösliches
BÜCHI Labortechnik GmbH
 BÜCHI Labortechnik GmbH Stickstoff-/Proteinbestimmung nach Kjeldahl: Wie geht es richtig? Kjeldahl 2016 Seite 1 Übersicht Wie funktioniert die Methode? Theorie Die einzelnen Arbeitsschritte - Aufschluss
BÜCHI Labortechnik GmbH Stickstoff-/Proteinbestimmung nach Kjeldahl: Wie geht es richtig? Kjeldahl 2016 Seite 1 Übersicht Wie funktioniert die Methode? Theorie Die einzelnen Arbeitsschritte - Aufschluss
Säure-Base-Titrationen
 Säure-Base-Titrationen Dieses Skript gehört: Säure Base - Titrationen Seite 2 Hinweis: Mit den Säuren und Basen ist vorsichtig umzugehen, um Verätzungen zu vermeiden! Versuch 1: Herstellen einer Natronlauge
Säure-Base-Titrationen Dieses Skript gehört: Säure Base - Titrationen Seite 2 Hinweis: Mit den Säuren und Basen ist vorsichtig umzugehen, um Verätzungen zu vermeiden! Versuch 1: Herstellen einer Natronlauge
Kjeldahlsche Stickstoffbestimmung
 Kjeldahlsche Stickstoffbestimmung Kjeldahlsche Stickstoffbestimmung Mit der Kjeldahl-Methode wird der Stickstoffgehalt in organischen und anorganischen Proben bestimmt. Seit mehr als 100 Jahren wird die
Kjeldahlsche Stickstoffbestimmung Kjeldahlsche Stickstoffbestimmung Mit der Kjeldahl-Methode wird der Stickstoffgehalt in organischen und anorganischen Proben bestimmt. Seit mehr als 100 Jahren wird die
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
I N H A L T S Ü B E R S I C H T
 STICKSTOFFBESTIMMUNG 1 I N H A L T S Ü B E R S I C H T Prinzip der Methode 2 Aufschlusskatalysatoren 2 Aufschlussgeräte 2 geeignete Probenarten bzw. Verbindungsklassen 2 Ausführung des Aufschlusses 3 Ausführung
STICKSTOFFBESTIMMUNG 1 I N H A L T S Ü B E R S I C H T Prinzip der Methode 2 Aufschlusskatalysatoren 2 Aufschlussgeräte 2 geeignete Probenarten bzw. Verbindungsklassen 2 Ausführung des Aufschlusses 3 Ausführung
Protokoll 2. Labor für Physikalische Chemie. Modul IV. Versuch 8
 Protokoll 2 Labor für Physikalische Chemie Modul IV Versuch 8 Bestimmung des Schwefelsäuregehaltes einer Schwefelsäurelösung mit unbekannter Massekonzentration und Herstellung einer Lösung mit c(h2 S04)
Protokoll 2 Labor für Physikalische Chemie Modul IV Versuch 8 Bestimmung des Schwefelsäuregehaltes einer Schwefelsäurelösung mit unbekannter Massekonzentration und Herstellung einer Lösung mit c(h2 S04)
Arbeitsanweisung zur Ermittlung und Bewertung des Kalkstein-/Dolomit- Fülleranteils im Asphalt
 Arbeitsanweisung zur Ermittlung und Bewertung des Kalkstein-/Dolomit- Fülleranteils im Asphalt 2016, LISt Gesellschaft für Verkehrswesen und ingenieurtechnische Dienstleistungen mbh Impressum Auftraggeber:
Arbeitsanweisung zur Ermittlung und Bewertung des Kalkstein-/Dolomit- Fülleranteils im Asphalt 2016, LISt Gesellschaft für Verkehrswesen und ingenieurtechnische Dienstleistungen mbh Impressum Auftraggeber:
Protokoll Tag 4, Teil 1
 Protokoll Tag 4, Teil 1 D. Titrationsverfahren D.1. Einführung in die quantitative Analyse; D.2. Acidimetrie (Bestimmung der Konzentration einer Säure) Am heutigen letzten Tag des Praktikums geht es um
Protokoll Tag 4, Teil 1 D. Titrationsverfahren D.1. Einführung in die quantitative Analyse; D.2. Acidimetrie (Bestimmung der Konzentration einer Säure) Am heutigen letzten Tag des Praktikums geht es um
Oxidation = Elektronenabgabe Erhöhung der Oxidationszahl. Reduktion = Elektronenaufnahme Erniedrigung der Oxidationszahl
 Oxidation = Elektronenabgabe Erhöhung der Oxidationszahl Reduktion = Elektronenaufnahme Erniedrigung der Oxidationszahl Oxidans = Oxidationsmittel System, das Elektronen aufnehmen kann Reduktor = Reduktionsmittel
Oxidation = Elektronenabgabe Erhöhung der Oxidationszahl Reduktion = Elektronenaufnahme Erniedrigung der Oxidationszahl Oxidans = Oxidationsmittel System, das Elektronen aufnehmen kann Reduktor = Reduktionsmittel
Applikationsfeld / Industriezweig:
 Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Analysenprotokoll zur Bestimmung der NaOH-Konzentration durch Neutralisationstitration
 Bestimmung von NaOH durch Neutralisationstitration Seite 1 Studiengang: (bitte ankreuzen) CHE LEB BC MBT Bestimmung der NaOH-Konzentration durch Neutralisationstitration Note Ergebnis: Reaktionsgleichung(en):
Bestimmung von NaOH durch Neutralisationstitration Seite 1 Studiengang: (bitte ankreuzen) CHE LEB BC MBT Bestimmung der NaOH-Konzentration durch Neutralisationstitration Note Ergebnis: Reaktionsgleichung(en):
Titration. Weiterbildung für fachfremd unterrichtende Lehrkräfte
 Titration Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Destillation von Rotwein Zerlegung der Verbindung Wasser Herstellung von Natronlauge Öltröpfchen versuch
Titration Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Destillation von Rotwein Zerlegung der Verbindung Wasser Herstellung von Natronlauge Öltröpfchen versuch
Was ist drin in der Cola?
 Was ist drin in der Cola? - Nachweisreaktionen für Anionen, Kationen und Zucker - Ein Nachweis ist eine Methode der Analytischen Chemie, die dazu dient, eine Stoffprobe zu untersuchen. Nachweisreaktionen
Was ist drin in der Cola? - Nachweisreaktionen für Anionen, Kationen und Zucker - Ein Nachweis ist eine Methode der Analytischen Chemie, die dazu dient, eine Stoffprobe zu untersuchen. Nachweisreaktionen
Übungsaufgabe 1. Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz
 Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Übungsaufgabe 1 Photometrische Bestimmung von Chrom als Chromat Chemikalien: H 2 O 2, Natronlauge, Chrom-(III)-salz Versuchsbeschreibung: 20 ml der erhaltenen Probelösung werden in ein 150 ml Becherglas
Applikationsfeld / Industriezweig:
 Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Protokoll zur Herstellung von Essigsäureethylester
 Protokoll zur Herstellung von Essigsäureethylester 1) Ziel des Versuches: Herstellung von Essigsäureethylester unter säurekatalytischen Bedingungen. 2) Theoretischer Hintergrund: Ester sind eine Klasse
Protokoll zur Herstellung von Essigsäureethylester 1) Ziel des Versuches: Herstellung von Essigsäureethylester unter säurekatalytischen Bedingungen. 2) Theoretischer Hintergrund: Ester sind eine Klasse
Protokoll 2. Labor für Physikalische Chemie. Modul IV. Versuch 6
 Protokoll 2 Labor für Physikalische Chemie Modul IV Versuch 6 Herstellung einer Titerbestimmung von 500mL einer Salzsäure Maßlösung mit der Äquivalentkonzentration c(hcl) = 0,1 mol/l Fachbereich MT 1 Wintersemester
Protokoll 2 Labor für Physikalische Chemie Modul IV Versuch 6 Herstellung einer Titerbestimmung von 500mL einer Salzsäure Maßlösung mit der Äquivalentkonzentration c(hcl) = 0,1 mol/l Fachbereich MT 1 Wintersemester
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Applikationsfeld / Industriezweig:
 Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Applikationsfeld / Industriezweig: Chemie / Polymerindustrie Elektronik Energie Ernährung / Landwirtschaft Geologie / Bergbau Halbleiter-Technologie Klinische Chemie / Medizin / Hygiene / Gesundheitswesen
Titrimetrische Analyse von Konfitüren, Frucht- und Gemüsesäften und deren Konzentraten
 Titrimetrische Analyse von Konfitüren, Frucht- und Gemüsesäften und deren Konzentraten Von Interesse für: Lebensmittel und Getränke A, G 7 Zusammenfassung Das Bulletin beschreibt Analysenmethoden zur Bestimmung
Titrimetrische Analyse von Konfitüren, Frucht- und Gemüsesäften und deren Konzentraten Von Interesse für: Lebensmittel und Getränke A, G 7 Zusammenfassung Das Bulletin beschreibt Analysenmethoden zur Bestimmung
Titration von Phosphorsäure mit Natronlauge mit pks-wertbestimmung
 Prinzip Phosphorsäure wird mit Natronlauge titriert. Durch Ermittlung eines Äquivalenzpunktes lässt sich der Gehalt der Säure berechnen, durch Ermittlung der Halbäquivalenzpunkte die pks- Werte. Aufbau
Prinzip Phosphorsäure wird mit Natronlauge titriert. Durch Ermittlung eines Äquivalenzpunktes lässt sich der Gehalt der Säure berechnen, durch Ermittlung der Halbäquivalenzpunkte die pks- Werte. Aufbau
Probenvorbereitung LCW 909. Gesamt-Kjeldahl-Stickstoff, TKN
 Prinzip Organisch gebundener Stickstoff wird in Gegenwart von Katalysatoren durch heiße, rauchende Schwefelsäure aufgeschlossen und in Ammonium überführt, das nach Wasserdampfdestillation zusammen mit
Prinzip Organisch gebundener Stickstoff wird in Gegenwart von Katalysatoren durch heiße, rauchende Schwefelsäure aufgeschlossen und in Ammonium überführt, das nach Wasserdampfdestillation zusammen mit
Anorganisches Praktikum 1. Semester. FB Chemieingenieurwesen. Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften
 Anorganisches Praktikum 1. Semester FB Chemieingenieurwesen Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften 1 Gravimetrie Bestimmung von Nickel Sie erhalten eine Lösung, die 0.1-0.2g
Anorganisches Praktikum 1. Semester FB Chemieingenieurwesen Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften 1 Gravimetrie Bestimmung von Nickel Sie erhalten eine Lösung, die 0.1-0.2g
Anorganisches Praktikum 1. Semester. FB Chemieingenieurwesen. Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften
 Anorganisches Praktikum 1. Semester FB Chemieingenieurwesen Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften 1 Gravimetrie Bestimmung von Nickel Sie erhalten eine Lösung, die 0.1-0.2g
Anorganisches Praktikum 1. Semester FB Chemieingenieurwesen Labor für Anorg. Chemie Angew. Materialwiss. Versuchsvorschriften 1 Gravimetrie Bestimmung von Nickel Sie erhalten eine Lösung, die 0.1-0.2g
Wissenkompakt. Stickstoffbestimmung. Grundlagen, optimierte Prozessführung und Anwendungen
 Wissenkompakt Stickstoffbestimmung Grundlagen, optimierte Prozessführung und Anwendungen 1. Bedeutung der Lebensmittelanalytik Die Produktqualität von Lebensmitteln gewinnt im Zuge eines bewussten und
Wissenkompakt Stickstoffbestimmung Grundlagen, optimierte Prozessführung und Anwendungen 1. Bedeutung der Lebensmittelanalytik Die Produktqualität von Lebensmitteln gewinnt im Zuge eines bewussten und
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom 23.09.2016 A1 A2 A3 A4 A5 Note 12 12 8 10 8 NAME:... VORNAME:... Stichpunkte zu den Lösungen Pseudonym für Ergebnisveröffentlichung:...
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom 23.09.2016 A1 A2 A3 A4 A5 Note 12 12 8 10 8 NAME:... VORNAME:... Stichpunkte zu den Lösungen Pseudonym für Ergebnisveröffentlichung:...
Versuch: Reaktion von Magnesium ( ) und Iod ( )
 Name: Datum: Station 1 Versuch: Reaktion von Magnesium ( ) und Iod ( ) Gib zunächst den Bildern mit Nummern eine sinnvolle Reihenfolge und formuliere anschließend eine Durchführung. 1 Führe den Versuch
Name: Datum: Station 1 Versuch: Reaktion von Magnesium ( ) und Iod ( ) Gib zunächst den Bildern mit Nummern eine sinnvolle Reihenfolge und formuliere anschließend eine Durchführung. 1 Führe den Versuch
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom 23.09.2016 A1 A2 A3 A4 A5 Note 12 12 8 10 8 NAME:... VORNAME:... Pseudonym für Ergebnisveröffentlichung:... Schreiben Sie bitte gut leserlich:
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2016/17 vom 23.09.2016 A1 A2 A3 A4 A5 Note 12 12 8 10 8 NAME:... VORNAME:... Pseudonym für Ergebnisveröffentlichung:... Schreiben Sie bitte gut leserlich:
Praktikum Analytische Chemie SS 2008
 Praktikum Analytische Chemie SS 2008 Antworten zu den Zusatzaufgaben Frage 2 5,3 ml einer Schwefelsäure, konz.,w=96%, Dichte δ=1,84kg/l, werden auf 1l verdünnt. Von dieser Lösung werden 25ml auf 200ml
Praktikum Analytische Chemie SS 2008 Antworten zu den Zusatzaufgaben Frage 2 5,3 ml einer Schwefelsäure, konz.,w=96%, Dichte δ=1,84kg/l, werden auf 1l verdünnt. Von dieser Lösung werden 25ml auf 200ml
Application Bulletin
 Nr. 275/1 d Application Bulletin Von Interesse für: Waschmittelanalyse A 1, 3, 12 Potentiometrische Zweiphasen-Titration anionischer Tenside in Waschpulvern und Flüssigwaschmitteln Zusammenfassung Die
Nr. 275/1 d Application Bulletin Von Interesse für: Waschmittelanalyse A 1, 3, 12 Potentiometrische Zweiphasen-Titration anionischer Tenside in Waschpulvern und Flüssigwaschmitteln Zusammenfassung Die
Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin. Steffen Blaurock Thomas Zimmermann
 Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin Steffen Blaurock Thomas Zimmermann 1.1 Einleitung Titrationen werden in der chemischen Analytik durchgeführt, um die Stoffmenge
Handbuch zum Chemischen Praktikum für Studierende der Human- und Zahnmedizin Steffen Blaurock Thomas Zimmermann 1.1 Einleitung Titrationen werden in der chemischen Analytik durchgeführt, um die Stoffmenge
Untersuchung und Beurteilung von Lebensmitteln
 Untersuchung und Beurteilung von Lebensmitteln Wurst Institut für Lebensmittelchemie Inhaltsverzeichnis 1 Einleitung 3 2 Analysen 4 2.1 Sinnesprüfung..................................... 4 2.2 Probenvorbereitung..................................
Untersuchung und Beurteilung von Lebensmitteln Wurst Institut für Lebensmittelchemie Inhaltsverzeichnis 1 Einleitung 3 2 Analysen 4 2.1 Sinnesprüfung..................................... 4 2.2 Probenvorbereitung..................................
AUSWERTUNG DES RINGVERSUCHS Nonylphenol, Oktylphenol, Bisphenol A NP02
 AUSWERTUNG DES RINGVERSUCHS Nonylphenol, Oktylphenol, Bisphenol A NP02 Probenversand am 24. Februar 2015 Anschrift: Umweltbundesamt GmbH Spittelauer Lände 5 1090 Wien/Österreich Ansprechpartner: Dr. Sandra
AUSWERTUNG DES RINGVERSUCHS Nonylphenol, Oktylphenol, Bisphenol A NP02 Probenversand am 24. Februar 2015 Anschrift: Umweltbundesamt GmbH Spittelauer Lände 5 1090 Wien/Österreich Ansprechpartner: Dr. Sandra
Fehlerrechnung EXPERIMENTELLE FEHLER ANALYTIK II IAAC, TU-BS, 2004 ANALYTIK II IAAC, TU-BS, 2004. Dr. Andreas Martens a.mvs@tu-bs.
 Fehlerrechnung ANALYTIK II Dr. Andreas Martens a.mvs@tu-bs.de Institut f. Anorg.u. Analyt. Chemie, Technische Universität Braunschweig, Braunschweig, Germany EXPERIMENTELLE FEHLER ANALYTIK II - 2 - Signifikante
Fehlerrechnung ANALYTIK II Dr. Andreas Martens a.mvs@tu-bs.de Institut f. Anorg.u. Analyt. Chemie, Technische Universität Braunschweig, Braunschweig, Germany EXPERIMENTELLE FEHLER ANALYTIK II - 2 - Signifikante
Volumenprüfung nach EN DIN ISO 8655/6
 Applikation TitroLine alpha plus Volumenprüfung nach EN DIN ISO 8655/6 Anwendung Die Überprüfung von Volumenmeßgeräte mit Hubkolben" - darunter fallen alle Kolbenbüretten und Titratoren mit eigenem Bürettenteil
Applikation TitroLine alpha plus Volumenprüfung nach EN DIN ISO 8655/6 Anwendung Die Überprüfung von Volumenmeßgeräte mit Hubkolben" - darunter fallen alle Kolbenbüretten und Titratoren mit eigenem Bürettenteil
Fettanalytik. Anna Ertl
 Fettanalytik Anna Ertl Allgemeines Aufbau: Eigenschaften (wie Schmelzpunkt) variieren und hängen von Fettsäuremuster ab Allgemeines Gesättigte Fettsäure Ungesättigte Fettsäure Stearinsäure (C 18 ) Ölsäure
Fettanalytik Anna Ertl Allgemeines Aufbau: Eigenschaften (wie Schmelzpunkt) variieren und hängen von Fettsäuremuster ab Allgemeines Gesättigte Fettsäure Ungesättigte Fettsäure Stearinsäure (C 18 ) Ölsäure
Application Bulletin
 Nr. 249/1 d Application Bulletin Von Interesse für: Allgemein analytische Laboratorien A G 1, 2, 7, 10, 13 Trink- und Brauchwasseranalytik Titrimetrische Bestimmung von Total- und Restchlor in Trink- und
Nr. 249/1 d Application Bulletin Von Interesse für: Allgemein analytische Laboratorien A G 1, 2, 7, 10, 13 Trink- und Brauchwasseranalytik Titrimetrische Bestimmung von Total- und Restchlor in Trink- und
Verfahren zur Bestimmung von Phosphor-32 im Abwasser
 Verfahren zur Bestimmung von Phosphor-32 im Abwasser H-P-32-AWASS-01 Bearbeiter: H.U. Fusban H. Rühle I. Gans Diese Version entspricht der Druckfassung mit den Lieferungen 1 bis 7, Stand: 1.3.2006 Leitstelle
Verfahren zur Bestimmung von Phosphor-32 im Abwasser H-P-32-AWASS-01 Bearbeiter: H.U. Fusban H. Rühle I. Gans Diese Version entspricht der Druckfassung mit den Lieferungen 1 bis 7, Stand: 1.3.2006 Leitstelle
Titration von Speise-Essig
 Titration von Speise-Essig Wir werden in diesem Versuch die Titration [frz.titer = Feingehalt] Konzentration der Essigsäure in Analytisches Verfahren, bei dem die Reagenzlösung tropfenweise zugesetzt wird,
Titration von Speise-Essig Wir werden in diesem Versuch die Titration [frz.titer = Feingehalt] Konzentration der Essigsäure in Analytisches Verfahren, bei dem die Reagenzlösung tropfenweise zugesetzt wird,
Praktikum Innovative Werkstoffkunde
 Labor für Werkstoffe Prof. Dr.-Ing. Karin Lutterbeck Polymere Werkstoffe und Keramik Prof. Dr.-Ing. Helmut Winkel Metallische Werkstoffe Praktikum Innovative Werkstoffkunde Verhalten von Kunststoffen beim
Labor für Werkstoffe Prof. Dr.-Ing. Karin Lutterbeck Polymere Werkstoffe und Keramik Prof. Dr.-Ing. Helmut Winkel Metallische Werkstoffe Praktikum Innovative Werkstoffkunde Verhalten von Kunststoffen beim
Limitenprüfung NDMA und NDEA in Sartanen mittels GC-MS
 Limitenprüfung NDMA und NDEA in Sartanen mittels GC-MS 1 Zweck und Anwendungsbereich Die Methode dient zur Prüfung der zulässigen Limiten von N-Nitrosodimethylamin und N-Nitrosodiethylamin in verschiedenen
Limitenprüfung NDMA und NDEA in Sartanen mittels GC-MS 1 Zweck und Anwendungsbereich Die Methode dient zur Prüfung der zulässigen Limiten von N-Nitrosodimethylamin und N-Nitrosodiethylamin in verschiedenen
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Säure-Base-Titrationen
 Martin Raiber Chemie Protokoll Nr.3 19.2.2006 Säure-Base-Titrationen 1. Titration von Salzsäure mit Natronlauge Chemikalien: Salzsäure (100ml; c(hcl)=0,1 mol/l) Natronlauge (c(naoh)=1 mol/l) Bromthymolblau
Martin Raiber Chemie Protokoll Nr.3 19.2.2006 Säure-Base-Titrationen 1. Titration von Salzsäure mit Natronlauge Chemikalien: Salzsäure (100ml; c(hcl)=0,1 mol/l) Natronlauge (c(naoh)=1 mol/l) Bromthymolblau
Standardarbeitsanweisung
 1 von 11 Inhalt 1 Zweck / Prinzip... Fehler! Textmarke nicht definiert. 2 Einsatzbereich...3 3 Messprinzip...3 3.1 ICP...3 3.2 VAMM...3 4 Geräte, Geräte-Einstellungen...4 4.1 Probenbehälter...4 4.2 Probenahme...4
1 von 11 Inhalt 1 Zweck / Prinzip... Fehler! Textmarke nicht definiert. 2 Einsatzbereich...3 3 Messprinzip...3 3.1 ICP...3 3.2 VAMM...3 4 Geräte, Geräte-Einstellungen...4 4.1 Probenbehälter...4 4.2 Probenahme...4
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2010/11 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2010/11 vom 21.09.2010 A1 A2 A3 A4 A5 Σ Note 13 13 7 9 8 NAME:... VORNAME:... Pseudonym für Ergebnisveröffentlichung:... Schreiben Sie bitte gut leserlich:
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2010/11 vom 21.09.2010 A1 A2 A3 A4 A5 Σ Note 13 13 7 9 8 NAME:... VORNAME:... Pseudonym für Ergebnisveröffentlichung:... Schreiben Sie bitte gut leserlich:
Metrologie = Wissenschaft vom Messen. Messunsicherheit von Analysenergebnissen. VU Chemisch Rechnen
 Metrologie = Wissenschaft vom Messen Messunsicherheit von Analysenergebnissen Wer mißt, mißt Mist!! Metrologie Meteorologie Kräht der Hahn am Mist, Ändert sich das Wetter oder es bleibt, wie es ist!! Inhalt
Metrologie = Wissenschaft vom Messen Messunsicherheit von Analysenergebnissen Wer mißt, mißt Mist!! Metrologie Meteorologie Kräht der Hahn am Mist, Ändert sich das Wetter oder es bleibt, wie es ist!! Inhalt
Intelligenzquotient 13,5 % 13,5 % 2,5 %
 Aufgabennummer: B-C9_11 Intelligenzquotient Technologieeinsatz: möglich erforderlich S Der Intelligenzquotient (IQ) ist eine Kenngröße zur Bewertung des allgemeinen intellektuellen Leistungsvermögens (Intelligenz)
Aufgabennummer: B-C9_11 Intelligenzquotient Technologieeinsatz: möglich erforderlich S Der Intelligenzquotient (IQ) ist eine Kenngröße zur Bewertung des allgemeinen intellektuellen Leistungsvermögens (Intelligenz)
Ergänzende Aufgaben zu Säure-Base-Titrationen und deren ph-titrationskurven
 Ergänzende Aufgaben zu Säure-Base-Titrationen und deren ph-titrationskurven 1. Einfachere Aufgaben ohne ph-kurvenverläufe einfache Umsatzberechnungen 1.1 Eine Maßlösung hat eine angestrebte Stoffmengenkonzentration
Ergänzende Aufgaben zu Säure-Base-Titrationen und deren ph-titrationskurven 1. Einfachere Aufgaben ohne ph-kurvenverläufe einfache Umsatzberechnungen 1.1 Eine Maßlösung hat eine angestrebte Stoffmengenkonzentration
FISCH ALS LEBENSMITTEL. Vergleich verschiedener Methoden zur Essigsäure- und Kochsalzbestimmung
 nfn Fischw. 39 (3), 1992 137 FSCH ALS LEBENSMTTEL Vergleich verschiedener Methoden zur Essigsäure- und Kochsalzbestimmung in Marinaden H. Karl, nstitut für Biochemie und Technologie, Hamburg Nach dem nkrafttreten
nfn Fischw. 39 (3), 1992 137 FSCH ALS LEBENSMTTEL Vergleich verschiedener Methoden zur Essigsäure- und Kochsalzbestimmung in Marinaden H. Karl, nstitut für Biochemie und Technologie, Hamburg Nach dem nkrafttreten
Untersuchung und Validierung sequenzieller Extraktionsverfahren durch X-ray Absorption Fine Structure Spectroscopy (XAFS)
 Untersuchung und Validierung sequenzieller Extraktionsverfahren durch X-ray Absorption Fine Structure Spectroscopy (XAFS) Dissertation zur Erlangung des naturwissenschaftlichen Doktorgrades der Technischen
Untersuchung und Validierung sequenzieller Extraktionsverfahren durch X-ray Absorption Fine Structure Spectroscopy (XAFS) Dissertation zur Erlangung des naturwissenschaftlichen Doktorgrades der Technischen
2. Klausur zum Chemischen Grundpraktikum im WS 2015/16 vom 21. März 2016
 2. Klausur zum Chemischen Grundpraktikum im WS 2015/16 vom 21. März 2016 A1 A2 A3 A4 A5 A6 A7 P8 P9 P10 Note 8 10 10 10 10 12 10 11 9 10 100 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung
2. Klausur zum Chemischen Grundpraktikum im WS 2015/16 vom 21. März 2016 A1 A2 A3 A4 A5 A6 A7 P8 P9 P10 Note 8 10 10 10 10 12 10 11 9 10 100 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung
Chemisches Rechnen. Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen:
 Chemisches Rechnen Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen: Verständnis der unterschiedlichen Größen Sichere Anwendung
Chemisches Rechnen Diese Lerneinheit befasst sich mit verschiedenen chemisch relevanten Größen Konzentrationsangaben mit den folgenden Lehrzielen: Verständnis der unterschiedlichen Größen Sichere Anwendung
Experimentieranleitungen zu Schülerexperimenten über Vitamine
 Experimentieranleitungen zu Schülerexperimenten über Vitamine Inhalt: - Nachweis von Vitamin A und Provitamin A - Nachweis von Vitamin E - Nachweis von Vitamin B 1 - Nachweis von Vitamin B 2 - Nachweis
Experimentieranleitungen zu Schülerexperimenten über Vitamine Inhalt: - Nachweis von Vitamin A und Provitamin A - Nachweis von Vitamin E - Nachweis von Vitamin B 1 - Nachweis von Vitamin B 2 - Nachweis
Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH)
 Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH) Material 250 mlbecherglas 100 ml Messzylinder 50 mlbürette, Magnetrührer, Magnetfisch, Stativmaterial phmeter Chemikalien Natronlauge
Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH) Material 250 mlbecherglas 100 ml Messzylinder 50 mlbürette, Magnetrührer, Magnetfisch, Stativmaterial phmeter Chemikalien Natronlauge
Versuch: Nachweis von Salicylsäure
 Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Untersuchung von Kosmetischen Mitteln und Bedarfsgegenständen. Diskussion zur Bestimmung von Kationtensiden in Wasch- und Reinigungsmitteln
 Praktikumsmethodensammlung Universität Hamburg, Institut für Biochemie und Lebensmittelchemie, Abteilung Lebensmittelchemie Untersuchung von Kosmetischen Mitteln und Bedarfsgegenständen Diskussion zur
Praktikumsmethodensammlung Universität Hamburg, Institut für Biochemie und Lebensmittelchemie, Abteilung Lebensmittelchemie Untersuchung von Kosmetischen Mitteln und Bedarfsgegenständen Diskussion zur
wird titriert mit Salzsäure der Konzentration c(hcl) = 1 mol/l.
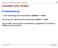 1 Problemstellung 1 Liter Natronlauge der Konzentration c(naoh) = 1 mol/l wird titriert mit Salzsäure der Konzentration c(hcl) = 1 mol/l. Der ph-wert Lösung soll für verschiedene zugegebene HCl-Volumina
1 Problemstellung 1 Liter Natronlauge der Konzentration c(naoh) = 1 mol/l wird titriert mit Salzsäure der Konzentration c(hcl) = 1 mol/l. Der ph-wert Lösung soll für verschiedene zugegebene HCl-Volumina
Fallstudie: Dumas-Stickstoffbestimmung Sind Makro-Einwaagen bei Makro-Kosten noch zeitgemäß? Von Dr. Werner Küppers, Königswinter, Deutschland
 Fallstudie: Dumas-Stickstoffbestimmung Sind Makro-Einwaagen bei Makro-Kosten noch zeitgemäß? Von Dr. Werner Küppers, Königswinter, Deutschland Sonderdruck 2015 Veröffentlicht in Mühle + Mischfutter 152.
Fallstudie: Dumas-Stickstoffbestimmung Sind Makro-Einwaagen bei Makro-Kosten noch zeitgemäß? Von Dr. Werner Küppers, Königswinter, Deutschland Sonderdruck 2015 Veröffentlicht in Mühle + Mischfutter 152.
Säurekonstante des p-nitrophenols
 Säurekonstante des p-nitrophenols Grundlagen Sie bestimmen spektralphotometrisch die Säurekonstante einer schwachen Säure. Voraussetzung dafür ist, dass die undissoziierte Säure in einem anderen Spektralbereich
Säurekonstante des p-nitrophenols Grundlagen Sie bestimmen spektralphotometrisch die Säurekonstante einer schwachen Säure. Voraussetzung dafür ist, dass die undissoziierte Säure in einem anderen Spektralbereich
BGI (bisher ZH 1/120.59) Verfahren zur Bestimmung von α-chlortoluol
 BGI 505.59 (bisher ZH 1/120.59) Verfahren zur Bestimmung von α-chlortoluol Hauptverband der gewerblichen Berufsgenossenschaften Fachausschuß "Chemie" Dezember 1996 Erprobtes und von den Berufsgenossenschaften
BGI 505.59 (bisher ZH 1/120.59) Verfahren zur Bestimmung von α-chlortoluol Hauptverband der gewerblichen Berufsgenossenschaften Fachausschuß "Chemie" Dezember 1996 Erprobtes und von den Berufsgenossenschaften
Konduktometrische und potenziometrische Titration von Salzsäure mit Natronlauge 2-Kanalmessung (normale Bürette)
 Prinzip Da sich bei der Neutralisation die Leitfähigkeit und der ph-wert ändern, kann man die Titration sowohl konduktometrisch wie auch potenziometrisch verfolgen Mit (Mobile / Pocket) CASSY / kann man
Prinzip Da sich bei der Neutralisation die Leitfähigkeit und der ph-wert ändern, kann man die Titration sowohl konduktometrisch wie auch potenziometrisch verfolgen Mit (Mobile / Pocket) CASSY / kann man
Titration einer Säure mit einer Base
 Titration einer Säure mit einer Base Peter Bützer Inhalt 1 Einleitung... 1 2 Modellannahmen (Systemdynamik)... 2 3 Simulationsdiagramm (Typ 1)... 2 4 Dokumentation (Gleichungen, Parameter)... 3 5 Simulation...
Titration einer Säure mit einer Base Peter Bützer Inhalt 1 Einleitung... 1 2 Modellannahmen (Systemdynamik)... 2 3 Simulationsdiagramm (Typ 1)... 2 4 Dokumentation (Gleichungen, Parameter)... 3 5 Simulation...
Labworld.at. Ihre Laborchemikalien. Stickstoffbestimmung nach Kjeldahl
 Labworld.at Ihre Laborchemikalien Stickstoffbestimmung nach Kjeldahl Stickstoffbestimmung nach Kjeldahl vor über 120 Jahren entwickelte quantitative Be- zeptierter Standard wird Kjeldahl in der Nahrungsmittelindustrie,
Labworld.at Ihre Laborchemikalien Stickstoffbestimmung nach Kjeldahl Stickstoffbestimmung nach Kjeldahl vor über 120 Jahren entwickelte quantitative Be- zeptierter Standard wird Kjeldahl in der Nahrungsmittelindustrie,
Messunsicherheit nach GUM* Praxisgerecht für chemische Laboratorien
 Messunsicherheit nach GUM* Praxisgerecht für chemische Laboratorien *) Guide to the Expression of Uncertainty in Measurement - F 1 Einführung und Motivation Gliederung: 1. Notwendigkeit und Nutzen der
Messunsicherheit nach GUM* Praxisgerecht für chemische Laboratorien *) Guide to the Expression of Uncertainty in Measurement - F 1 Einführung und Motivation Gliederung: 1. Notwendigkeit und Nutzen der
Biochemisches Grundpraktikum
 Biochemisches Grundpraktikum Versuch Nummer G-01 01: Potentiometrische und spektrophotometrische Bestim- mung von Ionisationskonstanten Gliederung: I. Titrationskurve von Histidin und Bestimmung der pk-werte...
Biochemisches Grundpraktikum Versuch Nummer G-01 01: Potentiometrische und spektrophotometrische Bestim- mung von Ionisationskonstanten Gliederung: I. Titrationskurve von Histidin und Bestimmung der pk-werte...
Übungen zur VL Chemie für Biologen und Humanbiologen 14.01.2011
 Übungen zur VL Chemie für Biologen und Humanbiologen 14.01.011 Redoxchemie 1. a) Was beobachten Sie, wenn Sie in getrennten Experimenten einen Eisen-, Kupfer-, Zink- und Goldstab in eine Salzsäurelösung
Übungen zur VL Chemie für Biologen und Humanbiologen 14.01.011 Redoxchemie 1. a) Was beobachten Sie, wenn Sie in getrennten Experimenten einen Eisen-, Kupfer-, Zink- und Goldstab in eine Salzsäurelösung
Versuchsprotokoll. Adsorption von Essigsäure an Aktivkohle
 Versuchsprotokoll Versuchsdatum: 5.10.2004 Zweitabgabe: Sttempell Durchgeführt von: Adsorption von Essigsäure an Aktivkohle 1. Inhaltsangabe 1..Inhaltsangabe---------------------------------------------------------------------------------
Versuchsprotokoll Versuchsdatum: 5.10.2004 Zweitabgabe: Sttempell Durchgeführt von: Adsorption von Essigsäure an Aktivkohle 1. Inhaltsangabe 1..Inhaltsangabe---------------------------------------------------------------------------------
Institut für Technische Chemie Technische Universität Clausthal
 Institut für echnische Chemie echnische Universität Clausthal echnisch-chemisches Praktikum CB Versuch: Extraktion Einleitung Die Flüssig-Flüssig-Extraktion ist ein thermischer Prozess zur rennung eines
Institut für echnische Chemie echnische Universität Clausthal echnisch-chemisches Praktikum CB Versuch: Extraktion Einleitung Die Flüssig-Flüssig-Extraktion ist ein thermischer Prozess zur rennung eines
Whitekalorimeter. Wärmekapazitätsbestimmung verschiedener Materialien. Dominik Büchler 5HL. Betreuer: Mag. Dr. Per Federspiel
 Dominik Büchler Physikalisch chemisches Laboratorium Betreuer: Mag. Dr. Per Federspiel 5HL Whitekalorimeter sbestimmung verschiedener Materialien Note: Datum: Unterschrift: Whitekalorimetrie Seite 1 von
Dominik Büchler Physikalisch chemisches Laboratorium Betreuer: Mag. Dr. Per Federspiel 5HL Whitekalorimeter sbestimmung verschiedener Materialien Note: Datum: Unterschrift: Whitekalorimetrie Seite 1 von
Versuche zum Thema Aminosäuren
 Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
E3: Potentiometrische Titration
 Theoretische Grundlagen Als potentiometrische Titration bezeichnet man ein Analyseverfahren, bei dem durch Messung der Gleichgewichtsspannung einer galvanischen Kette auf die Menge des zu titrierenden
Theoretische Grundlagen Als potentiometrische Titration bezeichnet man ein Analyseverfahren, bei dem durch Messung der Gleichgewichtsspannung einer galvanischen Kette auf die Menge des zu titrierenden
BGI Verfahren zur Bestimmung von Thioharnstoff
 BGI 505-69 Verfahren zur Bestimmung von Thioharnstoff (bisher ZH 1/120.69) Hauptverband der gewerblichen Berufsgenossenschaften Fachausschuss "Chemie" April 2001 Erprobtes und von den Berufsgenossenschaften
BGI 505-69 Verfahren zur Bestimmung von Thioharnstoff (bisher ZH 1/120.69) Hauptverband der gewerblichen Berufsgenossenschaften Fachausschuss "Chemie" April 2001 Erprobtes und von den Berufsgenossenschaften
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung
 V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
Trisacetylacetonatoferrat(III) Fe(acac) 3
 Trisacetylacetonatoferrat(III) Fe(acac) 3 Mols, 21. 11. 2004 Marco Lendi, AC II 1. Synthese 1.1 Methode Wasserfreies Eisen(III)chlorid wird in wässriger, basischer Lösung durch Erhitzen in Eisen(III)hydroxid
Trisacetylacetonatoferrat(III) Fe(acac) 3 Mols, 21. 11. 2004 Marco Lendi, AC II 1. Synthese 1.1 Methode Wasserfreies Eisen(III)chlorid wird in wässriger, basischer Lösung durch Erhitzen in Eisen(III)hydroxid
Zu Chemiedidaktik: Ein preiswertes Photometer für den Chemieunterricht
 Zu Chemiedidaktik: Ein preiswertes Photometer für den Chemieunterricht Marc Sören Homeyer, Brigitte Duvinage Nachr. Chem. 2017, 65, 63 Versuchsbeschreibungen Bestimmung der Patentblau V-Konzentration in
Zu Chemiedidaktik: Ein preiswertes Photometer für den Chemieunterricht Marc Sören Homeyer, Brigitte Duvinage Nachr. Chem. 2017, 65, 63 Versuchsbeschreibungen Bestimmung der Patentblau V-Konzentration in
Titration mit dem Tropfenzähler
 Mit Hilfe des Tropfenzählers kann die Zahl von Tropfen gemessen werden. Hat man in einem Vorversuch das Volumen eines Tropfens bestimmt, kann über eine Formel in CASSY Lab das Volumen der zugetropften
Mit Hilfe des Tropfenzählers kann die Zahl von Tropfen gemessen werden. Hat man in einem Vorversuch das Volumen eines Tropfens bestimmt, kann über eine Formel in CASSY Lab das Volumen der zugetropften
Gefrieren von Lebensmitteln: Eiskristallisation aus zuckerhaltigen Lösungen
 Versuchsbeschreibung LVT: Gefrieren von Lebensmitteln: Eiskristallisation aus zuckerhaltigen Lösungen Ziel des Versuchs: Durch die Aufnahme des Temperaturverlaufs beim Gefrieren von Zuckerlösungen verschiedener
Versuchsbeschreibung LVT: Gefrieren von Lebensmitteln: Eiskristallisation aus zuckerhaltigen Lösungen Ziel des Versuchs: Durch die Aufnahme des Temperaturverlaufs beim Gefrieren von Zuckerlösungen verschiedener
Protokoll zur Übung Atomabsorptionsspektroskopie
 Protokoll zur Übung Atomabsorptionsspektroskopie im Rahmen des Praktikums Labor an der TU Wien Durchgeführt bei Privatdoz. Dipl.-Ing. Dr.techn. Andreas Limbeck Verfasser des Protokolls: Gwendolin Korinek
Protokoll zur Übung Atomabsorptionsspektroskopie im Rahmen des Praktikums Labor an der TU Wien Durchgeführt bei Privatdoz. Dipl.-Ing. Dr.techn. Andreas Limbeck Verfasser des Protokolls: Gwendolin Korinek
CHEMISCHES RECHNEN II ANALYT. CHEM. FÜR FORTGS
 Arbeitsunterlagen zu den VU CHEMISCHES RECHNEN II - 771.119 Einheit 5 ANALYT. CHEM. FÜR FORTGS. - 771.314 Einheit 4 ao. Prof. Dr. Thomas Prohaska (Auflage Mai 2005) Einführung in die Metrology in Chemistry
Arbeitsunterlagen zu den VU CHEMISCHES RECHNEN II - 771.119 Einheit 5 ANALYT. CHEM. FÜR FORTGS. - 771.314 Einheit 4 ao. Prof. Dr. Thomas Prohaska (Auflage Mai 2005) Einführung in die Metrology in Chemistry
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Es soll eine schriftliche Ausarbeitung abgegeben werden (1 Exemplar pro Gruppe).
 Gruppe 1 Thema: Wissenswertes über Essig 1. Bestimme den ph-wert von Haushaltsessig. 2. Wie viel Essigsäure (in mol/l und in g/l) ist in Haushaltsessig enthalten? 3. Wie wird Essigsäure hergestellt (Ausgangsstoffe,
Gruppe 1 Thema: Wissenswertes über Essig 1. Bestimme den ph-wert von Haushaltsessig. 2. Wie viel Essigsäure (in mol/l und in g/l) ist in Haushaltsessig enthalten? 3. Wie wird Essigsäure hergestellt (Ausgangsstoffe,
RIAG Zn 230. Cyanidisches Glanzzinkverfahren
 Postfach 169 CH-9545 Wängi TG 20.08.2009 RIAG Zn 230 Cyanidisches Glanzzinkverfahren Eigenschaften Das cyanidische Glanzzinkverfahren RIAG Zn 230 erzeugt glänzende Niederschläge über einen weiten Stromdichtebereich.
Postfach 169 CH-9545 Wängi TG 20.08.2009 RIAG Zn 230 Cyanidisches Glanzzinkverfahren Eigenschaften Das cyanidische Glanzzinkverfahren RIAG Zn 230 erzeugt glänzende Niederschläge über einen weiten Stromdichtebereich.
Titration von Metallorganylen und Darstellung der dazu benötigten
 Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
Dichteanomalie von Wasser
 Prinzip Die Veränderung der Dichte von Wasser bei Änderung der Temperatur lässt sich mit einfachen Mitteln messen. Dazu wird die Volumenänderung in Abhängigkeit von der Temperatur gemessen. Die Daten werden
Prinzip Die Veränderung der Dichte von Wasser bei Änderung der Temperatur lässt sich mit einfachen Mitteln messen. Dazu wird die Volumenänderung in Abhängigkeit von der Temperatur gemessen. Die Daten werden
Praktische Übungen Chemie. Versuch 6
 Bauhaus-Universität Weimar Professur Bauchemie Prof. Dr. rer. nat. habil. Christian Kaps Praktische Übungen Chemie Versuch 6 Bestimmung der Wasserhärte Stand: April 2008 1. Grundlagen und Zielstellung
Bauhaus-Universität Weimar Professur Bauchemie Prof. Dr. rer. nat. habil. Christian Kaps Praktische Übungen Chemie Versuch 6 Bestimmung der Wasserhärte Stand: April 2008 1. Grundlagen und Zielstellung
Geräte Küvette λ Messbereich MD 100, MD 600, MD 610, ø 24 mm 660 nm mg/l P
 Phosphat LR T 0.02-1.3 mg/l P Phosphormolybdänblau 320 PO4 Instrumentspezifische Informationen Der Test kann auf den folgenden Geräten durchgeführt werden. Zusätzlich sind die benötigte Küvette und der
Phosphat LR T 0.02-1.3 mg/l P Phosphormolybdänblau 320 PO4 Instrumentspezifische Informationen Der Test kann auf den folgenden Geräten durchgeführt werden. Zusätzlich sind die benötigte Küvette und der
Alkalische Verseifung von Ethansäureethylester. Stativ Muffe Elektrodenklemme Magnetrührer Rührfisch. evtl. pneumat. Wanne
 Prinzip Bei der alkalischen Verseifung werden Hydroxidionen durch Acetationen ersetzt. Daher kann die Reaktion mit Hilfe der Leitfähigkeitsmessung verfolgt werden. Aufbau und Vorbereitung Benötigte Geräte
Prinzip Bei der alkalischen Verseifung werden Hydroxidionen durch Acetationen ersetzt. Daher kann die Reaktion mit Hilfe der Leitfähigkeitsmessung verfolgt werden. Aufbau und Vorbereitung Benötigte Geräte
Datum: Name: Klasse: 1 von 6
 Salz in Chips Bestimmung des Kochsalz-Gehaltes verschiedener Chips-Sorten Prinzip Im vorliegenden Fall handelt es sich um eine Fällungsreaktion: Die Chlorid-Ionen werden durch Zugabe von Silbernitrat-Lösung
Salz in Chips Bestimmung des Kochsalz-Gehaltes verschiedener Chips-Sorten Prinzip Im vorliegenden Fall handelt es sich um eine Fällungsreaktion: Die Chlorid-Ionen werden durch Zugabe von Silbernitrat-Lösung
