Praktische Einführung in die Chemie Integriertes Praktikum:
|
|
|
- Joachim Kaufer
- vor 7 Jahren
- Abrufe
Transkript
1 Praktische Einführung in die Chemie Integriertes Praktikum: Versuch 1-7 (KOG) Komplexgleichgewicht Versuchs-Datum: 16. Mai 2012 Gruppenummer: 8 Gruppenmitglieder: Domenico Paone Patrick Küssner Michael Schmid Assistent/-in: Herr Lotter
2 Inhaltsverzeichnis 1 Theorie Komplexreaktionen und Komplexstabilität Der räumliche Aufbau der Komplexe Die Ligandenfeldtheorie (Kristallfeldtheorie) Die Valenzbindungstheorie Eigenschaften von Komplexen Beobachtung der Farben von Komplexen Aufgabenstellung Versuchsdurchführung Beobachtungen Deutung und Auswertung Untersuchung der Stabilität von Komplexen Aufgabenstellung Versuchsdurchführung Beobachtungen Deutung und Auswertung Beobachtungen der Hydratisomerie Aufgabenstellung Versuchsdurchführung Beobachtungen Deutung und Auswertung Stabilität von Chelatkomplexen Aufgabenstellung Versuchsaufbau Versuchsdurchführung Beobachtungen Auswertung Zusatzaufgabe
3 1 Theorie Eine Komplexverbindung ist eine Koordinationsverbindung, bei der mehrere Liganden an ein (im Normalfall) kationisches Metallzentrum koordinieren. Der gesamte Komplex kann sowohl positiv als auch negativ geladen sein. Ungeladene Komplexe sind genauso möglich. 1.1 Komplexreaktionen und Komplexstabilität Die Reaktion zur Bildung eines Komplexes stellt eine Säure-Base Reaktion nach der Lewis-Theorie dar. Das Zentralkation übernimmt dabei die Rolle der Lewis-Säure (d.h es besitzt freie Orbitale), während die Liganden die Lewis-Base darstellen (d.h sie stellen Elektronenpaare zur Verfügung). Komplexreaktionen sind Gleichgewichtsreaktionen. Sie müssen dennoch in einzelnen Reaktionsschritten unterteilt werden. Das Produkt der Gleichgewichtskonstanten aus den Einzelreaktionen ergibt die Gleichgewichtskonstante für die Gesamtreaktion. Diese nennt man Komplexbildungskonstante. Sie wird aber auch Komplexstabilitätskonstante genannt, da sie angibt, wie stabil ein Komplex ist. 1.2 Der räumliche Aufbau der Komplexe Das Zentralatom besitzt eine verhältnismäßig hohe Punktladung. Diese versucht er durch seine Liganden nach außen abzuschirmen, was besonders gut möglich ist, wenn sich die Liganden auf einer Kugeloberfläche gleichmäßig um das Zentralatom anordnen. Beliebte Geometrien sind das Oktaeder, das Tetraeder und die trigonale Bipyramide. Es existieren verschiedene Theorien die erklären, warum sich Liganden in einem konkreten Fall um ein Zentralatom anordnen. 1.3 Die Ligandenfeldtheorie (Kristallfeldtheorie) Die Ligandenfeldtheorie kommt erst dann zum tragen, wenn das Zentralatom eine d Elektronenkonfiguration von minimal d 1 und maximal d 9 besitzt. Die Hauptaussage dieser Theorie ist, dass die Entartung der fünf d-orbitale durch die Annäherung von Liganden aufgehoben wird. Oktaedrische Komplexe Oktaedrische Komplexe entstehen, wenn sich sechs Liganden dem Zentralatom näheren. Die Entartung wird aufgehoben, indem die drei Orbitale, die nicht im Weg sind (d xy, d xz, d yz ), energetisch abgesenkt werden. Die anderen beiden d-orbitale werden energetisch angehoben, sodass sie gut für die Bindung zum Liganden verwendet werden können. Die Aufspaltung der Orbitalenergie wird Ligandenfeldaufspaltungsenergie genannt. Tetraedrische Komplexe Tetraedrische Komplexe entstehen, wenn sich vier Liganden dem Zentralatom nähern. Dabei werden die d z 2 und d x2 y2 Orbitale energetisch abgesenkt und bevorzugt für die Restelektronen des Zentralatoms verwendet. Die anderen drei Orbitale werden energetisch angehoben. Dies führt dazu, dass das Aufspaltungsverhältnis genau umgedreht zur Oktaederaufspaltung ist. Die Ligandenfeldaufspaltungsenergie ist im Vergleich mit einem oktaedrischen Ligandenfeld nur 4/9 so groß wie diejenige des Oktaederfelds. Die spektrochemische Reihe Die Größe der Ligandenfeldaufspaltungsenergie ist von einige Dingen abhängig. Zum einen ist die Geometrie des Komplexes wichtig. Zum anderen hat die Elektronenkonfiguration des Zentralatoms eine wichtige Bedeutung. Der größte Einfluss der Aufspaltungsenergie kommt jedoch 3
4 von den Liganden. Daher werden Liganden ihrer stärke nach in der spektrochemischen Reihe aufgelistet. Die Ligandenfeldaufspaltungsenergie tritt mit der Spinpaarungsenergie in Konkurrenz. Dies hat einen großen Einfluss auf die Besetzung der d-orbitale. Ist die Spinpaarungsenergie kleiner als die Aufspaltungsenergie, so werden zuerst die energetisch tiefer liegenden Orbitale einfach, dann doppelt besetzt und dann die energetisch höher liegenden Orbitale einfach dann doppelt besetzt. Somit entstehen sogenannte low-spin Komplexe. Ist die Spinpaarungsenergie größer als die Aufspaltungsenergie, so werden zuerst die energetisch tiefer liegenden Orbitale einfach besetzt, dann die energetisch höher liegenden Orbitale einfach besetzt. Schließlich werden die energetisch tiefer liegenden Orbitale doppelt besetzt und zum Schluss die energetisch höher liegenden Orbitale doppelt besetzt. Es entstehen high-spin Komplexe. Allgemein kann man sich merken, dass tetraedische low-spin Komplexe nie zu beobachten sind, das die Aufspaltungsenergie von tetraederische Komplexe viel zu klein ist. Bei oktaedrischen Komplexen genügt es die Konfigurationen von d 4 bis d 7 zu untersuchen, da nur hier eine Entscheidungsmöglichkeit zwischen low-spin und high-spin existiert. Das quadratisch-planare Ligandenfeld Bei Komplexverbindungen existieren ebenfalls Geometrien, die keine ideale kugelförmige Abschirmung um das Zentralkation gewährleisten. Ein Beispiel hierfür ist die quadratisch-planare Geometrie, die entsteht, wenn ein Zentralkation der Elektronenkonfiguration d 8 mit einem starken Liganden gepaart wird. Das oktaedrische Feld bietet dafür keinen ausreichenden Energiegewinn, wodurch es zu einer energetischen Trennung der beiden höherliegenden Orbitale kommt. Der Jahn-Teller Effekt Sind die energetisch höchstliegenden Orbitale aufgrund der Elektronenkonfiguration des Zentralkations unterschiedlich besetzt, so ist ein Energiegewinn durch die Aufhebung der Entartung dieser Orbitale möglich. Dies hat Auswirkungen auf die Komplexgeometrie, da man sowohl gestreckte, als auch gestauchte Oktaeder erhalten kann. 1.4 Die Valenzbindungstheorie Bei der Valenzbindungstheorie wird die Entartung der Orbitale beibehalten. Trotzdem wird entsprechend der Ligandenstärke zwischen low-spin und high spin unterschieden. 1.5 Eigenschaften von Komplexen Magnetismus in Komplexen Ein Komplex besitzt kein magnetisches Moment, wenn er keine ungepaarte Elektronen besitzt. In diesem Fall ist er diamagnetisch. Besitzt ein Komplex ungepaarte Elektronen ist er paramagnetisch, das heißt sie können sich in einem Magnetfeld ausrichten. Farben von Komplexen Bei der Farberscheinung in Komplexen handelt es sich um das Absorptionsspektrum. Dabei werden Elektronen durch eine bestimmte Wellenlänge des sichtbaren Lichts auf ein höheres Niveau angeregt. Chelatkomplexe Besitzt ein Ligand mehrere Koordinationsstellen spricht man von einen Chelatliganden. Chelatkomplexe besitzen sowohl thermodynamisch als auch kinetisch eine höhere Stabilität. 4
5 2 Beobachtung der Farben von Komplexen 2.1 Aufgabenstellung Die Farbigkeit von Komplexen ist in Abhängigkeit derer Liganden zu untersuchen. 2.2 Versuchsdurchführung Beide Versuchsteile finden unter dem Abzug statt. a) Es werden zwei Reagenzgläser mit je einer Spatelspitze CuSO 4 befüllt und in wenig demineralisiertem Wasser gelöst. Danach wird die Lösung mit Natronlauge bzw. Ammoniaklösung (ca. 2 cm hoch) versetzt. b) Es wird eine Spatelspitze Co 2 in einem Reagenzglas mit wenig konzentrierter Salzsäure gelöst. Die entstehende blaue Lösung wird mit Wasser bis zum Farbwechsel nach rosa verdünnt. 2.3 Beobachtungen Ammoniaklösung Natronlauge Farbe Blau (Königsblau) Hellblau 1 a) CuSO 4 ohne mit ca. 1 cm hoch Farbe tiefblau rosa 2 b) Co Deutung und Auswertung Versuch a Wird Kupfer-Sulfat in Wasser gelöst, so findet folgende Reaktion statt: CuSO 4 + [Cu() 6 ] 2+ + SO 2 4 Es entsteht ein Hexaaquakupfer(II)-Komplex Durch Zugabe von Ammoniaklösung, ersetzen die Ammoniak-Moleküle die schwächeren Wasserliganden und es entsteht ein Tetraaminkupfer(II)-Komplex. [Cu() 6 ] 2+ + NH 3 [Cu(NH 3 ) 4 ] 2+ Wird statt Ammoniaklösung konzentrierte Natronlauge hinzugegeben, so entsteht ein Dihydroxocuprat(II)- Komplex. [Cu() 6 ] 2+ + NaOH Cu(OH) 2 + Na + 5
6 Versuch b Durch Zugabe von konzentrierter Salzsäure bilden die Chloridionen mit den Cobaldationen einen Tetrachlorocobaltat(II)-Komplex. Wird wasser hinzugegeben, so werden die Chloridliganden durch Wasserliganden ersetzt. Es entsteht ein Hexaaquacobaltat(II)-Komplex. Co H [Co() 4 ] H + [Co() 4 ] [Co() 2 () 2 ]+2 [Co() 2 () 2 ]+2 [Co() 4 ] [Co() 4 ] [Co() 6 ] 2+ Einordung der Liganden in die spektrochemische Reihe: Von links nach recht nimmt die Aufspaltungsenergie zu. < OH < < NH 3 Wie sind die beobachteten Farben zu erklären? Indem ein Ligandenaustausch am Zentralatom stattfindet wird die Ligandenfeldaufspaltungsenergie verändert, wobei stärkere Liganden eine höhere Ligandenaufspaltung bewirken. Dadurch wird Licht zur Anregung der Elektronenübergänge absorbiert, wodurch die entsprechenden Komplementärfarben als Farbigkeit des Komplexes wahrgenommen werden. 6
7 3 Untersuchung der Stabilität von Komplexen 3.1 Aufgabenstellung Es soll mit Hilfe unterschiedlicher Komplexstabilitäten zwei verschiedene Ionen in wässriger Lösung voneinander getrennt werden. 3.2 Versuchsdurchführung Der Versuch findet unter dem Abzug statt. Es wird jeweils eine Spatelspitze CuSO 4 und CdSO 4 in ein Reagenzglas gegeben. In ein drittes Reagenzglas werden beide Chemikalien gegeben. In alle drei Reagenzgläser wird 1 2 cm hoch demineralisiertes Wasser hinzugegeben und geschwenkt, um die Reagenzien zu lösen. Anschließend sind alle drei Lösungen mittels Ammoniaklösung auf einen ph Wert über 10 zu bringen. Nun wird in die Lösung mit der Mischung aus CuSO 4 und CdSO 4 (möglichst wenig) festes KCN gegeben, bis sich der gebildete Niederschlag wieder auflöst. Zu allen drei Lösungen wird nun (ca. 1 cm hoch) H 2 S Wasser gegeben. 3.3 Beobachtungen CuSO 4 und CdSO 4 CuSO 4 CdSO 4 Farbe mit blau blau Farblos Farbe mit NH 4 OH dunkelblau dunkelblau Farblos Farbe mit KCN Farblos Farbe mit H 2 S gelb dunkelbraun bis schwarz gelb 3 Beobachtungen Versuch Deutung und Auswertung In der wässrigen Lösung liegen sowohl Hexaauquakupfer(II)-Komlexe als auch Hexaauqacadmium(II)- Komplexe vor. CuSO 4 + CdSO [Cu() 6 ] 2+ + [Cd() 6 ] SO 2 4 Durch Zugabe von Ammoniak entsteht ein Tetraaminkupfer(II)-Komplex und ein Hexamincadmium(II)- Komplex [Cu() 6 ] 2+ + [Cd() 6 ] NH 3 [Cu(NH 3 ) 4 ] 2+ + [Cd(NH 3 ) 6 ] Durch Zugabe von Kaliumcyanid reagieren dies zu Kupfer(II)- bzw. Cadmium(II)-Cyanid, die als Feststoffe ausfallen. Wird noch mehr Kaliumcyanid hinzugegeben entsteht ein Tetracyanocuprat(I)- und ein Tetracyanocadmat(II)- Komplex. [Cu(NH 3 ) 4 ] KCN 2 K NH 3 + Cu(CN) 2 2 Cu(CN) 2 2 CuCN+(CN) 2 CN OH CN + OCN + CuCN+3 CN [Cu(CN) 4 ] 3 7
8 Dabei wird Cu 2+ zu Cu + reduziert. Für die Komplexierung von Cadmium durch Kaliumcyanid gilt: [Cd(NH 3 ) 6 ] KCN 2 K NH 3 + Cd(CN) 2 Cd(CN) KCN [Cd(CN) 4 ] K + Durch Zugabe von H 2 S-Wasser entsteht Cadmium(II)-Sulfid. [Cd(CN) 4 ] 2 + H 2 S CdS+2 H CN Gefahren Von Kaliumcyanid gehen mehrere Gefahren aus. Cyanid-Ionen sind in der Lage in saurer Lösung zur leicht flüchtigen Blausäure (HCN) zu protolysieren, die eine stark toxische Wirkung auf lebende Organismen hat, da das Cyanid Sauerstoffbindungsstellen blockieren kann, was zur inneren Erstickung führt. Zudem ist Cyanid Hautresorptiv. Aus diesem Grund sollte der Versuch im alkalischen durchgeführt werden, damit keine HCN entstehen kann. Versuch in getrennten Reagenzgläsern: Kupfer(II)-Sulfat-Lösung: [Cu() 6 ] NH 3 [Cu(NH 3 ) 4 ] [Cu(NH 3 ) 4 ] 2+ + H 2 S CuS+2 H NH 3 Cadmium(II)-Sulfat-Lösung: [Cd() 6 ] 2+ + NH 3 [Cd(NH 3 ) 6 ] [Cd(NH 3 ) 6 ] 2+ + H 2 S CdS+2 H NH 3 Unterschiede der Fällungen durch Zugabe von H 2 S Im ersten Teilversuch wird Kupfer durch das Cyanid-Ion zu Cu + reduziert. Die Kupfer(I)- Ionen im Tetracyanocuprat(I)-Komplex gehen mit den Sulfid-Ionen keine Verbindung ein. Es fällt also nur Cadmiumsulfid aus, da dieses nach Zugabe von Kaliumcyanid in Oxidationsstufe 2 als Tetracyanocadmat(II)-Komplex vorliegt. Im zweiten Teilversuch liegen beide Metall-Ionen (2 fach positiv geladen) mit der Oxidationsstufe 2 im obigen Komplex vor. Durch Zugabe von Sulfid-Ionen bilden sich die charakteristischen Niederschläge. 8
9 4 Beobachtungen der Hydratisomerie 4.1 Aufgabenstellung Es soll ermittelt werden, dass auch ein teilweiser Ligandenaustausch die Farbe von Komplexen ändern kann. 4.2 Versuchsdurchführung Dieser Versuch findet unter dem Abzug statt. Eine Spatelspitze von feingepulvertem Chromalauns (KCr[SO 4 ] 2 12 ) wird in einem Reagenzglas in einigen ml demineralisiertem Wasser gelöst. Die nun blau violett gefärbte Lösung wird mit dem Bunsenbrenner erhitzt bis eine Farbänderung nach grün stattfindet. 4.3 Beobachtungen Die Lösung hat bei Raumtemperatur eine leichte dunkle blau violette Färbung. Nach kurzem erhitzen (ca. 20 Sekunden) ist die Lösung tiefgrün. 4.4 Deutung und Auswertung Lösen des Chromalaun in Wasser führt zur Entstehung eines Hexaqua-Chromat(III)-Komplexes: Erhitzen der Lösung: KCr[SO 4 ] SO K + + [Cr() 6 ] [Cr() 6 ] 3+ [Cr() 4 SO 4 ] Es entsteht ein Tetraquasulfatochrom(III)-Komplex Hydratisomerie Grenzfall der Ionisationsisomerie, bei der nur Wasser Moleküle als Solvat-Moleküle angesehen werden. Diese können entweder in einem Kristallgitter als Solvat-Moleküle oder als Ligand des Metallkations vorliegen. Welche zwei verschiedenen Isomere sind denkbar für die oktaedrischen Komplexe? [Cr 2 () 4 ] + : Es können zwei verschiedene Isomere gebildet werden, ein cis-tetraquadichloro- Chrom(III)- und trans-tetraquadichloro-crom(iii)-komplex. 9
10 Cr Cr 1 Iso- und trans-form 1 trans-form cis-form [Cr 3 () 3 ]: Kann als mer-triaquatrichloro-chrom(iii)- oder fac-triaquatrichloro-chrom(iii)- Komplex dargestellt werden. Cr Cr 2 mer- und fac-form 2 mer-form trans-form H 2 O fac-form cis-form 1 selbsterstellt 2 selbsterstellt 10
11 5 Stabilität von Chelatkomplexen 5.1 Aufgabenstellung Es soll die Anwendung von Chelatkomplexen in der qualitativen (Versuchsteil a) und der quantitativen Analytik (Versuchsteil b) ermittelt werden. 5.2 Versuchsaufbau a) Eine Tüpfelplatte wird gereinigt und unter dem Abzug bereit gestellt. b) Eine Bürette wird in einen Bürettenhalter eingespannt. Unter der Bürette steht der Erlenmeyerkolben mit der zu Analysierenden Lösung. 5.3 Versuchsdurchführung a) Eine sehr kleine Spatelspitze Ni 2 wird auf die Tüpfelplatte gegeben und mit Ammoniaklösung (2 4 Tropfen) gelöst. Die so entstandene Lösung wird mit Dimethylglyoximlösung (Diacetyldioximlösung) versetzt (1 2 Tropfen). b) Der Kolben mit der Analyselösung wird auf 100 ml aufgefüllt und durchmischt. Es werden von der Lösung 25 ml abpipettiert und in einen Erlenmeyerkolben gegeben. Dieser wird auf ungefähr 100 ml aufgefüllt und die Lösung mit einer Indikatorpuffertablette versetzt. Nach Auflösung der Indikatorpuffertablette wird ca 1 ml Ammoniaklösung hinzugegeben. Nun wird mit 0.1 Molarer EDTA Maßlösung bis zum Umschlagpunkt von braun orange nach grün titriert. 5.4 Beobachtungen a) Das Ni 2 färbt sich blau, wenn es in Ammoniaklösung gelöst wird. Bei Zugabe der Dimethylglyoximlösung färbt sich die Mischung rosa rot. b) Der Titrationsstart ist bei 1.4 ml und das Titrationsende ist bei 12.7 ml. 5.5 Auswertung Versuch a Durch Zugabe von Ammoniaklösung entsteht ein Hexaminnickel(II)-Komplex: Ni 2 6H2O+6 NH 3 [Ni(NH 3 ) 6 ] Entstehung des Dimethylglyoximnickel(II)-Komplexes: [Ni(NH 3 ) 6 ] HC 2 H 6 N 2 O 2 [Ni(C 4 H 6 N 2 O 2 ) 2 ]+2 11
12 Versuch b n sei die Stoffmenge an Ca 2+, c die Konzentration, V das titrierte Volumen und F A der aliquote Faktor ist. n = c EDTA V EDTA F A = 0.1 mol ( ) ml l = 0.1 mol (11.3) ml 4 l = 4.52 mmol 100 ml 25 ml Die bestimmte Stoffmenge an Ca 2+ Ionen in der Lösung beträgt 4.52 mmol, der Sollwert ist 4.46 mmol. Die Prozentuale Abweichung beträgt 1.3%. 5.6 Zusatzaufgabe Struktur des roten Ni 2+ Komplex 3 Ni 2+ Komplex 3 Struktur des EDTA-Calcium(II) Komplex (EDTA = Ethylendiamintetraacetat, M = Ca 2+ ) 4 EDTA
Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O
![Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O](/thumbs/78/78095730.jpg) Matthias Hinrichs 22.11.1999 Praktikum Anorganische Chemie II Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O 1. Theorie: Die rklärung zur Art und Struktur von Komplexen, werden am besten durch die Kristallfeldtheorie
Matthias Hinrichs 22.11.1999 Praktikum Anorganische Chemie II Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O 1. Theorie: Die rklärung zur Art und Struktur von Komplexen, werden am besten durch die Kristallfeldtheorie
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+
![Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ Elektronenspektrum von [Ti(H 2 O) 6 ] 3+](/thumbs/66/55543366.jpg) Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Komplexchemie des Nickels Ligandenaustauschreaktionen
 Komplexchemie des Nickels Ligandenaustauschreaktionen Jorge Ferreiro, 1. Semester, D-CHAB, fjorge@student.ethz.ch Assistent: Kyrill Stanek Abstract: In diesem Versuch ging es darum, verschiedene Ligandenaustauschreaktionen
Komplexchemie des Nickels Ligandenaustauschreaktionen Jorge Ferreiro, 1. Semester, D-CHAB, fjorge@student.ethz.ch Assistent: Kyrill Stanek Abstract: In diesem Versuch ging es darum, verschiedene Ligandenaustauschreaktionen
Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment
 1 Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment Zusatzaufgaben zu Versuch 316 : 1. Berechnen Sie das magnetische Moment des Co + - Ions.. Welche Niveaus der Valenzelektronen sind beim Co +
1 Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment Zusatzaufgaben zu Versuch 316 : 1. Berechnen Sie das magnetische Moment des Co + - Ions.. Welche Niveaus der Valenzelektronen sind beim Co +
Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO 2-4 PO 3-4 +H + -H+ +H + Stefan Wuttke # 1
 Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO - 4 HPO 2-4 PO 3-4 +H + -H+ +H + -H+ +H + Stefan Wuttke # 1 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner + AgNO 3 AgCl +
Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO - 4 HPO 2-4 PO 3-4 +H + -H+ +H + -H+ +H + Stefan Wuttke # 1 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner + AgNO 3 AgCl +
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl
2. Woche. Anorganische Analysenmethodik
 2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
Komplexchemie und Molekülgeometrie. Aufbau und Nomenklatur von Komplexverbindungen
 Aufbau und Nomenklatur von Komplexverbindungen Komplexverbindungen sind chemische Verbindungen, die aus einem Zentralatom und Molekülen bzw. Ionen gebildet werden. Aufbau von Komplexverbindungen Zentralatom
Aufbau und Nomenklatur von Komplexverbindungen Komplexverbindungen sind chemische Verbindungen, die aus einem Zentralatom und Molekülen bzw. Ionen gebildet werden. Aufbau von Komplexverbindungen Zentralatom
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel )
 EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
AC II Praktikum SoSe 04
 AC II Praktikum SoSe 04 Julia Blechinger Saal K Assistent: Constanze Vogler Durchführung: 05.05.04 Protokoll zur Präparategruppe 8: Übergangsmetallkomplexe Darstellung von [Co(NH 3 ) 5 Br]Br 2 I. Theoretischer
AC II Praktikum SoSe 04 Julia Blechinger Saal K Assistent: Constanze Vogler Durchführung: 05.05.04 Protokoll zur Präparategruppe 8: Übergangsmetallkomplexe Darstellung von [Co(NH 3 ) 5 Br]Br 2 I. Theoretischer
Beispielaufgaben IChO 2. Runde 2019 Koordinationschemie
 Beispiel 1 Metalle und Elektronen Bei der Besetzung von Atomorbitalen werden die Elektronen ausgehend vom energetisch am tiefsten liegenden Atomorbital in Richtung ansteigender Energie mit den Elektronen
Beispiel 1 Metalle und Elektronen Bei der Besetzung von Atomorbitalen werden die Elektronen ausgehend vom energetisch am tiefsten liegenden Atomorbital in Richtung ansteigender Energie mit den Elektronen
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 13. Juli 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 13. Juli 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Meistens sind die Komplexe jedoch nicht so stabil und dissoziieren in Lösung teilweise in ihre Bestandteile.
 Stabilität von Komplexen Gleichgewichte - Komplexionen In manchen Fällen sind die Komplexe so stabil, dass sie Salze bilden, die keine Eigenschaften der ursprünglichen Ionen mehr aufweisen. z.b. Das Komplexion
Stabilität von Komplexen Gleichgewichte - Komplexionen In manchen Fällen sind die Komplexe so stabil, dass sie Salze bilden, die keine Eigenschaften der ursprünglichen Ionen mehr aufweisen. z.b. Das Komplexion
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 29. Januar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 29. Januar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Versuch VI.2: Komplexchemie des Nickels Auswertung von Lars Müller
 Name: Lars Müller Gruppe: Donati (HCI J196/168) Datum: 15. Jan. 2004 Versuch VI.2: Komplexchemie des ckels Auswertung von Lars Müller Ziel ckel(ii) kann sehr verschiedene Metallkomplexe bilden, die meist
Name: Lars Müller Gruppe: Donati (HCI J196/168) Datum: 15. Jan. 2004 Versuch VI.2: Komplexchemie des ckels Auswertung von Lars Müller Ziel ckel(ii) kann sehr verschiedene Metallkomplexe bilden, die meist
Farbe der anorganischen Pigmente
 Farbe der anorganischen Pigmente 1. Farbigkeit der Komplex-Ionen (Ligandenfeld-Theorie) Einführung Versuch 1 Geben Sie einen halben Löffel festes Kupfersulfat in ein grosses Reagenzglas (RG) und erwärmen
Farbe der anorganischen Pigmente 1. Farbigkeit der Komplex-Ionen (Ligandenfeld-Theorie) Einführung Versuch 1 Geben Sie einen halben Löffel festes Kupfersulfat in ein grosses Reagenzglas (RG) und erwärmen
Komplexbildung. CoCl 3 5 NH 3. CoCl 3 6 NH 3. CoCl 3 4 NH 3 Alfred Werner The Nobel Prize in Chemistry 1913
 Komplexbildung CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner 1866-1919 The Nobel Prize in Chemistry 1913 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH
Komplexbildung CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner 1866-1919 The Nobel Prize in Chemistry 1913 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH
Ligandenfeldtheorie Magnetismus von Komplexen
 Arbeitsblätter zum Ausdrucken von sofatutor.com Ligandenfeldtheorie Magnetismus von Komplexen Schildere die Unterschiede zwischen highspin- und lowspin-komplexen. 2 Gib die Orbitale an, die im oktaedrischen
Arbeitsblätter zum Ausdrucken von sofatutor.com Ligandenfeldtheorie Magnetismus von Komplexen Schildere die Unterschiede zwischen highspin- und lowspin-komplexen. 2 Gib die Orbitale an, die im oktaedrischen
Anorganische Chemie für Biologen. Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/
 Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Inhalte Stöchiometrie chemisches Rechnen Chemisches Gleichgewicht
Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Inhalte Stöchiometrie chemisches Rechnen Chemisches Gleichgewicht
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen
 Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Anorganische Chemie II Veröffentlichung vom 26. Juni Valende Bond Theorie Grundlagen Mängel des Modells...
 Anorganische Chemie II Veröffentlichung vom 26. Juni 2005 Inhaltsverzeichnis 1 Valende Bond Theorie 2 1.1 Grundlagen............................................. 2 1.2 Mängel des Modells.........................................
Anorganische Chemie II Veröffentlichung vom 26. Juni 2005 Inhaltsverzeichnis 1 Valende Bond Theorie 2 1.1 Grundlagen............................................. 2 1.2 Mängel des Modells.........................................
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 24. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Anorganische Chemie II B. Sc. Chemieingenieurwesen 24. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Spezielle Chemie Vorlesungsteil Koordinationschemie (Stand SS 2014) Institut für Organische Chemie Leibniz Universität Hannover
 Spezielle Chemie Vorlesungsteil Koordinationschemie (Stand SS 2014) Institut für Organische Chemie Leibniz Universität Hannover verantwortlich: Prof. Dr. A. Kirschning 1 Co Vitamin B12 Chemische Bindungstypen
Spezielle Chemie Vorlesungsteil Koordinationschemie (Stand SS 2014) Institut für Organische Chemie Leibniz Universität Hannover verantwortlich: Prof. Dr. A. Kirschning 1 Co Vitamin B12 Chemische Bindungstypen
AnC I Protokoll: 7.1 Synthese und Charakterisierung von Tetraamminkupfer(II)-sulfat! SS Analytische Chemie I.
 Analytische Chemie I Versuchsprotokoll 7.1 Synthese und Charakterisierung der Komplexverbindung Tetraamminkupfer(II)-sulfat 1.! Theoretischer Hintergrund Aus Kupfer(II)-sulfat und Ammoniak wird zunächst
Analytische Chemie I Versuchsprotokoll 7.1 Synthese und Charakterisierung der Komplexverbindung Tetraamminkupfer(II)-sulfat 1.! Theoretischer Hintergrund Aus Kupfer(II)-sulfat und Ammoniak wird zunächst
H1 Bestimmung des Löslichkeitsprodukts von Magnesiumhydroxid
 H Löslichkeitsprodukt und Komplexgleichgewichte Auch bei den Komplex-Reaktionen beschäftigen wir uns im Wesentlichen mit Gleichgewichtsreaktionen, in denen Liganden ausgetauscht werden. Dabei sollen Kriterien
H Löslichkeitsprodukt und Komplexgleichgewichte Auch bei den Komplex-Reaktionen beschäftigen wir uns im Wesentlichen mit Gleichgewichtsreaktionen, in denen Liganden ausgetauscht werden. Dabei sollen Kriterien
Übungsaufgaben zur Koordinationschemie
 Übungsaufgaben zur Koordinationschemie 1. Wie entstehen Komplexe und wie sind sie zusammengesetzt? Warum bilden die Nebengruppenelemente besonders stabile Koordinationsverbindungen? 2. Formulieren Sie
Übungsaufgaben zur Koordinationschemie 1. Wie entstehen Komplexe und wie sind sie zusammengesetzt? Warum bilden die Nebengruppenelemente besonders stabile Koordinationsverbindungen? 2. Formulieren Sie
Chemie Protokoll. Versuch 2 5 (NGE) Nebengruppenelemente. Stuttgart, Sommersemester 2012
 Chemie Protokoll Versuch 2 5 (NGE) Nebengruppenelemente Stuttgart, Sommersemester 2012 Gruppe 10 Jan Schnabel Maximilian Möckel Henri Menke Assistent: Bischoff 6. Juni 2012 Inhaltsverzeichnis 1 Theorie
Chemie Protokoll Versuch 2 5 (NGE) Nebengruppenelemente Stuttgart, Sommersemester 2012 Gruppe 10 Jan Schnabel Maximilian Möckel Henri Menke Assistent: Bischoff 6. Juni 2012 Inhaltsverzeichnis 1 Theorie
Franziska Schleusser und Sarah Zurmühle Labor - Komplexreaktionen 1
 Franziska Schleusser und Sarah Zurmühle Labor - Komplexreaktionen 1 Laborbericht Repetition Komplexreaktionen 1 Fragestellung / Problemstellung Wie können Komplexe hergestellt und verändert werden? Wie
Franziska Schleusser und Sarah Zurmühle Labor - Komplexreaktionen 1 Laborbericht Repetition Komplexreaktionen 1 Fragestellung / Problemstellung Wie können Komplexe hergestellt und verändert werden? Wie
Ligandenaustausch am Chrom(III)-ion. Gefährdungsbeurteilung. Lehrerexperiment. Schülerexperiment
 Ligandenaustausch am Chrom(III)-ion keine! Chrom(III)-chlorid-Lösung (0,1 mol/l) R-Sätze: 22 S-Sätze: 24-25 Ammoniak-Lösung (20%ig) Eine Chrom(III)-chloridlösung wird im Reagenzglas tropfenweise bis zur
Ligandenaustausch am Chrom(III)-ion keine! Chrom(III)-chlorid-Lösung (0,1 mol/l) R-Sätze: 22 S-Sätze: 24-25 Ammoniak-Lösung (20%ig) Eine Chrom(III)-chloridlösung wird im Reagenzglas tropfenweise bis zur
Chemie Praktikum Protokoll Seminartag 5, 6, 7 Qualitative Analyse
 Chemie Praktikum Protokoll Seminartag 5, 6, 7 Qualitative Analyse Michael Schlagmüller 10. Februar 2006 1 Spektralanalyse Die Spektralanalyse wird im Praktikum mittels Flammspektroskopie durchgeführt.
Chemie Praktikum Protokoll Seminartag 5, 6, 7 Qualitative Analyse Michael Schlagmüller 10. Februar 2006 1 Spektralanalyse Die Spektralanalyse wird im Praktikum mittels Flammspektroskopie durchgeführt.
Versuche zur Ligandenfeldtheorie
 Praktikum IV, Herbstsemester 10 Versuch C2; 14.04.2010 Autoren: Michael Schwarzenberger (michschw@student.ethz.ch) Philippe Knüsel (pknuesel@student.ethz.ch) Teilnehmer: Michael Schwarzenberger und Philippe
Praktikum IV, Herbstsemester 10 Versuch C2; 14.04.2010 Autoren: Michael Schwarzenberger (michschw@student.ethz.ch) Philippe Knüsel (pknuesel@student.ethz.ch) Teilnehmer: Michael Schwarzenberger und Philippe
Die Bindung in Übergangsmetallkomplexenn. Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth
 Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Komplexe SPF BCH am Inhaltsverzeichnis Ihr könnt die Formeln von Komplexsalzen korrekt aufschreiben... 2
 Komplexe Inhaltsverzeichnis Ihr könnt die Formeln von Komplexsalzen korrekt aufschreiben... 2 Ihr könnt die Namen von Komplexsalzen aus den Formeln herleiten... 2 Ihr könnt aus der Beschreibung einer Komplexreaktion
Komplexe Inhaltsverzeichnis Ihr könnt die Formeln von Komplexsalzen korrekt aufschreiben... 2 Ihr könnt die Namen von Komplexsalzen aus den Formeln herleiten... 2 Ihr könnt aus der Beschreibung einer Komplexreaktion
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP4 - Gesamtanalyse» Martin Wolf Betreuerin: Frau Sachse Datum: 05.05.2006 8:00 Uhr bis 12:00 Uhr
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP4 - Gesamtanalyse» Martin Wolf Betreuerin: Frau Sachse Datum: 05.05.2006 8:00 Uhr bis 12:00 Uhr
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum SS
 Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum SS 2003 20.10.2003 Name: Vorname: Matrikelnummer: Fachsemester: Punkte: Note: Frage 1 Bei 25 C lösen sich 0,02869 g CuBr in einem
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum SS 2003 20.10.2003 Name: Vorname: Matrikelnummer: Fachsemester: Punkte: Note: Frage 1 Bei 25 C lösen sich 0,02869 g CuBr in einem
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 27. September 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Anorganische Chemie II B. Sc. Chemieingenieurwesen 27. September 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Synthese von cis-bis(glycinato)kupfer(ii)
 ZÜRCHER HOCHSCHULE FÜR ANGEWANDTE WISSENSCHAFTEN DEPARTEMENT LIFE SCIENCES UND FACILITY MANAGEMENT INSTITUT FÜR CHEMIE UND BIOLOGISCHE CHEMIE (ICBC) WÄDENSWIL Synthese von cis-bis(glycinato)kupfer(ii)
ZÜRCHER HOCHSCHULE FÜR ANGEWANDTE WISSENSCHAFTEN DEPARTEMENT LIFE SCIENCES UND FACILITY MANAGEMENT INSTITUT FÜR CHEMIE UND BIOLOGISCHE CHEMIE (ICBC) WÄDENSWIL Synthese von cis-bis(glycinato)kupfer(ii)
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 18. Juli 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 18. Juli 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 04. Februar 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 04. Februar 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Thema: Komplexverbindungen, die koordinative Bindung. Koordinationszahl, 18-Elektronen-Schale, ein- mehrzähnige Liganden, EDTA,
 Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Konfigurationsisomerie (Stereoisomerie)
 Konfigurationsisomerie (Stereoisomerie) Komplexe, die dieselbe chemische Zusammensetzung (gleiche Summenformel) und Ladung, aber einen verschiedenen räumliche Anordnung (Konfiguration) der Atome haben,
Konfigurationsisomerie (Stereoisomerie) Komplexe, die dieselbe chemische Zusammensetzung (gleiche Summenformel) und Ladung, aber einen verschiedenen räumliche Anordnung (Konfiguration) der Atome haben,
Anorganische Chemie II
 Anorganische Chemie II Christian Lehmann 11. Mai 2004 Inhaltsverzeichnis I Komplexchemie 2 1 Aufbau und Eigenschaften von Komplexen 2 2 Nomenklatur 2 3 Der räumliche Aufbau von Komplexen 3 3.1 Koordinationszahlen
Anorganische Chemie II Christian Lehmann 11. Mai 2004 Inhaltsverzeichnis I Komplexchemie 2 1 Aufbau und Eigenschaften von Komplexen 2 2 Nomenklatur 2 3 Der räumliche Aufbau von Komplexen 3 3.1 Koordinationszahlen
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 07. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 07. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
4. Komplexe 4.7. Komplexe in wässriger Lösung Stufenweise Komplexbildung
 4. Komplexe 4.7. Komplexe in wässriger Lösung 4.7.. Stufenweise Komplexbildung 17 Der schrittweise Austauschprozess der Wassermoleküle in einem Aquakomplex [M z+ (aq)] mit einem neutralen (oder geladenen)
4. Komplexe 4.7. Komplexe in wässriger Lösung 4.7.. Stufenweise Komplexbildung 17 Der schrittweise Austauschprozess der Wassermoleküle in einem Aquakomplex [M z+ (aq)] mit einem neutralen (oder geladenen)
Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen?
 Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen? Michael Kalcher 7AM In h a l t Eisen - Eigenschaften 2 Wertigkeit und Oxidationszahl 2 Üb e r g a n g s m e ta l l e 3
Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen? Michael Kalcher 7AM In h a l t Eisen - Eigenschaften 2 Wertigkeit und Oxidationszahl 2 Üb e r g a n g s m e ta l l e 3
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 16. Juli 2015 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 16. Juli 2015 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
F2 Magnetische Waage
 F Magnetische Waage 1. Aufgabenstellung: Für anorganische Komplexverbindungen soll aus der Messung der magnetischen Suszeptibilität die Zahl der ungepaarten Elektronen und aus der Messung der UV- Spektren
F Magnetische Waage 1. Aufgabenstellung: Für anorganische Komplexverbindungen soll aus der Messung der magnetischen Suszeptibilität die Zahl der ungepaarten Elektronen und aus der Messung der UV- Spektren
Lösungen. Vorprüfungsklausur. Leistungskurs Chemie 2008 / 09
 Gymnasium St. Augustin zu Grimma Lösungen Vorprüfungsklausur Leistungskurs Chemie 2008 / 09 Name: Experiment: C1 / C2 Seitenzahl: Grimma, 27. Februar 2009 TEIL A 1.) 1.1 Elektronenkonfiguration: 50Sn:
Gymnasium St. Augustin zu Grimma Lösungen Vorprüfungsklausur Leistungskurs Chemie 2008 / 09 Name: Experiment: C1 / C2 Seitenzahl: Grimma, 27. Februar 2009 TEIL A 1.) 1.1 Elektronenkonfiguration: 50Sn:
A. Mezzetti Fragenkatalog X
 Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
Mößbauer-Spektroskopie
 Mößbauer-Spektroskopie Westfälische Wilhelms-Universität Münster Ansgar Stüken & Thomas Dröge 12.05.2005 Überblick Elektrische Monopolwechselwirkung (Isomerieverschiebung) Elektrische Quadrupolwechselwirkung
Mößbauer-Spektroskopie Westfälische Wilhelms-Universität Münster Ansgar Stüken & Thomas Dröge 12.05.2005 Überblick Elektrische Monopolwechselwirkung (Isomerieverschiebung) Elektrische Quadrupolwechselwirkung
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Kapitel 18: Analytik und Ionennachweise
 1 Kapitel 18: Analytik und Ionennachweise 2 Inhalt Kapitel 18: Analytik und Ionennachweise...1 Inhalt... 2 von Ionen...3 durch Fällungsreaktionen oder Farbreaktionen...3 Wie entsteht ein schwerlösliches
1 Kapitel 18: Analytik und Ionennachweise 2 Inhalt Kapitel 18: Analytik und Ionennachweise...1 Inhalt... 2 von Ionen...3 durch Fällungsreaktionen oder Farbreaktionen...3 Wie entsteht ein schwerlösliches
Vorgehen bei der qualitativen Analyse. Nachweisreaktion. Nachweisreaktionen. molekular gebauter Stoffe
 Vorgehen bei der qualitativen Analyse 1. Vorprobe liefert Hinweise auf die mögliche Zusammensetzung der Probe ; Bsp. Flammenfärbung 2. Blindprobe zeigt aus Aussehen der Nachweisreagenzien; Vergleichsprobe
Vorgehen bei der qualitativen Analyse 1. Vorprobe liefert Hinweise auf die mögliche Zusammensetzung der Probe ; Bsp. Flammenfärbung 2. Blindprobe zeigt aus Aussehen der Nachweisreagenzien; Vergleichsprobe
Aufgabe Punkte (je 10) Name: Vorname: Matrikel-Nr.
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt) Abschlußklausur
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt) Abschlußklausur
Säuren und Basen nach Brönsted
 Säuren und Basen nach Brönsted Es gibt versch. Definitionen von Säuren und Basen. Nach Brönsted ist eine Säure (HA) ein Protonendonator und eine Base (B) ein Protonenakzeptor, d.h. eine Säure reagiert
Säuren und Basen nach Brönsted Es gibt versch. Definitionen von Säuren und Basen. Nach Brönsted ist eine Säure (HA) ein Protonendonator und eine Base (B) ein Protonenakzeptor, d.h. eine Säure reagiert
Praktische Einführung in die Chemie Integriertes Praktikum:
 Praktische Einführung in die Chemie ntegriertes Praktikum: Versuch 1-6 (ROG) Redoxgleichgewicht Versuchs-Datum: 9. Mai 212 Gruppenummer: 8 Gruppenmitglieder: Domenico Paone Patrick Küssner Michael Schmid
Praktische Einführung in die Chemie ntegriertes Praktikum: Versuch 1-6 (ROG) Redoxgleichgewicht Versuchs-Datum: 9. Mai 212 Gruppenummer: 8 Gruppenmitglieder: Domenico Paone Patrick Küssner Michael Schmid
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
Struktur von Komplexverbindungen
 Struktur von Komplexverbindungen 23.2.99 Alexander Slomian Wenn Du sie nicht überzeugen kannst, dann verwirre sie Alexander Slomian Seite 1 29.09.2000 Einleitung Im Dezember 1892 wachte Alfred Werner,
Struktur von Komplexverbindungen 23.2.99 Alexander Slomian Wenn Du sie nicht überzeugen kannst, dann verwirre sie Alexander Slomian Seite 1 29.09.2000 Einleitung Im Dezember 1892 wachte Alfred Werner,
Grundlagen der Chemie Säuren und Basen
 Säuren und Basen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Säure-Base-Theorien Die Begriffe Säure und Base
Säuren und Basen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Säure-Base-Theorien Die Begriffe Säure und Base
Versuch: Nachweis von Salicylsäure
 Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Abschlußklausur (Nachklausur)
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt) Abschlußklausur
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt) Abschlußklausur
Oxidation = Elektronenabgabe Erhöhung der Oxidationszahl. Reduktion = Elektronenaufnahme Erniedrigung der Oxidationszahl
 Oxidation = Elektronenabgabe Erhöhung der Oxidationszahl Reduktion = Elektronenaufnahme Erniedrigung der Oxidationszahl Oxidans = Oxidationsmittel System, das Elektronen aufnehmen kann Reduktor = Reduktionsmittel
Oxidation = Elektronenabgabe Erhöhung der Oxidationszahl Reduktion = Elektronenaufnahme Erniedrigung der Oxidationszahl Oxidans = Oxidationsmittel System, das Elektronen aufnehmen kann Reduktor = Reduktionsmittel
Zusatzinformation zum Anorganisch Chemischen Grundpraktikum. 3. Teil: Komplexe
 Zusatzinformation zum Anorganisch Chemischen Grundpraktikum 3. Teil: Komplexe Dr. A. Hepp (29.06.2011) Nomenklatur von Komplexverbindungen Allgemeines: Im Mittelpunkt einer Komplexverbindung steht das
Zusatzinformation zum Anorganisch Chemischen Grundpraktikum 3. Teil: Komplexe Dr. A. Hepp (29.06.2011) Nomenklatur von Komplexverbindungen Allgemeines: Im Mittelpunkt einer Komplexverbindung steht das
Protokoll Tag 3. C. Kationennachweise. C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4
 Protokoll Tag 3 C. Kationennachweise C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4 V16 Nachweis von Na +, K +, Ca 2+, Sr 2+ und Ba 2+ durch Flammenfärbung Bei der Flammenprobe geht es
Protokoll Tag 3 C. Kationennachweise C.1. Nachweis von Na +, Mg 2+, Ca 2+, Sr 2+, BA 2+ sowie NH + 4 V16 Nachweis von Na +, K +, Ca 2+, Sr 2+ und Ba 2+ durch Flammenfärbung Bei der Flammenprobe geht es
AnC I Protokoll: 5.5 Simultanbestimmung von Bi/Pb! SS Analytische Chemie I. Versuchsprotokoll. 5.5 Simultanbestimmung von Bi/Pb
 Analytische Chemie I Versuchsprotokoll 5.5 Simultanbestimmung von Bi/Pb.! Theoretischer Hintergrund Bi 3+ und Pb 2+ werden nebeneinander bestimmt. Bismut(III) bildet bereits im Sauren einen EDTA-Komplex,
Analytische Chemie I Versuchsprotokoll 5.5 Simultanbestimmung von Bi/Pb.! Theoretischer Hintergrund Bi 3+ und Pb 2+ werden nebeneinander bestimmt. Bismut(III) bildet bereits im Sauren einen EDTA-Komplex,
Mehrprotonige Säuren (z.b. H 2 SO 4 )
 Mehrprotonige Säuren (z.b. H SO 4 ) Mehrprotonige Säuren protolysieren stufenweise. Jede Stufe hat eine eigene Säurekonstante, deren Werte von Stufe zu Stufe kleiner werden (die Protolyse wird immer unvollständiger).
Mehrprotonige Säuren (z.b. H SO 4 ) Mehrprotonige Säuren protolysieren stufenweise. Jede Stufe hat eine eigene Säurekonstante, deren Werte von Stufe zu Stufe kleiner werden (die Protolyse wird immer unvollständiger).
Laborprotokoll Qualitative Analyse Ralph Koitz, Einzelsalz
 1. Einzelsalz Aufgabenstellung: Nasschemische qualitative Analyse eines anorganischen Einzelsalzes. o Farblose, grobkörnige Kristalle o Flammenfärbung: leicht orange, nicht charakteristisch da vermutlich
1. Einzelsalz Aufgabenstellung: Nasschemische qualitative Analyse eines anorganischen Einzelsalzes. o Farblose, grobkörnige Kristalle o Flammenfärbung: leicht orange, nicht charakteristisch da vermutlich
Al OH Al(OH) 3
 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH Al(OH) 3 Al(OH) 3 + OH - [Al(OH) 4 ] - Tetrahydroxoaluminat (III) 1 Hydrate Amphoteres Verhalten von Hydroxiden (z.b. Al 3+, Sn
Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH Al(OH) 3 Al(OH) 3 + OH - [Al(OH) 4 ] - Tetrahydroxoaluminat (III) 1 Hydrate Amphoteres Verhalten von Hydroxiden (z.b. Al 3+, Sn
Versuche zum Thema Aminosäuren
 Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Abschlußklausur (Nachklausur)
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Praktikum Anorganische und Analytische Chemie Abschlußklausur (Nachklausur) 13.1.2012 Name: Vorname: Matrikel-Nr. Hinweis: Verwenden Sie für die Antworten den
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Praktikum Anorganische und Analytische Chemie Abschlußklausur (Nachklausur) 13.1.2012 Name: Vorname: Matrikel-Nr. Hinweis: Verwenden Sie für die Antworten den
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Musterlösung. Bitte eintragen: Matrikelnummer: 0815 Name: Musterstudi.
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/
 Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/2003 22.04.2003 Name: Vorname: Matrikelnummer: Fachsemester: Punkte: Note: Frage 1 Welche Flammenfärbung zeigen folgende
Studienbegleitende Prüfung Modul 12 Anorganisch-Chemisches Grundpraktikum WS 2002/2003 22.04.2003 Name: Vorname: Matrikelnummer: Fachsemester: Punkte: Note: Frage 1 Welche Flammenfärbung zeigen folgende
Aufgabe 1.1 Welche der folgenden Aussagen in Bezug auf nachfolgende Reaktionsgleichung ist falsch? HCl + NH3 NH4 + + Cl -
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen in Bezug auf nachfolgende Reaktionsgleichung ist falsch? HCl + NH3 NH4 + + Cl - A) Salzsäure ist eine stärkere
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen in Bezug auf nachfolgende Reaktionsgleichung ist falsch? HCl + NH3 NH4 + + Cl - A) Salzsäure ist eine stärkere
Aufgabe Punkte (je 10) Anorganisches Grund-Praktikum (Lehramt/2-Fach Bachelor) Abschlußklausur (Nachklausur)
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt/2-Fach
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt/2-Fach
Aufgabe Punkte (je 10) Anorganisches Grund-Praktikum (Poly-BSc/Lehramt) Abschlußklausur (Nachklausur) Name: Vorname: Matrikel-Nr.
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Poly-BSc/Lehramt)
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Poly-BSc/Lehramt)
Protokolle zu den Analysen
 Qualitative Analysen Protokolle zu den Analysen Namen, Datum und Analysennummer angeben Möglicherweise enthaltene Ionen angeben Merkmale wie Farbe, Homogenität, (Geruch) feststellen Vorproben wie, Flammenfärbung,
Qualitative Analysen Protokolle zu den Analysen Namen, Datum und Analysennummer angeben Möglicherweise enthaltene Ionen angeben Merkmale wie Farbe, Homogenität, (Geruch) feststellen Vorproben wie, Flammenfärbung,
Versuch Synthese von Kupfer(I)-oxid. Einleitung. Material und Methoden. Versuchsdurchführung
 Synthese von Kupfer(I)-oxid Versuch 3.16 Ausgehend von Kupfersulfat soll Kupfer(I)oxid gebildet werden. Kupfer(I) neigt in wässriger Lösung zur Disproportionierung und ist daher instabil. Die Gleichung
Synthese von Kupfer(I)-oxid Versuch 3.16 Ausgehend von Kupfersulfat soll Kupfer(I)oxid gebildet werden. Kupfer(I) neigt in wässriger Lösung zur Disproportionierung und ist daher instabil. Die Gleichung
Kaliumdioxalatocuprat(II)- dihydrat
 Kaliumdioxalatocuprat(II)- dihydrat K[Cu(C4)]H Zürich, 17. November 004 Raphael Aardoom, ACP 300 o C 00 50 150 50 ml 100 A N AUS AN AUS 1000 50 ml 0 U/min 1500 50 750 500 1 Synthese 1.1 Methode [1] Kupfer(II)sulfat-pentahydrat
Kaliumdioxalatocuprat(II)- dihydrat K[Cu(C4)]H Zürich, 17. November 004 Raphael Aardoom, ACP 300 o C 00 50 150 50 ml 100 A N AUS AN AUS 1000 50 ml 0 U/min 1500 50 750 500 1 Synthese 1.1 Methode [1] Kupfer(II)sulfat-pentahydrat
Versuchsüberschrift nach dem Schema: Protonierung der Base mit der Säure
 Arbeitsheft Säuren und Basen Inhalt Jakob 1 Inhaltsverzeihnis: Seite: 1 Definition für wässrige Lösungen (Arrhenius) 1.1 Wasser Chlorwasserstoff 2 1.2 Ammoniak Wasser 3 2 Allgemeine Definition (Brönsted)
Arbeitsheft Säuren und Basen Inhalt Jakob 1 Inhaltsverzeihnis: Seite: 1 Definition für wässrige Lösungen (Arrhenius) 1.1 Wasser Chlorwasserstoff 2 1.2 Ammoniak Wasser 3 2 Allgemeine Definition (Brönsted)
Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit und Lesbarkeit. Spätere Beanstandungen werden nicht berücksichtigt!
 Klausur zur Grundvorlesung Allg. und Anorg. Chemie vom 11.01.2005 Seite 1 von 10 Punkte: Matrikelnummer: Name: Vorname: Bitte eintragen: Fachsemester: Fachrichtung: Bitte ankreuzen: Biologie Molekulare
Klausur zur Grundvorlesung Allg. und Anorg. Chemie vom 11.01.2005 Seite 1 von 10 Punkte: Matrikelnummer: Name: Vorname: Bitte eintragen: Fachsemester: Fachrichtung: Bitte ankreuzen: Biologie Molekulare
Anorganische Chemie für Biologen
 Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Arten chemischer Bindung Die entscheidende Größe für den
Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Arten chemischer Bindung Die entscheidende Größe für den
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Punkte. Bitte eintragen: Matrikelnummer: Bitte ankreuzen: Biotechnologie Pharmazie
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
4. Isomerie von Komplexverbindungen
 4. Isomerie von Komplexverbindungen 4. Isomerie bei Koordinationsverbindungen Grundsätzlich unterscheidet man Konstitutionsisomerie Strukturisomerie) und Stereoisomerie (Konfigutationsisomerie). Konstitutionsisomerie:
4. Isomerie von Komplexverbindungen 4. Isomerie bei Koordinationsverbindungen Grundsätzlich unterscheidet man Konstitutionsisomerie Strukturisomerie) und Stereoisomerie (Konfigutationsisomerie). Konstitutionsisomerie:
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Extraktion/Komplexbildung
 Extraktion/Komplexbildung Inhalte dieser Lerneinheit: Quantitativer Nachweis von Eisen mit o-phenanthrolin Quantitativer Nachweis von Kupfer mit Bichinolin Dabei werden Grundlagen der: Komplexbildung und
Extraktion/Komplexbildung Inhalte dieser Lerneinheit: Quantitativer Nachweis von Eisen mit o-phenanthrolin Quantitativer Nachweis von Kupfer mit Bichinolin Dabei werden Grundlagen der: Komplexbildung und
LAF-Wiederholungsklausur. Wintersemester 2011/12
 LAF-Wiederholungsklausur Wintersemester 2011/12 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene
LAF-Wiederholungsklausur Wintersemester 2011/12 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene
Pentan enthält 12 Atome Wasserstoff, ein Wassermolekül 2 Atome. Es entstehen also 6 Moleküle Wasser:
 VERTIEFUNG Aufstellen und Einrichten von Gleichungen Reaktionsgleichungen fassen eine chemische Reaktion knapp zusammen. Es werden die Edukte (Ausgangsstoffe) angegeben, die in der chemischen Reaktion
VERTIEFUNG Aufstellen und Einrichten von Gleichungen Reaktionsgleichungen fassen eine chemische Reaktion knapp zusammen. Es werden die Edukte (Ausgangsstoffe) angegeben, die in der chemischen Reaktion
Anorganische Chemie. Versuch 16 Titration einer schwachen Säure gegen eine starke Base. Versuchsteil 16.1 Potentiometrische Titration
 Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Anorganische Chemie Versuch 16 Titration einer schwachen Säure gegen eine starke Base Versuchsteil 16.1 Potentiometrische Titration
Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Anorganische Chemie Versuch 16 Titration einer schwachen Säure gegen eine starke Base Versuchsteil 16.1 Potentiometrische Titration
Übungsblatt 1. Anmerkung zu allen Aufgaben: Entnehmen Sie weitere eventuell notwendige Angaben dem Periodensystem!
 Übungsblatt 1 1. Wieviel Atome enthält 1.0 g Eisen? Wieviel Moleküle enthält 1.0 L Wasser (Dichte ρ = 1.0 g/cm 3 )? 2. Die Untersuchung von Pyrit zeigt, dass er zu 46.6 % aus Eisen und zu 53.4 % aus Schwefel
Übungsblatt 1 1. Wieviel Atome enthält 1.0 g Eisen? Wieviel Moleküle enthält 1.0 L Wasser (Dichte ρ = 1.0 g/cm 3 )? 2. Die Untersuchung von Pyrit zeigt, dass er zu 46.6 % aus Eisen und zu 53.4 % aus Schwefel
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 31. Januar 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 31. Januar 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
3. Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14
 3. Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14 Teil des Moduls MN-C-AlC S. Sahler, M. Wolberg 20.01.14 Titrimetrie (Volumetrie) Prinzip: Messung des Volumenverbrauchs einer Reagenslösung
3. Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14 Teil des Moduls MN-C-AlC S. Sahler, M. Wolberg 20.01.14 Titrimetrie (Volumetrie) Prinzip: Messung des Volumenverbrauchs einer Reagenslösung
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
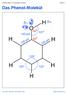 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Glycerin-Projekt Fällt die Fehling Probe mit Glycerin positiv aus?
 Glycerin-Projekt Fällt die Fehling Probe mit Glycerin positiv aus? Melanie Ripsam, Christoph Hille Technische Universität München 13. Dezember 2016 Dieses Werk ist lizenziert unter CC BY 3.0 DE 1 Einleitung
Glycerin-Projekt Fällt die Fehling Probe mit Glycerin positiv aus? Melanie Ripsam, Christoph Hille Technische Universität München 13. Dezember 2016 Dieses Werk ist lizenziert unter CC BY 3.0 DE 1 Einleitung
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2017 Die Klausur besteht aus 10 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
Chemisches Praktikum für Biologen Klausur am 13.02.2017 Die Klausur besteht aus 10 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
3. Wieviel bindig sind folgende Elemente in kovalenten Bindungen? Einige Elemente können auch verschiedene Bindigkeiten zeigen
 Übungen zur VL Chemie für Biologen und umanbiologen 26. 11.2010 1. ennen Sie mindestens 2 Arten der chemischen Bindungen und geben Sie je 2 Beispielverbindungen dafür an (Strukturformel). 1) Ionische Bindung:
Übungen zur VL Chemie für Biologen und umanbiologen 26. 11.2010 1. ennen Sie mindestens 2 Arten der chemischen Bindungen und geben Sie je 2 Beispielverbindungen dafür an (Strukturformel). 1) Ionische Bindung:
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
3 Elektronenübergänge an Ort : d-d-übergänge
 3 Elektronenübergänge an Ort : d-d-übergänge 3.1 Übersicht, Lernziele Übersicht In diesem Kapitel steht ein weit verbreiteter Mechanismus der Lichtabsorption durch Übergangsmetallverbindungen im Zentrum.
3 Elektronenübergänge an Ort : d-d-übergänge 3.1 Übersicht, Lernziele Übersicht In diesem Kapitel steht ein weit verbreiteter Mechanismus der Lichtabsorption durch Übergangsmetallverbindungen im Zentrum.
Wiederholungsklausur zur Vorlesung "Allgemeine Chemie" am
 Wiederholungsklausur zur Vorlesung "Allgemeine Chemie" am 14.02.2007 Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte eintragen Wievieltes Fachsemester: Fachrichtung: Sonstiges (bitte angeben): Bitte
Wiederholungsklausur zur Vorlesung "Allgemeine Chemie" am 14.02.2007 Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte eintragen Wievieltes Fachsemester: Fachrichtung: Sonstiges (bitte angeben): Bitte
