6.2 Ligandenfeldtheorie
|
|
|
- Berndt Koenig
- vor 7 Jahren
- Abrufe
Transkript
1 6.2 Ligandenfeldtheorie Annahmen: Das isolierte Metallatom hat 5 entartete d-orbitale. Das Metallatom befindet sich in einer chemischen Umgebung aus elektrischen Punktladungen. Es existieren nur ionische oder elektrostatische Wechselwirkungen zwischen den äußersten d-orbitalen des Zentralions und den elektrischen Feldern der umgebenden Liganden.
2 Bildung eines Komplexes nach der Ligandenfeldtheorie kugelsymmetrisches Ligandenfeld freies Ion Liganden Elektrostatische Abstoßung zwischen den d-elektronen und den negativen Punktladungen e cfs Elektrostatische Anziehung zwischen Metallatom und den negativen Punktladungen Kristallfeldaufspaltung
3 Abstoßung im oktaedrischen Ligandenfeld x
4
5 Aufspaltung der d-orbitale im Oktaedrischen Kristallfeld ld kugelsymmetrisches Feld oktaedrisches Feld Der Energieabstand zwischen den t 2g und den e g*-orbitalen wird auch historisch bedingt als 10 Dq oder Δ bezeichnet(10dq~1-3ev~ cm -1 ).
6 Aufspaltung im oktaedrischen Ligandenfeld d-orbitale sind nicht mehr energetisch gleichwertig, Entartung ist aufgehoben Aufspaltung in zwei Gruppen von Orbitalen: e g - Obi Orbitale mit höherem Energieniveau i (d z 2, d x 2-y2) t 2g - Orbitale mit geringerem Energieniveau (d xy,d xz,d yz ) Energiedifferenz zwischen e g - und t 2g -Orbitalen btät10 beträgt Dq Erhöhung und Verringerung heben sich auf: Erhöhung und Verringerung heben sich auf: (+4 Elektronen 6Dq) - (6 Elektronen 4Dq) =0
7 Entstehung der Farbe des Komplexions [Ti(H 2 O) 6 ] 3+ [Ti(H 2 O) 6 ] 3+, oktaedrisch, paramagnetisch violett, λ = 500 nm [Ti(H 2 O) 6 ] 3+ [Ti(H 2 O) 6 ] 3+ * Δ O = h c/λ = J/Photon = 239 kj/mol Photonen
8 Wellenlängen des sichtbaren Spektrums Energie /10 3 cm cm -1 = 11,96 kj/mol Komplementärfarben (Absorption der entsprechenden Wellenlängen)
9 log ε Absorptionsspektrum der Lösung ν/cm -1
10 Elektronenanregungsspektrum eines Übergangsmetallkomplexes log ε d-elektronenbanden Charge-Transfer- und Ligandenbanden d ν [cm -1 ]
11 Ligandenfeldstabilisierungsenergie und Magnetismus von Komplexen Zentralion besitzt größtmögliche Anzahl ungepaarter d-elektronen high-spin-zustand Zentralion besitzt geringstmögliche Anzahl ungepaarter d-elektronen low-spin- Zustand
12 Ligandenfeldaufspaltungsenergie (10 Dq, Δ O ) und Magnetismus von Komplexen abhängig von der Differenz zwischen Ligandenfeldaufspaltungsenergie (10Dq, Δ O ) O und aufzuwendender Energie für die Spinpaarung Spinpaarungsenergie P 10Dq, Δ O > P low- Spin- Anordnung 10Dq, Δ O <P high-h Spin- Anordnung
13 Δ-Werte (in kj/mol) in oktaedrischen Komplexen (hs = high-spin, ls = low-spin)
14 d 1 [Ti(H 2 O) 6 ] 3+ Oktaedrisches Kristallfeld d 4 [Cr(H 2 O) 6 ] [V(H 2 O) 6 ] 3+ [Ni(H 2 O) 6 ] 2+ -4Dq -6Dq -12Dq d 8 [Mn(H 2 O) 6 ] 2+ [Cu(H 2 O) 6 ] 2+ d Dq d 5 d 0Dq 9-6Dq [Cr(H 2 O) 6 ] 3+ [CoF 6 ] 3+ [Zn(H 2 O) 6 ] d 3 d 6 d -12Dq -4Dq 10 0Dq [Co(H 2 O) 6 ] 2+ 3 d 7-8Dq
15 Bei d 1 -d 3 Komplexen ist nach der Hund schen Regel nur eine Elektronenkonfiguration k ti möglich, dies ändert sich z.b. bei d 6 -Ionen: FeSO 4 7H 2 O K 4 [Fe(CN) 6 ] Eisenvitriol gelbes Blutlaugensalz N 4- OH 2+ 2 C N N H 2 O OH 2 C C Fe Fe H 2 O H 2 O C C OH N 2 C N paramagnetisch diamagnetischi N
16 Der high-spin Komplex bildet sich unter Verlust an LFSE, dies geschieht nur, wenn die Oktaederfeldaufspaltungsenergie g (Δ O ) klein und damit der Verlust an LFSE klein ist. Ist die Oktaederauspaltung groß, bildet sich der Komplex mit gepaarten Spins. Der Energieverlust durch Verletzung der Hund schen Regel wird durch die größere LFSE ausgeglichen. Entscheidend ist die Frage nachdemenergiebetrag der für die Spinpaarung p (P) nötig ist relativ zur Oktaederfeldaufspaltungsenergie (Δ O ).
17 Beispiel d 4 und d 5 Ionen: d 4 (Cr 2+ ) d 5 (Mn 2+, Fe 3+ ) high-spin low-spin high-spin low-spin e g e g e g e g t 2g t 2g t 2g t 2g LFSE -6 Dq o LFSE -16 Dq + P LFSE 0 LFSE -20 Dq + 2P Δ O < P Δ O > P Δ O < P Δ O > P
18 Oktaedrisches Kristallfeld high-spin Konfiguration low-spin Konfiguration [Cr(CN) 6 ] Dq+P [Fe(CN) 6 ] Dq+2P [Co(CN) 6 ] Dq+2P [Co(NO 2 ) 6 ] Dq+P
19 Kristallfeldstabilisierungsenergie im oktaedrischen Kristallfeld ld KFSE = x(-4dq) + y(+6dq) + P P = Spinpaarungsenergie x = Anzahl Elektronen in t 2g y = Anzahl Elektronen in e g * d n KFSE high-spin KFSE low-spin ΔKFSE 1-4 Dq 2-8 Dq 3-12 Dq 4-6Dq Dq 7-8 Dq 8-12 Dq 9-6 Dq Dq + P -10 Dq + P -20 Dq + 2P -20 Dq + 2P -24 Dq + 2P -20 Dq + 2P -18 Dq + P -10 Dq + P
20 Kristallfeldauspaltung im oktaedrischen Kristallfeld 1. Konsequenzen High-spin Komplexe sind instabiler als low-spin Komplexe. Ionen mit d 3 -(Cr 3+ ) bzw. d 6 -low-spin-(co 3+ ) Konfiguration bilden besonders inerte Komplexe.
21 2. Größe der Kristallfeldaufspaltung 2.1. Art des Liganden Liganden erzeugen an identischen Metallzentren unterschiedlich starke Ligandenfelder und Aufspaltungen Δ O : Spektrochemische Reihe: Zunahme Δ I - < Br - < Cl - < F - < OH - < H < < 2- < - 2 O NH 3 NO CN < CO σ Donatoren schwache Liganden high-spin h i Komplexe σ Donatoren, π Akzeptoren starke Liganden low-spin Komplexe
22 Abhängigkeit gg der Oktaederaufspaltung von der Art der Liganden Elektronenspektren von drei Chrom(III)-komplexen: (a)[cr(en) 3 ] 3+ (b)[cr(ox) 3-3 ] (c)[crf 6 ] 3- ν 1 = Δ O CT = charge-transfer-bande
23 2.Größe der Kristallfeldaufspaltung 2.2. Ordnungszahl des Metallatoms (Stellung im Periodensystem) Mit steigender Ordnungszahl nimmt die Kernladung zu, wodurch die elektrostatische Feldstärke zunimmt. Der Wert von Δ O steigt innerhalb einer Gruppe von 3d über 4d zu den 5d Elementen. Allgemeiner Trend für 10 Dq: 3d ~+50% 4d ~+25% 5d [Co(NH 3+ 3 ) 6 ] [Rh(NH 3+ 3 ) 6 ] [Ir(NH 3+ 3 ) 6 ] cm cm cm -1
24 2.Größe der Kristallfeldaufspaltung 2.2. Oxidationsstufe des Metallatoms (Ionenladungsdichte) di Der Wert für Δ O steigt mit steigender Ionenladung an identischen Metallzentren für gleiche Liganden. [Co(H 2 O) 6 ] 2+ Δ O = 9200 cm -1 [Co(H 3+ 2 O) 6 ] Δ = -1 O cm Trend für 10 Dq: M 2+ <M 3+ <M 4+.. Metalle der 4d und 5d-Reihe und in hohen Oxidationsstufen Metalle der 4d und 5d Reihe und in hohen Oxidationsstufen bilden nur low-spin Komplexe.
25 2.Größe der Kristallfeldaufspaltung 2.3. Ligandenfeld Δ O > Δ T JAHN- TELLER- Effekt Aufhebung der durch freie Orbitalplätze hervorgerufenen Entartung durch Verzerrung mit Energiegewinn.
26 Tetragonale Verzerrung eines Oktaeders
27 Tetraedrisches Kristallfeld (1d-Elektron)
28 Aufspaltung der d-orbitale im Tetraedrischen Kristallfeld kugelsymmetrisches Feld tetraedrisches di Feld Fld Der Energieabstand zwischen den t 2 und den e-orbitalen Δ t ist nur 4/9 von Δ O, da nur vier anstelle von sechs Liganden vorhanden sind und diese auch nicht direkt in Richtung der d-orbitale ausgerichtet sind.
29 Tetraedrisches Kristallfeld
30 Kristallfeldstabilisierungsenergie im tetraedrischen und oktaedrischen Kristallfeld Berechnung mit Δ t =4/9Δ o Lagepräferenz
31 Kristallfeldauspaltung im tetraedrischen Kristallfeld Beträgt nur 4/9 von der im oktaedrischen Kristallfeld! Ausschließlich high-spin Komplexe Ionen mit einer Elektronenkonfiguration, aus der eine hohe KFSE resultiert, z.b. mit [Ar]d 3 -, [Ar]d 5 (lowspin) oder [Ar]d 6 (low-spin)-konfiguration bevor- zugen, wenn möglich, einen oktaedrischen Koordinationspolyeder Normale Spinelle Inverse Spinelle
32 Kristallfeldauspaltung im tetraedrischen Kristallfeld Tetraedrische Koordinationspolyeder werden beobachtet bei: Sterisch anspruchsvollen Liganden, wie z.b. Chloro-, Bromo- und Iodoliganden und Liganden mit Mehrfachbindungen zum Metallzentrum, wie z.b. Oxo- und Nitridoliganden
33 Kristallfeldauspaltung im tetraedrischen Kristallfeld Merke: Es gibt keine Elektronenkonfiguration, in der die elektronische Stabilisierung im Tetraeder größer ist als die im Oktaeder (Lagepräferenz) Oktaedergeometrie bevorzugt, Ausnahme: d 5 (high- spin) und d 10, da hier die KFSE im Oktaeder und Tetraeder null ist
34 Aufspaltung im quadratischen Komplex [PtCl 4 ] 2-
35 Die Kristallfeldtheorie Anwendungen und Konsequenzen
36 Ionenradien
37 für kugelsymmetrische Ionen Abnahme der Ionenradien innerhalb einer Periode mit steigender Kernladung nur die Ionen Ca 2+,Mn 2+ und Zn 2+ verhalten sich wie erwartet; der Ionenradius V 2+ ist kleiner als erwartet: V 2+ -Elektronenkonfiguration: (t 3 (e 0 2g ) g ) e g -Orbitale in Richtung der Liganden unbesetzt, Liganden rücken dichter an das Metall beim Übergang von V 2+ zu Mn 2+ [(t 2g ) 3 (e g ) 2 ]werdendie e g -Orbitale besetzt und die Liganden stärker abgestoßen; Mn 2+ pseudokugelsymmetrisch weitere Elektronen werden in die t 2g -Orbitale eingebaut (Fe 2+,Co 2+,Ni 2+ ); der Ionenradius nimmt erneut ab von Ni 2+ zu Zn 2+ werden erneut e g -Orbitale Obitl besetzt, t Zunahme des Ionenradius
38 Gitterenergien für die Difluoride der 3d-Metalle
39 Abweichungen von der berechneten Kurve ergeben sich durch den Beitrag der LFSE Beispiel: NiF 2 oktaedrisch koordiniert d 8 low spin LFSE = -12 Dq um diesen Beitrag ist die Gitterenergie negativer als der berechnete Wert Ca II d 0, highh spin / Mn II d 5 und Zn II d 10 LFSE = 0 Aus der zusätzlichen Gitterenergie lässt sich 10 Dq = Δ O bestimmen: 12 Dq = 165 kj 10Dq = 137kJ = cm -1 Wert deckt sich mit spektroskopisch ermittelten Wert für Ni II
40 Hydratationsenthalpien - Kurve analog zu der der Gitterenergien - Abweichungen ergeben sich durch den Beitrag an LFSE
41 Magnetische Eigenschaften Die Basiseinheit des magnetischen Momentes ist das Bohr sche Magneton und entspricht dem magnetischen Moment, das ein Elektron auf einer Kreisbahn mit dem Bohr schen Radius (53 pm) um ein Proton erzeugt. Für Elemente der 1. Übergangsmetallreihe mit n ungepaarten e - gilt näherungsweise: Spin only-wert Gesamtspin S = Σ s mit s = ½ d. h. S = n/2
42 Die berechneten spin-only Werte stimmen mit den experimentell ermittelten gut überein. Damit ist es möglich aus magnetischen Messungen für 3d Komplexe Damit ist es möglich, aus magnetischen Messungen für 3d-Komplexe direkt auf die Zahl der ungepaarten Elektronen zu schließen.
43 Spinzustände des Fe 2+ d x 2 -y 2 d z 2 d xy d xz, d yz () (a) (b) () (c) (d)
44 Spinzustände des Fe 2+ Im Falle eines starken Ligandenfeldes bildet sich der low-spin Komplex (a) Nimmt die Stärke des Ligandenfeldes ab, gelangt man über die Zustände (b) und (c) zum high-spin Komplex (d) mit S = 2. Ein S = 2 Zustand (tetragonal pyramidal) wird für das Fe 2+ Zentrum im Hämoglobin vor der Reaktion mit Triplett-Disauerstoff 3 O 2 gefunden.
45 Co II /Co III Redoxpotentiale in Abhängigkeit von der Ligandenart Das [Co(H 2 O) 6 ] 2+ high-spin d 7 IonistinWasserstabil und nur schwer zum Co III zu oxidieren. Die Oxidation wird wesentlich erleichtert, wenn NH 3 oder CN - Liganden vorhanden sind: LFSE wird größer Spinpaarung wird ermöglicht (t 6 2g ) Zustand wird stabilisiert
46
47 Struktur der Spinelle Verbindungen der Zusammensetzung M II M III 2O 4 DieO 2- Ionen bilden eine kubisch-dichteste Kugelpackung. Diese Formeleinheit enthält vier Oktaeder- und acht Tetraederlücken. Die zweiwertigen Ionen besetzen 1/8 aller Tetraederlücken und die dreiwertigen 1/2 aller Oktaederlücken. Z.B. MgAl 2 O 4 : 1/8 aller Tetraederlücken sind mit Mg-Atomen (M II ), 1/2 aller Oktaederlücken mit Al-AtomenAtomen (M III ) derart besetzt, dass jedes O-Atom verzerrt tetraedrisch von einem Mg- und drei Al-AtomenAtomen umgeben ist.
48 Oktaedrische und tetraedrische Lücken
49 Struktur der Spinelle Verbindungen der Zusammensetzung M II M III 2O 4 Bei inversen Spinellen besetzen die M II die Oktaederlücken und die M III die Tetraederlücken. z.b. NiAl 2 O 4 Triebkraft dafür ist der Unterschied in der LFSE für Ni II auf Oktaeder- und Tetraederplätzen im Vergleich zu Fe II. Auch wenn die LFSE nur ca. 15 % zur gesamten Bindungsenergie des Systems beiträgt, kann sie aber ausschlaggebend für den Aufbau sein. Ni II high-spin ist auf einem Oktaederplatz 86 kj/mol stabiler als auf einem Tetraederplatz; Fe II nur 14,8 kj/mol, das reicht nicht zur Bildung eines inversen Spinells.
50 Die Lagepräferenz bestimmt die Verteilung der Übergangsmetallkationen in Spinellen: Mn - II tetr. III okt. 3 O 4 Normaler Spinell [Mn ] [Mn ] 2O 4 Mn 2+ d 5 high-spin Mn 3+ d 4 high-spin Keine Lagepräferenz Lagepräferenz = Dq bevorzugt Oktaederplatz [B III ] okt. Fe 3 O 4 -InverserSpinell[Fe III ] tetr. [Fe II ] okt. [Fe III ] okt. O 4, d.h. alle Fe 2+ -Ionen besetzen Oktaederplätze und verdrängen dä die Hälfte der Fe 3+ -Ionen auf die Tetraederplätze Fe 2+ d 6 high-spin Lagepräferenz = Dq bevorzugt Oktaederplatz [B III ] okt. Fe 3+ d 5 high-spin Keine Lagepräferenz
51 Normale Spinell-Struktur : [M II ] tetr. [M III ] okt. 2O 4 Beispiele: MgAl 2 O 4, Mn 3 O 4, FeAl 2 O 4, Co 3 O 4 Inverse Spinell-Struktur: [M III ] tetr. [M II ] okt. [M III ] okt. O 4 Beispiele: i NiAl 2 O 4, CoFe 2 O 4, Fe 3 O 4, NiFe 2 O 4
52 Optische Eigenschaften Elektronische Übergänge zwischen d-orbitalen (d-d-übergänge) führen oft zu Absorptionsbanden im sichtbaren Spektralbereich. Beispiel: oktaedrische Ti 3+ -Komplexe
53 KFSE (10Dq): I - < Br - < S 2- < SCN - < Cl - < NO 3- < F - < OH - < H 2 O < NH 3 < CN - < CO Schwaches Feld Starkes Feld Spektrochemische Reihe: Ordnet Liganden nach der relativen Größe der resultierenden Kristallfeldaufspaltung Reihenfolge wird nicht durch die Kristallfeldtheorie (Punktladungen) erklärt
54 Beispiel: oktaedrische Cu 2+ -Komplexe (d 9 ) Ähnlich übersichtliche Verhältnisse, also eine Absorptionsbande, findet man noch hbei oktaedrischen di Komplexen mit d 4 high-spin h i bzw. d 6 high-spin Konfiguration am Metallzentrum. Bei den Elektronenkonfigurationen d 2 - d 8 ist die Situation durch Wechselwirkung zwischen den Elektronen merklich komplizierter.
55 Nachteil der Kristallfeldtheorie: Das rein elektrostatische Punktladungsmodell kann eine Reihe spektroskopischer Befunde nicht erklären EPR-Spektren, Reihenfolge der Liganden in der spektrochemischen Reihe Berücksichtigung der Kovalenz der Metall-Ligand- Bindung erforderlich
56 Effekte der Kovalenz: Delokalisierung der Elektronendichte aus den Metall d-orbitalen hin zu den Liganden (nephelauxetischer Effekt) Reduktion der interelektronischen Abstoßung am Metallzentrum Erhöhung der Elektronendichte auf den Liganden mit evtl. Schwächung von Intraligandbindungen (Rückbindungseffekte) Änderung elektronischer, magnetischer, de u g ee to sc e, ag et sc e, spektroskopischer Eigenschaften
57 Rückbindung zu den Liganden Typisch z.b. bei Metallcarbonylen und -nitrosylen Metall hat formal niedrige Oxidationsstufe bzw. hohe Elektronendichte, die durch Rückfluss von Ladung auf die Liganden reduziert wird Beispiel: M(CO) 6 Metallcarbonyle σ-donor-bindung π-akzeptorbindung d
58 Erklärung der Reihenfolge der Liganden in der spektrochemischen h Reihe I - <Br - <S - <SCN - <Cl - <NO - <F - <OH - <HO<NH <CN < 3 <CO Schwache Liganden keine π-rückbindung Starke Liganden π-rückbindung Die spektrochemische h Rih Reihe korreliert nicht ih mit der Ld Ladung der Liganden, sondern mit der Fähigkeit der Liganden Elektronendichte vom Metallatom zu delokalisieren und damit die positive Ladungsdichte bzw. Feldstärke am Metallatom zu erhöhen. π-akzeptorliganden: Stabilisieren Metalle in niedrigen Oxidationsstufen CO (Rückbindungen) π-donorliganden: Stabilisieren Metalle in hohen Oxidationsstufen O 2-, N 3- (Metall-Ligand-Mehrfachbindungen)
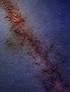
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+
![Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ Elektronenspektrum von [Ti(H 2 O) 6 ] 3+](/thumbs/66/55543366.jpg) Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel )
 EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
Die Bindung in Übergangsmetallkomplexenn. Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth
 Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment
 1 Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment Zusatzaufgaben zu Versuch 316 : 1. Berechnen Sie das magnetische Moment des Co + - Ions.. Welche Niveaus der Valenzelektronen sind beim Co +
1 Hinweise zur Zusatzaufgabe Permanentes magnetisches Moment Zusatzaufgaben zu Versuch 316 : 1. Berechnen Sie das magnetische Moment des Co + - Ions.. Welche Niveaus der Valenzelektronen sind beim Co +
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen
 Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 07. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 07. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Übungsaufgaben zur Koordinationschemie
 Übungsaufgaben zur Koordinationschemie 1. Wie entstehen Komplexe und wie sind sie zusammengesetzt? Warum bilden die Nebengruppenelemente besonders stabile Koordinationsverbindungen? 2. Formulieren Sie
Übungsaufgaben zur Koordinationschemie 1. Wie entstehen Komplexe und wie sind sie zusammengesetzt? Warum bilden die Nebengruppenelemente besonders stabile Koordinationsverbindungen? 2. Formulieren Sie
A. Mezzetti Fragenkatalog X
 Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 29. Januar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 29. Januar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 24. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Anorganische Chemie II B. Sc. Chemieingenieurwesen 24. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Ligandenfeldtheorie Magnetismus von Komplexen
 Arbeitsblätter zum Ausdrucken von sofatutor.com Ligandenfeldtheorie Magnetismus von Komplexen Schildere die Unterschiede zwischen highspin- und lowspin-komplexen. 2 Gib die Orbitale an, die im oktaedrischen
Arbeitsblätter zum Ausdrucken von sofatutor.com Ligandenfeldtheorie Magnetismus von Komplexen Schildere die Unterschiede zwischen highspin- und lowspin-komplexen. 2 Gib die Orbitale an, die im oktaedrischen
Mößbauer-Spektroskopie
 Mößbauer-Spektroskopie Westfälische Wilhelms-Universität Münster Ansgar Stüken & Thomas Dröge 12.05.2005 Überblick Elektrische Monopolwechselwirkung (Isomerieverschiebung) Elektrische Quadrupolwechselwirkung
Mößbauer-Spektroskopie Westfälische Wilhelms-Universität Münster Ansgar Stüken & Thomas Dröge 12.05.2005 Überblick Elektrische Monopolwechselwirkung (Isomerieverschiebung) Elektrische Quadrupolwechselwirkung
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 04. Februar 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 04. Februar 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 13. Juli 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 13. Juli 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O
![Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O Matthias Hinrichs Praktikum Anorganische Chemie II. Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O](/thumbs/78/78095730.jpg) Matthias Hinrichs 22.11.1999 Praktikum Anorganische Chemie II Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O 1. Theorie: Die rklärung zur Art und Struktur von Komplexen, werden am besten durch die Kristallfeldtheorie
Matthias Hinrichs 22.11.1999 Praktikum Anorganische Chemie II Übergangsmetallkomplexe: [Co(en) 3 ]Br 3 *3H 2 O 1. Theorie: Die rklärung zur Art und Struktur von Komplexen, werden am besten durch die Kristallfeldtheorie
1.) Geben Sie die Formeln oder Bestandteile folgender Substanzen an (6 Punkte): b) Zinnober ZnS e) Bronze Cu/Sn-Legierung
 Klausur zur Vorlesung Anorganische Chemie II am 8. Juli 003 Name: Vorname: Matrikelnummer: (11 Aufgaben; Erreichbare Gesamtpunktzahl: 90; Zum Bestehen notwendig sind 45 Punkte (50%); Schreiben Sie auf
Klausur zur Vorlesung Anorganische Chemie II am 8. Juli 003 Name: Vorname: Matrikelnummer: (11 Aufgaben; Erreichbare Gesamtpunktzahl: 90; Zum Bestehen notwendig sind 45 Punkte (50%); Schreiben Sie auf
F2 Magnetische Waage
 F Magnetische Waage 1. Aufgabenstellung: Für anorganische Komplexverbindungen soll aus der Messung der magnetischen Suszeptibilität die Zahl der ungepaarten Elektronen und aus der Messung der UV- Spektren
F Magnetische Waage 1. Aufgabenstellung: Für anorganische Komplexverbindungen soll aus der Messung der magnetischen Suszeptibilität die Zahl der ungepaarten Elektronen und aus der Messung der UV- Spektren
Beispielaufgaben IChO 2. Runde 2019 Koordinationschemie
 Beispiel 1 Metalle und Elektronen Bei der Besetzung von Atomorbitalen werden die Elektronen ausgehend vom energetisch am tiefsten liegenden Atomorbital in Richtung ansteigender Energie mit den Elektronen
Beispiel 1 Metalle und Elektronen Bei der Besetzung von Atomorbitalen werden die Elektronen ausgehend vom energetisch am tiefsten liegenden Atomorbital in Richtung ansteigender Energie mit den Elektronen
Anorganische Chemie II Veröffentlichung vom 26. Juni Valende Bond Theorie Grundlagen Mängel des Modells...
 Anorganische Chemie II Veröffentlichung vom 26. Juni 2005 Inhaltsverzeichnis 1 Valende Bond Theorie 2 1.1 Grundlagen............................................. 2 1.2 Mängel des Modells.........................................
Anorganische Chemie II Veröffentlichung vom 26. Juni 2005 Inhaltsverzeichnis 1 Valende Bond Theorie 2 1.1 Grundlagen............................................. 2 1.2 Mängel des Modells.........................................
Spezielle Chemie Vorlesungsteil Koordinationschemie (Stand SS 2014) Institut für Organische Chemie Leibniz Universität Hannover
 Spezielle Chemie Vorlesungsteil Koordinationschemie (Stand SS 2014) Institut für Organische Chemie Leibniz Universität Hannover verantwortlich: Prof. Dr. A. Kirschning 1 Co Vitamin B12 Chemische Bindungstypen
Spezielle Chemie Vorlesungsteil Koordinationschemie (Stand SS 2014) Institut für Organische Chemie Leibniz Universität Hannover verantwortlich: Prof. Dr. A. Kirschning 1 Co Vitamin B12 Chemische Bindungstypen
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 27. September 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Anorganische Chemie II B. Sc. Chemieingenieurwesen 27. September 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen?
 Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen? Michael Kalcher 7AM In h a l t Eisen - Eigenschaften 2 Wertigkeit und Oxidationszahl 2 Üb e r g a n g s m e ta l l e 3
Wie erklärt man die Wertigkeiten (+2/+3) natürlich vorkommender Eisenverbindungen? Michael Kalcher 7AM In h a l t Eisen - Eigenschaften 2 Wertigkeit und Oxidationszahl 2 Üb e r g a n g s m e ta l l e 3
Zusatzinformation zum Anorganisch Chemischen Grundpraktikum. 3. Teil: Komplexe
 Zusatzinformation zum Anorganisch Chemischen Grundpraktikum 3. Teil: Komplexe Dr. A. Hepp (29.06.2011) Nomenklatur von Komplexverbindungen Allgemeines: Im Mittelpunkt einer Komplexverbindung steht das
Zusatzinformation zum Anorganisch Chemischen Grundpraktikum 3. Teil: Komplexe Dr. A. Hepp (29.06.2011) Nomenklatur von Komplexverbindungen Allgemeines: Im Mittelpunkt einer Komplexverbindung steht das
AC II Praktikum SoSe 04
 AC II Praktikum SoSe 04 Julia Blechinger Saal K Assistent: Constanze Vogler Durchführung: 05.05.04 Protokoll zur Präparategruppe 8: Übergangsmetallkomplexe Darstellung von [Co(NH 3 ) 5 Br]Br 2 I. Theoretischer
AC II Praktikum SoSe 04 Julia Blechinger Saal K Assistent: Constanze Vogler Durchführung: 05.05.04 Protokoll zur Präparategruppe 8: Übergangsmetallkomplexe Darstellung von [Co(NH 3 ) 5 Br]Br 2 I. Theoretischer
Komplexchemie des Nickels Ligandenaustauschreaktionen
 Komplexchemie des Nickels Ligandenaustauschreaktionen Jorge Ferreiro, 1. Semester, D-CHAB, fjorge@student.ethz.ch Assistent: Kyrill Stanek Abstract: In diesem Versuch ging es darum, verschiedene Ligandenaustauschreaktionen
Komplexchemie des Nickels Ligandenaustauschreaktionen Jorge Ferreiro, 1. Semester, D-CHAB, fjorge@student.ethz.ch Assistent: Kyrill Stanek Abstract: In diesem Versuch ging es darum, verschiedene Ligandenaustauschreaktionen
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 18. Juli 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 18. Juli 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol]
![Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol] Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol]](/thumbs/49/25486820.jpg) Seite 22 22 Auflösung von Si in NaOH-Lösung Weiterführende Infos Quarzsand und Alkalicarbonate werden bei ca. 1300 C zusammengeschmolzen und das Produkt ((Na/K) 2 O* n SiO 2 ) bei 150 C und 5 bar in Wasser
Seite 22 22 Auflösung von Si in NaOH-Lösung Weiterführende Infos Quarzsand und Alkalicarbonate werden bei ca. 1300 C zusammengeschmolzen und das Produkt ((Na/K) 2 O* n SiO 2 ) bei 150 C und 5 bar in Wasser
Anorganische Chemie für Biologen. Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/
 Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Inhalte Stöchiometrie chemisches Rechnen Chemisches Gleichgewicht
Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Inhalte Stöchiometrie chemisches Rechnen Chemisches Gleichgewicht
Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO 2-4 PO 3-4 +H + -H+ +H + Stefan Wuttke # 1
 Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO - 4 HPO 2-4 PO 3-4 +H + -H+ +H + -H+ +H + Stefan Wuttke # 1 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner + AgNO 3 AgCl +
Mehrprotonige Säuren -H + H 3 PO 4 H 2 PO - 4 HPO 2-4 PO 3-4 +H + -H+ +H + -H+ +H + Stefan Wuttke # 1 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner + AgNO 3 AgCl +
Koordinations- und Übergangsmetallchemie
 Koordinations- und Übergangsmetallchemie Gliederung 1. Einteilung der Elemente 2. Die d-orbitale 3. Die koordinative Bindung 4. Komplexverbindungen 5. Nomenklatur der Koordinationsverbindungen 6. Liganden
Koordinations- und Übergangsmetallchemie Gliederung 1. Einteilung der Elemente 2. Die d-orbitale 3. Die koordinative Bindung 4. Komplexverbindungen 5. Nomenklatur der Koordinationsverbindungen 6. Liganden
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Komplexchemie CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Punkte. Bitte eintragen: Matrikelnummer: Bitte ankreuzen: Biotechnologie Pharmazie
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Punkte Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage 1 Skizzieren Sie die
UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische Chemie Prof. Dr. B. Dick
 UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische Chemie Prof. Dr. B. Dick PHYSIKALISCH-CHEMISCHES PRAKTIKUM II Spektroskopisches Verhalten von Chrom(III)-Komplexen (II) 1 1 Experimentelle
UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische Chemie Prof. Dr. B. Dick PHYSIKALISCH-CHEMISCHES PRAKTIKUM II Spektroskopisches Verhalten von Chrom(III)-Komplexen (II) 1 1 Experimentelle
Anorganische Chemie I/II
 Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 11. Februar 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 11. Februar 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Frage 1. Klausuraufgaben Grundvorlesung Testat vom , Seite 1 Musterlösung. Bitte eintragen: Matrikelnummer: 0815 Name: Musterstudi.
 Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Klausuraufgaben Grundvorlesung Testat vom 8.1.02, Seite 1 Musterlösung Matrikelnummer: 0815 Name: Musterstudi Bitte eintragen: Vorname: Bitte ankreuzen: Fachrichtung: Chemie Biotechnologie Pharmazie Frage
Anorganische Chemie I/II
 Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 20. September 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 20. September 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
4. Komplexe 4.7. Komplexe in wässriger Lösung Stufenweise Komplexbildung
 4. Komplexe 4.7. Komplexe in wässriger Lösung 4.7.. Stufenweise Komplexbildung 17 Der schrittweise Austauschprozess der Wassermoleküle in einem Aquakomplex [M z+ (aq)] mit einem neutralen (oder geladenen)
4. Komplexe 4.7. Komplexe in wässriger Lösung 4.7.. Stufenweise Komplexbildung 17 Der schrittweise Austauschprozess der Wassermoleküle in einem Aquakomplex [M z+ (aq)] mit einem neutralen (oder geladenen)
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Komplexchemie und Molekülgeometrie. Aufbau und Nomenklatur von Komplexverbindungen
 Aufbau und Nomenklatur von Komplexverbindungen Komplexverbindungen sind chemische Verbindungen, die aus einem Zentralatom und Molekülen bzw. Ionen gebildet werden. Aufbau von Komplexverbindungen Zentralatom
Aufbau und Nomenklatur von Komplexverbindungen Komplexverbindungen sind chemische Verbindungen, die aus einem Zentralatom und Molekülen bzw. Ionen gebildet werden. Aufbau von Komplexverbindungen Zentralatom
Workshop: Kristallstrukturen
 Workshop: Kristallstrukturen Literatur: Anorganische Strukturchemie, Ullrich Müller, Teubner-Verlag Borchardt-Ott: Kristallographie, Springer-Verlag Smart/Moore: Einführung in die Festkörperchemie, Vieweg
Workshop: Kristallstrukturen Literatur: Anorganische Strukturchemie, Ullrich Müller, Teubner-Verlag Borchardt-Ott: Kristallographie, Springer-Verlag Smart/Moore: Einführung in die Festkörperchemie, Vieweg
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 16. Juli 2015 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 16. Juli 2015 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie 1 Version 1.5b Thema:
 Lösliche Gruppe: NH 4 +, Na +, Mg 2+, K + (Quelle: Qualitative Anorganische Analyse, Eberhard Gerdes) Anorganische Chemie 1 Version 1.5b Thema: 1. Säurestärke Allgemein gesprochen existieren Neutralsäuren,
Lösliche Gruppe: NH 4 +, Na +, Mg 2+, K + (Quelle: Qualitative Anorganische Analyse, Eberhard Gerdes) Anorganische Chemie 1 Version 1.5b Thema: 1. Säurestärke Allgemein gesprochen existieren Neutralsäuren,
IV Atomlehre und Periodensystem (Mortimer: Kap. 2 u. 6; Atkins: Kap. 7)
 IV Atomlehre und Periodensystem (Mortimer: Kap. u. 6; Atkins: Kap. 7) 13. Aufbau der Atome Stichwörter: Elementarteilchen und ihr Nachweis, Atom, Atomkern, Proton, Neutron, Kanalstrahlen, Kathodenstrahlen,
IV Atomlehre und Periodensystem (Mortimer: Kap. u. 6; Atkins: Kap. 7) 13. Aufbau der Atome Stichwörter: Elementarteilchen und ihr Nachweis, Atom, Atomkern, Proton, Neutron, Kanalstrahlen, Kathodenstrahlen,
Koordinations- und Übergangsmetallchemie
 Koordinations- und Übergangsmetallchemie Gliederung 1. Einteilung der Elemente 2. Die d-orbitale 3. Die koordinative Bindung 4. Komplexverbindungen 5. Nomenklatur der Koordinationsverbindungen 6. Liganden
Koordinations- und Übergangsmetallchemie Gliederung 1. Einteilung der Elemente 2. Die d-orbitale 3. Die koordinative Bindung 4. Komplexverbindungen 5. Nomenklatur der Koordinationsverbindungen 6. Liganden
Wiederholung der letzten Vorlesungsstunde: Thema: PSE
 Wiederholung der letzten Vorlesungsstunde: Thema: PSE Das Periodensystem der Elemente, historische Entwicklung, Gruppen, Perioden, Hauptgruppen, Nebengruppen, Lanthanide, Actinide, besondere Stabilität
Wiederholung der letzten Vorlesungsstunde: Thema: PSE Das Periodensystem der Elemente, historische Entwicklung, Gruppen, Perioden, Hauptgruppen, Nebengruppen, Lanthanide, Actinide, besondere Stabilität
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 5: )
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
5. Komplexbildungsgleichgewichte, Chelateffekt und Stabilität von Metallkomplexen
 5. Komplexbildungsgleichgewichte, Chelateffekt und Stabilität von Metallkomplexen 5.1 Komplexbildungsgleichgewichte Die Bildung und der Zerfall von Komplexverbindungen sind Gleichgewichtsreaktionen, auf
5. Komplexbildungsgleichgewichte, Chelateffekt und Stabilität von Metallkomplexen 5.1 Komplexbildungsgleichgewichte Die Bildung und der Zerfall von Komplexverbindungen sind Gleichgewichtsreaktionen, auf
Quantenzahlen. Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale.
 Quantenzahlen Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale. l = 0, 1, 2, 3, (Orbital-)Symbol s, p, d, f, Zahl der Orbitale
Quantenzahlen Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale. l = 0, 1, 2, 3, (Orbital-)Symbol s, p, d, f, Zahl der Orbitale
Anorganische Chemie II
 Anorganische Chemie II B. Sc. Chemieingenieurwesen 31. Januar 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Anorganische Chemie II B. Sc. Chemieingenieurwesen 31. Januar 2017 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Komplexbildung. CoCl 3 5 NH 3. CoCl 3 6 NH 3. CoCl 3 4 NH 3 Alfred Werner The Nobel Prize in Chemistry 1913
 Komplexbildung CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner 1866-1919 The Nobel Prize in Chemistry 1913 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH
Komplexbildung CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner 1866-1919 The Nobel Prize in Chemistry 1913 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH
MO-Theorie: Molekülorbitale, Bindungsordnung, Molekülorbitaldiagramme von F 2, O 2, N 2, H 2 O, Benzol, Wasserstoffbrückenbindungen
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen VI Molkülorbitaltheorie II MO-Theorie: Molekülorbitale, Bindungsordnung, Molekülorbitaldiagramme von F 2, O 2, N 2, H 2 O, Benzol,
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen VI Molkülorbitaltheorie II MO-Theorie: Molekülorbitale, Bindungsordnung, Molekülorbitaldiagramme von F 2, O 2, N 2, H 2 O, Benzol,
Kristallchemie. Atome Ionen Moleküle Chemische Bindungen
 Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Zirkon Kristallchemie Atome Ionen Moleküle Chemische Bindungen Bohr sches Atommodell Kernteilchen: p: Proton n: Neutron Elektronenhülle: e - Elektron Nukleus: Massenzahl A = p + n, Ordnungszahl Z = p =
Aquakomplexe. +4NH 3 [ Cu(H 2 O) 6 ] 2+ -2H 2 O [ Cu(NH 3 ) 4 (H 2 O) 2 ] 2+ Cu H 3 N
![Aquakomplexe. +4NH 3 [ Cu(H 2 O) 6 ] 2+ -2H 2 O [ Cu(NH 3 ) 4 (H 2 O) 2 ] 2+ Cu H 3 N Aquakomplexe. +4NH 3 [ Cu(H 2 O) 6 ] 2+ -2H 2 O [ Cu(NH 3 ) 4 (H 2 O) 2 ] 2+ Cu H 3 N](/thumbs/69/60049254.jpg) (352) 28 Kmplexverbindungen 281 Definitinen Kmplexverbindungen = Verbindungen höherer Ordnung cmplexus (lat) = umschlungen, zusammengefasst Verbindungen erster Ordnung entstehen aus Atmen im Bestreben
(352) 28 Kmplexverbindungen 281 Definitinen Kmplexverbindungen = Verbindungen höherer Ordnung cmplexus (lat) = umschlungen, zusammengefasst Verbindungen erster Ordnung entstehen aus Atmen im Bestreben
Leibniz-Institut für Katalyse e. V. an der Universität Rostock, Außenstelle Berlin
 Leibniz-Institut für Katalyse e. V. an der Universität Rostock, Außenstelle Berlin Angelika Brückner UV-vis und EPR-Spektroskopie: Grundlagen und Anwendungen in der Heterogenen Katalyse Inhalt Gesetzmäßigkeiten
Leibniz-Institut für Katalyse e. V. an der Universität Rostock, Außenstelle Berlin Angelika Brückner UV-vis und EPR-Spektroskopie: Grundlagen und Anwendungen in der Heterogenen Katalyse Inhalt Gesetzmäßigkeiten
Farbe der anorganischen Pigmente
 Farbe der anorganischen Pigmente 1. Farbigkeit der Komplex-Ionen (Ligandenfeld-Theorie) Einführung Versuch 1 Geben Sie einen halben Löffel festes Kupfersulfat in ein grosses Reagenzglas (RG) und erwärmen
Farbe der anorganischen Pigmente 1. Farbigkeit der Komplex-Ionen (Ligandenfeld-Theorie) Einführung Versuch 1 Geben Sie einen halben Löffel festes Kupfersulfat in ein grosses Reagenzglas (RG) und erwärmen
4. Isomerie von Komplexverbindungen
 4. Isomerie von Komplexverbindungen 4. Isomerie bei Koordinationsverbindungen Grundsätzlich unterscheidet man Konstitutionsisomerie Strukturisomerie) und Stereoisomerie (Konfigutationsisomerie). Konstitutionsisomerie:
4. Isomerie von Komplexverbindungen 4. Isomerie bei Koordinationsverbindungen Grundsätzlich unterscheidet man Konstitutionsisomerie Strukturisomerie) und Stereoisomerie (Konfigutationsisomerie). Konstitutionsisomerie:
Klassifizierung repräsentativer Elementhydride I II III IV V VI VII. LiH BeH 2 BH 3, CH 4 NH 3 H 2 O HF. NaH MgH 2 AlH 3 SiH 4 PH 3 H 2 S HCl
 Klassifizierung repräsentativer Elementhydride I II III IV V VI VII Li Be 2 B 3, C 4 N 3 2 F B n m Na Mg 2 Al 3 Si 4 P 3 2 S Cl K Ca 2 Ga 3 Ge 4 As 3 2 Se Br Rb Sr 2 In 3 Sn 4 Sb 3 2 Te I Ionisch Polymer
Klassifizierung repräsentativer Elementhydride I II III IV V VI VII Li Be 2 B 3, C 4 N 3 2 F B n m Na Mg 2 Al 3 Si 4 P 3 2 S Cl K Ca 2 Ga 3 Ge 4 As 3 2 Se Br Rb Sr 2 In 3 Sn 4 Sb 3 2 Te I Ionisch Polymer
Elektronenspinresonanz-Spektroskopie
 Elektronenspinresonanz-Spektroskopie (ESR-Spektroskopie) engl.: Electron Paramagnetic Resonance Spectroscopy (EPR-Spectroscopy) Stephanie Dirksmeyer, 671197 Inhalt 1. Grundidee 2. physikalische Grundlagen
Elektronenspinresonanz-Spektroskopie (ESR-Spektroskopie) engl.: Electron Paramagnetic Resonance Spectroscopy (EPR-Spectroscopy) Stephanie Dirksmeyer, 671197 Inhalt 1. Grundidee 2. physikalische Grundlagen
Thema: Chemische Bindungen Wasserstoffbrückenbindungen
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen Wasserstoffbrückenbindungen Wasserstoffbrückenbindungen, polare H-X-Bindungen, Wasser, Eigenschaften des Wassers, andere Vbg. mit H-Brücken
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen Wasserstoffbrückenbindungen Wasserstoffbrückenbindungen, polare H-X-Bindungen, Wasser, Eigenschaften des Wassers, andere Vbg. mit H-Brücken
Anorganische Chemie I/II
 Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 16. März 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und
Anorganische Chemie I/II MODULPRÜFUNG B. Sc./Dipl.-Ing. Chemieingenieurwesen 16. März 2005 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und
Wie kommen Metalle vor? CaO, MgO, Al 2 O 3, CaCO 3, CaSO 4 vs. Cu 2 S, HgS, PbS. Welche Kombinationen führen zu hohen Oxidationsstufen?
 HSAB-Prinzip Wie kommen Metalle vor? CaO, MgO, Al 2 O 3, CaCO 3, CaSO 4 vs. Cu 2 S, HgS, PbS Welche Kombinationen führen zu hohen Oxidationsstufen? XeO 6 4, ClO 4, MnO 4, MnS 4, ClS 4 Warum entsteht der
HSAB-Prinzip Wie kommen Metalle vor? CaO, MgO, Al 2 O 3, CaCO 3, CaSO 4 vs. Cu 2 S, HgS, PbS Welche Kombinationen führen zu hohen Oxidationsstufen? XeO 6 4, ClO 4, MnO 4, MnS 4, ClS 4 Warum entsteht der
b) Darstellung am Beispiel oktaedrischer Koordination: Komplexe
 Hinweis Bei dieser Datei handelt es sich um ein Protokoll, das einen Vortrag im Rahmen des Chemielehramtsstudiums an der Uni Marburg referiert. Zur besseren Durchsuchbarkeit wurde zudem eine Texterkennung
Hinweis Bei dieser Datei handelt es sich um ein Protokoll, das einen Vortrag im Rahmen des Chemielehramtsstudiums an der Uni Marburg referiert. Zur besseren Durchsuchbarkeit wurde zudem eine Texterkennung
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
6. Die Chemische Bindung
 6. Die Chemische Bindung Hauptbindungsarten Kovalente Bindung I Kovalente Bindung II Ionenbindung Metallische Bindung Nebenbindungsarten Van der Waals Wechselwirkung Wasserstoffbrückenbindung Salzartige
6. Die Chemische Bindung Hauptbindungsarten Kovalente Bindung I Kovalente Bindung II Ionenbindung Metallische Bindung Nebenbindungsarten Van der Waals Wechselwirkung Wasserstoffbrückenbindung Salzartige
Kapitel 8 MO-Verbindungen der Übergangsmetalle - Bindungsverhältnisse und Strukturen
 Kapitel 8 MO-Verbindungen der Übergangsmetalle - Bindungsverhältnisse und Strukturen 8.1 Vergleich Hauptgruppen-Nebengruppen Hauptgruppen (p-block) Bindigkeit: entsprechend der 8-n-Regel (Ausnahme: hypervalente
Kapitel 8 MO-Verbindungen der Übergangsmetalle - Bindungsverhältnisse und Strukturen 8.1 Vergleich Hauptgruppen-Nebengruppen Hauptgruppen (p-block) Bindigkeit: entsprechend der 8-n-Regel (Ausnahme: hypervalente
Probeklausur zur anorganischen Chemie II
 Probeklausur zur anorganischen Chemie II Prof. Dr. K. Heinze Johannes Gutenberg-Universität Mainz Institut für Anorganische und Analytische Chemie xx. xxxx xxx xx - xx Uhr, C01 Beantworten Sie die Fragen
Probeklausur zur anorganischen Chemie II Prof. Dr. K. Heinze Johannes Gutenberg-Universität Mainz Institut für Anorganische und Analytische Chemie xx. xxxx xxx xx - xx Uhr, C01 Beantworten Sie die Fragen
Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s 2 3p 6. Geben Sie isoelektronische Ionen zu den folgenden Atomen an
 Übung 05.11.13 Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 Ne / F - / O 2- / N 3- / Na + / Mg 2+ / Al 3+. Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s
Übung 05.11.13 Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 Ne / F - / O 2- / N 3- / Na + / Mg 2+ / Al 3+. Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Stern-Gerlach-Versuch, Orbitalmodell, Heisenberg sche Unschärferelation, Schrödinger Gleichung, Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen
Wiederholung der letzten Vorlesungsstunde: Stern-Gerlach-Versuch, Orbitalmodell, Heisenberg sche Unschärferelation, Schrödinger Gleichung, Zustände der Elektronen sind Orbitale, die durch 4 Quantenzahlen
Das Versagen der klassischen Physik Die Entwicklung der Quantenphysik. Quantenmechanische Lösung
 Das Versagen der klassischen Physik Die Entwicklung der Quantenphysik Problem Thermisches Strahlungsspektrum Photoelektrischer Effekt, Compton Effekt Quantenmechanische Lösung Planck sche Strahlungsformel:
Das Versagen der klassischen Physik Die Entwicklung der Quantenphysik Problem Thermisches Strahlungsspektrum Photoelektrischer Effekt, Compton Effekt Quantenmechanische Lösung Planck sche Strahlungsformel:
Valenz-Bindungstheorie H 2 : s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie
 Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
Die 18 Valenzelektronen-Regel
 Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Anorganische Chemie I A. Mezzetti Musterlösung VI
 Anorganische Chemie I O-LCAO A. ezzetti usterlösung VI π-bindungen in quadratisch-planaren Kompleen (a) Schreiben Sie die reduzible Darstellung Γπ für die π-ligandengruppenorbitale auf und bestimmen Sie
Anorganische Chemie I O-LCAO A. ezzetti usterlösung VI π-bindungen in quadratisch-planaren Kompleen (a) Schreiben Sie die reduzible Darstellung Γπ für die π-ligandengruppenorbitale auf und bestimmen Sie
Chemische Bindung. Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung
 Chemische Bindung Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung 1 Was sind Ionen? Ein Ion besteht aus einem oder mehreren Atomen und hat elektrische Ladung Kationen
Chemische Bindung Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung 1 Was sind Ionen? Ein Ion besteht aus einem oder mehreren Atomen und hat elektrische Ladung Kationen
Aufgabe Punkte (je 10) Anorganisches Grund-Praktikum (Lehramt/2-Fach Bachelor) Abschlußklausur (Nachklausur)
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt/2-Fach
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt/2-Fach
Oktett-Theorie von Lewis
 Oktett-Theorie von Lewis Oktettregel Atome versuchen durch die Nutzung gemeinsamer Elektronenpaare möglichst ein Elektronenoktett zu erlangen. allgemeiner: Edelgasregel Atome streben durch Vereinigung
Oktett-Theorie von Lewis Oktettregel Atome versuchen durch die Nutzung gemeinsamer Elektronenpaare möglichst ein Elektronenoktett zu erlangen. allgemeiner: Edelgasregel Atome streben durch Vereinigung
Dia- und Paramagnetismus. Brandner Hannes Schlatter Nicola
 Dia- und Paramagnetismus Brandner Hannes Schlatter Nicola Ursachen des magnetischen Moments eines freien Atoms Spin der Elektronen (paramagn.) Deren Bahndrehimpuls bezüglich ihrer Bewegung um den Kern
Dia- und Paramagnetismus Brandner Hannes Schlatter Nicola Ursachen des magnetischen Moments eines freien Atoms Spin der Elektronen (paramagn.) Deren Bahndrehimpuls bezüglich ihrer Bewegung um den Kern
Aufgabe Punkte (je 10) Anorganisches Grund-Praktikum (Lehramt) Abschlußklausur (Nachklausur) Name: Vorname: Matrikel-Nr.
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt) Abschlußklausur
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt) Abschlußklausur
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Redoxreaktionen. Elektrochemische Spannungsreihe
 Elektrochemische Spannungsreihe Eine galvanische Zelle bestehend aus einer Normal-Wasserstoffelektrode und einer anderen Halbzelle erzeugen eine Spannung, die, in 1-molarer Lösung gemessen, als Normal-
Elektrochemische Spannungsreihe Eine galvanische Zelle bestehend aus einer Normal-Wasserstoffelektrode und einer anderen Halbzelle erzeugen eine Spannung, die, in 1-molarer Lösung gemessen, als Normal-
3 Elektronenübergänge an Ort : d-d-übergänge
 3 Elektronenübergänge an Ort : d-d-übergänge 3.1 Übersicht, Lernziele Übersicht In diesem Kapitel steht ein weit verbreiteter Mechanismus der Lichtabsorption durch Übergangsmetallverbindungen im Zentrum.
3 Elektronenübergänge an Ort : d-d-übergänge 3.1 Übersicht, Lernziele Übersicht In diesem Kapitel steht ein weit verbreiteter Mechanismus der Lichtabsorption durch Übergangsmetallverbindungen im Zentrum.
Ligandbeiträge g zum VE-Zählen
 Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor, wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor, wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie,
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische h Bindungen Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie, unterschiedliche Arten chemischer Bindungen, Atombindung, kovalente
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische h Bindungen Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie, unterschiedliche Arten chemischer Bindungen, Atombindung, kovalente
3. Bausteine der Materie: Atomhülle. Form der Atomorbitale. s-orbitale kugelsymmetrische Elektronendichteverteilung
 3. Bausteine der Materie: Atomhülle Form der Atomorbitale s-orbitale kugelsymmetrische Elektronendichteverteilung 1s 2s 3d - Orbitale 3. Bausteine der Materie: Atomhülle 3. Bausteine der Materie: Atomhülle
3. Bausteine der Materie: Atomhülle Form der Atomorbitale s-orbitale kugelsymmetrische Elektronendichteverteilung 1s 2s 3d - Orbitale 3. Bausteine der Materie: Atomhülle 3. Bausteine der Materie: Atomhülle
Auf n-kugeln einer dichtesten Packung kommen n-oktaederlücken und 2n-Tetraederlücken
 2.1 Kugelpackungen In einer Verbindung A m X n haben die X-Atome die Anordnung einer dichtesten Kugelpackung und A-Atome besetzen die Oktaederlücken (OL). Geben Sie die resultierenden Formeln A m X n an,
2.1 Kugelpackungen In einer Verbindung A m X n haben die X-Atome die Anordnung einer dichtesten Kugelpackung und A-Atome besetzen die Oktaederlücken (OL). Geben Sie die resultierenden Formeln A m X n an,
2.3. Atome in äusseren Feldern
 .3. Atome in äusseren Feldern.3.1. Der Zeeman-Effekt Nobelpreis für Physik 19 (...researches into the influence of magnetism upon radiation phenomena ) H. A. Lorentz P. Zeeman Die Wechselwirkung eines
.3. Atome in äusseren Feldern.3.1. Der Zeeman-Effekt Nobelpreis für Physik 19 (...researches into the influence of magnetism upon radiation phenomena ) H. A. Lorentz P. Zeeman Die Wechselwirkung eines
Spektroskopische Charakterisierung von Komplexverbindungen
 Lehrstuhl für Bioanorganische- und Koordinationschemie Prof. Dr. H.-C. Böttcher Im Praktikum erschöpfend anwenden: Spektroskopische Charakterisierung von Komplexverbindungen 27. Februar 2015 Vortrag AC3-Praktikum
Lehrstuhl für Bioanorganische- und Koordinationschemie Prof. Dr. H.-C. Böttcher Im Praktikum erschöpfend anwenden: Spektroskopische Charakterisierung von Komplexverbindungen 27. Februar 2015 Vortrag AC3-Praktikum
Versuche zur Ligandenfeldtheorie
 Praktikum IV, Herbstsemester 10 Versuch C2; 14.04.2010 Autoren: Michael Schwarzenberger (michschw@student.ethz.ch) Philippe Knüsel (pknuesel@student.ethz.ch) Teilnehmer: Michael Schwarzenberger und Philippe
Praktikum IV, Herbstsemester 10 Versuch C2; 14.04.2010 Autoren: Michael Schwarzenberger (michschw@student.ethz.ch) Philippe Knüsel (pknuesel@student.ethz.ch) Teilnehmer: Michael Schwarzenberger und Philippe
Magnetochemie. 1. Einleitung. 2. Messung der magnetischen Suszeptibilität. 3. Spin-Only-Paramagnetismus. 4. Bahnbeitrag zum magnetischen Moment
 Magnetochemie 1. Einleitung 2. Messung der magnetischen Suszeptibilität 3. Spin-Only-Paramagnetismus 4. Bahnbeitrag zum magnetischen Moment 5. Temperaturabhängigkeit des magnetischen Moments 1 Literaturempfehlung
Magnetochemie 1. Einleitung 2. Messung der magnetischen Suszeptibilität 3. Spin-Only-Paramagnetismus 4. Bahnbeitrag zum magnetischen Moment 5. Temperaturabhängigkeit des magnetischen Moments 1 Literaturempfehlung
Praktikum Physikalische Chemie II
 Praktikum Physikalische Chemie II Licht-Absorption und -Emission von Übergangsmetallkomplexen Experimentelle Bestimmung eines Orgeldiagramms für Chrom(III)-Komplexe Universität Regensburg Institut für
Praktikum Physikalische Chemie II Licht-Absorption und -Emission von Übergangsmetallkomplexen Experimentelle Bestimmung eines Orgeldiagramms für Chrom(III)-Komplexe Universität Regensburg Institut für
Einführungskurs 7. Seminar
 ABERT-UDWIGS- UNIVERSITÄT FREIBURG Einführungskurs 7. Seminar Prof. Dr. Christoph Janiak iteratur: Riedel, Anorganische Chemie,. Aufl., 00 Kapitel.8.0 und Jander,Blasius, ehrb. d. analyt. u. präp. anorg.
ABERT-UDWIGS- UNIVERSITÄT FREIBURG Einführungskurs 7. Seminar Prof. Dr. Christoph Janiak iteratur: Riedel, Anorganische Chemie,. Aufl., 00 Kapitel.8.0 und Jander,Blasius, ehrb. d. analyt. u. präp. anorg.
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Versuch Nr. 9 Magnetische Suszeptibilität
 Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: 1.1.4 1. Ziel des Versuches Versuch Nr. Magnetische Suszeptibilität Bei diesem Versuch soll die Suszeptibilität von verschiedenen Komplexsalzen
Magdalena Boeddinghaus Gruppe Nr.: Dennis Fischer Datum: 1.1.4 1. Ziel des Versuches Versuch Nr. Magnetische Suszeptibilität Bei diesem Versuch soll die Suszeptibilität von verschiedenen Komplexsalzen
Wiederholungsklausur zur Vorlesung "Allgemeine Chemie" am
 Wiederholungsklausur zur Vorlesung "Allgemeine Chemie" am 14.02.2007 Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte eintragen Wievieltes Fachsemester: Fachrichtung: Sonstiges (bitte angeben): Bitte
Wiederholungsklausur zur Vorlesung "Allgemeine Chemie" am 14.02.2007 Matrikelnummer: Name: Bitte eintragen: Vorname: Bitte eintragen Wievieltes Fachsemester: Fachrichtung: Sonstiges (bitte angeben): Bitte
Fachsemester: Studiengang: Biologie Molekulare Zellbiologie Andere
 Klausur zur Grundvorlesung Allg. und Anorg. Chemie vom 18.01.2008 Seite 1 von 9 Punkte: von 91 Matrikelnummer: Name: Vorname: Bitte eintragen: Bitte ankreuzen: Fachsemester: Studiengang: Biologie Molekulare
Klausur zur Grundvorlesung Allg. und Anorg. Chemie vom 18.01.2008 Seite 1 von 9 Punkte: von 91 Matrikelnummer: Name: Vorname: Bitte eintragen: Bitte ankreuzen: Fachsemester: Studiengang: Biologie Molekulare
c = Ausbreitungsgeschwindigkeit (2, m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 )
 2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
Atome und Bindungen. Was sollen Sie mitnehmen?
 Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Was sollen Sie mitnehmen? Elementare Grundlagen: Atome und Bindungen Schalenmodell Orbitalmodell Periodensystem der Elemente Typische Eigenschaften der Elemente Die vier Bindungstypen Kovalente Bindung
Festkörper-EPR-Messungen an Mn 2+ -dotierten Mg-Kristallen
 -1- EPR in Festkörpern Festkörper-EPR-Messungen an Mn + -dotierten Mg-Kristallen Die EPR-Spektren von Mn + bestehen aus einer großen Zahl von Linien. Das zweiwertige Mangan als d 5 - Ion hat einen 6 S
-1- EPR in Festkörpern Festkörper-EPR-Messungen an Mn + -dotierten Mg-Kristallen Die EPR-Spektren von Mn + bestehen aus einer großen Zahl von Linien. Das zweiwertige Mangan als d 5 - Ion hat einen 6 S
Thema: Komplexverbindungen, die koordinative Bindung. Koordinationszahl, 18-Elektronen-Schale, ein- mehrzähnige Liganden, EDTA,
 Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
