Auswertung der Lernbegleitbögen zu Beginn der Unterrichtseinheit
|
|
|
- Gerd Adenauer
- vor 7 Jahren
- Abrufe
Transkript
1 Fragestellung des Lernbegleitbogens Du hast bereits verschiedene Oxidationsreaktionen (hier als Reaktionen von Stoffen mit Sauerstoff) kennen gelernt. Auffällig ist, dass sich Oxidationsreaktionen deutlich in ihrer Heftigkeit unterscheiden. Wie erklärst du dir diese Beobachtungen? Analyse der Lernbegleitbögen: Die unterschiedlichen Erklärungsansätze der 23 Schülerinnen und Schüler zu Beginn der Unterrichtseinheit werden in der folgenden Übersicht (Tabelle 2) entsprechend der absoluten Anzahl ihrer Nennungen dargestellt Menge an Sauerstoff 11 Aggregatzustand Art des brennbaren Stoffes Menge an brennbarem Stoff Zufuhr von Energie Energieinhalt der Ausgangsstoffe 10 Versuchsapparatur Tabelle 1: Auswertung der Lernbegleitbögen zu Beginn der Unterrichtseinheit Analyse der Überarbeitungen der Lernbegleitbögen: In der folgenden Übersicht (Tabelle 3) werden die Erklärungsansätze der 23 Schülerinnen und Schüler nach der Behandlung der Reaktionsbedingungen im Unterricht entsprechend der absoluten Anzahl ihrer Nennungen dargestellt. Menge an Sauerstoff Temperatur Zerteilungsgrad Durchmischung Art des brennbaren Stoffes Aggregatzustand Menge an brennbarem Stoff Energieinhalt der Ausgangsstoffe Tabelle 2: Auswertung der Überarbeitungen der Lernbegleitbögen 1
2 Vergleich der Ergebnisse: Die Erklärungsansätze der 23 Schülerinnen und Schüler zu Beginn der Unterrichtseinheit (blau) und nach der selbstständigen Korrektur (rot) werden in der Tabelle 4 entsprechend der absoluten Anzahl ihrer Nennungen im Vergleich dargestellt. Menge an Sauerstoff Temperatur Art des brennbaren Stoffes Menge an brennbarem Stoff 1.Einsatz Einsatz Zerteilungsgrad Durchmischung Aggregatzustand Energieinhalt der Ausgangsstoffe Versuchsapparatur Tabelle 3: Vergleichende Auswertung des 1. und 2. Einsatzes der Lernbegleitbögen Vermutung: Menge an Sauerstoff Zitat Nr. 1 Na ja, also ich würde sagen, es hängt immer davon ab, wie viel Sauerstoff vorhanden ist. Zitat Nr. 2 Ich würde sagen, dass die Oxidationsheftigkeit von der Menge des Sauerstoffs abhängt. Wenn man mehr bzw. weniger vom Sauerstoff nimmt, nimmt die Oxidation zu bzw. ab. Zitat Nr. 3 Je mehr prozentual gesehen Sauerstoff im Gemisch enthalten ist und je mehr von dem Gemisch da ist, um so heftiger wird die Reaktion. Zitat Nr. 4 Ich denke, dass der Sauerstoff wirkt. Also je mehr Sauerstoff den Stoffen zugeführt wird, desto heftiger ist die Reaktion. Denn durch Sauerstoff wird ja Feuer gefördert (das Feuer braucht Sauerstoff zum Brennen). Zitat Nr. 5 Ich erkläre mir diese Beobachtung wie folgt: Bei den Reaktionen kam unterschiedlich viel Sauerstoff an die Reaktion. Wenn mehr an die Reaktion gelangte, fiel die Oxidationsreaktion heftiger aus. Wenn weniger Sauerstoff daran gelangte, fiel sie weniger heftig aus. Da Sauerstoff ein wichtiger Ausgangsstoff bei Oxidationsreaktionen ist, fallen die Oxidationsreaktionen so unterschiedlich aus. 2
3 Vermutung: Aggregatzustand Zitat Nr. 1 Verbrennen von Wachs, Verbrennen von Eisen, Verbrennen von Magnesium, Verbrennen von Wasserstoff. Bei den einzelnen Verbrennungen ist es unterschiedlich von der Heftigkeit, da die einzelnen Stoffe alle verschiedene Dichten haben. Zitat Nr. 2 Das kommt wahrscheinlich auf die Anordnungen und Aufbauarten der Teilchen, aus denen die Stoffe bestehen, an. Auch glaube ich, dass die Kräfte zwischen den Teilchen etwas mit der Reaktion zu tun haben. So sind z.b. feste Körper schwieriger zu teilen als flüssige. Zitat Nr. 3 Ich glaube, es hat vielleicht etwas mit der Anordnung der Teilchen zu tun. Deswegen auch mit dem Aggregatzustand. Ich glaube, je weiter die Teilchen voneinander entfernt sind, desto heftiger ist die Reaktion. Zitat Nr. 4 Es liegt an der Dichte der Teilchen, denn umso ruhiger und langsamer die Oxidation abläuft, umso dichter liegen beim Ausgangsstoff die Teilchen zusammen und umso stärker waren die Kräfte, die die Teilchen zusammenhielten, denn umso mehr Energie wird benötigt, um diese Kräfte zu lockern und die Teilchen auseinanderzuteilen, sodass sie ihre Ordnung verlieren und eine Reaktion eingehen können. Zitat Nr. 5 Weil jeder Stoff anders aufgebaut ist! Bei dem Metall Magnesium glüht es hell auf, da Magnesium ein fester Stoff ist. Beim Verbrennen der Kerze war es eine Aggregatzustandsänderung von fest zu gasförmig. Bei den Wasserstoffexperimenten ging es sehr heftig zu, da Wasserstoff ein gut brennbares Gas ist es knallt. Zitat Nr. 6 Vielleicht hat es was mit dem Aggregatzustand zu tun. Magnesium ist ja ein fester Stoff, und dort war eine ziemlich heftige Reaktion. Und bei einem Gas ist vielleicht nicht so eine heftige Reaktion. Zitat Nr. 7 Ich glaube, dass bei den Stoffen die heftiger reagieren vielleicht mehr Teilchen vorhanden sind und so die Verbrennung heftiger ist. Vielleicht kommt es aber auch auf den Aggregatzustand an, wenn der Körper fest ist und die Teilchen enger und geordneter zusammen sind, reagieren sie schneller und es entsteht so etwas wie eine Kettenreaktion und die Verbrennung ist dadurch heftiger, da mehr Teilchen auf einem engen Raum vorhanden sind und nicht frei in der Luft herumschweben. 3
4 Vermutung: Art des brennbaren Stoffes Zitat Nr. 1 Das hängt vom Stoff ab. Zitat Nr. 2 Jeder Stoff reagiert anders auf äußere Einwirkungen. Die daraufhin folgenden Reaktionen sind daher von Stoff zu Stoff unterschiedlich. Einige Reaktionen sind kaum wahrnehmbar und andere um so mehr. Das kommt wahrscheinlich auf die Anordnungen und Aufbauarten der Teilchen, aus denen die Stoffe bestehen, an. Zitat Nr. 3 Ich denke, dass es auch auf die anderen Ausgangsstoff und die Energiezufuhr ankommt. Metalle (z.b. Kupfer) reagieren nur sehr langsam mit Sauerstoff und Wasserstoff dagegen kann unter Umständen knallartig reagieren. Da sich die Eigenschaften der Einzelnen Stoffe ja auch unterscheiden, ist es doch gut möglich, dass die Oxidationen der verschiedenen Stoffe anders verlaufen. Ich glaube, die Heftigkeit und die Auswirkung verschiedener Oxidationsreaktionen sind abhängig von der Kombination der Ausgangsstoffe bei chemischen Reaktionen. Zitat Nr. 4 Ich denke, dass die Ausgangsstoffe verschieden große Energien haben und dass die Oxidationsreaktionen die Energie der Ausgangsstoffe mit übernehmen und sich so in ihrer Heftigkeit unterscheiden. Zitat Nr. 5 Außerdem ist jeder Stoff anders aufgebaut, z.b. sind manchmal brandfördernde Stoffe enthalten, dann läuft die Reaktion besonders heftig ab. Weitere Erklärungsansätze Zitat Nr. 1 Dass die Verbrennungen unterschiedliche Wärmeenergie benötigen oder Energie abgeben. Zitat Nr. 2 Es kommt darauf an, welche Konzentration da zwischen Sauerstoff und anderen Stoffen besteht, z.b. Wasserstoff und Sauerstoff haben wir in der Schule rausgefunden, dass 1 Sauerstoffatom zwei Wasserstoffatome tragen kann. Aus 2 Molekülen Wasserstoff und 1 Molekül Sauerstoff entstanden 2 Wassermoleküle. Die Konzentration steht also 2:1. Es gab einen dicken Knall. Wäre mehr Sauerstoff gewesen, hätte der Wasserstoff mehr Angriffsfläche und der Knall ist lauter. Wäre mehr Wasserstoff, gäbe es einen leiseren Knall, weil Wasserstoff nicht so viel Sauerstoff angreifen könnte. Zitat Nr. 3 Die Teilchen wollen sich unterschiedlich schnell bewegen und je besser sie es finden, sich schnell hin und her zu bewegen, umso besser brennt der Stoff, da sie von sich aus eine größere Wärme produzieren wollen und nicht gerne so eng beieinander sitzen wollen, suchen sie nach Alternativen und in diesem Fall ist es die Verbrennung. Zitat Nr. 4 Ich glaube, dass das daher kommt, wie groß der Druck jeweils in der Umgebung ist. Wie z.b. bei der Knallgasprobe da hat es mit einem kleinem Rohr nicht so doll gekracht wie mit einer Dose. 4
5 Lernbegleitbogen - ursprüngliche Aussagen (a) und Überarbeitungen (b) Die Variante (a) gibt die erste Aussage im Lernbegleitbogen wider, Variante (b) stellt die Antwort dar, die beim zweiten Einsatz gegeben wurde. Beispiel 1 (a) Dass die Verbrennungen unterschiedliche Wärmeenergie benötigen oder Energie abgeben. (b) Die Oxidationsreaktion ist abhängig von der Zerteilung und Durchmischung der Stoffe, Menge an Sauerstoff, Temperatur, der Art des brennbaren Stoffes und der chemischen Energie der Ausgangsstoffe und Reaktionsprodukte, weil das alles Reaktionsbedingungen sind. Beispiel 2 (a) Ich denke, dass der Sauerstoff wirkt. Also je mehr Sauerstoff den Stoffen zugeführt wird, desto heftiger ist die Reaktion. Denn durch Sauerstoff wird ja Feuer gefördert (das Feuer braucht Sauerstoff zum Brennen). (b) Je mehr Sauerstoff vorhanden ist, umso heftiger ist die Reaktion. Das ist aber nur ein Teilfaktor von Heftigkeiten der Reaktionen. Ein weiterer Fakt ist, je kleiner die Stoffe zerteilt sind, desto heftiger ist die Reaktion. Je höher die Temperatur ist, umso heftiger ist die chemische Reaktion. Denn mit höherer Temperatur bewegen sich die Teilchen heftiger und dadurch ist die Reaktion auch heftiger. Meine erste Vermutung war, dass es an der Menge von Sauerstoff liegt. Dies ist auch ein Grund von der Heftigkeit von Reaktionen. Beispiel 3 (a) Ich erkläre mir diese Beobachtung wie folgt: Bei den Reaktionen kam unterschiedlich viel Sauerstoff an die Reaktion. Wenn mehr an die Reaktion gelangte, fiel die Oxidationsreaktion heftiger aus. Wenn weniger Sauerstoff daran gelangte, fiel sie weniger heftig aus. Da Sauerstoff ein wichtiger Ausgangsstoff bei Oxidationsreaktionen ist, fallen die Oxidationsreaktionen so unterschiedlich aus. (b) Die Sauerstoffmenge ist wichtig für die Heftigkeit der Oxidationsreaktionen aber auch die Art des Stoffes, der Aggregatzustand des Stoffes, aber auch der Zerstäubungsgrad des Stoffes. Die Sauerstoffmenge ist wichtig, da wenn mehr Sauerstoff vorhanden ist mehr Reaktionen stattfinden können. Ist ein Körper gasförmig, dann verbrennt er heftiger, schneller. Ist der Zerstäubungsgrad hoch, dann läuft die Reaktion heftig ab. Aber auch die Menge des brennbaren Stoffes ist wichtig. Mehr brennbarer Stoff heftigere Reaktion. 5
6 Beispiel 4 (a) Je mehr prozentual gesehen Sauerstoff im Gemisch enthalten ist und je mehr von dem Gemisch da ist, umso heftiger wird die Reaktion. Außerdem ist jeder Stoff anders aufgebaut, z.b. sind manchmal brandfördernde Stoffe enthalten, dann läuft die Reaktion besonders heftig ab. (b) Reaktionsbedingungen sind: 1. Sauerstoffmenge (hatte ich schon) 2. Temperatur 3. Art des brennbaren Stoffes (hatte ich schon) 4. Menge des brennbaren Stoffes 5. Berührungsfläche zwischen brennbarem Stoff und Sauerstoff 1. Je mehr Sauerstoff vorhanden ist, umso heftiger läuft die Reaktion ab. 2. Je höher die Temperatur ist, umso heftiger und schneller läuft die Reaktion ab. 3. Es gibt brandfördernde, brennbare und nicht brennbare Stoffe. 4. Je mehr von dem brennbaren Stoff vorhanden ist, umso heftiger läuft die Reaktion ab. 5. Je mehr Sauerstoff an den brennbaren Stoff herankommt, umso schneller und heftiger läuft die Reaktion ab. Beispiel 5 (a) Vielleicht hat es was mit dem Aggregatzustand zu tun. Magnesium ist ja ein fester Stoff, und dort war eine ziemlich heftige Reaktion. Und bei einem Gas ist vielleicht nicht so eine heftige Reaktion. Oder die Anzahl der Sauerstoffmoleküle ist bei den heftigen Reaktionen höher. Oder anders herum. (b) Die Oxidation in ihrer Heftigkeit ist abhängig von der Menge an Sauerstoff. Umso weniger Sauerstoff bei der Oxidation dabei ist, umso weniger heftig verläuft die Oxidation und umso mehr Sauerstoff dabei ist, umso heftiger verläuft auch die Oxidation. Außerdem spielt der Zerteilungsgrad eine wichtige Rolle, denn umso zerlegter der Stoff ist, umso heftiger verläuft die Oxidation: z.b. Eisennagel Eisenschwamm Eisenwolle Eisenpulver In dieser Reihenfolge verläuft die Oxidation heftiger (also Eisennagel am wenigsten, Eisenpulver am heftigsten). Die Temperatur spielt außerdem noch eine sehr wichtige Rolle, umso wärmer es ist, umso heftiger verläuft die Reaktion. Die Durchmischung ist auch sehr wichtig. Beim ersten Mal hatte ich etwas zum Teil richtig. Jetzt weiß ich viel mehr über die Oxidation. 6
7 Beispiel 6 (a) Jeder Stoff reagiert anders auf äußere Einwirkungen. Die daraufhin folgenden Reaktionen sind daher von Stoff zu Stoff unterschiedlich. Einige Reaktionen sind kaum wahrnehmbar und andere um so mehr. Das kommt wahrscheinlich auf die Anordnungen und Aufbauarten der Teilchen, aus denen die Stoffe bestehen, an. Auch glaube ich, dass die Kräfte zwischen den Teilchen etwas mit der Reaktion zu tun haben. So sind z.b. feste Körper schwieriger zu teilen als flüssige. (b) Jeder Stoff reagiert anders auf äußere Einwirkungen. Die daraufhin folgenden Reaktionen sind daher von Stoff zu Stoff unterschiedlich. Auch sind Sauerstoffmoleküle notwendig. Je mehr Sauerstoff vorhanden ist, desto heftiger ist die Reaktion. Auch wenn der Stoff zerteilt ist und somit eine größere Angriffsfläche bietet, ist sie größer. Wenn die Teilchen dann auch noch mit der Luft vermischt werden, kann die Reaktion schneller und heftiger sein. Die Temperatur spielt auch eine Rolle. Je mehr Wärme zugeführt wird, desto eher und kräftiger stoßen die sich immer heftiger bewegenden Teilchen zusammen. Beispiel 7 (a) Ich glaube, dass bei den Stoffen die heftiger reagieren vielleicht mehr Teilchen vorhanden sind und so die Verbrennung heftiger ist. Vielleicht kommt es aber auch auf den Aggregatzustand an, wenn der Körper fest ist und die Teilchen enger und geordneter zusammen sind, reagieren sie schneller und es entsteht so etwas wie eine Kettenreaktion und die Verbrennung ist dadurch heftiger, da mehr Teilchen auf einem engen Raum vorhanden sind und nicht frei in der Luft herumschweben. (b) Es ist richtig, dass es vom Aggregatzustand abhängt, doch die Verbrennung läuft heftiger, umso weiter die Teilchen auseinander sind und nicht umgekehrt, z.b. bei einem gasförmigen Stoff können sich die Teilchen besser mit Sauerstoff durchmischen und dadurch verläuft die Reaktion heftiger. Es hängt auch von der Menge an Sauerstoff ab, desto mehr Sauerstoffmoleküle vorhanden sind, umso schneller und heftiger die Verbrennung, da sie dann besser mit den anderen Teilchen zusammenstoßen können. Die Temperatur ist auch eine Bedingung, da wenn die Temperatur höher ist, bewegen sich die Teilchen heftiger, also die Geschwindigkeit nimmt zu und die Teilchen stoßen dadurch heftiger zusammen. Also habe ich nur ein wenig richtig gedacht. 7
8 Beispiel 8 (a) Ich denke, dass es auch auf die anderen Ausgangsstoff und die Energiezufuhr ankommt. Metalle (z.b. Kupfer) reagieren nur sehr langsam mit Sauerstoff und Wasserstoff dagegen kann unter Umständen knallartig reagieren. Da sich die Eigenschaften der Einzelnen Stoffe ja auch unterscheiden, ist es doch gut möglich, dass die Oxidationen der verschiedenen Stoffe anders verlaufen. Ich glaube, die Heftigkeit und die Auswirkung verschiedener Oxidationsreaktionen sind abhängig von der Kombination der Ausgangsstoffe bei chemischen Reaktionen. (b) Die Heftigkeit einer Oxidationsreaktion ist wirklich von der Art des Ausgangsstoffes abhängig. Das habe ich ja schon ganz gut erkannt. Wichtig ist aber auch, wie groß der Zerteilungsgrad ist und ob und wie stark ein Stoff mit Sauerstoff durchmischt ist. Außerdem entscheiden auch der Aggregatzustand, die Temperatur und die Menge des Sauerstoffs über die Heftigkeit und die Geschwindigkeit der Reaktion. Begründung: Zerteilungsgrad: Umso mehr Oberfläche vorhanden ist, umso mehr Teilchen können mit Sauerstoff reagieren. Durchmischung: Wenn der Stoff bereits mit Sauerstoff durchmischt ist, können die Teilchen leichter reagieren. Aggregatzustand: Gasförmige Stoffe oxidieren meist heftiger. Temperatur: Wärme beschleunigt die Oxidation. Menge des Sauerstoffs: Wenn mehr Sauerstoffmoleküle da sind, können auch mehr Teilchen reagieren. Beispiel 9 (a) Die Teilchen wollen sich unterschiedlich schnell bewegen und je besser sie es finden, sich schnell hin und her zu bewegen, umso besser brennt der Stoff, da sie von sich aus eine größere Wärme produzieren wollen und nicht gerne so eng beieinander sitzen wollen, suchen sie nach Alternativen und in diesem Fall ist es die Verbrennung. (b) Je mehr Sauerstoff vorhanden ist, umso heftiger verläuft die Oxidation. Ebenso wenn die Temperatur erhöht ist, da der Stoff einen anderen Aggregatzustand hat und die Angriffsfläche größer ist. Wenn mehr Sauerstoff vorhanden ist, sind viel mehr Sauerstoffmoleküle vorhanden, die mit den Atomen der anderen Stoffe reagieren können. Wenn die Temperatur höher ist, bewegen sich die Teilchen schneller und so können mehr in einer bestimmten Zeit reagieren. Auch wenn der Aggregatzustand flüssig oder gasförmig ist, verläuft die Oxidation schneller als bei Feststoffen, da sich die Teilchen schneller bewegen. Wenn sie (die Stoffe) zerkleinert worden sind, ist mehr prozentuale Angriffsfläche zur Verfügung und die Teilchen können sich schneller bewegen. 8
9 Zur Überprüfung des Konzeptverständnisses wurde zum Ende der Einheit im Rahmen einer Lernerfolgskontrolle eine Transferaufgabe eingesetzt (Abb. 1), in der die SchülerInnen aufgefordert waren, ein Experiment zu planen, um die Verbrennung von Wachs durch Variation der Reaktionsbedingungen gezielt zu fördern und ihre Versuchsplanung zu begründen. Aufgabe: Wachs wird in einem Reagenzglas geschmolzen. Die entstehenden Wachsdämpfe lassen sich entzünden und verbrennen mit ruhiger Flamme. a) Mache begründete Vorschläge, wie man die Heftigkeit der Verbrennung von Wachs im Experiment durch Veränderungen von Reaktionsbedingungen steigern könnte! b) Fertige zu deinen Vorschlägen eine Versuchsskizze an! Abb. 1: Transferaufgabe aus der Lernerfolgskontrolle Die Ergebnisse zu dieser Aufgabe fielen sehr positiv aus; die Lernenden waren tatsächlich in der Lage, ihre Kenntnisse um den Einfluss von Reaktionsbedingungen sinnvoll anzuwenden und geeignete Experimente zu entwickeln (vgl. Abb. 2, 3 und 4). Der Großteil der Schüler entwarf kombinierte Versuchsskizzen bzw. eine logische Abfolge von Teilversuchen, in denen es ihnen gelang, das Wissen über die verschiedenen Reaktionsbedingungen nicht nur sachgerecht zur Lösung des gestellten Problems anzuwenden und dabei planerisch vorzugehen, sondern darüber hinaus die einzelnen Reaktionsbedingungen sinnvoll miteinander zu kombinieren. Abb. 2: Versuchsskizze zur Transferaufgabe Lösung mit 1 Schritt Abb. 3: Versuchsskizze zur Transferaufgabe Lösung mit 2 Schritten Abb. 4: Versuchsskizze zur Transferaufgabe Lösung mit 3 Schritten 9
Bundesrealgymnasium Imst. Chemie 2010-11. Klasse 4. Einführung Stoffe
 Bundesrealgymnasium Imst Chemie 2010-11 Einführung Stoffe Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 Einführung Stoffe Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Aufgaben. 2 Physikalische Grundlagen
 Der Verdampfungs- oder Kondensationspunkt jedes Stoffes ist von der Temperatur und dem Druck abhängig. Für jede Verdampfungstemperatur gibt es nur einen zugehörigen Verdampfungsdruck und für jeden Verdampfungsdruck
Der Verdampfungs- oder Kondensationspunkt jedes Stoffes ist von der Temperatur und dem Druck abhängig. Für jede Verdampfungstemperatur gibt es nur einen zugehörigen Verdampfungsdruck und für jeden Verdampfungsdruck
Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann.
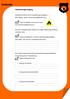 Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Robert-Koch-Gymnasium Deggendorf. Grundwissen Chemie. 8. Jahrgangsstufe
 Robert-Koch-Gymnasium Deggendorf Grundwissen Chemie 8. Jahrgangsstufe Teilchenmodell und Stoffeigenschaften Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, vereinfacht dargestellt als Kugeln.
Robert-Koch-Gymnasium Deggendorf Grundwissen Chemie 8. Jahrgangsstufe Teilchenmodell und Stoffeigenschaften Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, vereinfacht dargestellt als Kugeln.
Chemische Reaktionen. Wir erzeugen Wasser
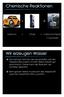 hemische Reaktionen + Natrium + -> hlor -> Natriumchlorid = Kochsalz Wir erzeugen Wasser Die kleinsten Teilchen des Sauerstoffes und des Wasserstoffes waren im roten Ballon bereits gut durchmischt. Daher
hemische Reaktionen + Natrium + -> hlor -> Natriumchlorid = Kochsalz Wir erzeugen Wasser Die kleinsten Teilchen des Sauerstoffes und des Wasserstoffes waren im roten Ballon bereits gut durchmischt. Daher
Pentan enthält 12 Atome Wasserstoff, ein Wassermolekül 2 Atome. Es entstehen also 6 Moleküle Wasser:
 VERTIEFUNG Aufstellen und Einrichten von Gleichungen Reaktionsgleichungen fassen eine chemische Reaktion knapp zusammen. Es werden die Edukte (Ausgangsstoffe) angegeben, die in der chemischen Reaktion
VERTIEFUNG Aufstellen und Einrichten von Gleichungen Reaktionsgleichungen fassen eine chemische Reaktion knapp zusammen. Es werden die Edukte (Ausgangsstoffe) angegeben, die in der chemischen Reaktion
Inhalt. Methode Methode Aktion. Aktion Fakten Projekt Projekt Projekt Projekt. Ausblick Aktion Fakten Ausblick Methode Ausblick Wissen & Training
 Stoffe im Alltag 8 Experimentieren in der Chemie 10 Wärmequellen im Unterricht 12 Sicherheit in der Chemie Lernen an Stationen 14 Stoffe und ihren Eigenschaften 16 Den Stoffen auf der Spur 16 Körper und
Stoffe im Alltag 8 Experimentieren in der Chemie 10 Wärmequellen im Unterricht 12 Sicherheit in der Chemie Lernen an Stationen 14 Stoffe und ihren Eigenschaften 16 Den Stoffen auf der Spur 16 Körper und
Modelle helfen Erscheinungen und Vorgänge zu beschreiben und Wesentliches zu erkennen, geben jedoch die Wirklichkeit nie vollständig wieder.
 I. Stoffen auf der Spur 1. Eigenschaften von Stoffen erkennen Farbe Geruch Geschmack Kristallform Klang Zustandsform 2. Eigenschaften von Stoffen ermitteln/ messen Wärmeleitfähigkeit Elektrische Leitfähigkeit
I. Stoffen auf der Spur 1. Eigenschaften von Stoffen erkennen Farbe Geruch Geschmack Kristallform Klang Zustandsform 2. Eigenschaften von Stoffen ermitteln/ messen Wärmeleitfähigkeit Elektrische Leitfähigkeit
Was passiert denn genau?
 Was passiert denn genau? - Bei chemischen Reaktionen entstehen neue Stoffe, mit neuen Eigenschaften. - Im Teilchenmodell stellen wir uns vor, dass Kugelteilchen (Edukte) neu kombiniert werden. - Wenn wir
Was passiert denn genau? - Bei chemischen Reaktionen entstehen neue Stoffe, mit neuen Eigenschaften. - Im Teilchenmodell stellen wir uns vor, dass Kugelteilchen (Edukte) neu kombiniert werden. - Wenn wir
Beispiel: Fällung von Bariumsulfat aus einer Sulfat-Ionen enthaltenden Lösung mit Hilfe von Bariumchlorid
 Reaktionsgleichungen In der Chemie ist eine Reaktionsgleichung die Kurzschreibweise für eine chemische Reaktion. Sie gibt die Ausgangs und Endstoffe (Reaktanten und Produkte) einer Stoffumwandlung in richtigem
Reaktionsgleichungen In der Chemie ist eine Reaktionsgleichung die Kurzschreibweise für eine chemische Reaktion. Sie gibt die Ausgangs und Endstoffe (Reaktanten und Produkte) einer Stoffumwandlung in richtigem
Wie lässt sich Stickstoff gewinnen, welche Eigenschaften hat er?
 Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P753800) 2.6 Stickstoff - Darstellung und Eigenschaften Experiment von: P753900D Gedruckt: 24.03.204 0:54:2 intertess (Version
Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P753800) 2.6 Stickstoff - Darstellung und Eigenschaften Experiment von: P753900D Gedruckt: 24.03.204 0:54:2 intertess (Version
Verbrennung einer Kerze
 Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
John Daltons Atomhypothese. 1. Wie kommt Dalton auf die Atomhypothese? a. Die Eigenschaften des Wassers
 John Daltons Atomhypothese 1. Wie kommt Dalton auf die Atomhypothese? a. Die Eigenschaften des Wassers 2. Welche Aussagen trifft Dalton mit Hilfe des Atommodells? A. Verhalten von Stoffen bei chem. Reaktionen
John Daltons Atomhypothese 1. Wie kommt Dalton auf die Atomhypothese? a. Die Eigenschaften des Wassers 2. Welche Aussagen trifft Dalton mit Hilfe des Atommodells? A. Verhalten von Stoffen bei chem. Reaktionen
Protokoll Checker Code Hinweis Ratgeber Beispiel
 I: INHALT UND FACHLICHKEIT I1 Das ist fachlich nicht richtig. Du solltest das Eperiment nochmal Schritt für Schritt durchdenken. Bei Unklarheiten kannst Du im Schulbuch nachschlagen oder deine Mitschüler/
I: INHALT UND FACHLICHKEIT I1 Das ist fachlich nicht richtig. Du solltest das Eperiment nochmal Schritt für Schritt durchdenken. Bei Unklarheiten kannst Du im Schulbuch nachschlagen oder deine Mitschüler/
Was bedeuten die Zahlen auf den orangenen Warntafeln, die an Gefahrgut-Transportern angebracht sind?
 Was bedeuten die Zahlen auf den orangenen Warntafeln, die an Gefahrgut-Transportern angebracht sind? Die obere Zahl gibt die Gefahr an, die vom transportierten Stoff ausgeht, die untere Zahl dient zur
Was bedeuten die Zahlen auf den orangenen Warntafeln, die an Gefahrgut-Transportern angebracht sind? Die obere Zahl gibt die Gefahr an, die vom transportierten Stoff ausgeht, die untere Zahl dient zur
Hallo, liebe Schülerinnen und Schüler!
 Hallo, liebe Schülerinnen und Schüler! Wir, die Arbeitsgruppe Physikdidaktik am Fachbereich Physik der Universität Osnabrück, beschäftigen uns damit, neue und möglichst interessante Themen für den Physikunterricht
Hallo, liebe Schülerinnen und Schüler! Wir, die Arbeitsgruppe Physikdidaktik am Fachbereich Physik der Universität Osnabrück, beschäftigen uns damit, neue und möglichst interessante Themen für den Physikunterricht
Lernmaterial Lernfeld 1 Grundlagen Physik und Chemie. Chemische Grundlagen, Bindungsarten. Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms
 Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
I. Chemische Bindung und Zwischenmolekulare Kräfte
 I. Chemische Bindung und Zwischenmolekulare Kräfte MINT-UNTERRICHTSEINHEIT A. Ausgangslage Die klare Unterscheidung der chemischen Bindung- und der Zwischenmolekularen Kräfte und die korrekte Zuordnung
I. Chemische Bindung und Zwischenmolekulare Kräfte MINT-UNTERRICHTSEINHEIT A. Ausgangslage Die klare Unterscheidung der chemischen Bindung- und der Zwischenmolekularen Kräfte und die korrekte Zuordnung
SICHERHEIT IM HAUSHALT: FEUERGEFAHR IN DER KÜCHE
 Material: SICHERHEIT IM HAUSHALT: FEUERGEFAHR IN DER KÜCHE Wie entsteht überhaupt Feuer? Warum kann es in der Küche leicht zu einem Brand kommen, und wie verhalte ich mich richtig? Eine Unterrichtseinheit,
Material: SICHERHEIT IM HAUSHALT: FEUERGEFAHR IN DER KÜCHE Wie entsteht überhaupt Feuer? Warum kann es in der Küche leicht zu einem Brand kommen, und wie verhalte ich mich richtig? Eine Unterrichtseinheit,
Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm Klasse 8 Themen Experimentieren im Chemieunterricht Grundregeln des Experimentierens 5. - mit Laborgeräten sachgerecht umgehen und die Sicherheitsmaßnahmen
Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm Klasse 8 Themen Experimentieren im Chemieunterricht Grundregeln des Experimentierens 5. - mit Laborgeräten sachgerecht umgehen und die Sicherheitsmaßnahmen
Lösungen Kap. 4 Die chemische Reaktion
 Elemente Grundlagen der Chemie für Schweizer Maturitätsschulen Klett und Balmer Verlag Zug 2007 Verwendung für den Gebrauch in der eigenen Klasse gestattet Lösungen Kap. 4 Die chemische Reaktion Lösungen
Elemente Grundlagen der Chemie für Schweizer Maturitätsschulen Klett und Balmer Verlag Zug 2007 Verwendung für den Gebrauch in der eigenen Klasse gestattet Lösungen Kap. 4 Die chemische Reaktion Lösungen
MAGNESIUM. 1. Bei Verbrennungsreaktionen entstehen in der Regel (kreuze richtig an):
 MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
2.9 Aufbau und Funktion eines Bunsenbrenners. Aufgabe. Wie ist der Bunsenbrenner aufgebaut?
 Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P75400) 2.9 Aufbau und Funktion eines Bunsenbrenners Experiment von: Seb Gedruckt: 24.03.204 ::49 intertess (Version 3.2 B24,
Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P75400) 2.9 Aufbau und Funktion eines Bunsenbrenners Experiment von: Seb Gedruckt: 24.03.204 ::49 intertess (Version 3.2 B24,
Die chemische Reaktion
 Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Aus den beiden Ausgangsstoffen (Edukten) entsteht ein neuer Stoff (Produkt) mit eigenen,
Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Aus den beiden Ausgangsstoffen (Edukten) entsteht ein neuer Stoff (Produkt) mit eigenen,
Vieles in unserem Alltag hat mit Chemie zu tun. Walter Caprez Kinderuniversität Winterthur 24. Okt 2012
 Vieles in unserem Alltag hat mit Chemie zu tun Walter Caprez Kinderuniversität Winterthur 24. Okt 2012 Wie ist unsere Welt aufgebaut? Wir bestehen aus Atomen. Alle Lebewesen (Menschen, Tiere, Pflanzen)
Vieles in unserem Alltag hat mit Chemie zu tun Walter Caprez Kinderuniversität Winterthur 24. Okt 2012 Wie ist unsere Welt aufgebaut? Wir bestehen aus Atomen. Alle Lebewesen (Menschen, Tiere, Pflanzen)
Aufbau der Körper. Was ist in der Physik ein Körper?
 Aufbau der Körper Was ist in der Physik ein Körper? Lies im Lehrbuch S. 70/71 Zähle 4 verschiedene Körper auf! Jeder Körper besteht aus einem Stoff oder aus mehreren Stoffen. Es gibt 3 Aggregatzustände:
Aufbau der Körper Was ist in der Physik ein Körper? Lies im Lehrbuch S. 70/71 Zähle 4 verschiedene Körper auf! Jeder Körper besteht aus einem Stoff oder aus mehreren Stoffen. Es gibt 3 Aggregatzustände:
EINE KERZE INTERPRETATIONEN BEOBACHTUNGEN FLAMME REAKTIONEN WACHS DOCHT GASE. Reaktionsgleichungen Prozesse. Theorien
 Reaktionsgleichungen Prozesse INTERPRETATIONEN BEOBACHTUNGEN Theorien Licht Produkte Reaktionsgleichungen Thermodynamik Geschwindigkeit REAKTIONEN EINE KERZE FLAMME Farbe Form Bewegung Einflüsse WACHS
Reaktionsgleichungen Prozesse INTERPRETATIONEN BEOBACHTUNGEN Theorien Licht Produkte Reaktionsgleichungen Thermodynamik Geschwindigkeit REAKTIONEN EINE KERZE FLAMME Farbe Form Bewegung Einflüsse WACHS
Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer
 Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer chemischen Reaktion? In der letzten Chemiestunde hast du eine Hypothese zu der Frage formuliert: Verändert sich die Masse von
Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer chemischen Reaktion? In der letzten Chemiestunde hast du eine Hypothese zu der Frage formuliert: Verändert sich die Masse von
1 Verbrennung und Sauerstoff
 1 Verbrennung und Sauerstoff 1.1 Feuer und Flamme 1.2 Ein Feuer entsteht 1.3 Lagerfeuer Unterrichtsidee Unterrichtsphase Methoden und Materialien Leitfrage Erarbeitung Sicherung Hausaufgabe Unterrichtsziele
1 Verbrennung und Sauerstoff 1.1 Feuer und Flamme 1.2 Ein Feuer entsteht 1.3 Lagerfeuer Unterrichtsidee Unterrichtsphase Methoden und Materialien Leitfrage Erarbeitung Sicherung Hausaufgabe Unterrichtsziele
Verbrennung einer Kerze
 Verbrennung einer Kerze Zünde eine Kerze an und notiere deine Beobachtungen: Was passiert eigentlich genau bei der Verbrennung einer Kerze? Diese Frage versuchen wir in diesem Kapitel zu beantworten. Schauen
Verbrennung einer Kerze Zünde eine Kerze an und notiere deine Beobachtungen: Was passiert eigentlich genau bei der Verbrennung einer Kerze? Diese Frage versuchen wir in diesem Kapitel zu beantworten. Schauen
Protokoll Checker I: INHALT UND FACHLICHKEIT. Dieser Protokoll Checker gehört:
 I: INHALT UND FACHLICHKEIT I1 Das ist fachlich nicht richtig. Durchdenke das Eperiment nochmal Schritt für Schritt. Schlage zur Kontrolle im Schulbuch nach oder frage deine Mitschüler/innen. I2 Hier fehlt
I: INHALT UND FACHLICHKEIT I1 Das ist fachlich nicht richtig. Durchdenke das Eperiment nochmal Schritt für Schritt. Schlage zur Kontrolle im Schulbuch nach oder frage deine Mitschüler/innen. I2 Hier fehlt
Die Brandbekämpfung (Gruppenversuche)
 Die Brandbekämpfung (Gruppenversuche) Führt die folgenden Versuche nacheinander durch. Lest die Versuchsbeschreibungen (Kopie) genau durch und klebt sie sofort in eure Haushefte ein. Notiert mit Bleistift
Die Brandbekämpfung (Gruppenversuche) Führt die folgenden Versuche nacheinander durch. Lest die Versuchsbeschreibungen (Kopie) genau durch und klebt sie sofort in eure Haushefte ein. Notiert mit Bleistift
1.5 X - Y ungelöst? Welcher Stoff wird hier gesucht?
 1.5 X - Y ungelöst? Welcher Stoff wird hier gesucht? X ist gelb und fest, nicht in Wasser löslich. Beim Verbrennen bildet X ein giftiges stechend riechendes Gas. In der Natur kommt X rein oder als vulkanische
1.5 X - Y ungelöst? Welcher Stoff wird hier gesucht? X ist gelb und fest, nicht in Wasser löslich. Beim Verbrennen bildet X ein giftiges stechend riechendes Gas. In der Natur kommt X rein oder als vulkanische
Wenn es glüht und leuchtet: Wie erklärt die Chemie Feuer und Flamme. Roger Alberto und Heinz Spring Institut für Chemie, Universität Zürich
 Wenn es glüht und leuchtet: Wie erklärt die Chemie Feuer und Flamme Kinderuni Hochrhein Roger Alberto und Heinz Spring Institut für Chemie, Universität Zürich 27. Januar 2016 KHR-1 KHR-1 KHR-2 Feuer und
Wenn es glüht und leuchtet: Wie erklärt die Chemie Feuer und Flamme Kinderuni Hochrhein Roger Alberto und Heinz Spring Institut für Chemie, Universität Zürich 27. Januar 2016 KHR-1 KHR-1 KHR-2 Feuer und
Inhalt. WAS IST CHEMIE? Stoffe mit Messinstrumenten unterscheiden 28 STOFFGEMISCHE 46 STOFFEN AUF DER SPUR 20
 Inhalt WAS IST CHEMIE? Stoffe mit Messinstrumenten unterscheiden 28 Ordnen von Stoffen 30 Selbst untersucht Wasser als Lösemittel 32 Lösemittel Wasser 34 Saure und alkalische Lösungen 36 Selbst untersucht
Inhalt WAS IST CHEMIE? Stoffe mit Messinstrumenten unterscheiden 28 Ordnen von Stoffen 30 Selbst untersucht Wasser als Lösemittel 32 Lösemittel Wasser 34 Saure und alkalische Lösungen 36 Selbst untersucht
Nachholschulaufgabe aus der Chemie
 Nachholschulaufgabe aus der Chemie 1. In einer Kneipe findet man auf der Getränkekarte die Spezialität des Hauses: einen rostigen Nagel. Er besteht aus Pfefferpulver und Chilistückchen in Olivenöl, aufgefüllt
Nachholschulaufgabe aus der Chemie 1. In einer Kneipe findet man auf der Getränkekarte die Spezialität des Hauses: einen rostigen Nagel. Er besteht aus Pfefferpulver und Chilistückchen in Olivenöl, aufgefüllt
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Die Außerirdischen sind da! - Eine Einführung ins Thema Verbrennung
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die Außerirdischen sind da! - Eine Einführung ins Thema Verbrennung Das komplette Material finden Sie hier: School-Scout.de V Chemische
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die Außerirdischen sind da! - Eine Einführung ins Thema Verbrennung Das komplette Material finden Sie hier: School-Scout.de V Chemische
Untersuche die Kerzenflamme sowie die Vorgänge, die beim Verbrennen des Kerzenwachses ablaufen.
 Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P7154200) 2.10 Die Kerzenflamme Experiment von: Seb Gedruckt: 24.03.2014 11:14:37 intertess (Version 13.12 B214, Export 2000)
Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P7154200) 2.10 Die Kerzenflamme Experiment von: Seb Gedruckt: 24.03.2014 11:14:37 intertess (Version 13.12 B214, Export 2000)
Protokoll: Gefärbte Rose
 Protokoll: Gefärbte Rose 1)Fragestellung: Wie wird in einer Pflanze bzw. Blume Wasser befördert und wohin? 2.) Hypothese: Die Blume nimmt die Farbe der Tinte auf und transportiert sie weiter. 3.) Material:
Protokoll: Gefärbte Rose 1)Fragestellung: Wie wird in einer Pflanze bzw. Blume Wasser befördert und wohin? 2.) Hypothese: Die Blume nimmt die Farbe der Tinte auf und transportiert sie weiter. 3.) Material:
Die Wirkung von Wärme und Kälte auf Stoffe oder Alles nur heiße Luft?
 Kurzinformation Lehrkräfte (Sachanalyse) Die Wirkung oder Sachanalyse Naturwissenschaftlich betrachtet ist alles, was eine beobachtbare Masse besitzt, ein Stoff. Alle Körper/Gegenstände bestehen demnach
Kurzinformation Lehrkräfte (Sachanalyse) Die Wirkung oder Sachanalyse Naturwissenschaftlich betrachtet ist alles, was eine beobachtbare Masse besitzt, ein Stoff. Alle Körper/Gegenstände bestehen demnach
Steckbrief von Sauerstoff, O 2
 Steckbrief von Sauerstoff, O 2 farblos, d.h. unsichtbar, nur in sehr dicken Schichten himmelblau geruch- und geschmacklos - Etwas schwerer als Luft - notwendig für die Verbrennung, brennt aber nicht selbst
Steckbrief von Sauerstoff, O 2 farblos, d.h. unsichtbar, nur in sehr dicken Schichten himmelblau geruch- und geschmacklos - Etwas schwerer als Luft - notwendig für die Verbrennung, brennt aber nicht selbst
Illustrierende Aufgaben zum LehrplanPLUS. Gymnasium, Natur und Technik (Schwerpunkt Biologie), Jahrgangsstufe 6. Keimung
 Keimung Jahrgangsstufen 6 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Natur und Technik (Schwerpunkt Biologie) --- Aus den nachfolgenden Aufgaben kann je nach Zeitrahmen, Unterrichtszielen
Keimung Jahrgangsstufen 6 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Natur und Technik (Schwerpunkt Biologie) --- Aus den nachfolgenden Aufgaben kann je nach Zeitrahmen, Unterrichtszielen
Experimente mit Feuer in der Sek. 1
 in der Sek. 1 Workshop im Forum Brandschutzerziehung und Brandschutzaufklärung Celle 2. April 2011 Dr. Doris Schmidt Es gibt Vorführexperimente...wie diese Fettexplosion und es gibt Schülerexperimente...wie
in der Sek. 1 Workshop im Forum Brandschutzerziehung und Brandschutzaufklärung Celle 2. April 2011 Dr. Doris Schmidt Es gibt Vorführexperimente...wie diese Fettexplosion und es gibt Schülerexperimente...wie
Arbeitsblatt Ist groß besser als klein?
 Arbeitsblatt Ist groß besser als klein? Aufgabe 1: Führe folgendes Experiment durch und notiere deine Beobachtungen. Materialien: 4 Reagenzgläser, Reagenzglasständer, Spatel Chemikalien: Gefahrenstoffe
Arbeitsblatt Ist groß besser als klein? Aufgabe 1: Führe folgendes Experiment durch und notiere deine Beobachtungen. Materialien: 4 Reagenzgläser, Reagenzglasständer, Spatel Chemikalien: Gefahrenstoffe
D1 Abhängigkeit der Reaktionsgeschwindigkeit von der Temperatur
 Chemische Reaktionen verlaufen nicht alle mit der gleichen Geschwindigkeit. Sehr schnelle Reaktionen, wie z.b. die Neutralisationsreaktion oder die Knallgasreaktion erfolgen in Bruchteilen einer Sekunde.
Chemische Reaktionen verlaufen nicht alle mit der gleichen Geschwindigkeit. Sehr schnelle Reaktionen, wie z.b. die Neutralisationsreaktion oder die Knallgasreaktion erfolgen in Bruchteilen einer Sekunde.
Wovon hängt das Reaktionsverhalten der Metalle beim Erhitzen an Luft ab?
 Naturwissenschaften - Chemie - Anorganische Chemie - Metalle (P75300).2 Abhängigkeit des Reaktionsverhaltens von Metallen Experiment von: Phywe Gedruckt:.0.203 5:7:52 intertess (Version 3.06 B200, Export
Naturwissenschaften - Chemie - Anorganische Chemie - Metalle (P75300).2 Abhängigkeit des Reaktionsverhaltens von Metallen Experiment von: Phywe Gedruckt:.0.203 5:7:52 intertess (Version 3.06 B200, Export
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 2001/2002 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 2001/2002 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
LB1 Stoffe. LB1 Stoffe. LB1 Stoffe. Womit beschäftigt sich die Chemie?
 Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht?
 Posten 1a Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht? a) es entsteht Wasserdampf (Wassertropfen kondensieren am Streifen) (=> Posten 5l) b) der Schwefeldampf wird
Posten 1a Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht? a) es entsteht Wasserdampf (Wassertropfen kondensieren am Streifen) (=> Posten 5l) b) der Schwefeldampf wird
Verbrennung von Eisenwolle und Holz
 Name: Datum: Versuch: Verbrennung von Eisenwolle und Holz Geräte: 1 Stativ 2 Muffen 2 Klemmen 1 Laborboy (hier Holzklotz) 1 Porzellanschale 1 Analysetrichter 1 Gaswaschflasche 1 Wasserstrahlpumpe 1 Gummischlauch
Name: Datum: Versuch: Verbrennung von Eisenwolle und Holz Geräte: 1 Stativ 2 Muffen 2 Klemmen 1 Laborboy (hier Holzklotz) 1 Porzellanschale 1 Analysetrichter 1 Gaswaschflasche 1 Wasserstrahlpumpe 1 Gummischlauch
Kapitel 1: Ich im Wir
 Kapitel 1: Ich im Wir So bin ich Gehe zu einem Mitschüler und tausche diese Seite mit ihm aus. Er soll dir ein Kompliment in deine Schatzkiste schreiben und du schreibst ihm ein Kompliment in seine Schatzkiste.
Kapitel 1: Ich im Wir So bin ich Gehe zu einem Mitschüler und tausche diese Seite mit ihm aus. Er soll dir ein Kompliment in deine Schatzkiste schreiben und du schreibst ihm ein Kompliment in seine Schatzkiste.
Schlüsselbegriffe. Übungsaufgaben:
 I. Energetik chemischer Reaktionen 1) Licht als Energieform 2) Wärme als Energieform 3) Elektrizität als Energieform 4) Die Triebkraft chemischer Reaktionen Schlüsselbegriffe 1. "Licht als Energieform":
I. Energetik chemischer Reaktionen 1) Licht als Energieform 2) Wärme als Energieform 3) Elektrizität als Energieform 4) Die Triebkraft chemischer Reaktionen Schlüsselbegriffe 1. "Licht als Energieform":
man sagt : Phosphor + Sauerstoff reagieren Tetraphosphorzu dekaoxid
 Die Luft 1.Versuch Wir entzünden eine Kerze und stülpen ein Becherglas darüber. Beobachtung : Nach kurzer Zeit erlischt die Flamme. Feststellung : Für die Verbrennung in unserer Umwelt ist Luft notwendig.
Die Luft 1.Versuch Wir entzünden eine Kerze und stülpen ein Becherglas darüber. Beobachtung : Nach kurzer Zeit erlischt die Flamme. Feststellung : Für die Verbrennung in unserer Umwelt ist Luft notwendig.
Kerncurriculum Chemie Eichsfeld-Gymnasium Duderstadt Juni 2012
 Kerncurriculum Chemie Eichsfeld-Gymnasium Duderstadt Juni 2012 Jahrgänge 7 und 8 Jeweils 1 Jahreswochenstunde pro Schuljahr (epochal, entspricht 40 Stunden pro Schuljahr). Basiskonzepte: BK1: Stoff-Teilchen;
Kerncurriculum Chemie Eichsfeld-Gymnasium Duderstadt Juni 2012 Jahrgänge 7 und 8 Jeweils 1 Jahreswochenstunde pro Schuljahr (epochal, entspricht 40 Stunden pro Schuljahr). Basiskonzepte: BK1: Stoff-Teilchen;
Die Kerzenflamme (Artikelnr.: P )
 Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
Lehrer-/Dozentenblatt Die Kerzenflamme (Artikelnr.: P7154200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Luft und Verbrennungen
4.3 Reaktionsgeschwindigkeit und Katalysator
 4.3 Reaktionsgeschwindigkeit und Katalysator Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Einstellung des Gleichgewichts,
4.3 Reaktionsgeschwindigkeit und Katalysator Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Einstellung des Gleichgewichts,
Die Einheit Mol Stoffmengen können in verschiedenen Einheiten gemessen werden:
 Cusanus-Gymnasium Wittlich W. Zimmer 1/5 Die Einheit Mol Stoffmengen können in verschiedenen Einheiten gemessen werden: a) durch die Angabe ihrer Masse b) durch die Angabe ihres Volumens c) durch die Anzahl
Cusanus-Gymnasium Wittlich W. Zimmer 1/5 Die Einheit Mol Stoffmengen können in verschiedenen Einheiten gemessen werden: a) durch die Angabe ihrer Masse b) durch die Angabe ihres Volumens c) durch die Anzahl
3.11 Zerlegung von Wasser durch Reduktionsmittel. Aufgabe. Aus welchen Elementen besteht Wasser?
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P755500) 3. Zerlegung von Wasser durch Reduktionsmittel Experiment von: Seb Gedruckt: 24.03.204 :42:33
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P755500) 3. Zerlegung von Wasser durch Reduktionsmittel Experiment von: Seb Gedruckt: 24.03.204 :42:33
Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt VORANSICHT
 V Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) 1 von 30 Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt Tobias Dunst, Kißlegg Welche Verbindung besteht zwischen dem mysteriösen
V Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) 1 von 30 Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt Tobias Dunst, Kißlegg Welche Verbindung besteht zwischen dem mysteriösen
0.1 Geschwindigkeit bei Reaktionen
 1 0.1 Geschwindigkeit bei Reaktionen Salzsäure reagiert mit Magnesium Erklärung 2HCl + Mg MgCl 2 + H 2 Das M g-pulver reagiert schneller mit der Salzsäure als die Mg-Späne. Definition: Reaktionsgeschwindigkeit
1 0.1 Geschwindigkeit bei Reaktionen Salzsäure reagiert mit Magnesium Erklärung 2HCl + Mg MgCl 2 + H 2 Das M g-pulver reagiert schneller mit der Salzsäure als die Mg-Späne. Definition: Reaktionsgeschwindigkeit
Fragen der Schüler der Birkenau-Volksschule
 Fragen der Schüler der Birkenau-Volksschule Warum gibt es Klima? Warum gibt es Wärme? Wissenschaftler können die tiefe Frage, warum es etwas überhaupt gibt, meist gar nicht beantworten. Wir befassen uns
Fragen der Schüler der Birkenau-Volksschule Warum gibt es Klima? Warum gibt es Wärme? Wissenschaftler können die tiefe Frage, warum es etwas überhaupt gibt, meist gar nicht beantworten. Wir befassen uns
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Stationenlernen: Licht und Optik. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 48292 Kurzvorstellung: Dieses Material beinhaltet sieben
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 48292 Kurzvorstellung: Dieses Material beinhaltet sieben
Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser"
 Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser" a) Identifizierung des entstehenden Gases: Chemikalien: Geräte: Lithium [C] [F], Natrium [C] [F] (jeweils in Benzin mit Siedebereich 90-110
Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser" a) Identifizierung des entstehenden Gases: Chemikalien: Geräte: Lithium [C] [F], Natrium [C] [F] (jeweils in Benzin mit Siedebereich 90-110
Arbeitsheft Organische Redoxreaktionen Inhalt Jakob 1 Inhaltsverzeichnis: Seite: Vorkenntnisse:
 Arbeitsheft Organishe Reoxreaktionen Inhalt Jakob Inhaltsverzeihnis: Seite: Vorkenntnisse: Bestimmung er OZ bei organishen Molekülen Arbeitsheft Reoxreaktionen Verbrennung von Kohlenwasserstoffen. Oxiation
Arbeitsheft Organishe Reoxreaktionen Inhalt Jakob Inhaltsverzeihnis: Seite: Vorkenntnisse: Bestimmung er OZ bei organishen Molekülen Arbeitsheft Reoxreaktionen Verbrennung von Kohlenwasserstoffen. Oxiation
Süsse Chemie. Untersuche Stoffeigenschaften und wandle Stoffe um.
 Stoffe. Süsse Chemie Untersuche Stoffeigenschaften und wandle Stoffe um. 1. Betrachte den Haushaltszucker auf allen Bildern sowie einen Würfelzucker vor dir. Woran erkennst du «Haushalts zucker»? 2. Beschreibe
Stoffe. Süsse Chemie Untersuche Stoffeigenschaften und wandle Stoffe um. 1. Betrachte den Haushaltszucker auf allen Bildern sowie einen Würfelzucker vor dir. Woran erkennst du «Haushalts zucker»? 2. Beschreibe
Echt ätzend! - Was ist und wie wirkt Abflussreiniger?
 Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
Erwartete Kompetenzen. Kompetenzbereich Erkenntnisgewinnung Die Schülerinnen und Schüler E1 E2 E3 E4 E5 E6 E7 E8 E9 E10 E11 E12 E13 E14 E15 E16 E17
 Stoffverteilungsplan Kerncurriculum für die Oberschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1 Lehrer:
Stoffverteilungsplan Kerncurriculum für die Oberschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1 Lehrer:
Schulversuchspraktikum. Stefan Krüger. SoSe 2014. Klassenstufen 5/6. Feuer und Kerzen
 0 Schulversuchspraktikum Stefan Krüger SoSe 2014 Klassenstufen 5/6 Feuer und Kerzen 1 Auf einen Blick: In diesem Protokoll werden verschiedene Aspekte des (Kerzen-)Feuers anhand ausgewählter Experimente
0 Schulversuchspraktikum Stefan Krüger SoSe 2014 Klassenstufen 5/6 Feuer und Kerzen 1 Auf einen Blick: In diesem Protokoll werden verschiedene Aspekte des (Kerzen-)Feuers anhand ausgewählter Experimente
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat
 1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat Geräte/Chemikalien: Mörser mit Pistill, feuerfeste Unterlage, Zucker, Kaliumnitrat, Zünder: Kaliumpermanganat
1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat Geräte/Chemikalien: Mörser mit Pistill, feuerfeste Unterlage, Zucker, Kaliumnitrat, Zünder: Kaliumpermanganat
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 1999/ Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 1999/ Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Untersuche die ausgegebenen Stoffe auf Brennbarkeit und Schmelztemperatur.
 Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt: 07.2.205 :7:33 intertess (Version
Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt: 07.2.205 :7:33 intertess (Version
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt für die Klassen 5 bis 6: Temperatur und Wärme
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 5 bis 6: Temperatur und Wärme Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Lernwerkstatt
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 5 bis 6: Temperatur und Wärme Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Lernwerkstatt
Warum korrodiert Eisen?
 Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Abschlusstest der Unterrichtseinheit Astronomische Entfernungsbestimmung
 Abschlusstest der Unterrichtseinheit Astronomische sbestimmung Codename: Expertengruppe: 1. Vielleicht haben Sie nun eine Vorstellung über Größen und en im Sonnensystem: Stellen Sie sich vor, die Sonne
Abschlusstest der Unterrichtseinheit Astronomische sbestimmung Codename: Expertengruppe: 1. Vielleicht haben Sie nun eine Vorstellung über Größen und en im Sonnensystem: Stellen Sie sich vor, die Sonne
Übung 4. SS 2013 Übung - Einführung in die Verbrennung - Methling, Özuylasi 1
 Ziel: Grundlagen der chemischen Reaktionskinetik verstehen Verstehen qualitativer Reaktionsverläufe Aufstellung des Zeitgesetzes Umgang mit nicht reagierenden Stoßpartner (M) Berechnung Geschwindigkeitskoeffizient
Ziel: Grundlagen der chemischen Reaktionskinetik verstehen Verstehen qualitativer Reaktionsverläufe Aufstellung des Zeitgesetzes Umgang mit nicht reagierenden Stoßpartner (M) Berechnung Geschwindigkeitskoeffizient
Kompetenzerwartungen/ Medienkompetenz
 Internes Schulcurriculum HGE Chemie 8 Insgesamt ca. 60 h Kontext/Aspekte von Unterrichtsvorhaben 1. Die Welt der Metalle 16 h Inhaltsfelder und Schwerpunkte Metalle und Metallgewinnung Das Rosten eine
Internes Schulcurriculum HGE Chemie 8 Insgesamt ca. 60 h Kontext/Aspekte von Unterrichtsvorhaben 1. Die Welt der Metalle 16 h Inhaltsfelder und Schwerpunkte Metalle und Metallgewinnung Das Rosten eine
Feuerwehr Riegelsberg
 Feuerwehr Riegelsberg Brennen und Löschen Anlage zur Versuchsreihe Erstellt: Jörg Klein Folie 1 Löschmittel der Feuerwehr Wasser Schaum Pulver Kohlendioxid CO 2 Sonstige Sand Graugußspäne Zement u.a. Erstellt:
Feuerwehr Riegelsberg Brennen und Löschen Anlage zur Versuchsreihe Erstellt: Jörg Klein Folie 1 Löschmittel der Feuerwehr Wasser Schaum Pulver Kohlendioxid CO 2 Sonstige Sand Graugußspäne Zement u.a. Erstellt:
Bundesrealgymnasium Imst. Chemie 2010-11. Klasse 4. Chemische Reaktionen
 Bundesrealgymnasium Imst Chemie 2010-11 Klasse 4 Chemische Reaktionen Inhalt 6 Chemische Reaktionen... 18 6.1 Reaktionsgleichungen... 18 6.2 Mol, molare Masse... 19 6.3 Säuren und Laugen... 19 6.4 Neutralisationsreaktionen...
Bundesrealgymnasium Imst Chemie 2010-11 Klasse 4 Chemische Reaktionen Inhalt 6 Chemische Reaktionen... 18 6.1 Reaktionsgleichungen... 18 6.2 Mol, molare Masse... 19 6.3 Säuren und Laugen... 19 6.4 Neutralisationsreaktionen...
Eigenschaften Reinstoffe Elemente Kugelteilchen Elementes Atom
 Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Wasser-Woche in der Klasse 2a
 Wasser-Woche in der Klasse 2a Zu Beginn der Wasserwoche haben wir uns überlegt, was wir schon über Wasser wissen und was wir gerne noch wissen möchten. All das haben wir auf große blaue Papiertropfen geschrieben.
Wasser-Woche in der Klasse 2a Zu Beginn der Wasserwoche haben wir uns überlegt, was wir schon über Wasser wissen und was wir gerne noch wissen möchten. All das haben wir auf große blaue Papiertropfen geschrieben.
Reaktionen von Metallen mit Sauerstoff und mit Luft
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
LUFT CHEMIE DER VERBRENNUNG (SEKP)
 1 KSO LUFT CHEMIE DER VERBRENNUNG (SEKP) Skript Luft Chemie der Verbrennung (SekP) V1.0 04/15 Bor 2 INHALTSVERZEICHNIS "LUFT CHEMIE DER VERBRENNUNG" 1. Einleitung...03 2. Reaktionspartner Luft... 03 3.
1 KSO LUFT CHEMIE DER VERBRENNUNG (SEKP) Skript Luft Chemie der Verbrennung (SekP) V1.0 04/15 Bor 2 INHALTSVERZEICHNIS "LUFT CHEMIE DER VERBRENNUNG" 1. Einleitung...03 2. Reaktionspartner Luft... 03 3.
1.1 Oxidation von Metallen. Aufgabe. Wie verändern sich Metalle beim Erhitzen? Naturwissenschaften - Chemie - Anorganische Chemie - 1 Metalle
 Naturwissenschaften - Chemie - Anorganische Chemie - Metalle (P753000). Oxidation von Metallen Experiment von: Phywe Gedruckt:.0.203 5:6:40 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe Wie
Naturwissenschaften - Chemie - Anorganische Chemie - Metalle (P753000). Oxidation von Metallen Experiment von: Phywe Gedruckt:.0.203 5:6:40 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe Wie
mischbar Lösung Feststoffen
 Kristalle züchten Mischen und Lösen - Nicht alle Stoffe sind miteinander mischbar. --> Hexan (Bestandteil von Benzin) und Wasser --> Hast du Beispiele aus dem Alltag? - Kann man die Stoffe nach dem Mischen
Kristalle züchten Mischen und Lösen - Nicht alle Stoffe sind miteinander mischbar. --> Hexan (Bestandteil von Benzin) und Wasser --> Hast du Beispiele aus dem Alltag? - Kann man die Stoffe nach dem Mischen
Anhand welcher Eigenschaften lässt sich Wasserstoff identifizieren?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75500) 5.2 Nachweis von Wasserstoff Experiment von: Phywe Gedruckt:.0.203 3:02:34 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75500) 5.2 Nachweis von Wasserstoff Experiment von: Phywe Gedruckt:.0.203 3:02:34 intertess (Version 3.06 B200, Export 2000) Aufgabe
Reaktion von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad
 Schulversuchspraktikum Name: Philie Kiecksee Semester: SS2012 Klassenstufen 7&8 Reaktion von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad Auf einen Blick: Das Protokoll stellt eine Sammlung von
Schulversuchspraktikum Name: Philie Kiecksee Semester: SS2012 Klassenstufen 7&8 Reaktion von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad Auf einen Blick: Das Protokoll stellt eine Sammlung von
Die freie Energie wird also bei konstantem Volumen und konstanter Temperatur minimal
 Die freie Energie wird also bei konstantem Volumen und konstanter Temperatur minimal 7.2 Die Enthalpie Die Enthalpie H ist definiert als H = U + pv, womit wir für die Änderung erhalten dh = pdv + TdS +
Die freie Energie wird also bei konstantem Volumen und konstanter Temperatur minimal 7.2 Die Enthalpie Die Enthalpie H ist definiert als H = U + pv, womit wir für die Änderung erhalten dh = pdv + TdS +
10. Versuch: Schiefe Ebene
 Physikpraktikum für Pharmazeuten Universität Regensburg Fakultät Physik 10. Versuch: Schiefe Ebene In diesem Versuch untersuchen Sie Mechanik der schiefen Ebene, indem Sie mithilfe dem statischen und dynamischen
Physikpraktikum für Pharmazeuten Universität Regensburg Fakultät Physik 10. Versuch: Schiefe Ebene In diesem Versuch untersuchen Sie Mechanik der schiefen Ebene, indem Sie mithilfe dem statischen und dynamischen
[FREIER FALL MIT UND OHNE LUFTWIDERSTAND] 10. Oktober 2010
![[FREIER FALL MIT UND OHNE LUFTWIDERSTAND] 10. Oktober 2010 [FREIER FALL MIT UND OHNE LUFTWIDERSTAND] 10. Oktober 2010](/thumbs/41/22511000.jpg) Inhalt Freier Fall ohne Luftwiderstand... 1 Herleitung des Luftwiderstandes... 3 Freier Fall mit Luftwiderstand... 4 Quellen... 9 Lässt man einen Körper aus einer bestimmt Höhe runter fallen, so wird er
Inhalt Freier Fall ohne Luftwiderstand... 1 Herleitung des Luftwiderstandes... 3 Freier Fall mit Luftwiderstand... 4 Quellen... 9 Lässt man einen Körper aus einer bestimmt Höhe runter fallen, so wird er
!!! Du darfst eine Teilaufgabe von Nr. 2 und zwei der Teilaufgaben von Nr 4 streichen!!!
 1 Klassenarbeit Chemie 1/5 A TIPP alle Rechenaufgaben mit Einheit, Ergebnis und Antwortsatz! In der Tabelle links stehende Elemente haben eher die maximale Wertigkeit! In der Tabelle rechts stehende Elemente
1 Klassenarbeit Chemie 1/5 A TIPP alle Rechenaufgaben mit Einheit, Ergebnis und Antwortsatz! In der Tabelle links stehende Elemente haben eher die maximale Wertigkeit! In der Tabelle rechts stehende Elemente
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 Einteilung der Stoffe: Stoff Reinstoff Mischen Gemisch Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b. Farbe,
Einteilung der Stoffe: Stoff Reinstoff Mischen Gemisch Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b. Farbe,
Entscheide bei jeder Aussage, ob es eine reine Beobachtung ist oder nicht, und kreuze an!
 Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
4. Chemische Reaktion
 Chemie GU 9 4. Chemische Reaktion 4.1 Stoffe wandeln sich um Aus Kupfer und Schwefel entsteht ein neuer Stoff Metalle reagieren mit Schwefel zu Metallsulfiden o Edukte und Produkte Das Reaktionsschema
Chemie GU 9 4. Chemische Reaktion 4.1 Stoffe wandeln sich um Aus Kupfer und Schwefel entsteht ein neuer Stoff Metalle reagieren mit Schwefel zu Metallsulfiden o Edukte und Produkte Das Reaktionsschema
