Stereochemie. Vorlesung SS 2003 FU-Berlin Professor M. Kalesse
|
|
|
- Reiner Braun
- vor 7 Jahren
- Abrufe
Transkript
1 Stereochemie Vorlesung SS 2003 FU-Berlin Professor M. Kalesse
2 Einführung in die Stereochemie 1) Molekulare Konnektivität beschreibt, in welcher Reihenfolge die Atome einer Substanz miteinander verbunden sind. 2) Verbindungen mit identischer Summenformel aber unterschiedlicher Konnektivität nennt man Isomere. Z.B. für C 2 6 : C 3 C 2 oder C 3 C 3 3) Verbindungen mit identischer Konnektivität aber unterschiedlicher Anordnung der Atome im Raum werden Stereoisomere genannt.
3 Verschiedene Isomere Isomere Konstitutions-Isomere Stereoisomere Diastereomere (keine Spiegelbilder) Enantiomere (Spiegelbilder) cis-trans-diastereomere Konfigurations-Diastereomere
4 Einführung in die Stereochemie 1) Zwei Strukturen werden Enantiomere genannt, wenn sie Spiegelbilder von einander darstellen, die nicht zur Deckung gebracht werden können. F Cl Br Cl Br F 2) Zwei Strukturen werden Diastereomere genannt, wenn es Stereoisomere sind und sie keine nicht-zur- Deckung-gebrachte-Spiegelbilder (Enantiomere) voneinander darstellen. 3 C C 3 und 3 C und Weinsäure C 3 Buten
5 Symmetrieoperationen Was sind Symmetrieoperationen? Eine Symmetrieoperation ist eine Manipulation einer Struktur, bei der äquivalente Bereiche ausgetauscht werden. Nach einer Symmetrieoperation ist die Verbindung identisch mit der Verbindung vor der Symmetrieoperation. z x y C Drehung um 120 um die z-achse C Wenn man die Augen während einer Symmetrieoperation schließt, lässt sich nicht feststellen, ob überhaupt eine Symmetrieoperation stattgefunden hat. 180 Drehung um die X-Achse Symmetrieoperation 180 Drehung um die Z-Achse keine Symmetrieoperation
6 Symmetrieoperationen 1. Rotation: 1, Rotation um eine Achse (von 0 bis 360 ) 2. Spiegelung: Spiegelung in einer Ebene, die durch die Struktur verläuft 3. Inversion aller Atome durch einen zentralen Punkt: Die peration verändert alle Punkte (x, y, z) zu (-x, -y, -z) 4. Rotation-Reflektion: 1Wiederholungen der folgenden perationen: Rotation um eine Achse, dann Reflektion in einer Ebene senkrecht zur Rotationsachse Anwendung dieser perationen auf molekulare Strukturen Ein Symmetrieelement ist eine geometrische Einheit (Punkt, Linie, Ebene), an welcher die Symmetrieoperation durchgeführt wird. Achse, um welche die Symmetrieoperation (Rotation um 120 ) durchgeführt wurde. C C
7 Symmetrieoperationen und Symmetrieelemente Symmetrieelement Symmetrieoperation 1. Drehachse = C n n Drehungen von (360 /n) 2. Spiegelebene = σ Spiegelung an einer Ebene 3. Inversionszentrum = i Inversion 4. Dreh-Spiegel-Achse = S n n Wiederholungen von: Drehungen um (360 /n) dann Spiegelung an einer Ebene senkrecht zur Achse
8 Beispiele der C n -Symmetrie z 1. C 4 y x 4 C 3 -Achsen (Drehung um 120 ) C C 3 C 2 Achsen (Drehung um 180 ) z 2. C C 2 Achsen y 3. C 2 2 unendliche Zahl C 2 Achsen C x
9 Beispiele für Spiegelebenen z 1. C 4 6 σ-ebenen (jede mit einem C und zwei ) C 2. C σ-ebenen (jeweils senkrecht zueinander) x y 3. C σ-ebenen und zusätzlich eine unendliche Anzahl von Spiegelebenen (σ) durch alle 4 Atome des Moleküls
10 Beispiele für Inversionszentren 1. C C C 2 2
11 Beispiele für S-Symmetrie 1) C 4 hat 3 S 4 -Achsen. Drehung um eine 4- zählige Drehachse, dann Spiegelung senkrecht zur Achse. C 90 C S 4 C Spiegelung C 2) S 1 = σ, die erste Rotation ergibt wieder das Ausgangsmolekül. b a C d c 360 b a C d c Spiegelung b a C c d 3) S 2 = i, Eine 2-zählige Drehspiegelachse entspricht einem Inversionszentrum. a2 a1 a3 b1 b2 b3 180 (Y) a3 a2 a1 b2b3 b1 Spiegelung b2 b3 b1 a3 a2 a1
12 Wann sind Moleküle chiral? Generalisierung: 1. Moleküle mit einer Spiegelebene (σ) oder einem Inversionszentrum (i) sind achiral! Merke: Das sind Sonderfälle der S 1 -und S 2 -Achsen. 2. Moleküle mit einer Drehspiegelachse (S n ) sind achiral! 3. Moleküle ohne S n -Achse sind chiral! 4. Chirale Moleküle können Drehachsen (C n ) besitzen!!!! 5. Moleküle ohne Symmetrieelement werden asymmetrisch oder chiral genannt. Br F Cl F Cl Br achiral (σ- und C 2 -Symmetrie) Cl F achiral (σ-symmetrie) Cl F achiral (i-symmetrie) Weinsäure chiral (C 2 -Symmetrie) 3 C C 3 chiral (C 2 -Symmetrie) Me Me
13 Was sind chirale Moleküle? 1) Moleküle mit einem chiralen Zentrum: Ein Chiralitätszentrum ist ein Atom (meistens ein C-Atom) mit vier verschiedenen Substituenten; auch oft stereogenes Zentrum genannt. Achtung: Jedes Chiralitätszentrum ist auch immer ein stereogenes Zentrum. Aber ein stereogenes Zentrum muss nicht unbedingt ein Chiralitätszentrum sein. Ein streogenes Zentrum ist dadurch definiert, dass der Positionstausch von zwei Substituenten ein Enantiomer oder Diastereomer erzeugt. Beispiele: Chirale Verbindung mit Chiralitätszentren (stereogenen Zentren) C2 und C3 sind Chiralitätszentren oder auch stereogene Zentren. Das Molekül ist chiral. Weinsäure meso-weinsäure C2 und C3 sind Chiralitätszentren oder auch stereogene Zentren. Aber: Das Molekül ist achiral. Meso-Verbindungen sind achirale-verbindungen mit mehr als einem Chiralitätszentrum aufgrund der internen Symmetrie. ier: Ein Beispiel für ein Inversionszentrum (i, bzw. S 2 ) oder eine Spiegelebene nach Rotation. meso-weinsäure i = S 2 Rotation Spiegelebene (S 1 )
14 Stereogene Zentren Cl Cl F Austausch von 2 Substituenten am stereogenen Zentrum Cl Cl F Stereogenes Zentrum Achirale Verbindung (Spiegelebene); das stereogene Zentrum ist kein Chiralitätszentrum (zwei Substituenten sind identisch). Ebenfalls keine chirale Verbindung Die achirale Verbindung ist ein Diastereomer der ursprünglichen achiralen Verbindung.
15 Die Nomenklatur in der Stereochemie Messung der optischen Aktivität R/S- Nomenklatur nach Cahn-Ingold-Prelog D/L-Nomenklatur, Fischer-Projektion Stereochemie der Kohlenhydrate Mutarotation Der anomere Effekt
16 ptische Aktivität elektromagnetischer Feldvektor Meßzell mit chiraler Verbindung α Schwingungsebene des linear polarisierten Lichtes. Schwingungsebene des linear polarisierten Lichtes ist um den Winkel α gedreht. Die Ebene des linear-polarisierten Lichtes wird beim Durchstrahlen einer Lösung einer chiralen Verbindung um den Winkel α gedreht. Dieses Phänomen wird als optische Drehung bezeichnet; die betreffende Verbindung ist optisch aktiv. Ein Polarimeter benutzt meist eine monochromatische Natrium-D-Lampe (λ = 589 nm). Die spezifische Drehung einer chiralen Verbindung ist eine physikalische Konstante und wird wie folgt berechnet: [α] λ = α/l. c. [α] = spezifische Drehung; λ = Wellenlänge; α = beobachtete optische Drehung; Länge der Küvette in dm (meist 1 dm), Konzentration in g/ml.
17 R/S-Nomenklatur (für Moleküle mit Chiralitätszentrum) Die absolute Konfiguration von Chiralitätszentren wird durch die R/S-Nomenklatur angegeben. Zur Bestimmung der Konfiguration werden im ersten Schritt alle vier Substituenten an einem Zentralatom (Meistens Kohlenstoff) nach abnehmender Priorität geordnet. Diese Priorität wird an and von Sequenzregeln bestimmt. Die Priorität von Atomen entspricht ihrer Stellung im Periodensystem. D.h., Atome mit höherer rdnungszahl haben eine höhere Priorität. Im zweiten Schritt wird der Substituent mit der niedrigsten Priorität, meistens ein, vom Betrachter aus gesehen hinter dem Zentralatom (meistens ein C ) zu liegen kommt. In der Papierebene befinden sich nun drei, das Zentralatom umgebende Substituenten. Bewegt man sich von der höchsten über die mittlere zur niedrigsten Priorität dieser drei Substituenten im Uhrzeigersinn, so besitzt das Chiralitätszentrum eine R-Konfiguration. Bewegt man sich entgegen dem Uhrzeigersinn, so besitzt das Zentrum eine S- Konfiguration. 2. Cl 4. C 1. 3 C Br 3. "" nach hinten 3 C Cl C Br 1. S Achtung: Das Vorzeichen (+ oder -) bei der Drehung der Ebene des linear polarisierten Lichtes korreliert NICT mit den Symbolen R oder S!
18 D/L-Nomenklatur nach Fischer Einführung: I. Die Fischer-Projektion: In der Fischer-Projektion sind die waagerechten Linien auf den Betrachter zu gerichtet. Die senkrechten Linien weisen vom Betrachter weg. Glucose C II. Stereoisomere: 4 chirale Zentren, kein Symmetrieelement. 2 4 = 16 Aldohexosen-Stereoisomere. 8 diastereomere Paare von Enantiomeren. C R=D-Glucose 2-epi-Glucose = Mannose C C S = L-Glucose III. D/L-Nomenklatur: Die D/L-Nomenklatur für Monosaccharide definiert die absolute Konfigurationam höchst nummerierten chiralen Zentrum. Die Nomenklatur kann auch auf Aminosäuren angewandt werden. R D-Zucker (vom lat. Wort dexter für rechts) S L-Zucker (vom lat. Wort laevus für links) Nützliche Links: Kohlenhydratstrukturen;
19 R/S-Nomenklatur der Mosher-Ester und Mosher-Säurechloride Me Ph R CF 3 Ph Me S CF 3 Durch Prioritätsumkehr entsteht aus dem (R)-Säurechlorid der (S)-Ester (und umgekehrt). Me Ph R R CF 3 R Ph Me S CF 3 Vergleich der D/L- mit R/S-Nomenklatur bei Aminosäuren Me Ph Cl S CF 3 Cl Ph Me R CF 3 3 N C 2 R L-(S) L-Aminosäure in fast allen Fällen auch (S) aber C 2 3 N L-(R) S Cystein Cystein ist eine natürliche L-Aminosäure aber (R) durch Prioritätsumkehr
20 Stereochemie - Kohlenhydrate Monosaccharide Aldosen Fischer-Projektion in der D-Serie der Aldosen. E. Fischer: Bestimmung der relativen Konfiguration aller exosen. Erythrose C C D-Glycerinaldehyd C C C C C Ribose Arabinose Xylose Lyxose Threose C C C C C C C C Allose Altrose Glucose Mannose Gulose Idose Galactose Talose
21 Stereochemie - Kohlenhydrate Monosaccharide Ketosen Fischer-Projektion in der D-Serie der Ketosen. Erythrulose Ribulose Xylulose Psicose Fructose Sorbose Tagatose
22 Stereochemie - Kohlenhydrate Mutarotation: Einstellung eines Gleichgewichtes der Anomeren über eine offenkettigen Zwischenstufe. Allgemeine Säuren-Basen-Katalyse. B B B B
23 Stereochemie - Kohlenhydrate Der thermodynamische anomere Effekt α-glycosylbindungen sind auf Grund von n-σ* Wechselwirkungen stabilisiert. Als stereochemische Konsequenz ergibt sich daraus ein höherer Anteil des α- Anomer. Auf Grund der Delokalisierung der nicht-bindenden Elektronenpaare in das σ*-rbital wird eine C--Bdg. verkürzt und der Abstand der glycosidischen Bindung vergrößert. n-rbital Bindung wird kürzer (Doppelbindungsanteil) σ*-rbital Bindung wird länger
24 Stereochemie - Kohlenhydrate Stereochemie der Trichloracetimidat-Bildung - Der kinetische anomere Effekt β-glycosyloxid-anionen sind aufgrund des kinetischen anomeren Effektes stärker nucleophil als α-glycosyloxid-anionen. 1. ß-Glycoside sind sterisch leichter zugänglich (mehr Platz in der äquatorialen Position). 2. Wechselwirkungen zwischen Dipolen und freien Ionenpaaren destabilisieren das β-glycosyloxid-anion.
25 Stereochemie - Kohlenhydrate 1. Kinetische Bedingungen: β-trichloracetimidat (kinetischer anomerer Effekt) 2. Thermodynamische Bedingungen: α-trichloracetimidat (anomerer Effekt) Thermodynamisch Ac Ac Ac Ac K 2 C 3, Cl 3 CN, C 2 Cl 2, 48h, r.t. 98% Ac Ac Ac Ac N Kinetisch Ac Ac Ac Ac K 2 C 3, Cl 3 CN, C 2 Cl 2, 2h, r.t. 78% Ac Ac Ac Ac CCl 3 N CCl 3 Thermodynamisch Bn Bn Bn Bn K 2 C 3, Cl 3 CN, C 2 Cl 2, 48h, r.t. 78% Bn Bn Bn Bn N CCl 3 Kinetisch Bn Bn Bn Bn K 2 C 3, Cl 3 CN, C 2 Cl 2, 2h, r.t. 90% Bn Bn Bn Bn N CCl 3
26 Stereochemie - Kohlenhydrate Die Trichloracetimidat-Methode R R R R K 2 C 3, Cl 3 CN, C 2 Cl 2, 48h, r.t. 98% R R R R A N BF 3 A-, BF 3 R R R R A CCl 3 R R R R K 2 C 3, Cl 3 CN, C 2 Cl 2, 2h, r.t. 78% R R R R N CCl 3 A-, BF 3 BF 3 R R R R A A Kontrolle über das anomere Zentrum durch: 1. Nachbargruppen-Effekte (R = Ac, Bz, NAc: 1,2-trans-Konfiguration. 2. Keine Nachbargruppen-Effekte (R = Bn) a) Milde Lewis-Säure (BF 3 ) und tiefe Temperatur: Inversion an C1. b) Starke Lewis-Säure (TMSTf): Bildung der thermodynamischen Glycoside. c) Lösungsmittel-Effekte: Et 2 begünstigt die α-konfiguration; MeCN begünstigt die β-konfiguration.
27 Moleküle ohne Chiralitätszentrum - axiale Chiralität Axiale Chiralität C 3 3 C 3 C C 3 Me 1) Me Allene (C 2 -Symmetrie) 2) Bestimmung der R/S-Nomenklatur für Allene: 3) Me 2 Me Me 3 S a oder M R a oder P Die Methylgruppe hat eine höhere Priorität als das -Atom (wie bei der CIP-Nomenklatur). Man schaut entlang der C-C-Achse (Newman-Projektion) und dreht das Molekül derart, dass die Gruppe mit der niedrigsten Priorität nach unten und nach hinten zeigt. Man beginnt mit der vorderen Gruppe (unten) und geht dann zur Gruppe mit der höchsten Priorität am hinteren (oben) C-Atom. Dann zur niedrigeren Priorität. Entsprechen den CIP-Regeln wird mit Ra oder Sa (a für axiale Chiralität) oder M für minus und P für positiv (im Uhrzeigersinn) bezeichnet. 1 Me
28 Beispiele für axial-chirale Verbindungen in der Synthese R 1 Bu 3 Sn P C 3 + R 2 BF 3 R 2 R 1 R R 1 Zn Ms P C 3 + R 2 R 2 Ausgehend von chiralen Allenyl-Metall-Verbindungen können Lewis-Säure-katalysierte Additionen (Aldol-artig) an Aldehyde vorgenommen werden. Die Wahl des Metalls bestimmt den Übergangszustand (chelatisiert oder offenkettig) und damit die Diastereoselektivität der Reaktion (syn/anti). R 1 J.A. Marshall et al. J. rg. Chem. 1998, 63, J.A. Marshall et al. J. rg. Chem. 1998, 63, Ms Pd(PPh 3 ) 4 R 1 Synthese chiraler Allenyl-Metall-Verbindungen R R 1 Zn Ms C 3 R 1 L Pd L Ms Et 2 Zn C 3
29 Moleküle ohne Chiralitätszentrum - axiale Chiralität Die in diesen Beispielen vorliegende Art der axialen Chiralität, bei der es sich um eine gehinderte Drehbarkeit um eine Einfachbindung handelt, wird auch Atropisomerie (engl. Atropisomerism) genannt. Ein wichtiges Beispiel ist das BINL, ein Ligand für die enantioselektive Katalyse. 1',1-Binaphthol (BINL) 2,6,2',6'-substituierte Biphenyle Cl Cl R R (S)-1',1-Binaphthol (BINL) Bestimmung der CIP-Nomenklatur: Wie im Fall der Allene wird das Molekül derart gedreht, dass die Achse von oben nach unten verläuft. Dann wird am unteren Zentrum mit der Zählung begonnen. Dann dreht man zur höheren Priorität am oberen Zentrum und schließlich zur niedrigeren Priorität. Ra oder P bzw. Sa oder M S
30 Moleküle ohne Chiralitätszentrum - helikale Chiralität elizität ist die Chiralität aufgrund einer Schrauben-artigen Form des Moleküls. Gezeigt ist (M)-exahelicen. Zur Festlegung der Richtung können unsere ände benutzt werden. Dabei zeigt der Daumen nach unten in die Richtung der elix-achse. Die übrigen Finger sollten dann die Drehung in der vom Daumen angegebene Richtung der elix beschreiben. In dem hier vorliegenden Fall beschreibt nur die linke and korrekt die vorliegende elix. Daher ist es eine M-(minus) elix; oder auch linkshändige elix genannt. Rechtshändige elix = P (plus). Moleküle ohne Chiralitätszentrum - planare Chiralität CIP, Angew. Chem. 1966,78, ; Angew. Chem. Internat. Ed. Eng. 1966, 5, Planare Chiralität ist die Chiralität aufgrund eingeschränkter konformativer Flexibilität in gespannten Ringsystemen und der Anordnung von Substituenten außerhalb einer Ebene. Als Beispiel ist (E)-Cycloocten angeführt. In einem Achtring ist die E-Doppelbindung stabil, die Konformation jedoch bei Raumtemperatur fixiert. Daher können zwei verschiedene Enantiomere isoliert werden. Bestimmung der Chiralität: Die Doppelbindungsebene wird nach oben gelegt und dann bestimmt, in welche Richtungsich die Reste wegdrehen. Im linken Fall im Uhrzeigersinn (P oder R p ), im rechten Fall entgegen des Uhrzeigersinns (M oder S p ). (P) (M)
31 omotope Gruppen Im 1,3-Propandiol betrachten wir die beiden -Atome an C2. Werden beide -Atome jeweils durch ein Deuterium ersetzt, entstehen zwei neue Moleküle, die jedoch beide achiral sind und die ihre gegenseitigen Spiegelbilder darstellen. Man sagt, diese Atome sind homotopisch (engl. homotopic). b 2 a D a b identische Moleküle D Zwei Gruppen (hier -Atome) sind homotopisch, wenn sie durch eine C n -Drehachse ineinander überführbar sind. ier überführt eine C 2 -Achse die beiden -Atome ineinander.
32 eterotope Gruppen b a Die beiden -Atome sind NICT durch eine Rotation um eine C n -Achse austauschbar. D.h.: sie sind heterotopisch. Falls die beiden -Atome durch eine Spiegelebene, ein Inversionszentrum oder eine Drehspiegelung ineinander überführbar sind, werden sie enantiotopisch genannt. Anders: Wird jeweils ein -Atom gegen ein Deuterium ausgetauscht, handelt es sich um Enantiomere. Prochiralität: Wenn der Austausch einer Gruppe an einem C-Atom in einer achiralen Verbindung zu einer chiralen Verbindung führt, wird das betreffende C-Atom als prochirales C-Atom bezeichnet. b D D a Enantiomere
33 Diastereotope Gruppen b a a und b sind heterotopisch und können NICT durch eine Spiegelung, Inversion, Drehspiegelung oder Drehung ineinander überführt werden. Man nennt sie daher: Diastereotop der anders: Der Austausch eines -Atoms führt zu Diastereomeren. b D D a Diastereomere
34 Prochirale Flächen R Nu- R Nu Nu + R R Enantiomere R Ein trigonal planares Molekül hat zwei prochirale Flächen, wenn die Addition eines vierten Liganden ein chirales Molekül erzeugt. Die beiden Flächen sind enantiotope Flächen R R Nu Gegen den Uhrzeigersinn = si Fläche (engl. si face) Nu Im Uhrzeigersinn = re Fläche (engl. re face)
35 Dynamische Stereochemie Moleküle sind NICT statisch. Sie unterliegen Rotationen und Streckungen. Eine Konformation beschreibt die exakte Anordnung der Atome im Raum. Verschiedene Konformationen können durch Drehungen um Einfachbindungen ineinander überführt werden. Unter Konformationsanalyse versteht man die Abschätzung der relativen Energie-Werte verschiedener Konformationen eines Moleküls und deren Einfluss auf die chemischen Eigenschaften. Konformationsanalyse von Ethan: Jede ekliptische-anordnung (engl. eclipsed) zweier benachbarter -Atome führt zu einem Anstieg der relativen Energie um 1 kcal/mol. Daher hat die ekliptische-konformation eine um 3 kcal/mol höher Energie als die gestaffelte Konformation (engl. staggered). E rel = 0 (kcal/mol) Gestaffelte Konformation Ekliptische Konformation E rel = 3 (kcal/mol)
36 Ethan Konformation 60 gestaffelt: E rel = 0 (kcal/mol) 0 ekliptisch: E rel = 3 (kcal/mol) Jede der drei ekliptischen --Interaktionen trägt 1 kcal/mol zur Gesamtenergie bei. 3 kcal/mol
37 Butan Konformationen 180 C 3 C 3 Me/Me anti (0) C 3 3 C C 3 C 3 Me/ ekliptisch Gauche (+3,4), chiral, C 2 (+0,9), chiral, C C 3 3 C 3 C 3 C Me/ ekliptisch Gauche (+3,4), chiral, C 2 (+0,9), chiral, C CC 3 Me/Me ekliptisch (+6) Die beiden gauche- und Me/-ekliptischen Konformationen sind Spiegelbilder voneinander.
38 Beiträge der sterischen Spannung 1R R 2 R1 R2 Beitrag zur Energie 1,0 kcal/mol C 3 1,4 kcal/mol C 3 C 3 3,0 kcal/mol C 3 C 3 0 kcal/mol C 3 C 3 C 3 0 kcal/mol C 3 C 3 + 0,7 kcal/mol C 3 C 3 C kcal/mol offmann, R. W.; Angew. Chem. 1992, 104, ; Angew. Chem. Int. Ed. 1992, 31, ; offmann, R. W.; Angew. Chem. 2000, 112, ; Angew. Chem. Int. Ed. 2000, 39, Konformation in Lösung
39 Konformationsanalyse beim Cyclohexan R = äquatorial R R = axial R 3 R 6 6 anti äquatorial R 3 R gauche axial R Man schaut in Richtung der C1-C2-Bindung. Die gleiche Sichtweise ist ebenfalls in der Newman-Projektion dargestellt. Im äquatorialen Fall steht die R-Gruppe zu beiden älften des Ringes anti. Im axialen Fall kommt es zu zwei gauche-interaktionen und damit zu einer Erhöhung der Energie um zweimal 0,9 kcal/mol. Daher ist die axiale Position gegenüber der äquatorialen Position destabilisiert. Für R = Me wären das 1,8 kcal/mol.
40 Die A-Werte für Cyclohexane R G Der A-Wert = - G Für den Fall, dass R vorzugsweise äquatorial liegt, ist A positiv und somit G negativ. Je größer der Rest ist, um so größer ist der A-Wert. R R A-Werte (kcal/mol) -CC 0,45 -C 3 1,7 -C 2 C 3 1,8 -C(C 3 ) 2 2,2 -Si(C 3 ) 3 2,5 -C 6 5 2,8 -C(C 3 ) 3 4,8
41 Der Zusammenhang zwischen Energie und Selektivität Betrachtet wird die Transformation von A zu B oder C. A B oder C Thermodynamische Kontrolle: Selektivität = B/C = e (- G /RT) R = Gaskonstante (1,99 cal/mol K) T = Temperatur in Kelvin (Raumtemp. = 25 C, 298 K) Ein G von 1,4 kcal/mol ergibt ein Verhältnis von 10:1 für B/C. Ein G von 2,8 kcal/mol ergibt ein Verhältnis von 100:1 für B/C. Kinetische Kontrolle: Selektivität = B/C = e (- G+/RT) R = Gaskonstante (1,99 cal/mol K) T = Temperatur in Kelvin (Raumtemp. = 25 C, 298 K) Ein G + von 1,4 kcal/mol ergibt ein Verhältnis von 10:1 für B/C. Ein G + von 2,8 kcal/mol ergibt ein Verhältnis von 100:1 für B/C.
42 Thermodynamische oder kinetische Kontrolle 1) B und C sind Diastereomere E G + B A G + B - G + C = G + C wird schneller generiert. G + C G + bestimmt die kinetische Selektivität der Reaktion. In diesem Beispiel ist C das kinetische Produkt und B das Produkt thermodynamischer Kontrolle. Beide Wege können für die stereoselektive Synthese benutzt werden. C G C - G B = G B Reaktionskoordinate G bestimmt die thermodynamische Selektivität. Β ist das thermodynamische Loch. 2) B und C sind Enantiomere E G + B G + C A G + B - G + C = G + C wird schneller generiert. G + bestimmt die kinetische Selektivität der Reaktion. Lediglich die kinetische Kontrolle gibt Produktselektivität. B C
43 Thermodynamische Kontrolle oder kinetische Kontrolle Betrachtet wird die Transformation von A zu B oder C. A B oder C Die Produktverteilung wird von einem der folgenden zwei Faktoren beeinflusst: 1. Thermodynamische Kontrolle: Die Reaktionszusammensetzung und Produktverteilung wird durch die relative Energie der Produkte bestimmt. Um eine Reaktion unter thermodynamischer Kontrolle durchzuführen, müssen entweder a) die Produkte B und C reversibel A wiederherstellen können, oder b) B und C müssen in einem direkten Gleichgewicht stehen, welches nicht notwendiger Weise über A gehen muss. 2. Kinetische Kontrolle: Die Reaktions- und Produktverteilung wird von der Geschwindigkeit bestimmt, mit der B und C gebildet werden. Das Produkt, welches schneller gebildet wird, entsteht im Überschuß. Merke: 1) Diastereomere haben unterschiedliche Bildungsenthalpien. Wenn B und C Diastereomere sind, dann kann sowohl die kinetische Kontrolle als auch die thermodynamische Kontrolle zu Stereoselektivitäten führen. 2) Enantiomere haben identische Bildungsenthalpien: Wenn B und C Enantiomere sind, dann kann lediglich die kinetische Kontrolle zur stereoselektiven Bildung eines Enantiomeren führen.
44 Zusammenhang zwischen Temperatur und Selektivität G oder G + Temperatur Selektivität 1,4 kcal/mol 25 C 10:1 1,4 kcal/mol -25 C 17:1 1,4 kcal/mol -78 C 37:1 1,4 kcal/mol 25 C 10:1 1,1 kcal/mol -25 C 10:1 0,9 kcal/mol -78 C 10:1 Eine Temperaturerniedrigung erhöht die Selektivität einer Reaktion.
45 Es gibt verschiedene Formen, eine Reaktion zu beschreiben Betrachtet wird die Transformation von A zu B oder C. A B oder C Wir nehmen an, dass B und C Diastereomere sind und in einem Verhältnis von 3: 1 für B:C entstehen. Die Selektivität kann dann wie folgt wiedergegeben werden. a) Diastereomeren Verhältnis oder kurz er (engl. diastereomer ratio). Selektivität = B/C = 3:1 oder auch 75 : 25 b) Diastereoselektivität oder kurz ds (engl. diastereoselectivity) ier würde man von 75% Diastereoselektivität sprechen. c) % Diastereomerenüberschuss oder kurz %de (engl. diastereomeric excess) ier wären es 50%de %de = %auptprodukt - %Unterschussisomer = 75% - 25% =50% Für Enantiomere gelten die analogen Ausdrücke: Enantiomerenverhältnis, kurz er (engl. Enantiomeric ratio; Enantioselektivität, kurz es (engl. Enantioselectivity); Enantiomerenüberschuss oder %ee (engl. enantiomeric excess).
46 Stereochemische Kontrolle 1) Substrat-Kontrolle oder auch chirale Induktion: Die in einem Substrat vorhandenen chiralen Zentren können zum selektiven Aufbau neuer chiraler Zentren genutzt werden. Me Me Me Me B Me Me Me Me Me + TBS TBS + TBS C 61:39 Diastereoselektivität Roush et al. Acyclic Diastereoselective Synthesis Using Tartrate Ester Modified Crotylboronates. Double Asymmetric Reactions with a-methyl Chiral Aldehydes and Synthesis of the C(19)-C(29) Segment of Rifamycin S, J. Am. Chem. Soc. 1990, 112, ) Reagenz-Kontrolle: ier wird eine chirale ilfsgruppe eingeführt, und das so erzeugte chirale Enola kann selektiv alkyliert werden. Ph Me N Me Ph Me N Me R 1 Ph Me + N Me R 1 Meyers et al. Pseudoephedrine as a Practical Chiral Auxiliary for the Synthesis of ighly Enantiomerically Enriched Carboxylic Acid, Alcohols, Aldehydes and Ketones. J. Am.. Chem. Soc. 1997, 119,
47 Enzymatische kinetische Racemattrennung R 1 R 2 enantioselektive Veresterung R 1 R 2 + Ac R 1 R 2 enantioselektive hydrolyse Ac R 1 R 2 R1 R2 Biokatalysator ee% a: Alkyl Me ANL, CRL, ML, PPL b: C 2 C=CMe 2 Me PPL, PFL c: 4-MeC 6 4 Me PFL, SAMII 100 d: PhC=C Me Penicillin 85 acylase Andere Substrate, die über eine enzymatische Racemattrennung erhalten werden können. R 2 R 1 R 3 CR 4 Acyl Ph Boland et al. Esterolytic and Lipolytic Enzymes in rganic Synthesis. Synthesis, 1991,
48 Enzymatische Racemattrennung: Desymmetriesierung Enzymatische Veresterungen können symmetrische, achirale Verbindungen in eine einzige Enantiomeren-reine Verbindung überführen. Dabei beträgt die theoretische Ausbeute der Desymmetriesierung 100%. Meso-Verbindungen erzeugen dabei Produkte mit mehreren chiralen Zentren C 2 Ac Ac C 2 Me PLE or PPL 90-95% ee PFL (ydrolyse) 95% ee, 79% (ydrolyse) 98% ee, 98% Me 2 C Me C 2 (ydrolyse) 99% ee, 82% Bn Ac N N Bn PLE (ydrolyse) 92% ee, 76% C 2 C 2 Me (ydrolyse) 75% ee, 86% Johnson et al. Biotransformations in Synthesis of Enantiopure Bioactive Molecules, Acc. Chem. Res. 1998, 31,
49 Desymmetriesierung und Trennung Ac Ac PLE Ac + Ac meso p 7 Puffer < desymmetriesierung> langsame ydrolyse schnelle ydrolyse langsame ydrolyse schnelle ydrolyse Eine zweite ydrolyse des ersten kinetischen Alkohols führt zu einer Trennung der beiden mono-funktionalisierten Enantiomere. Der Enantiomerenüberschuß steigt mit fortschreitender Reaktion. Sih et al. Bifunctional Chiral Synthons via Biochemical Methods, J. Am. Chem. Soc. 1984, 106, 3695; Deardorff et al. Enantioselective ydrolysis of cis-3,5-diacetoxycyclopentene... rg. Synth. 1995, 73,
50 Desymmetriesierung und Racemattrennung: Chemische Methoden langsam Ti(iPr) 4 tbu (-)-DIPT + schnell langsam schnell plus threo-isomere top faces: enantiotopic bottom faces: enantiotopic left faces: diastereotopic right faces: diastereotopic Me (Ipc) 2 B 2 2 Na Me Schreiber et al. JACS 1987, 109, 1525.
4. Stereochemie. Das wichtigste Kriterium für Chiralität ist, dass sich Objekt und Spiegelbild nicht zur Deckung bringen lassen.
 4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
Konfigurationsisomerie
 Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Stereoisomerie. C 2 H 4 O 2 Schmelzpunkt 17 Grad Celcius
 3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
Grundlagen zum Verständnis chemischer Reaktionen = Handwerkszeug
 Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
- Punktsymmetriegruppe Gesamtheit aller Symmetrieelemente: Gruppentheorie
 195 14. Stereochemie Bereits am Anfang der Vorlesung einige Grundbegriffe: Konformation, Enantio- und Diastereomerie Jetzt nochmals systematisch und genauer a) Symmetrie und hiralität α) Symmetrieelemente
195 14. Stereochemie Bereits am Anfang der Vorlesung einige Grundbegriffe: Konformation, Enantio- und Diastereomerie Jetzt nochmals systematisch und genauer a) Symmetrie und hiralität α) Symmetrieelemente
Vokabular zur Stereochemie
 Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind!
 4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism ball de.svg OC I Lehramt F. H. Schacher 1 Stereoisomerie andere
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism ball de.svg OC I Lehramt F. H. Schacher 1 Stereoisomerie andere
b) Sauerstoff-Nucleophile: Wasser H 2 O => Hydrate
 b) Sauerstoff-Nucleophile: Wasser 2 => ydrate [ - ] [ + ] Basenkatalyse Säurekatalyse - + R 1 + R 2 + 2 + 2 -[ - ] -[ + ] Aldehydhydrat R 1 und/oder R 2 = Ketonhydrat R 1 und R 2 = Gleichgewichtslage:
b) Sauerstoff-Nucleophile: Wasser 2 => ydrate [ - ] [ + ] Basenkatalyse Säurekatalyse - + R 1 + R 2 + 2 + 2 -[ - ] -[ + ] Aldehydhydrat R 1 und/oder R 2 = Ketonhydrat R 1 und R 2 = Gleichgewichtslage:
OC 3 - Stereochemie. Allgemeine Hintergründe
 OC 3 - Stereochemie Allgemeine Hintergründe Einführung Folie Nr. 2 3-dimensionale Anordnung (relativ/absolut) in der realen Welt sind extrem wichtig Bild rechts: http://de.wikipedia.org/wiki/pfefferminz,
OC 3 - Stereochemie Allgemeine Hintergründe Einführung Folie Nr. 2 3-dimensionale Anordnung (relativ/absolut) in der realen Welt sind extrem wichtig Bild rechts: http://de.wikipedia.org/wiki/pfefferminz,
Stereochemie. mit Vitamin C. Süßstoff Aspartam (QWKlOWÃHLQHÃ3KHQ\ODODQLQTXHOOH. L(+)-Milchsäure. Zuckeraustauschstoff Sorbit
 Stereochemie mit Vitamin Süßstoff Aspartam (QWKlWÃLQÃ3KQ\DDQLQTX L(+)-Milchsäure Zuckeraustauschstoff Sorbit hemie für Mediziner Isomerie organischer Verbindungen Isomere Konstitutionsisomere Stereoisomere
Stereochemie mit Vitamin Süßstoff Aspartam (QWKlWÃLQÃ3KQ\DDQLQTX L(+)-Milchsäure Zuckeraustauschstoff Sorbit hemie für Mediziner Isomerie organischer Verbindungen Isomere Konstitutionsisomere Stereoisomere
Symmetrieelemente C 3 C 2 C 3 O H H N H H H
 Symmetrieelemente Ein Symmetrielement liegt vor, wenn ein Objekt (hier: Molekül) durch eine Symmetrieoperation mit sich selbst zur Deckung gebracht werden kann. neue und alter Orientierung nicht unterscheidbar
Symmetrieelemente Ein Symmetrielement liegt vor, wenn ein Objekt (hier: Molekül) durch eine Symmetrieoperation mit sich selbst zur Deckung gebracht werden kann. neue und alter Orientierung nicht unterscheidbar
Kohlenhydrate. Monosaccharide
 Kohlenhydrate Monosaccharide Konstitution = Verkettung der Atome; Konstitutionsisomere oder Strukturisomere: gleiche Summenformel, aber unterschiedliche Struktur; z.b. Propanol und Isopropanol. Aldosen
Kohlenhydrate Monosaccharide Konstitution = Verkettung der Atome; Konstitutionsisomere oder Strukturisomere: gleiche Summenformel, aber unterschiedliche Struktur; z.b. Propanol und Isopropanol. Aldosen
Moleküle mit mehr als einem Chiralitätselement
 Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
4. Stereoisomerie. ! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! Organische Chemie I LA / J. C.
 4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism-ball-de.svg Organische Chemie I LA / J. C. Brendel 1 Stereoisomerie
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism-ball-de.svg Organische Chemie I LA / J. C. Brendel 1 Stereoisomerie
Stereochemie organischer Verbindungen
 Stereochemie organischer Verbindungen Stereochemische Prinzipien 1.1 Symmetrie, Symmetrieoperationen, Punktgruppen Der Begriff Stereochemie (griech: stereos = Feststoff) bezieht sich auf die Betrachtung
Stereochemie organischer Verbindungen Stereochemische Prinzipien 1.1 Symmetrie, Symmetrieoperationen, Punktgruppen Der Begriff Stereochemie (griech: stereos = Feststoff) bezieht sich auf die Betrachtung
Thema: Komplexverbindungen, die koordinative Bindung. Koordinationszahl, 18-Elektronen-Schale, ein- mehrzähnige Liganden, EDTA,
 Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Organische Chemie für MST 6. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
Racematspaltung via Clatrate:
 Racematspaltung Racematspaltung durch Bildung diastereomerer Salze Racematspaltung durch Bildung diastereomerer Lactole Racematspaltung via Clatrate Enzymatische Racematspaltung Racematspaltung via Clatrate:
Racematspaltung Racematspaltung durch Bildung diastereomerer Salze Racematspaltung durch Bildung diastereomerer Lactole Racematspaltung via Clatrate Enzymatische Racematspaltung Racematspaltung via Clatrate:
weiteres Beispiel für Stereoisomere: Enantiomere Spiegelebene
 Stereoisomere - Isomerie I: Konstitutionsisomere (siehe oben) - Isomerie II: Konformationsisomere (Konformere, siehe oben) - Isomerie III: Stereoisomere; Stereoisomere weisen eine identische Konstitution
Stereoisomere - Isomerie I: Konstitutionsisomere (siehe oben) - Isomerie II: Konformationsisomere (Konformere, siehe oben) - Isomerie III: Stereoisomere; Stereoisomere weisen eine identische Konstitution
Chiralität in der Natur und synthetisch
 Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Seminar Biotechnologie. Isomerases for Biotransformation of D- hexoses
 Seminar Biotechnologie Isomerases for Biotransformation of D- hexoses Wanmeng Mu, Lina Yu, Wenli Zhang, Tao Zhang, Bo Jiang (2015) Gläser Lars 2545317 3. SEMESTER MSC. BIOTECHNOLOGIE 2 D-Hexosen Hexosen
Seminar Biotechnologie Isomerases for Biotransformation of D- hexoses Wanmeng Mu, Lina Yu, Wenli Zhang, Tao Zhang, Bo Jiang (2015) Gläser Lars 2545317 3. SEMESTER MSC. BIOTECHNOLOGIE 2 D-Hexosen Hexosen
Isomerie organischer Verbindungen
 15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
III. Cycloalkane (Stereochemie II)
 49 III. Cycloalkane (Stereochemie II) (C 2 ) n-2 2 C C 2 (C 2 ) n-2 2 C C 2 C n 2n+2 Cn 2n Nomenklatur: Alkan Cycloalkan für n = 5 n-pentan Cyclopentan Bruttoformel allgemein C n 2n oder (C 2 ) n Cycloalkane
49 III. Cycloalkane (Stereochemie II) (C 2 ) n-2 2 C C 2 (C 2 ) n-2 2 C C 2 C n 2n+2 Cn 2n Nomenklatur: Alkan Cycloalkan für n = 5 n-pentan Cyclopentan Bruttoformel allgemein C n 2n oder (C 2 ) n Cycloalkane
Prof. Dr. Stephen Hashmi, Sommersemester Organische Chemie für Technische Biologen, Organische Chemie für Lehramtskandidaten, Teil 5
 Prof. Dr. ashmi, Sommersemester 2005 45 Mechanismus der 1,2-Isomerisierung: Start: [o III ] Kette: reversible omolyse nur 65 kj/mol Metall--Bindung Organometall-Verbindung X + [o II ] + -Abstraktion das
Prof. Dr. ashmi, Sommersemester 2005 45 Mechanismus der 1,2-Isomerisierung: Start: [o III ] Kette: reversible omolyse nur 65 kj/mol Metall--Bindung Organometall-Verbindung X + [o II ] + -Abstraktion das
Campherchinon (teuer)
 chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 10 Stereochemie (Thema 11.1 11.4) Aufgabe 1: a) Zeichnen Sie den Isomeren-Stammbaum auf. b) Erklären Sie folgende Isomerie-Arten: i) Konstitutionsisomere Konstitutionsisomere
Chemie für Biologen, 2017 Übung 10 Stereochemie (Thema 11.1 11.4) Aufgabe 1: a) Zeichnen Sie den Isomeren-Stammbaum auf. b) Erklären Sie folgende Isomerie-Arten: i) Konstitutionsisomere Konstitutionsisomere
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Die kleinsten Zuckermoleküle. Zucker zeigen gemeinsame funktionelle Gruppen
 Ein Kapitel Zuckerchemie Die Strukturen der Zucker Das Geheimnis aller Zucker ist: Stoffe mit mindestens 2 Hydroxygruppen (-OH) schmecken süß. Glykol (=Ethandiol) oder Glycerin (=Propantriol) schmecken
Ein Kapitel Zuckerchemie Die Strukturen der Zucker Das Geheimnis aller Zucker ist: Stoffe mit mindestens 2 Hydroxygruppen (-OH) schmecken süß. Glykol (=Ethandiol) oder Glycerin (=Propantriol) schmecken
Stereochemische Einflüsse Topizität
 Stereochemische Einflüsse Topizität Lage und Form von NMR-Signalen werden nicht nur durch die unmittelbare chemische Umgebung der betreffenden Kerne, also durch die Konstitution, beeinflusst, sondern auch
Stereochemische Einflüsse Topizität Lage und Form von NMR-Signalen werden nicht nur durch die unmittelbare chemische Umgebung der betreffenden Kerne, also durch die Konstitution, beeinflusst, sondern auch
AC I (AC) HS 2011 Übungen + Lösungen Serie 10
 rof. A. Togni, D-CHAB, HCI H 239 AC I (AC) HS 2011 Übungen ösungen Serie 10 Koordinationschemie A 1. rinzipiell liessen sich sechs iganden () in einem Metallkomplex M 6 nicht nur oktaedrisch sondern auch
rof. A. Togni, D-CHAB, HCI H 239 AC I (AC) HS 2011 Übungen ösungen Serie 10 Koordinationschemie A 1. rinzipiell liessen sich sechs iganden () in einem Metallkomplex M 6 nicht nur oktaedrisch sondern auch
Weiterführende Fragen und Knobeleien zur Vorlesung Organische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach.
 Weiterführende Fragen und Knobeleien zur Vorlesung rganische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach Teil II Mit diesem Blatt will ich Sie anregen, weiter über das Thema Chiralität
Weiterführende Fragen und Knobeleien zur Vorlesung rganische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach Teil II Mit diesem Blatt will ich Sie anregen, weiter über das Thema Chiralität
Tetraeder mit gleichen und verschiedenen Ecken (1, 2, 3, 4)
 Prof. Dr..-U. Reißig rganische hemie 7. Tetraeder mit gleichen und verschiedenen Ecken (,,, ) Diese drei Tetraeder sind mit ihrem Spiegelbild deckbar, d. h. es ist achiral. gleiche Ecken "chemisches Beispiel"
Prof. Dr..-U. Reißig rganische hemie 7. Tetraeder mit gleichen und verschiedenen Ecken (,,, ) Diese drei Tetraeder sind mit ihrem Spiegelbild deckbar, d. h. es ist achiral. gleiche Ecken "chemisches Beispiel"
Spezielle Methoden der pharmazeutischen Chemie 2
 Spezielle thoden der pharmazeutischen Chemie 2 Asymmetrische Synthese (für Diplomanden und Dissertanten im Fach Pharmazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Symmetrie, Asymmetrie, Chiralität
Spezielle thoden der pharmazeutischen Chemie 2 Asymmetrische Synthese (für Diplomanden und Dissertanten im Fach Pharmazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Symmetrie, Asymmetrie, Chiralität
Allgemeine Chemie Symmetrie von Molekülen
 Allgemeine Chemie Symmetrie von Molekülen AC_Molekuelsymmetrie.doc Seite 1 von 23 Fck / 12.10.05 Inhaltsverzeichnis 1 Einleitung...3 1.1 Anwendungsbereiche der Molekülsymmetrie...3 1.2 Sinn und Zweck der
Allgemeine Chemie Symmetrie von Molekülen AC_Molekuelsymmetrie.doc Seite 1 von 23 Fck / 12.10.05 Inhaltsverzeichnis 1 Einleitung...3 1.1 Anwendungsbereiche der Molekülsymmetrie...3 1.2 Sinn und Zweck der
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Kohlenhydrate C n (H 2 O) m
 I_folie7 Kohlenhydrate n ( ) m Die Kohlenhydrate sind wichtige Naturstoffe, die in der Natur hauptsächlich durch die Photosynthese und anschließende eaktionen aufgebaut werden. hν ( ) [hlorophyll] Katalysator
I_folie7 Kohlenhydrate n ( ) m Die Kohlenhydrate sind wichtige Naturstoffe, die in der Natur hauptsächlich durch die Photosynthese und anschließende eaktionen aufgebaut werden. hν ( ) [hlorophyll] Katalysator
7. Stereochemie. Isomere. Alkene. Cycloalkane
 7. Stereochemie 56 In den vorhergehenden Kapiteln haben wir zwei Arten von Isomerie kennengelernt (z.b. Seiten 12, 20 und 23), die Konstitutionsisomerie, und die Stereoisomerie : Isomere Konstitutionsisomerie
7. Stereochemie 56 In den vorhergehenden Kapiteln haben wir zwei Arten von Isomerie kennengelernt (z.b. Seiten 12, 20 und 23), die Konstitutionsisomerie, und die Stereoisomerie : Isomere Konstitutionsisomerie
Molekülsymmetrie und Kristallographie
 Substituierte Cyclohexane Der wichtigste Fall ist in diesem Zusammenhang das monosubstituierte Cyclohexan, weil man an ihm die relativen Stabilitäten von Substituenten abschätzen kann. Die dabei gewonnenen
Substituierte Cyclohexane Der wichtigste Fall ist in diesem Zusammenhang das monosubstituierte Cyclohexan, weil man an ihm die relativen Stabilitäten von Substituenten abschätzen kann. Die dabei gewonnenen
Nucleophile Katalyse am Beispiel von 4-(Dimethylamino)pyridin
 Nucleophile Katalyse am Beispiel von 4-(Dimethylamino)pyridin Matthias Kellermeier Einordnung der nucleophilen Katalyse und Beispiele nucleophiler Katalysatoren Nucleophile Katalyse bislang wenig erforscht;
Nucleophile Katalyse am Beispiel von 4-(Dimethylamino)pyridin Matthias Kellermeier Einordnung der nucleophilen Katalyse und Beispiele nucleophiler Katalysatoren Nucleophile Katalyse bislang wenig erforscht;
Fachbereich Chemie Philipps-Universität Marburg. Stereochemie
 Fachbereich Chemie Philipps-Universität Marburg Stereochemie Dies ist kein vollständiges Skript. ier finden Sie vorlesungsbegleitende Unterlagen (Definitionen, Abbildungen, Literatur), die kein Ersatz
Fachbereich Chemie Philipps-Universität Marburg Stereochemie Dies ist kein vollständiges Skript. ier finden Sie vorlesungsbegleitende Unterlagen (Definitionen, Abbildungen, Literatur), die kein Ersatz
Palladiumkatalysierte C-C-Bindungsknüpfungsreaktionen:
 Palladiumkatalysierte C-C-Bindungsknüpfungsreaktionen: Palladium (Pd) hat die Elektronenkonfiguration [Kr] 4d 10 Gruppe VIIIc, spätes Übergangsmetall, xidationsstufen 0 und 2 typische Verwendung: wegen
Palladiumkatalysierte C-C-Bindungsknüpfungsreaktionen: Palladium (Pd) hat die Elektronenkonfiguration [Kr] 4d 10 Gruppe VIIIc, spätes Übergangsmetall, xidationsstufen 0 und 2 typische Verwendung: wegen
Cyclohexan und Dekalin
 Cyclohexan und Dekalin Die wohl wichtigste ringförmige Struktur in der organischen Chemie ist der Sechsring, im gesättigten Fall Cyclohexan. Dies gilt schon deshalb, weil dieser Ring zentraler Bestandteil
Cyclohexan und Dekalin Die wohl wichtigste ringförmige Struktur in der organischen Chemie ist der Sechsring, im gesättigten Fall Cyclohexan. Dies gilt schon deshalb, weil dieser Ring zentraler Bestandteil
Zucker und Polysaccharide (Voet Kapitel 10)
 Zucker und Polysaccharide (Voet Kapitel 10) 1. Monosaccharide 2. Polysaccharide 3. Glycoproteine Kohlenhydrate oder Saccharide = essentielle Bestandteile der Organismen = Hydrate des Kohlenstoffs Grundbaustein
Zucker und Polysaccharide (Voet Kapitel 10) 1. Monosaccharide 2. Polysaccharide 3. Glycoproteine Kohlenhydrate oder Saccharide = essentielle Bestandteile der Organismen = Hydrate des Kohlenstoffs Grundbaustein
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Kohlenhydrate und ihre Funktionen
 Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Prochiralität H 3 C O
 Prochiralität Es gibt Verbindungen, die selber nicht chiral sind, aber eine Vorform der hiralität enthalten. Solche Verbindungen (oder Strukturelemente einer komplexeren Verbindung) enthalten eine Spiegelebene,
Prochiralität Es gibt Verbindungen, die selber nicht chiral sind, aber eine Vorform der hiralität enthalten. Solche Verbindungen (oder Strukturelemente einer komplexeren Verbindung) enthalten eine Spiegelebene,
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Kohlenhydrate Einleitung
 Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Vorlesung Organische Chemie II, Teil 2, WS 2008/09. Trainings-Aufgabenset Nr. 1: Stereochemie
 Vorlesung rganische Chemie II, Teil 2, WS 2008/09 Prof. Dr. Christoph A. Schalley Trainings-Aufgabenset r. 1: Stereochemie Aufgabe 1 a) Wiederholen Sie, was Spiegelebenen, Inversionszentren, Drehachsen
Vorlesung rganische Chemie II, Teil 2, WS 2008/09 Prof. Dr. Christoph A. Schalley Trainings-Aufgabenset r. 1: Stereochemie Aufgabe 1 a) Wiederholen Sie, was Spiegelebenen, Inversionszentren, Drehachsen
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Versuchsprotokoll: Polarimetrische Untersuchung von Saccharose
 Versuchsprotokoll: Polarimetrische Untersuchung von Saccharose Zeitaufwand: Aufbau: 5-10 Minuten Durchführung: 35 Minuten Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Polarimetrische Untersuchung von Saccharose Zeitaufwand: Aufbau: 5-10 Minuten Durchführung: 35 Minuten Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Aldolreaktion und ihre Stereokontrolle. Stefan Benson und Tobias Brodmann
 Aldolreaktion und ihre Stereokontrolle Stefan Benson und Tobias Brodmann 13.12.2004 0 Gliederung Allgemeine Grundlagen zur Aldoladditions-Reaktion Stereokontrolle bei d. Bildung von Li-Enolaten Stereokontrolle
Aldolreaktion und ihre Stereokontrolle Stefan Benson und Tobias Brodmann 13.12.2004 0 Gliederung Allgemeine Grundlagen zur Aldoladditions-Reaktion Stereokontrolle bei d. Bildung von Li-Enolaten Stereokontrolle
(+) - Boronolid. O OAc. OAc. 4. Syntheseübung SS Bestandteil der Rinde und Blätter verschiedener Pflanzen
 4. Syntheseüung SS 2007 Ac Ac Ac () - oronolid - estandteil der inde und lätter verschiedener Pflanzen - Planzenzuereitungen finden Verwendung als Naturheilmittel gegen Malaria und als Emetikum (rechmittel)
4. Syntheseüung SS 2007 Ac Ac Ac () - oronolid - estandteil der inde und lätter verschiedener Pflanzen - Planzenzuereitungen finden Verwendung als Naturheilmittel gegen Malaria und als Emetikum (rechmittel)
Chiralitätszentrum X X
 hiralitätszentrum Die weitaus meisten chiralen Verbindungen ist deswegen chiral, weil sie sog. asymmetrische Kohlenstoffatome enthalten. Dies sind tetraedrisch konfigurierte -Atome mit vier verschiedenen
hiralitätszentrum Die weitaus meisten chiralen Verbindungen ist deswegen chiral, weil sie sog. asymmetrische Kohlenstoffatome enthalten. Dies sind tetraedrisch konfigurierte -Atome mit vier verschiedenen
Chiralität und Leben
 Chiralität und Leben Symmetrie: Ebenmaß Geometrie: Bestimmte Operationen bilden Objekt auf sich selbst ab (dabei bleibt es quasi unverändert) Rotationssymmetrie Achsensymmetrie - Spiegelsymmetrie Punktsymmetrie
Chiralität und Leben Symmetrie: Ebenmaß Geometrie: Bestimmte Operationen bilden Objekt auf sich selbst ab (dabei bleibt es quasi unverändert) Rotationssymmetrie Achsensymmetrie - Spiegelsymmetrie Punktsymmetrie
Lösungen 2.Übungsblatt SS NBS, AIBN Br K +
 Lösungen 2.Übungsblatt 2002 1. Aufgabe: ubstitutionsreaktionen NB, AIBN racemisch Erklärung: Die radikalische ubstitution erfolgt wegen der hohen elektivität des omatoms am tertiären (und zugleich auch
Lösungen 2.Übungsblatt 2002 1. Aufgabe: ubstitutionsreaktionen NB, AIBN racemisch Erklärung: Die radikalische ubstitution erfolgt wegen der hohen elektivität des omatoms am tertiären (und zugleich auch
Die Verwendung von Rot- und Bleistift ist untersagt! Analysieren Sie das abgebildete Antibiotikum Ampicillin unter Beantwortung folgender Fragen:
 ufgabe 1 nalysieren Sie das abgebildete ntibiotikum mpicillin unter eantwortung folgender Fragen: N 2 N S N a) Geben Sie drei funktionelle Gruppen an: (3 Pkt.) 1. 2. 3. b) erechnen Sie die Summenformel:
ufgabe 1 nalysieren Sie das abgebildete ntibiotikum mpicillin unter eantwortung folgender Fragen: N 2 N S N a) Geben Sie drei funktionelle Gruppen an: (3 Pkt.) 1. 2. 3. b) erechnen Sie die Summenformel:
Lernpaket 3: Monosaccharide
 Lernpaket 3: Monosaccharide Saccharide Bei der Photosynthese werden aus Wasser und Kohlendioxid unter Freisetzung von Sauerstoff Kohlenhydrate (Zucker, Saccharide 1 ) hergestellt. Sie enthalten Kohlenstoff,
Lernpaket 3: Monosaccharide Saccharide Bei der Photosynthese werden aus Wasser und Kohlendioxid unter Freisetzung von Sauerstoff Kohlenhydrate (Zucker, Saccharide 1 ) hergestellt. Sie enthalten Kohlenstoff,
Klausur WS 03/04. 1 Schutzgruppen 10
 Institut für rganische Chemie rganisch-chemisches Fortgeschrittenenpraktikum http://www.chm.tu-dresden.de/organik/hierse/c_fp.htm Name: Erfolgreiche Teilnahme am Praktikum: WS Erfolgreiche Teilnahme am
Institut für rganische Chemie rganisch-chemisches Fortgeschrittenenpraktikum http://www.chm.tu-dresden.de/organik/hierse/c_fp.htm Name: Erfolgreiche Teilnahme am Praktikum: WS Erfolgreiche Teilnahme am
= {e} U (1) U (2) U (3) = {e,a,b,c} 4 : e a b e e a b a a c e b b e c
 KONZEPT DER GRUPPE 6.7 Untergruppen U ist eine Gruppe mit derselben Gruppenoperation wie G und der Ordnung h U h G U ist dann eine Untergruppe von G, wenn alle u i G sind. Beispiel 9: Untergruppen von
KONZEPT DER GRUPPE 6.7 Untergruppen U ist eine Gruppe mit derselben Gruppenoperation wie G und der Ordnung h U h G U ist dann eine Untergruppe von G, wenn alle u i G sind. Beispiel 9: Untergruppen von
Organokatalytische Transferhydrierung. Von Mathias Ronellenfitsch und Christoph Krämer
 rganokatalytische Transferhydrierung Von Mathias Ronellenfitsch und Christoph Krämer 03.12.2009 Gliederung 1. Metallkatalysierte ydrierung von Doppelbindungen 2. Enantioselektive ydrierung in der atur
rganokatalytische Transferhydrierung Von Mathias Ronellenfitsch und Christoph Krämer 03.12.2009 Gliederung 1. Metallkatalysierte ydrierung von Doppelbindungen 2. Enantioselektive ydrierung in der atur
Stereochemie. Grundbegriffe. Bearbeitet von K.-H Hellwich
 Stereochemie Grundbegriffe Bearbeitet von K.-H Hellwich Neuausgabe 2007. Taschenbuch. xii, 120 S. Paperback ISBN 978 3 540 71707 2 Format (B x L): 14 x 21,6 cm Gewicht: 181 g Weitere Fachgebiete > Chemie,
Stereochemie Grundbegriffe Bearbeitet von K.-H Hellwich Neuausgabe 2007. Taschenbuch. xii, 120 S. Paperback ISBN 978 3 540 71707 2 Format (B x L): 14 x 21,6 cm Gewicht: 181 g Weitere Fachgebiete > Chemie,
Wiederholung Grundlagen OC
 Wiederholung Grundlagen C 28.04.2017 Auswertung Stichprobe Frage 1: Die oben abgebildete Strukturformel zeigt 25 20 15 10 5 0 Ether Ester Acetal Keton Ester+Weiteres Frage 2: Die absolute Konfiguration
Wiederholung Grundlagen C 28.04.2017 Auswertung Stichprobe Frage 1: Die oben abgebildete Strukturformel zeigt 25 20 15 10 5 0 Ether Ester Acetal Keton Ester+Weiteres Frage 2: Die absolute Konfiguration
4. Isomerie von Komplexverbindungen
 4. Isomerie von Komplexverbindungen 4. Isomerie bei Koordinationsverbindungen Grundsätzlich unterscheidet man Konstitutionsisomerie Strukturisomerie) und Stereoisomerie (Konfigutationsisomerie). Konstitutionsisomerie:
4. Isomerie von Komplexverbindungen 4. Isomerie bei Koordinationsverbindungen Grundsätzlich unterscheidet man Konstitutionsisomerie Strukturisomerie) und Stereoisomerie (Konfigutationsisomerie). Konstitutionsisomerie:
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine Chemie II (rganische Chemie) für Studierende mit Chemie als Nebenfach zum Üben 1. Zeichnen Sie für die folgenden Stoffklassen jeweils die Strukturformel einer dazu passenden
Beispielklausur Allgemeine Chemie II (rganische Chemie) für Studierende mit Chemie als Nebenfach zum Üben 1. Zeichnen Sie für die folgenden Stoffklassen jeweils die Strukturformel einer dazu passenden
Racematspaltung durch Bildung diastereomerer Lactole
 Racematspaltung durch Bildung diastereomerer Lactole "endo"-lactol "exo"-lactol R 1 R 2 R 1 L* R 2 + 2 -L* R 1 R 2 + L* - 2 + R 1 R 2 R 1 L* R 2 + 2 -L* R 1 R 2 Racemat diasteteomere Acetale enantiomerenreine
Racematspaltung durch Bildung diastereomerer Lactole "endo"-lactol "exo"-lactol R 1 R 2 R 1 L* R 2 + 2 -L* R 1 R 2 + L* - 2 + R 1 R 2 R 1 L* R 2 + 2 -L* R 1 R 2 Racemat diasteteomere Acetale enantiomerenreine
Modul: BS Chemie II Organische Chemie Klausur zum Organisch-Chemischen Grundpraktikum für. Studierende der Biologie
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Institut für rganische Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Klausur
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Institut für rganische Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Klausur
Basisprüfung Allgemeine Chemie (Teil OC) Montag, 3. September 2007
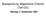 Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Übung 9: Aufbau und Struktur organischer Verbindungen Übung für Medizinische Biologen - Jun.-Prof. Dr. Michael Giese.
 Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Modul: BS Chemie II Organische Chemie Nachklausur zum Organisch-Chemischen Grundpraktikum für. Studierende der Biologie
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Institut für rganische Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Nachklausur
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Institut für rganische Chemie Prof. Dr. A. G. Griesbeck Greinstr. 4 50939 Köln Modul: BS Chemie II rganische Chemie Nachklausur
b) Zeichnen Sie die beiden möglichen Isomere der Aldol-Kondensation und bezeichnen Sie die Stereochemie der Produkte.
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
Die Verwendung von Rot- und Bleistift sowie Tipp-Ex ist untersagt!!!
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Prof. Dr. Th. K. Lindhorst, SS 2003, Übungsklausur. Übungsklausur. zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, OC I
 Übungsklausur zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, C I Diese Auswahl von Aufgaben wurde auf Anfrage zusammengestellt; die Klausur könnte also beispielsweise wie folgt lauten
Übungsklausur zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, C I Diese Auswahl von Aufgaben wurde auf Anfrage zusammengestellt; die Klausur könnte also beispielsweise wie folgt lauten
ACF-Vorkurs: Symmetrie in der Anorganischen Chemie
 ACF-Vorkurs: Symmetrie in der Anorganischen Chemie Stichworte: - Symmetrielemente - Punktgruppen - Charaktertafeln - Anwendung in der MO-Theorie I.1 Zur qualitativen Beschreibung genügt es oft, die Form
ACF-Vorkurs: Symmetrie in der Anorganischen Chemie Stichworte: - Symmetrielemente - Punktgruppen - Charaktertafeln - Anwendung in der MO-Theorie I.1 Zur qualitativen Beschreibung genügt es oft, die Form
Einige Aufgaben zu Kohlenhydraten
 Einige Aufgaben zu Kohlenhydraten Manchmal unterscheidet sich die Nummerierung auf dem kopierten Arbeitsblatt und der online-version unter www.laborberufe.de. In der online-version sind häufig am Ende
Einige Aufgaben zu Kohlenhydraten Manchmal unterscheidet sich die Nummerierung auf dem kopierten Arbeitsblatt und der online-version unter www.laborberufe.de. In der online-version sind häufig am Ende
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
1. Übung zur Vorlesung OC IV
 1. Übung zur Vorlesung C IV 19.05.03 ufgabe 1 a) Zeichnen Sie in das unten abgebildete Schema für die Reaktionsgleichung I das Produkt (wählen Sie ein beliebiges Enantiomer) bzw. für die Reaktionsgleichung
1. Übung zur Vorlesung C IV 19.05.03 ufgabe 1 a) Zeichnen Sie in das unten abgebildete Schema für die Reaktionsgleichung I das Produkt (wählen Sie ein beliebiges Enantiomer) bzw. für die Reaktionsgleichung
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 07.07.09
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 07.07.09
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 12.07.10
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 12.07.10
Wichtige Konzepte der Grundvorlesung Organischen Chemie
 Wichtige Konzepte der Grundvorlesung rganischen Chemie 1: Struktur und Bindung ybridisierung bei Kohlenstoffverbindungen: Abhängig von der Zahl der Zahle der Atome, mit denen der Kohlenstoff verbunden
Wichtige Konzepte der Grundvorlesung rganischen Chemie 1: Struktur und Bindung ybridisierung bei Kohlenstoffverbindungen: Abhängig von der Zahl der Zahle der Atome, mit denen der Kohlenstoff verbunden
Kohlenhydrate Einleitung
 Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Alkylwanderungen. Mechanismus: HCl. HCl. Cl β-pinen. Bornylchlorid. OC4_folie185
 Alkylwanderungen 4_folie185 l l amphen Isobornylchlorid l l β-pinen Bornylchlorid Mechanismus: l l l l Pinakol-Umlagerung 4_folie186 2 + - 2 2-2 + 3 3 3 1,2-3 ~ 3 3 3 3 3 3 3 3 3-3 ( 3 ) 3 Dienon-Phenol-Umlagerung
Alkylwanderungen 4_folie185 l l amphen Isobornylchlorid l l β-pinen Bornylchlorid Mechanismus: l l l l Pinakol-Umlagerung 4_folie186 2 + - 2 2-2 + 3 3 3 1,2-3 ~ 3 3 3 3 3 3 3 3 3-3 ( 3 ) 3 Dienon-Phenol-Umlagerung
11. Syntheseübung WS 2006/2007
 11. Syntheseübung WS 2006/2007 isoliert aus Streptomyces sp.#9885 potente Antitumorverbindung, stabilisiert Microtubuli Totalsynthesen durch die Gruppen von - Erik Sorensen (Princeton University) JACS
11. Syntheseübung WS 2006/2007 isoliert aus Streptomyces sp.#9885 potente Antitumorverbindung, stabilisiert Microtubuli Totalsynthesen durch die Gruppen von - Erik Sorensen (Princeton University) JACS
Seminar zum Praktikum Anorganische Chemie III III
 Seminar zum Praktikum Anorganische Chemie III III Metallorganische Chemie Dr. J. Wachter IR-Teil3 www.chemie.uni-regensburg.de/anorganische_chemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_chemie/wachter/lehre.html
Seminar zum Praktikum Anorganische Chemie III III Metallorganische Chemie Dr. J. Wachter IR-Teil3 www.chemie.uni-regensburg.de/anorganische_chemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_chemie/wachter/lehre.html
Versuchsprotokoll: Mutarotation von Glucose
 Versuchsprotokoll: Mutarotation von Glucose Zeitaufwand: Aufbau: 10 Minuten Durchführung: 24 Stunden Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Glucose
Versuchsprotokoll: Mutarotation von Glucose Zeitaufwand: Aufbau: 10 Minuten Durchführung: 24 Stunden Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Glucose
2 Symmetrieoperationen und -elemente. 1.8 Klassen 2 SYMMETRIEOPERATIONEN UND -ELEMENTE 7
 SYMMETRIEOPERATIONEN UND -ELEMENTE 7.8 Klassen Zweck: Zusammenfassen zueinander ähnlicher (konjugierter) Elemente einer Gruppe. Durch Bestimmung aller Klassen ergibt sich eine eindeutige Zerlegung on G:
SYMMETRIEOPERATIONEN UND -ELEMENTE 7.8 Klassen Zweck: Zusammenfassen zueinander ähnlicher (konjugierter) Elemente einer Gruppe. Durch Bestimmung aller Klassen ergibt sich eine eindeutige Zerlegung on G:
Übungen zur VL Chemie für Biologen und Humanbiologen Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur:
 Übungen zur VL Chemie für Biologen und Humanbiologen 21.01.2011 1. Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur: a) 3-Methyl-4-propylhexan Erklärung: Es liegt keine funktionelle Gruppe
Übungen zur VL Chemie für Biologen und Humanbiologen 21.01.2011 1. Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur: a) 3-Methyl-4-propylhexan Erklärung: Es liegt keine funktionelle Gruppe
Spektroskopie-Seminar WS 17/18 5 NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
Kohlenwasserstoffe. sp 3 -Orbitale. Alkane. Alkene. sp 2 - Orbitale p z - Orbital. sp -Orbitale p y, p z - Orbitale. Alkine
 Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Chemie der Kohlenhydrate
 Chemie der Kohlenhydrate Grundlegendes Der Begriff Kohlenhydrate: Wurde ursprünglich aus der Formel für Glukose abgeleitet. C 6 H 12 O 6 = C 6 (H 2 O) 6 Bzw. allgemein: C n (H 2 O) m Diese missleitende
Chemie der Kohlenhydrate Grundlegendes Der Begriff Kohlenhydrate: Wurde ursprünglich aus der Formel für Glukose abgeleitet. C 6 H 12 O 6 = C 6 (H 2 O) 6 Bzw. allgemein: C n (H 2 O) m Diese missleitende
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion:
 Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt.
 Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
Lebewesen enthalten weitaus mehr Molekülarten und beherbergen weitaus mehr chemische Reaktionsarten als die ganze anorganische Welt. Die aus Biomolekülen aufgebauten biologischen Strukturen sind äußerst
