Ergebnisprotokoll 3. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen
|
|
|
- Hannah Auttenberg
- vor 7 Jahren
- Abrufe
Transkript
1 Ergebnisprotokoll 3. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Freitag, 21. November 2014, bis 17:30 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer H Ergebnisprotokoll der letzten Sitzung Keine Änderungen 2. Begrüssung und Einleitung Cordula Landgraf, Verantwortliche Networking, begrüsste die Teilnehmenden zum dritten Treffen der Arbeitsgruppe. In der anschliessenden Vorstellungsrunde stellten sich die Teilnehmenden seitens Swissmedic und der Patienten- und Konsumentenorganisationen kurz vor. 3. Verabschiedung der Agenda Die Agenda wurde ohne Änderungen verabschiedet. 4. Biosimilars Biologisch ähnliche Arzneimittel Regulatorische Anforderungen in der Schweiz Frau Dr. Sandra Zaugg Kunz, Case Management, und Frau Dr. Anna Barbara Stalder, Regulatory Management, stellten den Teilnehmenden die regulatorischen Anforderungen an biologisch ähnliche Arzneimittel, sog. Biosimilars, in der Schweiz vor. Zusammenfassend lässt sich sagen, dass der Wirkstoff eines Biosimilars und seines Referenzpräparates im Wesentlichen die gleiche biologische Substanz ist. Durch die nie zu 100% übereinstimmenden Herstellprozesse gibt es jedoch geringfügige Unterschiede bei den komplexen Molekülen. Biosimilars unterscheiden sich deshalb zum Referenzpräparat und zu den anderen Biosimilars mit demselben Wirkstoff. Die rechtliche Grundlage ermöglicht gewisse Vereinfachungen in der Dokumentation von Biosimilars. Die entsprechenden Anforderungen an die Dokumentation sind in der Verwaltungsverordnung Zulassung ähnlicher biologischer Arzneimittel (Biosimilars) dargelegt. Ergebnisprotokoll Treffen 21. November 2014 ausgedruckt am / 5
2 Zentrales Element der sich anschliessenden Diskussion waren die Sorgen und Bedenken seitens Patientenorganisationen: fehlende Studien bzw. Extrapolation von Studien nur einer Krankheit (gleiche Wirksamkeit, andere Nebenwirkungen) Sicherheitsbedenken wegen gleich lautenden Wirkstoffnamen Bedenken, dass die Krankenkassen nur noch die günstigere Variante bezahlen werden (Wahlmöglichkeit) Anmerkung Swissmedic: Die Vergütung und Rückerstattung der Kosten seitens Krankenkassen liegt nicht im Verantwortungsbereich von Swissmedic. Hier ist das Bundesamt für Gesundheit (BAG) zuständig. Übernahme der Vorgaben der EMA Pharmakovigilanz Konkrete Beispiele und Probleme von Seiten Patienten- und Konsumentenorganisationen werden am nächsten Treffen der Arbeitsgruppe vorgestellt und diskutiert. 5. EUPATI European Patients Academy on Therapeutic Innovation Nationale Plattform Schweiz Frau Dr. Caecilia Schmid, Swiss Clinical Trial Organisation (SCTO), stellte den Teilnehmenden das EUPATI Konsortium Projekt vor und erläuterte, was EUPATI auf nationaler Ebene erreichen möchte. Die Gründung der Länderplattform Schweiz ist für nächstes Jahr vorgesehen. Zur Vorbereitung wurde bereits unter Mithilfe der SCTO ein Nationales Liaison Team etabliert, das die Verbreitung von Informationsressourcen sowie auch die Anpassung der von EUPATI erstellten Ausbildungsunterlagen an nationale Bedürfnisse zum Ziel hat. Die Länderplattform Schweiz hält EUPATI im Gespräch und versteht sich als Botschafterin für die Belange des Projekts im eigenen Land. Frau Schmid informierte über den ersten Nationalen Anlass Patienteneinbindung, der am 11. Dezember 2014 in Bern stattfindet. Diese nationale Tagung möchte die interessierten Patientenorganisationen und deren Vertreter zu einem ersten Austausch zusammenführen, wobei auch Vertreter der Behörden, der akademischen Forschung sowie der Industrie einbezogen werden. Link zur online-anmeldung und zum Programm: Ergebnisprotokoll Treffen 21. November 2014 ausgedruckt am / 5
3 6. Erfahrungen mit der Arbeitsgruppe Patients and Consumers Working Group der Europäischen Arzneimittelbehörde (EMA) Herr David Haerry, Positivrat, stellte den Mitgliedern der Arbeitsgruppe die Patients and Consumers Working Group der Europäischen Arzneimittelbehörde (EMA) vor und gab einen Überblick über die Art und Anzahl der Aktivitäten der Behörde, in die Patienten/Innen, Konsumenten/Innen sowie deren Organisationen im Laufe des Jahres 2014 einbezogen wurden. Auch für das Jahr 2014 konnte wieder ein hoher Grad an Einbezug in verschiedene Tätigkeiten der Behörde festgestellt werden, von denen nachfolgend ein paar Beispiele genannt seien: Input bei der Erstellung der sog. EPAR Summary for the Public, der Packungsbeilagen sowie in der Kommunikation (DHPC als Beispiel) Mitgliedschaft in EMA Entscheidgremien, wie z.b. dem Management Board, dem Pharmacovigilance Risk Assessment Committee (PRAC), dem Paediatric Committee (PDCO), dem Committee for Orphan Medicinal Products (COMP) usw. Einzig im Committee for Human Medicinal Products (CHMP) sind die Patienten noch nicht involviert; gegenwärtig läuft jedoch eine Versuchsphase bei Nutzen/Risiko Konsultationen Teilnahme an EMA Workshops zu spezifischen Themengebieten Teilnahme im Scientific Advice und den Scientific Advisory Groups Zusammenfassend lässt sich sagen, dass der Einbezug von Patienten/Innen, Konsumenten/Innen sowie deren Organisationen über die letzten Jahre ( ) stetig zugenommen hat und von beiden Seiten geschätzt wird. Diese Zusammenarbeit ermöglicht es den Patienten/Innen, Konsumenten/Innen sowie deren Organisationen, ihre ganz konkreten Erfahrungen mit der Erkrankung und deren Behandlung in die Begutachtung eines Arzneimittels einzubringen, was wertvolle Informationen liefert und schlussendlich zur Qualität der Entscheidfindung beiträgt. Link zum Glossar: &mid=&startletter=a Ergebnisprotokoll Treffen 21. November 2014 ausgedruckt am / 5
4 7. Diverse Punkte Vergütung der Reisekosten Eine Vergütung der Reisekosten sollte gemäss Voten der Teilnehmenden Patienten- und Konsumentenorganisationen auf Antrag für diejenigen Organisationen möglich sein, die ansonsten nicht an den Treffen der Arbeitsgruppe teilnehmen könnten. Swissmedic hat den Antrag entsprechend geprüft und führt dazu Folgendes aus: Swissmedic ist an das Legalitätsprinzip gebunden. Das Institut trägt die ihm entstehenden Kosten für diejenigen Aufgaben, die Gesetz und Verordnung Swissmedic übertragen. So auch die Kosten der Informationstätigkeit gemäss Artikel 67 Abs. 1 HMG (Heilmittelgesetz). Dies bedeutet, dass Swissmedic die Treffen der Arbeitsgruppe vorbereitet, organisiert und als Gastgeber durchführt. Dem gegenüber fehlt es an einer gesetzlichen Grundlage, die es Swissmedic erlauben würde, die Informationsbeschaffung Dritter, hier die Teilnahme an den Treffen der Arbeitsgruppe, (mit) zu finanzieren. Mangels einer gesetzlichen Grundlage kann das Institut daher die den Vertretern/Vertreterinnen von Patienten- und Konsumentenorganisationen entstehenden Kosten (Reisespesen, etc.) nicht vergüten. Sollte eine aktive Teilnahme an den Treffen der Arbeitsgruppe auf Grund Ressourcen bedingter Einschränkungen nicht möglich sein, so besteht nach Satzung der Arbeitsgruppe die Möglichkeit, eine passive Mitgliedschaft zu beantragen. 8. Zusammenfassung und nächste Schritte Als weiteres Thema im Rahmen der Weiterbildung zu regulatorischen Prozessen in der Schweiz wird das Thema Zulassung von Arzneimitteln in der Schweiz bei der nächsten Sitzung im Februar 2015 adressiert. Des Weiteren ist für die nächste Sitzung eine Rückmeldung seitens Patienten- und Konsumentenorganisationen hinsichtlich konkreter Sorgen und Bedenken betreffend die sog. Biosimilars geplant. 9. Nächste Treffen der Arbeitsgruppe Für 2015 sind insgesamt vier Treffen der Arbeitsgruppe geplant. Folgende Termine wurden vereinbart: - Freitag, 13. Februar 15; 14:15 bis 17:15 Uhr - Mittwoch, 20. Mai 15; 14:15 bis 17:15 Uhr - Mittwoch, 9. September 15; 14:15 bis 17:15 Uhr - Dienstag, 1. Dezember 15; 9:15 bis 12:15 Uhr Ergebnisprotokoll Treffen 21. November 2014 ausgedruckt am / 5
5 Anhang: Teilnehmende Patienten- und Konsumentenorganisationen - Fédération Romande des Consommateurs (FRC) - Positivrat - Retina Suisse - ProRaris, Allianz Seltener Krankheiten Schweiz - Schweizer Patientenschutz (SPO) - Schweizerische Patientenorganisation für Lymphombetroffene und Angehörige (ho/noho) - Schweizerischer Morbus Crohn und Colitis Ulcerosa Verein (SMCCV) - Schweizerische Arbeitsgemeinschaft für Patientinnen- und Patienteninteressen (SAPI) - Schweizerische Gesellschaft für Cystische Fibrose (CFCH) - Schweizerische Psoriasis und Vitiligo Gesellschaft (SPVG) - Schweizerische Vereinigung Morbus Bechterew - Verein Morbus Wilson Entschuldigt - Schweizerische Diabetes Gesellschaft - Multiple Sklerose Gesellschaft (MS-G) - Dachverband Schweizerische Patientenstellen (DVSP) Gast - Swiss Clinical Trial Organisation (SCTO) Ergebnisprotokoll Treffen 21. November 2014 ausgedruckt am / 5
Swissmedic, Schweizerisches Heilmittelinstitut
 Patienteneinbindung in der Arzneimittel Forschung und Entwicklung; EUPATI Nationale Plattform Schweiz, 11. Dezember 14 Swissmedic, Schweizerisches Heilmittelinstitut Swissmedic Arbeitsgruppe mit Patienten-
Patienteneinbindung in der Arzneimittel Forschung und Entwicklung; EUPATI Nationale Plattform Schweiz, 11. Dezember 14 Swissmedic, Schweizerisches Heilmittelinstitut Swissmedic Arbeitsgruppe mit Patienten-
Ergebnisprotokoll 6. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen
 Ergebnisprotokoll 6. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Mittwoch, 9. September 2015, 14.15 bis 17:15 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer
Ergebnisprotokoll 6. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Mittwoch, 9. September 2015, 14.15 bis 17:15 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer
Ergebnisprotokoll 8. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen
 Ergebnisprotokoll 8. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Dienstag, 2. Februar 2016, 09:15 bis 12:15 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer
Ergebnisprotokoll 8. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Dienstag, 2. Februar 2016, 09:15 bis 12:15 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer
Ergebnisprotokoll 13. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen
 Ergebnisprotokoll 13. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Freitag, 19. Mai, 09:15 bis 16:15 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer H44
Ergebnisprotokoll 13. Treffen Swissmedic Arbeitsgruppe Patienten- und Konsumentenorganisationen Traktandum Freitag, 19. Mai, 09:15 bis 16:15 Uhr Swissmedic Hallerstrasse 7, 3000 Bern, Sitzungszimmer H44
HMG 2 / HMV IV Transparenz Veröffentlichung von Gesuchseingang, Zulassungsentscheid bis SwissPAR
 Swissmedic Regulatory News aus dem Bereich Zulassung 2017 11. Dezember 2017, Hotel Allegro/Kursaal Bern HMG 2 / HMV IV Transparenz Veröffentlichung von Gesuchseingang, Zulassungsentscheid bis SwissPAR
Swissmedic Regulatory News aus dem Bereich Zulassung 2017 11. Dezember 2017, Hotel Allegro/Kursaal Bern HMG 2 / HMV IV Transparenz Veröffentlichung von Gesuchseingang, Zulassungsentscheid bis SwissPAR
Statuten Swissmedic Pilot Arbeitsgruppe mit Patienten-/Konsumentenorganisationen
 Stab/Networking 6. Februar 2017 Version 01 Statuten Swissmedic Pilot Arbeitsgruppe mit Patienten-/Konsumentenorganisationen 1. Einführung Swissmedic ist bestrebt, die Anliegen der Stakeholder Gruppe Patienten/Innen
Stab/Networking 6. Februar 2017 Version 01 Statuten Swissmedic Pilot Arbeitsgruppe mit Patienten-/Konsumentenorganisationen 1. Einführung Swissmedic ist bestrebt, die Anliegen der Stakeholder Gruppe Patienten/Innen
ACSS Consortium International Generic Drug Regulators Programme (IGDRP)
 Swissmedic Regulatory News aus dem Bereich Zulassung 2015 8. Dezember 2015, Stade de Suisse, Bern ACSS Consortium International Generic Drug Regulators Programme (IGDRP) Chantal Pfäffli, Case Manager,
Swissmedic Regulatory News aus dem Bereich Zulassung 2015 8. Dezember 2015, Stade de Suisse, Bern ACSS Consortium International Generic Drug Regulators Programme (IGDRP) Chantal Pfäffli, Case Manager,
Grundsätze der Neuerungen bei der Zulassung von Arzneimitteln mit bekannten Wirkstoffen (BWS) ab 1. Januar 2014
 Swissmedic Regulatory News aus dem Bereich Zulassung Freitag, 8. November 2013, Stade de Suisse Bern Grundsätze der Neuerungen bei der Zulassung von Arzneimitteln mit bekannten Wirkstoffen (BWS) ab 1.
Swissmedic Regulatory News aus dem Bereich Zulassung Freitag, 8. November 2013, Stade de Suisse Bern Grundsätze der Neuerungen bei der Zulassung von Arzneimitteln mit bekannten Wirkstoffen (BWS) ab 1.
HMG 2 / HMV IV - Harmonisierung Änderungen mit EU Variations
 Swissmedic Regulatory News aus dem Bereich Zulassung 2017 11. Dezember 2017, Hotel Allegro/Kursaal Bern HMG 2 / HMV IV - Harmonisierung Änderungen mit EU Variations Anna Barbara Stalder, Prozessmanagerin,
Swissmedic Regulatory News aus dem Bereich Zulassung 2017 11. Dezember 2017, Hotel Allegro/Kursaal Bern HMG 2 / HMV IV - Harmonisierung Änderungen mit EU Variations Anna Barbara Stalder, Prozessmanagerin,
Ressort: Bundesministerium für Gesundheit
 Bundesgremienbesetzungsgesetz BGremBG- Aufsichts-Gremien und Wesentliche Gremien Ressort: Bundesministerium für Gesundheit Stand: 3.2.205 Aufsichts-Gremien Name Aufsichtsgremium (Berufungsgremium/Entsendegremium)
Bundesgremienbesetzungsgesetz BGremBG- Aufsichts-Gremien und Wesentliche Gremien Ressort: Bundesministerium für Gesundheit Stand: 3.2.205 Aufsichts-Gremien Name Aufsichtsgremium (Berufungsgremium/Entsendegremium)
Was macht eigentlich die SCTO?
 Was macht eigentlich die SCTO? Bern, 17. Mai 2016 Übersicht über die Aktivitäten der SCTO im In- und Ausland sowie ein kurzer Exkurs zur Zusammenarbeit mit Patienten (und der Öffentlichkeit) in der klinischen
Was macht eigentlich die SCTO? Bern, 17. Mai 2016 Übersicht über die Aktivitäten der SCTO im In- und Ausland sowie ein kurzer Exkurs zur Zusammenarbeit mit Patienten (und der Öffentlichkeit) in der klinischen
Pflanzliche Arzneimittel Tradition und Zukunft aus regulatorischer Sicht Prof. Dr. Werner Knöss
 Pflanzliche Arzneimittel Tradition und Zukunft aus regulatorischer Sicht Prof. Dr. Werner Knöss Bundesinstitut für Arzneimittel, Bonn Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums
Pflanzliche Arzneimittel Tradition und Zukunft aus regulatorischer Sicht Prof. Dr. Werner Knöss Bundesinstitut für Arzneimittel, Bonn Das BfArM ist ein Bundesinstitut im Geschäftsbereich des Bundesministeriums
Bundesgremienbesetzungsgesetz BGremBG- Aufsichts-Gremien Ressort: Bundesministerium für Gesundheit
 Bundesgremienbesetzungsgesetz BGremBG- Aufsichts-Gremien Ressort: Bundesministerium für Gesundheit Stand: 30.06.205 Aufsichts-Gremien Name Aufsichtsgremium Ministerium Verwaltungsrat des Europäischen Zentrums
Bundesgremienbesetzungsgesetz BGremBG- Aufsichts-Gremien Ressort: Bundesministerium für Gesundheit Stand: 30.06.205 Aufsichts-Gremien Name Aufsichtsgremium Ministerium Verwaltungsrat des Europäischen Zentrums
Die Aufgaben des Pharmacovigilance Risk Assessment Committee (PRAC)
 Die Aufgaben des Pharmacovigilance Risk Assessment Committee (PRAC) November 2012 Hintergrund Verordnung (EU) Nr. 1235/2010 des Europäischen Parlaments und des Rates vom 15. Dezember 2010 (8) Um sicherzustellen,
Die Aufgaben des Pharmacovigilance Risk Assessment Committee (PRAC) November 2012 Hintergrund Verordnung (EU) Nr. 1235/2010 des Europäischen Parlaments und des Rates vom 15. Dezember 2010 (8) Um sicherzustellen,
AGES Medizinmarktaufsicht (MEA) steht für sichere und wirksame Arzneimittel und Medizinprodukte ein Überblick des Aufgabenbereichs
 AGES Medizinmarktaufsicht (MEA) steht für sichere und wirksame Arzneimittel und Medizinprodukte ein Überblick des Aufgabenbereichs DI., Dr. Christa Wirthumer-Hoche Geschäftsfeldleiterin AGES Medizinmarktaufsicht
AGES Medizinmarktaufsicht (MEA) steht für sichere und wirksame Arzneimittel und Medizinprodukte ein Überblick des Aufgabenbereichs DI., Dr. Christa Wirthumer-Hoche Geschäftsfeldleiterin AGES Medizinmarktaufsicht
Liechtensteinisches Landesgesetzblatt Jahrgang 2016 Nr... ausgegeben am
 Referendumsvorlage Liechtensteinisches Landesgesetzblatt Jahrgang 2016 Nr.... ausgegeben am... 2016 Abkommen zwischen der Regierung des Fürstentums Liechtenstein und der Österreichischen Bundesregierung
Referendumsvorlage Liechtensteinisches Landesgesetzblatt Jahrgang 2016 Nr.... ausgegeben am... 2016 Abkommen zwischen der Regierung des Fürstentums Liechtenstein und der Österreichischen Bundesregierung
Nationales Konzept Seltene Krankheiten: Stand der Arbeiten
 Nationales Konzept Seltene Krankheiten: Stand der Arbeiten Stakeholder-Informationsanlass Bern, 23. Mai 2017 Thomas Christen, Bundesamt für Gesundheit Vizedirektor, Leiter Direktionsbereich Kranken-und
Nationales Konzept Seltene Krankheiten: Stand der Arbeiten Stakeholder-Informationsanlass Bern, 23. Mai 2017 Thomas Christen, Bundesamt für Gesundheit Vizedirektor, Leiter Direktionsbereich Kranken-und
Ihre Therapie verstehen Fragen und Antworten zu Remsima kurz und verständlich
 Ihre Therapie verstehen Fragen und Antworten zu Remsima kurz und verständlich 1 2 Bei welchen Erkrankungen wird Remsima eingesetzt? Remsima ist ein Arzneimittel, das bei chronischent zündlichen Erkrankungen
Ihre Therapie verstehen Fragen und Antworten zu Remsima kurz und verständlich 1 2 Bei welchen Erkrankungen wird Remsima eingesetzt? Remsima ist ein Arzneimittel, das bei chronischent zündlichen Erkrankungen
Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung
 Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn Gesundheit e.v. 10.
Beteiligung von Patienten an der Bewertung von Arzneimitteln bei der Zulassung und der Nutzen-Schaden- Bewertung U. Hagemann Bundesinstitut für Arzneimittel und Medizinprodukte, Bonn Gesundheit e.v. 10.
Nationales Konzept Seltene Krankheiten: Stand der Arbeiten
 Nationales Konzept Seltene Krankheiten: Stand der Arbeiten 7. Internationaler Tag der Seltenen Krankheiten in der Schweiz Centre hospitalier universitaire vaudois, Lausanne, 4. März 2017 Esther Neiditsch,
Nationales Konzept Seltene Krankheiten: Stand der Arbeiten 7. Internationaler Tag der Seltenen Krankheiten in der Schweiz Centre hospitalier universitaire vaudois, Lausanne, 4. März 2017 Esther Neiditsch,
Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis?
 D A CH Symposium für klinische Prüfungen 07. und 08. März 2016, Freiburg Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis? Alexander Mion, Leiter GCP/GVP Inspektorat - Abteilung Klinische Versuche,
D A CH Symposium für klinische Prüfungen 07. und 08. März 2016, Freiburg Inspektion am Prüfzentrum Gute Vorbereitung = Gutes Ergebnis? Alexander Mion, Leiter GCP/GVP Inspektorat - Abteilung Klinische Versuche,
Was ist beim Verfahren mit Voranmeldung (VmV) im
 Swissmedic Regulatory News aus dem Bereich Zulassung Freitag, 8. November 2013, Stade de Suisse Bern Fast Tracks bei Swissmedic: Was ist beim Verfahren mit Voranmeldung (VmV) im Vergleich zum beschleunigten
Swissmedic Regulatory News aus dem Bereich Zulassung Freitag, 8. November 2013, Stade de Suisse Bern Fast Tracks bei Swissmedic: Was ist beim Verfahren mit Voranmeldung (VmV) im Vergleich zum beschleunigten
Swissmedic Regulatory News aus dem Bereich Zulassung Dezember 2017, Hotel Allegro/Kursaal Bern
 Swissmedic Regulatory News aus dem Bereich Zulassung 2017 11. Dezember 2017, Hotel Allegro/Kursaal Bern Volldeklaration Dr. Philipp Weyermann, Leiter Einheit Case Management 2 Swissmedic Schweizerisches
Swissmedic Regulatory News aus dem Bereich Zulassung 2017 11. Dezember 2017, Hotel Allegro/Kursaal Bern Volldeklaration Dr. Philipp Weyermann, Leiter Einheit Case Management 2 Swissmedic Schweizerisches
Swissmedic Regulatory News aus dem Bereich Zulassung Stade de Suisse, 1. Dez Vergleich Zulassungsentscheide SMC / EMA / FDA
 Swissmedic Regulatory News aus dem Bereich Zulassung Stade de Suisse, 1. Dez. 2016 Vergleich Zulassungsentscheide SMC / EMA / FDA 2005-2014 Simon Dalla Torre, Prozessentwicklungs-Manager, Bereich Zulassung
Swissmedic Regulatory News aus dem Bereich Zulassung Stade de Suisse, 1. Dez. 2016 Vergleich Zulassungsentscheide SMC / EMA / FDA 2005-2014 Simon Dalla Torre, Prozessentwicklungs-Manager, Bereich Zulassung
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V
Statuten der Schweizerischen Morbus Crohn / Colitis ulcerosa Vereinigung SMCCV
 Statuten der Schweizerischen Morbus Crohn / Colitis ulcerosa Vereinigung SMCCV 1 Name, Sitz und Geschäftsjahr Unter dem Namen Schweizerische Morbus Crohn / 1.1 Colitis ulcerosa Vereinigung (SMCCV) besteht
Statuten der Schweizerischen Morbus Crohn / Colitis ulcerosa Vereinigung SMCCV 1 Name, Sitz und Geschäftsjahr Unter dem Namen Schweizerische Morbus Crohn / 1.1 Colitis ulcerosa Vereinigung (SMCCV) besteht
zur Umsetzung der Mo. Eder "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement" in der Arzneimittel-Werbeverordnung (AWV)
 Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Februar 2016 Erläuternder Bericht zur Umsetzung der Mo. Eder 13.3393 "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement"
Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Februar 2016 Erläuternder Bericht zur Umsetzung der Mo. Eder 13.3393 "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement"
Wir hören auf dein Bauchgefühl
 Wir hören auf dein Bauchgefühl Du bist nicht allein! Wir machen uns stark für dich Chronisch entzündliche Darmerkrankungen (CED) gehören in der Schweiz zu den häufigsten Erkrankungen: Eine von 350 Personen,
Wir hören auf dein Bauchgefühl Du bist nicht allein! Wir machen uns stark für dich Chronisch entzündliche Darmerkrankungen (CED) gehören in der Schweiz zu den häufigsten Erkrankungen: Eine von 350 Personen,
zur Umsetzung der Mo. Eder "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement" in der Arzneimittel-Werbeverordnung (AWV)
 Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Dezember 2014 Erläuternder Bericht zur Umsetzung der Mo. Eder 13.3393 "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement"
Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Dezember 2014 Erläuternder Bericht zur Umsetzung der Mo. Eder 13.3393 "Swissmedic-Zulassung eines Arzneimittels als erlaubtes Werbeelement"
Herzlich Willkommen! Swissmedic das Schweizerische Heilmittelinstitut stellt sich vor
 Herzlich Willkommen! Swissmedic das Schweizerische Heilmittelinstitut stellt sich vor Dr. Petra Dörr Leiterin Stab, Swissmedic 29. Juni 2011 Swissmedic Schweizerisches Heilmittelinstitut Hallerstrasse
Herzlich Willkommen! Swissmedic das Schweizerische Heilmittelinstitut stellt sich vor Dr. Petra Dörr Leiterin Stab, Swissmedic 29. Juni 2011 Swissmedic Schweizerisches Heilmittelinstitut Hallerstrasse
Biosimilar Anleitung
 Swissmedic Regulatory News aus dem Bereich Zulassung Freitag, 8. November 2013, Stade de Suisse Bern Aktueller Stand der Revision i der Biosimilar Anleitung Dr. Claudia Ruch Stv. Einheitsleitung, Case
Swissmedic Regulatory News aus dem Bereich Zulassung Freitag, 8. November 2013, Stade de Suisse Bern Aktueller Stand der Revision i der Biosimilar Anleitung Dr. Claudia Ruch Stv. Einheitsleitung, Case
Referenzzentren für Seltene Krankheiten und die Schaffung einer «Nationalen Koordination Seltene Krankheiten»
 Referenzzentren für Seltene Krankheiten und die Schaffung einer «Nationalen Koordination Seltene Krankheiten» Agnes Nienhaus Geschäftsführerin unimedsuisse Internationaler Tag der Seltenen Krankheiten
Referenzzentren für Seltene Krankheiten und die Schaffung einer «Nationalen Koordination Seltene Krankheiten» Agnes Nienhaus Geschäftsführerin unimedsuisse Internationaler Tag der Seltenen Krankheiten
Die Sicht der EMEA. für Zulassungs-, Therapie- und. Berlin-Brandenburgische Akademie der
 Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Lebensqualität und Patientennutzen Die Sicht der EMEA PMS-Workshop: Lebensqualität als Kriterium für Zulassungs-, Therapie- und Erstattungsentscheidungen. Berlin-Brandenburgische Akademie der Wissenschaften
Wissen, worauf es ankommt
 Wissen, worauf es ankommt www.tuev-sued.de/akademie GmbH Westendstraße 160 80339 München Telefon: 089 5791 2389 E-Mail: akademie@tuev-sued.de Bleiben wir in Kontakt! AC46-Pharma-fly-210x297-w-15-07-03
Wissen, worauf es ankommt www.tuev-sued.de/akademie GmbH Westendstraße 160 80339 München Telefon: 089 5791 2389 E-Mail: akademie@tuev-sued.de Bleiben wir in Kontakt! AC46-Pharma-fly-210x297-w-15-07-03
Swissmedic Informationsanlass: Fach- und Medizinpersonen 20. Juni Jörg Schläpfer, Prozessentwicklung und Support, Projektleiter Umsetzung HMV IV
 Swissmedic Informationsanlass: Fach- und Medizinpersonen 20. Juni 2018 Befristete Zulassung Jörg Schläpfer, Prozessentwicklung und Support, Projektleiter Umsetzung HMV IV Swissmedic Schweizerisches Heilmittelinstitut
Swissmedic Informationsanlass: Fach- und Medizinpersonen 20. Juni 2018 Befristete Zulassung Jörg Schläpfer, Prozessentwicklung und Support, Projektleiter Umsetzung HMV IV Swissmedic Schweizerisches Heilmittelinstitut
Zur Gründung der Nationalen Koordination Seltene Krankheiten kosek
 Zur Gründung der Nationalen Koordination Seltene Krankheiten kosek Jean-Blaise Wasserfallen Präsident kosek 22. Juni 2017 Vorgeschichte kosek 2010 Postulat Humbel: Anstoss für ein «Nationales Konzept»
Zur Gründung der Nationalen Koordination Seltene Krankheiten kosek Jean-Blaise Wasserfallen Präsident kosek 22. Juni 2017 Vorgeschichte kosek 2010 Postulat Humbel: Anstoss für ein «Nationales Konzept»
Das Projekt Assessment Migration ist in vollem Gange und soll voraussichtlich im nächsten Vereinsjahr zu einem Abschluss kommen.
 Positivrat Schweiz Postfach 1925 8031 Zürich Tel. +41 76 576 36 64 sekretariat@positivrat.ch PC-Konto: 85-77527-3 Tätigkeitsbericht des Positivrat Schweiz Juli 2012 bis Juni 2013 Der Positivrat kann nun
Positivrat Schweiz Postfach 1925 8031 Zürich Tel. +41 76 576 36 64 sekretariat@positivrat.ch PC-Konto: 85-77527-3 Tätigkeitsbericht des Positivrat Schweiz Juli 2012 bis Juni 2013 Der Positivrat kann nun
UNSERE VERANTWORTUNG FÜR DIE PATIENTENSICHERHEIT
 UNSERE VERANTWORTUNG FÜR DIE PATIENTENSICHERHEIT Im Gleichgewicht bleiben Ein gesunder Körper ist im Gleichgewicht. Wenn wir krank sind, bemüht sich der Körper, diese Balance wiederherzustellen. Doch manchmal
UNSERE VERANTWORTUNG FÜR DIE PATIENTENSICHERHEIT Im Gleichgewicht bleiben Ein gesunder Körper ist im Gleichgewicht. Wenn wir krank sind, bemüht sich der Körper, diese Balance wiederherzustellen. Doch manchmal
Verordnung des Schweizerischen Heilmittelinstituts über die vereinfachte Zulassung von Allergenpräparaten
 Verordnung des Schweizerischen Heilmittelinstituts über die vereinfachte Zulassung von Allergenpräparaten (Allergenverordnung, AllergV) vom 11. Dezember 2009 Der Institutsrat des Schweizerischen Heilmittelinstituts
Verordnung des Schweizerischen Heilmittelinstituts über die vereinfachte Zulassung von Allergenpräparaten (Allergenverordnung, AllergV) vom 11. Dezember 2009 Der Institutsrat des Schweizerischen Heilmittelinstituts
Mitgliedstaat Inhaber der Marketing-genehmigung (Name und Adresse) Erfundener Name Stärke Darreichungsform Verabreichungsform SIMVASTATIN BMM PHARMA
 ANHANG I LISTE DER NAMEN, DARREICHUNGSFORM, STÄRKEN DER MEDIZINISCHEN PRODUKTE, VERABREICHUNGSFORM UND INHABER DER MARKETINGGENEHMIGUNG (MA) IN DEN MITGLIEDSTAATEN 1 Mitgliedstaat Inhaber der Marketing-genehmigung
ANHANG I LISTE DER NAMEN, DARREICHUNGSFORM, STÄRKEN DER MEDIZINISCHEN PRODUKTE, VERABREICHUNGSFORM UND INHABER DER MARKETINGGENEHMIGUNG (MA) IN DEN MITGLIEDSTAATEN 1 Mitgliedstaat Inhaber der Marketing-genehmigung
Pharmakovigilanz update Umsetzung in nationale Gesetzgebung
 Pharmakovigilanz update Umsetzung in nationale Gesetzgebung 13. DGRA Jahreskongress Jan Farzan Brigitte Keller-Stanislawski Überblick UAW Definition und Meldungen Koordinierungsgruppe Risikomanagement
Pharmakovigilanz update Umsetzung in nationale Gesetzgebung 13. DGRA Jahreskongress Jan Farzan Brigitte Keller-Stanislawski Überblick UAW Definition und Meldungen Koordinierungsgruppe Risikomanagement
Praktisches Vorgehen zur Erreichung der MDR Readiness SAQ Fachgruppe Medizinprodukte 14. Juni 2018, Olten
 Praktisches Vorgehen zur Erreichung der MDR Readiness SAQ Fachgruppe Medizinprodukte 14. Juni 2018, Olten André Sauter Manager Regulatory Affairs Agenda 1. Yspomed s Infusions- und Injektions-Systeme (Beispiele)
Praktisches Vorgehen zur Erreichung der MDR Readiness SAQ Fachgruppe Medizinprodukte 14. Juni 2018, Olten André Sauter Manager Regulatory Affairs Agenda 1. Yspomed s Infusions- und Injektions-Systeme (Beispiele)
Informationen zur Ausnahmebewilligung für verbotene Betäubungsmittel des Bundesamtes für Gesundheit (BAG)
 Informationen zur Ausnahmebewilligung für verbotene Betäubungsmittel des Bundesamtes für Gesundheit (BAG) 1. Zweck dieses Merkblatts Dieses Merkblatt gibt eine Übersicht darüber, welche Tätigkeiten im
Informationen zur Ausnahmebewilligung für verbotene Betäubungsmittel des Bundesamtes für Gesundheit (BAG) 1. Zweck dieses Merkblatts Dieses Merkblatt gibt eine Übersicht darüber, welche Tätigkeiten im
Beschluss. im Alter von 5 Jahren und älter)
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Änderung der Verordnung (EG) Nr. 726/2004: Weitreichende Auswirkungen auf die frühe Nutzenbewertung
 22.03.2016 Änderung der Verordnung (EG) Nr. 726/2004: Weitreichende Auswirkungen auf die frühe Nutzenbewertung Die Europäische Kommission hat am 10.09.2014 einen Vorschlag für eine Verordnung des Europäischen
22.03.2016 Änderung der Verordnung (EG) Nr. 726/2004: Weitreichende Auswirkungen auf die frühe Nutzenbewertung Die Europäische Kommission hat am 10.09.2014 einen Vorschlag für eine Verordnung des Europäischen
Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung
 Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Bundesrat Drucksache 768/12 (Beschluss) 01.02.13 Beschluss des Bundesrates Dreizehnte Verordnung zur Änderung der Arzneimittelverschreibungsverordnung Der Bundesrat hat in seiner 906. Sitzung am 1. Februar
Nationalkonferenz zu Seltenen Erkrankungen
 Berlin 13./14. Oktober 2010 Nationalkonferenz zu Seltenen Erkrankungen Welche Rahmenbedingungen braucht die Forschung der pharmazeutischen Industrie was soll ein Nationalplan verbessern? Dr. Christian
Berlin 13./14. Oktober 2010 Nationalkonferenz zu Seltenen Erkrankungen Welche Rahmenbedingungen braucht die Forschung der pharmazeutischen Industrie was soll ein Nationalplan verbessern? Dr. Christian
Das EUPATI Projekt. Ingrid Klingmann, Work Package 2 Leiterin, EFGCP. 03. Februar 2016, Bern.
 Das EUPATI Projekt Ingrid Klingmann, Work Package 2 Leiterin, EFGCP 03. Februar 2016, Bern http://www.eupati.eu Die heutige Rolle des Patienten: Leistungsempfänger 2 Die heute typische Situation des Patienten:
Das EUPATI Projekt Ingrid Klingmann, Work Package 2 Leiterin, EFGCP 03. Februar 2016, Bern http://www.eupati.eu Die heutige Rolle des Patienten: Leistungsempfänger 2 Die heute typische Situation des Patienten:
Name / Firma / Organisation : Schweizerischer Verband für komplementärmedizinische Heilmittel
 Stellungnahme von Name / Firma / Organisation : Schweizerischer Verband für komplementärmedizinische Heilmittel Abkürzung der Firma / Organisation : Adresse : Amthausgasse 18, 3011 Bern Kontaktperson :
Stellungnahme von Name / Firma / Organisation : Schweizerischer Verband für komplementärmedizinische Heilmittel Abkürzung der Firma / Organisation : Adresse : Amthausgasse 18, 3011 Bern Kontaktperson :
Stelara ist ein Arzneimittel, das zur Behandlung der folgenden Erkrankungen angewendet wird:
 EMA/636854/2016 EMEA/H/C/000958 Zusammenfassung des EPAR für die Öffentlichkeit Ustekinumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/636854/2016 EMEA/H/C/000958 Zusammenfassung des EPAR für die Öffentlichkeit Ustekinumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
HD-Verzeichnis Fristen Zulassungsgesuche
 Legende AM Arzneimittel NA Neuanmeldung AMZV Arzneimittel-Zulassungsverordnung NAS Neue aktive Substanz / II Begutachtungsphase I / II TAM Tierarzneimittel BZV Beschleunigtes Zulassungsverfahren TCM Traditionelle
Legende AM Arzneimittel NA Neuanmeldung AMZV Arzneimittel-Zulassungsverordnung NAS Neue aktive Substanz / II Begutachtungsphase I / II TAM Tierarzneimittel BZV Beschleunigtes Zulassungsverfahren TCM Traditionelle
Service-Angebote des BPI
 Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
Pharmakovigilanz Service-Angebote des BPI BPI-Pharmakovigilanz Knowledge Base Mit dem EU-Pharmapackage und dem Zweiten Gesetz zur Änderung arzneimittelrechtlicher und anderer Vorschriften vom 19. Oktober
ENDGÜLTIGES GUTACHTEN DES AUSSCHUSSES FÜR ARZNEISPEZIALITÄTEN GEMÄSS ARTIKEL 12 DER RICHTLINIE 75/319/EWG DES RATES, EINSCHLIESSLICH ÄNDERUNGEN, FÜR
 The European Agency for the Evaluation of Medicinal Products Human Medicines Evaluation Unit CPMP/375/97-DE ENDGÜLTIGES GUTACHTEN DES AUSSCHUSSES FÜR ARZNEISPEZIALITÄTEN GEMÄSS ARTIKEL 12 DER RICHTLINIE
The European Agency for the Evaluation of Medicinal Products Human Medicines Evaluation Unit CPMP/375/97-DE ENDGÜLTIGES GUTACHTEN DES AUSSCHUSSES FÜR ARZNEISPEZIALITÄTEN GEMÄSS ARTIKEL 12 DER RICHTLINIE
Als Krebspatient an einer Studie teilnehmen was sollte man wissen?
 Als Krebspatient an einer Studie teilnehmen was sollte man wissen? Krebsinformationsdienst, Heidelberg Dr. Susanne Weg-Remers Seite 2 Grundlage für evidenzbasiertes medizinisches Wissen sind klinische
Als Krebspatient an einer Studie teilnehmen was sollte man wissen? Krebsinformationsdienst, Heidelberg Dr. Susanne Weg-Remers Seite 2 Grundlage für evidenzbasiertes medizinisches Wissen sind klinische
Hohe Anforderungen für die Marktzulassungen im Bereich Tissue Engineering
 Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/hohe-anforderungen-fuerdie-marktzulassungen-im-bereich-tissue-engineering/ Hohe Anforderungen für die Marktzulassungen
Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/hohe-anforderungen-fuerdie-marktzulassungen-im-bereich-tissue-engineering/ Hohe Anforderungen für die Marktzulassungen
GVP Module VII Periodic Safety Update Report
 GVP Module VII Periodic Safety Update Report Dr. Claudia Reichelt Institut für Pharmakovigilanz AGES Gespräche Wien, 26.04.2012 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Änderung
GVP Module VII Periodic Safety Update Report Dr. Claudia Reichelt Institut für Pharmakovigilanz AGES Gespräche Wien, 26.04.2012 Österreichische Agentur für Gesundheit und Ernährungssicherheit GmbH Änderung
Die Aufgaben der Abteilung Preclinical Review
 Swissmedic Regulatory News aus dem Bereich Zulassung 2014 13. November 2014, Stade de Suisse Die Dr. Elisabeth Klenke, Leiterin Abteilung Preclinical Review und GLP Fachstelle/ Bereich Zulassung/ Swissmedic
Swissmedic Regulatory News aus dem Bereich Zulassung 2014 13. November 2014, Stade de Suisse Die Dr. Elisabeth Klenke, Leiterin Abteilung Preclinical Review und GLP Fachstelle/ Bereich Zulassung/ Swissmedic
Wie kann die Lebensqualität bei der Entwicklung von Arzneimitteln besser berücksichtigt werden?
 vfa/vfabio/achse Veranstaltung Stellenwert der Lebensqualität bei Arzneimitteln ein 360 -Blick Wie kann die Lebensqualität bei der Entwicklung von Arzneimitteln besser berücksichtigt werden? Berlin, 02.
vfa/vfabio/achse Veranstaltung Stellenwert der Lebensqualität bei Arzneimitteln ein 360 -Blick Wie kann die Lebensqualität bei der Entwicklung von Arzneimitteln besser berücksichtigt werden? Berlin, 02.
Merkblatt Erläuterungen zu Orphan Drugs
 Inhaltsverzeichnis 1 Begriffe, Definitionen, Abkürzungen... 2 1.1 Definition Orphan Drug Status... 2 1.2 Abkürzungen... 2 2 Einleitung... 2 3 Zielsetzung... 2 4 Geltungsbereich... 2 5 Mitgeltende Dokumente...
Inhaltsverzeichnis 1 Begriffe, Definitionen, Abkürzungen... 2 1.1 Definition Orphan Drug Status... 2 1.2 Abkürzungen... 2 2 Einleitung... 2 3 Zielsetzung... 2 4 Geltungsbereich... 2 5 Mitgeltende Dokumente...
Umteilung Abgabekategorien
 Info-Veranstaltung zur Revision des Heilmittelgesetzes (HMG) Tag 1 25. Oktober 2018, Hotel Allegro/Kursaal Bern Umteilung Abgabekategorien Dr. Bernhard Spörri, Leiter Einheit-2, Abteilung Quality Review,
Info-Veranstaltung zur Revision des Heilmittelgesetzes (HMG) Tag 1 25. Oktober 2018, Hotel Allegro/Kursaal Bern Umteilung Abgabekategorien Dr. Bernhard Spörri, Leiter Einheit-2, Abteilung Quality Review,
Verordnung über die Krankenversicherung
 Verordnung über die Krankenversicherung (KVV) Änderung vom [DATUM] Der Schweizerische Bundesrat verordnet: I Die Verordnung vom 27. Juni 1995 1 über die Krankenversicherung wird wie folgt geändert: Art.
Verordnung über die Krankenversicherung (KVV) Änderung vom [DATUM] Der Schweizerische Bundesrat verordnet: I Die Verordnung vom 27. Juni 1995 1 über die Krankenversicherung wird wie folgt geändert: Art.
Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international
 Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international Dr. med. Dirk Mentzer Referatsleiter Arzneimittelsicherheit Facharzt für Kinder- und Jugendmedizin Paul-Ehrlich-Institut Bundesinstitut
Gesetzliche Grundlagen der Arzneimittelentwicklung national/ international Dr. med. Dirk Mentzer Referatsleiter Arzneimittelsicherheit Facharzt für Kinder- und Jugendmedizin Paul-Ehrlich-Institut Bundesinstitut
Du bist nicht allein! WIR HÖREN AUF DEIN BAUCHGEFÜHL
 Du bist nicht allein! WIR HÖREN AUF DEIN BAUCHGEFÜHL WIR MACHEN UNS STARK FÜR DICH Chronisch entzündliche Darmerkrankungen (CED) gehören in der Schweiz zu den häufigsten Erkrankungen: Eine von 350 Personen,
Du bist nicht allein! WIR HÖREN AUF DEIN BAUCHGEFÜHL WIR MACHEN UNS STARK FÜR DICH Chronisch entzündliche Darmerkrankungen (CED) gehören in der Schweiz zu den häufigsten Erkrankungen: Eine von 350 Personen,
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission
 Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
Gute Klinische Praxis : Prüfungsmaßstäbe für die Ethik-Kommission ass. iur. Jan Paus, LL.M. Rechtsreferent Ethik-Kommission der Ärztekammer Westfalen-Lippe und der Medizinischen Fakultät der WWU Münster
Pharmacovigilance Risk Advisory Committee- PRAAC Responsibilities and Cooperation with NCAs
 Pharmacovigilance Risk Advisory Committee- PRAAC Responsibilities and Cooperation with NCAs Paul-Ehrlich-Institut Brigitte Keller-Stanislawski Paul-Ehrlich-Str. 51-59 63225 Langen GERMANY +49 6103 77-1010
Pharmacovigilance Risk Advisory Committee- PRAAC Responsibilities and Cooperation with NCAs Paul-Ehrlich-Institut Brigitte Keller-Stanislawski Paul-Ehrlich-Str. 51-59 63225 Langen GERMANY +49 6103 77-1010
TÜV SÜD Product Service GmbH Medical and Health Services Safely and successfully on the health market.
 TÜV SÜD Product Service GmbH Medical and Health Services Safely and successfully on the health market. TÜV SÜD Product Service GmbH Prof. Dr. Sabine Kloth 1 Arzneimittel/Medizinprodukt-Kombinationen: Die
TÜV SÜD Product Service GmbH Medical and Health Services Safely and successfully on the health market. TÜV SÜD Product Service GmbH Prof. Dr. Sabine Kloth 1 Arzneimittel/Medizinprodukt-Kombinationen: Die
Pharmaceuticals. Das Wichtigste zum Thema Generika. Sandoz legt Wert auf höchste Qualität, weltweite Präsenz und permanente Innovation.
 Pharmaceuticals Das Wichtigste zum Thema Generika Sandoz legt Wert auf höchste Qualität, weltweite Präsenz und permanente Innovation. 2 3 WAS SIND GENERIKA? Generika sind viel günstiger und dies bei gleicher
Pharmaceuticals Das Wichtigste zum Thema Generika Sandoz legt Wert auf höchste Qualität, weltweite Präsenz und permanente Innovation. 2 3 WAS SIND GENERIKA? Generika sind viel günstiger und dies bei gleicher
Abgeschlossen durch Notenaustausch vom 11. Dezember 2001 Inkrafttreten: 1. Januar 2002
 0.812.101 Liechtensteinisches Landesgesetzblatt Jahrgang 2001 Nr. 190 ausgegeben am 20. Dezember 2001 Notenaustausch zwischen dem Fürstentum Liechtenstein und der Schweiz betreffend die Geltung der schweizeri-
0.812.101 Liechtensteinisches Landesgesetzblatt Jahrgang 2001 Nr. 190 ausgegeben am 20. Dezember 2001 Notenaustausch zwischen dem Fürstentum Liechtenstein und der Schweiz betreffend die Geltung der schweizeri-
Geldwerte Vorteile nach dem revidierten Heilmittelgesetz Risiken und Nebenwirkungen. 25. September 2014 Basel RA Felix Kesselring, LL.M.
 Geldwerte Vorteile nach dem revidierten Heilmittelgesetz Risiken und Nebenwirkungen 25. September 2014 Basel RA Felix Kesselring, LL.M. "Leistungserbringer wie Ärzte, Spitäler und Apotheken können Medikamente
Geldwerte Vorteile nach dem revidierten Heilmittelgesetz Risiken und Nebenwirkungen 25. September 2014 Basel RA Felix Kesselring, LL.M. "Leistungserbringer wie Ärzte, Spitäler und Apotheken können Medikamente
Off-label-use von Arzneimittel in der Palliativmedizin
 Off-label-use von Arzneimittel in der Palliativmedizin Kurzvorstellung des Dissertationsvorhabens Katrin Seibold April 2008 Ausgangssituation Projekt betacare Schmerz & Palliativ Ziel: Aufbau eines umfassenden,
Off-label-use von Arzneimittel in der Palliativmedizin Kurzvorstellung des Dissertationsvorhabens Katrin Seibold April 2008 Ausgangssituation Projekt betacare Schmerz & Palliativ Ziel: Aufbau eines umfassenden,
5. Forum Patientennahe klinische Forschung 24.10.2013
 5. Forum Patientennahe klinische Forschung 24.10.2013 Aktive Patienten: Patientenvereinigungen und ihre Rolle bei der Planung, Umsetzung und Finanzierung von klinischen Studien Ein Wollen, Dürfen oder
5. Forum Patientennahe klinische Forschung 24.10.2013 Aktive Patienten: Patientenvereinigungen und ihre Rolle bei der Planung, Umsetzung und Finanzierung von klinischen Studien Ein Wollen, Dürfen oder
Patiententreffen lysosuisse/ Fabrysuisse
 Perspektiven der neuen Strategie zur Verbesserung der gesundheitlichen Situation von Menschen mit seltenen Erkrankungen Patiententreffen lysosuisse/ Fabrysuisse 8. September 2012 Sorell Hotel Zürichberg,
Perspektiven der neuen Strategie zur Verbesserung der gesundheitlichen Situation von Menschen mit seltenen Erkrankungen Patiententreffen lysosuisse/ Fabrysuisse 8. September 2012 Sorell Hotel Zürichberg,
Sponsoring-Richtlinien
 Sponsoring-Richtlinien 1. Rheumaliga Schweiz (RLS) Die Rheumaliga Schweiz setzt sich für Menschen mit einer rheumatischen Erkrankung ein und fördert die Gesundheit. Sie erbringt ihre Dienstleistungen schweizweit
Sponsoring-Richtlinien 1. Rheumaliga Schweiz (RLS) Die Rheumaliga Schweiz setzt sich für Menschen mit einer rheumatischen Erkrankung ein und fördert die Gesundheit. Sie erbringt ihre Dienstleistungen schweizweit
Verordnung des Schweizerischen Heilmittelinstituts über die vereinfachte Zulassung von Allergenpräparaten
 Verordnung des Schweizerischen Heilmittelinstituts über die vereinfachte Zulassung von Allergenpräparaten (Allergenverordnung, AllergV) vom 11. Dezember 2009 (Stand am 1. Januar 2019) Der Institutsrat
Verordnung des Schweizerischen Heilmittelinstituts über die vereinfachte Zulassung von Allergenpräparaten (Allergenverordnung, AllergV) vom 11. Dezember 2009 (Stand am 1. Januar 2019) Der Institutsrat
QMS Klinische Forschung
 Standard Operating Procedures (SOP) - Prozessbeschreibung ID P2_PM_01 Version: 1.0 Gültig ab: Erstellt von: Astrid Mattes (am 04. Februar 2013) Freigegeben von: Christiane Pauli-Magnus (am 05. März 2013)
Standard Operating Procedures (SOP) - Prozessbeschreibung ID P2_PM_01 Version: 1.0 Gültig ab: Erstellt von: Astrid Mattes (am 04. Februar 2013) Freigegeben von: Christiane Pauli-Magnus (am 05. März 2013)
NEUE BEHANDLUNGSMÖGLICHKEITEN MONOKLONALE ANTIKÖRPER
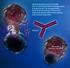 NEUE BEHANDLUNGSMÖGLICHKEITEN MONOKLONALE ANTIKÖRPER Was sind Antikörper? Antikörper patrouillieren wie Wächter im Blutkreislauf des Körpers und achten auf Krankheitserreger wie Bakterien, Viren und Parasiten
NEUE BEHANDLUNGSMÖGLICHKEITEN MONOKLONALE ANTIKÖRPER Was sind Antikörper? Antikörper patrouillieren wie Wächter im Blutkreislauf des Körpers und achten auf Krankheitserreger wie Bakterien, Viren und Parasiten
Safety Measures in the New Pharmaceutical Vigilance System
 Safety Measures in the New Pharmaceutical Vigilance System Paul-Ehrlich-Institut Brigitte Keller-Stanislawski Paul-Ehrlich-Str. 51-59 63225 Langen GERMANY +49 6103 77-1010 +49 6103 77-1263 pharmacovigilance1@pei.de
Safety Measures in the New Pharmaceutical Vigilance System Paul-Ehrlich-Institut Brigitte Keller-Stanislawski Paul-Ehrlich-Str. 51-59 63225 Langen GERMANY +49 6103 77-1010 +49 6103 77-1263 pharmacovigilance1@pei.de
Schweizerische Adipositas-Stiftung SAPS
 Die Schweizerische Adipositas-Stiftung SAPS und das Adipositas-Netzwerk Forum Obesity Schweiz FOS Heinrich von Grünigen, Präsident SAPS Adipositas-Symposium 2008 St. Gallen 14./15. Februar 2008 Die SAPS/FOSO
Die Schweizerische Adipositas-Stiftung SAPS und das Adipositas-Netzwerk Forum Obesity Schweiz FOS Heinrich von Grünigen, Präsident SAPS Adipositas-Symposium 2008 St. Gallen 14./15. Februar 2008 Die SAPS/FOSO
Anlage 5 Förderung einer qualitätsgesicherten, evidenzbasierten und wirtschaftlichen Versorgung im Bereich der Biologika/Biosimilars ( Biolike )
 Anlage 5 Förderung einer qualitätsgesicherten, evidenzbasierten und wirtschaftlichen Versorgung im Bereich der Biologika/Biosimilars ( Biolike ) zum Vertrag nach 140a SGB V zur Verbesserung und Förderung
Anlage 5 Förderung einer qualitätsgesicherten, evidenzbasierten und wirtschaftlichen Versorgung im Bereich der Biologika/Biosimilars ( Biolike ) zum Vertrag nach 140a SGB V zur Verbesserung und Förderung
Therese Stutz Steiger, Vorstandsmitglied Esther Neiditsch, Geschäftsleiterin
 Therese Stutz Steiger, Vorstandsmitglied Esther Neiditsch, Geschäftsleiterin 17. März 2014 Überblick ProRaris Rare Disease Days in der Schweiz Nationale Strategie für Seltene Krankheiten Aktuelle Fragen;
Therese Stutz Steiger, Vorstandsmitglied Esther Neiditsch, Geschäftsleiterin 17. März 2014 Überblick ProRaris Rare Disease Days in der Schweiz Nationale Strategie für Seltene Krankheiten Aktuelle Fragen;
Ausgangslage: Der Artikel mit den markierten Änderungen ist im Anhang angefügt. Was ist neu?
 Position von ProRaris-Allianz Seltene Krankheiten Schweiz zu den Anpassungen der KVV Vergütung von Arzneimitteln im Einzelfall, welche am. März 07 in Kraft treten Ausgangslage: Eine Evaluation der am.
Position von ProRaris-Allianz Seltene Krankheiten Schweiz zu den Anpassungen der KVV Vergütung von Arzneimitteln im Einzelfall, welche am. März 07 in Kraft treten Ausgangslage: Eine Evaluation der am.
Inwiefern sind Menschen mit Seltenen Erkrankungen nicht bedarfsgerecht versorgt?
 Inwiefern sind Menschen mit Seltenen Erkrankungen nicht bedarfsgerecht versorgt? Parlamentarische Begegnung der ACHSE 29. September 2010 Birgit Dembski Mukoviszidose e.v. Seltene Erkrankungen EU: Prävalenz:
Inwiefern sind Menschen mit Seltenen Erkrankungen nicht bedarfsgerecht versorgt? Parlamentarische Begegnung der ACHSE 29. September 2010 Birgit Dembski Mukoviszidose e.v. Seltene Erkrankungen EU: Prävalenz:
zwischen der Kassenärztlichen Vereinigung Sachsen Schützenhöhe Dresden - nachfolgend KV Sachsen genannt - und
 Vertrag über ein strukturiertes Arzneimittel-Management von Biologika und Biosimilars (Biolike) in Sachsen gemäß 84 Abs. 1 Satz 5 SGB V (Rahmenvertrag) zwischen der Kassenärztlichen Vereinigung Sachsen
Vertrag über ein strukturiertes Arzneimittel-Management von Biologika und Biosimilars (Biolike) in Sachsen gemäß 84 Abs. 1 Satz 5 SGB V (Rahmenvertrag) zwischen der Kassenärztlichen Vereinigung Sachsen
Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation. Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group
 Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group Hämatologie im Wandel, Frankfurt 28. Februar 2015 2 Überblick Einführung
Klinische Prüfung: Planung, Verantwortlichkeiten und Organisation Michael Fuchs Leiter der Studienzentrale der German Hodgkin Study Group Hämatologie im Wandel, Frankfurt 28. Februar 2015 2 Überblick Einführung
Curriculum Vitae Professor Dr. Johannes Eckert
 Curriculum Vitae Professor Dr. Johannes Eckert Name: Johannes Eckert Geboren: 14. Mai 1931 Forschungsschwerpunkte: Epidemiologie, Diagnose und Chemotherapie der Alveolären Echinococcose, Entwicklung internationaler
Curriculum Vitae Professor Dr. Johannes Eckert Name: Johannes Eckert Geboren: 14. Mai 1931 Forschungsschwerpunkte: Epidemiologie, Diagnose und Chemotherapie der Alveolären Echinococcose, Entwicklung internationaler
Europäische Verfahren
 Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
Europäische Verfahren Zur Zeit existieren 3 verschieden Zulassungsverfahren in der EU: Verfahren der gegenseitigen Anerkennung (MRP) dezentrales Verfahren (DCP) zentrales Verfahren Alle Biotech Produkte
Position of the Co-ordination Group for Mutual Recognition and Decentralised Procedures for human use on Periodic Safety Update Reports for
 London, 30 January 2019 EMA/28476/2019 Co-ordination group for Human Use PSUSA/00010665/201805 Position of the Co-ordination Group for Mutual Recognition and Decentralised Procedures for human use on Periodic
London, 30 January 2019 EMA/28476/2019 Co-ordination group for Human Use PSUSA/00010665/201805 Position of the Co-ordination Group for Mutual Recognition and Decentralised Procedures for human use on Periodic
Change Request Prozess Wie verändern sich Standards?
 Change Request Prozess Wie verändern sich Standards? Swiss Banking Operations Forum, 16. Mai 2018 Istvan Teglas, Senior Product Manager, SIX Interbank Clearing AG Agenda Was ist ein Standard? Standards
Change Request Prozess Wie verändern sich Standards? Swiss Banking Operations Forum, 16. Mai 2018 Istvan Teglas, Senior Product Manager, SIX Interbank Clearing AG Agenda Was ist ein Standard? Standards
Monitoring - Grundlage für Risk-Adapted Monitoring
 Departement Klinische Forschung Clinical Trial Unit Monitoring - Grundlage für Risk-Adapted Monitoring Klaus Ehrlich Projektmanager Leitung Studienkoordination und Projektmanagement Clinical Trial Unit
Departement Klinische Forschung Clinical Trial Unit Monitoring - Grundlage für Risk-Adapted Monitoring Klaus Ehrlich Projektmanager Leitung Studienkoordination und Projektmanagement Clinical Trial Unit
Gadolinium-haltige Kontrastmittel, Ablagerungen u.a. in Haut, Knochen und Gehirn Verfahren nach Art. 31 der RL 2001/83/EG
 Gadolinium-haltige Kontrastmittel, Ablagerungen u.a. in Haut, Knochen und Gehirn Verfahren nach Art. 31 der RL 2001/83/EG 78. Routinesitzung, 26. April 2016 Absender Titel 19.05.2016 Seite 1 Verwendung
Gadolinium-haltige Kontrastmittel, Ablagerungen u.a. in Haut, Knochen und Gehirn Verfahren nach Art. 31 der RL 2001/83/EG 78. Routinesitzung, 26. April 2016 Absender Titel 19.05.2016 Seite 1 Verwendung
Medizin- und IVD-Produkte- Verordnung Tagung 2017
 EINLADUNG Medizin- und IVD-Produkte- Verordnung Tagung 2017 Mittwoch 20. September 2017 Kursaal Bern Kooperation mit: Inhalt der Tagung Sehr geehrte Interessenten Die diesjährige Compliance Tagung steht
EINLADUNG Medizin- und IVD-Produkte- Verordnung Tagung 2017 Mittwoch 20. September 2017 Kursaal Bern Kooperation mit: Inhalt der Tagung Sehr geehrte Interessenten Die diesjährige Compliance Tagung steht
Umsetzung HMV IV - Einführung
 Swissmedic Regulatory News aus dem Bereich Zulassung 2017 11. Dezember 2017, Hotel Allegro/Kursaal Bern Umsetzung HMV IV - Einführung Jörg Schläpfer, Prozessentwicklung und Support, Projektleiter Umsetzung
Swissmedic Regulatory News aus dem Bereich Zulassung 2017 11. Dezember 2017, Hotel Allegro/Kursaal Bern Umsetzung HMV IV - Einführung Jörg Schläpfer, Prozessentwicklung und Support, Projektleiter Umsetzung
Grenzen der Bindungswirkung der Zulassung für die Nutzenbewertung nach 35 a SGB V
 Grenzen der Bindungswirkung der Zulassung für die Nutzenbewertung nach 35 a Rechtsanwalt Prof. Burkhard Sträter Sträter Rechtsanwälte Kronprinzenstraße 20 Fon: +49 (0) 228-934 54-0 mail@straeterlawyers.de
Grenzen der Bindungswirkung der Zulassung für die Nutzenbewertung nach 35 a Rechtsanwalt Prof. Burkhard Sträter Sträter Rechtsanwälte Kronprinzenstraße 20 Fon: +49 (0) 228-934 54-0 mail@straeterlawyers.de
Erfahrungen aus der Umsetzung der Teilrevision AMZV
 Swissmedic Regulatory News aus dem Bereich Zulassung 2014 13. November 2014, Stade de Suisse Erfahrungen aus der Umsetzung der Teilrevision AMZV Dr. Renate Essen, Leiterin Einheit 2 der Abteilung Case
Swissmedic Regulatory News aus dem Bereich Zulassung 2014 13. November 2014, Stade de Suisse Erfahrungen aus der Umsetzung der Teilrevision AMZV Dr. Renate Essen, Leiterin Einheit 2 der Abteilung Case
Verordnung des EDI über Leistungen in der obligatorischen Krankenpflegeversicherung
 Verordnung des EDI über Leistungen in der obligatorischen Krankenpflegeversicherung (Krankenpflege-Leistungsverordnung, KLV) Änderung vom [DATUM] Das Eidgenössische Departement des Innern (EDI) verordnet:
Verordnung des EDI über Leistungen in der obligatorischen Krankenpflegeversicherung (Krankenpflege-Leistungsverordnung, KLV) Änderung vom [DATUM] Das Eidgenössische Departement des Innern (EDI) verordnet:
Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika
 Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika - Unterlagenschutz bei topisch angewendeten Produkten und Hilfsstoffen Markus Ambrosius ANWALTSKANZLEI STRÄTER Kronprinzenstraße
Symposium Anforderungen an neue Rezepturbestandteile für Dermatika und Kosmetika - Unterlagenschutz bei topisch angewendeten Produkten und Hilfsstoffen Markus Ambrosius ANWALTSKANZLEI STRÄTER Kronprinzenstraße
Erläuterungen zur Änderung der Arzneimittel-Bewilligungsverordnung und der Arzneimittelverordnung
 Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Erläuterungen zur Änderung der Arzneimittel-Bewilligungsverordnung und der Arzneimittelverordnung März 2017 1 Änderung der Arzneimittel-Bewilligungsverordnung
Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Erläuterungen zur Änderung der Arzneimittel-Bewilligungsverordnung und der Arzneimittelverordnung März 2017 1 Änderung der Arzneimittel-Bewilligungsverordnung
Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v.
 Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v. DVMD-Symposium Hannover / K. Thorn Warum Qualitätssicherung in der Klinischen Forschung?
Qualitätssicherung in der Klinischen Forschung / SOPs, Audits und Inspektionen Katharina Thorn Vorsitzende DVMD e.v. DVMD-Symposium Hannover / K. Thorn Warum Qualitätssicherung in der Klinischen Forschung?
Änderung der Verordnung über die Verhütung von Unfällen und Berufskrankheiten (VUV)
 Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Direktionsbereich Kranken- und Unfallversicherung Änderung der Verordnung über die Verhütung von Unfällen und Berufskrankheiten (VUV)
Eidgenössisches Departement des Innern EDI Bundesamt für Gesundheit BAG Direktionsbereich Kranken- und Unfallversicherung Änderung der Verordnung über die Verhütung von Unfällen und Berufskrankheiten (VUV)
