Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel
|
|
|
- Paulina Geiger
- vor 7 Jahren
- Abrufe
Transkript
1 Leitlinie Kommentar rbeitshilfe Leitlinie der Bundesapothekerkammer Herstellung und Prüfung der nicht zur parenteralen nwendung bestimmten Rezeptur- Stand der Revision:
2 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische nforderungen... 3 III Zuständigkeiten... 3 IV Herstellung und Prüfung der nicht zur parenteralen nwendung bestimmten Rezepturund Defekturarzneimittel... 4 Stand der Revision: Seite 2 von 7
3 I Zweckbestimmung und Geltungsbereich Die Leitlinie beschreibt die Verfahrensweise bei der Herstellung und Prüfung der nicht zur parenteralen nwendung bestimmten Rezeptur- in der potheke. Berücksichtigt werden auch Rezepturgrundlagen und Rezepturkonzentrate, die in der potheke als Zwischenprodukte auf Vorrat hergestellt werden. II Regulatorische nforderungen Die Sicherstellung der ordnungsgemäßen Qualität der in der potheke hergestellten Rezeptur- hat sich nach 6, 7, 8, 11, 13 und 14 pothekenbetriebsordnung (pbetro) zu richten (29, 31, 32*). Demnach müssen rzneimittel die nach der pharmazeutischen Wissenschaft erforderlichen Qualität haben ( 6 bs. 1 pbetro). Es dürfen nur usgangsstoffe verwendet werden, deren ordnungsgemäße Qualität worden ist ( 11 pbetro). Nach 4 bs. 7 pbetro muss jede potheke so mit Geräten ausgestattet sein, dass alle rzneimittel in den dort aufgeführten Darreichungsformen ordnungsgemäß hergestellt werden können (15*). Ein Rezepturarzneimittel wird als Einzelanfertigung aufgrund der Verordnung eines rztes oder auf Wunsch eines Patienten angefertigt. Im Rahmen der Herstellung von Defekturarzneimitteln werden aufgrund häufiger ärztlicher oder zahnärztlicher Verschreibungen rzneimittel im Voraus in Chargengrößen bis zu hundert abgabefertigen Packungen oder in einer diesen entsprechenden Menge an einem Tag hergestellt. Die rzneimittel werden unter Beachtung der anerkannten pharmazeutischen Regeln des rzneibuchs ( 55 bs. 1 rzneimittelgesetz) und des DC/NRF hergestellt und geprüft (2*). III Zuständigkeiten Die Herstellung und Prüfung von rzneimitteln ist eine pharmazeutische Tätigkeit ( 1a bs. 3 pbetro) und wird von pharmazeutischem Personal durchgeführt ( 3 bs. 5 pbetro). Nichtpharmazeutisches Personal, insbesondere Pharmazeutischkaufmännische ngestellte (PK), können unter ufsicht des pothekers im Rahmen der pharmazeutischen Tätigkeiten das pharmazeutische Personal bei der Herstellung unterstützen ( 3 bs. 5a pbetro), wenn sie für diese ufgabe qualifiziert sind und über die bei der jeweiligen Tätigkeit gebotene Sorgfalt nachweislich zu nfang und danach fortlaufend von pharmazeutischem Personal unterwiesen werden. Es empfiehlt sich, in der potheke einen Verantwortlichen für die Herstellung der Rezepturund Defekturarzneimittel zu benennen. *Literaturverzeichnis siehe Kapitel 8 Literaturverzeichnis im Kommentar der Leitlinie Stand der Revision: Seite 3 von 7
4 IV Herstellung der Rezepturarzneimittel Vorliegen einer ärztlichen Verordnung oder einer Rezepturanforderung des Patienten 1 Prüfung auf Plausibilität und nwendungsdauer durch den potheker Verweis auf Leitlinie - Risiken bei rzneimitteln und Medizinprodukten - Maßnahmen in der potheke 1 Prüfung der Plausibilität der Verordnung und nwendungsdauer des rzneimittels Prüfung der Verordnung auf: - Therapiekonzept des rztes erkennbar? - Für den Patienten geeignet? (lter, Geschlecht, Schwangerschaft, llergien) - rt der nwendung, ggf. ngaben zur nwendungsdauer, Behandlungszeitraum (Menge des verordneten rzneimittels) - Geeignetes bgabebehältnis; pplikation sinnvoll ; Dosierhilfsmittel erforderlich - Dosierung der Wirkstoffe - Therapeutisch sinnvolle Kombination mehrerer Wirkstoffe - Nutzen-Risiko-bwägung (Bedenkliche rzneimittel gem. 5 MG) - rt, Menge und Qualität der usgangsstoffe (Prüfzertifikat?) - Kompatibilität der usgangsstoffe - Qualität der Zubereitung, z. B. Homogenität, geeignete Partikelgröße - Physikalisch-chemische Stabilität der Zubereitung, z. B. geeignete rezeptierbare ph-bereiche, geeignetes Primärbehältnis - Mikrobiologische Stabilität (Sterilität, Konservierung) - Haltbarkeit - Gebrauchsanweisung und nwendungshinweis für den Patienten Die Plausibilitätsprüfung ist vom potheker durchzuführen und zu unterschreiben. Rezepturarzneimittel plausibel? Bedenken/ Unklarheiten Rücksprache mit dem Verordner/Patient - Lösungsvorschläge unterbreiten - Kommunikationshilfen DC/NRF (I.5.), mit den Änderungen ist die Rezepturverordnung plausibel Wurden die Änderungsvorschläge vom rzt/ Patienten akzeptiert? Verordner/Patient besteht auf Rezepturarzneimittel Rezepturarzneimittel bedenklich ( 5 MG) oder Qualität erheblich gemindert ( 8 MG)? Fertigstellungstermin festlegen blehnung der Herstellung und Dokumentation Fertigstellungstermin festlegen unter Berücksichtigung - usgangsstoffe und Primärpackmittel vorhanden und geprüft? Ggf. bestellen? Lieferzeitpunkt? Prüfaufwand? - Herstellungsaufwand? - Verfügbare Mitarbeiter? Informationen für den Herstellenden dokumentieren Nutzen-Risiko-bwägung verbietet die Herstellung 2.2 Erstellung der Herstellungsanweisung 2.8 Vorbereitung des rbeitsplatzes Verweis auf Leitlinien - Prüfung und Lagerung der usgangsstoffe - Prüfung und Lagerung der Primärpackmittel - Hygienemanagement 2.2 Herstellungsanweisung Festlegungen treffen zu: - Plausibilitätsprüfung - nsatzgröße (ggf. Überschüssen und Produktionszuschlägen) - usgangsstoffen, ggf. Verwendung von Rezepturkonzentraten - Herstellungstechnik und usrüstungsgegenständen - Primären Verpackungsmaterialien und ggf. pplikationshilfen - Hygienemaßnahmen - rbeitsschutzmaßnahmen bei Verwendung von Gefahrstoffen - Vorbereitung des rbeitsplatzes - Einzelnen rbeitsschritten mit Sollwerten - Einwaagekorrektur bei Gehaltsabweichung des Wirkstoffes - uswahl der geeigneten Waage, Wägetechnik - Inprozesskontrollen (Sollwerten, Geräteparameter) - Kennzeichnung (ggf. Kopie des Etiketts) - Freigabeprüfung und Dokumentation Rezepturarzneimittel st nach standardisierten und anerkannten bzw. davon abgeleiteten Herstellungsvorschriften zubereiten. Herstellungsanweisung ist vom zuständigen potheker zu unterschreiben. 2.8 Vorbereitung des rbeitsplatzes - rbeitsplatz von nicht benötigten Materialien befreien - Hygienemaßnahmen entsprechend den Hygieneplänen durchführen - rznei- und Hilfsstoffe, Geräte und Primärpackmittel am rbeitsplatz bereitstellen - Ggf. rbeitsschutzmaßnahmen ergreifen entspr. Betriebsanweisung - Herstellungsprotokoll bereitlegen Stand der Revision: Seite 4 von 7
5 Fortsetzung nachträglich zu beseitigen? Keine nsatz vernichten Mängel 3 Herstellung des Rezepturarzneimittels und Herstellungsdokumentation 3.2 Durchführung der Inprozesskontrolle Inprozesskontrolle ist ohne Mängel? Keine Mängel bfüllung in das bgabebehältnis ( 13 pbetro) Verweis auf Leitlinie - Prüfung und Lagerung der Primärpackmittel 5.1 Kennzeichnung des bgabebehältnisses ( 14 pbetro) 3 Herstellung - Umsetzung der Herstellungsanweisung - Vier-ugen-Prinzip insbesondere in kritischen Fällen beachten (DC/NRF I ) 3.1 Herstellungsprotokoll - Dokumentation gemäß 7 bs. 1c pbetro (rbeitsvorlagen DC/NRF-Kapitel II) ngaben im Herstellungsprotokoll: - Name des Patienten, ggf. des rztes bzw. Herstellnummer - Bezeichnung des M, Darreichungsform - ngabe der Herstellungsanweisung - Evtl. ergriffene rbeitsschutz- und Hygienemaßnahmen - usgangsstoffe nach rt, Menge, Qualität, Charge oder Prüfnummer, Verfallsdatum - Dokumentation der Einwaagen (Ist+Soll), ggf. Unterschrift bei Vier-ugen-Prinzip - Verwendete Waagentypen - Herstellungsparameter, z. B. Rührzeit, Drehzahl - Ergebnisse der Inprozesskontrollen - Herstellungsdatum, Herstellender, ufbrauchsfrist, Laufzeit bei Einzeldosisbehältnissen - Kriterien der Freigabeprüfung - Besonderheiten der Etikettierung (evtl. Beispieletikett) - Datum, Unterschrift des verantwortlichen pothekers 3.2 Inprozesskontrollen Beispiele für Inprozesskontrollen: - Berührungslose Temperaturbestimmung mit Infrarot- Laser-Thermometer - Visuelle Prüfung auf gleichmäßige Beschaffenheit und physikalische Stabilität - Ungelöste Teilchen, Pulveragglomerate (bei halbfesten Zubereitungen usstrich) - Farbe, Geruch - ph-wert - Dichte, Schüttdichte - Filterintegritätsprüfung durch Blasendrucktest bei der Sterilfiltration (Inprozesskontrolle auch bei Zubereitungen, die mit elektrischen Rührsystemen hergestellt werden) - Bei Mängeln diensthabenden potheker hinzuziehen 5.1 Kennzeichnung der Rezepturarzneimittel - Name, nschrift der potheke - Name des Patienten, Hinweis bei Tierarzneimittel - Inhalt nach Gewicht, Rauminhalt oder Stückzahl - rt der nwendung, z. B. zum uftragen auf die Haut - Gebrauchsanweisung - Wirkstoffe nach rt und Menge oder Bezeichnung des verwendeten FM - Sonstige Bestandteile nach der rt (auch bei standardisierten Rezepturen) oder Bezeichnung des verwendeten FM - Herstelllungsdatum - Laufzeit bei Einzeldosisbehältnissen ( verwendbar bis ), ufbrauchsfrist bei Mehrdosenbehältnissen ( verwendbar bis mit Enddatum der Haltbarkeit nach Öffnen oder Herstellung der gebrauchsfertigen Lösung) - Soweit erforderlich, Hinweise auf besondere Vorsichtsmaßnahmen für die ufbewahrung, nwendung oder Entsorgung, z. B. Umschütteln, Verdünnung vor Gebrauch, ufbewahrungstemperatur, kein Kontakt mit den ugen, von Zündquellen fernhalten und Hinweise auf Umweltgefahren - Ggf. Warnhinweis nach MWarnV Prüfung jedes Rezepturarzneimittels durch den potheker: - Übereinstimmung mit der Rezepturanforderung/Verordnung - Ergebniss der Inprozesskontrolle - Sensorische (organoleptische) Prüfung des Endproduktes - Kennzeichnung - Ggf. beigelegte pplikationshilfen nachträglich zu beseitigen? Mängel Freigabeprüfung ist ohne Mängel? Keine Keine Mängel Rezepturarzneimittel vernichten Rezepturarzneimittel zur bgabe freigegeben - Dokumentation der Freigabe Stand der Revision: Seite 5 von 7
6 Herstellung der Defekturarzneimittel Bedarf für Defekturarzneimittel Einordnung des Defekturarzneimittels - Vorratsherstellung für Standgefäß: rzneimittel-bulkware - Fertigarzneimittel ohne Zulassung: Verlängerte Rezeptur/100er-Regelung ( 21 bs. 2 MG) - Fertigarzneimittel mit Zulassung: Standardzulassung ( 36 MG), echte/fiktive Zulassung, z. B. Stada-Präparate ( 21 bs. 3 MG) 2.2 Herstellungsanweisung Festlegungen treffen zu: - nsatzgröße (ggf. Überschüssen und Produktionszuschlägen) - usgangsstoffen, ggf. Verwendung von Rezepturkonzentraten - Herstellungstechnik und usrüstungsgegenständen - Primären Verpackungsmaterialien und ggf. pplikationshilfen - Hygienemaßnahmen - rbeitsschutzmaßnahmen bei Verwendung von Gefahrstoffen - Vorbereitung des rbeitsplatzes, ggf. technischen und organisatorischen Maßnahmen zur Vermeidung von Kreuzkontaminationen und Verwechslungen - Einzelnen rbeitsschritten mit Sollwerten - Einwaagekorrektur bei Gehaltsänderung des Wirkstoffes - uswahl der geeigneten Waage, Wägetechnik - Inprozesskontrollen - Kennzeichnung (einschließlich Herstellungsdatum, Verfallsdatum oder Nachprüfdatum) - Lagerungsbedingungen und ggf. Vorsichtsmaßahmen - Freigabeprüfung und Dokumentation Defekturarzneimittel st nach standardisierten und anerkannten bzw. davon abgeleiteten Herstellungsvorschriften zubereiten. Herstellungsanweisung ist vom zuständigen potheker zu unterschreiben. 2.2/6.2.1Erstellung einer Herstellungs- und Prüfanweisung 3.1 Vorbereitung des rbeitsplatzes Verweis auf Leitlinien - Prüfung und Lagerung der usgangsstoffe - Prüfung und Lagerung der Primärpackmittel - Hygienemanagement Prüfanweisung Festlegungen treffen zu: - Probenahme - Prüfmethode (ggf. Verweis auf standardisierte Prüfvorschrift) - rt der Prüfung einschl. der zulässigen Soll- und Grenzwerte Die Prüfanweisung ist vom zuständigen potheker zu unterschreiben. 3.1 Vorbereitung des rbeitsplatzes - Hygienemaßnahmen entsprechend den Hygieneplänen durchführen - rznei- und Hilfsstoffe, Geräte und Primärpackmittel am rbeitsplatz bereitstellen; ggf. gereinigte und desinfizierte Standgefäße - Ggf. rbeitsschutzmaßnahmen ergreifen entspr. Betriebsanweisung - Herstellungsprotokoll bereitlegen 3 Herstellung - Umsetzung der Herstellungsanweisung - Vier-ugen-Prinzip insbesondere in kritischen Fällen beachten (NRF I ) 3 Herstellung des Defekturarzneimittels und Herstellungsdokumentation 3.2 Herstellungsprotokoll - Dokumentation gemäß 8 bs. 2 pbetro ngaben im Herstellungsprotokoll: - Bezeichnung des rzneimittels - Darreichungsform - ngabe der Herstellungsanweisung - Evtl. ergriffene rbeitsschutzmaßnahmen/hygienemaßnahmen - usgangsstoffe nach rt, Menge, Qualität, Charge, Prüfnummer, Verfallsdatum - Dokumentation der Einwaagen (Ist- und Soll-Einwaage), ggf. Unterschrift bei Vier-ugen-Prinzip - Verwendete Waagentypen - Dokumentation der Herstellungsparameter, z. B. Rührzeit, Drehzahl - Ergebnisse der Inprozesskontrollen - Herstellungsdatum oder Chargenbezeichnung - Herstellende Person - Laufzeit oder Verwendbarkeitsfrist, ufbrauchsfrist (der gebrauchsfertigen Zubereitung nach nbruch) - usbeute (Gesamtmenge und nzahl der abgefüllten Gebinde) - Datum, Unterschrift des verantwortlichen pothekers (Freigabe zur Prüfung) Stand der Revision: Seite 6 von 7
7 Fortsetzung nachträglich zu beseitigen? Mängel Durchführung der Inprozesskontrolle Inprozesskontrolle ist ohne Mängel? 3.3 Inprozesskontrollen Beispiele für Inprozesskontrollen: - Berührungslose Temperaturbestimmung mit Infrarot- Laser-Thermometer - Visuelle Prüfung auf gleichmäßige Beschaffenheit und physikalische Stabilität - Ungelöste Teilchen, Pulveragglomerate (bei halbfesten Zubereitungen usstrich) - Farbe, Geruch - ph-wert - Dichte, Schüttdichte - Filterintegritätsprüfung durch Blasendrucktest bei der Sterilfiltration (Inprozesskontrolle auch bei Zubereitungen, die mit elektrischen Rührsystemen hergestellt werden) - Bei Mängeln diensthabenden potheker hinzuziehen nicht nsatz vernichten keine Mängel bfüllung ls Bulkware ins Standgefäß Kennzeichnung ls FM ins bgabegefäß Kennzeichnung Kennzeichnung Defekturarzneimittel als Fertigarzneimittel - Kennzeichnung gemäß 10 MG Defekturarzneimittel als Bulkware - Genaue Bezeichnung - Bestandteile nach rt und Menge empfehlenswert - Herstellungsdatum oder Chargenbezeichnung - Enddatum der Laufzeit - Kennzeichnung gefährlicher Eigenschaften nach GefStoffV - Lagerungshinweis 6.2 Prüfung der Defekturarzneimittel - Prüfung der Defekturarzneimittel gemäß Prüfanweisung 6.2 Prüfung und Dokumentation Prüfprotokoll Das Prüfprotokoll muss ngaben enthalten zu: - Zugrunde liegender Prüfanweisung - Prüfendem - Datum der Prüfung - Prüfergebnissen - Unterschrift des verantwortlichen pothekers nachträglich zu beseitigen? Mängel Freigabeprüfung ist ohne Mängel? Prüfung des Defekturarzneimittels durch den potheker: - Ergebniss der Inprozesskontrolle (Herstellungsprotokoll) - Ergebnisse der Prüfung (Prüfprotokoll) - Sensorische (organoleptische) Prüfung des Endproduktes - Kennzeichnung - Ggf. beigelegte pplikationshilfen Keine Keine Mängel Defekturarzneimittel vernichten Defekturarzneimittel freigegeben Lagerung Stand der Revision: Seite 7 von 7
Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel
 Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel Stand der Revision: 25.11.2008 Inhaltsübersicht I II III
Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel Stand der Revision: 25.11.2008 Inhaltsübersicht I II III
Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- Stand der Revision: 25.11.2008 Inhaltsübersicht
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- Stand der Revision: 25.11.2008 Inhaltsübersicht
Plausibilitätsprüfung Wurde für das vorliegende Rezepturarzneimittel bereits die Plausibilitätsprüfung vorgenommen?
 I Hinweis zur Bearbeitung des Arbeitsbogens Erstellen Sie die Herstellungsanweisung für ein Rezepturarzneimittel. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer
I Hinweis zur Bearbeitung des Arbeitsbogens Erstellen Sie die Herstellungsanweisung für ein Rezepturarzneimittel. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Herstellung und Prüfung applikationsfertiger Parenteralia ohne toxisches Potenzial
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne toxisches Potenzial Stand der Revision: 25.11.2008 Inhaltsübersicht I II III IV
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne toxisches Potenzial Stand der Revision: 25.11.2008 Inhaltsübersicht I II III IV
Herstellung und Abgabe der Betäubungsmittel zur Opiatsubstitution
 Leitlinie Kommentar rbeitshilfe Leitlinie der Bundesapothekerkammer zur Herstellung und bgabe der Betäubungsmittel zur Opiatsubstitution Stand der Revision: 26.11.2014 Inhaltsverzeichnis I Zweckbestimmung
Leitlinie Kommentar rbeitshilfe Leitlinie der Bundesapothekerkammer zur Herstellung und bgabe der Betäubungsmittel zur Opiatsubstitution Stand der Revision: 26.11.2014 Inhaltsverzeichnis I Zweckbestimmung
Prüfung und Lagerung der Ausgangsstoffe
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
ARBEITSBOGEN 5: HERSTELLUNG VON REZEPTURARZNEIMITTELN
 I Hinweis zur Bearbeitung des Arbeitsbogens Stellen Sie ein wirkstoffhaltiges Rezepturarzneimittel her. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
I Hinweis zur Bearbeitung des Arbeitsbogens Stellen Sie ein wirkstoffhaltiges Rezepturarzneimittel her. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
Prüfung der Fertigarzneimittel
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung der Fertigarzneimittel und apothekenpflichtigen
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung der Fertigarzneimittel und apothekenpflichtigen Medizinprodukte Stand der Revision:16.06.2016 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung der Fertigarzneimittel und apothekenpflichtigen Medizinprodukte Stand der Revision:16.06.2016 Inhaltsverzeichnis
Die neue Apothekenbetriebsordnung
 - Pharmazie 04. Juli 2012 Die neue Apothekenbetriebsordnung Parenteraliaherstellung Reiner Herkner Darmstadt, den 4. Juli 2012 Entscheidende Änderungen Rezepturen Plausibilitätsprüfung Herstellungsanweisung
- Pharmazie 04. Juli 2012 Die neue Apothekenbetriebsordnung Parenteraliaherstellung Reiner Herkner Darmstadt, den 4. Juli 2012 Entscheidende Änderungen Rezepturen Plausibilitätsprüfung Herstellungsanweisung
Sommersemester 2010 Vorlesung - Spezielles Arzneimittelrecht. Teil VIII Mittwoch, 2. Juni 2010
 Ministerium für,,, und Sommersemester 2010 Vorlesung - Spezielles Arzneimittelrecht Teil VIII Mittwoch, 2. Juni 2010 Folie 1 Ministerium für,,, und 4 Beschaffenheit, Größe und Einrichtung der Apothekenbetriebsräume
Ministerium für,,, und Sommersemester 2010 Vorlesung - Spezielles Arzneimittelrecht Teil VIII Mittwoch, 2. Juni 2010 Folie 1 Ministerium für,,, und 4 Beschaffenheit, Größe und Einrichtung der Apothekenbetriebsräume
Herstellung und Abgabe der Betäubungsmittel zur Opiatsubstitution
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Abgabe der Betäubungsmittel zur Opiatsubstitution Stand: 23.11.2011 Inhaltsübersicht I II III
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Abgabe der Betäubungsmittel zur Opiatsubstitution Stand: 23.11.2011 Inhaltsübersicht I II III
Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit toxischem Potenzial
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit toxischem Potenzial Stand der Revision: 25.11.2008 Inhaltsübersicht I
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit toxischem Potenzial Stand der Revision: 25.11.2008 Inhaltsübersicht I
Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Einnahmezeitpunkte
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Stand: 26.11.2014 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Stand: 26.11.2014 Inhaltsverzeichnis
Fischer /Schüler. Rezeptur - Qualität in 7 Schritten. Ulrike Fischer, Dresden Katrin Schüler, Dresden. Mit 55 Abbildungen und 101 Tabellen
 Fischer /Schüler Rezeptur - Qualität in 7 Schritten Ulrike Fischer, Dresden Katrin Schüler, Dresden Mit 55 Abbildungen und 101 Tabellen Ä Checklisten, Arbeitsblätter und Fallbeispiele unterwww.online-plusbase.de
Fischer /Schüler Rezeptur - Qualität in 7 Schritten Ulrike Fischer, Dresden Katrin Schüler, Dresden Mit 55 Abbildungen und 101 Tabellen Ä Checklisten, Arbeitsblätter und Fallbeispiele unterwww.online-plusbase.de
Unter welchen Voraussetzungen werden Betriebe für den Bezug von Ausgangsstoffen anerkannt?
 I Hinweis zur Bearbeitung des Arbeitsbogens Führen Sie die Prüfung eines Ausgangsstoffes durch. Grundlage des Arbeitsbogens ist die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung und
I Hinweis zur Bearbeitung des Arbeitsbogens Führen Sie die Prüfung eines Ausgangsstoffes durch. Grundlage des Arbeitsbogens ist die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung und
Tab. 3.1 Was muss im Einzelnen dokumentiert werden? A Ausgangsstoff/Bezeichnung. B Lieferdatum/Herstellungsdatum. C Lieferant/Hersteller
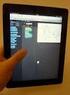 51 3.1 Prüfung von Ausgangsstoffen und Defekturarzneimitteln Tab. 3.1 Was muss im Einzelnen dokumentiert werden? Was Wer Apothekenbetriebsordnung 6 Allgemeine Vorschriften über die Herstellung und Prüfung
51 3.1 Prüfung von Ausgangsstoffen und Defekturarzneimitteln Tab. 3.1 Was muss im Einzelnen dokumentiert werden? Was Wer Apothekenbetriebsordnung 6 Allgemeine Vorschriften über die Herstellung und Prüfung
Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
 Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Stand der
Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Stand der
Rezepturarzneimittel und Defekturarzneimittel. (Dr. Andreas Kiefer)
 Rezepturarzneimittel und Defekturarzneimittel (Dr. Andreas Kiefer) 1 Arzneimittelherstellung im europäischen Kontext Aus der Resolution des Ministerrates des Europarates: Fertigarzneimittel genügen nicht
Rezepturarzneimittel und Defekturarzneimittel (Dr. Andreas Kiefer) 1 Arzneimittelherstellung im europäischen Kontext Aus der Resolution des Ministerrates des Europarates: Fertigarzneimittel genügen nicht
DOSSIER FÜR DEFEKTURARZNEIMITTEL 1
 Defekturbezeichnung DOSSIER FÜR DEFEKTURARZNEIMITTEL 1 Zu den unten genannten Punkten sind gegeben falls entsprechende Unterlagen im Anhang beigefügt. 1. Mehrwert 2 Herstellung aufgrund wiederkehrender
Defekturbezeichnung DOSSIER FÜR DEFEKTURARZNEIMITTEL 1 Zu den unten genannten Punkten sind gegeben falls entsprechende Unterlagen im Anhang beigefügt. 1. Mehrwert 2 Herstellung aufgrund wiederkehrender
Stellen der Arzneimittel
 Empfehlungen der Bundesapothekerkammer zur Qualitätssicherung Stand: 14.11.2006 Kapitel VII-1.1im Flussdiagramm aktualisiert am 20.09.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich
Empfehlungen der Bundesapothekerkammer zur Qualitätssicherung Stand: 14.11.2006 Kapitel VII-1.1im Flussdiagramm aktualisiert am 20.09.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich
ARBEITSBOGEN 4: PRÜFUNG DER FERTIGARZNEIMITTEL UND APOTHEKENPFLICHTIGEN MEDIZIN- PRODUKTE
 I Hinweis zur Bearbeitung des Arbeitsbogens Überprüfen Sie ein Fertigarzneimittel (FAM) oder ein apothekenpflichtiges Medizinprodukt (MP) gemäß 12 Apothekenbetriebsordnung (ApBetrO). Grundlage des Arbeitsbogens
I Hinweis zur Bearbeitung des Arbeitsbogens Überprüfen Sie ein Fertigarzneimittel (FAM) oder ein apothekenpflichtiges Medizinprodukt (MP) gemäß 12 Apothekenbetriebsordnung (ApBetrO). Grundlage des Arbeitsbogens
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung und Lagerung der Ausgangsstoffe
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B Stand
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B Stand
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 08.05.2018 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 08.05.2018 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV Zweckbestimmung
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV Zweckbestimmung
Herstellung und Prüfung der nicht sterilen Rezeptur- und Defekturarzneimittel
 Herstellung und Prüfung der nicht sterilen Rezeptur- und Defekturarzneimittel Qualitätsmanagement Handbuch 20148 Hamburg Herstellung und Prüfung der nicht sterilen Rezeptur- und Defekturarzneimittel Version
Herstellung und Prüfung der nicht sterilen Rezeptur- und Defekturarzneimittel Qualitätsmanagement Handbuch 20148 Hamburg Herstellung und Prüfung der nicht sterilen Rezeptur- und Defekturarzneimittel Version
Herstellung der Zubereitungen zur Anwendung am Auge
 Leitlinie Kommentar Arbeitshilfe Arbeitshilfe der Bundesapothekerkammer zur Qualitätssicherung ANWENDUNGSBEISPIEL Herstellung der Zubereitungen zur Anwendung am Auge Stand der Revision: 08.05.2018 Leitlinie:
Leitlinie Kommentar Arbeitshilfe Arbeitshilfe der Bundesapothekerkammer zur Qualitätssicherung ANWENDUNGSBEISPIEL Herstellung der Zubereitungen zur Anwendung am Auge Stand der Revision: 08.05.2018 Leitlinie:
ARBEITSBOGEN 11: ARZNEIMITTELBERATUNG ÄRZTLICHE VERORDNUNGEN
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten über ein Fertigarzneimittel (FAM) bei der Abgabe im Rahmen einer ärztlichen Verordnung. Grundlage des Arbeitsbogens
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten über ein Fertigarzneimittel (FAM) bei der Abgabe im Rahmen einer ärztlichen Verordnung. Grundlage des Arbeitsbogens
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Versand der Arzneimittel aus der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 28.04.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 28.04.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Was ist geändert? Apothekenbetriebsordnung Amtsapotheker Georg Bühmann. Warum neue Apothekenbetriebsordnung?
 Apothekenbetriebsordnung 2012 Was ist geändert? Amtsapotheker Georg Bühmann Gesetze macht der Bund, die Einhaltung überwachen die Länder Warum neue Apothekenbetriebsordnung? NRW: Amtsapotheker bei den
Apothekenbetriebsordnung 2012 Was ist geändert? Amtsapotheker Georg Bühmann Gesetze macht der Bund, die Einhaltung überwachen die Länder Warum neue Apothekenbetriebsordnung? NRW: Amtsapotheker bei den
Vierte Verordnung zur Änderung der Apothekenbetriebsordnung. Krankenhausapotheken? Dr. Gabriele Wanninger Regierung von Oberbayern
 Vierte Verordnung zur Änderung der Apothekenbetriebsordnung Was ändert sich für f r die Krankenhausapotheken? Dr. Gabriele Wanninger Begriffsbestimmungen 1a (neu) Begriffsbestimmungen Einführung von 17
Vierte Verordnung zur Änderung der Apothekenbetriebsordnung Was ändert sich für f r die Krankenhausapotheken? Dr. Gabriele Wanninger Begriffsbestimmungen 1a (neu) Begriffsbestimmungen Einführung von 17
Einführung 9. 1 Die amtliche Besichtigung der Apotheke l.i
 3 Inhaltsverzeichnis Einführung 9 1 Die amtliche Besichtigung der Apotheke l.i 1.1 Die verschiedenen Besichtigungsarten 1.1 1.1.1 Die Abnahmebesichtigung 1.2 1.1.2 Die routinemäßige Überwachung (Regelbesichtigung)
3 Inhaltsverzeichnis Einführung 9 1 Die amtliche Besichtigung der Apotheke l.i 1.1 Die verschiedenen Besichtigungsarten 1.1 1.1.1 Die Abnahmebesichtigung 1.2 1.1.2 Die routinemäßige Überwachung (Regelbesichtigung)
Versand der Arzneimittel aus der Apotheke
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 23.11.2016 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 23.11.2016 Inhaltsverzeichnis
Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit CMR-Eigenschaften der Kategorie 1A oder 1B
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit CMR-Eigenschaften der Kategorie 1A oder
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Aseptische Herstellung und Prüfung applikationsfertiger Parenteralia mit CMR-Eigenschaften der Kategorie 1A oder
Durchführung der Plausibilitätsprüfung nach 7 Apothekenbetriebsordnung
 11 Durchführung der Plausibilitätsprüfung nach 7 Apothekenbetriebsordnung Seit der Novellierung der Apothekenbetriebsordnung im Frühjahr 2012 ist jede Apotheke verpflichtet, vor der Herstellung einer Rezeptur
11 Durchführung der Plausibilitätsprüfung nach 7 Apothekenbetriebsordnung Seit der Novellierung der Apothekenbetriebsordnung im Frühjahr 2012 ist jede Apotheke verpflichtet, vor der Herstellung einer Rezeptur
Durchführung der Plausibilitätsprüfung nach 7 Apothekenbetriebsordnung
 11 Durchführung der Plausibilitätsprüfung nach 7 Apothekenbetriebsordnung Seit der Novellierung der Apothekenbetriebsordnung im Frühjahr 2012 ist jede Apotheke verpflichtet, vor der Herstellung einer Rezeptur
11 Durchführung der Plausibilitätsprüfung nach 7 Apothekenbetriebsordnung Seit der Novellierung der Apothekenbetriebsordnung im Frühjahr 2012 ist jede Apotheke verpflichtet, vor der Herstellung einer Rezeptur
Gewusst wie Basistipps für die Rezeptur
 Gewusst wie Basistipps für die Rezeptur In der Herstellung von Rezepturen wird die neue Apothekenbetriebsordnung (ApBetrO) einiges ändern. So ist etwa eine Plausibilitätskontrolle offiziell vorgeschrieben,
Gewusst wie Basistipps für die Rezeptur In der Herstellung von Rezepturen wird die neue Apothekenbetriebsordnung (ApBetrO) einiges ändern. So ist etwa eine Plausibilitätskontrolle offiziell vorgeschrieben,
ARBEITSBOGEN 1: HALTBARKEIT, LAGERUNG UND ENTSORGUNG DER FERTIGARZNEIMITTEL, MEDI- ZINPRODUKTE, APOTHEKENÜBLICHEN WAREN UND AUSGANGSSTOFFE
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren Sie sich über die Haltbarkeit, Lagerung und Entsorgung der Fertigarzneimittel (FAM), Medizinprodukte (MP), apothekenüblichen Ware und Ausgangsstoffe
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren Sie sich über die Haltbarkeit, Lagerung und Entsorgung der Fertigarzneimittel (FAM), Medizinprodukte (MP), apothekenüblichen Ware und Ausgangsstoffe
Selbstinspektionsprotokoll gemäß 2a ApBetrO
 Mielke / Paul Selbstinspektionsprotokoll gemäß 2a ApBetrO Mitra Mielke, Köln Monika Paul, Köln Für die Durchführung der Selbstinspektion im Zeitraum (Monat/Jahr) bis (Monat/Jahr) Allgemeine Angaben zur
Mielke / Paul Selbstinspektionsprotokoll gemäß 2a ApBetrO Mitra Mielke, Köln Monika Paul, Köln Für die Durchführung der Selbstinspektion im Zeitraum (Monat/Jahr) bis (Monat/Jahr) Allgemeine Angaben zur
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement. Stand der Revision:
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 04.05.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 04.05.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Fallbeispiel Cora Emsig Schritt 4: Rezeptur herstellen. Lösungen und Diskussionsansätze
 Fallbeispiel Cora Emsig Schritt : Rezeptur herstellen Lösungen und Diskussionsansätze Fallbeispiel Cora Emsig, Teil Hygienemanagement bei der Herstellung Zeitplanung/Arbeitsorganisation Verpflichtung der
Fallbeispiel Cora Emsig Schritt : Rezeptur herstellen Lösungen und Diskussionsansätze Fallbeispiel Cora Emsig, Teil Hygienemanagement bei der Herstellung Zeitplanung/Arbeitsorganisation Verpflichtung der
Wareneingang und Prüfung von Fertigarzneimitteln
 30 7 Wareneingang und Prüfung von Fertigarzneimitteln 7.1 Prüfung von Fertigarzneimitteln Wird pro Arbeitstag mindestens ein Fertigarzneimittel organoleptisch geprüft und die Prüfung dokumentiert? Es Auslegung
30 7 Wareneingang und Prüfung von Fertigarzneimitteln 7.1 Prüfung von Fertigarzneimitteln Wird pro Arbeitstag mindestens ein Fertigarzneimittel organoleptisch geprüft und die Prüfung dokumentiert? Es Auslegung
Hygiene und Lagerung. 11. Juli Neue Apothekenbetriebsordnung Informationsveranstaltung von LAK und LAV
 Hygiene und Lagerung 11. Juli 2012 1 HYGIENEMAßNAHMEN 11. Juli 2012 2 Hygienemaßnahmen Neu aufgenommen in 4a ApoBetrO Der Apothekenleiter muss für das Personal und die Betriebsräume, die zur Arzneimittelherstellung
Hygiene und Lagerung 11. Juli 2012 1 HYGIENEMAßNAHMEN 11. Juli 2012 2 Hygienemaßnahmen Neu aufgenommen in 4a ApoBetrO Der Apothekenleiter muss für das Personal und die Betriebsräume, die zur Arzneimittelherstellung
Regulatorische und rechtliche Aspekte zur Zulassungspflicht von Magistralrezepturen
 Regulatorische und rechtliche Aspekte zur Zulassungspflicht von Magistralrezepturen Symposium Anforderungen an Rezepturbestandteile für topische Dermatika GD Gesellschaft für Dermopharmazie e.v. 08.10.2013
Regulatorische und rechtliche Aspekte zur Zulassungspflicht von Magistralrezepturen Symposium Anforderungen an Rezepturbestandteile für topische Dermatika GD Gesellschaft für Dermopharmazie e.v. 08.10.2013
Fischer / Schüler Rezeptur Qualität in 7 Schritten
 Fischer / Schüler Rezeptur Qualität in 7 Schritten Fischer / Schüler Rezeptur Qualität in 7 Schritten Ulrike Fischer, Dresden Katrin Schüler, Dresden Mit 55 Abbildungen und 101 Tabellen Checklisten, Arbeitsblätter
Fischer / Schüler Rezeptur Qualität in 7 Schritten Fischer / Schüler Rezeptur Qualität in 7 Schritten Ulrike Fischer, Dresden Katrin Schüler, Dresden Mit 55 Abbildungen und 101 Tabellen Checklisten, Arbeitsblätter
Dokumentationshilfe Einzelhändler - Arzneimittelrecht
 Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Aktueller Stand der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer
 Aktueller der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer Name des Dokumentes ARZNEIMITTELINFORMATION Arzneimittelinformation in der Apotheke (Leitlinie und Kommentar ) Dokumentationsbogen
Aktueller der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer Name des Dokumentes ARZNEIMITTELINFORMATION Arzneimittelinformation in der Apotheke (Leitlinie und Kommentar ) Dokumentationsbogen
Informationsquellen. für die Erstellung der Plausibilität von Rezepturarzneimitteln. Susanne Funke, Apothekerin bei pharma4u
 Informationsquellen für die Erstellung der Plausibilität von Rezepturarzneimitteln Susanne Funke, Apothekerin bei pharma4u 14.01.2015 Rezepturanforderung: Augentropfen Tropicamid 0,5g Phenylephrinhydrochlorid
Informationsquellen für die Erstellung der Plausibilität von Rezepturarzneimitteln Susanne Funke, Apothekerin bei pharma4u 14.01.2015 Rezepturanforderung: Augentropfen Tropicamid 0,5g Phenylephrinhydrochlorid
Physiologisch-chemische Untersuchungen Durchführung der Blutuntersuchungen
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Physiologisch-chemische Untersuchungen Durchführung der Blutuntersuchungen Stand der Revision: 15.05.2014 Inhaltsübersicht
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Physiologisch-chemische Untersuchungen Durchführung der Blutuntersuchungen Stand der Revision: 15.05.2014 Inhaltsübersicht
Wenn der Pharmazierat kommt
 Wenn der Pharmazierat kommt Überwachung der öffentlichen Apotheken in Hessen durch das Regierungspräsidium Darmstadt 1 Besichtigung erfolgt in der Regel alle 3 Jahre Besichtigungen werden nicht angemeldet
Wenn der Pharmazierat kommt Überwachung der öffentlichen Apotheken in Hessen durch das Regierungspräsidium Darmstadt 1 Besichtigung erfolgt in der Regel alle 3 Jahre Besichtigungen werden nicht angemeldet
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Medikationsanalyse. Leitlinie Kommentar Arbeitshilfe. Stand der Revision:
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 29.11.2017 (S. 3 aktualisiert am 12. Juni 2018 wegen des Inkrafttretens der DS-GVO) Leitlinie
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 29.11.2017 (S. 3 aktualisiert am 12. Juni 2018 wegen des Inkrafttretens der DS-GVO) Leitlinie
UPDATE 1/2015 PROGRAMMVERSION 7.3.1
 UPDATE 1/2015 PROGRAMMVERSION 7.3.1 TOPITEC DokuManager TOPITEC DokuManager 7.3.1 Was ist neu? Mit TOPITEC DokuManager 7.3.1 erhalten Sie neue Programmfeatures, die Ihnen den Arbeitsablauf erleichtern.
UPDATE 1/2015 PROGRAMMVERSION 7.3.1 TOPITEC DokuManager TOPITEC DokuManager 7.3.1 Was ist neu? Mit TOPITEC DokuManager 7.3.1 erhalten Sie neue Programmfeatures, die Ihnen den Arbeitsablauf erleichtern.
Die Prüfung der Ausgangsstoffe. Eine Hilfe zur Umsetzung
 Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung Gesetzliche Vorgaben Apothekenbetriebsordnung (ApBetrO) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen
Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung Gesetzliche Vorgaben Apothekenbetriebsordnung (ApBetrO) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen
ADKA-Leitlinie für die Herstellung und Prüfung von Arzneimitteln in der Krankenhausapotheke
 Leitlinie Inhaltsverzeichnis I II III IV V I Präambel ADKA-Leitlinie für die Herstellung und Prüfung von Arzneimitteln in der Krankenhausapotheke Stand der letzten Änderung: 2.6.2016 Expertengremium: Cornelia
Leitlinie Inhaltsverzeichnis I II III IV V I Präambel ADKA-Leitlinie für die Herstellung und Prüfung von Arzneimitteln in der Krankenhausapotheke Stand der letzten Änderung: 2.6.2016 Expertengremium: Cornelia
Bundesverband Deutscher Krankenhausapotheker e.v.
 Bundesverband Deutscher Krankenhausapotheker e.v. Leitlinie für die Herstellung und Prüfung von Arzneimitteln in der Krankenhausapotheke Stand der letzten Änderung: 02.06.2016 Expertengremium: Cornelia
Bundesverband Deutscher Krankenhausapotheker e.v. Leitlinie für die Herstellung und Prüfung von Arzneimitteln in der Krankenhausapotheke Stand der letzten Änderung: 02.06.2016 Expertengremium: Cornelia
Kommentar zu den Empfehlungen der Bundesapothekerkammer zur Qualitätssicherung
 Leitlinie Kommentar Arbeitshilfe Kommentar zu den Empfehlungen der Bundesapothekerkammer zur Qualitätssicherung Stand: 14.11.2006 (Kapitel VII-1.1 aktualisiert am 20.09.2010) Die Erläuterungen sind eine
Leitlinie Kommentar Arbeitshilfe Kommentar zu den Empfehlungen der Bundesapothekerkammer zur Qualitätssicherung Stand: 14.11.2006 (Kapitel VII-1.1 aktualisiert am 20.09.2010) Die Erläuterungen sind eine
Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr. Abnahme-, Regel-, Kurz-, Nachbesichtigung
 Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr Apothekenanschrift mit Telefon (Stempel): Abnahme-, Regel-, Kurz-, Nachbesichtigung Teilnehmer:......... Datum der letzten Besichtigung:...
Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr Apothekenanschrift mit Telefon (Stempel): Abnahme-, Regel-, Kurz-, Nachbesichtigung Teilnehmer:......... Datum der letzten Besichtigung:...
FIT FÜR DIE ANALYTIK. Ingrid Tieke Caesar & Loretz GmbH
 FIT FÜR DIE ANALYTIK Ingrid Tieke Caesar & Loretz GmbH Interpharm 2017 Fit für die Analytik Ingrid Tieke Caesar & Loretz GmbH Interpharm, 1. April 2017 Gliederung 1. Gesetzliche Anforderungen an die Qualität
FIT FÜR DIE ANALYTIK Ingrid Tieke Caesar & Loretz GmbH Interpharm 2017 Fit für die Analytik Ingrid Tieke Caesar & Loretz GmbH Interpharm, 1. April 2017 Gliederung 1. Gesetzliche Anforderungen an die Qualität
Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch
 Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch Click here if your download doesn"t start automatically Deutscher Arzneimittel-Codex
Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch Click here if your download doesn"t start automatically Deutscher Arzneimittel-Codex
Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch
 Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch Click here if your download doesn"t start automatically Deutscher Arzneimittel-Codex
Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch Click here if your download doesn"t start automatically Deutscher Arzneimittel-Codex
Aktueller Stand der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer
 Aktueller der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer Name des Dokumentes ARZNEIMITTELINFORMATION Arzneimittelinformation in der Apotheke und in Informationsstellen der Apothekerschaft
Aktueller der Leitlinien, Kommentare und Arbeitshilfen der Bundesapothekerkammer Name des Dokumentes ARZNEIMITTELINFORMATION Arzneimittelinformation in der Apotheke und in Informationsstellen der Apothekerschaft
Fit für die Plausibilitätsprüfung. Ingrid Tieke Caesar & Loretz GmbH
 Fit für die Plausibilitätsprüfung Ingrid Tieke Caesar & Loretz GmbH Hilden, 22. Juni 2016 Gliederung 1. Dosierung 2. Applikationsart 3. Wirkstoffart 4. Menge 5. Bedenkliche Arzneistoffe? 6. Kompatibilitätsprüfung
Fit für die Plausibilitätsprüfung Ingrid Tieke Caesar & Loretz GmbH Hilden, 22. Juni 2016 Gliederung 1. Dosierung 2. Applikationsart 3. Wirkstoffart 4. Menge 5. Bedenkliche Arzneistoffe? 6. Kompatibilitätsprüfung
ARBEITSBOGEN 6: ARZNEIMITTELBERATUNG SELBSTMEDIKATION
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten im Rahmen der Selbstmedikation. Grundlage des Arbeitsbogens ist die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten im Rahmen der Selbstmedikation. Grundlage des Arbeitsbogens ist die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
Defekturherstellung in der Apotheke
 Defekturherstellung in der Apotheke 28. Januar 2014 Magdeburg Dr. Michael Hörnig Deutscher Arzneimittel-Codex Eschborn DAC/NRF-Publikationen DAC/NRF Govi Verlag Carl Mannich Str. 20 65760 Eschborn Dr.
Defekturherstellung in der Apotheke 28. Januar 2014 Magdeburg Dr. Michael Hörnig Deutscher Arzneimittel-Codex Eschborn DAC/NRF-Publikationen DAC/NRF Govi Verlag Carl Mannich Str. 20 65760 Eschborn Dr.
18. Symposium Herstellung in der Krankenhausapotheke 18. Januar 2019, Berlin Defekturprüfung: Plausibilität abschätzen Prüfungen reduzieren
 18. Symposium Herstellung in der Krankenhausapotheke 18. Januar 2019, Berlin Defekturprüfung: Plausibilität abschätzen Prüfungen reduzieren Dr. Michael Hörnig DAC/NRF, Eschborn Herstellung von Defekturarzneimitteln
18. Symposium Herstellung in der Krankenhausapotheke 18. Januar 2019, Berlin Defekturprüfung: Plausibilität abschätzen Prüfungen reduzieren Dr. Michael Hörnig DAC/NRF, Eschborn Herstellung von Defekturarzneimitteln
ALLE MENSCHEN SIND GLEICH
 ALLE MENSCHEN SIND GLEICH Ihr Medikament sollte es auch sein. Nur in Ihrer Apotheke. MENSCHEN SIND EINZIGARTIG IHRE GESUNDHEIT IST ES AUCH Individuell gefertigte Medikamente. Damit es Ihnen gut geht. Alle
ALLE MENSCHEN SIND GLEICH Ihr Medikament sollte es auch sein. Nur in Ihrer Apotheke. MENSCHEN SIND EINZIGARTIG IHRE GESUNDHEIT IST ES AUCH Individuell gefertigte Medikamente. Damit es Ihnen gut geht. Alle
Dermatologische Rezepturen
 Leitlinie der GD Gesellschaft für Dermopharmazie e. V. Dermatologische Rezepturen GD Gesellschaft für Dermopharmazie Gustav-Heinemann-Ufer 92 50968 Köln Tel.: 02162/67454 Fax: 02162/80589 E-Mail: webmaster@gd-online.de
Leitlinie der GD Gesellschaft für Dermopharmazie e. V. Dermatologische Rezepturen GD Gesellschaft für Dermopharmazie Gustav-Heinemann-Ufer 92 50968 Köln Tel.: 02162/67454 Fax: 02162/80589 E-Mail: webmaster@gd-online.de
TOPITEC DokuManager Update-Version 7.3.1
 Inhalt der Power-Point-Präsentation Teil 1: NEU! Aktivierung Teil 2: NEU! Filialverbund Teil 3: Vorstellung der neuen Menüleiste Teil 4: Systemverwaltung Teil 5: NEU! Fernwartung Teil 6: NEU! Herstellungsanweisung
Inhalt der Power-Point-Präsentation Teil 1: NEU! Aktivierung Teil 2: NEU! Filialverbund Teil 3: Vorstellung der neuen Menüleiste Teil 4: Systemverwaltung Teil 5: NEU! Fernwartung Teil 6: NEU! Herstellungsanweisung
Vorblatt. Vierte Verordnung zur Änderung der Apothekenbetriebsordnung
 Vorblatt Vierte Verordnung zur Änderung der Apothekenbetriebsordnung A. Problem und Ziel Die Apothekenbetriebsordnung vom 9. Februar 1987 wurde seit ihrem Inkrafttreten punktuell geändert, sie bedarf nunmehr
Vorblatt Vierte Verordnung zur Änderung der Apothekenbetriebsordnung A. Problem und Ziel Die Apothekenbetriebsordnung vom 9. Februar 1987 wurde seit ihrem Inkrafttreten punktuell geändert, sie bedarf nunmehr
Gesetzliche Vorgaben. Sammlung pharmazeutischer Regeln. Gesetzliche Vorgaben. Die Prüfung der Ausgangsstoffe. Eine Hilfe zur Umsetzung
 Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung 19.02.2008 Monika Paul 2 Sammlung pharmazeutischer Regeln Europäische Arzneibuch (Ph. Eur.) mit den harmonisierten Monographien Deutsche Arzneibuch
Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung 19.02.2008 Monika Paul 2 Sammlung pharmazeutischer Regeln Europäische Arzneibuch (Ph. Eur.) mit den harmonisierten Monographien Deutsche Arzneibuch
Vierte Verordnung zur Änderung der Apothekenbetriebsordnung
 Bundesrat Drucksache 61/12 03.02.12 Verordnung des Bundesministeriums für Gesundheit G - Fz Vierte Verordnung zur Änderung der Apothekenbetriebsordnung A. Problem und Ziel Die Apothekenbetriebsordnung
Bundesrat Drucksache 61/12 03.02.12 Verordnung des Bundesministeriums für Gesundheit G - Fz Vierte Verordnung zur Änderung der Apothekenbetriebsordnung A. Problem und Ziel Die Apothekenbetriebsordnung
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Vierte Verordnung zur Änderung der Apothekenbetriebsordnung
 - 1 - Vierte Verordnung zur Änderung der Apothekenbetriebsordnung Auf Grund des Vom... 21 Absatz 1 in Verbindung mit Absatz 2 und 3 des Apothekengesetzes, dessen Absatz 1 zuletzt durch Artikel 34 der Verordnung
- 1 - Vierte Verordnung zur Änderung der Apothekenbetriebsordnung Auf Grund des Vom... 21 Absatz 1 in Verbindung mit Absatz 2 und 3 des Apothekengesetzes, dessen Absatz 1 zuletzt durch Artikel 34 der Verordnung
Vorschriftenbuch für STADA-Lizenznehmer
 Vorschriftenbuch für STADA-Lizenznehmer Gesamtausgabe 11.06.2012 Herausgeber: STADA Arzneimittel AG Stadastraße 2 18 61118 Bad Vilbel Telefon: 06101 603-0 Telefax: 06101 603-259 Vorstand: Hartmut Retzlaff
Vorschriftenbuch für STADA-Lizenznehmer Gesamtausgabe 11.06.2012 Herausgeber: STADA Arzneimittel AG Stadastraße 2 18 61118 Bad Vilbel Telefon: 06101 603-0 Telefax: 06101 603-259 Vorstand: Hartmut Retzlaff
ARBEITSBOGEN 21: BESTIMMUNG PHYSIOLOGISCHER PARAMETER BLUTUNTERSUCHUNGEN
 I Hinweis zur Bearbeitung des Arbeitsbogens Führen Sie bei einem Patienten eine Blutuntersuchung durch und informieren und beraten Sie ihn über die Ergebnisse. Grundlage des Arbeitsbogens ist die Leitlinie
I Hinweis zur Bearbeitung des Arbeitsbogens Führen Sie bei einem Patienten eine Blutuntersuchung durch und informieren und beraten Sie ihn über die Ergebnisse. Grundlage des Arbeitsbogens ist die Leitlinie
Physiologisch-chemische Untersuchungen Durchführung der Blutuntersuchungen
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Physiologisch-chemische Untersuchungen Durchführung der Blutuntersuchungen Stand der Revision: 29.11.2017 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Physiologisch-chemische Untersuchungen Durchführung der Blutuntersuchungen Stand der Revision: 29.11.2017 Inhaltsverzeichnis
Ihr Fahrplan für Labor und Rezeptur
 Dr. Lennartz Ihr Fahrplan für Labor und Rezeptur BASISPROGRAMM Komfortable Prüfungs- und Herstellungsdokumentation nach ApBetrO für Ausgangsstoffe, Rezepturen, Defekturen und Fertigarzneimittel ZRB-MODUL
Dr. Lennartz Ihr Fahrplan für Labor und Rezeptur BASISPROGRAMM Komfortable Prüfungs- und Herstellungsdokumentation nach ApBetrO für Ausgangsstoffe, Rezepturen, Defekturen und Fertigarzneimittel ZRB-MODUL
Gerne stehen wir für Fragen und ergänzende Erläuterungen während der geplanten Anhörung zur Verfügung.
 BPAV e.v. Bundesministerium für Gesundheit Referat 114: Arzneimittelzulassung und -qualität, Apothekenbetrieb Heilsbachstr. 18 53123 Bonn Anhörung zur beabsichtigten Änderung der Apothekenbetriebsordnung
BPAV e.v. Bundesministerium für Gesundheit Referat 114: Arzneimittelzulassung und -qualität, Apothekenbetrieb Heilsbachstr. 18 53123 Bonn Anhörung zur beabsichtigten Änderung der Apothekenbetriebsordnung
Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am
 Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am 28.12.2005 Verordnung zur Neuordnung der Verschreibungspflicht von Arzneimitteln Es verordnen Vom 21. Dezember 2005 - das Bundesministerium
Bundesgesetzblatt Jahrgang 2005 Teil I Nr. 75, S. 3632, ausgegeben zu Bonn am 28.12.2005 Verordnung zur Neuordnung der Verschreibungspflicht von Arzneimitteln Es verordnen Vom 21. Dezember 2005 - das Bundesministerium
Praxishilfe Rezeptur Schritt-für-Schritt-Anleitungen für die Apotheke
 Reihe PTAheute Buch Müller-Bohn Betriebswirtschaft für die Apotheke, 2009 Weber Rezepte für die Beratung, 2009 PTAheute Redaktion Schwangerschaft und Apotheke, 2011 Rall Ernährungsberatung in der Apotheke,
Reihe PTAheute Buch Müller-Bohn Betriebswirtschaft für die Apotheke, 2009 Weber Rezepte für die Beratung, 2009 PTAheute Redaktion Schwangerschaft und Apotheke, 2011 Rall Ernährungsberatung in der Apotheke,
ARBEITSBOGEN 11: ARZNEIMITTELBERATUNG ÄRZTLICHE VERORDNUNGEN
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten über ein Fertigarzneimittel (FAM) bei der Abgabe im Rahmen einer ärztlichen Verordnung. Grundlage des Arbeitsbogens
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten über ein Fertigarzneimittel (FAM) bei der Abgabe im Rahmen einer ärztlichen Verordnung. Grundlage des Arbeitsbogens
VERANTWORTUNGSABGRENZUNGSVERTRAG (VAV)
 VERANTWORTUNGSABGRENZUNGSVERTRAG (VAV) für die Herstellung von Arzneimitteln in kleinen Mengen im Lohnauftrag 1. Gegenstand und Inhalt 1.1 Dieser VAV bildet den vertraglichen Rahmen zwischen Elvetix Pharma
VERANTWORTUNGSABGRENZUNGSVERTRAG (VAV) für die Herstellung von Arzneimitteln in kleinen Mengen im Lohnauftrag 1. Gegenstand und Inhalt 1.1 Dieser VAV bildet den vertraglichen Rahmen zwischen Elvetix Pharma
Zu 1 a Begriffsbestimmungen. Zu 2 a Qualitätsmanagementsystem
 Stellungnahme des Bundesverbandes Deutscher Apothekenkooperationen e.v. zum Referentenentwurf (RefE) zur Novellierung der Apothekenbetriebsordnung vom 20. Oktober 2011 gegenüber dem Bundesgesundheitsministerium
Stellungnahme des Bundesverbandes Deutscher Apothekenkooperationen e.v. zum Referentenentwurf (RefE) zur Novellierung der Apothekenbetriebsordnung vom 20. Oktober 2011 gegenüber dem Bundesgesundheitsministerium
4 Anforderungen und Voraussetzungen
 26 4 Anforderungen und Voraussetzungen 34 der Apothekenbetriebsordnung regelt die besonderen Vorrausetzungen und Bedingungen für das patientenindividuelle Stellen und Verblistern von Arzneimitteln in Apotheken.
26 4 Anforderungen und Voraussetzungen 34 der Apothekenbetriebsordnung regelt die besonderen Vorrausetzungen und Bedingungen für das patientenindividuelle Stellen und Verblistern von Arzneimitteln in Apotheken.
Niederschrift über die Apothekenbesichtigung gemäß 64 ff. des Arzneimittelgesetzes
 Landesamt für Gesundheit und Soziales 1 Landesamt für Gesundheit und Soziales Berlin Postfach 31 09 29, 10639 Berlin (Postanschrift) Tel.: 90229 2330, 2331 Fax: 90229 2097 Niederschrift über die Apothekenbesichtigung
Landesamt für Gesundheit und Soziales 1 Landesamt für Gesundheit und Soziales Berlin Postfach 31 09 29, 10639 Berlin (Postanschrift) Tel.: 90229 2330, 2331 Fax: 90229 2097 Niederschrift über die Apothekenbesichtigung
Seite 1 von 5. Merkblatt. betreffend die
 Seite 1 von 5 Landesuntersuchungsamt Rheinland-Pfalz Institut für Lebensmittelchemie und Arzneimittelprüfung, Mainz Merkblatt betreffend die Kennzeichnung von Arzneimitteln, die in öffentlichen Apotheken
Seite 1 von 5 Landesuntersuchungsamt Rheinland-Pfalz Institut für Lebensmittelchemie und Arzneimittelprüfung, Mainz Merkblatt betreffend die Kennzeichnung von Arzneimitteln, die in öffentlichen Apotheken
Ihr Fahrplan für Labor und Rezeptur
 Dr. Lennartz Ihr Fahrplan für Labor und Rezeptur BASISPROGRAMM Komfortable Prüfungs- und Herstellungsdokumentation nach ApBetrO für Ausgangsstoffe, Rezepturen, Fertigarzneimittel und Defekturen ZRB-MODUL
Dr. Lennartz Ihr Fahrplan für Labor und Rezeptur BASISPROGRAMM Komfortable Prüfungs- und Herstellungsdokumentation nach ApBetrO für Ausgangsstoffe, Rezepturen, Fertigarzneimittel und Defekturen ZRB-MODUL
Die neue Apothekenbetriebsordnung
 Die neue Apothekenbetriebsordnung Fortbildungsveranstaltung der Apothekerkammer Nordrhein Dr. Dagmar Krüger Bundesministerium für Gesundheit D. Krüger 2012 1 Verlauf nicht offizieller Arbeitsentwurf 2010
Die neue Apothekenbetriebsordnung Fortbildungsveranstaltung der Apothekerkammer Nordrhein Dr. Dagmar Krüger Bundesministerium für Gesundheit D. Krüger 2012 1 Verlauf nicht offizieller Arbeitsentwurf 2010
WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht. Mittwoch, 6. Januar Pandemie - Teil IX
 Ministerium für,,, und WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht Mittwoch, 6. Januar 2010 Pandemie - Teil IX -Dr. Michael Cramer-2010-01-06 Folie 1 Ministerium für,,, und Gesegnetes und Gesundes
Ministerium für,,, und WS 2009/2010 Vorlesung - Spezielles Arzneimittelrecht Mittwoch, 6. Januar 2010 Pandemie - Teil IX -Dr. Michael Cramer-2010-01-06 Folie 1 Ministerium für,,, und Gesegnetes und Gesundes
Apothekenbetriebsordnung 2012- Was ist neu für Rezeptur und Defektur? (ohne 35)
 Apothekenbetriebsordnung 2012- Was ist neu für Rezeptur und Defektur? (ohne 35) Ausschuss für Arzneimittelherstellung und Analytik R. Heimke-Brinck Neue Apothekenbetriebsordnung 12.Juni 2012 Ein Jahr später
Apothekenbetriebsordnung 2012- Was ist neu für Rezeptur und Defektur? (ohne 35) Ausschuss für Arzneimittelherstellung und Analytik R. Heimke-Brinck Neue Apothekenbetriebsordnung 12.Juni 2012 Ein Jahr später
Übersicht der Umstrukturierung
 F Regularien Schweiz und Österreich N.1 F.1 Regularien Schweiz N.1.1 F.1.1 Bundesgesetz über Arzneimittel und Medizinprodukte (Heilmittelgesetz, HMG) N.1.2 F.1.2 Verordnung über die Bewilligungen im Arzneimittelbereich
F Regularien Schweiz und Österreich N.1 F.1 Regularien Schweiz N.1.1 F.1.1 Bundesgesetz über Arzneimittel und Medizinprodukte (Heilmittelgesetz, HMG) N.1.2 F.1.2 Verordnung über die Bewilligungen im Arzneimittelbereich
Apothekenbetriebsordnung 2012
 Apothekenbetriebsordnung 2012 1 Anwendungsbereich (1) Diese Verordnung findet Anwendung auf den Betrieb und die Einrichtung von öffentlichen Apotheken einschließlich der krankenhausversorgenden Apotheken,
Apothekenbetriebsordnung 2012 1 Anwendungsbereich (1) Diese Verordnung findet Anwendung auf den Betrieb und die Einrichtung von öffentlichen Apotheken einschließlich der krankenhausversorgenden Apotheken,
Dermatologische Rezepturen
 Leitlinie der GD Gesellschaft Dermopharmazie e.v Dermatologische Rezepturen in der Fassung vom 18.03.2008 Gustav-Heinemann-Ufer 92 D-50968 Köln Tel.: +49 (0)2162/67454 Fax: + 49 (0)2162/80589 E-Mail: webmaster@gd-online.de
Leitlinie der GD Gesellschaft Dermopharmazie e.v Dermatologische Rezepturen in der Fassung vom 18.03.2008 Gustav-Heinemann-Ufer 92 D-50968 Köln Tel.: +49 (0)2162/67454 Fax: + 49 (0)2162/80589 E-Mail: webmaster@gd-online.de
Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke
 Landesamt für soziale Dienste Schleswig-Holstein - Abt. Gesundheitsschutz - Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke (ohne Versandhandel, Stellen/Verblistern, Krankenhaus-und Heimbelieferung,
Landesamt für soziale Dienste Schleswig-Holstein - Abt. Gesundheitsschutz - Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke (ohne Versandhandel, Stellen/Verblistern, Krankenhaus-und Heimbelieferung,
Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
 Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Stand der Revision:
Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Stand der Revision:
