Status der pränatalen Therapie von Risikoschwangerschaften mit Adrenogenitalem Syndrom und 21-Hydroxylase Defekt in Deutschland
|
|
|
- Sabine Albert
- vor 7 Jahren
- Abrufe
Transkript
1 Aus der Kinder- und Jugendklinik der Friedrich Alexander Universität Erlangen Nürnberg Direktor: Prof. Dr. med. Dr. h. c. W. Rascher Status der pränatalen Therapie von Risikoschwangerschaften mit Adrenogenitalem Syndrom und 21-Hydroxylase Defekt in Deutschland Effekte auf Fetus und Neugeborenes. Inaugural-Dissertation zur Erlangung der Doktorwürde an der Medizinischen Fakultät der Friedrich Alexander Universität Erlangen-Nürnberg vorgelegt von Mareike Vehorn aus Erlangen 2011
2 - 2 - Gedruckt mit Erlaubnis der Medizinischen Fakultät der Friedrich Alexander Universität Erlangen Nürnberg Dekan: Referent: Koreferent: Prof. Dr. med. Dr. h. c. Jürgen Schüttler Prof. Dr. med. H.G. Dörr Prof. Dr. med. Dr. h. c. Rascher Tag der mündlichen Prüfung: 14. Juli 2011
3 - 3 - Inhaltsverzeichnis I. Zusammenfassung S. 05 II. Summary S Einleitung S Pathophysiologie und Genetik S Klinik und Diagnostik S Therapie S Pränatale Diagnostik und Therapie S Zielsetzung der Arbeit S Methoden und Patienten S Datenerfassung in Erlangen S Methoden S Daten zur Familie und zum Indexfall S Angaben zur pränatalen Therapie S Klinische Parameter S Laborchemische Daten S Patientenkollektiv S Bis zum Termin therapierte Schwangerschaften S Bis zum Ergebnis der pränatalen Diagnostik therapierte S. 26 Schwangerschaften 3.4. Statistische Methoden S Ergebnisse S Intrauterine / Fetale Probleme S Gestationsalter / Entbindungsmodus / APGAR S Geburstsdaten S Geburtsgewicht S Geburtslänge S Kopfumfang bei Geburt S Komplikationen und Fehlbildungen bei Geburt S Praderstadien der weiblichen AGS Neugeborenen bei Geburt S Neugeborenenperiode der bis zur Geburt therapierten S. 36 Neugeborenen 4.7. Neugeborenenperiode aller AGS Neugeborenen S Diskussion S Glukokortikoide im Tierversuch S. 40
4 Glukokortikoide in der Schwangerschaft S Intrauterine / fetale Probleme S Gestationsalter / Entbindungsmodus / APGAR S Geburtsmaße S Geburtsgewicht S Geburtslänge S Kopfumfang S Komplikationen und Fehlbildungen S Praderstadien S Dexamethason in der Schwangerschaft und Nebenwirkungen der S. 50 Mutter 5.9. Neugeborenenperiode S Langzeitfolgen S Literaturverzeichnis S Anlagen S Fragebogen an die betroffenen Familien S Fragebogen an die behandelnden Ärzte S Danksagung S Lebenslauf S. 73
5 - 5 - I. Zusammenfassung 1. Hintergrund und Ziele Die pränatale Therapie des klassischen AGS mit 21-Hydroxylase-Defekt hat das Ziel, die intrauterine Virilisierung weiblicher Feten mit AGS zu verhindern, den Mädchen aufwendige Genitalkorrekturoperationen zu ersparen und den psychosozialen Stress, der für die Familie mit der Geburt eines Mädchens mit intersexuellem Genitale verbunden ist, zu vermeiden. Die Therapie ist auch 30 Jahre nach ihrer Einführung weiterhin eine experimentelle Therapie; die Anwendung von Dexamethason in der Schwangerschaft ist Off-Label-use. Alle Risikoschwangerschaften müssen zunächst "blind" behandelt werden. Die Familie muss wissen, dass statistisch betrachtet sieben von 8 Feten unnötig behandelt werden. Als Dosis wird Dexamethason in 3 Einzeldosen zu je 0.5 mg/d (Richtdosis: 20 µg/kg/d) empfohlen. Nur wenn die pränatale Diagnostik ergibt, dass der Fetus weiblich und homozygot erkrankt ist, wird die Therapie kontinuierlich bis zum Ende der Schwangerschaft fortgeführt. In allen anderen Fällen wird sie beendet. Die bisher publizierten Daten zeigen, dass die Therapie sicher und effektiv ist, wenn sie adäquat durchgeführt wird. Mütterliche Nebenwirkungen traten selten auf (vermehrte Gewichtszunahme, Striae, Ödeme) und waren nach Absetzen von Dexamethason reversibel. Die pränatal behandelten Neugeborenen hatten bei Geburt nahezu alle normale Geburtsmaße, Fehlbildung wie eine Lippen-Kiefer-Gaumenspalte wurden nicht berichtet. 2. Methoden Im Jahr 1990 wurde von der Arbeitsgemeinschaft/Sektion für Pädiatrische Endokrinologie (APE/SPE) beschlossen, dass die Fälle, die den Kinderendokrinologen bekannt sind, auch zentral (Kinder- und Jugendklinik der Universität Erlangen) dokumentiert werden. Eine finanzielle Unterstützung des Projekts war dabei nicht vorgesehen. Ein Fragebogen wurde entwickelt und an alle Pädiatrischen Endokrinologen unter der Vorstellung verschickt, dass diese von der Familie (mit Indexfall) auch über künftige Schwangerschaften informiert werden. Der Fragebogen wurde aber auch an die betroffenen Familien und an die Gynäkologen verschickt, deren Name und Adresse bekannt waren. Das Ausfüllen der Fragebögen erfolgte auf freiwilliger Basis; es gab keine finanzielle Unterstützung.
6 Ergebnisse und Beobachtungen Ziel der vorliegenden Arbeit war es, die Daten, die in Erlangen seit 1990 gesammelt wurden, auszuwerten. Dabei lag der Schwerpunkt auf den Daten, die den Fetus und das Neugeborene betrafen. Anhand der Unterlagen konnten wir 158 AGS Risikoschwangerschaften identifizieren. Aufgrund der Unvollständigkeit der Daten, konnten aber letzthin nur 94 Risikoschwangerschaften erfasst werden. Davon wurden 34 bis zum Geburtstermin behandelt und bei 60 Schwangerschaften wurde die Therapie vorzeitig beendet. Bis zum Geburtstermin wurden 31 weibliche Feten behandelt, wobei das AGS in 28 Fällen auch postnatal bestätigt werden konnte. Bei einem weiblichen Feten wurde pränatal eine Fehldiagnose gestellt, in zwei Fällen (beide nicht betroffen) wurde keine pränatale Diagnostik durchgeführt. Alle behandelten weiblichen AGS-Feten wurden am Termin geboren (22 spontan vaginal, 6 per Sectio). Das Praderstadium der behandelten Neugeborenen mit AGS lag im Median bei Prader 2, während die weiblichen Index-Patientinnen ein Stadium Prader 4 hatten. Die Kinder, die vor der 8. Schwangerschaftswoche pränatal behandelt wurden, hatten ein Prader-Genitale von im Mittel 0,97, während diejenigen, die nach der 8. Woche mit der Therapie begonnen wurde, ein Prader-Genitale von 3,56 hatten. Die pränatale Therapie hatte keinen signifikanten Einfluss auf Geburtsgewicht, Geburtslänge, Kopfumfang oder eine erhöhte Rate an postnatalen Fehlbildungen oder Komplikationen. Die Geburtsmaße lagen bis auf 2 Fälle (Geburtsgewicht < -2 SD) im Normbereich. Eine detaillierte Auswertung der Daten aus der Neugeborenenphase war nicht möglich, da der postnatale Verlauf der Neugeborenen sehr lückenhaft dokumentiert wurde. 4. Praktische Schlussfolgerungen Unsere Daten zeigen, dass die Dokumentation der pränatalen Therapie und die Qualität der pränatalen Therapie dringend verbessert werden muss. Protokolle zur Nachsorge der pränatal behandelten Kinder und Mütter müssen entwickelt und umgesetzt werden.
7 - 7 - II. Summary Prenatal Dexamethasone (Dex) treatment of pregnant women at risk for congenital adrenal hyperplasia (CAH) should prevent female genital virilization in order to avoid complex reconstructive surgery and the emotional distress associated with the birth of a child with ambiguous genitalia. The published results are promising, yet, this treatment, more than 30 years after its introduction, is still an experimental therapeutic option. There is an ongoing discussion regarding ethical concerns with this therapy. All pregnancies at risk for CAH have to be treated, because pathologically excessive androgen synthesis begins before prenatal diagnosis is possible. The treatment is potentially beneficial for only one in eight fetuses. Treatment must be started as soon as the woman knows that she is pregnant (ideally before 6 wks of gestation). The pregnant mother is given 0.5 mg dexamethasone three times a day (guideline dose: 20 µg/kg and day). If prenatal diagnosis reveals that the fetus is female and homozygous for CAH, therapy is continued to the end of pregnancy. In all other cases, the treatment is discontinued after stepwise dose reduction. The limited data published in the literature show that prenatal therapy is effective in eliminating virilization of external genitalia. Among the women treated until term, there is data on a greater weight gain, increased rate of striae and increased edema. But overall, no enduring complications in the mothers were found and to date the treated newborns have not demonstrated any teratological effects from dexamethasone. In 1990, the German Working Group for Pediatric Endocrinology proposed documenting all prenatally treated cases in one institution (Dept. Pediatrics, Erlangen). A questionnaire was developed and sent out primarily to all pediatric endocrinologists, as they were likely to treat the index cases and to know about prenatal treatments. The questionnaire was also sent out to affected families (treated women) and gynecologists when names and addresses became announced. The completion of the questionnaire was voluntarily; there was no support by any institution. At present, data of 158 pregnancies at risk for CAH have been collected. Due to incompleteness of the data, only a cohort of 94 pregnancies could be analyzed yet. To date, we have identified 34 pregnancies (31 female fetuses) that were treated with Dex until term. Prenatal diagnosis was confirmed postnatally in 28/31 female newborns. In one case, the prenatal
8 - 8 - diagnosis was incorrect; and 2 fetuses (not affected) were treated without any prenatal diagnosis. The female newborns treated prenatally with CAH were born at term (22 spontaneous, 6 caesarean section) with a normal birthweight in 26 cases; only 2 newborns had a birth weight < -2 SD. All prenatally treated female CAH newborns had a median genital stage of Prader 2, whereas their untreated female CAH siblings had a stage Prader 4. Those newborns, who were treated before week 8 of gestational age, had a mean Prader stage of 0,97 in contrast to those who were treated after week 8 of gestation who had a mean Prader stage of 3,56. There are no long-term data available on the outcome of prenatally treated mothers and children in Germany. Despite published recommendations, there is strong evidence that prenatal therapy with Dex has been used in recent years in a rather uncritical way. Our data show that the documentation and quality of prenatal therapy has to be improved. It is necessary to develop standardized protocols to analyse the long-term followup of prenatally treated children and their mothers.
9 Einleitung 1.1. Pathophysiologie und Genetik Das Adrenogenitale Syndrom (AGS, engl. Congenital Adrenal Hyperplasia (CAH)) ist eine autosomal - rezessive Stoffwechselerkrankung, die durch Störungen der Kortisolbiosynthese in der Nebennierenrinde (NNR) gekennzeichnet ist. Die NNR produziert drei Hormongruppen: Mineralokortikoide, Glukokortikoide und Androgene (Abb.1). Abb. 1. Steroidbiosynthese der Nebennierenrinde. Steroide: DOC = 11-Desoxycorticosteron, 17-OH-Preg = 17-Hydroxy-pregnenolon, 17-OH-Prog = 17-Hydroxyprogesteron, DHEA = Dehydro-epiandrosteron. Trivialnamen der Enzyme: P450SCC = 20,22 Desmolase, 3βHSD2 = 3β- Hydroxysteroiddehydrogenase Typ 2, P450C17 = 17-Hydroxylase/17,20-Lyase, P450C21 = 21-Hydroxylase, P450Aldo = Aldosteronsynthase, P450C11 = 11- Hydroxlyase. In 90-95% der Fälle besteht ein 21-Hydroxylase-Mangel, der mit einer Inzidenz von 1: : und mit einer Heterozygotenfrequenz von 1:55 vorkommt. Aufgrund des Enzymdefekts können AGS Patienten nur unzureichend Cortisol produzieren, weshalb es zu einer Überstimulierung durch ACTH kommt, dadurch zu einem Überangebot an Steroiden vor dem Enzymdefekt und zu einem Mangel an Steroiden nach dem Enzymdefekt. Betrachtet man die Abb. 1, dann sind beim AGS mit 21-Hydroxylasedefekt vor allem Progesteron und 17-OH-Progesteron massiv erhöht und Aldosteron und Cortisol erniedrigt. Der Genort für die 21-Hydroxylase liegt auf dem kurzen Arm des 6. Chromosoms. Es existieren 2 dicht beieinander liegende Gene, ein aktives Gen CYP21A2 und ein inaktives Pseudogen CYP21A1. Beide Gene haben eine hohe Homologie, die enge Nachbarschaft des Pseudogens mit dem aktiven Gen hat eine kausale Bedeutung
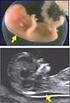
10 für die Entstehung zahlreicher Gendefekte. Bisher wurden über 70 verschiedene Gendefekte beim klassischen 21-Hydroxylase-Defekt beschrieben z.b. Mutationen im CYP21A2 Gen oder Gendefekte, die im Pseudo-Gen vorkommen und durch Genkonversion ins aktive Gen gelangen. Am häufigsten kommen bei den klassischen AGS-Patienten folgende drei Mutationen vor: 8bp-Deletion, Intron-2- Mutation sowie eine Exon-4-Mutation (Sperling et al., 2008) Die Restaktivität der 21-Hydroxylase im in-vitro System bestimmt den Phänotyp. Eine Aktivität von 2-4% reicht aus, um einen Salzverlust zu verhindern. Allerdings kann es bei unzureichender Substitution auch bei diesen Patienten zu einer Dekompensation mit Salzverlustkrise kommen. Bei einer homozygoten Mutation mit einer Restaktivität über 20% entwickelt sich in fast allen Fällen ein nicht-klassisches AGS. Bei den meisten Patienten werden Kombinationen verschiedener Mutationen nachgewiesen (compound Heterozygotie), was zu einer weiteren Unsicherheit bei der Beurteilung des Phänotyps führt Klinik und Diagnostik Beim klassischen AGS mit 21-OHlase-Defekt sind die betroffenen Feten bereits pränatal, vor allem in der Phase der Geschlechtsdifferenzierung, hohen Androgenspiegeln ausgesetzt, sodass es bei den weiblichen Feten zu einer Vermännlichung der äußeren Genitalorgane kommt. Die pränatale Virilisierung wird als eine Störung der Geschlechtsdifferenzierung (disorder of sexual differentiation = DSD 46 XX) charakterisiert; in Abhängigkeit von der Schwere des Enzymdefekts kommt es zu unterschiedlichen Ausprägungen der Genitalveränderungen, die nach Prader mit 1-5 klassifiziert werden (Abb. 2). Betroffene männliche Neugeborene mit klassischem AGS fallen postnatal nicht auf, weil sie oft nur eine Hyperpigmentierung des Genitales aufweisen. Der Androgenexzess führt unbehandelt postnatal bei beiden Geschlechtern zu einer Pseudopubertas praecox. Ca. 75 % der Kinder mit 21-Hydroxylase-Mangel haben eine schwere Form des AGS mit Salzverlust. Die betroffenen Neugeborenen mit Salzverlust werden meistens ca. 2-3 Wochen nach Geburt auffällig, wenn es zu einer Salzverlustkrise kommt. Die Kinder fallen durch Gedeihstörung, Erbrechen, Apathie, Hyponatriämie, Hyperkaliämie, metabolische Azidose und Exsikkose auf.
11 Abb. 2: Einteilung der Virilisierung des äußeren Genitales nach Prader (Nimkarn and New, 2009) Die Diagnostik erfolgt mittels Bestimmung von 17-Hydroxy-progesteron (17-OHP) im Serum, wobei die Konzentrationen bereits postnatal massiv erhöht sind. Ein generelles Neugeborenen-Screening mit Bestimmung von 17-OHP im Vollblut am 3. Lebenstag wird durchgeführt. Im Harn findet man mittels Kapillargaschromatographie / Gaschromatographie-Massenspektrometrie ein charakteristisches Steroidprofil, wobei insbesondere Pregnantriol (Abbauprodukt von 17-OHP) massiv erhöht ist. Neben 17-OHP sind im Serum auch Testosteron, 21-Desoxycortisol und Androstendion erhöht. Beim Salzverlust findet man neben den typischen Elektrolytveränderungen eine erhöhte Renin-Konzentration im Serum Therapie Mittel der Wahl ist die Substitution mit dem physiologischen Glukokortikoid Hydrokortison (HC) und beim Salzverlustsyndrom zusätzlich mit einem Mineralokortikoid (9α-Fludrocortison). Die HC-Tagesdosis (ca mg/m 2 KOF) wird üblicherweise in 3 Dosen verabreicht, wobei in der Regel 50 % der Tagesdosis morgens, 25 % mittags und abends verabreicht werden. Die Morgendosis wird in der Regel morgens nach dem Aufstehen eingenommen. Es liegen aber keine kontrollierten Studien vor, die belegen, dass dieses Vorgehen richtiger ist als drei gleiche Dosen oder abends die höhere Dosis zu geben. Jeder Patient muss
12 individuell eingestellt und regelmäßig geschult (auch die Familie) werden. Die Glukokortikoiddosis muss bei Stresssituationen auf Tagesdosen von bis zu 100 mg/ m 2 /d angehoben werden. Besonders bei Infektionen, chirurgischen Eingriffen und großen Operationen muss die Therapie intensiviert werden. Bei einer Unterdosierung mit Glukokortikoiden verbleibt das Problem der Hyperandrogenämie, während bei einer Überdosierung mit Glukokortikoiden ein iatrogener Hyperkortisolismus die Folge ist. In beiden Fällen kommt es bei Kindern zu negativen Effekten auf das Längenwachstum. Eine Optimierung der Mineralokortikoidtherapie (Dosis ca µg/tag; 2-3 x täglich) ist ebenfalls umstritten, zumal es auch bei den klassischen AGS-Formen zu fließenden Übergängen kommt. Findet man auch beim unkomplizierten AGS über einen Zeitraum von einigen Monaten konstant erhöhte Renin-Konzentrationen sollte mit einer Mineralokortikoidsubstitution begonnen werden, wobei dann oft die Gesamtmenge an Glukokortikoiden reduziert werden kann. Die Ziele der Therapie sind im Kindesalter klar definiert: adäquate Genitalkorrekturoperation (Mädchen), normales Gedeihen und Längenwachstum, Verhinderung von Übergewicht, normaler Blutdruck, Erreichen einer normalen Erwachsenengröße (im genetischen Zielbereich), normale Pubertätsentwicklung, sowie Verhinderung von Salzverlustkrisen. Die adäquate und geregelte Weiterbetreuung der jungen erwachsenen Patienten mit AGS durch einen erfahrenen Erwachsenenendokrinologen sollte für jeden Kinderendokrinologen selbstverständlich sein. Ein weiterer wichtiger Aspekt betrifft die Korrekturoperation des Genitales der weiblichen AGS-Patienten, die meistens zwischen dem 10. und 15. Lebensmonat vorgenommen wird. Generell gehört zu einer feminisierenden Korrektur-OP die sensibilitätserhaltende Reduktion der Klitoris und die Vaginalplastik (Ogilvie et al., 2006a;Ogilvie et al., 2006b) Dabei können die kosmetischen Ergebnisse recht unterschiedlich sein (vgl. Abb. 3 A-C) und auch in der Pubertät noch Probleme machen. Mögliche Komplikationen sind Stenosen, Sensibilitätsstörungen und Schmerzen beim Geschlechtsverkehr (Ogilvie et al., 2006a).
13 Abb. 3 A: Genitale einer Patientin vor und nach OP ein als hervorragend gewertetes Ergebnis Abb. 3 B: Patientin vor und nach OP ein als gut gewertetes Ergebnis
14 Abb. 3 C: Patientin vor und nach OP als normal gewertetes Ergebnis Abb. 3 A-C: Beispiele für Ergebnisse nach Korrektur OPs bei Mädchen mit AGS (Sircili et al., 2006) Die meisten AGS-Frauen haben eine eindeutige Geschlechtsidentität, dennoch haben einige von ihnen Probleme mit der Sexualität. Sei es in Form von Schamgefühl und Hemmungen im täglichen Umgang, aber auch bzgl. Parästhesien im OP-Gebiet (Crouch et al., 2004). So konnte eine Untersuchung zeigen, dass im Vergleich zu einer Kontrollgruppe mehr AGS-Frauen als Single leben und wenn sie verheiratet waren, dann weniger Kinder hatten (Kuhnle et al., 1995;Jaaskelainen et al., 2000;Helleday et al., 1993). Ursächlich werden verschiedene Aspekte genannt: Anovulation aufgrund des Androgen-Überschusses, Hyperandrogenismus, erhöhte adrenale Progesteronproduktion, mangelhaftes Ergebnis der Genitalkorrekturoperation sowie psychosexuelle Probleme (Jaaskelainen et al., 2001) Pränatale Diagnostik und Therapie Die pränatale Diagnostik des AGS mit 21-OHLase-Defekt ist mittels Amniozentese und Chorionzottenbiopsie möglich. Bei Einführung der pränatalen Therapie war nur die Diagnostik mittels Amniozentese (HLA-Typisierung von Zellen und/oder Messung von 17OHP + Androstendion) möglich. Hierfür muss die Dexamethason- Therapie ca. 5 Tage vor Amniozentese unterbrochen werden, da sonst die Steroidspiegel im Fruchtwasser supprimiert sind. Die pränatale Therapie wird noch am Tag der Amniozentese wieder aufgenommen.
15 Das Risiko einer Fehlgeburt, liegt bei der Amniozentese bei ca. 0,3 1 % und bei der Chorionzottenbiopsie etwa bei 1 2 %. Dennoch ist heute ist die Chorionzottenbiopsie in der 9. bzw. 10. Woche Mittel der ersten Wahl, da sie eine frühere Diagnosestellung als die Amniozentese (ca Woche) ermöglicht. Die Zeit einer unnötigen Einnahme von Dexamethason wird durch die Chorionzottenbiopsie verkürzt. Eine Unterbrechung der pränatalen Therapie ist ebenfalls nicht nötig. Eine Indikation zur Amniozentese kann sich aber in den Fällen ergeben, wo keine Chorionzottenbiopsie möglich ist (z.b. heterozygote Eltern ohne Indexfall, Kontraindikation für die transzervikale Chorionzottenbiopsie). Vor der pränatalen Diagnostik und Therapie muß eine eingehende Beratung in einem humangenetischen Institut durchgeführt werden. Die pränatale Diagnostik sollte im Falle eines pathologischen Befundes nicht zwangsläufig einen Schwangerschaftsabbruch implizieren. Eine Kontaktaufnahme mit dem molekularbiologischen Labor, welches die spezielle molekulargenetische Diagnostik durchführt, ist notwendig. Die Aufklärung der Eltern über mögliche Nebenwirkungen der pränatalen Therapie für Mutter und Kind sollte schriftlich erfolgen. Um eine möglichst rasche Diagnostik in der Schwangerschaft zu ermöglichen, sollte das Ergebnis der molekulargenetischen DNA-Analyse des Indexfalles und der Eltern bereits vorliegen. Die Beratung sollte daher bereits vor einer erneuten geplanten Schwangerschaft erfolgen. Nach Etablierung der pränatalen Diagnostik des AGS mittels Amniozentese oder Chorionzottenbiopsie, wurde die Frage gestellt, ob nicht auch eine pränatale Therapie möglich sei. Die pränatale Therapie des AGS mit 21-Hydroxylase-Defekt hat das Ziel, die intrauterine Virilisierung weiblicher Feten mit AGS zu verhindern und den Mädchen aufwendige Genitalkorrekturoperationen zu ersparen. Hierfür ist die pränatale Therapie in der Frühschwangerschaft nötig, da die Entwicklung und Ausbildung des Genitale bereits vor der 9. Woche beginnt und eine Behandlung zur Verhinderung der Vermännlichung vor diesem Zeitpunkt begonnen werden muss [3]. Die Therapie wird vor Kenntnis des Genotyps bzw. vor Kenntnis der genauen Diagnostik begonnen und entsprechend des Befundes beendet oder fortgeführt (Abb. 5). Der Vorteil der Chorionzottenbiopsie ist, dass das Ergebnis eher vorliegt, als wenn eine Amniozentese durchgeführt werden würde. Der weltweit erste Fall einer erfolgreichen pränatalen Therapie wurde 1984 publiziert, die pränatale Therapie ist somit bereits über 25 Jahre alt [1, 2].
16 Mittel der Wahl ist das potente Glukokortikoid Dexamethason, das von der Plazenta nicht metabolisiert werden kann und dadurch ein materno-fetaler Gradient von 1:1 erreicht wird. Da die Genitaldifferenzierung zwischen der 7. und 13. Woche abläuft, muss mit der Therapie unmittelbar nach Feststellung der Schwangerschaft (5./6.Woche) begonnen werden. Die Therapie muss initial blind begonnen werden, d.h. es werden auch gesunde bzw. betroffene heterozygote weibliche und männliche, sowie homozygote männliche Feten behandelt. Die Familie muss wissen, dass - statistisch betrachtet - sieben von 8 Feten unnötig behandelt werden. Als Startdosis wird Dexamethason (20 µg/kg KG) aufgeteilt in 3 Einzeldosen pro Tag empfohlen. Ein einfaches Flussschema für die pränatale Therapie ist in der Abb.4 dargestellt. Die Betreuung der Risiko-Schwangerschaft kann nur von erfahrenen Gynäkologen durchgeführt werden. Neben der regelmäßigen Kontrolle von Blutdruck, Gewicht, Blutzucker, HBA1c und Urin müssen mögliche Nebenwirkungen von Dexamethason sorgfältig beobachtet werden. Um die Effektivität der Therapie, d.h. Suppression der fetalen Nebenniere, zu überwachen, empfiehlt sich die Bestimmung von Östriol im mütterlichen Serum oder Harn. Abb. 4: Zeitachse der pränatalen sexuellen Differenzierung in Relation zum Zeitpunkt der Chorionzottenbiopsie (CVS) bzw. Amniozentese {Saenger, /id}
17 Im Jahr 1990 wurde von der Arbeitsgemeinschaft/Sektion für Pädiatrische Endokrinologie (APE/SPE) beschlossen, dass die Fälle, die den Kinderendokrinologen bekannt gemacht werden, zentral in Erlangen (Kinder- und Jugendklinik der Universität Erlangen, Prof. Dr. HG Dörr) dokumentiert werden sollen. Eine finanzielle Unterstützung des Projekts war dabei nicht vorgesehen. Ein Fragebogen wurde entwickelt und zunächst an alle Pädiatrischen Endokrinologen unter der Vorstellung verschickt, dass diese von der Familie (mit Indexfall) auch über künftige Schwangerschaften informiert werden. Der Fragebogen wurde in den letzten Jahren regelmäßig überarbeitet und zuletzt eine Version für die betroffene Mutter/Familie und eine Version für den Arzt entwickelt, wobei der Arztfragebogen vom zuständigen Gynäkologen ausgefüllt werden soll. Die Fragebögen können auch über das Internet (Homepage der APE/SPE und der AGS Selbsthilfegruppe abgerufen werden bzw. werden auch auf Anfrage zur Verfügung gestellt. Das Ausfüllen der Fragebögen erfolgt auf freiwilliger Basis Abb. 5: Vorgehensweise bei der pränatalen Diagnose und Therapie; nach (Speiser and White, 2003) modifiziert
18 Zielsetzung der Arbeit Ziel dieser Arbeit ist es, die in der Datenbank in Erlangen erfassten Fälle von pränatal therapierten AGS-Risikoschwangerschaften auszuwerten, wobei der Fokus auf die Kinder gelegt wurde. In einer anderen Doktorarbeit wurde der Schwerpunkt auf die Schwangerschaft und die Mutter gelegt. In dieser Arbeit sollen folgende Fragen beantwortet werden: 1. Wie ist der aktuelle Stand der erfassten Fälle im Jahr 2009? 2. Wie vollständig liegen die Daten vor? 3. Welche Einflüsse hat die Therapie auf Geburtsgewicht, Länge, Kopfumfang und Praderstadium bei den Neugeborenen? 4. Gibt es Unterschiede bei den Neugeborenen, die intrauterin nur über wenige Wochen behandelt wurden im Vergleich zu denen, die bis zum Termin therapiert wurden? 5. Kommt es im Rahmen der Therapie gehäuft zu Fehlbildungen oder andere Auffälligkeiten? 6. Wie war der postnatale Verlauf bei den Neugeborenen?
19 Methoden und Patienten 3.1. Datenerfassung in Erlangen Die erste erfolgreiche pränatale Therapie in Deutschland wurde 1983 in München bei einer Patientin von Professor Dr. D. Knorr durchgeführt. Zusammen mit diesem Fall wurden seitdem in Erlangen (Stichtag: ) bisher 158 AGS Risikoschwangerschaften erfasst, die sich über ganz Deutschland verteilen. Da anfangs in München im Labor der von Haunerschen Kinderklinik auch die Steroidbestimmung im Fruchtwasser zur pränatalen Diagnostik erfolgte, wurde von den einsendenden Humangenetischen Instituten neben dem Datum der Amniozentese oft nur der Name der betroffenen Frau, der Beginn der Dexamethason-Therapie und die Dosis übermittelt. So fehlten anfänglich Daten zum Verlauf der Schwangerschaft oder zur Geburt komplett. Daher wurde 1990 von der Arbeitsgemeinschaft/Sektion für Pädiatrische Endokrinologie (APE/SPE) beschlossen, dass die Fälle, die den Kinderendokrinologen bekannt gemacht wurden, zentral in Erlangen (Kinder- und Jugendklinik der Universität Erlangen, Prof. Dr. Dörr) dokumentiert werden sollen. Die Datensammlung erfolgte zunächst retrospektiv und seit 1990 prospektiv mittels standardisierter Fragebogen (siehe Anlage). Man musste allerdings rasch erkennen, dass viele Bögen von den Ärzten nur sehr unvollständig ausgefüllt wurden. Daher wurde versucht, die Eltern einzubeziehen und neben dem Arztfragebogen ein spezieller Elternbogen entwickelt. Auch hier kamen oft unvollständig ausgefüllte Fragebögen zurück. Erst als die AGS-Eltern-/Patienteninitiative e.v. mit in die Verantwortung genommen wurde, verbesserte sich die Qualität. Der Fragebogen wurde in den letzten Jahren mehrfach überarbeitet und in den abgefragten Parametern vereinfacht. So werden z.b. folgende Parameter abgefragt: Geburtsdatum von Mutter, Indexfall und Risikokind; Angaben zu Gewichtszunahme, Nebenwirkungen, Überwachung und Art der Dexamethasontherapie bei der behandelten Mutter sowie Geschlecht, Gestationsalter, Körperlänge, Geburtsgewicht, Prader - Stadium und Salzverlust des Neugeborenen aus der behandelten Risikoschwangerschaft. In den letzten Jahren wurde der Bogen um Daten in der Neonatalphase sowie um Fragen zum aktuellen Befinden des Kindes ergänzt (siehe Anhang). Trotz aller Anstrengungen blieben die Daten zu 64 Risikoschwangerschaften so unvollständig, sodass sie nicht für die Auswertung in Frage kamen. Für die weitere Auswertung wurden daher nur die Fragebögen eingeschlossen, die zu ca. 80 % ausgefüllt
20 waren. Nur diese wurden als vollständig gewertet wurden. So lagen insgesamt 94 auswertbare Fragebögen vor Methoden Die Angaben zum Schwangerschaftsverlauf und den Patienten wurden aus den vorliegenden Fragebögen, z.t. aus zusätzlich vorhandenen Arztbriefen, Krankenakten, diversen Unterlagen und Vorsorgeheften der Kinder gewonnen und in einem SPSS Datenblatt erfasst. Im Anhang sind die aktuell verwendeten Fragebögen (Arzt-/Elternbogen) dargestellt Daten zur Familie und dem Indexfall Erhoben wurden Angaben zum Alter der Mutter und des Indexfalles, Geschlecht, Art der vorliegenden AGS-Form (Salzverlust oder unkompliziertes AGS) und bei weiblichen Index-Kindern auch das Praderstadium Angaben zur pränatalen Therapie Für den Therapieverlauf wurden Therapiebeginn (SSW), Therapiedosis (Einzeldosis, Tages- und kumulative Dosis) ermittelt. Aus diesen Werten wurde die Therapiedauer berechnet. Bei der Mutter wurde erfasst, ob während der Therapie verschiedene Hormone (Östriol und Cortisol im Serum der Mutter sowie Östriol im Urin der Mutter) überwacht und kontrolliert wurden. Die von den Müttern gemachten Angaben zu Nebenwirkungen und Auffälligkeiten während der Schwangerschaft wurden ebenfalls erfasst Klinische Parameter Erhoben wurden bei Geburt Daten wie Gestationsalter, Körpergewicht und länge, Kopfumfang und APGAR der Neugeborenen nach pränataler Therapie. Im Falle eines mit AGS betroffenen Kindes auch ob ein Salzverlust vorlag und bei weiblichen Neugeborenen das Praderstadium des Genitales. Erfasst wurden ob Fehlbildungen vorlagen, zusätzlich der Beginn der postnatalen Therapie sowie die Art und Höhe der verabreichten Medikamente. Ergänzend wurden die Daten zum Gewicht der Mutter vor Beginn und bei Ende der Therapie erfasst bzw. bei Schwangerschaftsende. Für die Geburtsgewichte und Körperlängen bei Geburt der
21 Kinder wurden die Standardabweichungen und die Perzentilen nach Voigt et al. berechnet (Voigt, 2006) Laborchemische Daten Erfasst wurden die postnatalen 17-OHP-Werte, sowie die Serumwerte für Natrium und Kalium 3.3. Patientenkollektiv Für die vorliegende Auswertung standen die Daten von 94 AGS- Risikoschwangerschaften zur Verfügung. Es gab vier Familien ohne Indexfall, wobei die Eltern als heterozygote Genträger bekannt waren. In 78 Fällen lag der Indexfall vor (38 männliche und 40 weibliche Indexfälle). In 12 Fällen konnten sich retrospektiv die Daten nicht mehr einholen oder ergänzen lassen, sodass deren genauer Status unbekannt blieb. Die weiblichen Indexkinder (n=44) waren überwiegend schwer virilisiert. So hatten 4,5% (n=2) ein Genitale nach Prader 5, 63,6% (n=28) ein äußeres Genitale Grad 4, 20, 5% (n=9) ein Genitale Grad 3, 9,1% (n=4) ein Genitale nach Prader 2 und 2,3% (n=1) ein Genitale nach Prader 1. Das Alter der Mütter lag zwischen 19 und 40 Jahren (Median 31,5 Jahre). Die pränatale Diagnostik wurde zwischen der 8. und 23. SSW durchgeführt: Chorionzottenbiopsie n = 39; Amniozentese n = 35; Chorionzottenbiopsie + Amniozentese n = 1. In 5 Fällen konnte nicht mehr nachvollzogen werden, ob eine Amniozentese oder eine Chorionzottenbiopsie gemacht worden ist. Zu nur 2 Fällen erhielten wir die Angabe, dass die betroffene Frau die Diagnostik abgelehnt hatte, jedoch im Verlauf durchtherapiert wurde. Bei 12 Schwangerschaften waren keine Daten zu Art und Zeitpunkt der pränatalen Diagnostik zu ermitteln. Die Amniozentesen erfolgten in den Jahren von 1983 bis 1999, sowie zur Bestätigung des Ergebnisses der Chorionzottenbiopsie in einem Fall im Jahr 2005; sonst wurde in den Jahren von 1990 bis 2008 ausschließlich die Chorionzottenbiopsien durchgeführt. Für die Amniozentese wurde die Dexamethasontherapie pausiert. Die Pausen vor der Amniozentese betrugen zwischen einem Tag und 77 Tagen. Der Median lag bei 5 Tagen.
22 Nach dem Ergebnis der genetischen Untersuchung wird über das Fortführen der Therapie entschieden (vgl. Abb.4). Nur in den Fällen, in denen die pränatale Diagnostik homozygot betroffene weibliche Feten ergab, sollte bis zum Geburtstermin weiterbehandelt werden. Auch in einigen Fällen, in denen keine pränatale Diagnostik erfolgte, wurde Dexamethason bis zur Geburt verabreicht. In allen anderen Fällen (männlicher Fet mit oder ohne AGS, weiblich heterozygot bzw. nicht betroffen) sollte die Therapie beendet werden. Die Dexamethasontherapie wurde in ausschleichender Dosierung (n = 34) oder durch Absetzen (n = 13) des Dexamethason beendet. Bei ausschleichender Variante der Dexamethasondosis wurde zunächst um ein mg reduziert im weiteren Verlauf jeweils im Abstand von einigen Tagen um ½ bzw ¼ mg, sodass nach im Schnitt 10 Tagen die Dosis beendet wurde. Diese langsame Reduktion der Dexamethasondosen über Wochen sollte die Nebenwirkungen bei der Mutter verhindern oder so gering wie möglich zu halten. Leider fehlten auch bei diesem Parameter in 13 Fällen die Angaben, in welcher Art und Weise die Therapie beendet wurde. Die Therapie mit Dexamethason wurde zwischen der 5. und 13. Schwangerschaftswoche (Mittelwert 7,15 SSW) begonnen. Therapiert wurden die Mütter mit Tagesdosen zwischen 0,5 mg und 2,0 mg Dexamethason (MW: 1,33 mg), wobei die Dauer zwischen 3 und 37 Wochen (im Mittel über 17,8 Wochen) lag. Die Dexamethasondosis wurde zu Beginn in den ersten Jahren empirisch und versuchsweise mit 1 x 0.5 mg / Tag begonnen. Aufgrund der Ergebnisse der Virilisierung der Mädchen wurde die Dosis dann sukzessiv gesteigert, sodass sich ab ca die auch derzeit übliche Dosis von 3 x 0.5 mg / Tag etabliert hatte. In 4 Fällen wurde die Dexamethasondosis in der Spätschwangerschaft (ab SSW) reduziert.
23 Anzahl der Fälle keine Angabe Therapiedauer in SSW Abb. 6: Anzahl der therapierten Fälle mit Therapiedauer in Wochen Bei Betrachtung des Gesamtkollektivs ergeben sich zwei Gruppen (siehe Abb. 5): Erstens die Schwangerschaften, bei denen Dexamethason bis zum Termin verabreicht wurde, und zweitens die Schwangerschaften, in denen die Therapie beendet wurde, weil nach dem Ergebnis der pränatalen Diagnostik kein weiblicher homozygoter AGS-Fetus vorlag. In der Gruppe, die bis zum Termin behandelt wurde, war kein Spontanabort in der Frühschwangerschaft zu verzeichnen. In der Gruppe, bei der die Therapie beendet wurde, zeigte sich ein Spontanabort und zwei durchgeführte Schwangerschaftsabbrüche. Der Grund für den Spontanabort in der Frühschwangerschaft war nicht mehr nachzuvollziehen. Bei den beiden Abruptios handelte es sich um ein Kind mit Klinefelter-Syndrom und AGS, sowie um ein AGS Mädchen. In beiden Fällen sah sich die Mutter nach Erhalt des Ergebnisses der Amniozentese nicht in der Lage das Kind auszutragen, sodass eine Abruptio durchgeführt wurde. In einem einzigen Fall musste die Therapie aufgrund von Nebenwirkungen bei der Mutter beendet werden, wobei der weibliche Fetus ein AGS hatte. Zusammenfassend wurden von den 94 Risiko-Schwangerschaften, 34 bis zum Geburtstermin therapiert und bei 60 Schwangerschaften die pränatale Therapie vorzeitig beendet.
24 Bis zum Termin mit Dexamethason behandelte Schwangerschaften Insgesamt wurden 34 Risiko-Schwangerschaften mit Einlingen von 33 Frauen (eine Frau wurde bei 2 Risikoschwangerschaften therapiert) im Alter zwischen 19 und 40 Jahren (Mittelwert 31,4 Jahre) bis zum Termin mit Dexamethason behandelt. In zwei Fällen lag kein Indexfall vor, in 9 Fällen handelte es sich um einen männlichen Indexfall und in 13 Fällen um weibliche Indexfälle. Zu den übrigen Indexfällen (n=10) lagen bzgl. des Geschlechts keine Daten vor. Bei den Frauen handelte es sich in den meisten Fällen um die 2. bzw. 3. Schwangerschaft (Mittelwert 2,91). Lediglich in 2 Fällen war die behandelte Schwangerschaft die erste und in jeweils 2 Fällen handelte es sich um die 5. Schwangerschaft bzw. um die 6. Schwangerschaft. Die Frauen nahmen Dexamethason insgesamt zwischen 26 und 37 Wochen lang ein (MW 31,6 Wochen). In vier Fällen wurde die Dexamethason Dosis in der Spätschwangerschaft reduziert. Es wurden keine Fehlgeburten oder Aborte verzeichnet. Es wurden 11 Chorionzottenbiopsien und 15 Amniozentesen durchgeführt. In einem Fall verweigerte die Mutter die pränatale Diagnostik, jedoch mit dem Wunsch bis zum Schwangerschaftsende weitertherapiert zu werden. Sie wurde dann eines Jungen entbunden. In 7 Fällen war nicht nachzuvollziehen, was an pränataler Diagnostik gemacht wurde. Die Therapie wurde bei den Frauen zwischen der 5. und 13. Woche (Mittelwert: 7,76) begonnen und die Kinder kamen zwischen der 35. und 42. SSW (Median: 40. SSW) Schwangerschaftswoche in vielen Fällen per spontan vaginaler Entbindung (n = 25) zur Welt. Nur wenige kamen per Sectio caesarea (n =8: primär n=4 bzw. sekundär n=4) zur Welt. In einem Fall waren keine Angeben zum Entbindungsmodus gemacht worden. Im Kollektiv befand sich ein Frühgeborenes aus der 35. SSW. Die Frauen wurden insgesamt zwischen 26 und 37 Wochen (Mittelwert: 31,7) mit einer mittleren kumulativen Dexamethasondosis von 303,5 mg therapiert. Diese kumulative Dexamethasondosis wurde als objektiver Wert zur Vergleichbarkeit der individuellen Dosen berechnet. Dafür wurde die jeweilige Tagesdosis mit der Anzahl der Wochen und den 7 Tagen einer Woche multipliziert.
25 Postnatal wurden 31 weibliche Neugeborene geboren, von denen 28 an einem AGS erkrankt waren, Bei einem weiblichen Neugeborenen Mädchen konnte die pränatale Diagnose nicht bestätigt werden und zwei Mädchen hatten kein AGS (allerdings keine pränatale Diagnostik). Von den 3 männlichen Neugeborenen war eines gesund und zwei hatten ein AGS (vgl. Abb. 7). Patientenkollektiv - 94 Risikoschwangerschaften mit pränataler Therapie - 99 Feten 34 Schwangerschaften bis zum Termin therapiert 60 Schwangerschaften, vorzeitig beendet - 34 Einlinge (33 Frauen) postnatal: 31 weibliche Neugeborene - 28 AGS - 1 AGS postnatal nicht bestätigt - 2 kein AGS (keine pränatale Diagnostik) - 53 Einlinge (28 x m, 24x w); 1x NW Mutter (w, AGS) 1x w, AGS, pränatale Fehldiagnose 8x m, AGS 3 Zwillinge 2x m, kein AGS 2x m, kein AGS 1x w, kein AGS; 1x m, AGS - 1 Drillinge 1x w, AGS; 1x m; AGS; 1x w, 3 männliche Neugeborene postnatal: n = 62 Kinder - 49 kein AGS - 13 AGS: - 10 männlich - 3 weiblich Abb. 7.: Überblick über das Patientenkollektiv
26 Bis zum Ergebnis der pränatalen Diagnostik therapierte Schwangerschaften Von den 94 behandelten Risikoschwangerschaften wurde bei 60 Frauen nach Kenntnis des Befundes der pränatalen Diagnostik die Therapie beendet (siehe auch Abb.7). In 11 Fällen wurde die Therapie abrupt abgesetzt, in 22 Fällen wurde sie über 10 Tage langsam ausgeschlichen und in 27 Fällen fehlten die Angaben zur Art der Beendigung der Therapie. In zwei Fällen waren die Eltern ohne Indexfall als heterozygot bekannt, in 24 Fällen handelte es sich um männliche und in 26 Fällen um weibliche Indexfälle. In 8 Fällen lagen leider keine Daten vor. Auch in dieser Gruppe handelte es sich bei den meisten Frauen um die 2. bzw. 3. Schwangerschaft (Mittelwert 2,74). In 2 Fällen war es die erste Schwangerschaft und in jeweils einem Fall war es die 5. bzw. die 6. Schwangerschaft. 2/60 Frauen waren Erstgebärende, bei 8 Frauen (13%) handelte es sich bereits um die 4. Schwangerschaft. In der Frühschwangerschaft zeigte sich in dieser Gruppe unter Therapie ein Spontanabort. Nach dem Ergebnis der Pränataldiagnostik erfolgten 2 Abruptios. In einem Fall bei einem weiblichen AGS-Feten, im anderen Fall bei einem Feten mit Klinefelter-Syndrom und AGS. In beiden Fällen sah sich die Mutter nicht in der Lage das Kind auszutragen. Bei den Frauen wurde zwischen der 5. und 10. Woche (Mittelwert: 6,82) mit der Therapie begonnen und zwischen der 8. und 24. Schwangerschaftswoche (Mittelwert: 15,8 SSW) beendet. Insgesamt wurden zwischen 3 und 20 Wochen behandelt (MW 9,02 Wochen) mit einer mittleren Dexamethasondosis von 84 mg therapiert. Eine Frau wurde ausschließlich in der Spätschwangerschaft von der 32. bis 36. SSW (1,0 mg Dexamethason-Tagesdosis in 2 Einzel-Dosen) behandelt. Bezüglich der Pränataldiagnostik wurde in 28 Fällen die Chorionzottenbiopsie, in 17 Fällen die Amniozentese, in einem Fall die Chorionzottenbiopsie und im Anschluss eine Amniozentese durchgeführt. In einem Fall verweigerte die Mutter die Diagnostik, sodass die Therapie beendet wurde und sie eines Jungen entbunden werden konnte. In 14 Fällen waren die Daten nicht mehr zu rekonstruieren. Die Neugeborenen kamen zwischen der 25. und 42. Schwangerschaftswoche (Median 40.SSW) zur Welt. Von den 5 Frühgeborenen war jeweils eines in der 25., 31. und 33. Schwangerschaftswoche, sowie zwei in der 36. SSW geboren worden.
27 Bei den 60 Schwangerschaften, in denen die pränatale Therapie vorzeitig beendet wurde, kamen 62 Neugeborene zur Welt, Es lagen neben 53 Einlingen (28 m und 24 w) auch 3 Zwillings- und eine Drillingsschwangerschaft vor. In 1 Fall kam es zu einem Spontanabort und bei 2 Fällen wurde eine Abruptio durchgeführt. (vgl. Abb. Patientenkollektiv). Geboren wurden in dieser Gruppe 62 Kinder (34 Jungen, 28 Mädchen), von denen hatten 49 Kinder kein AGS und 13 Kinder ein AGS (n=3 w, n=10 m). Von den drei weiblichen Neugeborenen mit AGS wurde in einem Fall die Therapie (Beginn 5. SSW; Dosis 3 x 0.5 mg/tag) aufgrund von Nebenwirkungen bei der Mutter in der 21. SSW beendet (Prader 4). Die mütterlichen Nebenwirkungen bestanden aus einer vermehrten Müdigkeit, rezidivierendem Erbrechen, Wechsel aus Appetitsteigerung und Inappetenz, generalisierte Ödeme, Gewichtszunahme um 20 kg). Bei den beiden anderen Fällen wurde pränatal eine Fehldiagnose gestellt. Diese beiden weiblichen Neugeborenen hatten bei Geburt ein Praderstadium 2 bzw. 4. Die Kinder kamen alle zwischen den Jahren 1985 und 2006 und zwischen der 25 und 42 Schwangerschaftswoche (Mittelwert 38,8 SSW) zur Welt. 43 Schwangerschaften endeten in einer vaginalen Entbindung (z. T. mit Hilfsmitteln wie einer gynäkologischen Zange oder einer Vakuumextraktion), 8 in einem primären, elektiven Kaiserschnitt und 3 in einem sekundären Kaiserschnitt. In einem Fall kam es zu einem Frühabort, in 2 Fällen erfolgte ein Abbruch der Schwangerschaft. In drei Fällen liegen keine Angaben vor. (vgl. Abb. 7) 3.4. Statistische Methoden Die Daten wurden in tabellarischer Form in eine SPSS Datei eingegeben. Mit Hilfe einer Excel Datei wurden unterschiedliche Parameter berechnet, neu adjustiert und für die Auswertung in SPSS vorbereitet. Für die endgültige Auswertung stand das SPSS Programm Version 18 zur Verfügung. Im Rahmen dessen wurden Minimum, Maximum, Standardfehler, Varianz, Mittelwerte, Signifikanz sowie qualitative und quantitative Häufigkeiten berechnet.
28 Ergebnisse 4.1. Intrauterine / fetale Probleme Bei vier Frauen wurde pränatal mittels Sonographie eine verzögerte Entwicklung des Kindes festgestellt. In drei Fällen war das in der durchtherapierten Gruppe zu beobachten, in einem Fall in der Gruppe, bei der die pränatale Therapie vorzeitig beendet wurde. Betrachtet man die Daten bei Geburt, so zeigt sich, dass alle auxologischen Parameter im Referenzbereich lagen, d.h. die Neugeborenen hatten das Defizit ausgeglichen. Die Längen-SDS lagen zwischen -0,77 und -1,5 SDS, die Gewichts-SDS zwischen -1,32 und +0,32 SDS und der SDS des Kopfumfangs zwischen -1,9 und +0,5 SDS. In der Gruppe der durchtherapierten AGS-Schwangerschaften fand sich kein Abort, während in der Gruppe der Schwangerschaften mit vorzeitig beendeter pränataler Therapie ein Abort in der Frühschwangerschaft berichtet wurde Gestationsalter/Entbindungsmodus/APGAR Sowohl beim Vergleich des Gestationsalters als auch beim 5-Minuten APGAR zeigt sich kein statistisch signifikanter Unterschied zwischen den Gruppen (Tab. 1). Tab. 1: Vergleich Gestationsalter und 5-Min.-APGAR-Werte in den beiden Gruppen; dargestellt MW und Range Gruppe durchtherapiert vorzeitig beendet Gestationsalter (MW in SSW) Range Mädchen 39, Jungen 39, Mädchen 39, Jungen 39, APGAR 5 Range Mädchen 8, Jungen 9, Mädchen 9, Jungen 9, Bei den 34 Schwangerschaften, die bis zum Termin behandelt wurden, erfolgte die Geburt zwischen der 35. und 42. SSW. in 25 Fällen vaginal (z. T. mit Hilfsmitteln wie einer gynäkologischen Zange oder einer Vakuumextraktion) bzw. in 8 Fällen (n=4
29 elektiv und n=4 sekundär) per Sectio caesarea. Zu einer Schwangerschaft fehlte die Angabe. Bei den 60 Schwangerschaften, die bis zum Termin behandelt wurden, erfolgte die Geburt zwischen der 35. und 42. SSW. Spontan-vaginal in 40 Fällen (z. T. mit Hilfsmitteln wie einer gynäkologischen Zange oder einer Vakuumextraktion), und per Sectio caesarea in 8 Fällen (n=5 elektiv und n=3 sekundär). Zu zwölf Schwangerschaften fehlen die Angaben. Vergleicht man den Entbindungsmodus (spontan vaginal vs. Schnittentbindung) und die Therapiedauer in Bezug auf die APGAR Werte, so zeigt sich bei der vaginalen Entbindung ein mittlerer 5 Minuten APGAR Wert von 9,05. Im Vergleich dazu haben die Kinder bei der Schnittentbindung mit einem 5 Minuten APGAR-Wert von 8,0 zwar niedrigere Werte, die aber statistisch nicht signifikant waren. Von den bis zur Geburt durchtherapierten Neugeborenen waren 3 männlich und 31 weiblich; die pränatale Diagnose AGS konnte bei 30/31 der weiblichen Neugeborenen bestätigt werden, in einem Fall handelte es sich um eine Fehldiagnose. Bei 3 Schwangerschaften, bei denen keine pränatale Diagnostik erfolgte, stellten sich die zwei weiblichen Neugeborenen als gesund heraus. Von den drei durchtherapierten Jungen hatten zwei ein AGS mit Salzverlust, während das dritte Kind gesund war. Die 62 Neugeborenen, bei denen die pränatale Therapie bereits intrauterin beendet wurde, kamen im Median in der 40. Schwangerschaftswoche (d.h. zwischen der 25. und 42. Schwangerschaftswoche) zur Welt. In diesem Kollektiv befand sich ein Frühgeborenes aus der 25. SSW. Von den 62 Neugeborenen wurden 44 spontanvaginal geboren (z. T. mit Hilfsmitteln wie einer gynäkologischen Zange oder einer Vakuumextraktion) und 11 nach Sektio (8 nach einer primären und 3 nach einer sekundären Sektio) geboren. In 7 Fällen fehlen die Angaben. Bei den APGAR Werten nach 5 und 10 Minuten, zeigte sich kein Unterschied zwischen den beiden Gruppen. Vergleicht man im den Entbindungsmodus (spontan vaginal vs. Schnittentbindung) und die Art der Therapiedauer in Bezug auf die APGAR Werte, so zeigt sich bei der vaginalen Entbindung ein 5 Min. APGAR Wert von im Mittel 9,05 (Range: 5-10 ) und ein 10 Min.-Wert von 9,51 (Range: 1-10). Im Vergleich dazu haben die Neugeborenen nach Sectio caesarea einen 5 Minuten
30 APGAR-Wert von 8,0 (Range: 6-10) und einen 10 Minuten-Wert von 9,0 (Range: 7-10). Ein signifikanter Zusammenhang zwischen der Dexamethasondosis und den APGAR Werten oder zwischen dem Entbindungsmodus und den APGAR Werten findet sich aber nicht Geburtsdaten Geburtsgewicht Die Kinder wurden zwischen der 25. und 42. Gestationswoche mit unterschiedlichen Geburtsgewichten geboren. Dabei lag das Gewicht zwischen 1530 g und 4990 g bzw. bei -2,47 und +3,59 SDS. In der Gruppe der Neugeborenen, die bis zur Geburt mit Dexamethason behandelt wurden, war ein SGA-Neugeborenes mit -2,19 SDS zu finden. In der Gruppe, wo die pränatale Therapie vorzeitig beendet wurde, fand sich ebenfalls ein SGA-Neugeborenes mit -2,47 SDS. In dieser Gruppe fand sich aber auch ein hypertrophes (Large for gestational age) Neugeborenes mit einem Gewicht von +3,59 SDS. Analysiert man die Geburtsgewichte genauer, so zeigt sich, dass die Kinder, die bis zum Termin behandelt wurden, im Mittel etwas leichter als die waren, bei denen die Therapie vorzeitig beendet wurde. (Tab.2). Dieser Unterschied war statistisch nicht signifikant.
31 Tab. 2: Vergleich der Geburtsmaße nach pränataler Therapie in Relation zur Referenzgruppe Gewicht (g) MW SDS SDS-Range Länge (cm) MW SDS SDS-Range Kopfumfang MW SDS SDS-Range durchtherapiert Mädchen Jungen N = 29 N = ,52 ± -0,66-2,19-1,34-1, ,13 Mädchen Jungen 49,8 50,3-0,62-0,60-1,92-1,77-0, ,08 Mädchen Jungen 34,0 ± 33,2-0,02-0,63-2,12-1,29-1, ,63 vorzeitig beendet Mädchen Jungen N = 25 N = ,20 +0,02-2,47-3,59-1,81-1,72 Mädchen Jungen 52,2 51,8 +0,36 + 0,91-1,23-2,64-1,70-1,58 Mädchen Jungen 34,8 35,4 1,09 1,14-1,88-1,84-2,27-1,35 Betrachtet man das Geburtsgewicht und die kumulative Dexamethasondosis (Multiplikation aus Tagesdosis und Tage der Behandlung), so zeigt sich statistisch kein signifikanter Unterschied. (p =0,8; Abb. 8).
32 kumulative Dexamethasondosis (mg) y = - 0,0129x + 343, Geburtsgewicht der Neugeboren (g) Abb. 8: Vergleich der Geburtsgewichte der durchtherapierten Neugeborenen und der kumulativen Dexamethason-Dosis Auch der Zeitpunkt des Beginns der Dexamethasontherapie hat keinen signifikanten Einfluss auf das Geburtsgewicht der Neugeborenen Geburtslänge Die weiblichen AGS-Neugeborenen, bei denen die pränatale Therapie bis zur Geburt mit Dexamethason fortgeführt wurde, kamen mit einer mittleren Länge von 49,8 cm (-0,62 SDS) zur Welt (vgl. Tab. 2). Die weiblichen Neugeborenen, bei denen die Therapie bereits intrauterin beendet wurde, kamen im Mittel mit einer Länge von 52,2 cm (+0,36 SDS) zur Welt. Dieser Unterschied ist statistisch signifikant (p=0,038). Keines der Neugeborenen, bei denen die pränatale Therapie vorzeitig beendet, hatte eine Länge < -2 SDS; in einem Fall fand sich sogar eine Länge, die mit 2,64 SDS über dem Referenzwert lag.
33 Vergleicht man die beiden Gruppen, so kann man keine signifikante Korrelation zwischen Geburtslänge und Beginn der Therapie in SSW bzw. zwischen Geburtslänge und kumulativer Dexa-Dosis sehen Kopfumfang bei Geburt Die weiblichen Neugeborenen, bei denen die pränatale Therapie bis zum Termin durchgeführt wurde, hatten bei Geburt einen mittleren Kopfumfang von 33,9 cm (- 0,02 SDS), während der Kopfumfang bei den Neugeborenen bei denen die Therapie vorzeitig beendet wurde im Mittel bei 35,1 cm (1,09 SDS) lag. (Tab. 2). Dieser Unterschied ist jedoch statistisch nicht signifikant. Korreliert man den die Kopfumfänge der Neugeborenen und die kumulative Dexamethasondosis, so zeigt sich kein signifikanter Zusammenhang (p=0,19). 4.4 Komplikationen und Fehlbildungen bei Geburt In der Gruppe, die bis zum Schwangerschaftsende therapiert wurde, wurden keine Fehlbildungen berichtet. Als Komplikationen wurden von den Eltern / behandelnden Ärzten notiert: Hydrops fetalis (n=1), Schädellage (n=1), Hypoglykämie und Kephalhämatom (n=1). In drei Fällen kam es zu einem Ikterus praecox. In keinem Fall wurde die Durchführung einer Fototherapie oder eines Blutaustausches übermittelt. In der Gruppe, bei der die pränatale Therapie intrauterin beendet wurde, verstarb ein nicht-betroffenes Mädchen aufgrund einer großen Zwerchfellhernie und schweren kardialen Fehlbildungen. Bei einem Jungen war eine Syndaktylie des 2. bis 5. Fingers aufgefallen. Ein gesundes männliches Neugeborenes (Therapiegruppe: vorzeitig beendet) wurde aus grünem Fruchtwasser geboren, in dessen Folge es perinatal zu einer Asphyxie mit einer neonatalen Infektion kam. Ebenso waren hier eine Clavikulafraktur (n=1), ein Neugeborenenikterus (n=1); in 3 Fällen eine Nabelschnurumschlingung, sowie ein postnatales Atemnotsyndrom (n=1) zu verzeichnen (Tab. 3),
APE/SPE-Projekt. Dokumentation der pränatalen Therapie des Adrenogenitalen Syndroms (21-Hydroxylase-Defekt) mit Dexamethason
 APE/SPE-Projekt Arbeitsgemeinschaft Pädiatrische Endokrinologie (APE) Sektion Pädiatrische Endokrinologie (SPE) der Deutschen Gesellschaft für Endokrinologie Dokumentation der pränatalen Therapie des Adrenogenitalen
APE/SPE-Projekt Arbeitsgemeinschaft Pädiatrische Endokrinologie (APE) Sektion Pädiatrische Endokrinologie (SPE) der Deutschen Gesellschaft für Endokrinologie Dokumentation der pränatalen Therapie des Adrenogenitalen
Adrenogenitales Syndrom mit 21-Hydroxylase- Defekt (AGS) - Pränatale Therapie
 Adrenogenitales Syndrom mit 21-Hydroxylase- Defekt (AGS) - Pränatale Therapie Federführender Autoren: Prof. Dr. HG Dörr (federführend für die AGS-Leitliniengruppe der DGKED), Dr. biol. hum. Anja Moss (Leitlinienkoordinatorin
Adrenogenitales Syndrom mit 21-Hydroxylase- Defekt (AGS) - Pränatale Therapie Federführender Autoren: Prof. Dr. HG Dörr (federführend für die AGS-Leitliniengruppe der DGKED), Dr. biol. hum. Anja Moss (Leitlinienkoordinatorin
kommt es aufgrund Mehrsekretion von ACTH zur NNR-Hyperplasie.
 Pädiatrie Adrenogenitales Syndrom (AGS) Stellglied = Kortisolplasmaspiegel Bei Kortisolmangel kommt es aufgrund Mehrsekretion von ACTH zur NNR-Hyperplasie. Adrenale Steroidsynthese normal bei AGS: Kortisolmangel
Pädiatrie Adrenogenitales Syndrom (AGS) Stellglied = Kortisolplasmaspiegel Bei Kortisolmangel kommt es aufgrund Mehrsekretion von ACTH zur NNR-Hyperplasie. Adrenale Steroidsynthese normal bei AGS: Kortisolmangel
AGS Kongenitale adrenale Hyperplasie
 AGS Kongenitale adrenale Hyperplasie Dr. med. Reinhold Gellner gellner@uni-muenster.de Medizinische Klinik und Poliklinik B Universitätsklinikum Münster AGS - Pathophysiologie - AGS Kongenitale adrenale
AGS Kongenitale adrenale Hyperplasie Dr. med. Reinhold Gellner gellner@uni-muenster.de Medizinische Klinik und Poliklinik B Universitätsklinikum Münster AGS - Pathophysiologie - AGS Kongenitale adrenale
Risikoadaptierte HIV-1 Transmissionsprophylaxe. Effektivität einer verkürzten neonatalen. Zidovudin-Prophylaxe
 Risikoadaptierte HIV-1 Transmissionsprophylaxe Effektivität einer verkürzten neonatalen Zidovudin-Prophylaxe Klinik für Kinder-Onkologie, -Hämatologie und klinische Immunologie Universitätsklinikum Düsseldorf
Risikoadaptierte HIV-1 Transmissionsprophylaxe Effektivität einer verkürzten neonatalen Zidovudin-Prophylaxe Klinik für Kinder-Onkologie, -Hämatologie und klinische Immunologie Universitätsklinikum Düsseldorf
AGS / second tier Steroid-Profiling
 Kompetenznetz Neugeborenen Screening Berlin. Dresden. Greifswald. Magdeburg. Weiden 19.06.2015 AGS / second tier Steroid-Profiling H.-W. Schultis Das Adrenogenitale Syndrom (AGS / CAH) Adrenogenitales
Kompetenznetz Neugeborenen Screening Berlin. Dresden. Greifswald. Magdeburg. Weiden 19.06.2015 AGS / second tier Steroid-Profiling H.-W. Schultis Das Adrenogenitale Syndrom (AGS / CAH) Adrenogenitales
Aus der Kinder- und Jugendklinik der. Friedrich Alexander Universität Erlangen Nürnberg. Direktor: Prof. Dr. med. Dr. h. c. W.
 Aus der Kinder- und Jugendklinik der Friedrich Alexander Universität Erlangen Nürnberg Direktor: Prof. Dr. med. Dr. h. c. W. Rascher Zeitpunkt und Ausmaß der Salzverlustkrise bei Neugeborenen mit klassischem
Aus der Kinder- und Jugendklinik der Friedrich Alexander Universität Erlangen Nürnberg Direktor: Prof. Dr. med. Dr. h. c. W. Rascher Zeitpunkt und Ausmaß der Salzverlustkrise bei Neugeborenen mit klassischem
Aus der Kinder- und Jugendklinik der Friedrich-Alexander-Universität Erlangen-Nürnberg Direktor: Prof. Dr. med. Dr. h. c. W.
 Aus der Kinder- und Jugendklinik der Friedrich-Alexander-Universität Erlangen-Nürnberg Direktor: Prof. Dr. med. Dr. h. c. W. Rascher Welche Faktoren beeinflussen die Geburtsmaße der Neugeborenen mit klassischem
Aus der Kinder- und Jugendklinik der Friedrich-Alexander-Universität Erlangen-Nürnberg Direktor: Prof. Dr. med. Dr. h. c. W. Rascher Welche Faktoren beeinflussen die Geburtsmaße der Neugeborenen mit klassischem
Abbildung 5: Darstellung des Studienkollektivs. In die vorliegende Arbeit eingeschlossene und untersuchte Fälle sind rot markiert.
 30 4. ERGEBNISSE Von insgesamt 39 Schwangerschaften mit kongenitaler Zwerchfellhernie waren 3 mit rechtsseitiger Zwerchfellhernie (7,69%). Vorzeitige Schwangerschaftsbeendigungen wurden in 7 Fällen (17,94%)
30 4. ERGEBNISSE Von insgesamt 39 Schwangerschaften mit kongenitaler Zwerchfellhernie waren 3 mit rechtsseitiger Zwerchfellhernie (7,69%). Vorzeitige Schwangerschaftsbeendigungen wurden in 7 Fällen (17,94%)
Folien. www.diabetes.uni-muenster.de/downloads.html. oder. gellner@uni-muenster.de
 Folien www.diabetes.uni-muenster.de/downloads.html oder gellner@uni-muenster.de AGS Kongenitale adrenale Hyperplasie Dr. med. Reinhold Gellner gellner@uni-muenster.de Medizinische Klinik und Poliklinik
Folien www.diabetes.uni-muenster.de/downloads.html oder gellner@uni-muenster.de AGS Kongenitale adrenale Hyperplasie Dr. med. Reinhold Gellner gellner@uni-muenster.de Medizinische Klinik und Poliklinik
Pränatale Diagnostik und Therapie des Adrenogenitalen Syndroms (AGS) mit 21-Hydroxylasedefekt
 Medizinische Universitäts-Kinderklinik Prof. Dr. med. Primus E. Mullis Abteilungsleiter Pädiatrische Endokrinologie / Diabetologie & Stoffwechsel CH 3010 Bern Pränatale Diagnostik und Therapie des Adrenogenitalen
Medizinische Universitäts-Kinderklinik Prof. Dr. med. Primus E. Mullis Abteilungsleiter Pädiatrische Endokrinologie / Diabetologie & Stoffwechsel CH 3010 Bern Pränatale Diagnostik und Therapie des Adrenogenitalen
81,9% 71,5% Abbildung 1: Inzidenz von neonataler und fetaler Makrosomie
 3 ERGEBNISSE 21 3 Ergebnisse 3.1 Inzidenz von Makrosomie Es wurde die Inzidenz von neonataler Makrosomie (Anteil der Large for Gestational Age Kinder) und die Inzidenz von fetaler Makrosomie (Anteil der
3 ERGEBNISSE 21 3 Ergebnisse 3.1 Inzidenz von Makrosomie Es wurde die Inzidenz von neonataler Makrosomie (Anteil der Large for Gestational Age Kinder) und die Inzidenz von fetaler Makrosomie (Anteil der
Merkblatt. zur. Vorgeburtlichen Diagnostik und Therapie. beim Adrenogenitalem Syndrom mit 21-Hydroxylase-Defekt. Herausgegeben von der
 1 Merkblatt zur Vorgeburtlichen Diagnostik und Therapie beim Adrenogenitalem Syndrom mit 21-Hydroxylase-Defekt Herausgegeben von der AGS Eltern- und Patienteninitiative Schweiz 2 Inhalt Seite 2 Voraussetzung
1 Merkblatt zur Vorgeburtlichen Diagnostik und Therapie beim Adrenogenitalem Syndrom mit 21-Hydroxylase-Defekt Herausgegeben von der AGS Eltern- und Patienteninitiative Schweiz 2 Inhalt Seite 2 Voraussetzung
Anhang 11
 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Tab. A2: Entwicklung der Geborenen-Anzahlen (Lebend- und Totgeborene) im Land Sachsen-Anhalt zwischen 1994 und 2006 Jahr
Anhang 11 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Anhang 11 Tab. A2: Entwicklung der Geborenen-Anzahlen (Lebend- und Totgeborene) im Land Sachsen-Anhalt zwischen 1994 und 2006 Jahr
Start frei für Glandulinchen
 Magazin für Kinder- und Jugendendokrinologie Netzwerk Hypophysen- und Nebennierenerkrankungen e.v. Netzwerk www.glandula-online.de Hypophysen- und Nebennierenerkrankungen e.v. www.glandula-online.de mit
Magazin für Kinder- und Jugendendokrinologie Netzwerk Hypophysen- und Nebennierenerkrankungen e.v. Netzwerk www.glandula-online.de Hypophysen- und Nebennierenerkrankungen e.v. www.glandula-online.de mit
Strukturierter Dialog bei häufiger Azidose und kritischem Zustand des Kindes bei Geburt Der Hessische Weg. W. Künzel und B.
 Strukturierter Dialog bei häufiger Azidose und kritischem Zustand des Kindes bei Geburt Der Hessische Weg Qualitätssicherung in der Geburtshilfe, Neonatologie, operativen Gynäkologie und Mammachirurgie
Strukturierter Dialog bei häufiger Azidose und kritischem Zustand des Kindes bei Geburt Der Hessische Weg Qualitätssicherung in der Geburtshilfe, Neonatologie, operativen Gynäkologie und Mammachirurgie
Was bedeutet Pränataldiagnostik für mich in der Praxis?
 Was bedeutet Pränataldiagnostik für mich in der Praxis? 1 Dr. Johannes Hovhannesian Zukunftsweg 15, 1210 Wien Mitarbeiter des Ultraschallteams in der Semmelweisfrauenklinik Wien 2 Was ist Pränataldiagnostik?
Was bedeutet Pränataldiagnostik für mich in der Praxis? 1 Dr. Johannes Hovhannesian Zukunftsweg 15, 1210 Wien Mitarbeiter des Ultraschallteams in der Semmelweisfrauenklinik Wien 2 Was ist Pränataldiagnostik?
Einsatz von Magnesiumsulfat in der Geburtshilfe Fetale Neuroprotektion und Eklampsieprophylaxe
 Einsatz von Magnesiumsulfat in der Geburtshilfe Fetale Neuroprotektion und Eklampsieprophylaxe Ioana Lakovschek Universitätsklinik für Frauenheilkunde Graz Eklampsie Eklampsie: Komplikation der Präeklampsie
Einsatz von Magnesiumsulfat in der Geburtshilfe Fetale Neuroprotektion und Eklampsieprophylaxe Ioana Lakovschek Universitätsklinik für Frauenheilkunde Graz Eklampsie Eklampsie: Komplikation der Präeklampsie
HIV und Schwangerschaft
 HIV und Schwangerschaft Katharina Weizsäcker Klinik für Geburtsmedizin Children (
HIV und Schwangerschaft Katharina Weizsäcker Klinik für Geburtsmedizin Children (
Äußere Wendung bei fetaler Beckenendlage eine Möglichkeit zur Qualitätsverbesserung?
 Klinik für Geburtshilfe und Pränatalmedizin Äußere Wendung bei fetaler Beckenendlage eine Möglichkeit zur Qualitätsverbesserung? Gerhard Ortmeyer Das Ziel der äußeren Wendung ist das Erreichen einer Schädellage,
Klinik für Geburtshilfe und Pränatalmedizin Äußere Wendung bei fetaler Beckenendlage eine Möglichkeit zur Qualitätsverbesserung? Gerhard Ortmeyer Das Ziel der äußeren Wendung ist das Erreichen einer Schädellage,
Adrenogenitales Syndrom update Karin Frank-Raue Endokrinologisch-humangenetische Gemeinschaftspraxis Heidelberg
 Adrenogenitales Syndrom update 2008 Karin Frank-Raue Endokrinologisch-humangenetische Gemeinschaftspraxis Heidelberg Epidemiologie Häufige genetische Erkrankung 1:40 Genträger (Südeuropa < 1:25) Autosomal
Adrenogenitales Syndrom update 2008 Karin Frank-Raue Endokrinologisch-humangenetische Gemeinschaftspraxis Heidelberg Epidemiologie Häufige genetische Erkrankung 1:40 Genträger (Südeuropa < 1:25) Autosomal
5 ZUSAMMENFASSUNG Zusammenfassung
 5 ZUSAMMENFASSUNG 56 5 Zusammenfassung Schwangere mit Gestationdiabetes (GDM) haben ein erhöhtes Risiko für die Entwicklung einer fetalen Makrosomie. Die Geburt eines makrosomen Neugeborenen erhöht nicht
5 ZUSAMMENFASSUNG 56 5 Zusammenfassung Schwangere mit Gestationdiabetes (GDM) haben ein erhöhtes Risiko für die Entwicklung einer fetalen Makrosomie. Die Geburt eines makrosomen Neugeborenen erhöht nicht
Methoden der invasiven Pränataldiagnostik. Methoden zur Beurteilung der fetalen Kondition
 Pränataldiagnostik Nicht-invasive invasive Methoden der Pränataldiagnostik Sonographie-Screening (10., 20., 30. SSW) und weiterführende Sonographie Ersttrimesterscreening Methoden der invasiven Pränataldiagnostik
Pränataldiagnostik Nicht-invasive invasive Methoden der Pränataldiagnostik Sonographie-Screening (10., 20., 30. SSW) und weiterführende Sonographie Ersttrimesterscreening Methoden der invasiven Pränataldiagnostik
Vaginal Operative Entbindung. Frank Louwen
 Vaginal Operative Entbindung Frank Louwen Quelle: Peristat 2010 Vag. Operationen in Hessen Entwicklung seit 1990 6 5 Anteil in % 4 3 2 Forzeps Vakuum 1 0 Forzeps Verteilung in Kliniken wording FAZ: grobe
Vaginal Operative Entbindung Frank Louwen Quelle: Peristat 2010 Vag. Operationen in Hessen Entwicklung seit 1990 6 5 Anteil in % 4 3 2 Forzeps Vakuum 1 0 Forzeps Verteilung in Kliniken wording FAZ: grobe
Jahresauswertung 2015 Geburtshilfe 16/1. Rheinland-Pfalz Gesamt
 16/1 Rheinland-Pfalz Teilnehmende Krankenhäuser/Abteilungen (Rheinland-Pfalz): 43 Anzahl Datensätze : 33.164 Datensatzversion: 16/1 2015 Datenbankstand: 01. März 2016 2015 - D16097-L101083-P48547 Eine
16/1 Rheinland-Pfalz Teilnehmende Krankenhäuser/Abteilungen (Rheinland-Pfalz): 43 Anzahl Datensätze : 33.164 Datensatzversion: 16/1 2015 Datenbankstand: 01. März 2016 2015 - D16097-L101083-P48547 Eine
3.4.1 Referenzwerte für das fetale Schätzgewicht in der SSW
 60 3.4 Die Bedeutung des fetalen und des mütterlichen Gewichts in der 21.-24.SSW als prädiktiver Parameter für das Geburtsgewicht bei Geburt in der 36.-43.SSW 3.4.1 Referenzwerte für das fetale Schätzgewicht
60 3.4 Die Bedeutung des fetalen und des mütterlichen Gewichts in der 21.-24.SSW als prädiktiver Parameter für das Geburtsgewicht bei Geburt in der 36.-43.SSW 3.4.1 Referenzwerte für das fetale Schätzgewicht
J.L. Ross, C.A. Quigley, D. Cao, P. Feuillan, K. Kowal, J.J. Chipman, and G.B. Cutler Jr.
 J.L. Ross, C.A. Quigley, D. Cao, P. Feuillan, K. Kowal, J.J. Chipman, and G.B. Cutler Jr. hormone plus childhood low-dose estrogen in Turner s syndrome. The New England Journal of Medicine 211, Vol. 364
J.L. Ross, C.A. Quigley, D. Cao, P. Feuillan, K. Kowal, J.J. Chipman, and G.B. Cutler Jr. hormone plus childhood low-dose estrogen in Turner s syndrome. The New England Journal of Medicine 211, Vol. 364
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen Wissenschaftliche Schlussfolgerungen Der CHMP ist unter Berücksichtigung
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen Wissenschaftliche Schlussfolgerungen Der CHMP ist unter Berücksichtigung
3.3.1 Referenzwerte für Fruchtwasser-Schätzvolumina ( SSW)
 50 3.3 Das Fruchtwasser-Schätzvolumen in der 21.-24.SSW und seine Bedeutung für das fetale Schätzgewicht in der 21.-24.SSW und für das Geburtsgewicht bei Geburt in der 36.-43.SSW 3.3.1 Referenzwerte für
50 3.3 Das Fruchtwasser-Schätzvolumen in der 21.-24.SSW und seine Bedeutung für das fetale Schätzgewicht in der 21.-24.SSW und für das Geburtsgewicht bei Geburt in der 36.-43.SSW 3.3.1 Referenzwerte für
PraenaTest. Nicht-invasive Untersuchung auf Trisomien beim ungeborenen Kind. Qualität aus Deutschland JETZT NEU
 JETZT NEU PraenaTest express Ihr Ergebnis in 1 Woche PraenaTest Qualität aus Deutschland Nicht-invasive Untersuchung auf Trisomien beim ungeborenen Kind Information und Aufklärung für Schwangere Liebe
JETZT NEU PraenaTest express Ihr Ergebnis in 1 Woche PraenaTest Qualität aus Deutschland Nicht-invasive Untersuchung auf Trisomien beim ungeborenen Kind Information und Aufklärung für Schwangere Liebe
Sozialpädiatrisches Zentrum am Klinikum Weiden (Ltd. Ärztin: Dr. med. Susanne Rinnert)
 Sozialpädiatrisches Zentrum am Klinikum Weiden (Ltd. Ärztin: Dr. med. Susanne Rinnert) Söllnerstrasse. 16 92637 Weiden Tel.: 0961 303 3331 Fax: 0961 303 3339 Zurück an: Stempel des behandelnden Kinderarztes:
Sozialpädiatrisches Zentrum am Klinikum Weiden (Ltd. Ärztin: Dr. med. Susanne Rinnert) Söllnerstrasse. 16 92637 Weiden Tel.: 0961 303 3331 Fax: 0961 303 3339 Zurück an: Stempel des behandelnden Kinderarztes:
Spezielle Situationen beim Mammakarzinom
 Spezielle Situationen beim Mammakarzinom DESO St.Gallen 20.2.2014 J. Huober Univ.-Frauenklinik Ulm Integratives Tumorzentrum des Universitätsklinikums und der Medizinischen Fakultät Comprehensive Cancer
Spezielle Situationen beim Mammakarzinom DESO St.Gallen 20.2.2014 J. Huober Univ.-Frauenklinik Ulm Integratives Tumorzentrum des Universitätsklinikums und der Medizinischen Fakultät Comprehensive Cancer
qs-nrw Jahresauswertung 2012 Geburtshilfe 16/1 Universitätsklinikum Aachen Aachen und Nordrhein-Westfalen Gesamt
 qs-nrw Geschäftsstelle Qualitätssicherung NRW Krankenhausgesellschaft Nordrhein-Westfalen Verbände der Kostenträger Nordrhein-Westfalen Ärztekammern in Nordrhein-Westfalen 16/1 Universitätsklinikum Aachen
qs-nrw Geschäftsstelle Qualitätssicherung NRW Krankenhausgesellschaft Nordrhein-Westfalen Verbände der Kostenträger Nordrhein-Westfalen Ärztekammern in Nordrhein-Westfalen 16/1 Universitätsklinikum Aachen
Zweigbibliothek Medizin
 Sächsische Landesbibliothek - Staats- und Universitätsbibliothek Dresden (SLUB) Zweigbibliothek Medizin Diese Hochschulschrift finden Sie original in Printform zur Ausleihe in der Zweigbibliothek Medizin
Sächsische Landesbibliothek - Staats- und Universitätsbibliothek Dresden (SLUB) Zweigbibliothek Medizin Diese Hochschulschrift finden Sie original in Printform zur Ausleihe in der Zweigbibliothek Medizin
Ersttrimester- Screening Was wird untersucht? MUSTER
 Ersttrimester- Screening Was wird untersucht? Sehr geehrte Patientin, schon seit vielen Jahrzehnten besteht die Möglichkeit durch eine Fruchtwasseruntersuchung (Amniocentese, AC) oder einer Mutterkuchenprobe
Ersttrimester- Screening Was wird untersucht? Sehr geehrte Patientin, schon seit vielen Jahrzehnten besteht die Möglichkeit durch eine Fruchtwasseruntersuchung (Amniocentese, AC) oder einer Mutterkuchenprobe
Sonographie des unteren Unterinsegmentes nach SC. Karim D Kalache Klinik für Geburtsmedizin Charité Campus Mitte Berlin
 Sonographie des unteren Unterinsegmentes nach SC Karim D Kalache Klinik für Geburtsmedizin Charité Campus Mitte Berlin - 29. SSW - Z. n. 2 x SC - 42 Jahre - PP - Rechtsanwältin - 32. SSW - Z. n. 2 x SC
Sonographie des unteren Unterinsegmentes nach SC Karim D Kalache Klinik für Geburtsmedizin Charité Campus Mitte Berlin - 29. SSW - Z. n. 2 x SC - 42 Jahre - PP - Rechtsanwältin - 32. SSW - Z. n. 2 x SC
FIVNAT-CH. Annual report 2002
 FIVNAT-CH Schweizerische Gesellschaft für Reproduktionsmedizin Annual report 2002 Date of analysis 15.01.2004 Source: FileMaker Pro files FIVNAT_CYC.FP5 and FIVNAT_PAT.FP5 SUMMARY TABLE SUMMARY RESULTS
FIVNAT-CH Schweizerische Gesellschaft für Reproduktionsmedizin Annual report 2002 Date of analysis 15.01.2004 Source: FileMaker Pro files FIVNAT_CYC.FP5 and FIVNAT_PAT.FP5 SUMMARY TABLE SUMMARY RESULTS
Informations- und Wissensstand der Mütter von Kindern mit angeborenem Herzfehler
 Informations- und Wissensstand der Mütter von Kindern mit angeborenem Herzfehler A Löbel 1, U Grosser 2, A Wessel 2, S Geyer 1 1 Medizinische Soziologie, Medizinische Hochschule Hannover 2 Pädiatrische
Informations- und Wissensstand der Mütter von Kindern mit angeborenem Herzfehler A Löbel 1, U Grosser 2, A Wessel 2, S Geyer 1 1 Medizinische Soziologie, Medizinische Hochschule Hannover 2 Pädiatrische
Nieren und Harnwege: Pränatale Diagnose und postpartaler Verlauf im Kindesalter
 Nieren und Harnwege: Pränatale Diagnose und postpartaler Verlauf im Kindesalter Thomas J. Neuhaus 19.4.2018 Indikationen für postpartale Abklärung Nachkontrolle von "Auffälligkeiten" im pränatalen US Indikationen
Nieren und Harnwege: Pränatale Diagnose und postpartaler Verlauf im Kindesalter Thomas J. Neuhaus 19.4.2018 Indikationen für postpartale Abklärung Nachkontrolle von "Auffälligkeiten" im pränatalen US Indikationen
Wenn das Erscheinungsbild Ihres Kindes in kein Geschlecht zu passen scheint
 1 Wenn das Erscheinungsbild Ihres Kindes in kein Geschlecht zu passen scheint Eine Broschüre für Eltern von Eltern Varianten der Geschlechtsentwicklung Intersexualität / Intergeschlechtlichkeit / DSD /
1 Wenn das Erscheinungsbild Ihres Kindes in kein Geschlecht zu passen scheint Eine Broschüre für Eltern von Eltern Varianten der Geschlechtsentwicklung Intersexualität / Intergeschlechtlichkeit / DSD /
Intrauterine instillation of diluted seminal plasma in in vitro fertilization a double-blind, placebo controlled, randomized study
 PLEASE NOTE: This trial has been registered retrospectively. Trial Description Title Intrauterine instillation of diluted seminal plasma in in vitro fertilization a double-blind, placebo controlled, randomized
PLEASE NOTE: This trial has been registered retrospectively. Trial Description Title Intrauterine instillation of diluted seminal plasma in in vitro fertilization a double-blind, placebo controlled, randomized
Ersttrimesterscreening
 Universitäts-Frauenklinik Essen Ersttrimesterscreening Was ist das Ersttrimesterscreening? Im Ersttrimesterscreening wird das individuelle Risiko der Mutter/des Paares für ein Kind mit einer numerischen
Universitäts-Frauenklinik Essen Ersttrimesterscreening Was ist das Ersttrimesterscreening? Im Ersttrimesterscreening wird das individuelle Risiko der Mutter/des Paares für ein Kind mit einer numerischen
GerOSS. Erste Ergebnisse zur Plazenta increta/percreta und Ausblick. Perinatalmedizin aktuell: Jahresversammlung der NPE 8.
 GerOSS Erste Ergebnisse zur Plazenta increta/percreta und Ausblick Perinatalmedizin aktuell: Jahresversammlung der NPE 8. Februar 2019 Dr. med. F. Fischer, Prof. C. von Kaisenberg Frauenklinik der Medizinischen
GerOSS Erste Ergebnisse zur Plazenta increta/percreta und Ausblick Perinatalmedizin aktuell: Jahresversammlung der NPE 8. Februar 2019 Dr. med. F. Fischer, Prof. C. von Kaisenberg Frauenklinik der Medizinischen
Vergleich: außerklinische und klinische Geburten 2011 in Deutschland
 Vergleich: außerklinische und klinische Geburten 2011 in Deutschland Daten Qualitätsbericht 2011 - Außerklinische Geburtshilfe in Deutschland im Auftrag der "Gesellschaft für Qualität in der außerklinischen
Vergleich: außerklinische und klinische Geburten 2011 in Deutschland Daten Qualitätsbericht 2011 - Außerklinische Geburtshilfe in Deutschland im Auftrag der "Gesellschaft für Qualität in der außerklinischen
Bluttransfer über die Plazenta - das fetomaternale Transfusionssyndrom. Maier JT, Schalinski E, Schneider W, Gottschalk U, Hellmeyer L
 Bluttransfer über die Plazenta - das fetomaternale Transfusionssyndrom Maier JT, Schalinski E, Schneider W, Gottschalk U, Hellmeyer L GGGB Sitzung Gliederung Fallbericht Vorstellung des Krankheitsbildes
Bluttransfer über die Plazenta - das fetomaternale Transfusionssyndrom Maier JT, Schalinski E, Schneider W, Gottschalk U, Hellmeyer L GGGB Sitzung Gliederung Fallbericht Vorstellung des Krankheitsbildes
SGA Früherkennung. Zu klein von Geburt an
 SGA Früherkennung Zu klein von Geburt an 1 Zu klein von Geburt an Liebe Mütter, liebe Väter, Ihr Kind gehört schon immer zu den Kleinsten. War das auch schon bei Geburt so? Jetzt ist es älter als 4 Jahre
SGA Früherkennung Zu klein von Geburt an 1 Zu klein von Geburt an Liebe Mütter, liebe Väter, Ihr Kind gehört schon immer zu den Kleinsten. War das auch schon bei Geburt so? Jetzt ist es älter als 4 Jahre
Beckenendlagengeburt spontan oder per Sectio?
 Beckenendlagengeburt spontan oder per Sectio? Nachuntersuchung und Outcome aus Sicht des Neonatologen H.Gerleve, D. Wüller, B. Ribbrock, C. Kolem, K-D. Jaspers* Kinder- und Jugendklinik, *Frauenklink der
Beckenendlagengeburt spontan oder per Sectio? Nachuntersuchung und Outcome aus Sicht des Neonatologen H.Gerleve, D. Wüller, B. Ribbrock, C. Kolem, K-D. Jaspers* Kinder- und Jugendklinik, *Frauenklink der
Management und Entbindungsmodus bei Gemini und bei Beckenendlage. Holger Stepan Abteilung für Geburtsmedizin, Universitätsklinikum Leipzig
 Management und Entbindungsmodus bei Gemini und bei Beckenendlage Holger Stepan Abteilung für Geburtsmedizin, Universitätsklinikum Leipzig 2. Tagung Junge Frauenärzte in Mitteldeutschland 10. Januar 2015
Management und Entbindungsmodus bei Gemini und bei Beckenendlage Holger Stepan Abteilung für Geburtsmedizin, Universitätsklinikum Leipzig 2. Tagung Junge Frauenärzte in Mitteldeutschland 10. Januar 2015
Methoden zur Untersuchung von Arzneimittelwirkungen in der Schwangerschaft
 Methoden zur Untersuchung von Arzneimittelwirkungen in der Schwangerschaft Reinhard Meister Beuth Hochschule für Technik Berlin, FB II Mathematik, Physik, Chemie Meister (Beuth Hochschule) Methoden Moskau
Methoden zur Untersuchung von Arzneimittelwirkungen in der Schwangerschaft Reinhard Meister Beuth Hochschule für Technik Berlin, FB II Mathematik, Physik, Chemie Meister (Beuth Hochschule) Methoden Moskau
Die Thrombin-Therapie beim Aneurysma spurium nach arterieller Punktion
 Aus der Universitätsklinik und Poliklinik für Innere Medizin III der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. K. Werdan) und dem Herzzentrum Coswig Klinik für Kardiologie und
Aus der Universitätsklinik und Poliklinik für Innere Medizin III der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. K. Werdan) und dem Herzzentrum Coswig Klinik für Kardiologie und
Ovarialinsuffizienz (POF Syndrom)
 Ovarialinsuffizienz (POF Syndrom) Bei der Ovarialinsuffizienz können die Eierstöcke der Frau verschiedene Funktionsstörungen aufweisen. Man unterscheidet dabei zwei große Gruppen, einerseits die primäre
Ovarialinsuffizienz (POF Syndrom) Bei der Ovarialinsuffizienz können die Eierstöcke der Frau verschiedene Funktionsstörungen aufweisen. Man unterscheidet dabei zwei große Gruppen, einerseits die primäre
Vorgeburtliche Untersuchung aus dem Blut der Schwangeren zur Abklärung einer möglichen fetalen Trisomie 21, 18 und 13
 Patientinneninformation zum NIPT ( nicht-invasiver pränataler Test ) Vorgeburtliche Untersuchung aus dem Blut der Schwangeren zur Abklärung einer möglichen fetalen Trisomie 21, 18 und 13 Sehr geehrte Patientin,
Patientinneninformation zum NIPT ( nicht-invasiver pränataler Test ) Vorgeburtliche Untersuchung aus dem Blut der Schwangeren zur Abklärung einer möglichen fetalen Trisomie 21, 18 und 13 Sehr geehrte Patientin,
Sozialpädiatrisches Zentrum am Klinikum Weiden (Ltd. Ärztin: Dr. med. Susanne Rinnert)
 Sozialpädiatrisches Zentrum am Klinikum Weiden (Ltd. Ärztin: Dr. med. Susanne Rinnert) Söllnerstr. 16 92637 Weiden Tel.: 0961 303 3331 Fax: 0961 303 3339 Zurück an: Stempel des behandelnden Kinderarztes:
Sozialpädiatrisches Zentrum am Klinikum Weiden (Ltd. Ärztin: Dr. med. Susanne Rinnert) Söllnerstr. 16 92637 Weiden Tel.: 0961 303 3331 Fax: 0961 303 3339 Zurück an: Stempel des behandelnden Kinderarztes:
Beschluss. II. Dieser Beschluss tritt mit Beschlussfassung in Kraft.
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung des Beschlusses zur Änderung des Beschlusses zur Neufassung der Richtlinien über die Früherkennung von Krankheiten bei Kindern bis zur Vollendung
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung des Beschlusses zur Änderung des Beschlusses zur Neufassung der Richtlinien über die Früherkennung von Krankheiten bei Kindern bis zur Vollendung
4 Ergebnisse. 4.1 Indikationen der Amniozentese. Ergebnisse
 4 Ergebnisse Die vorliegende Arbeit beschreibt die Ergebnisse der klinischen prospektiven Studie. Es wurden alle Schwangere in die Studie eingeschlossen, die sich im Zeitraum von 12 Monaten (August 23
4 Ergebnisse Die vorliegende Arbeit beschreibt die Ergebnisse der klinischen prospektiven Studie. Es wurden alle Schwangere in die Studie eingeschlossen, die sich im Zeitraum von 12 Monaten (August 23
5.3 Informationen zur jetzigen Schwangerschaft
 5.3 Informationen zur jetzigen Schwangerschaft 5.3.1 Anamnese Anzahl Zigaretten pro Tag 0 angegeben 480.899 80,1 82,3 191.353 82,1 289.546 78,8 1 bis 10 49.226 8,2 8,5 17.299 7,4 31.927 8,7 11 bis 20 21.378
5.3 Informationen zur jetzigen Schwangerschaft 5.3.1 Anamnese Anzahl Zigaretten pro Tag 0 angegeben 480.899 80,1 82,3 191.353 82,1 289.546 78,8 1 bis 10 49.226 8,2 8,5 17.299 7,4 31.927 8,7 11 bis 20 21.378
Ärztlicher Leiter: Prof. Dr. P. A. Fasching
 Pertuzumab in First Line Treatment of HER2-positive metastatic breast Cancer patients: A cohort study of patients treated either with docetaxel and EudraCT 2015-003157-17, UKT-FFG-2015-II, SEN2015-02,
Pertuzumab in First Line Treatment of HER2-positive metastatic breast Cancer patients: A cohort study of patients treated either with docetaxel and EudraCT 2015-003157-17, UKT-FFG-2015-II, SEN2015-02,
Funktion der Mindestreserve im Bezug auf die Schlüsselzinssätze der EZB (German Edition)
 Funktion der Mindestreserve im Bezug auf die Schlüsselzinssätze der EZB (German Edition) Philipp Heckele Click here if your download doesn"t start automatically Download and Read Free Online Funktion
Funktion der Mindestreserve im Bezug auf die Schlüsselzinssätze der EZB (German Edition) Philipp Heckele Click here if your download doesn"t start automatically Download and Read Free Online Funktion
Bedeutung der Bestimmung der Vitamin D 3 - Konzentration im Serum bei dialysepflichtiger terminaler Niereninsuffizienz
 Aus der Universitätsklinik und Poliklinik für Innere Medizin II an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. B. Osten) Bedeutung der Bestimmung der Vitamin D 3 - Konzentration
Aus der Universitätsklinik und Poliklinik für Innere Medizin II an der Martin-Luther-Universität Halle-Wittenberg (Direktor: Prof. Dr. med. B. Osten) Bedeutung der Bestimmung der Vitamin D 3 - Konzentration
Jubiläumsveranstaltung 20 Jahre Perinatalerhebung in Baden-Württemberg
 Jubiläumsveranstaltung 20 Jahre Perinatalerhebung in Baden-Württemberg Qualitätssicherung in der außerklinischen Geburtshilfe, Beteiligung von Hebammen an den innerklinischen Maßnahmen und Perspektiven
Jubiläumsveranstaltung 20 Jahre Perinatalerhebung in Baden-Württemberg Qualitätssicherung in der außerklinischen Geburtshilfe, Beteiligung von Hebammen an den innerklinischen Maßnahmen und Perspektiven
Information zum Ultraschall in der Schwangerschaft
 Information zum Ultraschall in der Schwangerschaft Sehr geehrte Schwangere Das Heranwachsen des Kindes mit dem Ultraschall zu verfolgen, gehört für die meisten zu den schönen Ereignissen in der Schwangerschaft
Information zum Ultraschall in der Schwangerschaft Sehr geehrte Schwangere Das Heranwachsen des Kindes mit dem Ultraschall zu verfolgen, gehört für die meisten zu den schönen Ereignissen in der Schwangerschaft
Infektion mit dem Zytomegalievirus (CMV) in der Schwangerschaft. CMV-Serologie: IgM, IgG und Avidität? Christoph Koidl April 2013
 Infektion mit dem Zytomegalievirus (CMV) in der Schwangerschaft CMV-Serologie: IgM, IgG und Avidität? Christoph Koidl April 2013 Einleitung-Systematik - Familie: Herpesviridae - Subfamilie: Betaherpesvirinae
Infektion mit dem Zytomegalievirus (CMV) in der Schwangerschaft CMV-Serologie: IgM, IgG und Avidität? Christoph Koidl April 2013 Einleitung-Systematik - Familie: Herpesviridae - Subfamilie: Betaherpesvirinae
Tuberkulose in Schwangerschaft und Stillzeit: Update Vorgehen und Therapie
 Tuberkulose in Schwangerschaft und Stillzeit: Update Vorgehen und Therapie Stefan Zimmerli Universitätsklinik für Infektiologie Inselspital 3010 Bern Tuberkulose in der Schwangerschaft Schwangere Frauen
Tuberkulose in Schwangerschaft und Stillzeit: Update Vorgehen und Therapie Stefan Zimmerli Universitätsklinik für Infektiologie Inselspital 3010 Bern Tuberkulose in der Schwangerschaft Schwangere Frauen
Hagman A, Källén K, Bryman I, Landin-Wilhelmsen K, Barrenäs ML, Wennerholm UB. Morbidity and Mortality after Childbirth in Women with Turner Karyotype
 Geburten, Morbidität, Mortalität Hagman A, Källén K, Bryman I, Landin-Wilhelmsen K, Barrenäs ML, Wennerholm UB Morbidity and Mortality after Childbirth in Women with Turner Karyotype Hum Reprod 2013; 28
Geburten, Morbidität, Mortalität Hagman A, Källén K, Bryman I, Landin-Wilhelmsen K, Barrenäs ML, Wennerholm UB Morbidity and Mortality after Childbirth in Women with Turner Karyotype Hum Reprod 2013; 28
Qualität aus ärztlichen Händen. Nicht invasiver Pränataltest (NIPT) Information für werdende Mütter
 Qualität aus ärztlichen Händen Nicht invasiver Pränataltest (NIPT) Information für werdende Mütter Liebe Schwangere, als werdende Mutter befinden Sie sich wahrscheinlich in einer der emotionalsten Phasen
Qualität aus ärztlichen Händen Nicht invasiver Pränataltest (NIPT) Information für werdende Mütter Liebe Schwangere, als werdende Mutter befinden Sie sich wahrscheinlich in einer der emotionalsten Phasen
Informationsbroschüre Adrenogenitales Syndrom mit 21-Hydroxylase-Defekt (AGS)
 Informationsbroschüre Adrenogenitales Syndrom mit 21-Hydroxylase-Defekt (AGS) für Patientinnen und Patienten Wichtiger Hinweis: Medizin und Wissenschaft unterliegen ständigen Entwicklungen. Autor, Herausgeber
Informationsbroschüre Adrenogenitales Syndrom mit 21-Hydroxylase-Defekt (AGS) für Patientinnen und Patienten Wichtiger Hinweis: Medizin und Wissenschaft unterliegen ständigen Entwicklungen. Autor, Herausgeber
Prävention der Mutter-Kind- Transmission von HIV
 Prävention der Mutter-Kind- Transmission von HIV Cornelia Feiterna-Sperling Klinik für Pädiatrie mit Schwerpunkt Pneumologie und Immunologie Sektion Immundefekte Mutter-Kind-Transmission von HIV Weltweit
Prävention der Mutter-Kind- Transmission von HIV Cornelia Feiterna-Sperling Klinik für Pädiatrie mit Schwerpunkt Pneumologie und Immunologie Sektion Immundefekte Mutter-Kind-Transmission von HIV Weltweit
Sozialpädiatrisches Zentrum am Klinikum Weiden (Chefärztin: Dr. med. Susanne Rinnert)
 Sozialpädiatrisches Zentrum am Klinikum Weiden (Chefärztin: Dr. med. Susanne Rinnert) Söllnerstr. 16 92637 Weiden Tel.: 0961 303 3331 Fax: 0961 303 3339 Zurück an: Sozialpädiatrisches Zentrum Weiden Sekretariat
Sozialpädiatrisches Zentrum am Klinikum Weiden (Chefärztin: Dr. med. Susanne Rinnert) Söllnerstr. 16 92637 Weiden Tel.: 0961 303 3331 Fax: 0961 303 3339 Zurück an: Sozialpädiatrisches Zentrum Weiden Sekretariat
KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM
 KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM 11.11.02 RANDOMISIERTE, OFFENE, NICHT-KOMPARATIVE PHASE II STUDIE ZUR BEURTEILUNG DER WIRKSAMKEIT UND VERTRÄGLICHKEIT VON ZWEI DOSIERUNGEN ZD1839 BEI PATIENTEN
KURZFASSUNG DES PRÜFPROTOKOLLS 1839IL/0079 VOM 11.11.02 RANDOMISIERTE, OFFENE, NICHT-KOMPARATIVE PHASE II STUDIE ZUR BEURTEILUNG DER WIRKSAMKEIT UND VERTRÄGLICHKEIT VON ZWEI DOSIERUNGEN ZD1839 BEI PATIENTEN
Referenzwerte pädiatrische Endokrinologie: Anthropometrische Parameter
 Referenzwerte pädiatrische Endokrinologie: Anthropometrische Parameter Martin Wabitsch Inhalt 1 Referenzwerte aus der Züricher Wachstumsstudie... 1 2 BMI sowie Körpergröße und -gewicht für deutsche Kinder
Referenzwerte pädiatrische Endokrinologie: Anthropometrische Parameter Martin Wabitsch Inhalt 1 Referenzwerte aus der Züricher Wachstumsstudie... 1 2 BMI sowie Körpergröße und -gewicht für deutsche Kinder
Tabelle 1: Altersverteilung der Patienten (n = 42) in Jahren
 3. Ergebnisse Die 42 Patienten (w= 16, m= 26) hatten ein Durchschnittsalter von 53,5 Jahren mit einem Minimum von und einem Maximum von 79 Jahren. Die 3 Patientengruppen zeigten hinsichtlich Alters- und
3. Ergebnisse Die 42 Patienten (w= 16, m= 26) hatten ein Durchschnittsalter von 53,5 Jahren mit einem Minimum von und einem Maximum von 79 Jahren. Die 3 Patientengruppen zeigten hinsichtlich Alters- und
CGM UND SUP IN DER SCHWANGERSCHAFT
 CGM UND SUP IN DER SCHWANGERSCHAFT ZUGANG: EINFLUSS DER GLYKÄMISCHEN QUALITÄT AUF DAS ERGEBNIS DER SCHWANGERSCHAFT BEI TYP-1-DIABETES ZIEL DER UNTERSUCHUNG: Ermittlung des Einflusses der Stoffwechseleinstellung
CGM UND SUP IN DER SCHWANGERSCHAFT ZUGANG: EINFLUSS DER GLYKÄMISCHEN QUALITÄT AUF DAS ERGEBNIS DER SCHWANGERSCHAFT BEI TYP-1-DIABETES ZIEL DER UNTERSUCHUNG: Ermittlung des Einflusses der Stoffwechseleinstellung
Additive wachstumsfördernde Effekte von Wachstumshormon und IGF-1 in der experimentellen Urämie
 Jun Oh Dr.med. Additive wachstumsfördernde Effekte von Wachstumshormon und IGF-1 in der experimentellen Urämie Geboren am 27.03.1968 in Heidelberg Reifeprüfung am 16.05.1987 Studiengang der Fachrichtung
Jun Oh Dr.med. Additive wachstumsfördernde Effekte von Wachstumshormon und IGF-1 in der experimentellen Urämie Geboren am 27.03.1968 in Heidelberg Reifeprüfung am 16.05.1987 Studiengang der Fachrichtung
Evaluationsbogen Endokrinologie und Schwangerschaft am mit Lösungen
 [Frage 1] Eine Schilddrüsenunterfunktion kann führen zu 1. Haarausfall 2. Zyklusstörungen 3. höherer Abortrate nach IVF 4. Intelligenzdefekten beim Feten C: nur 1 ist richtig [Frage 2] In der Schwangerschaft
[Frage 1] Eine Schilddrüsenunterfunktion kann führen zu 1. Haarausfall 2. Zyklusstörungen 3. höherer Abortrate nach IVF 4. Intelligenzdefekten beim Feten C: nur 1 ist richtig [Frage 2] In der Schwangerschaft
Menarche und Körpergewicht - Methoden zur Schätzung von Zeitverläufen aus Querschnittsdaten
 Menarche und Körpergewicht - Methoden zur Schätzung von Zeitverläufen aus Querschnittsdaten Peter Martus Ekkehart Dietz Anne Madeleine Bau Charité - Berlin Hintergrund Übergewicht bei Kindern ist ein relevantes
Menarche und Körpergewicht - Methoden zur Schätzung von Zeitverläufen aus Querschnittsdaten Peter Martus Ekkehart Dietz Anne Madeleine Bau Charité - Berlin Hintergrund Übergewicht bei Kindern ist ein relevantes
Studienprotokoll EURAP Erweiterungsprotokoll Nr.1 Pharmakokinetische Untersuchungen von Antiepileptika in der Schwangerschaft und Stillzeit
 CHARITÉ - UNIVERSITÄTSMEDIZIN BERLIN CAMPUS BENJAMIN FRANKLIN CAMPUS BERLIN-BUCH CAMPUS CHARITÉ-MITTE CAMPUS VIRCHOW-KLINIKUM CHARITÉ. D-13353 Berlin CAMPUS VIRCHOW-KLINIKUM Neurologische Klinik und Poliklinik
CHARITÉ - UNIVERSITÄTSMEDIZIN BERLIN CAMPUS BENJAMIN FRANKLIN CAMPUS BERLIN-BUCH CAMPUS CHARITÉ-MITTE CAMPUS VIRCHOW-KLINIKUM CHARITÉ. D-13353 Berlin CAMPUS VIRCHOW-KLINIKUM Neurologische Klinik und Poliklinik
Neues zur Methotrexat-Intoleranz
 Neues zur Methotrexat-Intoleranz Andrea Scheuern 17.01.2015 40. Garmisch-Partenkirchner Symposium für Kinder- und Jugendrheumatologie Hintergrund Methotrexat-Intoleranz MTX-Intoleranz: - ausgeprägtes Ekelgefühl
Neues zur Methotrexat-Intoleranz Andrea Scheuern 17.01.2015 40. Garmisch-Partenkirchner Symposium für Kinder- und Jugendrheumatologie Hintergrund Methotrexat-Intoleranz MTX-Intoleranz: - ausgeprägtes Ekelgefühl
KIDSSTEP OBESITY. Fragebogen zur medizinischen Vorgeschichte T0. Code,,.., Instrument 004
 KIDSSTEP OBESITY Schweizerisches Therapie-Evaluations-Programm der Adipositas bei Kindern und Jugendlichen Programme Suisse d évaluation de la thérapie de l obésité chez les enfants et les adolescents
KIDSSTEP OBESITY Schweizerisches Therapie-Evaluations-Programm der Adipositas bei Kindern und Jugendlichen Programme Suisse d évaluation de la thérapie de l obésité chez les enfants et les adolescents
Magic Figures. We note that in the example magic square the numbers 1 9 are used. All three rows (columns) have equal sum, called the magic number.
 Magic Figures Introduction: This lesson builds on ideas from Magic Squares. Students are introduced to a wider collection of Magic Figures and consider constraints on the Magic Number associated with such
Magic Figures Introduction: This lesson builds on ideas from Magic Squares. Students are introduced to a wider collection of Magic Figures and consider constraints on the Magic Number associated with such
Therapeutisches Drug Monitoring der Antidepressiva Amitriptylin, Clomipramin, Doxepin und Maprotilin unter naturalistischen Bedingungen
 Aus der Klinik und Poliklinik für Psychiatrie, Psychosomatik und Psychotherapie der Universität Würzburg Direktor: Professor Dr. med. J. Deckert Therapeutisches Drug Monitoring der Antidepressiva Amitriptylin,
Aus der Klinik und Poliklinik für Psychiatrie, Psychosomatik und Psychotherapie der Universität Würzburg Direktor: Professor Dr. med. J. Deckert Therapeutisches Drug Monitoring der Antidepressiva Amitriptylin,
Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie
 Neue Studie zu Iscador Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie Schwäbisch-Gmünd (2. Dezember 2009) - Eine prospektive randomisierte offene Pilotstudie ergab eine Verbesserung
Neue Studie zu Iscador Verbesserte Lebensqualität für Brustkrebspatientinnen unter Chemotherapie Schwäbisch-Gmünd (2. Dezember 2009) - Eine prospektive randomisierte offene Pilotstudie ergab eine Verbesserung
Logopädische Handlungsmöglichkeiten bei selektivem Mutismus im Kindes- und Jugendalter
 HAWK Hochschule für angewandte Wissenschaft und Kunst Fachhochschule Hildesheim/Holzminden/Göttingen Fakultät Soziale Arbeit und Gesundheit BSc-Studiengang Ergotherapie, Logopädie, Physiotherapie Tina
HAWK Hochschule für angewandte Wissenschaft und Kunst Fachhochschule Hildesheim/Holzminden/Göttingen Fakultät Soziale Arbeit und Gesundheit BSc-Studiengang Ergotherapie, Logopädie, Physiotherapie Tina
Pränataldiagnostik Dr. med. Regina Rasenack Universitäts-Frauenklinik Freiburg
 Pränataldiagnostik Dr. med. Regina Rasenack Universitäts-Frauenklinik Freiburg Pränataldiagnostik Definition Untersuchungen zur Erkennung von angeborenen Fehlbildungen und Krankheiten Kleine Fehlbildungen:
Pränataldiagnostik Dr. med. Regina Rasenack Universitäts-Frauenklinik Freiburg Pränataldiagnostik Definition Untersuchungen zur Erkennung von angeborenen Fehlbildungen und Krankheiten Kleine Fehlbildungen:
Patienten Prozent [%] zur Untersuchung erschienen 64 65,3
![Patienten Prozent [%] zur Untersuchung erschienen 64 65,3 Patienten Prozent [%] zur Untersuchung erschienen 64 65,3](/thumbs/98/135702962.jpg) 21 4 Ergebnisse 4.1 Klinische Ergebnisse 4.1.1 Untersuchungsgruppen In einer prospektiven Studie wurden die Patienten erfasst, die im Zeitraum von 1990 bis 1994 mit ABG I- und Zweymüller SL-Hüftendoprothesen
21 4 Ergebnisse 4.1 Klinische Ergebnisse 4.1.1 Untersuchungsgruppen In einer prospektiven Studie wurden die Patienten erfasst, die im Zeitraum von 1990 bis 1994 mit ABG I- und Zweymüller SL-Hüftendoprothesen
Seite Landeshauptstadt München Referat für Gesundheit und Umwelt
 Seite Landeshauptstadt 1 von 5 München Referat für Gesundheit und Umwelt I. Frau Stadträtin Lydia Dietrich Herr Stadtrat Thomas Niederbühl Rathaus Joachim Lorenz Berufsmäßiger Stadtrat 12.06.2012 Welchen
Seite Landeshauptstadt 1 von 5 München Referat für Gesundheit und Umwelt I. Frau Stadträtin Lydia Dietrich Herr Stadtrat Thomas Niederbühl Rathaus Joachim Lorenz Berufsmäßiger Stadtrat 12.06.2012 Welchen
Englisch-Grundwortschatz
 Englisch-Grundwortschatz Die 100 am häufigsten verwendeten Wörter also auch so so in in even sogar on an / bei / in like wie / mögen their with but first only and time find you get more its those because
Englisch-Grundwortschatz Die 100 am häufigsten verwendeten Wörter also auch so so in in even sogar on an / bei / in like wie / mögen their with but first only and time find you get more its those because
Vivantes-Klinikum am Urban Frauenklinik CA Dr. G. Nohe
 Vivantes-Klinikum am Urban Frauenklinik CA Dr. G. Nohe Äußere Wendung des Feten aus Beckenendlage Vivantes - Klinikum Am Urban Klinik für Gynäkologie und Geburtsmedizin Gerhard Nohe Häufigkeit BEL 21 24
Vivantes-Klinikum am Urban Frauenklinik CA Dr. G. Nohe Äußere Wendung des Feten aus Beckenendlage Vivantes - Klinikum Am Urban Klinik für Gynäkologie und Geburtsmedizin Gerhard Nohe Häufigkeit BEL 21 24
Adrenogenitalsyndrom. Informationsbroschüre für Ärzte/-innen
 Adrenogenitalsyndrom Informationsbroschüre für Ärzte/-innen Inhaltsverzeichnis: Einleitung 3 Funktion der Nebennierenrinde 3 Formen des AGS 4 Genetik 6 Diagnose des AGS 7 Therapie 8 Stresssituationen und
Adrenogenitalsyndrom Informationsbroschüre für Ärzte/-innen Inhaltsverzeichnis: Einleitung 3 Funktion der Nebennierenrinde 3 Formen des AGS 4 Genetik 6 Diagnose des AGS 7 Therapie 8 Stresssituationen und
Variablen-Übersicht des Kinder-Moduls im Kompetenznetz HIV/AIDS
 Variablen-Übersicht des Kinder-Moduls im Kompetenznetz HIV/AIDS Stand: März 2009 Variablen-Übersicht Kindermodul 2 Inhalt I. HIV-positive Kinder... 3 I.1. Registrierung / Soziodemographie... 3 I.2. Anamnese...
Variablen-Übersicht des Kinder-Moduls im Kompetenznetz HIV/AIDS Stand: März 2009 Variablen-Übersicht Kindermodul 2 Inhalt I. HIV-positive Kinder... 3 I.1. Registrierung / Soziodemographie... 3 I.2. Anamnese...
S erum -C reatinin unter T orasem id. A E Mittelwert+/- Stabw. am Beob.-anfang
 3. Ergebnisse Allgemein soll bereits an dieser Stalle darauf hingewiesen werden, dass neben den in den folgenden Abschnitten gezeigten Abbildungen weitere Tabellen und graphische Darstellungen zur Verbildlichung
3. Ergebnisse Allgemein soll bereits an dieser Stalle darauf hingewiesen werden, dass neben den in den folgenden Abschnitten gezeigten Abbildungen weitere Tabellen und graphische Darstellungen zur Verbildlichung
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION
 ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
Aus der Klinik für Allgemeine Kinder- und Jugendmedizin. der Albert-Ludwigs-Universität Freiburg im Breisgau. Gestationsdiabetes -
 Aus der Klinik für Allgemeine Kinder- und Jugendmedizin der Albert-Ludwigs-Universität Freiburg im Breisgau Gestationsdiabetes - Klinische Daten nach Änderung der deutschen Leitlinie INAUGURAL-DISSERTATION
Aus der Klinik für Allgemeine Kinder- und Jugendmedizin der Albert-Ludwigs-Universität Freiburg im Breisgau Gestationsdiabetes - Klinische Daten nach Änderung der deutschen Leitlinie INAUGURAL-DISSERTATION
Disorders of sex development (DSD)
 Disorders of sex development (DSD) Siegfried Zabransky, Homburg Während der Embryonalphase (1. 12. SSW) findet die Geschlechtsdeterminierung, in der Fetalphase (12. 40. SSW) die Geschlechtsdifferenzierung
Disorders of sex development (DSD) Siegfried Zabransky, Homburg Während der Embryonalphase (1. 12. SSW) findet die Geschlechtsdeterminierung, in der Fetalphase (12. 40. SSW) die Geschlechtsdifferenzierung
Praxis für Humangene k Tübingen Dr. med. Dr. rer. nat. Saskia Biskup Fachärz n für Humangene k
 Allgemeine Informationen Fötus von Name Mutter: Vorname Mutter: Geburtsdatum Mutter: Geschlecht des Fötus: q männlich q weiblich q unbekannt Ausschluss MCC bereits erfolgt? Untersuchungsmaterial q Fruchtwasser
Allgemeine Informationen Fötus von Name Mutter: Vorname Mutter: Geburtsdatum Mutter: Geschlecht des Fötus: q männlich q weiblich q unbekannt Ausschluss MCC bereits erfolgt? Untersuchungsmaterial q Fruchtwasser
DUQUE-DATENERHEBUNG ZU ENTBINDUNGEN
 Nein Einschluss Definitionen Entbindung Die Geburt eines Kindes. DUQUE-DATENERHEBUNG ZU ENTBINDUNGEN Diagnosekriterien Patientinnen über 5 hren mit einem Diagnosecode für Entbindung nach ICD-9 oder ICD
Nein Einschluss Definitionen Entbindung Die Geburt eines Kindes. DUQUE-DATENERHEBUNG ZU ENTBINDUNGEN Diagnosekriterien Patientinnen über 5 hren mit einem Diagnosecode für Entbindung nach ICD-9 oder ICD
