Gruppenpuzzle. Thema: Elektrophile Substitution an Aromaten. Unterthemen: Sulfonierung Nitrierung Friedel-Crafts-Alkylierung Azokupplung
|
|
|
- Evagret Wolf
- vor 7 Jahren
- Abrufe
Transkript
1 Gruppenpuzzle Thema: Elektrophile Substitution an Aromaten Unterthemen: Sulfonierung itrierung Friedel-rafts-Alkylierung Azokupplung Voraussetzung: Mechanismus der elektrophilen Substitution am Beispiel der Bromierung von Benzol Kurs: Gruppen: LK 13 (hemie) 4 Gruppen á 4 Teinehmer (16 Kursteilnehmer) Literatur: 1. ET-Zürich, andreichungen aus dem Internet 2. Lissautzki, rganische hemie 3. Graeb, rganische hemie 1
2 Sulfonierung: Eine reversible Substitution Konzentrierte Schwefelsäure reagiert bei aumtemperatur nicht mit Benzol, sieht man von Protonenübertragungen ab. Als sulfonierendes eagens wird daher eine reaktivere Form dieser Säure, die rauchende Schwefelsäure verwendet, in der Schwefeltrioxid (S 3 ) gelöst vorliegt. Z.T. entsteht sie auch durch Autoprotolyse der Schwefelsäure (2 2 S 4 S S 4 - ) Auf diesem Wege wird formal ein Wasserstoff-Atom des Benzolrings durch eine Sulfonsäure (S 3 -) Gruppe ersetzt. Es entsteht Benzolsulfonsäure. Sulfonierung von Benzol S 3, 2 S 4 S 3 Der Befund, daß in rauchender Schwefelsäure die Geschwindigkeit der Sulfonierung ihrem S 3 -Gehalt proportional ist (reines S 3 selbst sulfoniert sehr rasch), läßt darauf schließen, daß S 3 die eigentliche reaktive Spezies ist. 1 Das S 3 - Molekül ist so elektrophil, daß mit Benzol direkt reagiert. Anschließend entsteht durch Protonentransfer das Produkt Benzolsulfonsäure. Mesomerie am Schwefeltrioxid Benzolsulfonsäure S S S S I II III IV Mechanismus der aromatischen Sulfonierung + S - + S + + S Benzolsulfonsäure S Die Sulfonierung ist eine Gleichgewichtsreaktion. Da die «ück-eaktion» bei nicht allzu hoher Temperatur jedoch ziemlich langsam verläuft, ist die Bildung der Sulfonsäure praktisch irreversibel. Das Gleichgewicht kann jedoch auf die Seite der Edukte verschoben werden, wenn Schwefeltrioxid durch eaktion mit Wasser 1 Die handelsübliche rauchende Schwefelsäure enthält ungefähr 8% Schwefeltrioxid in konzentrierter Säure. 2
3 entfernt wird. Erhitzt man daher den sulfonierten Aromaten in wässriger Schwefelsäure, kehrt sich die Sulfonierung vollständig um. Umkehrung der Sulfonierung S S 4 Die reversible eaktion der Sulfonierung kann man sich bei mehrschrittigen Synthesen dadurch zu nutze machen, dass man unerwünschte eaktionen an reaktionsfähigen Positionen des Aromaten vorübergehend durch die S 3 -Gruppe blockiert und so weitere Substituenten in andere Stellungen dirigiert. Solche zum Schutz eingeführte Gruppen werden auch Schutzgruppen genannt. Da sich die Sulfonsäure-Gruppe zudem wieder leicht abspalten läßt, ist diese zugleich eine gute Abgangsgruppe. Die große technische Bedeutung der aromatischen Sulfonsäuren als Zwischenprodukte zur erstellung vieler anderer Verbindungen beruht vor allem darauf, dass die Einführung von S 3 -Gruppen in aromatische inge diese hydrophil macht. Beispielsweise enthält die Mehrzahl der synthetischen Farbstoffmoleküle eine oder (meist) mehrere Sulfonsäure-Gruppen. Bei der Sulfonierung langkettiger Alkylbenzole entstehen Alkylbenzolsulfonsäuren, deren atriumsalze als waschaktive Substanzen (anionische Tenside) verwendet werden. Dodecylbenzolsulfonat ist das wichtigste Alkylbenzolsulfonat und im Gegensatz zu den früher üblichen verzweigten Alkylbenzolsulfonaten biologisch abbaubar. 3 S 3 a atriumdodecylbenzolsulfonat Wichtige Derivate der Benzolsulfonsäure sind die Sulfonamide, von denen einige wegen ihrer antibakteriellen Wirkung als Arzneimittel eingesetzt werden. Ihre Wirkungsweise besteht darin, bakterielle Enzyme, die die Synthese der Folsäure katalysieren, kompetetiv zu hemmen. Mit der Entdeckung der Antibiotika rückten die Sulfonamide immer mehr in den intergrund. Experiment 1: Sulfonierung von tert-butylbenzol Durchführung: In einem großen eagenzglas werden 10 ml konzentrierte Schwefelsäure und tert- Butylbenzol unter Eiskühlung gemischt. Die klare Lösung gibt man dann unter Eiskühlung in 50 ml gesättigte atriumchlorid-lösung. Anschließend wird der iederschlag abgesaugt, mit Wasser gewaschen und dann getrocknet. Entsorgung: 3
4 Der iederschlag in eine PE-Folie eingeschweißt und in den Entsorgungsbehälter rganische Feststoffe gegeben Experiment 2: Sulfonierung von aphtalin Schutzmaßnahmen: Schutzbrille, Schutzhandschuhe, Adsorptionsröhrchen (Vermeidung von Geruchsbelästigung) Geräte: eagenzglas (klein), eagenzglas (groß), Becherglas (100 ml), eizelement hemikalien: aphtalin, konz. Schwefelsäure Versuchsdurchführung: Vorversuch: Man versetzt eine Spatelspitze aphthalin in einem eagenzglas mit etwa 4 ml Wasser und schüttelt. Durchführung: Man versetzt in einem trockenen eagenzglas eine kleine Spatelspitze aphthalin mit 3 ml konz. Schwefelsäure und erhitzt ca. 10 min. vorsichtig im Wasserbad. ach dem Abkühlen wird zur Überprüfung der Wasserlöslichkeit des eaktionsproduktes dieses in ein mit Wasser gefülltes großes eagenzglas gegossen. (Zur Abtrennung der aromatischen Sulfonsäure aus dem eaktionsgemisch kann man sich die Tatsache zu nutze machen, dass ihre Bariumsalze im Gegensatz zu BaS 4 in Wasser leicht löslich sind. So kann überschüssige Schwefelsäure durch Ausfällung mit Bal 2 leicht abgetrennt werden. Soll hier nicht durchgeführt werden!) Entsorgung: Das eaktionsprodukt kann in den Ausguß gegeben werden. Fragen zur Selbstkontrolle: 1. Erklären Sie, warum das S 3 -Molekül so elektrophil ist, dass es Benzol direkt angreift. 2. Formulieren Sie den Mechanismus für die Bildung von o-toluolsulfonsäure aus Toluol. (o-toluolsulfonsäure dient als Ausgangsstoff für die Synthese des gebräuchlichen Süßstoffs Saccharin). 3. Begründen Sie, weshalb durch das Anhängen von S 3 Gruppen an aromatische Systeme, diese wasserlöslich macht. 4. Formulieren Sie die eaktion von aphthalin mit 2 S 4. Welche eaktionsprodukte sind denkbar? 4
5 itrierung Die eaktion von Benzol mit konzentrierter Salpetersäure in Gegenwart konzentrierter Schwefelsäure bei mäßig erhöhter Temperatur führt zur itrierung des Benzolrings. itrierung von Benzol 2 3, 2 S 4 itrobenzol Da das Stickstoffatom in der itrogruppe von 3 nicht elektrophil ist, muß es zuvor aktiviert werden. Dies geschieht durch die zugefügte Schwefelsäure, die die Salpetersäure protoniert, worauf diese ein Molekül Wasser abspaltet unter Ausbildung des stark elektrophilen 2 + (.itryl-kation oder itronium-ion) Bildung des elektrophilen Teilchens + 2 S 4 + S S 4 Mechanismus der aromatischen itrierung + S 4 + S S 4 Die itrierung ist die weitaus wichtigste Methode zur Bildung von -Bindungen an aromatischen ingen und eine der wichtigsten aromatischen Substitutionsreaktionen. Die Bedeutung der itrierungsreaktionen ist darin begründet, daß itroverbindungen durch Wahl geeigneter eaktionsbedingungen in die verschiedensten stickstoffhaltigen Verbindungen überführt werden können. So kann beispielsweise itrobenzol mit naszierendem Wasserstoff 2 leicht zu Anilin (Aminobenzol) umgesetzt werden, das als Ausgangssubstanz für eine Unzahl weiterer Verbindungen, insbesondere Farbstoffe von großer Bedeutung ist (s. Gruppenthema»Diazotierung und Azokupplung«) aus Zn und l(aq) Experiment: itrobenzol Anilin itrierung von aphthalin 2 Frisch entstehender Wasserstoff, der noch nicht aus 2 -Molekülen, sondern aus -Atomen besteht und besonders reaktiv ist. 5
6 Gefahrenhinweis: Das eaktionsprodukt ist giftig und steht im Verdacht, krebserzeugend zu sein! Schutzmaßnahmen: Schutzbrille, Schutzhandschuhe, Abzug Geräte: eagenzglas, Becherglas (100 ml) hemikalien: aphthalin, konz. Salpetersäure (ρ = 1,4 g/ml, ca. 65%ig) Versuchsdurchführung: Eine Spatelspitze aphthalin wird in einem eagenzglas mit 2 ml konz. Salpetersäure versetzt und anschließend im Wasserbad schwach erwärmt. Die entstandene klare Lösung wird in ein eagenzglas mit Wasser gegeben und dieses in ein Eisbad gestellt. Es fallen gelbe Kristalle aus. Entsorgung: Das eaktionsprodukt wird in das Entsorgungsgefäß für organische Lösemittel gegeben. Auswertung: Formulieren Sie die zugehörige eaktionsgleichung (eaktionsschema). Fragen zur Selbstkontrolle: 1. Warum verläuft die itrierung von Benzol nur unter Zusatz von konzentrierter Schwefelsäure? 2. Formulieren Sie den Mechanismus für die itrierung von Toluol zu p-itrotoluol. 3. Warum kann bei der itrierung von Toluol auf den Zusatz von konzentrierter Schwefelsäure verzichtet werden? (inweis! Konzentrierte Salpetersäure zeigt in geringem Maße eine Autoprotolyse: 3 3 Ö ) 4. Stellen Sie Vermutungen darüber an, warum bei der itrierung von aphthalin auf den Zusatz von konz. Schwefelsäure verzichtet werden kann. 6
7 FIEDEL-AFTS -eaktion Die Friedel-rafts-eaktionen gehören zu den wichtigsten und bedeutendsten in der organischen hemie. Sie eröffnen ein weites Feld der organischen Synthese- hemie. Zum Verständnis ihrer Prinzipien gehört die Kenntnis der elektrophilen aromatischen Substitution. Es ist zweckmäßig, die Friedel-rafts-eaktion zu untergliedern, und zwar in die Friedel-rafts-Alkylierung, das ist die Einführung von Alkyl-Gruppen (bzw. Alkyl-Aryl-Gruppen) in aromatische Systeme, und in die Friedel-rafts-Acylierung, das ist die Einführung von Acylgruppen in Aromaten. inweis: Alkyl-Gruppen = Alkan-este Aryl-Gruppen = Aromatischer-est Acyl-Gruppe = I. FIEDEL-AFTS-Alkylierung Bei der Einwirkung von Alkylhalogeniden auf aromatische Kohlenwasserstoffe in Gegenwart katalytischer Mengen von wasserfreiem Aluminiumchlorid entstehen oft unter heftiger alogenwasserstoffentwicklung alkylierte Kohlenwasserstoffe, z.b. + l All3 + l Der Mechanismus der Alkylierung läßt sich folgendermaßen deuten: Das All 3 hat die Tendenz, das alogenatom des Alkylhalogenids zum Komplex, z.b. [All 4 ] -, zu binden. ierbei braucht es zu keiner völligen Trennung der Kohlenstoff-alogen-Bindung zu kommen. Das stark positivierte -Atom des Alkylhalogenids greift das aromatische π-elektronensystem elektrophil an: + l All3 [All 4 ]- π-komplex [All 4 ]- σ-komplex + All 3 + l 7
8 Der primär entstehende π-komplex stabilisiert sich zu einem positiv geladenen σ- Komplex, dessen Ladung delokalisiert ist. Bis zu dieser Stufe verläuft die eaktion völlig identisch mit der der elektrophilen Addition an =-Doppelbindungen. Während jedoch beim lefin ein Anion addiert wird, erfolgt am Benzolkern die Abspaltung eines Protons unter ückbildung des energetisch begünstigten aromatischen Systems. Beispiel: Darstellung von Triphenylmethan aus Trichlormethan und Benzol (Lehrerversuch) eagenzglas (18 mm x 180 mm), Uhrglasschale Benzol, Trichlormethan (hloroform), Aluminiumchlorid (wasserfrei), konzentrierte Ammoniaklösung Durchführung In ein völlig trockenes eagenzglas werden zu 1 g wasserfreiem Aluminiumchlorid 5 ml Benzol (Krebsklasse A1) und danach etwa 0,5 ml Trichlormethan tropfenweise hinzugegeben. Vorsicht! Wasserfreies Aluminiumchlorid reagiert heftig mit Wasser! ach dem Einsetzen der eaktion wird neben die Öffnung des eagenzglases eine geöffnete Flasche mit konzentrierter Ammoniaklösung gehalten. achdem die Gasentwicklung im eagenzglas beendet ist, wird etwas von der Flüssigkeit auf eine Uhrglasschale filtriert. ach einiger Zeit ist das restliche Benzol und Trichlormethan verdunstet. Auswertung Aufgabe: Auf der Uhrglasschale bleibt als fester Stoff Triphenylmethan zurück. Aus Benzol und Trichlormethan entsteht durch eine Friedel-rafts-Alkylierung das Triphenylmethan hlorwasserstoff entweicht, und bildet mit Ammoniak einen weißen auch von Ammoniumchlorid. Formuliere für die obige eaktion das eaktionsschema an. Welche Strukturformel hat Triphenylmethan? Durch den Eintritt von Alkylgruppen in den ing erhöht sich die Basizität des aromatischen Systems. Infolge der basischeren Eigenschaften gegenüber dem nichtsubstituierten ing kann die Alkylierung weitergehen,- nur im großen Überschuß von Aromaten sind Monoalkyl-Substitutionsprodukte möglich. Die Friedel-rafts-Alkylierungs-eaktion ist eine gut brauchbare Methode zur Synthese von aromatischen Kohlenwasserstoffen mit Seitenketten. So lassen sich z.b. im Benzol nacheinander alle Wasserstoffatome durch Alkyl- bzw. Alkyl-Aryl- este ersetzen. 8
9 Schematisch: l 2 + All l oder + l All l Benzylchlorid Diphenylmethan Anstelle von Alkylhalogeniden lassen sich auch Alkene zur Alkylierung von Benzol verwenden. Durch Protonierung mit Schwefelsäure entstehen stark elektrophile arbeniumionen (oder arbokationen). Die eaktion von Benzol mit Ethen führt zu Ethylbenzol, das durch Dehydrierung in Styrol überführt wird. Aus diesem stellt man durch Polymerisationen Polystyrol her. Ethen + 2 S 4 + S 4 + Ethylbenzol 3 + II. Friedel-rafts-Acylierung Die Acylierung aromatischer ingsysteme nach Friedel-rafts ist die wichtigste Synthese rein aromatischer oder gemischt aromatisch-aliphatischer Ketone. Im wesentlichen wendet man Elektrophile wie Säureanhydride oder Säurehalogenide -Säurechloride werden bevorzugt - als Acylierungsmittel in Gegenwart von Lewis- Säuren für die meist sehr glatt verlaufende eaktion an. Das eaktionsprinzip Die genannten Elektrophile, Säureanhydride und Säurehalogenide, werden unter dem Einfluß von wasserfrelem Aluminiumchlorid als Elektronenakzeptor erfolgt die Bildung von Acylium-Kationen Die positiv geladenen Acyl-lonen reagieren mit den aromatischen Systemen. 9
10 Die eaktion vollzieht sich in zwei Schritten: 1. Bildung des positiv geladenen Acyl-Kations: Säurechlorid als eagens: + All 3 + [All 4 ] l 2. Angriff des Elektrophils auf das aromatische System: +... etc. + Beispiel: Darstellung von Benzophenon (Diphenylketon) + l All3 + l Benzophenon Aufgaben zur Selbstkontrolle: 1. Stellen Sie dar, wie aus Acetylchlorid und Benzol mit ilfe von Aluminiumchlorid Acetophenon (Methylphenylketon) zu erhalten ist 10
11 Azokupplung Azofarbstoffe stellen die größte Klasse künstlicher Farbstoffe dar. Gemeinsam ist ihnen die Azo-Gruppe =, die jeweils zwei kleinere aromatische Systeme zu einem größeren verknüpft. 2 Anilingelb S 3 a S 3 a 2 2 Grenzformeln zweier Azofarbstoffe Mit der Synthese der Azofarbstoffe Ende des 19. Jahrhunderts eng verbunden ist der Aufschwung der chemischen Farbenindustrie, denn es gelang nun, Farbstoffe in allen Farbschattierungen und von erstaunlicher Brillanz herzustellen. Als Ausgangsstoff für Azofarbstoffe diente Anilin, ein Bestandteil des Steinkohlenteers. eute machen die Azofarbstoffe etwa 70% des gesamten Farbstoffbereichs aus. Die Synthese von Azofarbstoffen erfolgt in zwei Schritten: 1. der Diazotierung des Anilins oder eines Anilinderivats und 2. der anschließenden Azokupplung mit einer aromatischen Verbindung. 1. Schritt: Diazotierung Aromatische Amine, so auch Anilin und seine Derivate, reagieren mit salpetriger Säure 3 (gewonnen aus atriumnitrit und Salzsäure) zu Diazonium-Ionen: eaktionsschema der Diazotierung Kongorot a a Anilin Salpetrige Säure Diazonium-Ion 3 Salpetrige Säure ist instabil und muß daher frisch hergestellt werden. 11
12 Diazonium-Ionen zersetzen sich bei höheren Temperaturen leicht, daher muß die Diazotierung bei Temperaturen unter 5 durchgeführt werden. 2. Schritt: Azokupplung Die Azokupplung ist eine typische elektrophile Substitutionsreaktion, in der das Diazonium-Ion als elektrophiles Teilchen wirkt. Als Kupplungskomponente werden aktivierte Aromaten wie Phenol- oder Anilinderivate eingesetzt. eaktionsschema der Azokupplung Diazonium-Ion Aminoazobenzol (Anilingelb) Durch Variation der Diazokomponente und der Kupplungskomponente erhält man eine Vielzahl verschiedenster Azofarbstoffe in allen Farbnuancen. Die Seitengruppen beeinflussen die Eigenschaften dieser Farbstoffe. Eine Sulfonsäure-Gruppen beispielsweise macht die Farbstoffe wasserlöslich. Experiment: Synthese eines Azofarbstoffes Schutzmaßnahmen: Schutzbrille, Schutzhandschuhe, Abzug (evtl. Bildung nitroser Gase) Geräte: hemikalien: 5 Bechergläser (250 ml, 100 ml, 50 ml) Sulfanilsäurelösung (0,5g in 5mL atronlauge) Glaswanne atronlauge (c = 2 mol L -1 ) 2 Meßzylinder atriumnitrit (w = 0,8%) Glasstab Salzsäure (c = 4 mol L -1 ) Wasserstrahlpumpe 2-aphthollsg. (0,4g in 5 ml atronlauge) Saugflasche mit Trichter dest. Wasser undfilter Eis zum Kühlen Versuchsaufbau und Versuchsdurchführung: I. Diazotierung In das gekühlte Becherglas mit 25 ml Salzsäure wird ein Thermometer gestellt. Zuerst wird die Sulfanilsäurelösung in die gekühlte Salzsäure portionsweise eingerührt und die Mischung auf 0 heruntergekühlt. Danach erfolgt die Zugabe von 25 ml atriumnitritlösung in kleinen Portionen. Dabei ist darauf zu achten, daß die Temperatur der Mischung 5 nicht überschreitet. Gegebenenfalls Eis in die Mischung geben. Aromatische Diazoniumsalze sind in Lösung relativ stabil. 12
13 II. Azokupplung In die eisgekühlte Diazoniumlösung wird die 2-aphthollösung eingerührt. Dabei fällt der Farbstoff aus und kann abfiltriert werden. autkontakt mit dem Azofarbstoff vermeiden. Welche Farben nimmt der Farbstoff im sauren bzw. alkalischen Medium an? Entsorgung: Der Farbstoff sowie das Filtrat werden in den Sammelbehälter rganische Lösemittel entsorgt. Das Filterpapier soll im Behälter feste Abfälle - organisch getrennt verpackt gesammelt werden. Die mit dem Farbstoff kontaminierten Glasgeräte werden mit Spiritus gespült und die Spülung in den Sammelbehälter rganische Lösemittel gegeben. Auswertung: 1. Welches Diazonium-Ion wird aus Sulfanilsäure gebildet? 2. Geben Sie die Formel des entstehenden Azofarbstoffes range II (2- aphtholorange) an. 3 S 2 Sulfanilsäure 2-aphthol Fragen zur Selbstkontrolle: 1. Formulieren Sie die Synthese eines Farbstoffs aus Anthranilsäure und Dimethylanilin (Diazotierung und Azokupplung). 2 Anthranilsäure Diazoniumkomponente 3 3 Dimethylanilin Kupplungskomponente 13
Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, Natriumsalz) - Azofarbstoff -
 Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß. Schulversuch-Protokoll Jan gr.
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
4. Phthaleine 4.1. Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid
 4. Phthaleine 4.1 Phthaleine Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid ausgeht. Phenolphthalein erhält man durch Zusammenschmelzen von
4. Phthaleine 4.1 Phthaleine Mit den Triphenylmethanfarbstoffen eng verwandt sind die Phthaleine, deren Synthese vom Phthalsäureanhydrid ausgeht. Phenolphthalein erhält man durch Zusammenschmelzen von
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe.
 2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
Herstellung von Azofarbstoffen und Färben von Textilien
 Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Versuchsprotokoll. Gruppe 12, Typ: Pflichtversuch - H + Einsatz in der Schule Sulfanilsäure NH 2 C 6 H 4 SO 3 H Xi 36/38, 43 24, 37 S I
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.01.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Synthese von β-aphtolorange
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.01.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Synthese von β-aphtolorange
Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2
![Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2](/thumbs/95/126253543.jpg) Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Darstellung von Malachitgrün Präparat 5
 Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Herstellung des Benzoldiazoniumchlorids aus Anilin, Natriumnitrit und Salzsäure. Benzoldiazonium-Ion
 Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
8 Carbonsäuren und Derivate
 8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
Auswertung der Versuche mit Aminosäuren und Proteinen (Eiweiß)
 Auswertung der Versuche mit Aminosäuren und Proteinen (Eiweiß) Vorbereitung: Für die folgenden Versuche wird eine Eiweißlösung aus dem Eiklar eines ühnereis hergestellt, indem man dieses in 60 ml dest.
Auswertung der Versuche mit Aminosäuren und Proteinen (Eiweiß) Vorbereitung: Für die folgenden Versuche wird eine Eiweißlösung aus dem Eiklar eines ühnereis hergestellt, indem man dieses in 60 ml dest.
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Präparat 1: Darstellung von Essigsäurebutylester
 hristina Sauermann 1 - A- Praktikum Präparat 1: Darstellung von Essigsäurebutylester 3 3 ( 2 ) 3 2 S 4 (konz.) in l 3 3 4 9 Essigsäure Butanol Essigsäurebutylester ( 2 4 2 ) ( 4 10 ) ( 6 12 2 ) M = 60,05
hristina Sauermann 1 - A- Praktikum Präparat 1: Darstellung von Essigsäurebutylester 3 3 ( 2 ) 3 2 S 4 (konz.) in l 3 3 4 9 Essigsäure Butanol Essigsäurebutylester ( 2 4 2 ) ( 4 10 ) ( 6 12 2 ) M = 60,05
13. Amine und ihre Derivate
 Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
Synthese von 3-Aminophthalsäurehydrazid
 Illumina-Chemie.de - Artikel Synthesen Synthese von 3-Aminophthalsäurehydrazid Hier wird eine zweistufige Synthese von Luminol beschrieben. Luminol findet insbesondere für Chemilumineszenz Verwendung,
Illumina-Chemie.de - Artikel Synthesen Synthese von 3-Aminophthalsäurehydrazid Hier wird eine zweistufige Synthese von Luminol beschrieben. Luminol findet insbesondere für Chemilumineszenz Verwendung,
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Synthese des Azofarbstoff Orange II
 ynthese des Azofarbstoff range II a + - rganische Chemie Praktikum 1 Zürich, 05.12.2006 W 2006 / 07 Maresa Afthinos Assistenz: Michael chär Versuchsdurchführung: 27. ovember 2006-1 - CP1 ynthese 2 Maresa
ynthese des Azofarbstoff range II a + - rganische Chemie Praktikum 1 Zürich, 05.12.2006 W 2006 / 07 Maresa Afthinos Assistenz: Michael chär Versuchsdurchführung: 27. ovember 2006-1 - CP1 ynthese 2 Maresa
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2016
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23.11.2010 Gruppe 4: Aromaten Versuch (elektr.
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23.11.2010 Gruppe 4: Aromaten Versuch (elektr.
Von Arrhenius zu Brönsted
 Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Ableitung wieder aus einer einfachen anorganischen Verbindung, NH 3 :
 168 X. Amine 1. Übersicht Ableitung wieder aus einer einfachen anorganischen Verbindung, 3 : primär sekündär tertiär Achtung: Ausdrücke primär, sekundär und tertiär beziehen sich auf, nicht auf wie bei
168 X. Amine 1. Übersicht Ableitung wieder aus einer einfachen anorganischen Verbindung, 3 : primär sekündär tertiär Achtung: Ausdrücke primär, sekundär und tertiär beziehen sich auf, nicht auf wie bei
 Michael Woock Universität Duisburg Fakultät 4 / Didaktik der Chemie Lotharstr. 1 47057 Duisburg e-mail: woock@uni-duisburg.de ----------------------------------------------------------------------------------------------------------
Michael Woock Universität Duisburg Fakultät 4 / Didaktik der Chemie Lotharstr. 1 47057 Duisburg e-mail: woock@uni-duisburg.de ----------------------------------------------------------------------------------------------------------
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Herstellung und Oxidation von 2,4,6-Tri-tert-butylphenol
 2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Synthese von Essigsäureisopropylester (1) Präparat 1
 Synthese von Essigsäureisopropylester (1) Präparat 1 1. Reaktionstyp: Azeotrope Veresterung 2. Reaktionsgleichung: 3 3 3 3 2 3 3 Essigsäure Isopropanol Essigsäureisopropylester Wasser 60,05 g/mol 60,1
Synthese von Essigsäureisopropylester (1) Präparat 1 1. Reaktionstyp: Azeotrope Veresterung 2. Reaktionsgleichung: 3 3 3 3 2 3 3 Essigsäure Isopropanol Essigsäureisopropylester Wasser 60,05 g/mol 60,1
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Aromatische Substitution. Dr. Florian Achrainer AK Zipse
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan
 Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
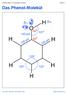 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Synthese eines Fruchtesters
 Synthese eines Fruchtesters 1/5 Synthese eines Fruchtesters Theorie arbonsäuren können mit Alkoholen unter Abspaltung eines Wasser-Moleküls zu arbonsäure-estern reagieren: ' ' Die Einstellung der Gleichgewichts-Lage
Synthese eines Fruchtesters 1/5 Synthese eines Fruchtesters Theorie arbonsäuren können mit Alkoholen unter Abspaltung eines Wasser-Moleküls zu arbonsäure-estern reagieren: ' ' Die Einstellung der Gleichgewichts-Lage
Organostickstoff- Verbindungen
 rganostickstoff- Verbindungen [1] Chiralität von Aminen [2] -Enantiomere Isomerisieren sehr schnell -E A 20-30 KJ/mol [2] Alkylierung von Ammoniak [2] [2] [2] -geringe Selektivität aufgrund von Mehrfachalkylierung
rganostickstoff- Verbindungen [1] Chiralität von Aminen [2] -Enantiomere Isomerisieren sehr schnell -E A 20-30 KJ/mol [2] Alkylierung von Ammoniak [2] [2] [2] -geringe Selektivität aufgrund von Mehrfachalkylierung
Reak%onen an der Carbonylgruppe
 Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Synthese von 1-Amino-2-naphthol
 Illumina-Chemie.de - Artikel Synthesen Synthese von Der wohl bekannteste Weg zu einer Aminogruppe ist die Nitrierung eines Kohlenwasserstoffes und anschließende Reduktion. Reaktive Aromaten wie Phenole
Illumina-Chemie.de - Artikel Synthesen Synthese von Der wohl bekannteste Weg zu einer Aminogruppe ist die Nitrierung eines Kohlenwasserstoffes und anschließende Reduktion. Reaktive Aromaten wie Phenole
7. Studieneinheit. Siebte Studieneinheit
 86 Siebte Studieneinheit 7. Studieneinheit Lernziele Löslichkeit organisch-chemischer Substanzen unter verschiedenen Bedingungen Charakteristische Reaktionen ausgewählter organisch-chemischer Stoffklassen
86 Siebte Studieneinheit 7. Studieneinheit Lernziele Löslichkeit organisch-chemischer Substanzen unter verschiedenen Bedingungen Charakteristische Reaktionen ausgewählter organisch-chemischer Stoffklassen
Lösungen 3. Übungsblatt SS 2002
 Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
1.1 V 1 Überprüfung des Satzes von Hess mit der Reaktion von Calcium und Salzsäure
 1.1 V 1 Überprüfung des Satzes von Hess mit der Reaktion von Calcium und Salzsäure In diesem Versuch soll der Satz von Hess (die umgesetzte Wärmemenge ist bei einer chemischen Reaktion unabhängig vom Weg)
1.1 V 1 Überprüfung des Satzes von Hess mit der Reaktion von Calcium und Salzsäure In diesem Versuch soll der Satz von Hess (die umgesetzte Wärmemenge ist bei einer chemischen Reaktion unabhängig vom Weg)
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser/Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Carbonsäuren und Derivate Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser/Dr. Martin Sumser September
Schulversuch-Protokoll Jan gr. Austing
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
Indanon ist das Produkt einer Friedel-Crafts-Acylierung Geben Sie die Reaktionsgleichung zu seiner Synthese an.
 Aromatenchemie für Fortgeschrittene 1.Wiederholung: Elektrophile aromatische Substitutionen 1.1. Geben Sie die Bruttogleichung für die zweistufige Synthese von Styren an. 1.2. Formulieren Sie die Reaktionsgleichung
Aromatenchemie für Fortgeschrittene 1.Wiederholung: Elektrophile aromatische Substitutionen 1.1. Geben Sie die Bruttogleichung für die zweistufige Synthese von Styren an. 1.2. Formulieren Sie die Reaktionsgleichung
Reaktionsmechanismen nach dem gleichnahmigen Buch von R. Brückner
 Reaktionsmechanismen nach dem gleichnahmigen Buch von R. ückner Kap. 5 Substitutionsreaktionen am Aromaten Dr. ermann A. Wegner hermann.wegner@unibas.ch lektrophile aromatische Substitution Wheland-Komplex
Reaktionsmechanismen nach dem gleichnahmigen Buch von R. ückner Kap. 5 Substitutionsreaktionen am Aromaten Dr. ermann A. Wegner hermann.wegner@unibas.ch lektrophile aromatische Substitution Wheland-Komplex
Schulversuch (Gruppe 6/Assistentenversuch): Vergleich aliphatischer Alkohole und Phenole
 Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure
 Illumina-Chemie.de - Artikel Synthesen Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure Geräte: Erlenmeyerkolben, Becherglas, Scheidetrichter, Pipetten, Trichter und Faltenfilter Chemikalien: Kaliumhexacyanoferrat(III)
Illumina-Chemie.de - Artikel Synthesen Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure Geräte: Erlenmeyerkolben, Becherglas, Scheidetrichter, Pipetten, Trichter und Faltenfilter Chemikalien: Kaliumhexacyanoferrat(III)
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
5007 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin
 57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
Nährstoffe und Nahrungsmittel
 1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231
 Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231 Fachhochschule Aachen, Campus Jülich Fachprüfung 32330/32231 Organische Chemie für Biotechnologen II Prüfungsdatum: 10.07.2013 Prüfungsdauer:
Klausur Organische Chemie II für Biotechnoligen Prüfung 32330/32231 Fachhochschule Aachen, Campus Jülich Fachprüfung 32330/32231 Organische Chemie für Biotechnologen II Prüfungsdatum: 10.07.2013 Prüfungsdauer:
3. Aromatische Verbindungen Benzol(en)
 3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
Herstellung von Triphenylphosphin
 Aqua labor Herstellung von Triphenylphosphin Eigenschaften des Produktes: Triphenylphosphin, kurz TPP, ist eine farblose (oder in einem weniger reinem Zustand leicht gelbliche), aus monoklinen Kristallen
Aqua labor Herstellung von Triphenylphosphin Eigenschaften des Produktes: Triphenylphosphin, kurz TPP, ist eine farblose (oder in einem weniger reinem Zustand leicht gelbliche), aus monoklinen Kristallen
Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff -
 hristina Sauermann 1 - A- Praktikum Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff - Teil I: Isolierung von Trimyristin aus Muskatnuss 1. Prinzip Gepulverte Muskatnüsse
hristina Sauermann 1 - A- Praktikum Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff - Teil I: Isolierung von Trimyristin aus Muskatnuss 1. Prinzip Gepulverte Muskatnüsse
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Radikalische Substitution von Alkanen
 adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
Umweltschutz und Recycling
 Schulversuchspraktikum Hendrik Schöneich Sommersemester 2017 Klassenstufen 5/6 Umweltschutz und Recycling Kurzprotokoll Auf einen Blick: In diesem Protokoll werden drei Versuche zum Thema Recycling vorgestellt.
Schulversuchspraktikum Hendrik Schöneich Sommersemester 2017 Klassenstufen 5/6 Umweltschutz und Recycling Kurzprotokoll Auf einen Blick: In diesem Protokoll werden drei Versuche zum Thema Recycling vorgestellt.
Carbonsäurederivate lassen sich durch Hydrolyse in die Carbonsäuren überführen. O C R. abnehmende Reaktivität
 Vorlesung 40 arbonsäurederivate und X arbonsäurederivate lassen sich durch ydrolyse in die arbonsäuren überführen. arbonsäurechlorid arbonsäureanhydrid arbonsäureester arbonsäureamid abnehmende eaktivität
Vorlesung 40 arbonsäurederivate und X arbonsäurederivate lassen sich durch ydrolyse in die arbonsäuren überführen. arbonsäurechlorid arbonsäureanhydrid arbonsäureester arbonsäureamid abnehmende eaktivität
Inhaltsverzeichnis. 3 Organische Chemie. Vorwort Chemische Bindung Chemische Reaktionstypen Bindungen...
 VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
Wiederholungsklausur zur Grundvorlesung Organische Chemie im SS 2002
 Prof. Dr. B. König Institut für rganische hemie Universität Regensburg Wiederholungsklausur zur Grundvorlesung rganische hemie im SS 2002 am Samstag, dem 28. September 2002 Name:...Vorname:... Geburtsdatum:...Unterschrift:...
Prof. Dr. B. König Institut für rganische hemie Universität Regensburg Wiederholungsklausur zur Grundvorlesung rganische hemie im SS 2002 am Samstag, dem 28. September 2002 Name:...Vorname:... Geburtsdatum:...Unterschrift:...
Chemiepraktikum für Biologen. Versuchsprotokoll. Einzelanalyse Trennung, Reinigung, Nachweis von 3 Reinsubstanzen
 Johannes Gutenberg Universität Fachbereich Biologie hemiepraktikum für Biologen SS 2002 Versuchsprotokoll zum Thema Einzelanalyse Trennung, Reinigung, achweis von 3 Reinsubstanzen von Ausgangslösung: Die
Johannes Gutenberg Universität Fachbereich Biologie hemiepraktikum für Biologen SS 2002 Versuchsprotokoll zum Thema Einzelanalyse Trennung, Reinigung, achweis von 3 Reinsubstanzen von Ausgangslösung: Die
Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol
 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Dietikon, 3. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Dietikon, 3. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Organische Chemie für MST 5. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Verzeichnis der Wortabkürzungen... Verzeichnis der Zeichen und Symbole...XVII
 VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 21/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 11.2.211 Gruppe 12: Farb-, Spreng- und Wirkstoffe
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 21/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 11.2.211 Gruppe 12: Farb-, Spreng- und Wirkstoffe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Organisch-chemisches Praktikum Wintersemester 2005/06. o-chlortoluen. Stephan Steinmann
 rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
1. a) Geben sie den Reaktionsmechanismus für die Nitrierung und die Sulfonierung von Benzol an. Beginnen sie mit der Erzeugung des Elektrophils.
 Übungsblatt 05 - C I - SoSe 2014 (Prof. Bunz) 1. a) Geben sie den Reaktionsmechanismus für die itrierung und die Sulfonierung von Benzol an. Beginnen sie mit der rzeugung des lektrophils. I) rzeugung lektrophil:
Übungsblatt 05 - C I - SoSe 2014 (Prof. Bunz) 1. a) Geben sie den Reaktionsmechanismus für die itrierung und die Sulfonierung von Benzol an. Beginnen sie mit der rzeugung des lektrophils. I) rzeugung lektrophil:
uril Illumina-Chemie.de - Artikel (Cucurbituril, CB6, CB[6])
![uril Illumina-Chemie.de - Artikel (Cucurbituril, CB6, CB[6]) uril Illumina-Chemie.de - Artikel (Cucurbituril, CB6, CB[6])](/thumbs/88/114540367.jpg) Illumina-Chemie.de - Artikel Synthesen uril (, CB6, CB[6]) Cucurbit[6]uril (CB[6]) ist ein makrocyclisches Molekül, das aus 6 Glycoluril-Einheiten aufgebaut ist, die über 12 Methylenbrücken an den Stickstoffatomen
Illumina-Chemie.de - Artikel Synthesen uril (, CB6, CB[6]) Cucurbit[6]uril (CB[6]) ist ein makrocyclisches Molekül, das aus 6 Glycoluril-Einheiten aufgebaut ist, die über 12 Methylenbrücken an den Stickstoffatomen
Versuchsprotokoll. Nitrierung von Phenol. Gruppe 4, Typ: Pflichtversuch O O - N
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung)
 Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P )
 Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P1145600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
Saure, neutrale und alkalische Reaktionen von Salzlösungen (Artikelnr.: P1145600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema:
(±)-4-Methyl-3- heptanon
 Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Beispielaufgaben IChO 2. Runde 2019 Säurederivate. H2, Pd/C
 Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
Beispielaufgaben Ih 2. Runde 2019 Säurederivate Beispiel 1 ligocarbonsäuren Gegeben sei folgendes Reaktionsschema: A H2, Pd/ H 2, Lindlar Na/NH 3(l) B D Base E A hat eine molare Masse von 118,09 g mol
Synthese von Diphenylmethanol
 FS 2008 ET Zürich 23.06.2009 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von Diphenylmethanol Dietikon, 18. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 FS 2008
FS 2008 ET Zürich 23.06.2009 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von Diphenylmethanol Dietikon, 18. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 FS 2008
Zuckernachweis mit Tollens-Reagenz
 Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Nr. Aufgabe Pkt. 2.2 Erklären Sie die ungewöhnliche Stabilität aromatischer Systeme gegenüber Additionsversuchen!
 aromatische Kohlenwasserstoffe Jahrgang Index Nr. Aufgabe Pkt 15/IV 1 o-bromtoluol soll aus Benzol, Methan und Brom mit geeigneten Katalysatoren hergestellt werden. Beschreiben Sie unter Verwendung von
aromatische Kohlenwasserstoffe Jahrgang Index Nr. Aufgabe Pkt 15/IV 1 o-bromtoluol soll aus Benzol, Methan und Brom mit geeigneten Katalysatoren hergestellt werden. Beschreiben Sie unter Verwendung von
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und Herstellung
 6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
Organisch chemisches Praktikum II
 18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
