Kleine Formelsammlung Technische Thermodynamik
|
|
|
- Ruth Gärtner
- vor 7 Jahren
- Abrufe
Transkript
1 Kleine Formelsammlung Technische Thermodynamik on Hans-Joachim Kretzschmar, Ingo Kraft überarbeitet Kleine Formelsammlung Technische Thermodynamik Kretzschmar / Kraft schnell und ortofrei erhältlich bei beck-sho.de DIE FACHBUCHHANDLUNG Hanser München 2007 Verlag C.H. Beck im Internet: ISBN Inhaltserzeichnis: Kleine Formelsammlung Technische Thermodynamik Kretzschmar / Kraft
2 Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN-10: ISBN-13: Leserobe Weitere Informationen oder Bestellungen unter htt:// sowie im Buchhandel
3 6 Energiebilanz 1. Hautsatz der Thermodynamik 6.1 Ruhendes geschlossenes System Energiebilanz zwischen Zustand 1 und 2 1. Hautsatz bei geschlossenen Systemen Q12 Q12 + W12 = U2 U1 Summe der Wärmen, zu- (> 0) oder abgeführt (< 0) zwischen Anfangszustand 1 und Endzustand 2 W Summe der Arbeiten, zu- (> 0) oder abgeführt (< 0) U 12 2 U1 Differenz der inneren Energie des Systems zwischen Endzustand 2 und Anfangszustand 1 U U = m ( u u ) m Masse des Systems u2 u1 Differenz der sezifischen inneren Energie des Systems zwischen 2 und 1 Berechnung in 6.3 Beisiel eines geschlossenen Systems mit energetischen Bilanzgrößen Fluid W diss12 - Dissiationsarbeit m = const Rührer Systemgrenze Zustandsänderung W V12 - Volumenänderungsarbeit 1 2 u Umgebungsdruck V F K (z) äußere Kolbenkraft 1 V innere 2 Reibung 1 2 T 1 T 2 z 2 U Wärme 1 U 2 Q z z 1 12 W N12 äußere Kolbennutzarbeit Änderung der inneren Energie im System Brenner 2 1
4 68 6 Energiebilanz 1. Hautsatz der Thermodynamik Zu- oder abgeführte Arbeiten W12 = + Wdiss12 [ W ]= 1kJ W12 Summe der Arbeiten, zu- (> 0) oder abgeführt (< 0) Volumenänderungsarbeit, zu- (> 0) oder abgeführt (< 0) W dissiierte Arbeiten (> 0, da zugeführt) diss12 Sonderfall: = const Q12 Q12 + Wdiss12 = H2 H1 Summe der Wärmen, zu- (> 0) oder abgeführt (< 0) zwischen Anfangszustand 1 und Endzustand 2 W Summe der dissiierten Arbeiten (> 0, da zugeführt) H diss12 H Differenz der Enthalie des Systems zwischen 2 und H H = m ( h h ) m Masse des Systems h2 h1 Differenz der sezifischen Enthalie des Systems zwischen 2 und 1 Berechnung in Volumenänderungsarbeit Volumenänderungsarbeit zwischen Zustand 1 und 2 V ( ) V12 V2 ( ) d r12 [ WV ]= 1kJ V1 W = V V + W Volumenänderungsarbeit, zu- oder abgeführt zwischen Anfangszustand 1 und Endzustand 2 Bild in Gleichung der Zustandsänderung für den Druck als Funktion des Volumens V
5 6 Energiebilanz 1. Hautsatz der Thermodynamik 69 Wr12 Reibungsarbeit aufgrund innerer Reibung im Fluid, z. B. durch Verwirblung (> 0, da dissiiert) Sezifische Volumenänderungsarbeit zwischen Zustand 1 und 2 w12 m () wr12 2 w12 = = ()d + w m 1 r12 [ w ] = 1kJkg sezifische Volumenänderungsarbeit, zu- oder abgeführt zwischen Anfangszustand 1 und Endzustand 2 Volumenänderungsarbeit, zu- oder abgeführt Masse Gleichung der Zustandsänderung für den Druck als Funktion des sezifischen Volumens sezifische Reibungsarbeit (> 0, da dissiiert) 1 Sezifische Volumenänderungsarbeit im,-diagramm Beisiel: Komression ( ) d= w w 12 r12 1 d () d 1 V = m
6 70 6 Energiebilanz 1. Hautsatz der Thermodynamik Differenzielle Volumenänderungsarbeit δwv dv δw r δw = dv + δw V r differenzielle Volumenänderungsarbeit, zu- oder abgeführt (Das Differenzial δwv steht für dw V.Mit δ werden die Differenziale on Prozessgrößen gekennzeichnet.) Druck differenzielle Änderung des Volumens V differenzielle Reibungsarbeit (> 0, da dissiiert) Äußere Nutz- und Kolbenarbeit Äußere Nutzarbeit zwischen Zustand 1 und 2 WN12 ( ) W = W + V V = W N12 V12 U 2 1 K12 [ W N ] = 1kJ äußere Nutzarbeit, zu- oder abgeführt zwischen Anfangszustand 1 und Endzustand 2 Bild in W Volumenänderungsarbeit, zu- oder abgeführt V12 ( ) U V2 V1 Verschiebearbeit des Umgebungsdruckes U barometrischer Druck in der Umgebung des Systems 3.2 V1, V2 Volumen des Systems in den Zuständen 1 und 2 WK12 äußere Kolbenarbeit, zu- oder abgeführt zwischen Anfangszustand 1 und Endzustand 2 Bild in Äußere Kolbenarbeit zwischen Zustand 1 und 2 WK12 z2 WK12 = FK ( z ) d z [ WK ]= 1kJ z1 äußere Kolbenarbeit, zu- oder abgeführt zwischen Anfangszustand 1 und Endzustand 2 Bild in 6.1.1
Kleine Formelsammlung Technische Thermodynamik
 Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN-10: 3-446-41421-5 ISBN-13: 978-3-446-41421-1 Vorwort Weitere Informationen oder Bestellungen unter htt://www.hanser.de/978-3-446-41421-1
Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN-10: 3-446-41421-5 ISBN-13: 978-3-446-41421-1 Vorwort Weitere Informationen oder Bestellungen unter htt://www.hanser.de/978-3-446-41421-1
Technische Thermodynamik
 Technische Thermodynamik Theoretische Grundlagen und praktische Anwendungen von Günter Cerbe, Gernot Wilhelms 5., aktualis. Aufl Technische Thermodynamik Cerbe / Wilhelms schnell und portofrei erhältlich
Technische Thermodynamik Theoretische Grundlagen und praktische Anwendungen von Günter Cerbe, Gernot Wilhelms 5., aktualis. Aufl Technische Thermodynamik Cerbe / Wilhelms schnell und portofrei erhältlich
Leseprobe. Günter Cerbe, Gernot Wilhelms. Technische Thermodynamik. Theoretische Grundlagen und praktische Anwendungen ISBN:
 Leseprobe Günter Cerbe, Gernot Wilhelms Technische Thermodynamik Theoretische Grundlagen und praktische Anwendungen ISBN: 978-3-446-4464-7 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-4464-7
Leseprobe Günter Cerbe, Gernot Wilhelms Technische Thermodynamik Theoretische Grundlagen und praktische Anwendungen ISBN: 978-3-446-4464-7 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-4464-7
Leseprobe. Günter Cerbe, Gernot Wilhelms. Technische Thermodynamik. Theoretische Grundlagen und praktische Anwendungen. ISBN (Buch):
 Leseprobe Günter Cerbe, Gernot Wilhelms Technische Thermodynamik Theoretische Grundlagen und praktische Anwendungen ISBN (Buch): 978-3-446-43638- ISBN (E-Book): 978-3-446-43750-0 Weitere Informationen
Leseprobe Günter Cerbe, Gernot Wilhelms Technische Thermodynamik Theoretische Grundlagen und praktische Anwendungen ISBN (Buch): 978-3-446-43638- ISBN (E-Book): 978-3-446-43750-0 Weitere Informationen
Formel X Leistungskurs Physik 2005/2006
 System: Wir betrachten ein Fluid (Bild, Gas oder Flüssigkeit), das sich in einem Zylinder befindet, der durch einen Kolben verschlossen ist. In der Thermodynamik bezeichnet man den Gegenstand der Betrachtung
System: Wir betrachten ein Fluid (Bild, Gas oder Flüssigkeit), das sich in einem Zylinder befindet, der durch einen Kolben verschlossen ist. In der Thermodynamik bezeichnet man den Gegenstand der Betrachtung
12 Der erste Hauptsatz der Thermodynamik für geschlossene Systeme
 Der erste Hauptsatz der Thermodynamik für geschlossene Systeme Der erste Hauptsatz ist die thermodynamische Formulierung des Satzes von der Erhaltung der Energie. Er besagt, daß Energie weder erzeugt noch
Der erste Hauptsatz der Thermodynamik für geschlossene Systeme Der erste Hauptsatz ist die thermodynamische Formulierung des Satzes von der Erhaltung der Energie. Er besagt, daß Energie weder erzeugt noch
GPH2 Thermodynamik. 27. September Dieser Entwurf ist weder vollständig oder fehlerfrei noch ein offizielles Script zur Vorlesung.
 GPH2 Thermodynamik Dieser Entwurf ist weder ollständig oder fehlerfrei noch ein offizielles Scrit zur Vorlesung. Für Anregungen und Kritik: mail@sibbar.de 27. Setember 2004 GPH2 Thermodynamik Seite 2 on
GPH2 Thermodynamik Dieser Entwurf ist weder ollständig oder fehlerfrei noch ein offizielles Scrit zur Vorlesung. Für Anregungen und Kritik: mail@sibbar.de 27. Setember 2004 GPH2 Thermodynamik Seite 2 on
Was ist überhaupt Thermodynamik? Das Wort Thermodynamik kommt aus dem Griechischen von therme (Wärme) und dynamis (Kraft).
 Struktur Was ist Thermodynamik Geschichte Einstieg Thermodynamik Thermische Zustandsgrößen Thermische Zustandsgleichungen Thermodynamische Systeme Zustand und Prozess Hauptsätze Was ist überhaupt Thermodynamik?
Struktur Was ist Thermodynamik Geschichte Einstieg Thermodynamik Thermische Zustandsgrößen Thermische Zustandsgleichungen Thermodynamische Systeme Zustand und Prozess Hauptsätze Was ist überhaupt Thermodynamik?
Musterlösung Übung 3
 Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
III. Der erste Hauptsatz. - Summe dieser Energien bleibt in abgeschlossenem System konstant - Charakterisierung des äußeren Systemzustands.
 III. Der erste Hauptsatz Technische Thermodynamik Rückblick Mechanik: Anwendung der Energieerhaltung auf zwei Energiearten: - potentielle und kinetische Energie - Summe dieser Energien bleibt in abgeschlossenem
III. Der erste Hauptsatz Technische Thermodynamik Rückblick Mechanik: Anwendung der Energieerhaltung auf zwei Energiearten: - potentielle und kinetische Energie - Summe dieser Energien bleibt in abgeschlossenem
Kleine Formelsammlung Technische Thermodynamik
 Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 2., aktualisierte Auflage Fachbuchverlag
Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 2., aktualisierte Auflage Fachbuchverlag
Inhaltsverzeichnis. Hans-Joachim Kretzschmar, Ingo Kraft. Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6
 Inhaltsverzeichnis Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41781-6
Inhaltsverzeichnis Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN: 978-3-446-41781-6 Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-41781-6
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Die drei Engel der Weihnacht
 Die drei Engel der Weihnacht Freude, Liebe und Licht zum schönsten Fest des Jahres von Sabine Fels 1. Auflage tredition 2013 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 8495 5070 7 schnell und
Die drei Engel der Weihnacht Freude, Liebe und Licht zum schönsten Fest des Jahres von Sabine Fels 1. Auflage tredition 2013 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 8495 5070 7 schnell und
Thermodynamik Prof. Dr.-Ing. Peter Hakenesch
 Thermodynamik _ Thermodynamik Prof. Dr.-Ing. Peter Hakenesch peter.hakenesch@hm.edu www.lrz-muenchen.de/~hakenesch _ Thermodynamik Einleitung Grundbegriffe 3 Systembeschreibung 4 Zustandsgleichungen 5
Thermodynamik _ Thermodynamik Prof. Dr.-Ing. Peter Hakenesch peter.hakenesch@hm.edu www.lrz-muenchen.de/~hakenesch _ Thermodynamik Einleitung Grundbegriffe 3 Systembeschreibung 4 Zustandsgleichungen 5
wegen adiabater Kompression, d.h. kein Wärmeaustausch mit der Umgebung, gilt:
 Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
Ü 7. Adiabate Komression on Luft Luft wird in einem adiabaten Zylinder on. bar, T 5 C solange erdichtet bis eine Endtemeratur on T 00 C erreicht wird. Gesucht sind die zur Verdichtung erforderliche Arbeit
4.6 Hauptsätze der Thermodynamik
 Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Thermodynamik Prof. Dr.-Ing. Peter Hakenesch
 Thermodynamik Thermodynamik Prof. Dr.-Ing. Peter Hakenesch peter.hakenesch@hm.edu www.lrz-muenchen.de/~hakenesch Thermodynamik Einleitung Grundbegriffe 3 Systembeschreibung 4 Zustandsgleichungen 5 Kinetische
Thermodynamik Thermodynamik Prof. Dr.-Ing. Peter Hakenesch peter.hakenesch@hm.edu www.lrz-muenchen.de/~hakenesch Thermodynamik Einleitung Grundbegriffe 3 Systembeschreibung 4 Zustandsgleichungen 5 Kinetische
Polytrope Zustandsänderung
 Sowohl isotherme als auch isentroe Zustandsänderungen werden in Maschinen nie streng erreicht. Reale Komressions- und Exansionsrozesse lassen sich aber oft recht gut durch allgemeine Hyerbeln darstellen,
Sowohl isotherme als auch isentroe Zustandsänderungen werden in Maschinen nie streng erreicht. Reale Komressions- und Exansionsrozesse lassen sich aber oft recht gut durch allgemeine Hyerbeln darstellen,
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 2. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 2 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3 Bilanzgleichungen 3.3.1 Massebilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 2 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3 Bilanzgleichungen 3.3.1 Massebilanz 3.3.2 Energiebilanz und 1. Hauptsatz
( ) ( ) J =920. c Al. m s c. Ü 8.1 Freier Fall
 Ü 8. Freier Fall Ein Stück Aluminium fällt aus einer Höhe von z = 000 m auf den Erdboden (z = 0). Die Luftreibung wird vernachlässigt und es findet auch kein Energieaustausch mit der Umgebung statt. Beim
Ü 8. Freier Fall Ein Stück Aluminium fällt aus einer Höhe von z = 000 m auf den Erdboden (z = 0). Die Luftreibung wird vernachlässigt und es findet auch kein Energieaustausch mit der Umgebung statt. Beim
Kleine Formelsammlung Technische Thermodynamik
 Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker ft Fachbuchverlag Leipzig im Carl
Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker ft Fachbuchverlag Leipzig im Carl
Die zugeführte Wärmemenge bei isochorer Zustandsänderung berechnet sich aus
 Ü 9. Aufheizung einer Preßluftflasche Eine Preßluftflasche, in der sich.84 kg Luft bei einem Druck on.74 bar und einer Temeratur on T 0 C befinden, heizt sich durch Sonneneinstrahlung auf 98 C auf. Gesucht
Ü 9. Aufheizung einer Preßluftflasche Eine Preßluftflasche, in der sich.84 kg Luft bei einem Druck on.74 bar und einer Temeratur on T 0 C befinden, heizt sich durch Sonneneinstrahlung auf 98 C auf. Gesucht
Zur Thermodynamik des idealen Gases (GK Physik 1)
 Zur hermodynamik des idealen Gases (GK Physik 1 Zusammenfassung im Hinblick auf Prozesse. Reinhard Honegger, im Januar 2012. 1 Grundbegriffe 1.1 Zustandsgleichung = Ideale Gasgleichung Druck, olumen, emeratur
Zur hermodynamik des idealen Gases (GK Physik 1 Zusammenfassung im Hinblick auf Prozesse. Reinhard Honegger, im Januar 2012. 1 Grundbegriffe 1.1 Zustandsgleichung = Ideale Gasgleichung Druck, olumen, emeratur
Für den Fall, dass die Kraft während des Vorgangs konstant wirkt, lässt sich das Integral leicht berechnen. Man erhält:
 3 Der erste Hauptsatz der Thermodynamik Der Erste Hauptsatz der Thermodynamik bringt das Prinzip von der Erhaltung der Energie zum Ausdruck. Der Erfahrungssatz der Mechanik, der sich auf kinetische und
3 Der erste Hauptsatz der Thermodynamik Der Erste Hauptsatz der Thermodynamik bringt das Prinzip von der Erhaltung der Energie zum Ausdruck. Der Erfahrungssatz der Mechanik, der sich auf kinetische und
Der 1. Hauptsatz. Energieerhaltung:
 Der 1. Hauptsatz Energieerhaltung: Bei einer Zustandsänderung tauscht das betrachtete System Energie ( W, Q mit seiner Umgebung aus (oft ein Wärmereservoir bei konstantem. Für die Energiebilanz gilt: U
Der 1. Hauptsatz Energieerhaltung: Bei einer Zustandsänderung tauscht das betrachtete System Energie ( W, Q mit seiner Umgebung aus (oft ein Wärmereservoir bei konstantem. Für die Energiebilanz gilt: U
1. Thermodynamische Potentiale, Maxwellgleichungen
 69 KAPIEL G hermodynamische Potentiale 1. hermodynamische Potentiale, Maxwellgleichungen hermodynamische Potentiale sind Funktionen von den Zustandsvariablen. Wir haben schon die innere Energie kennengelernt,
69 KAPIEL G hermodynamische Potentiale 1. hermodynamische Potentiale, Maxwellgleichungen hermodynamische Potentiale sind Funktionen von den Zustandsvariablen. Wir haben schon die innere Energie kennengelernt,
Physikalische Aufgaben
 Physikalische Aufgaben Bearbeitet von Helmut Lindner 1. Auflage 2013. Buch. 339 S. Hardcover ISBN 978 3 446 43753 1 Format (B x L): 12,1 x 19 cm Gewicht: 365 g Weitere Fachgebiete > Physik, Astronomie
Physikalische Aufgaben Bearbeitet von Helmut Lindner 1. Auflage 2013. Buch. 339 S. Hardcover ISBN 978 3 446 43753 1 Format (B x L): 12,1 x 19 cm Gewicht: 365 g Weitere Fachgebiete > Physik, Astronomie
Kleine Formelsammlung Technische Thermodynamik
 Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 3., erweiterte Auflage Fachbuchverlag
Kleine Formelsammlung Technische Thermodynamik von Prof. Dr.-Ing. habil. Hans-Joachim Kretzschmar und Prof. Dr.-Ing. Ingo Kraft unter Mitarbeit von Dr.-Ing. Ines Stöcker 3., erweiterte Auflage Fachbuchverlag
T 300K,p 1,00 10 Pa, V 0, m,t 1200K, Kontrolle Physik Leistungskurs Klasse Hauptsatz, Kreisprozesse
 Kontrolle Physik Leistungskurs Klasse 2 7.3.207. Hauptsatz, Kreisprozesse. Als man früh aus dem Haus gegangen ist, hat man doch versehentlich die Kühlschranktür offen gelassen. Man merkt es erst, als man
Kontrolle Physik Leistungskurs Klasse 2 7.3.207. Hauptsatz, Kreisprozesse. Als man früh aus dem Haus gegangen ist, hat man doch versehentlich die Kühlschranktür offen gelassen. Man merkt es erst, als man
T p = T = RT. V b. ( ) 2 V p. V b. 2a(V b)2 V 3 RT. 2a(V b) V 3 (p+ a V 2 )
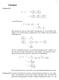 3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
Aufgabe 1 (60 Punkte, TTS & TTD1) Bitte alles LESBAR verfassen!!!
 Aufgabe (60 Punkte, TTS & TTD) Bitte alles LESBAR verfassen!!!. In welcher Weise ändern sich intensive und extensive Zustandsgrößen bei der Zerlegung eines Systems in Teilsysteme?. Welche Werte hat der
Aufgabe (60 Punkte, TTS & TTD) Bitte alles LESBAR verfassen!!!. In welcher Weise ändern sich intensive und extensive Zustandsgrößen bei der Zerlegung eines Systems in Teilsysteme?. Welche Werte hat der
(b) Schritt I: freie adiabatische Expansion, also ist δw = 0, δq = 0 und damit T 2 = T 1. Folglich ist nach 1. Hauptsatz auch U = 0.
 3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
Aufgabe 1 (10 Punkte, TTS & TTD1) Bitte alles LESBAR verfassen!!!
 Aufgabe 1 (10 Punkte, TTS & TTD1) Bitte alles LESBAR verfassen!!! 1.1. Wie erklärt man die dissipierte Energie in einem System? 1.. Kann man aus dieser noch etwas während der folgenden Prozesse in einer
Aufgabe 1 (10 Punkte, TTS & TTD1) Bitte alles LESBAR verfassen!!! 1.1. Wie erklärt man die dissipierte Energie in einem System? 1.. Kann man aus dieser noch etwas während der folgenden Prozesse in einer
Grundlagen: Thermodynamik Teil 2. Institut für Verbrennungskraftmaschinen und Thermodynamik. Michael Lang
 Grundlagen: Thermodynamik Teil 2 Michael Institut für Verbrennungskraftmaschinen und Thermodynamik Vorstand: Univ.-Prof. DI Dr. Helmut Eichlseder 1 System, Zustand, Prozess Grundlagen Thermodynamik: System,
Grundlagen: Thermodynamik Teil 2 Michael Institut für Verbrennungskraftmaschinen und Thermodynamik Vorstand: Univ.-Prof. DI Dr. Helmut Eichlseder 1 System, Zustand, Prozess Grundlagen Thermodynamik: System,
5.5 Zustandsänderungen idealer Gase
 5.5 Zustandsänderungen idealer Gase iele Gase verhalten sich bei technischen Anwendungen in guter Näherung wie ideale Gase (siehe Ka. 5..3). Bei einem technischen Prozess ändert sich nun der Zustand des
5.5 Zustandsänderungen idealer Gase iele Gase verhalten sich bei technischen Anwendungen in guter Näherung wie ideale Gase (siehe Ka. 5..3). Bei einem technischen Prozess ändert sich nun der Zustand des
1. Klausur in "Technischer Thermodynamik II" (SoSe2014, ) - VERSION 1 -
 UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Al. Professor Dr.-Ing. K. Sindler. Klausur in "Technischer Thermodynamik II" (SoSe04, 03.06.04) - VERSION - Name: Fachr.: Matr.-Nr.: Es
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Al. Professor Dr.-Ing. K. Sindler. Klausur in "Technischer Thermodynamik II" (SoSe04, 03.06.04) - VERSION - Name: Fachr.: Matr.-Nr.: Es
DIN EN ISO 9000:2000 ff. umsetzen
 DIN EN ISO 9000:2000 ff. umsetzen Gestaltungshilfen zum Aufbau Ihres Qualitätsmanagementsystems von Jörg-Peter Brauer 1. Auflage DIN EN ISO 9000:2000 ff. umsetzen Brauer schnell und portofrei erhältlich
DIN EN ISO 9000:2000 ff. umsetzen Gestaltungshilfen zum Aufbau Ihres Qualitätsmanagementsystems von Jörg-Peter Brauer 1. Auflage DIN EN ISO 9000:2000 ff. umsetzen Brauer schnell und portofrei erhältlich
Kleine Formelsammlung Technische Thermodynamik
 Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN-10: 3-446-22882-9 ISBN-13: 978-3-446-22882-5 Inhaltsverzeichnis Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-22882-5
Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN-10: 3-446-22882-9 ISBN-13: 978-3-446-22882-5 Inhaltsverzeichnis Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-22882-5
Einführung in die Verbrennungskraftmaschine
 Institut für erbrennungskraftmaschinen Einführung in die erbrennungskraftmaschine,.05.0 Institut für erbrennungskraftmaschinen Ed-Übung Übersicht Grundlagen der hermodynamik Prozess und thermischer Wirkungsgrad
Institut für erbrennungskraftmaschinen Einführung in die erbrennungskraftmaschine,.05.0 Institut für erbrennungskraftmaschinen Ed-Übung Übersicht Grundlagen der hermodynamik Prozess und thermischer Wirkungsgrad
Thermodynamik des Kraftfahrzeugs
 Thermodynamik des Kraftfahrzeugs Bearbeitet von Cornel Stan 1. Auflage 2012. Buch. xxiv, 598 S. Hardcover ISBN 978 3 642 27629 3 Format (B x L): 15,5 x 23,5 cm Gewicht: 1087 g Weitere Fachgebiete > Technik
Thermodynamik des Kraftfahrzeugs Bearbeitet von Cornel Stan 1. Auflage 2012. Buch. xxiv, 598 S. Hardcover ISBN 978 3 642 27629 3 Format (B x L): 15,5 x 23,5 cm Gewicht: 1087 g Weitere Fachgebiete > Technik
Baustatik 2. Berechnung statisch unbestimmter Tragwerke. von Raimond Dallmann. 2., aktualisierte Auflage. Hanser München 2009
 Baustatik 2 Berechnung statisch unbestimmter Tragwerke von Raimond Dallmann 2., aktualisierte Auflage Hanser München 2009 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 41998 8 Zu Leseprobe schnell
Baustatik 2 Berechnung statisch unbestimmter Tragwerke von Raimond Dallmann 2., aktualisierte Auflage Hanser München 2009 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 41998 8 Zu Leseprobe schnell
Zur Erinnerung. Wärmetransport durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung. Planck sches Strahlungsgesetz. Stefan-Boltzman-Gesetz
 Zur Erinnerung Stichworte aus der 9. orlesung: Wärmetransort durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung Planck sches Strahlungsgesetz Stefan-Boltzman-Gesetz Wiensches erschiebungsgesetz Hautsätze
Zur Erinnerung Stichworte aus der 9. orlesung: Wärmetransort durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung Planck sches Strahlungsgesetz Stefan-Boltzman-Gesetz Wiensches erschiebungsgesetz Hautsätze
Aufgaben Kreisprozesse. 1. Ein ideales Gas durchläuft den im V(T)- Diagramm dargestellten Kreisprozess. Es ist bekannt:
 Aufgaben Kreisrozesse. Ein ideales Gas durchläuft den im ()- Diagramm dargestellten Kreisrozess. Es ist bekannt: 8 cm 6 cm 00 K 8MPa MPa a) Geben Sie die fehlenden Zustandsgrößen, und für die Zustände
Aufgaben Kreisrozesse. Ein ideales Gas durchläuft den im ()- Diagramm dargestellten Kreisrozess. Es ist bekannt: 8 cm 6 cm 00 K 8MPa MPa a) Geben Sie die fehlenden Zustandsgrößen, und für die Zustände
5. Anwendungen des ersten und zweiten Hauptsatzes
 5. Anwendungen des ersten und zweiten Hautsatzes 5. Volumenänderungsarbeit und Druckänderungsarbeit bei Zustandsänderungen in geschlossenen und offenen Systemen In den vorangegangenen Kaiteln haben wir
5. Anwendungen des ersten und zweiten Hautsatzes 5. Volumenänderungsarbeit und Druckänderungsarbeit bei Zustandsänderungen in geschlossenen und offenen Systemen In den vorangegangenen Kaiteln haben wir
Technische Thermodynamik. FB Maschinenwesen. Formelsammlung. Technische Thermodynamik. Wärmeübertragung. University of Applied Sciences
 Uniersity of lied Sciences Formelsammlung echnische hermodynamik Wärmeübertragung Prof Dr-Ing habil H-J Kretzschmar FB Maschinenwesen echnische hermodynamik HOCHSCHULE ZIU/GÖRLIZ (FH) - Uniersity of lied
Uniersity of lied Sciences Formelsammlung echnische hermodynamik Wärmeübertragung Prof Dr-Ing habil H-J Kretzschmar FB Maschinenwesen echnische hermodynamik HOCHSCHULE ZIU/GÖRLIZ (FH) - Uniersity of lied
Leseprobe. Hans-Joachim Kretzschmar, Ingo Kraft. Kleine Formelsammlung Technische Thermodynamik. ISBN (Buch):
 Leseprobe Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN (Buch): 978-3-446-44668-7 ISBN (E-Book): 978-3-446-44857-5 Weitere Informationen oder Bestellungen unter
Leseprobe Hans-Joachim Kretzschmar, Ingo Kraft Kleine Formelsammlung Technische Thermodynamik ISBN (Buch): 978-3-446-44668-7 ISBN (E-Book): 978-3-446-44857-5 Weitere Informationen oder Bestellungen unter
1 Grundlagen der Strömungsvorgänge
 Grundlagen der svorgänge.0 Einleitung Hydro - (Aero) Mehanik Hydro - (Aero) Statik Hydro - (Aero) Dynamik -dimension. -dimension. 3-dimension. stationäre instationäre Die slehre auh als Fluiddynamik bezeihnet
Grundlagen der svorgänge.0 Einleitung Hydro - (Aero) Mehanik Hydro - (Aero) Statik Hydro - (Aero) Dynamik -dimension. -dimension. 3-dimension. stationäre instationäre Die slehre auh als Fluiddynamik bezeihnet
Formelsammlung. Experimentalphysik II. Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester Pascal Del Haye 27.
 Formelsammlung Experimentalphysik II Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester 2003 Pascal Del Haye www.delhaye.de 27. Juli 2003 Inhaltsverzeichnis Thermodynamik 3. Ideale Gasgleichung........................
Formelsammlung Experimentalphysik II Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester 2003 Pascal Del Haye www.delhaye.de 27. Juli 2003 Inhaltsverzeichnis Thermodynamik 3. Ideale Gasgleichung........................
Wahrscheinlichkeitsrechnung und Statistik
 Wahrscheinlichkeitsrechnung und Statistik Für Ingenieurstudenten an Fachhochschulen von Michael Sachs erweitert Wahrscheinlichkeitsrechnung und Statistik Sachs schnell und portofrei erhältlich bei beck-shopde
Wahrscheinlichkeitsrechnung und Statistik Für Ingenieurstudenten an Fachhochschulen von Michael Sachs erweitert Wahrscheinlichkeitsrechnung und Statistik Sachs schnell und portofrei erhältlich bei beck-shopde
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Thermodynamik. oder Website der Fachhochschule Osnabrück
 Thermodynamik Prof. Dr.-Ing. Matthias Reckzügel Vorlesung, Übung und Praktikum im 3. Semester für die Studiengänge: Maschinenbau Fahrzeugtechnik Maschinenbauinformatik Integrierte Produktentwicklung EMS
Thermodynamik Prof. Dr.-Ing. Matthias Reckzügel Vorlesung, Übung und Praktikum im 3. Semester für die Studiengänge: Maschinenbau Fahrzeugtechnik Maschinenbauinformatik Integrierte Produktentwicklung EMS
c ) Wie verhält sich die Enthalpieänderung, wenn das Wasser in einer Düse beschleunigt wird?
 Aufgabe 4 An einer Drosselstelle wird ein kontinuierlich fließender Strom von Wasser von p 8 bar auf p 2 2 bar entspannt. Die Geschwindigkeiten vor und nach der Drosselung sollen gleich sein. Beim des
Aufgabe 4 An einer Drosselstelle wird ein kontinuierlich fließender Strom von Wasser von p 8 bar auf p 2 2 bar entspannt. Die Geschwindigkeiten vor und nach der Drosselung sollen gleich sein. Beim des
Prüfungs- und Testaufgaben zur PHYSIK
 Prüfungs- und Testaufgaben zur PHYSIK Mechanik - Schwingungslehre - WärmelehreInteraktive Lernmaterialien zum Selbststudium für technische Studienrichtungen an Hochschulenfür technische Studienrichtungen
Prüfungs- und Testaufgaben zur PHYSIK Mechanik - Schwingungslehre - WärmelehreInteraktive Lernmaterialien zum Selbststudium für technische Studienrichtungen an Hochschulenfür technische Studienrichtungen
T 1 T T Zustandsverhalten einfacher Systeme (Starthilfe S ) - Prozess und Zustandsänderung. Prozess (Q 12
 . Zustandserhalten einfacher Systeme (Starthilfe S. 9-38) - Prozess und Zustandsänderung Zustandsänderung δq Prozess (Q ) - thermodynamisch einfache Systeme reiner Stoff feste flüssige damfförmige Phase
. Zustandserhalten einfacher Systeme (Starthilfe S. 9-38) - Prozess und Zustandsänderung Zustandsänderung δq Prozess (Q ) - thermodynamisch einfache Systeme reiner Stoff feste flüssige damfförmige Phase
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 2. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3Bilanzgleichungen 3.3.1Massenbilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3Bilanzgleichungen 3.3.1Massenbilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Praxis der Wärmeübertragung
 Praxis der Wärmeübertragung Grundlagen - Anwendungen - Übungsaufgaben von Rudi Marek, Klaus Nitsche 1. Auflage Hanser München 2010 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 42510 1 Zu Leseprobe
Praxis der Wärmeübertragung Grundlagen - Anwendungen - Übungsaufgaben von Rudi Marek, Klaus Nitsche 1. Auflage Hanser München 2010 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 42510 1 Zu Leseprobe
II. Wärmelehre. II.2. Die Hauptsätze der Wärmelehre. Physik für Mediziner 1
 II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
Lösungen zur Übungsklausur Thermodynamik WS 2003/04
 Lösungen zur Übungsklausur hermodynamik WS 003/04 Name: Vorname: Matrikelnummer: Aufgabe 3 4 5 Gesamt Note mögliche Punkte 9 0 8 9 4 40 erreichte Punkte Die Klausur wird bei Erreichen von insgesamt 0 Punkten
Lösungen zur Übungsklausur hermodynamik WS 003/04 Name: Vorname: Matrikelnummer: Aufgabe 3 4 5 Gesamt Note mögliche Punkte 9 0 8 9 4 40 erreichte Punkte Die Klausur wird bei Erreichen von insgesamt 0 Punkten
I el U el. P el W V 23+W F23. Musterlösung SS Aufgabe (34 Punkte) a) Energiebilanz für die Kammer A im Zeitintervall t 12 :
 Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Musterlösung SS. Aufgabe Punkte a Energiebilanz für die Kammer A im Zeitintervall t : W A, + W V A U A U A W A, P el t U el I el t W V A 0 U A U A m A c v A A 5 m A A V A R A 6 c v κ R 7 A A A A 8 A B
Qualitätstechniken. Werkzeuge zur Problemlösung und ständigen Verbesserung. von Dr. Philipp Theden, Hubertus Colsman. 1. Auflage
 Qualitätstechniken Werkzeuge zur Problemlösung und ständigen Verbesserung von Dr. Philipp Theden, Hubertus Colsman 1. Auflage Qualitätstechniken Theden / Colsman schnell und portofrei erhältlich bei beck-shop.de
Qualitätstechniken Werkzeuge zur Problemlösung und ständigen Verbesserung von Dr. Philipp Theden, Hubertus Colsman 1. Auflage Qualitätstechniken Theden / Colsman schnell und portofrei erhältlich bei beck-shop.de
Aufgabe 1: Theorie Punkte
 Aufgabe 1: Theorie.......................................... 30 Punkte (a) (2 Punkte) In einen Mischer treten drei Ströme ein. Diese haben die Massenströme ṁ 1 = 1 kg/s, ṁ 2 = 2 kg/s und ṁ 3 = 2 kg/s.
Aufgabe 1: Theorie.......................................... 30 Punkte (a) (2 Punkte) In einen Mischer treten drei Ströme ein. Diese haben die Massenströme ṁ 1 = 1 kg/s, ṁ 2 = 2 kg/s und ṁ 3 = 2 kg/s.
Grundlagen. 2.1 Das thermodynamische System
 Grundlagen 2 In diesem Kapitel werden einige benötigte Grundbegriffe und Definitionen der Thermodynamik zusammengefasst. Besonders wichtig ist in der Thermodynamik der Begriff des Systems. Dies ist der
Grundlagen 2 In diesem Kapitel werden einige benötigte Grundbegriffe und Definitionen der Thermodynamik zusammengefasst. Besonders wichtig ist in der Thermodynamik der Begriff des Systems. Dies ist der
Mathematische Formeln für das Studium an Fachhochschulen
 Mathematische Formeln für das Studium an Fachhochschulen von Richard Mohr. Auflage Hanser München 0 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 446 455 4 Zu Inhaltsverzeichnis schnell und portofrei
Mathematische Formeln für das Studium an Fachhochschulen von Richard Mohr. Auflage Hanser München 0 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 446 455 4 Zu Inhaltsverzeichnis schnell und portofrei
Wolfgang Heidemann. Technische Thermodynamik. Kompaktkurs für das Bachelorstudium. Wl LEY-VCH. Verlag GmbH & Co. KGaA
 Wolfgang Heidemann Technische Thermodynamik Kompaktkurs für das Bachelorstudium Wl LEY-VCH Verlag GmbH & Co. KGaA Inhaltsverzeichnis Vorwort XI Nomenklatur XIII 1 Einleitung 1 1.1 Technische Thermodynamik
Wolfgang Heidemann Technische Thermodynamik Kompaktkurs für das Bachelorstudium Wl LEY-VCH Verlag GmbH & Co. KGaA Inhaltsverzeichnis Vorwort XI Nomenklatur XIII 1 Einleitung 1 1.1 Technische Thermodynamik
Mathematische Modelle im Bauingenieurwesen
 Mathematische Modelle im Bauingenieurwesen Mit Fallstudien und numerischen Lösungen von Kerstin Rjasanowa 1. Auflage Hanser München 010 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 415 7 Zu
Mathematische Modelle im Bauingenieurwesen Mit Fallstudien und numerischen Lösungen von Kerstin Rjasanowa 1. Auflage Hanser München 010 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 415 7 Zu
Mathematik für Bauingenieure
 Mathematik für Bauingenieure von Kerstin Rjasanowa 1. Auflage Mathematik für Bauingenieure Rjasanowa schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG Hanser München 2006 Verlag C.H.
Mathematik für Bauingenieure von Kerstin Rjasanowa 1. Auflage Mathematik für Bauingenieure Rjasanowa schnell und portofrei erhältlich bei beck-shop.de DIE FACHBUCHHANDLUNG Hanser München 2006 Verlag C.H.
Aufgaben zum Stirlingschen Kreisprozess Ein Stirling-Motor arbeite mit 50 g Luft ( M= 30g mol 1 )zwischen den Temperaturen = 350 C und T3
 Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
Aufgaben zum Stirlingschen Kreisrozess. Ein Stirling-Motor arbeite mit 50 g Luft ( M 0g mol )zwischen den emeraturen 50 C und 50 C sowie den olumina 000cm und 5000 cm. a) Skizzieren Sie das --Diagramm
1. Klausur in "Technischer Thermodynamik I" (WiSe2013/14, ) - VERSION 1 -
 UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spndler 1. Klausur n "Technscher Thermodynamk I" (WSe2013/14, 12.12.2013) - VERSION 1 - Name: Fachr.: Matr.-Nr.:
UNIVERSITÄT STUTTGART INSTITUT FÜR THERMODYNAMIK UND WÄRMETECHNIK Apl. Professor Dr.-Ing. K. Spndler 1. Klausur n "Technscher Thermodynamk I" (WSe2013/14, 12.12.2013) - VERSION 1 - Name: Fachr.: Matr.-Nr.:
1 I. Thermodynamik. 1.1 Ideales Gasgesetz. 1.2 Vereinfachte kinetische Gastheorie. 1.3 Erster Hauptsatz der Thermodynamik.
 1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
1 I. hermodynamik 1.1 Ideales Gasgesetz eilchenzahl N Stoffmenge: n [mol], N A = 6.022 10 23 mol 1 ; N = nn A molare Größen: X m = X/n ideales Gasgesetz: V = nr, R = 8.314JK 1 mol 1 Zustandsgrößen:, V,,
Übungsaufgaben zur Thermodynamik
 Übungsaufgaben zur Thermodynamik Übungsbeispiel 1 Ein ideales Gas hat bei einem Druck von 2,5 bar und ϑl = 27 C eine Dichte von ρ1 = 2,7 kg/m 3. Durch isobare Wärmezufuhr soll sich das Gasvolumen Vl verdoppeln
Übungsaufgaben zur Thermodynamik Übungsbeispiel 1 Ein ideales Gas hat bei einem Druck von 2,5 bar und ϑl = 27 C eine Dichte von ρ1 = 2,7 kg/m 3. Durch isobare Wärmezufuhr soll sich das Gasvolumen Vl verdoppeln
Enthalpienullpunkt von Luft und Wasser am Tripelpunkt des siedenden Wassers T=T tr = 273,16 K:
 3.3.5 Energiebilanz bei der Mischung feuchter Luft Bezugsgröße: Masse der trockenen Luft m L Beladung: Auf die Masse der Luft bezogene Enthalpie Enthalpienullpunkt von Luft und Wasser am Tripelpunkt des
3.3.5 Energiebilanz bei der Mischung feuchter Luft Bezugsgröße: Masse der trockenen Luft m L Beladung: Auf die Masse der Luft bezogene Enthalpie Enthalpienullpunkt von Luft und Wasser am Tripelpunkt des
Hauptsätze der Thermodynamik
 Platzhalter für Bild, Bild auf Titelfolie hinter das Logo einsetzen Hauptsätze der Thermodynamik Dominik Pfennig, 31.10.2012 Inhalt 0. Hauptsatz Innere Energie 1. Hauptsatz Enthalpie Satz von Hess 2. Hauptsatz
Platzhalter für Bild, Bild auf Titelfolie hinter das Logo einsetzen Hauptsätze der Thermodynamik Dominik Pfennig, 31.10.2012 Inhalt 0. Hauptsatz Innere Energie 1. Hauptsatz Enthalpie Satz von Hess 2. Hauptsatz
Thermodynamik II Klausur SS 2006
 Thermodynamik II Klausur SS 0 Prof. Dr. G. Wilhelms Aufgabenteil / 00 Minuten / Blatt Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern
Thermodynamik II Klausur SS 0 Prof. Dr. G. Wilhelms Aufgabenteil / 00 Minuten / Blatt Das Aufgabenblatt muss unterschrieben und zusammen mit den (nummerierten und mit Namen versehenen) Lösungsblättern
Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch. Musterlösung Thermodynamik I SS Aachen, den 6. Oktober 2014.
 Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch Musterlösung Thermodynamik I SS 014 Aachen, den 6. Oktober 014 Bachelorprüfung Thermodynamik I SS 014 1/10 1 Aufgabe (5 Punkte) a) Die
Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch Musterlösung Thermodynamik I SS 014 Aachen, den 6. Oktober 014 Bachelorprüfung Thermodynamik I SS 014 1/10 1 Aufgabe (5 Punkte) a) Die
Der erste Hauptsatz der TD- Lernziele
 Der erste Hautsatz der D- Lernziele o Einleitung o Zustandgrössen und funktionen o Wärme, Arbeit und Energie o Innere Energie o Der erste Hautsatz der hermodynamik o olumenarbeit o Wärmeübergänge o Die
Der erste Hautsatz der D- Lernziele o Einleitung o Zustandgrössen und funktionen o Wärme, Arbeit und Energie o Innere Energie o Der erste Hautsatz der hermodynamik o olumenarbeit o Wärmeübergänge o Die
Höhere Experimentalphysik 1
 Höhere Experimentalphysik 1 Institut für Angewandte Physik Goethe-Universität Frankfurt am Main 8. Vorlesung 13.01.2017 Prüfung Postersession Thema soll innerhalb von Zweiergruppen bearbeitet werden Themenvergabe:
Höhere Experimentalphysik 1 Institut für Angewandte Physik Goethe-Universität Frankfurt am Main 8. Vorlesung 13.01.2017 Prüfung Postersession Thema soll innerhalb von Zweiergruppen bearbeitet werden Themenvergabe:
Zweiter Hauptsatz der Thermodynamik
 Thermodynamik I Kapitel 4 Zweiter Hauptsatz der Thermodynamik Prof. Dr.-Ing. Heinz Pitsch Kapitel 4: Ü bersicht 4 Zweiter Hauptsatz der Thermodynamik 4.1 Klassische Formulierungen 4.1.1 Kelvin-Planck-Formulierung
Thermodynamik I Kapitel 4 Zweiter Hauptsatz der Thermodynamik Prof. Dr.-Ing. Heinz Pitsch Kapitel 4: Ü bersicht 4 Zweiter Hauptsatz der Thermodynamik 4.1 Klassische Formulierungen 4.1.1 Kelvin-Planck-Formulierung
Thermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden.
 Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Kapitel 5: Methode der Bilanzierung und der erste Hauptsatz der Thermodynamik
 Kapitel 5: Methode der Bilanzierung und der erste Hauptsatz der Thermodynamik Der erste Haupsatz der Thermodynamik ist der Satz von der Erhaltung der Energie. In diesem Kapitel werden wir den ersten Hauptsatz
Kapitel 5: Methode der Bilanzierung und der erste Hauptsatz der Thermodynamik Der erste Haupsatz der Thermodynamik ist der Satz von der Erhaltung der Energie. In diesem Kapitel werden wir den ersten Hauptsatz
Klausur im Fach Thermodynamik I, SS 07 am
 e c o r e n e n o m g i y e c s n g i e n n v i e e r i n g..t. e n r o n m Technische Universität Berlin INSTITUT FÜR ENERGIETECHNIK Prof. Dr.-Ing. G. Tsatsaronis. Klausur im Fach Thermodynamik I, SS
e c o r e n e n o m g i y e c s n g i e n n v i e e r i n g..t. e n r o n m Technische Universität Berlin INSTITUT FÜR ENERGIETECHNIK Prof. Dr.-Ing. G. Tsatsaronis. Klausur im Fach Thermodynamik I, SS
2 Der erste Hauptsatz der Thermodynamik
 2 Der erste Hauptsatz der Thermodynamik 2. Das Prinzip von der Erhaltung der Energie In der Mechanik wird das Prinzip der Erhaltung der Energie auf zwei Energiearten angewandt, die bei der reibungsfreien
2 Der erste Hauptsatz der Thermodynamik 2. Das Prinzip von der Erhaltung der Energie In der Mechanik wird das Prinzip der Erhaltung der Energie auf zwei Energiearten angewandt, die bei der reibungsfreien
Physik 2 ET, SoSe 2013 Aufgaben mit Lösung 2. Übung (KW 17/18)
 2. Übung (KW 17/18) Aufgabe 1 (T 3.1 Sauerstoffflasche ) Eine Sauerstoffflasche, die das Volumen hat, enthält ab Werk eine Füllung O 2, die bei Atmosphärendruck p 1 das Volumen V 1 einnähme. Die bis auf
2. Übung (KW 17/18) Aufgabe 1 (T 3.1 Sauerstoffflasche ) Eine Sauerstoffflasche, die das Volumen hat, enthält ab Werk eine Füllung O 2, die bei Atmosphärendruck p 1 das Volumen V 1 einnähme. Die bis auf
Dampftafel Für den Homogenen Zustand. HEAT Haus-, Energie- und Anlagentechnik. Vorlesung Thermodynamik
 Dampftafel 1 Zur Berechnung thermodynamischer Prozesse (Kraftwerk, Wärmepumpe, etc.) reicht das ideale Gasgesetz nicht mehr aus Stoffdaten der realen Fluide werden benötigt Für die Bestimmung der Stoffdaten
Dampftafel 1 Zur Berechnung thermodynamischer Prozesse (Kraftwerk, Wärmepumpe, etc.) reicht das ideale Gasgesetz nicht mehr aus Stoffdaten der realen Fluide werden benötigt Für die Bestimmung der Stoffdaten
Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch. Aufgabenstellung Thermodynamik I SS Aachen, den 22.
 Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch Aufgabenstellung Thermodynamik I SS 2014 Aachen, den 22. September 2014 Bachelorprüfung Thermodynamik I SS 2014 1/4 1 Aufgabe (25 Punkte)
Institut für Technische Verbrennung Univ.-Prof. Dr.-Ing. H. Pitsch Aufgabenstellung Thermodynamik I SS 2014 Aachen, den 22. September 2014 Bachelorprüfung Thermodynamik I SS 2014 1/4 1 Aufgabe (25 Punkte)
Hauptsatz der Thermodynamik
 0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
Der Erste Hauptsatz der TD- Lernziele
 hermodynamik (D) Fundamentale heorie der makroskoischen Eigenschaften der Materie: - Sontane Prozesse - Konzet der emeratur - Phasenübergänge - Energetik makroskoischer Phasen und chemischer Reaktionen
hermodynamik (D) Fundamentale heorie der makroskoischen Eigenschaften der Materie: - Sontane Prozesse - Konzet der emeratur - Phasenübergänge - Energetik makroskoischer Phasen und chemischer Reaktionen
Datenbank-Programmierung mit Visual Basic 2012 (Buch + E-Book)
 Datenbank-Programmierung mit Visual Basic 2012 (Buch + E-Book) Grundlagen, Rezepte, Anwendungsbeispiele von Walter Doberenz, Thomas Gewinnus 1. Auflage Datenbank-Programmierung mit Visual Basic 2012 (Buch
Datenbank-Programmierung mit Visual Basic 2012 (Buch + E-Book) Grundlagen, Rezepte, Anwendungsbeispiele von Walter Doberenz, Thomas Gewinnus 1. Auflage Datenbank-Programmierung mit Visual Basic 2012 (Buch
Keine Panik vor Thermodynamik!
 Keine Panik vor Thermodynamik! Erfolg und Spaß im klassischen "Dickbrettbohrerfach" des Ingenieurstudiums Bearbeitet von Dirk Labuhn, Oliver Romberg 1. Auflage 2013. Taschenbuch. xii, 351 S. Paperback
Keine Panik vor Thermodynamik! Erfolg und Spaß im klassischen "Dickbrettbohrerfach" des Ingenieurstudiums Bearbeitet von Dirk Labuhn, Oliver Romberg 1. Auflage 2013. Taschenbuch. xii, 351 S. Paperback
Ergänzung im Web www.thermodynamik-formelsammlung.de
 Ergänzung im Web www.thermodynamik-formelsammlung.de Kapitel 13 Ideale Gasgemische Anhang B Zustandsdiagramme B5 B6 lg p,h-diagramm für Propan h 1+x,x w -Diagramm für feuchte Luft (farbig) AnhangC Stoffwert-Bibliotheken
Ergänzung im Web www.thermodynamik-formelsammlung.de Kapitel 13 Ideale Gasgemische Anhang B Zustandsdiagramme B5 B6 lg p,h-diagramm für Propan h 1+x,x w -Diagramm für feuchte Luft (farbig) AnhangC Stoffwert-Bibliotheken
4.1 Die Erscheinungsformen der Energie
 48 4 Die Energiebilanz 4. Die Erscheinungsformen der Energie Die Energie tritt in unterschiedlichen Erscheinungsformen auf. Wir beschränken uns hier auf die mechanischen, die thermischen und die chemischen
48 4 Die Energiebilanz 4. Die Erscheinungsformen der Energie Die Energie tritt in unterschiedlichen Erscheinungsformen auf. Wir beschränken uns hier auf die mechanischen, die thermischen und die chemischen
Stickstoff kann als ideales Gas betrachtet werden mit einer spezifischen Gaskonstante von R N2 = 0,297 kj
 Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Technische Mechanik für Wirtschaftsingenieure
 Technische Mechanik für Wirtschaftsingenieure von Ulrich Gabbert, Ingo Raecke 2. Auflage Hanser München 2004 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 22807 8 Zu Leseprobe schnell und portofrei
Technische Mechanik für Wirtschaftsingenieure von Ulrich Gabbert, Ingo Raecke 2. Auflage Hanser München 2004 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 446 22807 8 Zu Leseprobe schnell und portofrei
