Definition. Epidemiologie, Ätiologie und Klassifikation. Epidemiologie. H. U. Schmelz, P. Albers
|
|
|
- Adolph Knopp
- vor 7 Jahren
- Abrufe
Transkript
1 258 Kapitel Onkologie und Tumoren Thompson IM, Goodman PJ et al. (200) The influence of finasteride on the development of prostate cancer. N Engl J Med 49: Van der Poel HG (2004) Smart drugs in prostate cancer. Eur Urol 45:1 17 Wawroschek F, Vogt H et al. (2001) Radioisotope guided pelvic lymph node dissection for prostate cancer. J Urol 166: Wirth M (2001) Therapie des lokal begrenzten Prostatakarzinoms. In: Rübben H (Hrsg) Uroonkologie,. Aufl. Springer, Berlin Heidelberg New York Tokyo Wirth MP, Nippgen J (200) Chemotherapie beim fortgeschrittenen Prostatakarzinom. Urologe (A) 42: Wirth MP, Tyrell C et al. (2001) Bicalutamide (casodex) 150 mg as immediate therapy in patients with localized or locally advanced prostate cancer significantly reduces the risk of disease progression. Urology 58: Zelefsky M, Leibel S et al. (1998) Dose escalation with three-dimensional conformal radiation therapy affects the outcome in prostate cancer. Int J Radiat Oncol Biol Phys 41: Zietman AL, Chung CS et al. (2004) 10-year outcome for men with localized prostate cancer treated with external radiation therapy: results of a cohort study. J Urol 171: Hodentumoren H. U. Schmelz, P. Albers Definition Unter dem Begriff Hodentumoren werden zusammengefasst: Keimzelltumoren (KZT): 90% Seminome 40% aller KZT, nicht-seminomatöse KZT (»non-seminomatous germ cell tumors«/nsgct): 60% aller KZT, nichtgerminative Tumoren: 10% Leydig-Zell-Tumoren: % aller Hodentumoren (maligne und benigne), Sertoli-Zell-Tumoren: sehr selten, Granulosazelltumoren: sehr selten Maligne Keimzelltumoren des Hodens (KZT) Epidemiologie, Ätiologie und Klassifikation Epidemiologie KZT: häufigste maligne Erkrankung junger Männer, Inzidenz Deutschland: 9,78/ /Jahr (2001),.98 Erkrankungen, weltweit: 0,5 9,9/ /Jahr, geographische Unterschiede: höchste Inzidenz in Skandinavien, Deutschland und Neuseeland, mittlere Inzidenz in den USA, bei Schwarzafrikanern und Asiaten sehr selten, Inzidenz steigend; nur 1 2 % aller KZT treten bilateral auf, Altersgipfel: NSGCT: 25 5 Jahre, Seminome: zweigipflig: 25 5 Jahre und Jahre, 10% aller Patienten sind jünger als 20 Jahre, 70% sind Jahre alt und 20% sind älter als 40 Jahre.
2 .10 Hodentumoren 259 Ätiologie Bisher keine gesicherte Ursache der Hodentumoren bekannt; mehrere Risikofaktoren konnten identifiziert werden: vorangegangener Hodentumor: gegenüber Normalbevölkerung 0fach erhöhtes Risiko für kontralateralen Hodentumor, Maldescenus testis: 4- bis 8fach erhöhtes relatives Risiko gegenüber der Normalbevölkerung, an einem ispilateralen Hodentumor zu erkranken; 5 10% aller Patienten mit Kryptorchismus erleiden einen Hodentumor im kontralateralen Hoden, operative Korrektur eines Leistenhodens reduziert das Entartungsrisiko nicht, positive Familienanamnese: für Brüder eines Hodentumorpatienten besteht ein 11faches, für Söhne eines Hodentumorpatienten ein 2faches Erkrankungsrisiko, Infertilität (Inzidenz für Hodentumor: 1:200), Hodenatrophie, intersexuelle Fehlbildungen: Risiko für TIN bei testikulärer Feminisierung: 25%, Klinefelter-Syndrom: 25 40%, Trauma und Mumpsorchitis spielen keine Rolle bei der Entstehung eines Hodentumors. Pathogenese TIN (= Testikuläre intraepitheliale Neoplasie, Carcinoma in situ) ist Vorläufer aller malignen Hodentumoren mit Ausnahme des spermatozytären Seminoms, TIN-Zellen werden während des fetalen Lebens angelegt, bei Patienten mit einer TIN liegt die kumulative Wahrscheinlichkeit, einen Hodentumor innerhalb von 7 Jahren zu entwickeln bei 70%. Metastasierung Lymphogene Metastasierung: zunächst in ipsilaterale retroperitoneale Lymphknoten in Höhe des Nierenstiels, im weiteren Verlauf beidseits retroperitoneal und supradiaphragmal, hämatogene Metastasierung: in der Regel erst nach Lymphknotenbefall, in 10% (besonders beim Chorionkarzinom) auch primär hämatogen, meistens pulmonal; Hirn- und Knochenfiliae sind selten, aber prognostisch sehr ungünstig. Klassifikation Histologische Klassifikation: WHO-Klassifikation Tabelle.54 Klinische Klassifikation: Derzeit sind verschiedene Klassifikationen zur Einteilung primärer Hodentumoren gebräuchlich. TNM-Klassifikation (UICC 2002): Alle Patienten mit Hodentumor sollten nach der TNM- Klassifikation der UICC in der Fassung von 2002 klassifiziert werden; durch Voranstellen eines»c«(»clinical«) anstelle des»p«(»pathological«) wird darauf hingewiesen, dass die Befunde nicht histologisch abgesichert sind ( Tabelle.55),
3 260 Kapitel Onkologie und Tumoren Tabelle.54. WHO-Klassifikation der malignen KZT von 1998 (modifiziert) Tumoren von einem histologischen Typ Anteil an allen KZT [%] Seminom 40 Spermatozytäres Seminom 1 Embryonales Karzinom 11 Dottersacktumor 0,7 Polyembryom <0,1 Chorionkarzinom 0, Teratom reifes Teratom 1,6 unreifes Teratom 0,5 Teratom mit maligner Transformation 0,1 Tumoren von mehr als einem histologischen Typ Embryonales Karzinom und Teratom 9 Chorionkarzinom mit anderem Tumor 8 Andere Tumorkombinationen 27 Als Seminome werden nur die reinen Seminome bezeichnet. Alle anderen Tumoren, auch Mischtumoren mit Seminomanteilen, werden unter den nichtseminomatösen Hodentumoren (NSGCT) zusammengefasst. Tabelle.55. TNM-Klassifikation der Hodentumoren. (UICC 2002) pt Primärtumor ptx pt0 ptis pt1 pt2 pt pt4 Primärtumor kann nicht untersucht werden Kein Hinweis auf Primärtumor (z. B. histologisch nur Narbe im Hoden bei»burned out tumor«intratubuläre Keimzellneoplasie (CIS) Tumor auf Hoden/Nebenhoden beschränkt ohne Lymph- oder Blutgefäßinvasion und Tumor kann Tunica albuginea infiltrieren aber nicht Tunica vaginalis Tumor auf Hoden/Nebenhoden beschränkt mit Lymph- oder Blutgefäßinvasion oder Tumor infiltriert Tunica albuginea mit Einbeziehung der Tunica vaginalis Tumor infiltriert Samenstrang mit oder ohne Lymph- oder Blutgefäßinvasion Tumor infiltriert Skrotum mit oder ohne Lymph- oder Blutgefäßinvasion
4 .10 Hodentumoren 261 Tabelle.55 (Fortsetzung) pn regionale Lymphknoten pnx pn0 pn1 pn2 pn Regionale Lymhknoten können nicht beurteilt werden Keine Metastasierung in regionale Lymphknoten Maximal 5 Lymphknotenmetastasen alle mit einem Durchmesser 2 cm Lymphknotenmetastasen mit einem Durchmesser >2 cm aber 5 cm oder mehr als 5 Lymphknotenmetastasen mit Durchmesser <2 cm oder Nachweis einer extranodalen Tumorausbreitung Lymphknotenmetastasen mit einem Durchmesser >5 cm M Fernmetastasen MX M0 M1 Fernmetastasen nicht beurteilbar keine Nachweis von Fernmetastasen Nachweis von Fernmetastasen S Serumtumormarker Sx S0 Serumtumormarker nicht verfügbar oder nicht durchgeführt Serumtumormarker im Normbereich LDH (IE/l) β-hcg (mie/ml) AFP (ng/ml) S1 <1,5fach der Norm und <5000 und <1000 S2 1,5- bis 10fach der Norm oder oder S >10fach der Norm oder > oder > Klassifikation nach Lugano ( Tabelle.56): häufig gebrauchte Klassifikation in Deutschland, insbesondere zur Festlegung von Therapiestrategien oder Prognoseeinschätzung, sinnvoll nur bis zum Stadium IIb, IGCCCG-Klassifikation: Alle metastasierten Hodentumoren werden gemäß dem Prognosesystem der International Germ Cell Cancer Collaborative Group (IGCCCG) klassifiziert ( Tabelle.57). Klinik und Diagnostik Klinik Leitsymptome: % der Patienten präsentieren sich mit primärem Hodentumor, 5 10% mit einem primär extragonadalen Tumor, bzw. mit einem Primärtumor unbekannten Ursprungs, schmerzlose Größenzunahme des Hodens (70%), tastbare Induration innerhalb des Hodens oder an seiner Oberfläche,
5 262 Kapitel Onkologie und Tumoren Tabelle.56. Klassifikation nach Lugano Stadium Klinisch Pathologisch I IIA Kein klinischer oder bildgebender Metastasennachweis Retroperitoneale Lymphknoten mit einem Durchmesser <2 cm im transversalen Durchmesser Negative retroperitoneale Lymph knoten Nicht mehr als 5 Lymphknoten metastasen, keine >2 cm IIB Retroperitoneale Lymphknoten mit einem Durchmesser von 2 5 cm im transversalen Durchmesser Mehr als 5 Lymphknotenmetastasen oder Metastasen von 2 5 cm oder mikroskopische Infiltration des extranodulären Gewebes IIC Retroperitoneale Lymphknoten mit einem Durchmesser von >5 cm im transversalen Durchmesser Lymphknotenmetastasen >5 cm im größten Durchmesser oder retroperitonealer Tumor in benachbarte Strukturen eingebrochen III Supradiaphragmatische Lymphknotenmetastasen oder/und hämatogene Aussaat Supradiaphragmatische Lymphknotenmetastasen oder/und hämatogene Aussaat Durch Voranstellen eines»c«(»clinical«) anstelle des»p«(»pathological«) wird darauf hingewiesen, dass die Befunde nicht histologisch abgesichert sind. (»Clinical stage«= CS,»pathological stage«= PS, z. B. CS IIB bei CT morpholgisch nachgewiesenen Metastasen der Größe 2 5 cm, z. B. PS I bei tumorfreien retroperitonealen Lymphknoten nach RLA und histologischer Aufarbeitung.) uncharakteristische Schmerzen in den Hoden (10 20%) durch intratumorale Hämorrhagien, cave: Fehldiagnose Epididymitis, Gynäkomastie (2 5%): β-hcg- oder Östrogenproduktion des Tumors, supraklavikuläre Metastasen (Palpation!). Weitere Symptome: extratestikuläre Symptomatik (10%) durch Metastasen, Rückenschmerzen, Hämoptoe (Lungenfiliae), u. U. Begleithydrozele. > Wichtig: Wegen des geringen Informationsstandes der jungen Männer zum Thema Hodentumor werden 50% aller Hodentumoren erst innerhalb von 2 Monaten nach dem Beginn der Symptome diagnostiziert. Diagnostik Primärtumor: Körperliche Untersuchung, Sonographie mit 7,5 Mhz-Schallkopf: meist intratestikuläre hypoechogene Läsion; Sensitivität: praktisch 100%; die seltenen»burned-out-tumoren«imponieren meistens als kleine umschriebene Mikrokalzifizierung.
6 .10 Hodentumoren 26 Tabelle.57. Prognosesystem der IGCCCG für metastasierte Hodentumoren NSGCT Seminome Good prognosis group 56% aller Fälle 5 Jahre progressfreies Über leben 89% 5 Jahre Überleben >90% Primärtumor in Hoden/Retroperitoneum Keine Fernmetastasen außer pulmonalen Filiae Tumormarker (S1) AFP <1000 ng/ml und β-hcg <5000 mie/l und LDH <1,5fach des Norm wertes 90 % aller Fälle 5 Jahre progressfreies Überleben 82% 5 Jahre Überleben 86% Alle Primärlokalisationen Keine Fernmetastasen außer pulmonalen Filiae Tumormarker Normales AFP Alle β-hcg Alle LDH Intermediate prognosis group 28% aller Fälle 5 Jahre progressfreies Über leben 75% 5 Jahre Überleben 80% Primärtumor in Hoden/Retroperitoneum Keine Fernmetastasen außer pulmonalen Filiae Tumormarker (S2) AFP 1000 ng/ml und ng/ml oder β-hcg und mie/l oder LDH 1,5fach und 10fach des Normwertes 10% aller Fälle 5 Jahre progressfreies Über leben 68% 5 Jahre Überleben 7% Alle Primärlokalisationen Nichtpulmonale Fernmetastasen Tumormarker Normales AFP Alle β-hcg Alle LDH Poor prognosis group 16% aller Fälle 5 Jahre progressfreies Über leben 41% 5 Jahre Überleben 50% Gibt es beim Seminom nicht Mediastinaler Primärtumor Nichtpulmonale Fernmetastasen Tumormarker (S) AFP > ng/ml oder β-hcg > mie/l oder LDH >10fach des Normwertes
7 264 Kapitel Onkologie und Tumoren > Wichtig: Sonographie des kontralateralen Hodens zum Ausschluss eines kontralateralen Hodentumors, zur Volumetrie und Diagnostik einer kontralateralen testikulären Mikrolithiasis. explorative Freilegung: im Zweifel ist die operative, inguinale Freilegung mit Schnellschnittdiagnostik obligat, MRT: keine Routinediagnostik, da sich meistens keine Änderungen des klinischen Procedere ergeben. Staging: 90% der Patienten präsentieren sich in frühen Tumorstadien (CS I, CS IIA, CS IIB), nur 10% in fortgeschrittenen Tumorstadien, Tumormarker: entscheidend ist die Berechnung der individuellen Halbwertszeit des Tumormarkerabfalls nach Ablatio testis; Notwendig ist die Bestimmung vor der Ablatio testis, 5 7 Tage nach Ablatio testis, vor und nach (>8 Tage) jeder weiterführenden Therapie sowie im Rahmen der Nachsorge; 90% aller NSGCT präsentieren sich mit einer Erhöhung eines Tumormarkers, AFP: HWZ 5 7 Tage; Norm: bis 10 ng/ml (erhöht bei 50 70% aller Patienten mit NSGCT); wird hauptsächlich von Dottersackanteilen des Tumors und vom embryonalen Karzinom gebildet; kommt bei Seminom nicht vor; falsch-positiv bei Leberzellschaden (Zirrhose), hepatozellulärem Karzinom, Pankreas-, Kolon-, Magentumoren, β-hcg: HWZ: 1 Tag; Norm: <5 ng/ml (erhöht bei 40 60% aller Patienten mit NSGCT und in 0% aller Patienten mit Seminom); wird hauptsächlich von synzytiotrophoblastähnlichen Zellen des Chorionkarzinoms (bei reinem Chorionkarzinom oft exzessive Werte), aber auch von den übrigen histologischen Formen (dann selten hohe Werte) gebildet, LDH: erhöht bei 80% aller Patienten mit fortgeschrittenen Tumoren; unspezifischer Marker, dessen Konzentration proportional zur Tumormasse ist; Bestimmung der LDH-Isoenzyme bringt keine zusätzliche Information, PLAP (plazentare alkalische Phosphatase; optional): HWZ: 1 Tag; bei 50 65% aller Seminompatienten erhöht; sehr eingeschränkte Spezifität, da bei Rauchern praktisch immer erhöht. Bildgebung: 1. Röntgenthorax in 2 Ebenen: Sensitivtät für intrapulmonale Raumforderungen ist zu gering, wird heute weitgehend durch Thorax-CT ersetzt; bei pathologischem Thorax-CT- Befund kann ein Röntgenthorax als Ausgangsbefund für die Verlaufskontrolle durchgeführt werden. 2. Thorax-CT: obligat zum Staging bei Hodentumorpatienten, da bei 10% der Patienten kleine subpleural gelegenen Metastasen vorhanden sind, die sich im konventionellen Röntgen nicht darstellen lassen.. CT Abdomen/Becken: obligate Staging-Untersuchung bei allen Hodentumorpatienten (u. U. kann bei Kindern darauf verzichtet werden), Applikation von oralem (Darmkontrastierung) und i. v.-kontrastmittel obligat,
8 .10 Hodentumoren 265 Sensitivität und Spezifität hängen wesentlich von dem Cut-off-Wert ab, ab dem Lymphknoten als pathologisch betrachtet werden, sowie von der Schichtdicke im Bereich des Nierenhilus; Sensitivität bei üblichem Cut off von 0,5 cm: 70 80%. 4. Sonographie des Retroperitoneums: optionale zusätzliche Untersuchung zur Beurteilung retroperitonealer Lymphknoten (>2 cm), ggf. Harnstauung, Gefäßimpressionen, Sonographie allein reicht zur Staging-Diagnostik nicht aus. 5. MRT Abdomen/Becken: alternativ zu CT Abdomen/Becken bei Kontrastmittelallergie (vergleichbare Sensitivität und Spezifität). 6. Schädel-CT: nur bei entsprechender Symptomatik oder bei Patienten der»intermediate«oder»poor prognosis group«(igcccg). 7. Knochenszintigraphie: nur bei entsprechender Symptomatik (Erhöhung der AP oder klinischer Symptomatik) bei Patienten der»intermediate«oder»poor prognosis group«(igcccg). 8. PET: zur Detektion tumorbefallener retroperitonealer Lymphknoten: kein Routineverfahren, nur im Rahmen von Studien (falsch-negativ bei Teratomen, falsch-positiv bei Entzündungen), mit einem FDG-PET-Scan kann bei Seminompatienten nach Chemotherapie zwischen aktivem Tumorgewebe und Narbe in den retroperitonealen Lymphknoten unterschieden werden. Sonderfall: retroperitoneale Raumforderung ohne primären Hodentumor beim jungen Mann V. a. Hodentumor immer gegeben, diagnostisch-therapeutisches Vorgehen: Bestimmung der Hodentumormarker, eine Erhöhung von AFP oder β-hcg sichert die Diagnose (keine Histologie erforderlich), Biopsie/Feinnadelaspirationszytologie des verdächtigen Befundes bei normalen Tumormarkern; schlecht differenzierte Karzinome oder Adenokarzinome sind verdächtig auf einen extragonadalen KZT, bei unklarem Biopsiebefund oder persistierendem Verdacht (selten): operative Freilegung. Sonderfall: testikuläre Mikrolithiasis Bei 2% der Bevölkerung kann sonographisch eine testikuläre Mikrolithiasis (»Sternkartenmuster«) gefunden werden, die testikuläre Mikrolithiasis ist überdurchschnittlich häufig vergesellschaftet mit TIN, insbesondere bei Risikogruppen, bei sonographischem Nachweis wird die bilaterale Biopsie daher empfohlen bei: Maldescenus testis, verkleinertem Hodenvolumen (<12 ml), intersexuellen Fehlbildungen, Infertilität, kontralateralem Hodentumor.
9 266 Kapitel Onkologie und Tumoren Fertilität von Hodentumorpatienten: Aufgrund des jungen Prädilektionsalters und der sehr guten Heilungsrate, spielt die Fertilität bei Hodentumorpatienten eine große Rolle. Bei allen Patienten sollte im Rahmen der Primärdiagnostik eine Basis-Fertilitätsdiagnostik durchgeführt werden; dazu gehören: Gesamttestosteron, LH, FSH, Spermiogramm, 70% aller Hodentumorpatienten haben bereits zum Zeitpunkt der Diagnose Defekte in der Spermiogenese, 12% sind azoosperm, retrograde Ejakulation nach RLA (selten bei richtiger Operationstechnik) kann die Fertilität weiter beeinträchtigen, allen Hodentumorpatienten muss die Kryokonservierung von Spermien angeboten werden! Die Kryokonservierung sollte nach Möglichkeit vor der Ablatio testis erfolgen, bei bilateralem Tumor oder kontralateraler TIN mit Oligo- oder Azoospermie sollte der Patient über die Möglichkeiten einer testikulären Spermienextraktion (TESE) aufgeklärt werden, obwohl bisher kein erhöhtes Missbildungsrisiko für Kinder von Patienten nach Chemotherapie beschrieben wurde, wird eine Kontrazeption für mindestens 6 Monate empfohlen. Therapie Hodentumoren wurden während der letzten beiden Dekaden zu einem Modell einer heilbaren Tumorerkrankung, möglich wurde dies durch die Einführung der Cisplatin-basierten Chemotherapie, eine Vielzahl gut geplanter und gut durchgeführter Studien und ein konsequentes interdisziplinäres Therapiekonzept. Die moderne Hodentumortherapie stützt sich daher auf eine breite Basis evidenzbasierter Therapieempfehlungen, die mittlerweile auch in der Publikation einer S2-Leitlinie zur Therapie von Hodentumoren resultierte. Wesentlicher Punkt bei der erfolgreichen Behandlung ist die Erfahrung des behandelnden Zentrums ( > Wichtig: Für alle Stadien sind mehrere unterschiedliche therapeutische Optionen möglich; entscheidend ist daher ein fundiertes Gespräch zwischen Arzt und Patient, in dem Vor- und Nachteile der verschiedenen Optionen ausführlich besprochen werden. Therapie des Primärtumors Unilateraler Tumor Ablatio testis von inguinalem Zugang, Absetzen des Samenstrangs auf Höhe des inneren Leistenringes, ggf. intraoperative Schnellschnittdiagnostik, Ausnahme: ausgedehnte, vital bedrohliche Metastasierung, in diesem Fall: initiale Chemotherapie, Ablatio testis nach Abschluss der Chemotherapie. Kontralaterale Biopsie bei Patienten mit primärem Hodentumor: Eine kontralaterale TIN liegt in 5% aller Fälle vor, sie kann mit einer offenen Biopsie in 99% diagnostiziert werden, kontralaterale Biopsie umstritten,
10 .10 Hodentumoren 267 Risiko für TIN bei 4% wenn: Volumen <12 ml und Alter <0 Jahre, hier wird immer eine kontralaterale Probebiopsie empfohlen, Technik: transskrotale Freilegung, Entnahme von 2 kleinen Proben, Fixation in Bouinoder Stieve-Lösung, kein Formalin! Hodenbiopsie bei Patienten mit primär extragonadalem Hodentumor: Etwa ein Drittel aller Patienten mit extragonadalem Hodentumor haben eine TIN in einem oder beiden, sonographisch normal erscheinenden Hoden, Biopsie beider Hoden nach Möglichkeit vor Chemotherapie oder mindestens 6 Monate nach Chemotherapie. Sonderfall: bilateraler Tumor (synchron oder metachron) Organerhaltendes Vorgehen (wenn präoperatives Testosteron normal), um Hormonproduktion potenziell zu erhalten, Probebiopsien vom Tumorgrund, postoperative Radiatio zur Eradikation der TIN immer erforderlich, Therapie nur in erfahrenen Zentren. Therapie von TIN des Hodens: TIN im kontralateralen Hoden bei Hodentumorpatienten bzw. im ipsilateralen Hoden nach organerhaltender Chirurgie (fehlender kontralateraler Hoden): Prinzipiell sind bei TIN in einem Einzelhoden Therapieoptionen möglich: Radiotherapie, Orchiektomie und Surveillance, lokale Radiatio: definitive Therapie, aber Verlust der Fertilität; Radiatio mit 20 Gy in Fraktionen zu je 2 Gy innerhalb von 2 Wochen; regelmäßige Testosteronkontrollen nach Radiatio, da die Leydig-Zell-Funktion beeinträchtigt werden kann, Orchiektomie: definitive Therapie, aber immer iatrogener Hypogonadismus mit möglichen Folgeerscheinungen; lebenslange Testosteronsubstitution erforderlich, Surveillance: gerechtfertigt bei Patienten mit Kinderwunsch, da die Zeitspanne zwischen TIN-Diagnose und Entstehung eines Hodentumors in der Regel lang ist; sonographische Kontrollen des Hodens spätestens alle Monate. TIN bei Hodentumorpatienten, bei denen eine Chemotherapie geplant ist: 6 Monate nach Chemotherapie Kontrollbiopsie, da TIN durch Chemotherapie vernichtet sein kann (nicht muss, etwa 60%); bei persistierender TIN: lokale Radiatio. TIN bei Patienten ohne Hodentumor: meistens bei infertilen Patienten oder bei Patienten mit Kryptorchismus, Ablatio testis: Therapie der Wahl, da hierdurch definitive Sanierung; bei diesen Patienten droht kein iatrogener Hypogonadismus, Radiatio: weniger vorteilhaft; Gefahr der kontralateralen Hodenschädigung mit weiterer Einschränkung der Fertilität durch Streustrahlung, Surveillance: möglich mit engmaschiger sonographischer Kontrolle. Therapie nicht-seminomatöser KZT im CS I, CS IIA/B Therapie nicht-seminomatöser KZT im CS I: Mit bildgebenden Verfahren kann eine okkulte retroperitoneale Metastasierung nicht sicher ausgeschlossen werden, d.h. Patienten im CS I haben ein potenzielles Risiko, im
11 268 Kapitel Onkologie und Tumoren Nicht-Seminom CS I Abb..4. Risikoadaptierte Therapie von NSGCT im CS I basierend auf der Gefäßinvasion im Primärtumor Anschluss an die Therapie des Primärtumors (PTU) ein retroperitoneales Rezidiv zu erleiden, da die Heilungsrate der Patienten mit NSGCT im CS I 99% beträgt und diese Patienten oftmals mit einem Minimum an Interventionen geheilt werden können, sind sie heute hauptsächlich dem Risiko der Überhandlung ausgesetzt. im Anschluss an die Ablatio testis ist eine risikoadaptierte Therapie sinnvoll, die sich an der Wahrscheinlichkeit einer retroperitonealen Metastasierung orientiert, bester Prognoseparameter für eine okkulte retroperitoneale Metastasierung: Tumorinvasion in Blut- oder Lymphgefäße (»vascular invasion«/vi) im Primärtumor (cave: bis zu 0% Unterschiede zw. lokaler und Referenzpathologie im Festlegen der vaskulären Invasion): CS I ohne VI im PTU (»low risk«): Risiko für die okkulte Metastasierung 14 22%, CS I mit VI im PTU (»high risk«): Risiko für okkulte Metastasierung 48%, Standardtherapie der NSGCT im CS I ( Abb..4) ist die risikoadaptierte Therapie basierend auf der Gefäßinvasion. Weiterführende Therapie bei Low-risk-Patienten: Therapieoptionen: empfohlene Therapie: Surveillance, alternative Therapie: adjuvante Chemotherapie (2 Zyklen PEB), ( Tabelle.58).
12 .10 Hodentumoren 269 Tabelle.58. Chemotherapie bei malignen KZT, Therapieprotokolle Standard Chemotherapieschema: PEB-Schema Cisplatin (P) 20 mg/m 2 KO/Tag i. v. (20 min Infusion) Tag 1 5 Nephrotoxisch Ototoxisch Polyneuropathie Etoposid (E) 100 mg/m 2 KO/Tag i. v. Tag 1 5 Polyneuropathie Bleomycin (B) 0 mg (Bolus) Tag 1, 8, 15 Lungenfibrose (ab mg; insbes. nach Radiatio des Mediastinums) Zyklusdauer: 21 Tage, Tag 22 = Tag 1 des nächsten Zyklus Induktive Chemotherapie: 4 PEB-Zyklen Adjuvante Chemotherapie: 2 PEB-Zyklen PEI-Schema Cisplatin (P) 20 mg/m 2 KO/Tag i. v. (20 min Infusion) Tag 1 5 Nephrotoxisch Ototoxisch Polyneuropathie Etoposid (E) 100 mg/m 2 KO/Tag i. v. Tag 1 5 Polyneuropathie Ifosfamid (I) 1,2 g/m 2 KO/Tag i. v. (60 min Infusion) Wiederholung alle drei Wochen VeIP-Schema Cisplatin (P) 20 mg/m 2 KO/Tag i. v. (20 min Infusion) Ifosfamid (I) 1,2 g/m 2 KO/Tag i. v. (60 min Infusion) Tag 1 5 Tag 1 5 Tag 1 5 Hämorrhagische Zystitis Nephrotoxisch Ototoxisch Polyneuropathie Hämorrhagische Zystitis Vinblastin (Ve) 0,11 mg/kg KG i. v. Tag 1+2 Polyneuropathie Neurotoxizität wird verstärkt durch Kombination mit Cisplatin Cisplatin/Etoposid Cisplatin (P) 20 mg/m 2 KO/Tag i. v. (20 min Infusion) Tag 1 5 Nephrotoxisch Ototoxisch Polyneuropathie Etoposid (E) 100 mg/m 2 KO/Tag i. v. Tag 1 5 Polyneuropathie In der englischsprachigen Literatur wird mitunter auch das BEP-Schema erwähnt. Es entspricht im Wesentlichen dem PEB-Schema. Etoposid wird in einer Dosis von 120 mg/m 2 KO/Tag i. v. nur an den Tagen 1, und 5 appliziert. Bleomycin wird in diesem Schema an den Tagen 2, 9 und 16 gegeben.
13 270 Kapitel Onkologie und Tumoren Vor- und Nachteile der Surveillance: Übertherapie in 78 86% der Fälle wird vermieden, im Falle eines Rezidivs können 99% aller Patienten mit Zyklen PEB geheilt werden, Voraussetzung: hohes Maß an Compliance von Patient und Arzt, 5 Jahre engmaschiges Follow-up obligat, im Falle eines Rezidivs sind, statt 2 Zyklen PEB notwendig. Vor- und Nachteile der adjuvanten Chemotherapie: Rezidivrisiko nur bei %, Übertherapie in 78 82%, Auftreten Chemotherapie-assoziierter Akuttoxitzitäten möglich, vorübergehende Beeinträchtigung der Fertilität, wahrscheinlich geringes Risiko für Chemotherapie-induzierte Zweittumoren, unbekannte Spättoxizitäten der Chemotherapie. Weiterführende Therapie bei High-risk-Patienten: Therapieoptionen empfohlene Therapie: adjuvante Chemotherapie (2 Zyklen PEB), ( Tabelle.58), alternative Therapie: Surveillance oder nervenschonende, retroperitoneale Lymph adenektomie (RLA). Vor- und Nachteile der adjuvanten Chemotherapie: 97% der High-risk-Patienten bleiben rezidivfrei, Gesamtheilungsrate 99%, Übertherapie in 52%, Auftreten Chemotherapie-assoziierter Akuttoxitzitäten möglich, vorübergehende Beeinträchtigung der Fertilität, wahrscheinlich geringes Risiko für Chemotherapie-induzierte Zweittumoren, unbekannte Spättoxizitäten der Chemotherapie. Vor- und Nachteile der Surveillance: keine Übertherapie in 48% der Fälle, Gefahr einer zu späten Diagnosestellung des Rezidivs mit erhöhtem Mortalitäts risiko, erhöhte psychische Belastung aufgrund des 48%igen Rezidivrisikos. Nervenschonende, retroperitoneale Lymphadenektomie (RLA): wird sowohl bei Low- als auch bei High-risk-Patienten nur noch empfohlen, wenn sich ein Patient weder einer Surveillancestrategie noch einer adjuvanten Chemotherapie unterziehen möchte, Standard ist nervenerhaltende, modifizierte RLA (d. h. Ausräumung der Lymphknoten nur der ipsilateralen Seite: innerhalb der Dissektionsgrenzen werden die aus den Grenzstrangganglien austretenden sympathischen Fasern geschont), im Falle positiver Lymphknoten in der Schnellschnittdiagnostik: Ausweitung auf eine bilaterale nervenschonende Lymphadenektomie, Nachteile: Überbehandlung in 52 86% der Fälle, akute operative Morbidität 9%, postoperativer Ejakulationsverlust: 2% in Zentren, pulmonales Rezidivrisiko 8 10% trotz Operation,
14 .10 Hodentumoren 271 Vorteile: histopathologische Sicherung des Tumorstadiums, Rezidivrisiko nur 8 10%, meistens pulmonal, Risiko für retroperitoneales Rezidiv auf 0 2% gesenkt, in etwa 70% keine weiterführende Chemotherapie notwendig. Vorgehen bei fehlender Markernormalisierung bei NSGCT CS I: Fehlender Markerabfall innerhalb der HWZ oder Anstieg der Hodentumormarker nach Ablatio testis im CS I weist auf eine okkulte Metastasierung hin, Therapie: Chemotherapie mit Zyklen PEB ( Tabelle.58), Fallen die Marker im Rahmen dieser Chemotherapie nicht zeitgerecht ab, sollte ein Alternativregime mit Cisplatin und Ifosfamid oder Vincristin oder Vinblastin angewandt werden, wegen der schlechten Prognose: frühzeitige Überweisung an ein Zentrum mit Hodentumorerfahrung, ggf. Hochdosischemotherapie. Therapie nicht-seminomatöser KZT im CS IIA/B: Siehe Abb..5. Heilungsrate für Patienten mit nicht-seminomatösen Hodentumoren im CS IIA und IIB: 98%, zu unterscheiden sind: Marker-positive Nicht-Seminome CS IIA bzw. IIB, Marker-negative Nicht-Seminome CS IIA, von einem Marker-positiven Tumor wird gesprochen, wenn zum Zeitpunkt der Diagnose erhöhte Spiegel von AFP, β-hcg und/oder LDH vorliegen. Therapie Marker positiver NSGCT CS IIA/B Marker-positive Nicht-Seminome CS IIA und IIB: werden nach den Kriterien der IGCCCG für metastasierte Tumoren klassifiziert und therapiert ( unten). Markerpositives Nicht-Seminom CS IIA, CS IIB Markernegatives Nicht-Seminom CS IIA Abb..5. Therapie von NSGCT im CS IIA/B
15 272 Kapitel Onkologie und Tumoren Therapie Marker negativer NSGCT CS IIA stellen ein besonderes Problem dar; es ist unklar, ob es sich bei der retroperitonealen Raumforderung um vitales Tumorgewebe oder um eine unspezifische Lymphknotenvergrößerung handelt. Therapieoptionen: primär nervschonende, modifizierte RLA, engmaschige Surveillance (alle 6 Wochen). Nervschonende RLA: sollte in nervenschonender, modifizierter Technik durchgeführt werden, Ausweitung auf bilaterale RLA bei positivem Metastasennachweis im Schnellschnitt, Procedere hängt von dem histologischen Ergebnis der retroperitonealen Lymphkno ten ab, kein retroperitonealer Metastasenachweis: bei 12 1% der Patienten mit NSGCT im CS IIA werden in der histologischen Aufarbeitung keine Metastasen gefunden; bei diesen Patienten ist ein routinemäßiges Follow-up ausreichend (ein Vorteil des primär operativen Vorgehens); Nachteile: akute operative Morbidität 9%, möglicher postoperativer Ejakulationsverlust von 2% in Zentren, bis zu 2% in unerfahrenen Kliniken, retroperitonealer Metastasenachweis: im PS IIA/B beträgt die Rezidivrate nach retroperitonealer, nervenschonender Lymphadenktomie 0% (PS IIA) bzw. 50% (PS IIB); Therapieoptionen: Surveillance; adjuvante Chemotherapie (2 Zyklen PEB), ( Tabelle.58) Vor- und Nachteile der Surveillance: keine weiterführende Therapie für 70% der Patienten im PS IIA und 50% im PS IIB notwendig, u. U. hohe psychische Belastung für den Patienten wegen relativ hohem Rezidivrisiko, hohe Compliance von Patient und Arzt erforderlich, bei Progress sind statt 2 Zyklen PEB notwendig, Vor- und Nachteile einer adjuvanten Chemotherapie (2 Zyklen PEB): Rezidivfreiheit in 9 100%, Überbehandlung in 50 70%, Auftreten Chemotherapie-assoziierter Akuttoxitzitäten möglich, vorübergehende Beeinträchtigung der Fertilität, wahrscheinlich geringes Risiko für Chemotherapie-induzierte Zweittumoren, unbekannte Spättoxizitäten der Chemotherapie. Surveillance: Alternativ zur nervschonenden RLA kommt bei Marker-negativen Patienten im CS IIA auch ein engmaschiges Follow-up infrage, 6-wöchige Überwachung der Tumormarker und engmaschige CT-Kontrolle sind obligat, weiteres Procedere abhängig vom Nachsorgeergebnis, Tumorregression: keine weitere Therapie, engmaschiges Follow-up,
16 .10 Hodentumoren 27 keine Veränderung des Befundes (»no change«): nervenschonende RLA oben, Fortführung des engmaschingen Follow-up: keine weiterführende Therapie für 12 1% der Patienten notwendig; u. U. hohe psychische Belastung für den Patienten wegen relativ hohem Rezidivrisiko; hohe Compliance von Patient und Arzt erforderlich, Progress ohne Markeranstieg: nervenschonende, retroperitoneale RLA: das weitere Vorgehen ist analog dem Vorgehen bei Marker-negativen NSGCT im CS IIA, Progress mit Markeranstieg: Zyklen PEB-Chemotherapie analog den Richtlinien bei metastasierten Tumoren (entspricht dem Vorgehen bei Marker-positiven NSGCT im CS IIA/B). Therapie seminomatöser KZT im CS I, CS IIA/B Therapie seminomatöser KZT im CS I: Risiko für okkulte Metastasierung bei seminomatösen Hodentumoren im CS I: 20%, Prognosefaktoren für das Seminom: low-risk: Tumorgröße <4 cm, keine Rete-testis-Infiltration: Rezidivrisiko: 12%, high-risk: Tumorgröße >4 cm, Rete-testis-Infiltration: Rezidivrisiko: 2%, Heilungsrate für Patienten mit Seminom CS I: annähernd 100%. Therapieoptionen: ( Abb..6) Radiotherapie, Surveillance (mit Radiotherapie oder Chemotherapie im Falle eines Rezidivs), Chemotherapie mit 1 Zyklus Carboplatin mono, low-risk-tumoren: präferierte Therapie: Surveillance, high-risk-tumoren: Radiotherapie oder Carboplatin-mono-Therapie. Radiotherapie: Bestrahlung des Retroperitoneums mit 20 Gy, in Einzeldosen à 2 Gy 5-mal pro Woche, das Strahlenfeld schließt die infradiaphragmalen paraaortalen/parakavalen Lymphknotenstationen mit ein, obere Begrenzung des Bestrahlungsfeldes: Oberrand von BWK 11, untere Begrenzung: Unterrand von LWK 5, auch bei anamnestischem Maldescensus testis, inguinaler oder skrotaler Voroperation oder pt/4-tumoren ist keine Erweiterung des Feldes auf die iliakalen Lymphknoten indiziert, Seminom CS I Radiatio 20 Gy (5 2 Gy) parakaval/paraaortal Abb..6. Therapie seminomatöser KZT CS I Chemotherapie Carboplatin mono (1 Zyklus) Surveillance
17 274 Kapitel Onkologie und Tumoren Vorteile: Rezidivrisiko: 4%, meistens außerhalb des bestrahlten Feldes, nur milde bis moderate Akutnebenwirkungen: moderate akute gastrointestinale NW: 60%, moderate chronische gastrointestinale NW: 5%, schwere Nebenwirkungen: <2%, Nachteile: Übertherapie in 80%, wahrscheinlich geringes Risiko für Zweittumoren induziert durch Radiotherapie, Einschränkung der Fertilität durch Radiotherapie wird kontrovers diskutiert. Surveillance: Voraussetzung ist eine größtmögliche Compliance von Patient und Arzt, 20% der Patienten rezidivieren überwiegend (97%) in den retroperitonealen oder hohen iliakalen Lymphknoten, Rezidive können 10 Jahre oder später nach Primärtherapie auftreten, sodass ein verlängertes Follow-up notwendig ist, Vorteile: 80% der Patienten brauchen keine weitere Therapie, Gesamtüberlebensraten nach Surveillance in erfahrenen Zentren: %, Nachteile: Rezidivrate bis zu 20%, Spätrezidive ( oben), gute Compliance von Arzt und Patient ist unbedingte Voraussetzung. Chemotherapie: Chemotherapie mit Carboplatin mono ist äquieffektiv wie Radiatio mit 20 Gy (1 Zyklus wurde prospektiv randomisiert getestet: Rezidivrate 5%, 2 Zyklen (nicht prospektiv evaluiert): Rezidivrate 1,5%), Vorteil: bei Carboplatin mono praktisch kein Auftreten einer TIN. Therapie seminomatöser KZT im CS IIA/B: 15 20% aller Seminompatienten präsentieren sich mit einer Erkrankung im klinischen Stadium II, Gesamtüberlebensrate für Seminompatienten im CS IIA/B beträgt fast 100%. Therapieoptionen: ( Abb..7) Standartherapie: Radiotherapie, alternative Therapie: Chemotherapie ( Zyklen PEB) ( Tabelle.58). Seminom CS IIA/B Radiatio CS IIA 0 Gy (à 2 Gy) parakaval/paraaortal/ ipsilateral iliacal PEB CS IIB 6 Gy (à 2 Gy) parakaval/paraaortal/ ipsilateral iliacal Abb..7. Therapie seminomatöser KZT CS IIA/B
18 .10 Hodentumoren 275 Radiotherapie: Stadium IIA: Sechsjahresrezidivrisiko 5%; retroperitoneale Bestrahlung mit 0 Gy in Einzeldosen von 2 Gy 5-mal pro Woche unter Einbeziehung der ipsilateralen iliakalen Lymphknotenstation; obere Begrenzung des Bestrahlungsfeldes: Oberrand BWK 11, untere Begrenzung: Oberrand Acetabulum, laterale Begrenzung: Processus transversi der Lendenwirbelsäule, Stadium IIB: Rezidivrisiko 11%; retroperitoneale Bestrahlung mit 6 Gy in Einzeldosen von 2 Gy 5-mal pro Woche unter Einbeziehung der ipsilateralen iliakalen Lymphknotenstation; obere Begrenzung des Bestrahlungsfeldes: Oberrand BWK 11; untere Begrenzung: Oberrand Acetabulum, laterale Begrenzung: individuell abhängig von der Ausdehnung der retroperitonealen Lymphome, Sicherheitsrand 1 1,5 cm, weder im CS IIA noch im CS IIB ist bei anamnestischem Maldescensus testis, inguinaler oder skrotaler Voroperation oder pt/4-tumoren eine Erweiterung des Bestrahlungsfeldes auf die kontralaterale ilikale, inguinale oder skrotale Region indiziert. Chemotherapie: alternativ bei Patienten, die sich keiner Radiotherapie unterziehen wollen ( Zyklen PEB), Carboplatin-Monotherapie ist mit einem höheren Rezidivrisiko verbunden und daher bei Seminompatienten im CS IIA/B nicht indiziert. Therapie fortgeschrittener maligner KZT Therapie fortgeschrittener NSGCT: Das therapeutische Vorgehen orientiert sich bei fortgeschrittenen Hodentumorstadien an der IGCCCG-Klassifikation ( Tabelle.57). Therapie bei Good prognosis: Standardtherapie: induktive Chemotherapie mit Zyklen PEB, bei Kontraindikationen gegen Bleomycin (z. B. Lungenerkrankungen) Behandlung mit 4 Zyklen Cisplatin/Etoposid (gleichwertig). Therapie bei Intermediate prognosis: Standardtherapie: induktive Chemotherapie mit 4 Zyklen PEB, nach Möglichkeit Therapie nur in prospektiven Studien, wegen der schlechteren Prognose. Therapie bei Poor prognosis: Standardtherapie: induktive Chemotherapie mit 4 Zyklen PEB (alternativ: -mal BEP + 1-mal EP), 4 Zyklen PEI (Cisplatin, Etoposid, Ifosfamid) sind ebenso effizient wie 4 Zyklen PEB, aber verursachen häufiger eine Myelotoxizität, bisher konnte keine Überlegenheit einer primären Hochdosischemotherapie bei Pa tienten mit Poor prognosis nachgewiesen werden, sodass diese nicht außerhalb klinischer Studien durchgeführt werden sollte; Patienten mit Poor prognosis sollten ohne Verzug an ein erfahrenes Zentrum weitergeleitet werden (
19 276 Kapitel Onkologie und Tumoren Monitoring, Restaging und weitere Therapie bei fortgeschrittenen NSGCT nach Primärtherapie ( Abb..8): Während der Chemotherapie standardisiertes Restaging erforderlich: Kontrolle der radiologischen Markerläsion nach 2 Zyklen zum Ausschluss eines»growing-teratoma- Syndroms«; wöchentliche Kontrolle der Tumormarker (immer unmittelbar vor einem Zyklus messen!), weiteres Procedere ist vom Restaging-Ergebnis abhängig ( Abb..8). Vollremission: Surveillance, Radiologische Partialremission (Residualtumor >1 cm) mit Markernormalisierung: Residualtumorresektion (weiteres Vorgehen abhängig von Histologie): Narbengewebe (40%): Surveillance, reifes Teratom (50%): Surveillance, vitales Tumorgewebe (10%): vitales Tumorgewebe oder unreifes Teratom und R0-Resektion: Surveillance, da kein verbessertes Gesamtüberleben nach Konsolidierungschemotherapie nachgewiesen wurde; bei R1-Resektion Salvage-Chemotherapie (bei Erreichen der maximalen kumulativen Bleomycin-Dosis als PEI), beste Prognose für Patienten: good prognosis; komplette Resektion des Residual tumors; <10% vitales Tumorgewebe im Residualtumor, Vorhandensein mehrerer Residualtumoren: nach Möglichkeit Resektion aller Residualtumoren; bei multiplen Residualtumoren in unterschiedlichen Organen: individuelle Entscheidung (bei Residualtumoren außerhalb der Lunge oder des Abdomens: Gefahr Fortgeschrittene NSGCT Procedere nach Restaging Vollremission radiologische Partialremission Markeranstieg radiologischer Progress Marker negativ Surveillance Marker negativ Residualtumorresektion Narbe/reif. Teratom Surveillance vitaler Tumor: R0 Surveillance R1 Salvage Chemo Salvage Chemotherapie Residualtumorresektion Narbe/reif. Teratom Surveillance vitaler Tumor: Salvage Chemo Markerpersistenz Residualtumorresektion Narbe/reif. Teratom Surveillance vitaler Tumor: Salvage Chemo Abb..8. Weitere Therapie bei fortgeschrittenen NSGCT nach Primärtherapie in Abhängigkeit des Ergebnisses des Restagings
20 .10 Hodentumoren 277 einer unterschiedlichen Histologie bei 5 50%); wenn die histologische Aufarbeitung des ersten Residualtumors eine Nekrose ergibt, sind sowohl die Surveillance der restlichen Tumoren als auch deren Resektion eine gangbare Lösung; Residualtumorresektionen sollten wegen ihrer hohen operativen Morbidität nur an erfahrenen Zentren durchgeführt werden. Radiologische Partialremission und Markerpersistenz auf niedrigem Plateau: Residualtumorresektion und histologische Aufarbeitung: vitales Tumorgewebe oder unreifes Teratom: Konsolidierungschemotherapie, reifes Teratom oder Narbe: Surveillance. Markeranstieg unter Chemotherapie: Salvage-Chemotherapie ( unten; auch bei fehlendem radiologischen Progress); Überweisung an Hodentumorzentrum. Radiologischer Progress bei gleichzeitiger Markernormaliserung: am wahrscheinlichsten ist ein so genanntes»growing teratoma«, d. h. Wachstum eines reifen Teratoms retroperitoneal, Therapie: Residualtumoresektion und histologische Untersuchung: reifes Teratom: Surveillance, vitales Tumorgewebe: Salvage-Chemotherapie. Therapie von fortgeschrittenen Seminomen: 5% aller Seminompatienten präsentieren sich mit einer fortgeschrittenen Erkrankung, Vorgehen entsprechend NSGCT- und IGCCCG-Prognosegruppen ( oben), Vorgehen bei retroperitonealen Residualtumoren nach Chemotherapie: keine Residualtumorresektion notwendig, unabhängig von Größe des Residualtumors, engmaschige Kontrolle mittels CT, bei Größenzunahme: Salvage-Chemotherapie nach histologischer oder zytologischer Sicherung, PET (Positronen Emissions Tomographie): bei Seminompatienten nach induktiver Chemotherapie Unterscheidung zwischen einem vitalen Residualtumor und Narbengewebe; bei positivem PET-Scan und einem Residualtumor > cm in der CT sollte zwingend eine histologische oder zytologische Sicherung erfolgen, ggf. Salvage Chemotherapie. Therapie von Patienten mit Hirnmetastasen: Etwa 10% aller Patienten mit fortgeschrittenen Hodentumoren (1 2% aller Hodentumorpatienten) präsentieren sich mit Hirnmetastasen, Prognose von Patienten mit Hirnmetastasen: bei initialer Diagnose: Langzeitüberlebensrate: 0 40%, bei Entwicklung von Hirnmetastasen unter»first-line-therapie«oder im Rezidiv: Fünfjahresüberlebensrate: 2 5%, Therapie von Patienten mit Hirnmetastasen: kurative induktive Chemotherapie gemäß»poor prognosis«(igcccg), die adjuvante Radiatio des gesamten Gehirns scheint die Prognose zu verbessern, ob die Resektion einer solitären Metastase nach Chemotherapie erforderlich ist, bleibt unklar und sollte von der Resektabilität abhängig gemacht werden.
21 278 Kapitel Onkologie und Tumoren Vorgehen bei Hodentumorrezidiv oder therapierefraktärer Erkrankung Die Prognose von Patienten mit Hodentumorrezidiv nach First-line-Therapie oder therapierefraktärer Erkrankung hängt ab von: Lokalisation und Histologie des Primärtumors, Ansprechen auf First-line-Therapie, Dauer der vorangegangenen Remissionen, Tumormarkerspiegel AFP, β-hcg zum Zeitpunkt des Rezidivs oder des Progresses, alle Patienten mit Hodentumorrezidiv nach First-line-Therapie oder therapierefraktärer Erkrankung sollten in einem erfahrenen Zentrum therapiert werden. Salvage-Therapie bei seminomatösen KZT: ( Abb..9) Rezidiv nach Radiotherapie: Standardtherapie: Salvage-Chemotherapie mit -mal PEB (wie»good prognosis group«), >90% Heilungsrate, Rezidiv nach Zyklen PEB: Standardtherapie: Salvage-Chemotherapie mit 4-mal PEI (Cisplatin, Etoposid und Ifosfamid) oder VeIP (Vinblastin, Etposid, Cisplatin), Langzeitremission bei bis zu 50% der Patienten ( Tabelle.58). Salvage-Therapie bei NSGCT: ( Abb..10) Rezidiv nach First-line-Chemotherapie: Standardtherapie: Salvage-Chemotherapie mit 4-mal PEI (Cisplatin, Etoposid und Ifosfamid) oder VeIP (Vinblastin, Etposid, Cisplatin), Langzeitremission bei bis zu 15 40% der Patienten; eine 4fach-Chemotherapie steigert die Toxizität, ohne die Wirksamkeit zu verbessern; da die Ergebnisse dieser Salvage-Chemotherapie nicht zufriedenstellend sind, sollten diese Patienten immer im Rahmen von mulitzentrischen Studien an erfahrenen Zentren behandelt werden ( Tabelle.58), Rezidiv nach operativer First-line-Therapie: Standardtherapie: Salvage-Chemotherapie mit -mal PEB (wie»good prognosis group«), >90% Heilungsrate ( Tabelle.58). therapierefraktäre Erkrankung/Rezidiv Seminom Initialtherapie: Radiotherapie Initialtherapie: PEB PEB Salvagechemotherapie 4 PEI 4 VeIP Abb..9. Salvage-Therapie bei therapierefraktären Seminomen
22 .10 Hodentumoren 279 therapierefraktäre Erkrankung/Rezidiv NSGCT Initialtherapie: RLA Initialtherapie: PEB PEB Salvagechemotherapie 4 PEI 4 VeIP Abb..10. Salvage-Therapie bei therapiefraktären NSGCT oder beim Rezidiv eines NSGCT Vorgehen bei Residualtumoren nach Salvage-Therapie: Normalisierung der Tumormarker oder Tumormarkerstabilisierung auf niedrigem Niveau: Residualtumorresektion innerhalb von 6 Wochen nach Salvage-Chemotherapie. Tumormarkerprogress und fehlende chemotherapeutische Option: Residualtumorresektion, wenn: Entfernung aller Residualtumoren machbar, nur mäßig erhöhtes AFP, kein oder langsam ansteigendes β-hcg, lokalisierte Metastasen, in diesen Fällen Langzeitüberleben in bis zu 25%. > Wichtig: Bei schnell ansteigendendem β-hcg und schnell progredienter Erkrankung sollte keine Salvage-Chirurgie mehr durchgeführt werden. Vorgehen bei Spätrezidiven: Bei Patienten mit Spätrezidiven bringt eine Chemotherapie schlechte Ergebnisse; daher sollten Spätrezidive immer, auch im Falle erhöhter Tumormarker, operativ entfernt werden, bei Inoperabilität: histologische Sicherung und Salvage-Chemotherapie; bei Ansprechen derselben: Resektion des Rezidivs. Nachsorge und Prognose maligner KZT Nachsorge Die folgenden Vorschläge orientieren sich an der Empfehlungen der German Testicular Cancer Study Group (GTCSG; Tabelle.59). Untersuchungsintervalle im Rahmen der Hodentumornachsorge: Jahr 1+2: alle Monate, Jahr : alle 4 Monate, Jahr 4+5: alle 6 Monate, ab Jahr 6: alle 12 Monate,
23 280 Kapitel Onkologie und Tumoren Tabelle.59. Empfehlungen der GTCSG zur Nachsorge bei Hodentumorpatienten Stadium/Therapie Seminom CS I Klinische Untersuchung/ Sono Thorax Abdomen Rö CT Sono CT adjuvante Radiotherapie mal/Jahr Surveillance mal/ Jahr Seminom CS IIA/B Erst ab. Jahr Jahr alle Monate Ab. Jahr 1-mal/Jahr Radiotherapie mal/Jahr adjuvante Chemotherapie + + Wechselnd Nichtseminom CS I Surveillance (»low risk«) mal/ Jahr Erst ab. Jahr Jahr alle Monate ab. Jahr 1-mal/Jahr adjuvante Chemotherapie + + Wechselnd diagnostische RLA Nichtseminom CS II RLA + adjuvante CTX mal/Jahr RLA mal/Jahr primär CTX +/ sekundär RLA + + Wechselnd Surveillance 6-wöchig mal/ Jahr Erst ab. Jahr Jahr alle Monate ab. Jahr 1-mal/Jahr Fortgeschrittene Stadien»good prognosis«+ + Wechselnd»intermediate/poor prognosis«+ + Bei Mediastinalbefall Erst ab. Jahr Jahr alle Monate ab. Jahr 1-mal/Jahr
24 .10 Hodentumoren 281 wegen der Möglichkeit von Spätrezidiven: lebenslang einmal jährlich Nachsorge, Nachsorgeuntersuchungen sollten immer enthalten: eine klinische Untersuchung (inklusive supraklavikuläre Lymphknoten) und eine Untersuchung der Tumormarker, Sonographie des kontralateralen Hodens sollte durchgeführt werden, wenn nicht mittels Biopsie eine TIN ausgeschlossen wurde, FSH und Testosteron sollten ebenfalls regelmäßig untersucht werden. Prognose Zu den Gesamtüberlebensraten Tabelle.60. Tabelle.60. Gesamtüberlebensraten nach malignem Hodentumor NSGCT Seminom Stadium I % % Stadium IIA/B >90% >90% Stadium IIC und III Gesamtüberlebensrate ist abhängig von der IGCCCG Klassifizierung:»good prognosis group«: 92%»intermediate prognosis group«: 80%»poor prognosis group«: 48% Literatur Albers P, Weinknecht S, Krege S et al. (2002) Prediction of necrosis after chemotherapy of advanced germ cell tumors Results of a prospective multicenter trial of the GTCSG. J Urol 167 (Suppl): 172 (abstract 690) Albers P, Siener R, Kliesch S et al. (200) Risk factors for relapse in clinical stage I nonseminomatous testicular germ cell tumors: results of the German Testicular Cancer Study Group trial. J Clin Oncol 21: Classen J, Schmidberger H, Meisner C et al. (200) Radiotherapy for stages IIA/B testicular seminoma: final report of a prospective multicenter clinical trial. J Clin Oncol 21: Collette L, Sylvester RJ, Stenning SP et al. (1999) Impact of the treating institution on survival of patients with»poor-prognosis«metastatic nonseminoma. European Organization for Research and Treatment of Cancer Genito-Urinary Tract Cancer Collaborative Group and the Medical Research Council Testicular Cancer Working Party. J Natl Cancer Inst 91: De Wit R, Stoter G, Sleijfer DT et al. (1998) Four cycles of BEP vs four cycles of VIP in patients with intermediateprognosis metastatic testicular non-seminoma: a randomized study of the EORTC Genitourinary Tract Cancer Cooperative Group. European Organization for Research and Treatment of Cancer. Br J Cancer 78: Dieckmann KP, Loy V (1996) Prevalence of contralateral testicular intraepithelial neoplasia in patients with testicular germ cell neoplasms. J Clin Oncol 14: Fossa SD, Bokemeyer C, Gerl A et al. (1999 a) Treatment outcome of patients with brain metastases from malignant germ cell tumors. Cancer 85: Fossa SD, Horwich A, Russel JM et al. (1999 b) Optimal planning target volume for stage I testicular seminoma: a Medical Research Council randomized trial. J Clin Oncol 17: Fossa SD, Stenning SP, Gerl A et al. (1999 c) Prognostic factors in patients progressing after cisplatin-based chemotherapy for malignant non-seminomatous germ cell tumours. Br J Cancer 80: Heidenreich A, Weissbach L, Holtl W et al. German Testicular Cancer Study Group (2001) Organ sparing surgery for malignant germ cell tumor of the testis. J Urol 166:
25 282 Kapitel Onkologie und Tumoren International Germ Cell Cancer Collaborative Group/IGCCCG (1997) The International Germ Cell Consensus Classification: a prognostic factor based staging system for metastatic germ cell cancer. J Clin Oncol 15: Klepp O, Dahl O, Flodgren P et al. (1997) Risk-adapted treatment of clinical stage I non-seminoma testis cancer. Eur J Cancer : Krege S, Schmoll H-J, Souchon R (2001) Interdisciplinary consensus on diagnosis and treatment of testicular germ cell tumors: result of an update conference on evidence-based medicine (EBM). Eur Urol 40: Miller KD, Loehrer PJ, Gonin R et al. (1997) Salvage chemotherapy with vinblastine, ifosfamide, and cisplatin in recurrent seminoma. J Clin Oncol 15: Petersen PM, Giwercman A, Daugaard G et al. (2002) Effect of graded testicular doses of radiotherapy in patients treated for carcinoma-in-situ in the testis. J Clin Oncol 20: Read G, Stenning SP, Cullen MH et al. (1992) Medical Research Council prospective study of surveillance for stage I testicular teratoma. Medical Research Council Testicular Tumors Working Party. J Clin Oncol 10: Schmoll HJ, Souchon R, Krege S et al. (2004) European Germ Cell Cancer Consensus Group. European consensus on diagnosis and treatment of germ cell cancer: a report of the European Germ Cell Cancer Consensus Group (EGCCCG). Ann Oncol 15: Skakkebaek NE, Berthelsen JG, Müller J (1982) Carcinoma in situ of the undescended testis. Urol Clin North Am 9: Spermon JR, Roeleveld TA, van der Poel HG et al. (2002) Comparison of surveillance and retroperitoneal lymph node dissection in stage I nonseminomatous germ cell tumors. Urology 59: Steyerberg EW, Keizer HJ, Fossa SD et al. (1995) Prediction of residual retroperitoneal mass histology after chemotherapy for metastatic nonseminomatous germ cell tumor: multivariate analysis of individual patient data from six study groups. J Clin Oncol 1: Warde P, Specht L, Horwich A, Oliver T, Panzarella T, Gospodarowicz M, von der Maase H (2002) Prognostic factors for relapse in stage I seminoma managed by surveillance. J Clin Oncol 20: Weissbach L, Bussar-Maatz R, Flechtner H et al. (2000) RPLND or primary chemotherapy in clinical stage IIA/B nonseminomatous germ cell tumors? Results of a prospective multicenter trial including quality of life assessment. Eur Urol 7: Williams SD, Stablein DM, Einhorn LH et al. (1987) Immediate adjuvant chemotherapy versus observation with treatment at relapse in pathological stage II testicular cancer. N Engl J Med 17: Nichtgerminative Hodentumore Leydigzelltumore Epidemiologie 1 % aller Hodentumore, Altersgipfel: 5 10 Jahre und 0 5 Jahre, in 10% bilaterales Auftreten. Ätiologie und Pathogenese Meistens benigner Tumor, in 10% jedoch maligner Verlauf, insbesondere im höheren Alter (Medianes Alter bei malignem Verlauf: 60 Jahre), Klinikopathologische Faktoren, die prädiktiv für malignen Verlauf sind: ausgeprägter Pleomorphismus, hohe mitotische Aktivität, Gefäßinvasion, fehlende Zeichen einer hormonellen Aktivität (Gynäkomastie),
26 .10 Hodentumoren 28 Keine Hinweise auf Entstehung aus einem Carzinoma in situ, vergleichbar den Keimzelltumoren, in 0% pathologische endokrinologische Befunde (Erhöhung von Testosteron, Östrogen oder Kortikosteroiden). Metastasierung retroperitoneale Lymphknoten 70%, Leber 45%, Lunge 40%, Knochen 25%, Risiko für Metastasierung: 100% der initial metastasierten Tumore waren DNA aneuploid, im Gegensatz zu 9% der initial nicht metastasierten Tumore. Alle aneuplioden, nicht metastasierten Tumoren entwickeln im weiteren Verlauf Metastasen (oft nach Jahren), selbst wenn der Primärtumor keine pathomorphologischen malignen Zeichen zeigte. Klinik/Labor erstes Symptom meistens schmerzlose Vergrößerung des Hodens, andere, endokrinologische bedingte Symptome können einer testikulären Masse vorangehen (insbesondere bei malignen Leydigzelltumoren): Androgen/Östradiolerhöhung, Kindesalter: Pubertas Präcox, Erwachsenenalter: Feminisierung und/oder Gynäkomastie. Diagnostik Primärtumor körperliche Untersuchung, Sonographie mit 7,5 Mhz Schallkopf: meist intratestikuläre hypoechogene Läsion. Sensitivität: praktisch 100%. Die seltenen»burned out«tumore imponieren meist als kleine umschriebene Mikrokalzifizierung, explorative Freilegung: im Zweifel ist die operative, inguinale Freilegung mit Schnellschnittdiagnostik obligat. Staging 1. CT Thorax kleine subpleural gelegenen Metastasen lassen sich u.u. im konventionellen Röntgen nicht darstellen. 2. Röntgen Thorax in 2 Ebenen: Bei pathologischem CT Thorax Befund kann ein Röntgen Thorax als Ausgangsbefund für die Verlaufskontrolle durchgeführt werden.. CT Abdomen/Becken: Die Applikation von oralem (Darmkontrastierung) und intravenösem Kontrastmittel ist obligat. Sensitivität und Spezifität hängen wesentlich von dem Cut Off Wert ab, ab dem Lmyphknoten als pathologisch betrachtet werden, sowie von der Schichtdicke im Bereich des Nierenhilus. Sensitivität bei üblichem Cut off von 0,5 cm: 70 80%. 4. Sonographie des Retroperitoneums: Optionale zusätzliche Untersuchung zur Beurteilung retroperitonealer Lymphknoten (>2 cm), ggf. Harnstauung, Gefäßimpressionen. Die Sonographie allein reicht zur Stagingdiagnostik nicht aus. 5. NMR Abdomen/Becken: alternativ zu CT Abdomen/Becken bei Kontrastmittelallergie (gleiche Sensitivität und Spezifität).
27 284 Kapitel Onkologie und Tumoren Therapie Primärtumor im Kindesalter: meistens gutartiger Verlauf, jedoch wurden nach Tumorenukleation selbst bei tumorfreien Absetzungsrändern Lokalrezidive gefunden, so dass die Ablatio testis die Therapie der Wahl zu sein scheint, im Erwachsenenalter: Ablatio testis, die Tumorenukleation mit Biopsien vom Tumorgrund wird diskutiert. Therapie bei metastasiertem Tumor Es gibt keine Standardtherapie bei metastasierten Leydigzelltumoren. Leydigzelltumore sind strahlenresistent, Retroperitoneale Lymphadenektomie: häufig nicht resektable Tumore, Resektion retroperitonealer Tumore scheint Rezidivrate nicht zu senken, prophylaktische retroperitoneale Lymphadenektomie: Einzelfallbericht (Patient erlitt nach 5 Jahren ein Leberrezidiv), Polychemotherapie: keine wirkungsvolle Chemotherapie bekannt, Mitotane: bei einigen Patienten wurden kurz- und mittelfristige Remissionen bei einer täglichen Dosis zwischen 4 und 14 g/d beschrieben, alle Patienten verstarben an dem malignen Leydigzelltumor. Nachsorge Auch bei nicht malignen Leydigzell Tumoren ist eine regelmäßige Nachsorge empfehlenswert, da die Gefahr von Spätrezidiven besteht. Untersuchungen: CT Thorax, CT Abdomen, Testosteron/Östradiol. Die Nachsorgeintervalle bei Leydigzelltumore sollten denen bei malignen Keimzelltumoren entsprechen. Es gibt allerdings keine standardisierten Nachsorgeempfehlungen. Sertolizelltumore Nach dem histologischen Bild und dem Alter des Patienten bei Intialdiagnose werden unterschieden: klassischer Sertolizelltumor (C-SCT), großzelliger kalzifizierender Sertolizelltumor (LCC-SCT), early onset LCC-SCT (Auftreten im mittleren Alter von 17 Jahren, häufig kombiniert mit hereditären dysplastischen Syndromen: z. B. Carney Syndrom [kardiale oder ku tane Myxome, endokrin aktive Tumore der Hypophyse, Nebennieren- oder Hoden, Pigmentierung der buccalen Schleimhaut oder der Gesichtshaut]), late onset LCC-SCT (Auftreten im mittleren Alter von 9 Jahren), sklerosierender Sertolizelltumor (S-SCT). Epidemiologie 0,4 bis 1% aller Hodentumore.
28 .10 Hodentumoren 285 Charakteristika von Sertolizelltumoren Tabelle.61 Tabelle.61. Charakteristika von Sertolizelltumoren C-SCT LCC-SCT S-SCT Fälle in der Literatur > Mittleres Alter (Jahre) 45, nie präpuberal 0, selten präpuberal 5, nie präpuberal bilateral nein 4,5% nein multifokal nein 28% nein genetische Disposition nicht bekannt möglich nicht bekannt hormonelle Aktivität 11 25%, meistens Östrogenproduktion möglich, meistens Testosteronproduktion nein Assoziation mit dysplastischen Syndromen nein 6% häufig mit Carney Syndrom nein Ultraschallbefund unspezifisch runde hyperechogene Fläche mit Schallschatten oder hyperecho gene Spots unspezifisch Tumormarker (AFP, βhcg, PLAP, LDH) negativ negativ negativ Histologie mittelgroße Zellen, keine Kalzifizierungen große eosinophile Zellen, diffuse Kalzifizierung kleine Zellen mit viel Bindegewebe maligner Verlauf 10 20% 0% bei Erwachsenen 10% bei Jugendlichen 8/48 (16,7%) 5,5% bei early onset 2% bei late onset 0/1% (0%) Diagnostik C-SCT, S-SCT, late-onset LCC-SCT: Diagnosestellung durch inguinale Freilegung und histologische Untersuchung. Eine kontralaterale Biopsie zum Ausschluss eines Karzinoma in situ ist nicht indiziert, early onset LCC-SCT: zusätzlich Ausschluss endokrin aktiver, zerebraler Tumore, sowie von kardialen Myxomen. Im Falle eines dysplatischen Syndroms ist ein Familienscreening indiziert. Staging 1. CT Thorax: kleine subpleural gelegenen Metastasen lassen sich u.u. im konventionellen Röntgen nicht darstellen. 2. Röntgen Thorax in 2 Ebenen: Bei pathologischem CT Thorax Befund kann ein Röntgen Thorax als Ausgangsbefund für die Verlaufskontrolle durchgeführt werden.. CT Abdomen/Becken: Die Applikation von oralem (Darmkontrastierung) und intravenösem Kontrastmittel ist obligat. Sensitivität und Spezifität hängen wesentlich von dem Cut Off Wert ab, ab dem Lmyphknoten als pathologisch betrachtet werden, sowie von der Schichtdicke im Bereich des Nierenhilus. Sensitivität bei üblichem Cut off von 0,5 cm: 70 80%.
29 286 Kapitel Onkologie und Tumoren 4. Sonographie des Retroperitoneums: Optionale zusätzliche Untersuchung zur Beurteilung retroperitonealer Lymphknoten (>2 cm), ggf. Harnstauung, Gefäßimpressionen. Die Sonographie allein reicht zur Stagingdiagnostik nicht aus. 5. NMR Abdomen/Becken: alternativ zu CT Abdomen/Becken bei Kontrastmittelallergie (gleiche Sensitivität und Spezifität). Therapie C-SCT: inguinale Ablatio testis, early-onset LCC-SCT: Tumorenukleation und Surveillance, wenn möglich. Bei bilateralem Befall und präpuberalem Alter: wait-and-see Strategie bis zur Pubertät (Möglichkeit der Kryokonservierung von Spermien), anschließend muss eine bilaterale inguinale Ablatio testis diskutiert werden. Es existieren keine klaren Richtlinien für diesen Fall, late-onset LCC-SCT: inguinale Ablatio testis. Bei ungünstigen histopathologischen Faktoren (Tumor-Größe >4 cm, extratesikuläre Ausbreitung, schlechte Differenzierung, Gefäßinvasion oder Mitoserate > bei 10-facher Vergrößerung) muss aufgrund der schlechten therapeutischen Möglichkeiten bei metastasierten Tumoren, eine primäre nervenschonende retroperitoneale Lymphadenektomie diskutiert werden, S-SCT: Tumorenukleation (Problem: kann ein S-SCT im Schnellschnitt sicher als solches erkannt werden?), Fortgeschrittene Tumore (CS II und CS III): Cisplatin basierte Chemotherapie zeigt nur einen sehr begrenzten Erfolg. Auch die chirurgische Therapie bringt keine überzeugenden Heilungsraten. Prognose Bei malignem Sertolizelltumor aufgrund frühzeitiger retroperitonealer, ossärer und pulmonaler Metastasierung und einer geringen Radio- und Chemosensitivität schlecht. Literatur 1. Mati W, Lam G, Dahl C, Thorup Andersen J, Balslev E (2002) Leydig cell tumour a rare testicular tumour. Int Urol Nephrol (1): Bertram KA, Bratloff B, Hodges GF, Davidson H (1991) Treatment of malignant Leydig cell tumors. Cancer 68: Giglio M, Medica M, De Rose AF, Germinale F, Ravetti JL, Carmignani G (200) Testicular sertoli cell tumours and relative sub-types. Analysis of clinical and prognostic features. Urol Int 70(): Urologische Tumoren im Kindesalter A. Heidenreich, E. Özgür Definition Unter den wichtigen urologischen Tumoren im Kindesalter werden folgende Neoplasien zusammengefasst: Neuroblastom, Wilms-Tumor, andere Nierentumoren: klarzelliges Sarkom, rhabdoide Tumoren,
30
DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN
 DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN Allgemeines Wesentlich in der Therapie der Hodentumore sind: die exakte histologische Untersuchung die Bestimmung des Stadiums die Festlegung der
DIAGNOSTIK UND THERAPIE NICHTSEMINOMATÖSER HODENTUMOREN Allgemeines Wesentlich in der Therapie der Hodentumore sind: die exakte histologische Untersuchung die Bestimmung des Stadiums die Festlegung der
Hodentumoren: Diagnose und Therapie
 Hodentumoren: Diagnose und Therapie Dr. Axel Häcker Assistenzarzt, Urologische Universitätsklinik Mannheim Anamnese - Risikofaktoren Alter Gene 70%: 20-40 a -BrüderrR10 - Söhne rr 5.7 - Väter rr 2-4.3
Hodentumoren: Diagnose und Therapie Dr. Axel Häcker Assistenzarzt, Urologische Universitätsklinik Mannheim Anamnese - Risikofaktoren Alter Gene 70%: 20-40 a -BrüderrR10 - Söhne rr 5.7 - Väter rr 2-4.3
Therapie metastasierter Hodentumoren
 Therapie metastasierter Hodentumoren Prof. Dr. Jörg Beyer Vivantes Klinikum Am Urban Dieffenbachstrasse 1 joerg.beyer@vivantes.de Fall No 1: Patient 33 Jahre Hodentumor rechts Z.n. Orchidektomie reines
Therapie metastasierter Hodentumoren Prof. Dr. Jörg Beyer Vivantes Klinikum Am Urban Dieffenbachstrasse 1 joerg.beyer@vivantes.de Fall No 1: Patient 33 Jahre Hodentumor rechts Z.n. Orchidektomie reines
1% aller soliden Malignome des Mannes. Häufigster bösartiger Tumor der jährigen Männer. Risikofaktoren: Titel. Folie 1
 Hodentumor-Epidemiologie 1% aller soliden Malignome des Mannes Häufigster bösartiger Tumor der 20-40 jährigen Männer Risikofaktoren: Maldeszensus testis: Erkrankungsrisiko bei Brüdern: Erkrankungsrisko
Hodentumor-Epidemiologie 1% aller soliden Malignome des Mannes Häufigster bösartiger Tumor der 20-40 jährigen Männer Risikofaktoren: Maldeszensus testis: Erkrankungsrisiko bei Brüdern: Erkrankungsrisko
Aktuelle Aspekte in der Diagnose und Therapie von Hodentumoren
 Aktuelle Aspekte in der Diagnose und Therapie von Hodentumoren PD Dr. Axel Häcker Urologische Universitätsklinik Mannheim EAU Guidelines 2005 Tumormarker Tumormarker AFP (HWZ 5-7 d) HCG (HWZ 24-36 h) LDH
Aktuelle Aspekte in der Diagnose und Therapie von Hodentumoren PD Dr. Axel Häcker Urologische Universitätsklinik Mannheim EAU Guidelines 2005 Tumormarker Tumormarker AFP (HWZ 5-7 d) HCG (HWZ 24-36 h) LDH
Interdisziplinäre Arbeitsgruppe Hodentumoren
 Interdisziplinäre Arbeitsgruppe Hodentumoren Vorschlag Nachsorgekonzept Hodentumoren Version 01 vom 30.03.2010 Ausarbeitung: Verabschiedet: Gültig bis: Richard Cathomas (Chur), Silke Gillessen (St. Gallen),
Interdisziplinäre Arbeitsgruppe Hodentumoren Vorschlag Nachsorgekonzept Hodentumoren Version 01 vom 30.03.2010 Ausarbeitung: Verabschiedet: Gültig bis: Richard Cathomas (Chur), Silke Gillessen (St. Gallen),
Therapie von fortgeschrittenen Hodenkarzinomen. Annette Dieing
 Therapie von fortgeschrittenen Hodenkarzinomen Annette Dieing 14.01.2014 Stadieneinteilung Fortgeschrittene Stadien Heilungsraten Anteil der Patienten Langzeit- Überleben Frühe Stadien 75% 99% Fortgeschrittene
Therapie von fortgeschrittenen Hodenkarzinomen Annette Dieing 14.01.2014 Stadieneinteilung Fortgeschrittene Stadien Heilungsraten Anteil der Patienten Langzeit- Überleben Frühe Stadien 75% 99% Fortgeschrittene
Keimzelltumoren. N. Meidenbauer Medizinische Klinik 5 Universitätsklinikum Erlangen
 Keimzelltumoren N. Meidenbauer Medizinische Klinik 5 Universitätsklinikum Erlangen Folien nur zur privaten Verwendung Folien teilweise übernommen www.esmo.org Jörg Beyer Andrea Necchi (E-learning) Robert
Keimzelltumoren N. Meidenbauer Medizinische Klinik 5 Universitätsklinikum Erlangen Folien nur zur privaten Verwendung Folien teilweise übernommen www.esmo.org Jörg Beyer Andrea Necchi (E-learning) Robert
Diagnostik und Therapie germinaler Hodentumoren
 Diagnostik und Therapie germinaler Hodentumoren Stand November 2003 Diagnostik und Therapie germinaler Hodentumoren Weitere Informationen Tumor Zentrum Berlin e. V. Robert-Koch-Platz 7, 10115 Berlin Tel.
Diagnostik und Therapie germinaler Hodentumoren Stand November 2003 Diagnostik und Therapie germinaler Hodentumoren Weitere Informationen Tumor Zentrum Berlin e. V. Robert-Koch-Platz 7, 10115 Berlin Tel.
Hodenkrebs (1) D07.6 Carcinoma in situ: Sonstige und nicht näher bezeichnete männliche Genitalorgane
 Hodenkrebs (1) Epidemiologie: Hodenkrebs gehört zu den eher seltenen Malignomen. Das Robert-Koch-Institut in Berlin gibt für 2004 die rohe Rate der Neuerkrankungen pro 100 000 Männern mit 11,8 pro Jahr
Hodenkrebs (1) Epidemiologie: Hodenkrebs gehört zu den eher seltenen Malignomen. Das Robert-Koch-Institut in Berlin gibt für 2004 die rohe Rate der Neuerkrankungen pro 100 000 Männern mit 11,8 pro Jahr
European Germ Cell Cancer Consensus Group (EGCCCG) Urologische Universitätsklinik Essen Westdeutschen Tumorzentrum Essen e.v.
 Klinik und Poliklinik für Urologie, Uroonkologie und Kinderurologie Direktor: Prof. Dr. med. Dr. h.c. H. Rübben Ansprechpartner: Dr. med. F. vom Dorp Hufelandstraße 55 5 Essen Tel. 00 73 3 Fax 00 73 35
Klinik und Poliklinik für Urologie, Uroonkologie und Kinderurologie Direktor: Prof. Dr. med. Dr. h.c. H. Rübben Ansprechpartner: Dr. med. F. vom Dorp Hufelandstraße 55 5 Essen Tel. 00 73 3 Fax 00 73 35
Hodentumoren. F2.3 Diagnostik. F2.1 Epidemiologie. Skrotaler Ultraschall. F2.2 Risikofaktoren und Prävention. Serumtumormarker. Brust/Weibl.
 F2 Hodentumoren 1 Brust/Weibl. Genitale Diese Leitlinie basiert auf einem interdisziplinären Konsens unter Zuhilfenahme der publizierten S2-Leitlinien zum Hodentumor (DKG) und den Konsensusempfehlungen
F2 Hodentumoren 1 Brust/Weibl. Genitale Diese Leitlinie basiert auf einem interdisziplinären Konsens unter Zuhilfenahme der publizierten S2-Leitlinien zum Hodentumor (DKG) und den Konsensusempfehlungen
Thema. Hodenkarzinom. Aufbaukurs Krebswissen WS 2015.16. Gero Kramer. Urologie. Autor, Einrichtung, Abteilung...
 Aufbaukurs Krebswissen WS 2015.16 Hodenkarzinom Gero Kramer Urologie 1 Hodenkarzinom Epidemiologie 1% aller bösartiger Neubildungen beim Mann 3-10 neue Fälle / 100 000 Männer / Jahr (Westen) Anstieg in
Aufbaukurs Krebswissen WS 2015.16 Hodenkarzinom Gero Kramer Urologie 1 Hodenkarzinom Epidemiologie 1% aller bösartiger Neubildungen beim Mann 3-10 neue Fälle / 100 000 Männer / Jahr (Westen) Anstieg in
56 Hodentumoren. J.T. Hartmann und S. Krege Epidemiologie Pathologie und Stadieneinteilung Pathologie
 56 Hodentumoren 1079 56 Hodentumoren J.T. Hartmann und S. Krege 56.1 Epidemiologie Häufigkeit: Inzidenz: Altersverteilung: Ätiologie: 1 2% aller Malignome bei Männern; häufigster maligner Tumor der 20-
56 Hodentumoren 1079 56 Hodentumoren J.T. Hartmann und S. Krege 56.1 Epidemiologie Häufigkeit: Inzidenz: Altersverteilung: Ätiologie: 1 2% aller Malignome bei Männern; häufigster maligner Tumor der 20-
56 Hodentumoren. J.T. Hartmann und S. Krege Epidemiologie Pathologie und Stadieneinteilung Pathologie
 56 Hodentumoren 1079 56 Hodentumoren J.T. Hartmann und S. Krege 56.1 Epidemiologie Häufigkeit: Inzidenz: Altersverteilung: Ätiologie: 1 2% aller Malignome bei Männern; häufigster maligner Tumor der 20-
56 Hodentumoren 1079 56 Hodentumoren J.T. Hartmann und S. Krege 56.1 Epidemiologie Häufigkeit: Inzidenz: Altersverteilung: Ätiologie: 1 2% aller Malignome bei Männern; häufigster maligner Tumor der 20-
Therapiekonzepte Onkologie
 Therapiekonzepte Onkologie Bearbeitet von Siegfried Seeber, Hans-Joachim Schütte erweitert, überarbeitet 2007. Buch. lv, 1851 S. Hardcover ISBN 978 3 540 28588 5 Format (B x L): 12,7 x 20,3 cm Weitere
Therapiekonzepte Onkologie Bearbeitet von Siegfried Seeber, Hans-Joachim Schütte erweitert, überarbeitet 2007. Buch. lv, 1851 S. Hardcover ISBN 978 3 540 28588 5 Format (B x L): 12,7 x 20,3 cm Weitere
MALIGNE KEIMZELLTUMOREN DES OVARS. W. Schröder
 MALIGNE KEIMZELLTUMOREN DES OVARS W. Schröder INZIDENZ VON KEIMZELLTUMOREN DES OVARS 20-25% aller Ovarialtumoren 3% aller Keimzelltumoren sind maligne 60-70% aller Ovarialtumoren < 20 Jahren 3-10% aller
MALIGNE KEIMZELLTUMOREN DES OVARS W. Schröder INZIDENZ VON KEIMZELLTUMOREN DES OVARS 20-25% aller Ovarialtumoren 3% aller Keimzelltumoren sind maligne 60-70% aller Ovarialtumoren < 20 Jahren 3-10% aller
Was tun, wenn der Tumor wieder ausbricht
 Was tun, wenn der Tumor wieder ausbricht Sindelfingen 22.10.2016 Dr. Ulrich Haag, Urologie, Kliniken Nagold S3-Leitlinie Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie
Was tun, wenn der Tumor wieder ausbricht Sindelfingen 22.10.2016 Dr. Ulrich Haag, Urologie, Kliniken Nagold S3-Leitlinie Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie
Fehleranalyse der Diagnostik und Therapie testikulärer Keimzelltumoren
 Aus der Klinik für Urologie und Kinderurologie Direktor: Prof. Dr. med. R. Hofmann des Fachbereichs Medizin der Philipps-Universität Marburg in Zusammenarbeit mit dem Universitätsklinikum Gießen und Marburg
Aus der Klinik für Urologie und Kinderurologie Direktor: Prof. Dr. med. R. Hofmann des Fachbereichs Medizin der Philipps-Universität Marburg in Zusammenarbeit mit dem Universitätsklinikum Gießen und Marburg
Hodentumoren Highlights and Dark Zones
 Hodentumoren Highlights and Dark Zones Prof. Dr. Jörg Beyer Leitender Arzt Klinik für Onkologie Telefon 044 255 21 54 Fax 044 255 12 40 Mail: joerg.beyer@usz.ch Hotline 079 855 80 96 Themen: Aktuelle Diskussionen
Hodentumoren Highlights and Dark Zones Prof. Dr. Jörg Beyer Leitender Arzt Klinik für Onkologie Telefon 044 255 21 54 Fax 044 255 12 40 Mail: joerg.beyer@usz.ch Hotline 079 855 80 96 Themen: Aktuelle Diskussionen
Therapie von Keimzelltumoren ein Überblick. 32. Zwickauer Onkologie-Symposium Neue Entwicklungen in der Onkologie 21. März 2015
 Therapie von Keimzelltumoren ein Überblick 32. Zwickauer Onkologie-Symposium Neue Entwicklungen in der Onkologie 21. März 2015 Anja Lorch Fachärztin für Innere Medizin, Hämatologie und Onkologie Leitung
Therapie von Keimzelltumoren ein Überblick 32. Zwickauer Onkologie-Symposium Neue Entwicklungen in der Onkologie 21. März 2015 Anja Lorch Fachärztin für Innere Medizin, Hämatologie und Onkologie Leitung
Behandlungsergebnisse von Patienten mit nicht-seminomatösen Hodentumoren aus dem Universitätsklinikum des Saarlandes zwischen 1975 und 2005
 Aus der Klinik und Poliklinik für Urologie und Kinderurologie Universitätsklinikum des Saarlandes, Homburg/Saar - Direktor: Prof. Dr. med. M. Stöckle Behandlungsergebnisse von Patienten mit nicht-seminomatösen
Aus der Klinik und Poliklinik für Urologie und Kinderurologie Universitätsklinikum des Saarlandes, Homburg/Saar - Direktor: Prof. Dr. med. M. Stöckle Behandlungsergebnisse von Patienten mit nicht-seminomatösen
Aktuelle Entwicklungen in der Behandlung des Prostatakarzinoms. O.Kölbl Klinik und Poliklinik für Strahlentherapie Universitätsklinikum Regensburg
 Aktuelle Entwicklungen in der Behandlung des Prostatakarzinoms O.Kölbl Klinik und Poliklinik für Strahlentherapie Universitätsklinikum Regensburg 1. Sollen Patienten nach einer Operation zusätzlich bestrahlt
Aktuelle Entwicklungen in der Behandlung des Prostatakarzinoms O.Kölbl Klinik und Poliklinik für Strahlentherapie Universitätsklinikum Regensburg 1. Sollen Patienten nach einer Operation zusätzlich bestrahlt
Leitlinien Maligne Hodentumoren
 W. Albrecht, M. E. Bonner, D. Jahn-Kuch und die Mitglieder des Arbeitskreises Onkologie (AUO) der Österreichischen Gesellschaft für Urologie Leitlinien Maligne Hodentumoren Präambel Die Leitlinien folgen
W. Albrecht, M. E. Bonner, D. Jahn-Kuch und die Mitglieder des Arbeitskreises Onkologie (AUO) der Österreichischen Gesellschaft für Urologie Leitlinien Maligne Hodentumoren Präambel Die Leitlinien folgen
Behandlung von Patienten mit metastasierten Hodentumoren
 Serie Behandlung von Patienten mit metastasierten Hodentumoren Carsten Bokemeyer 1, Jörg Beyer 2, Axel Heidenreich 3 Zusammenfassung Hodentumoren gehören zu den häufigsten Krebserkrankungen junger Männer.
Serie Behandlung von Patienten mit metastasierten Hodentumoren Carsten Bokemeyer 1, Jörg Beyer 2, Axel Heidenreich 3 Zusammenfassung Hodentumoren gehören zu den häufigsten Krebserkrankungen junger Männer.
Aus der Klinik für Urologie der Medizinischen Fakultät Charité Universitätsmedizin Berlin DISSERTATION
 Aus der Klinik für Urologie der Medizinischen Fakultät Charité Universitätsmedizin Berlin DISSERTATION Analyse der Versorgungsqualität von Patienten mit Keimzelltumoren an der Charité Gegenüberstellung
Aus der Klinik für Urologie der Medizinischen Fakultät Charité Universitätsmedizin Berlin DISSERTATION Analyse der Versorgungsqualität von Patienten mit Keimzelltumoren an der Charité Gegenüberstellung
Welche Untersuchungen führt der Urologe bei Verdacht auf einen Hodentumor durch?
 Hodenkrebs Was ist ein Hodentumor, was ist Hodenkrebs? Ein Hodentumor ist ein in der Regel bösartiges Geschwulst (Tumor) im Hoden, der potentiell über den Blut oder Lymphweg Tochtergeschwulste (Metastasen)
Hodenkrebs Was ist ein Hodentumor, was ist Hodenkrebs? Ein Hodentumor ist ein in der Regel bösartiges Geschwulst (Tumor) im Hoden, der potentiell über den Blut oder Lymphweg Tochtergeschwulste (Metastasen)
Pathologie, Typisierung, Ausbreitungsstadien
 1 24 Anal(kanal)karzinom H. Wiesinger Pathologie, Typisierung, Ausbreitungsstadien Tumoren der Analregion werden in solche des Analkanals und des Analrandes unterteilt. Der Analkanal erstreckt sich vom
1 24 Anal(kanal)karzinom H. Wiesinger Pathologie, Typisierung, Ausbreitungsstadien Tumoren der Analregion werden in solche des Analkanals und des Analrandes unterteilt. Der Analkanal erstreckt sich vom
Interdisziplinärer Konsensus zur Diagnostik und Therapie von Hodentumoren
 Strahlentherapie und Onkologie Urban & Vogel 2000 Aktuelles Forum Interdisziplinärer Konsensus zur Diagnostik und Therapie von Hodentumoren Ergebnisse einer Update-Konferenz auf Grundlage evidenzbasierter
Strahlentherapie und Onkologie Urban & Vogel 2000 Aktuelles Forum Interdisziplinärer Konsensus zur Diagnostik und Therapie von Hodentumoren Ergebnisse einer Update-Konferenz auf Grundlage evidenzbasierter
PATIENTENINFORMATION. der. Deutschen Gesellschaft für Urologie (DGU) und des. Berufsverbandes Deutscher Urologen (BDU) über.
 PATIENTENINFORMATION der Deutschen Gesellschaft für Urologie (DGU) und des Berufsverbandes Deutscher Urologen (BDU) über den Hodenkrebs Der Hodentumor Was Sie wissen sollten Hodenkrebs ist zwar sehr selten
PATIENTENINFORMATION der Deutschen Gesellschaft für Urologie (DGU) und des Berufsverbandes Deutscher Urologen (BDU) über den Hodenkrebs Der Hodentumor Was Sie wissen sollten Hodenkrebs ist zwar sehr selten
Palliative Chemotherapie First line 04.Februar 2006
 Klinikum der Johann Wolfgang Goethe Universität Zentrum für Innere Medizin Medizinische Klinik I Pneumologie/Allergologie Palliative Chemotherapie First line 04.Februar 2006 W. Gleiber Klinikum der Johann
Klinikum der Johann Wolfgang Goethe Universität Zentrum für Innere Medizin Medizinische Klinik I Pneumologie/Allergologie Palliative Chemotherapie First line 04.Februar 2006 W. Gleiber Klinikum der Johann
Uterine Leiomyosarkome
 Uterine Leiomyosarkome U. A. Ulrich Martin-Luther-Krankenhaus, Berlin AGO State-of-the-Art München, 6. 8. April 2017 LMS: Epidemiologie 1,3 % der uterinen Malignome, 50 % der uterinen Sarkome medianes
Uterine Leiomyosarkome U. A. Ulrich Martin-Luther-Krankenhaus, Berlin AGO State-of-the-Art München, 6. 8. April 2017 LMS: Epidemiologie 1,3 % der uterinen Malignome, 50 % der uterinen Sarkome medianes
State of the art Gynäkologische Onkologie 2013 Berlin, 22. Juni 2013
 State of the art Gynäkologische Onkologie 2013 Berlin, 22. Juni 2013 INZIDENZ VON KEIMZELLTUMOREN DES OVARS 20-25% aller Ovarialtumoren 3% aller Keimzelltumoren sind maligne 60-70% aller Ovarialtumoren
State of the art Gynäkologische Onkologie 2013 Berlin, 22. Juni 2013 INZIDENZ VON KEIMZELLTUMOREN DES OVARS 20-25% aller Ovarialtumoren 3% aller Keimzelltumoren sind maligne 60-70% aller Ovarialtumoren
Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen Abteilung Nuklearmedizin
 Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen 1990-2008 Abteilung Nuklearmedizin Hintergrund Therapie differenzierter SD-CAs: multimodal und interdisziplinär (Chirurgie und
Therapie und Nachsorge differenzierter Schilddrüsenkarzinome in Göttingen 1990-2008 Abteilung Nuklearmedizin Hintergrund Therapie differenzierter SD-CAs: multimodal und interdisziplinär (Chirurgie und
Leitlinie Bronchialkarzinom 2011 IOZ Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009
 Nr 27724 Version 1-0-0 Datum 29.08.11 Seite 1 von 5 Leitlinie Bronchialkarzinom 2011 Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009 Tab.1: Beschreibung der TNM-Parameter
Nr 27724 Version 1-0-0 Datum 29.08.11 Seite 1 von 5 Leitlinie Bronchialkarzinom 2011 Passau (adaptiert an S3-Leitlinie Bronchialkarzinom 2010) UICC-Klassifikation 2009 Tab.1: Beschreibung der TNM-Parameter
Hodgkin-Lymphom. Dr. med. Christoph Engel. Institut für Medizinische Informatik, Statistik und Epidemiologie (IMISE) Universität Leipzig
 Hodgkin-Lymphom Dr. med. Christoph Engel Institut für Medizinische Informatik, Statistik und Epidemiologie (IMISE) Universität Leipzig Hodgkin-Lymphom: Definition und klinische Symptomatik Definition:
Hodgkin-Lymphom Dr. med. Christoph Engel Institut für Medizinische Informatik, Statistik und Epidemiologie (IMISE) Universität Leipzig Hodgkin-Lymphom: Definition und klinische Symptomatik Definition:
Homepage: Online-Datenbank mit Autoren- und Stichwortsuche. Diagnostik und Therapie. testikulärer. Keimzelltumoren.
 ISSN 1727-0669 Diagnostik und Therapie testikulärer Keimzelltumoren Heidenreich A Blickpunkt der Mann 2005; 3 (3-4) 5-12 Homepage: www.kup.at/dermann Online-Datenbank mit Autoren- und Stichwortsuche Krause
ISSN 1727-0669 Diagnostik und Therapie testikulärer Keimzelltumoren Heidenreich A Blickpunkt der Mann 2005; 3 (3-4) 5-12 Homepage: www.kup.at/dermann Online-Datenbank mit Autoren- und Stichwortsuche Krause
Offenlegung potentieller Interessenkonflikte für diese Sitzung
 Offenlegung potentieller Interessenkonflikte für diese Sitzung 1. Anstellungsverhältnis oder Führungsposition keine 2. Beratungstätigkeit Keine 3. Aktienbesitz keiner 4. Honorare Keine 5. Finanzierung
Offenlegung potentieller Interessenkonflikte für diese Sitzung 1. Anstellungsverhältnis oder Führungsposition keine 2. Beratungstätigkeit Keine 3. Aktienbesitz keiner 4. Honorare Keine 5. Finanzierung
Tumore der männlichen Genitalorgane
 Tumore der männlichen Genitalorgane Autoren: C. Bokemeyer, D. Hossfeld 1. Hodentumore Das hier empfohlene Vorgehen wurde interdisziplinär abgesprochen (AIO/AUO/ARO) (1). 1.1 Epidemiologie Inzidenz 8 9/100000
Tumore der männlichen Genitalorgane Autoren: C. Bokemeyer, D. Hossfeld 1. Hodentumore Das hier empfohlene Vorgehen wurde interdisziplinär abgesprochen (AIO/AUO/ARO) (1). 1.1 Epidemiologie Inzidenz 8 9/100000
Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr
 Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr Klinik für Allgemein-, Visceral- und Transplantationschirurgie Charité, Campus Virchow-Klinikum Universitätsmedizin
Die Pankreasoperation - Indikation zur Operation nach Whipple PD Dr. med. Jan Langrehr Klinik für Allgemein-, Visceral- und Transplantationschirurgie Charité, Campus Virchow-Klinikum Universitätsmedizin
Extragonadale Keimzelltumoren. Jörg Beyer, Bern
 Extragonadale Keimzelltumoren Jörg Beyer, Bern Lernziele Erkennen, Behandeln, Heilen Take home message Hodentumor ist die häufigste Krebserkrankung bei Männern zwischen 18 und 40 Jahren cave: ca. 3% der
Extragonadale Keimzelltumoren Jörg Beyer, Bern Lernziele Erkennen, Behandeln, Heilen Take home message Hodentumor ist die häufigste Krebserkrankung bei Männern zwischen 18 und 40 Jahren cave: ca. 3% der
Kleinzelliges Lungenkarzinom (SCLC)
 Kleinzelliges Lungenkarzinom (SCLC) Verantwortlich: Prof. Dr. Nestle, Dr. Rawluk, Prof. Waller, Dr. Wiesemann Freigabe: interdisziplinärer Qualitätszirkel Stand: 04/2016, gültig bis 10/2017 Version 3.2
Kleinzelliges Lungenkarzinom (SCLC) Verantwortlich: Prof. Dr. Nestle, Dr. Rawluk, Prof. Waller, Dr. Wiesemann Freigabe: interdisziplinärer Qualitätszirkel Stand: 04/2016, gültig bis 10/2017 Version 3.2
Behandlungspfade Interdisziplinäres Onkologisches Zentrum Klinikum Ernst von Bergmann Potsdam. Hodgkin- Lymphom. Stand Dezember 2017
 Hodgkin- Lymphom Stand Dezember 2017 Erstdiagnose Notwendige Diagnostik Risikofaktoren Hodgkin- Lymphom Referenzhistologie obligat Klinische Untersuchung Anamnese (Alkoholschmerz) B- Symptome Fieber Nachtschweiß
Hodgkin- Lymphom Stand Dezember 2017 Erstdiagnose Notwendige Diagnostik Risikofaktoren Hodgkin- Lymphom Referenzhistologie obligat Klinische Untersuchung Anamnese (Alkoholschmerz) B- Symptome Fieber Nachtschweiß
Wintersemester 2014/2015
 Wintersemester 2014/2015 Weichteilsarkome Extremitäten, retroperitonäal, sehr selten Gesicht Sarkome Knochen und Knorpel (Osteosarkom, Chondrosakrom) Ewingsarkom (prädominant im Kindesalter) präoperativ
Wintersemester 2014/2015 Weichteilsarkome Extremitäten, retroperitonäal, sehr selten Gesicht Sarkome Knochen und Knorpel (Osteosarkom, Chondrosakrom) Ewingsarkom (prädominant im Kindesalter) präoperativ
DIAGNOSTIK UND BEHANDLUNG VON NIERENTUMOREN. Norbert Graf
 DIAGNOSTIK UND BEHANDLUNG VON NIERENTUMOREN Norbert Graf Nierentumoren WT mit Metastasen 10% WT bilateral 7% Andere 11% CMN 3% CCSK 3% MRTK 1% WT lokalisiert 72% Andere 4% gutartig
DIAGNOSTIK UND BEHANDLUNG VON NIERENTUMOREN Norbert Graf Nierentumoren WT mit Metastasen 10% WT bilateral 7% Andere 11% CMN 3% CCSK 3% MRTK 1% WT lokalisiert 72% Andere 4% gutartig
Hodentumore. Einleitung. Epidemiologie. Diagnose und Abklärungen. Klinische Präsentation
 CURRICULUM Schweiz Med Forum Nr. 40 1. Oktober 2003 950 Hodentumore Hubert Schefer a, Alain Schöpfer b, Walter Arnold c, Susanna Mattmann a, Peter Thum d, Patrick Michael Stucki e Klinische Untersuchung:
CURRICULUM Schweiz Med Forum Nr. 40 1. Oktober 2003 950 Hodentumore Hubert Schefer a, Alain Schöpfer b, Walter Arnold c, Susanna Mattmann a, Peter Thum d, Patrick Michael Stucki e Klinische Untersuchung:
Verzicht auf die Operation bei DCIS? Senologie-Update 2018
 Verzicht auf die Operation bei DCIS? Senologie-Update 2018 Duktales Carcinoma in situ (DCIS) Mammakarzinomzellen beschränkt auf Milchgänge und Milchläppchen Histologische Klassifikation kribriform solide
Verzicht auf die Operation bei DCIS? Senologie-Update 2018 Duktales Carcinoma in situ (DCIS) Mammakarzinomzellen beschränkt auf Milchgänge und Milchläppchen Histologische Klassifikation kribriform solide
Diagnostik und Therapie primärer und metastasierter Mammakarzinome
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Loko-regionäres Rezidiv Version 2002-2009: Brunnert / Simon/ Audretsch / Bauerfeind / Costa / Dall/ Gerber / Göhring / Lisboa / Rezai
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Loko-regionäres Rezidiv Version 2002-2009: Brunnert / Simon/ Audretsch / Bauerfeind / Costa / Dall/ Gerber / Göhring / Lisboa / Rezai
Studienzentrum der Deutschen Gesellschaft für f. SYNCHRONOUS Trial
 Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
HODENTUMORE. Ákos Pytel MD., PhD.
 HODENTUMORE Ákos Pytel MD., PhD. Epidemiologie ie I 0,8-6,7 neue Faelle jaehrlich/100.000 Haufigste bösartige Tumor in den 15-35 Jaehrigen Epidemiologie ie II 3. führende Todesursache wegen Malignomen
HODENTUMORE Ákos Pytel MD., PhD. Epidemiologie ie I 0,8-6,7 neue Faelle jaehrlich/100.000 Haufigste bösartige Tumor in den 15-35 Jaehrigen Epidemiologie ie II 3. führende Todesursache wegen Malignomen
Radioonkologie ( ) Therapieoptionen gegen den Krebs. Frank Zimmermann und Mitarbeiter
 Radioonkologie ( 13.1.4.15 ) Therapieoptionen gegen den Krebs Frank Zimmermann und Mitarbeiter Institut für Radioonkologie, Universitätsspital Basel Petersgraben 4, CH 4031 Basel radioonkologie basel Was
Radioonkologie ( 13.1.4.15 ) Therapieoptionen gegen den Krebs Frank Zimmermann und Mitarbeiter Institut für Radioonkologie, Universitätsspital Basel Petersgraben 4, CH 4031 Basel radioonkologie basel Was
Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung. Universitäts- Klinikum Jena
 Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung 2 Lokalisationen: Analkanals Palpatorischer Verdacht dann Endoskopie mit ggf. Probeexcision
Blutung ex ano, Druckgefühl insbesondere beim längeren Sitzen, Analer Pruritus Tenesmen, Dranggefühl vor Stuhlentleerung 2 Lokalisationen: Analkanals Palpatorischer Verdacht dann Endoskopie mit ggf. Probeexcision
Untersuchung der MDR1-Expression und ihrer klinischen Relevanz beim Keimzelltumor des Hodens
 Aus der Klinik für Urologie und Kinderurologie Direktor: Prof. Dr. med. Rainer Hofmann des Fachbereichs Medizin der Philipps-Universität Marburg in Zusammenarbeit mit dem Universitätsklinikum Gießen und
Aus der Klinik für Urologie und Kinderurologie Direktor: Prof. Dr. med. Rainer Hofmann des Fachbereichs Medizin der Philipps-Universität Marburg in Zusammenarbeit mit dem Universitätsklinikum Gießen und
Karzinome in der Urologie
 VIII. Onkologisches Fachtagung Berlin, 11.-13. 13. Juni 2005 Karzinome in der Urologie PD Dr. med. J. Roigas Klinik und Poliklinik für Urologie Campus Mitte Charité Universitätsmedizin Berlin wichtige
VIII. Onkologisches Fachtagung Berlin, 11.-13. 13. Juni 2005 Karzinome in der Urologie PD Dr. med. J. Roigas Klinik und Poliklinik für Urologie Campus Mitte Charité Universitätsmedizin Berlin wichtige
Pro und contra Früherkennung. Thomas Enzmann Steffen Lebentrau Klinik für Urologie und Kinderurologie
 Pro und contra Früherkennung Prostatakarzinom Thomas Enzmann Steffen Lebentrau Klinik für Urologie und Kinderurologie Prostatakarzinom Inzidenz Neuerkrankungen: 70100 Männer in BRD Robert Koch Institut
Pro und contra Früherkennung Prostatakarzinom Thomas Enzmann Steffen Lebentrau Klinik für Urologie und Kinderurologie Prostatakarzinom Inzidenz Neuerkrankungen: 70100 Männer in BRD Robert Koch Institut
Prostatakarzinom lokal Dr. med. J. Heß
 Prostatakarzinom lokal 30.11.2011 Dr. med. J. Heß Risiko für Prostatakarzinom: 40% Risiko für klinisch relevantem PCA: 10% Risiko für PCA-spezifischen Tod.: 3% Prostata, Lung, Colorectal and Ovarian Cancer
Prostatakarzinom lokal 30.11.2011 Dr. med. J. Heß Risiko für Prostatakarzinom: 40% Risiko für klinisch relevantem PCA: 10% Risiko für PCA-spezifischen Tod.: 3% Prostata, Lung, Colorectal and Ovarian Cancer
D i s s e r t a t i o n
 Aus der Universitätsklinik und Poliklinik für Urologie an der Martin- Luther- Universität Halle- Wittenberg (Direktor: Univ.- Prof. Dr. med. habil. P. Fornara) Diagnostik und Therapie beim testikulären
Aus der Universitätsklinik und Poliklinik für Urologie an der Martin- Luther- Universität Halle- Wittenberg (Direktor: Univ.- Prof. Dr. med. habil. P. Fornara) Diagnostik und Therapie beim testikulären
Medulläres Schilddrüsenkarzinom
 Medulläres Schilddrüsenkarzinom Verantwortlich: PD Dr. Dierks, Prof. Thomusch, Prof. Mayer, Prof. Seufert Freigabe: interdisziplinärer Qualitätszirkel Stand: 02/2017, gültig bis 02/2019 Version 1.0 Struktur
Medulläres Schilddrüsenkarzinom Verantwortlich: PD Dr. Dierks, Prof. Thomusch, Prof. Mayer, Prof. Seufert Freigabe: interdisziplinärer Qualitätszirkel Stand: 02/2017, gültig bis 02/2019 Version 1.0 Struktur
Therapie der testikulären intraepithelialen Neoplasie
 Therapie der testikulären intraepithelialen Neoplasie J. Heinzelbecker* Klinik f ur Urologie und Kinderurologie, Universitätsklinikum des Saarlandes, Homburg, Deutschland 1 Ätiologie der testikulären intraepithelialen
Therapie der testikulären intraepithelialen Neoplasie J. Heinzelbecker* Klinik f ur Urologie und Kinderurologie, Universitätsklinikum des Saarlandes, Homburg, Deutschland 1 Ätiologie der testikulären intraepithelialen
Gastrointestinale Stromatumoren (GIST) Dr. Dietmar Reichert, Westerstede
 1 Gastrointestinale Stromatumoren (GIST) Dr. Dietmar Reichert, Westerstede 2 ESMO: Klinische Empfehlungen 2009 Diagnose, Behandlung und Nachsorge 3 Diagnose GIST = 2 cm (wenn mgl.) endoskopische Biopsie
1 Gastrointestinale Stromatumoren (GIST) Dr. Dietmar Reichert, Westerstede 2 ESMO: Klinische Empfehlungen 2009 Diagnose, Behandlung und Nachsorge 3 Diagnose GIST = 2 cm (wenn mgl.) endoskopische Biopsie
Adjuvante und neoadjuvante Therapie beim KRK. PD Dr. med. Christian Pox Bremen
 10. addz - Jahrestagung Adjuvante und neoadjuvante Therapie beim KRK PD Dr. med. Christian Pox Bremen S3 Leitlinie Kolorektales Karzinom 2017 Update 2017 Themenkomplex I Themenkomplex II Themenkomplex
10. addz - Jahrestagung Adjuvante und neoadjuvante Therapie beim KRK PD Dr. med. Christian Pox Bremen S3 Leitlinie Kolorektales Karzinom 2017 Update 2017 Themenkomplex I Themenkomplex II Themenkomplex
kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ
 WS 2014/2015 kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ (zur Symptomlinderung) wenn lokale Beschwerden
WS 2014/2015 kurativ (Ziel der langdauernden Tumorfreiheit, z. B. nach 5 oder 10 Jahren) bei lokal begrenztem Karzinom, Alternative zur Prostatektomie palliativ (zur Symptomlinderung) wenn lokale Beschwerden
Krebs der großen Speicheldrüsen (1)
 Krebs der großen Speicheldrüsen (1) Epidemiologie: Nur etwa 0,3 % aller Tumoren sind epitheliale Speicheldrüsentumoren mit einer geschätzten Inzidenz von 1-3 pro 100 000 Einwohner pro Jahr. Sie kommen
Krebs der großen Speicheldrüsen (1) Epidemiologie: Nur etwa 0,3 % aller Tumoren sind epitheliale Speicheldrüsentumoren mit einer geschätzten Inzidenz von 1-3 pro 100 000 Einwohner pro Jahr. Sie kommen
Pathologie des Hodens
 Pathologie des Hodens Fehlanlage Anorchie Kryporchismus Hodenektopie Intersexualität Durchblutungsstörungen Entzündungen Tumoren Anorchie obwohl kein Hoden nachweisbar finden sich Residuen mit Leydigzellen
Pathologie des Hodens Fehlanlage Anorchie Kryporchismus Hodenektopie Intersexualität Durchblutungsstörungen Entzündungen Tumoren Anorchie obwohl kein Hoden nachweisbar finden sich Residuen mit Leydigzellen
Keimzelltumore. Keimzell- tumore. und. Nierenzell- karzinome. 18. Potsdamer Onkologisches Gespräch
 18. Potsdamer Onkologisches Gespräch Keimzell- tumore und Nierenzell- karzinome A. Dukat Klinik für Hämatologie, Onkologie u. Palliativmedizin Prof. Dr. G. Maschmeyer Keimzelltumore Keimzelltumore Epidemiologie
18. Potsdamer Onkologisches Gespräch Keimzell- tumore und Nierenzell- karzinome A. Dukat Klinik für Hämatologie, Onkologie u. Palliativmedizin Prof. Dr. G. Maschmeyer Keimzelltumore Keimzelltumore Epidemiologie
Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom
 Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom Verantwortlich: M. Bossart, K.Henne Freigabe: interdisziplinärer Qualitätszirkel Stand: 06/16, gültig bis 07/18 Version 3.1
Vulvakarzinom Epitheliales Ovarialkarzinom Zervixkarzinom Endometriumkarzinom Verantwortlich: M. Bossart, K.Henne Freigabe: interdisziplinärer Qualitätszirkel Stand: 06/16, gültig bis 07/18 Version 3.1
Active Surveillance & Watchful Waiting. Überwachungsstrategien beim lokal begrenzten Prostatakarzinom ohne aggressive Tumoranteile
 Active Surveillance & Watchful Waiting Überwachungsstrategien beim lokal begrenzten Prostatakarzinom ohne aggressive Tumoranteile 2 3 Einleitung Für Patienten mit einem lokal begrenzten Prostatakarzinom
Active Surveillance & Watchful Waiting Überwachungsstrategien beim lokal begrenzten Prostatakarzinom ohne aggressive Tumoranteile 2 3 Einleitung Für Patienten mit einem lokal begrenzten Prostatakarzinom
Medizin im Vortrag. Herausgeber: Prof. Dr. med. Christoph Frank Dietrich. Kolorektales Karzinom
 Medizin im Vortrag Herausgeber: Prof. Dr. med. Christoph Frank Dietrich Kolorektales Karzinom Autoren: Dr. med. Stefan Krüger Dr. med. Edgar Hartung Kerstin Siehr Prof. Dr. med. Christoph Frank Dietrich
Medizin im Vortrag Herausgeber: Prof. Dr. med. Christoph Frank Dietrich Kolorektales Karzinom Autoren: Dr. med. Stefan Krüger Dr. med. Edgar Hartung Kerstin Siehr Prof. Dr. med. Christoph Frank Dietrich
Prostatakarzinom Überversorgung oder Unterversorgung? Rüdiger Heicappell Urologische Klinik Asklepios Klinikum Uckermark Frankfurt /Oder,
 Prostatakarzinom Überversorgung oder Unterversorgung? Rüdiger Heicappell Urologische Klinik Asklepios Klinikum Uckermark Frankfurt /Oder, 10.6..2009 Die Weisheit des Alters... In Brandenburg wird zu viel
Prostatakarzinom Überversorgung oder Unterversorgung? Rüdiger Heicappell Urologische Klinik Asklepios Klinikum Uckermark Frankfurt /Oder, 10.6..2009 Die Weisheit des Alters... In Brandenburg wird zu viel
PET-CT in der urologischen Diagnostik speziell bei Prostatakarzinom
 PET-CT in der urologischen Diagnostik speziell bei Prostatakarzinom PD Dr. Dietmar Dinter Leiter des Geschäftsfeldes Onkologische Bildgebung Institut für Klinische Radiologie und Nuklearmedizin (Direktor:
PET-CT in der urologischen Diagnostik speziell bei Prostatakarzinom PD Dr. Dietmar Dinter Leiter des Geschäftsfeldes Onkologische Bildgebung Institut für Klinische Radiologie und Nuklearmedizin (Direktor:
Re-Evaluation eines prognostischen Scores bei rezidivierten. Keimzelltumoren: Identifikation von Patienten, die zum Zeitpunkt des ersten
 Aus der Klinik für Innere Medizin mit Schwerpunkt Onkologie/Hämatologie der Medizinischen Fakultät Charité Universitätsmedizin Berlin DISSERTATION Re-Evaluation eines prognostischen Scores bei rezidivierten
Aus der Klinik für Innere Medizin mit Schwerpunkt Onkologie/Hämatologie der Medizinischen Fakultät Charité Universitätsmedizin Berlin DISSERTATION Re-Evaluation eines prognostischen Scores bei rezidivierten
Anaplastisches Schilddrüsenkarzinom
 Anaplastisches Schilddrüsenkarzinom Verantwortlich: PD Dr. Dierks, Prof. Thomusch, Prof. von Bubnoff Freigabe: interdisziplinärer Qualitätszirkel Stand: 11/16, gültig bis 01/18 Version 1.0 Struktur der
Anaplastisches Schilddrüsenkarzinom Verantwortlich: PD Dr. Dierks, Prof. Thomusch, Prof. von Bubnoff Freigabe: interdisziplinärer Qualitätszirkel Stand: 11/16, gültig bis 01/18 Version 1.0 Struktur der
Untersuchung zur Bedeutung der. Positronen-Emissions-Tomographie zur Stadieneinteilung. und Therapiekontrolle bei Keimzelltumoren
 Aus der Medizinischen Klinik und Poliklinik II Abteilung für Onkologie, Hämatologie, Knochenmarktransplantation des Universitätsklinikums Hamburg Eppendorf Direktor: Prof. Dr. med. D.K. Hossfeld Untersuchung
Aus der Medizinischen Klinik und Poliklinik II Abteilung für Onkologie, Hämatologie, Knochenmarktransplantation des Universitätsklinikums Hamburg Eppendorf Direktor: Prof. Dr. med. D.K. Hossfeld Untersuchung
Was steht in meinem Befund?
 Basiskurs Krebswissen 09.11.2016 Was steht in meinem Befund? (Staging, Grading, TNM, ) Rainer Hamacher, MUW-AKH, Univ. Klinik für Innere Medizin I / Onkologie TNM STAGING & GRADING Tumorstaging (=Staging)
Basiskurs Krebswissen 09.11.2016 Was steht in meinem Befund? (Staging, Grading, TNM, ) Rainer Hamacher, MUW-AKH, Univ. Klinik für Innere Medizin I / Onkologie TNM STAGING & GRADING Tumorstaging (=Staging)
Nachsorge in der Uroonkologie nach kurativer Therapie. Zusammenfassung aktueller Literatur.
 Zusammenfassung aktueller Literatur Nachsorge in der Uroonkologie nach kurativer Therapie Helios Klinikum Pirna Klinik für Urologie und Kinderurologie Priv.-Doz. Dr. med. Volker Janitzky 1. Auflage 2018
Zusammenfassung aktueller Literatur Nachsorge in der Uroonkologie nach kurativer Therapie Helios Klinikum Pirna Klinik für Urologie und Kinderurologie Priv.-Doz. Dr. med. Volker Janitzky 1. Auflage 2018
Tumorerkrankungen im Kindesalter. - ein Überblick -
 Tumorerkrankungen im Kindesalter - ein Überblick - Elisabeth Holfeld 2. Brandenburger Krebskongress 25.02.2011 Hauptunterschiede zwischen Tumoren im Kindes- und Erwachsenenalter Häufigkeit der Tumoren
Tumorerkrankungen im Kindesalter - ein Überblick - Elisabeth Holfeld 2. Brandenburger Krebskongress 25.02.2011 Hauptunterschiede zwischen Tumoren im Kindes- und Erwachsenenalter Häufigkeit der Tumoren
Hypopharynxkarzinom Stand Oktober 2017
 Behandlungspfade Interdisziplinäres Onkologisches Zentrum Klinikum Ernst von Bergmann Potsdam Hypopharynxkarzinom Stand Oktober 2017 und PD Dr. Badakhshi und Behandlungspfade Interdisziplinäres Onkologisches
Behandlungspfade Interdisziplinäres Onkologisches Zentrum Klinikum Ernst von Bergmann Potsdam Hypopharynxkarzinom Stand Oktober 2017 und PD Dr. Badakhshi und Behandlungspfade Interdisziplinäres Onkologisches
Tumormarker Nutzen und Schaden. Stefan Aebi Medizinische Onkologie Luzerner Kantonsspital
 Tumormarker Nutzen und Schaden Stefan Aebi Medizinische Onkologie Luzerner Kantonsspital stefan.aebi@onkologie.ch Zum Begriff A tumor marker is a substance found in the blood, urine, or body tissues that
Tumormarker Nutzen und Schaden Stefan Aebi Medizinische Onkologie Luzerner Kantonsspital stefan.aebi@onkologie.ch Zum Begriff A tumor marker is a substance found in the blood, urine, or body tissues that
Interdisziplinäre evidenz-basierte Empfehlungen zur Nachsorge von Patienten mit Hodentumoren
 Interdisziplinäre evidenz-basierte Empfehlungen zur Nachsorge von Patienten mit Hodentumoren Interdisciplinary evidence-based recommendations for the follow-up of testicular germ cell cancer patients Michael
Interdisziplinäre evidenz-basierte Empfehlungen zur Nachsorge von Patienten mit Hodentumoren Interdisciplinary evidence-based recommendations for the follow-up of testicular germ cell cancer patients Michael
Das Spätrezidiv des Hodentumors eine retrospektive Analyse des Krankengutes der Urologischen Universitätsklinik Bonn im Literaturvergleich
 Das Spätrezidiv des Hodentumors eine retrospektive Analyse des Krankengutes der Urologischen Universitätsklinik Bonn im Literaturvergleich Inaugural-Dissertation zur Erlangung des Doktorgrades der Hohen
Das Spätrezidiv des Hodentumors eine retrospektive Analyse des Krankengutes der Urologischen Universitätsklinik Bonn im Literaturvergleich Inaugural-Dissertation zur Erlangung des Doktorgrades der Hohen
GI-ONCOLOGY INTERDISZIPLINÄRES UPDATE. Die neue TNM-Klassifikation von Tumoren. des oberen Gastrointestinaltrakts
 GI-ONCOLOGY 2010 6. INTERDISZIPLINÄRES UPDATE Die neue TNM-Klassifikation von Tumoren des oberen Gastrointestinaltrakts Christian Wittekind, Institut für Pathologie des UKL, Liebigstrasse 26, 04103 Leipzig
GI-ONCOLOGY 2010 6. INTERDISZIPLINÄRES UPDATE Die neue TNM-Klassifikation von Tumoren des oberen Gastrointestinaltrakts Christian Wittekind, Institut für Pathologie des UKL, Liebigstrasse 26, 04103 Leipzig
Multimodale Therapie des Pankreaskarzinoms
 Department Chirurgische of Klinik Surgery und Poliklinik, Munich, Germany Multimodale Therapie des Pankreaskarzinoms Helmut Friess Juli 2010 Neue Fälle Todesfälle 5 Jahres-Überleben (in %) Department of
Department Chirurgische of Klinik Surgery und Poliklinik, Munich, Germany Multimodale Therapie des Pankreaskarzinoms Helmut Friess Juli 2010 Neue Fälle Todesfälle 5 Jahres-Überleben (in %) Department of
Besondere Situationen und Lokalisationen in der metastasierten Situation
 Diagnostik Diagnosis und and Therapie Treatment primärer of Patients und with metastasierter Primary and Metastatic Mammakarzinome Breast Cancer Besondere Situationen und Lokalisationen in der metastasierten
Diagnostik Diagnosis und and Therapie Treatment primärer of Patients und with metastasierter Primary and Metastatic Mammakarzinome Breast Cancer Besondere Situationen und Lokalisationen in der metastasierten
PROBASE: Große deutsche Studie zum Prostatakrebs-Screening. PROBASE Große deutsche Studie zum Prostatakrebs-Screening
 PROBASE Große deutsche Studie zum Prostatakrebs-Screening Dresden (27. September 2013) Ziel der PROBASE-Studie (Risk-adapted prostate cancer early detection study based on a baseline PSA value in young
PROBASE Große deutsche Studie zum Prostatakrebs-Screening Dresden (27. September 2013) Ziel der PROBASE-Studie (Risk-adapted prostate cancer early detection study based on a baseline PSA value in young
Strahlentherapie des Endometriumkarzinoms. Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg
 Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Strahlentherapie des Endometriumkarzinoms Aktuelle Studienlage
Strahlentherapie des Endometriumkarzinoms Dirk Vordermark Universitätsklinik für Strahlentherapie Martin-Luther-Universität Halle-Wittenberg Strahlentherapie des Endometriumkarzinoms Aktuelle Studienlage
Therapie des Hodentumors
 Therapie des Hodentumors In unserer Klinik werden alle Therapieformen des Hodentumors von der Hodenentfernung über die organerhaltende Therapie, die systemische Chemotherapie in der Primär- als auch in
Therapie des Hodentumors In unserer Klinik werden alle Therapieformen des Hodentumors von der Hodenentfernung über die organerhaltende Therapie, die systemische Chemotherapie in der Primär- als auch in
Solide Tumoren bei jungen Patienten
 Onkologie 2011;34(suppl 5):12 16 Published online: August 5, 2011 DOI: 10.1159/000329908 Solide Tumoren bei jungen Patienten Jörg T. Hartmann a Anja Lorch b a Klinik für Innere Medizin II, Universitätsklinikum
Onkologie 2011;34(suppl 5):12 16 Published online: August 5, 2011 DOI: 10.1159/000329908 Solide Tumoren bei jungen Patienten Jörg T. Hartmann a Anja Lorch b a Klinik für Innere Medizin II, Universitätsklinikum
Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation?
 Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation? H.-S. Hofmann Thoraxchirurgisches Zentrum Universitätsklinikum Regensburg Krankenhaus Barmherzige Brüder Regensburg Problem:
Therapie des Bronchialkarzinoms Welcher Patient profitiert von der Operation? H.-S. Hofmann Thoraxchirurgisches Zentrum Universitätsklinikum Regensburg Krankenhaus Barmherzige Brüder Regensburg Problem:
Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom
 Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom Prof. Dr. med. R. Fietkau Strahlenklinik Ngan et al. 2012 Rectal-Ca: 5 x 5 Gy vs. RCT (50,4 Gy + 5-FU) 5 x 5Gy (N=163) RCT (N=163) Locoreg. recurrences
Neues zur neoadjuvanten Vorbehandlung beim Rektumkarzinom Prof. Dr. med. R. Fietkau Strahlenklinik Ngan et al. 2012 Rectal-Ca: 5 x 5 Gy vs. RCT (50,4 Gy + 5-FU) 5 x 5Gy (N=163) RCT (N=163) Locoreg. recurrences
Interdisziplinäre Behandlung der Karzinome des gastroösophagealen Übergangs und der Magenkarzinome
 Interdisziplinäre Behandlung der Karzinome des gastroösophagealen Übergangs und der Magenkarzinome Priv.-Doz. Dr. René Hennig Klinik für Allgemein und Viszeralchirurgie Bad Cannstatt Magenkarzinom & AEG
Interdisziplinäre Behandlung der Karzinome des gastroösophagealen Übergangs und der Magenkarzinome Priv.-Doz. Dr. René Hennig Klinik für Allgemein und Viszeralchirurgie Bad Cannstatt Magenkarzinom & AEG
Bronchus - Karzinom. Bronchus - Karzinom. 2. Screening. Bronchus Karzinom - Allgemein. 1. Einleitung allgemeine Informationen. 3.
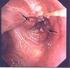 Bronchus - Karzinom J. Barandun LungenZentrum Hirslanden Zürich Screening Abklärung - Therapie Bronchus - Karzinom 1. Einleitung allgemeine Informationen 2. Screening 3. Abklärung 4. Therapie Bronchus
Bronchus - Karzinom J. Barandun LungenZentrum Hirslanden Zürich Screening Abklärung - Therapie Bronchus - Karzinom 1. Einleitung allgemeine Informationen 2. Screening 3. Abklärung 4. Therapie Bronchus
Duktales Carcinoma in situ (DCIS)
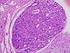 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Duktales Carcinoma in situ (DCIS) Duktales Carcinoma in situ (DCIS) Version 2002: Gerber Versionen 2003 2012: Audretsch / Brunnert / Costa
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Duktales Carcinoma in situ (DCIS) Duktales Carcinoma in situ (DCIS) Version 2002: Gerber Versionen 2003 2012: Audretsch / Brunnert / Costa
Was ist Strahlentherapie?
 Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
Was ist Strahlentherapie? Ionisierende Strahlen werden gezielt eingesetzt um Tumorgewebe zu beeinflussen / zu zerstören Wirkung erfolgt über zellbiologische Mechanismen lokale / lokoregionäre Therapieform
Therapie des "poor"-prognose Patienten: Was ist zu beachten?
 II. Medizinische Klinik, UCCH, Universitätsklinikum Hamburg Eppendorf DGHO Jahrestagung Stuttgart 2017 Therapie des "poor"-prognose Patienten: Was ist zu beachten? Prof. Dr. med. Carsten Bokemeyer Direktor
II. Medizinische Klinik, UCCH, Universitätsklinikum Hamburg Eppendorf DGHO Jahrestagung Stuttgart 2017 Therapie des "poor"-prognose Patienten: Was ist zu beachten? Prof. Dr. med. Carsten Bokemeyer Direktor
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung
 Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.01.2006 bis 30.06.2006 Erstellungstag: 30.06.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.01.2006 bis 30.06.2006 Erstellungstag: 30.06.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung
 Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.07.2005 bis 31.12.2005 Erstellungstag: 15.05.2006 Erstellungssoftware: Rückmeldesystem
Indikationsspezifischer Bericht zum Mammakarzinom für die Gemeinsame Einrichtung Ausgabe für den Berichtszeitraum 01.07.2005 bis 31.12.2005 Erstellungstag: 15.05.2006 Erstellungssoftware: Rückmeldesystem
Aus der Klinik für Urologie. der Medizinischen Fakultät Charité - Universitätsmedizin Berlin DISSERTATION. Seminom im klinischen Stadium I:
 Aus der Klinik für Urologie der Medizinischen Fakultät Charité - Universitätsmedizin Berlin DISSERTATION Seminom im klinischen Stadium I: Stellenwert der adjuvanten Therapie in der Versorgungsrealität.
Aus der Klinik für Urologie der Medizinischen Fakultät Charité - Universitätsmedizin Berlin DISSERTATION Seminom im klinischen Stadium I: Stellenwert der adjuvanten Therapie in der Versorgungsrealität.
Universität zu Lübeck Institut für Krebsepidemiologie e.v.
 Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
