Prüfungsarbeit eines Bewerbers A (Chemie)
|
|
|
- Erna Bader
- vor 7 Jahren
- Abrufe
Transkript
1 Prüfungsarbeit eines Bewerbers A (Chemie) Beschreibung Die vorliegende Erfindung betrifft Katalysatoren sowie deren Verwendung zur Alkylierung von Alkylbenzolen, insbesondere bei der Herstellung von 2,6-DNM. Des weiteren betrifft die Erfindung ein Verfahren zur Herstellung des Katalysators sowie Verfahren zur Alkylierung von Alkylbenzolen bzw. zur Herstellung von Dialkylnaphthalinen Im Stand der Technik sind Verfahren zur Herstellung von Dialkylnaphthalinen aus Alkylbenzolen bekannt. So beschreibt das Dokument 1 ein Verfahren zur Herstellung von Dialkylnaphthalinen, das folgende Schritte umfaßt: a) Reaktion eines Alkylbenzols mit einem Alken oder konjugierten Dien in Gegenwart eines Katalysators aus metallischem Natrium auf einem sauren Träger, b) Cyclisierung des so erhaltenen Reaktionsprodukts zu einem Dialkyltetralin, und c) Dehydrierung des Dialkyltetralins zu Dialkylnaphthalin Die Schritte b und c) des obigen Verfahrens, d. h. die Dehydrocyclisierung um Dialkylbenzolen zu Dialkylnaphtalin ist detailliert in Dokument 2 beschrieben. Das in Dokument 1 beschriebene Verfahren hat jedoch folgende Probleme, insbesondere bei der Herstellung von 2,6-DMN: a) Es handelt sich um ein mehrstufiges Verfahren mit vier oder fünf Reaktionsschritten. b) Die zugrunde liegenden Reaktionen sind nicht selektiv, und es entstehen zahlreiche Nebenprodukte, die in der Regel nur sehr schwer von 2,6-DMN zu trennen sind. Im Hinblick auf die Stand der Technik ergab sich somit die Aufgabe ein selektives Verfahren bereitzustellen, das mit einer Mindestzahl von Reaktionsschritten auskommt. Diese Aufgabe wird durch den Katalysator nach Anspruch 1 und die Verfahren nach Ansprüchen 4, 8, 13 und 15 sowie die Verwendung nach Anspruch 16 und 17 gelöst. Bevorzugte Ausführungsformen sind in den Unteransprüchen enthalten. Die Aufgabe wird bei dem erfindungsgemäßen Verfahren dadurch gelöst, daß ein Katalysator umfassend ein Alkalimetall auf einem basischen Träger eingesetzt wird. Dank dieses Katalysators wird erreicht, daß die Bildung von geradkettigen Reaktionsprodukten aus Alkylbenzol und Alken bzw. konjugiertem Dien soweit wie möglich verhindert wird. Die Erfindung zeichnet sich folglich durch eine höhere Selektivität bezüglich des verzweigten Reaktionsprodukts aus und ermöglicht die Herstellung von Dialkylnaphthalinen mit einer geringeren Anzahl an Reaktionsschritten. 1
2 Weder aus Dokument 1 noch aus Dokument 2 ist ein Katalysator nach Anspruch 1 zu entnehmen. Die Erfindung ist daher neu. Sie ergibt sich für den Fachmann auch nicht in naheliegender Weise aus dem Stand der Technik weil weder Dokument 1 als nächstliegender Stand der Technik noch die Kombination aus Dokument 1 und 2 einen Hinweis enthält, daß die Auswahl des Katalysatorträgers für den Alkalimetall-Trägerkatalysator das Verhältnis von verzweigten zu geradkettigen Reaktionsprodukten beeinflußt, und basische Träger die Selektivität für verzweigte Produkte erhöhen. Im folgenden wird die Ausführung der vorliegenden Erfindung näher beschrieben. Wir habe festgestellt, daß D die Alkylierung in Gegenwart eines Alkalimetall- Trägerkatalysators kann mit jedem beliebigen Alkylbenzol oder Alken durchgeführt werden kann, um alkylierte Produkte zu erhalten. Außerdem kann auch ein konjugiertes Dien (z. B. 1,3-Butadien) mit einem Alkylbenzol unter Verwendung desselben Katalysators umgesetzt werden, wobei als Reaktionsprodukt ein Alkenylbenzol entsteht. Die von den Erfindern durchgeführten Versuche zeigen, daß unabhängig davon, ob als Ausgangsmaterial ein Alken oder ein konjugiertes Dien verwendet wird, die genaue Auswahl des Katalysatorträgers das Verhältnis von verzweigten zu geradkettigen Reaktionsprodukten in exakt derselben Weise beeinflußt., wie wir das für die Reaktion zwischen p-xylol und Buten beobachtet haben. Alkenylbenzole können zu substituierten Naphthalinen dehydrocyclisiert werden mit genau denselben Katalysatoren und unter genau denselben Reaktionsbedingungen wie sie für die Alkylbenzole verwendet werden. Bevorzugt wird das erfindungsgemäße Verfahren bei der Herstellung von 2,6- Dimethylnaphthalin (2,6-DMN) eingesetzt, das als Schlüsselprodukt bei der Herstellung von Polyethylennaphthalat (PEN), einem für die Herstellung von Mehrweg- Plastikflaschen sehr gut geeignetem Kunststoff, wichtig ist. Das von uns entwickelte Ein bevorzugtes Verfahren umfaßt die folgenden Schritte: - Reaktion von para-xylol (p-xylol) und Buten (II) zu p- (2-Methylbutyl)-toluol (III) und - Dehydrocyclisierung von p-(2-methylbutyl)-toluol zu 2,6-Dimethylnaphthalin (2,6- DMN (IV)). Dabei wird der erfindungsgemäße Katalysator gemäß Anspruch 1 eingesetzt. 2
3 Die folgende Abbildung zeigt eine vereinfachte Darstellung des Reaktionsschemas: Die einzelnen Verfahrensschritte sind im folgenden beschrieben: I. Herstellung von p-(2-methylbutyl)-toluol (III) In einem ersten Schritt wird p-xylol mit Buten alkyliert. Durch die Alkylierung wird eine Butylgruppe zu einer Methylgruppe des Xylols addiert. Die dabei entstehenden Reaktionsprodukte haben entweder eine gerade Seitenkette (in diesem Fall ist das Reaktionsprodukt p-(n-pentyl)toluol) oder eine verzweigte Seitenkette (das Reaktionsprodukt ist in diesem Fall das gewünschte p-(2- Methylbutyl)-toluol). Je nachdem, welcher Katalysator genau verwendet wird, variiert das Verhältnis zwischen den Reaktionsprodukten mit verzweigter und denen mit gerader Seitenkette etwas. In unserer Reaktionsfolge kommt es darauf an, die Bildung von geradkettigen Reaktionsprodukten wie p-(n-pentyl)toluol so weit wie möglich zu verhindern. Wenn nämlich p-(n-pentyl)totuol in signifikanten Mengen gebildet wird, muß es vor der Dehydrocyclisierung entfernt werden (z. B. durch fraktionierte Kristallisation). Anderenfalls entstehen bei der Dehydrocyclisierung Isomere des 2,6-DMN in signifikanten Mengen. Die Abtrennung des 2,6-DMN von diesen Isomeren ist sehr schwierig. Um die Bildung von geradkettigen Produkten zu minimieren, muß die Reaktion in Gegenwart eines Alkalimetall-Trägerkatalysators ablaufen. Grundsätzlich kommen hierfür alle Alkalimetalle in Betracht, aus Gründen der Wirtschaftlichkeit wird jedoch vorzugsweise Natrium, Kalium oder eine Mischung aus diesen beiden Metallen verwendet. Die Metalle müssen auf einen Träger aufgezogen werden. 3
4 Für unsere Reaktion können werden die Alkalimetalle auf einem der üblichen basischen Träger verwendet werden. Die So werden höchste Ausbeuten an p-(2- Methylbutyl)-toluol (III) werden erreicht wenn der Träger selbst basisch ist. Ein basischer Träger nach unserer Definition ist ein Material, das Kohlendioxid bei höheren Temperaturen desorbiert als ein herkömmliches alpha-aluminiumoxid. Das Verfahren zur Messung dieser Desorptionstemperatur und die genauen Merkmale des zu verwendenden herkömmlichen alpha-aluminiumoxids sind der Patentschrift US-A zu entnehmen. Als basische Träger besonders bevorzugt sind pulverförmiges Natrium- oder Kaliumcarbonat, weil bei Verwendung dieser Katalysatoren mit diesen Trägern praktisch kein p-(n-pentyl)toluol entsteht. In diesem Fall entfällt der Abtrennungsschritt. A. Herstellung des Katalysators Ein für unsere Reaktion geeigneter Alkalimetall-Trägerkatalysator läßt sich erzeugen, indem das Alkalimetall und der Träger in einem Gewichtsverhältnis von 1 Teil Metall zu 0,5-500 Teilen Trägersubstanz unter inerter Atmosphäre in ein geschlossenes Gefäß, das ein organisches Lösungsmittel enthält, eingebracht werden. Das resultierende Gemisch wird mit hoher Geschwindigkeit üblicherweise bei einer Temperatur zwischen 30 und 60 C für die Dauer von 1-5 Stunden gerührt. Als organisches Lösungsmittel wird dabei vorzugsweise einer der Reaktanten verwendet. Beispiel 3 Teile metallisches Natrium und 97 Teile Kaliumcarbonat wurden gleichzeitig zu 200 Teilen p-xylol gegeben. Das Gemisch wird auf 50 C erhitzt und bei hoher Geschwindigkeit 2 Stunden lang gerührt. B. Herstellung von p-(2-methylbutyl)-toluol Die Reaktanten müssen trocken sein. Gegebenenfalls ist ein Trocknungsschritt vorzusehen. Das Reaktionssystem muß sauerstofffrei sein. Die Reaktion wird normalerweise bei einer Temperatur zwischen 100 und 200 C durchgeführt. Unter 100 C ist die Reaktionsgeschwindigkeit zu niedrig. Über 200 C nimmt die Selektivität ab. Der bevorzugte Temperaturbereich reicht von 110 bis 180 C. Üblicherweise wurde eine Reaktionszeit von 1 bis 10 Stunden gewählt. Das Verfahren kann entweder kontinuierlich in einem Röhrenreaktor oder diskontinuierlich in einem Batch-Reaktor durchgeführt werden. Wenn die Aktivität des Katalysators nachläßt, kann er aus dem System entfernt und ersetzt werden. Beispiel 4
5 Der gemäß obigem Beispiel hergestellte Katalysator, Natrium auf einem Kaliumcarbonat-Träger (suspendiert in p-xylol), wird in einen Reaktor eingebracht, der bei einer Temperatur von 120 C gehalten wird. Durch die Zugabe von weiterem p-xylol wird das Gewichtsverhältnis von p-xylol zum Katalysator auf 10:1 eingestellt. Anschließend läßt man für 5 Stunden langsam Buten durch den Reaktor strömen. Das Reaktionsprodukt p-(2-methylbutyl)-toluol wird vom Katalysator abfiltriert und kann ohne weitere Reinigung direkt der Dehydrocyclisierung zugeführt werden. II. Dehydrocyclisierung zu 2,6-Dimethylnaphthalin (IV) Diese Reaktion wird in der Gasphase unter Verwendung eines festen Katalysators durchgeführt. Zahlreiche der im Handel erhältlichen Katalysatoren können hierfür eingesetzt werden. Am besten geeignet sind auf Platinmetallen (z. B. Platin oder Palladium) basierende Katalysatoren mit einem Oxid (z. B. Chromoxid, Aluminiumoxid, Siliciumdioxid oder einem Zeolith) als Trägersubstanz. Die Reaktion ist aus der Literatur (z. B. Dokument 2) bekannt; auf eine genaue Beschreibung kann daher verzichtet werden. In unseren Versuchen haben wir als Katalysator Platin auf einem Zeolith-Träger verwendet, da dieser in unserer Anlage zur Verfügung stand. A. Herstellung des Katalysators Es kann ein auf Zeolith Y aufgezogener Platinkatalysator verwendet werden. Für seine Herstellung kommt jedes der bekannten Verfahren in Frage. Dabei wird der Zeolith üblicherweise mit der Lösung einer Platinverbindung imprägniert, bis eine Paste entsteht. Diese wird zu Pellets extrudiert, die getrocknet (mehrere Stunden bei einer Temperatur von etwas über 100 C) und anschließend calciniert werden (mindestens 3 Stunden in Luft bei 500 bis 600 C). Der Platingehalt sollte 0,5 bis 2,5 Gew.-% des Katalysators betragen. B. Herstellung von 2,6-DMN Die Dehydrocyclisierung kann erfolgen, indem ein Gas, das Wasserstoff und p-(2- Methylbutyl)-toluol (III) enthält, bei einer Temperatur zwischen 150 und 400 C, vorzugsweise im Bereich von 200 bis 300 C, über den Katalysator geleitet wird. Um Nebenreaktionen zu vermeiden, wird häufig ein inertes Glas wie Stickstoff, Kohlendioxid oder Wasserdampf zugesetzt. Um die gleichmäßige Überführung des festen Ausgangsstoffs in die Gasphase zu erleichtern, kann er in einem Lösungsmittel, z. B. einem aromatischen (Benzol, Toluol) oder alipathischen Kohlenwasserstoff (Hexan, Heptan), gelöst werden. 2,6- DMN läßt sich aus der Gasphase auskondensieren. Beispiel Ein Platin/Zeolith-Katalysator wurde in eine 3-mm-Quarzröhre gegeben. Dann wurden p-(2-methylbutyl)-toluol (III) und ein Stickstoff-Wasserstoff-Gemisch (1:1) zugeführt. Es wurden folgende Reaktionsbedingungen gewählt: Temperatur: 310 C, Druck: 1 bar, Kontaktzeit: 0,8 Sekunden. Die 2,6-DMN-Ausbeute lag bei 77,5 %. 5
6 III. Reinigung des Produkts Das durch die Dehydrocyclisierung gewonnene Produkt weist einige Verunreinigungen auf und kann durch Destillation gereinigt werden. Aufgrund dieser Versuche sind wir zu der wichtigen Erkenntnis gelangt, daß i In dem erfindungsgemäßen Herstellungsverfahren für 2,6-DMN kann statt Buten 1,3- Butadien als Ausgangsmaterial verwendet werden. In diesem Fall würde man als Reaktionsprodukt des ersten Verfahrensschrittes p-(2-methylbutenyl)-toluol erhalten. Diese Verbindung kann unter exakt denselben Reaktionsbedingungen wie p-(2-methylbutyl)-toluol zu 2,6-DMN dehydrocyclisiert werden. Der Einsatz von 1,3-Butadien ist aus kommerzieller Sicht sehr interessant und sollte nach Möglichkeit geschützt sein. In analoger Weise können jedoch auch beliebige andere Alkylbenzole mit beliebigen Alkenen oder konjugierten Dienen ungesetzt werden. Patentansprüche 1. Katalysator umfassend ein Alkalimetall auf einem basischen Träger. 2. Katalysator nach Anspruch 1, wobei als Alkalimetall Natrium, Kalium oder eine Mischung aus diesen beiden Metallen verwendet wird. 3. Katalysator nach Anspruch 1 oder 2, wobei als Träger pulverförmiges Natriumoder Kaliumcarbonat verwendet wird. 4. Verfahren zur Herstellung des Katalysators nach einem der Ansprüche 1-3, wobei das Alkalimetall und der basische Träger in einem Gewichtsverhältnis von 1 Teil Metall zu 0,5-500 Teilen Trägersubstanz unter inerter Atmosphäre in ein geschlossenes Gefäß, das ein organisches Lösungsmittel enthält, eingebracht wird und das Gemisch mit hoher Geschwindigkeit gerührt wird. 5. Verfahren nach Anspruch 4, wobei das Gemisch bei einer Temperatur zwischen 30 und 60 C für die Dauer von 1-5 Stunden gerührt wird. 6. Verfahren nach Anspruch 4 oder 5, wobei als organisches Lösungsmittel ein Alkylbenzol eingesetzt wird. 7. Verfahren nach Anspruch 5, wobei 3 Teile metallisches Natrium, 97 Teile Kaliumcarbonat zu 200 Teilen Xylol gegeben und bei 50 C mit hoher Geschwindigkeit 2 Stunden gerührt werden. 8. Verfahren zur Alkylierung von Alkylbenzolen umfassend die folgenden Schritte: a) gegebenenfalls Trocknen der Reaktanden b) Reaktion von trockenem Alkylbenzol mit trockenem Alken oder konjugiertem Dien in einem sauerstofffreien Reaktionssystem, dadurch gekennzeichnet, daß die Reaktion in Gegenwart des Katalysators nach einem der Ansprüche 1-3 durchgeführt wird. 6
7 9. Verfahren nach Anspruch 8, wobei das Verfahren bei einer Temperatur von C, bevorzugt C, durchgeführt wird. 10. Verfahren nach einem der Ansprüche 8 oder 9, wobei das Verfahren entweder kontinuierlich in einem Röhrenreaktor oder diskontinuierlich in einem Batch- Reaktor durchgeführt wird. 11. Verfahren nach einem der Ansprüche 8-10, wobei p-(2-methylbutyl)-toluol durch eine Reaktion von p-xylol mut Buten hergestellt wird. 12. Verfahren nach einem der Ansprüche 8-10, wobei p-(2-methylbutenyl)-toluol durch Reaktion von p-xylol mit 1,3-Butadien hergestellt wird. 13. Verfahren zur Herstellung von Dialkylnaphthalinen, umfassend die folgenden Schritte: a) das Verfahren zur Alkylierung nach einem der Ansprüche 8-12, b) Dehydrocyclisierung des erhaltenen Reaktionsprodukts zu Dialkylnaphthalin. 14. Verfahren nach Anspruch 12, wobei 2,6-DMN durch Reaktion von p-xylol mit Buten oder 1,3-Budadien hergestellt wird. 15. Verfahren zur Herstellung von PEN umfassend das Verfahren nach Anspruch Verwendung des Katalysators nach Anspruch 1-3 bei der Alkylierung von Alkylbenzolen. 17. Verwendung nach Anspruch 16 bei der Herstellung von 2,6-DMN. Anmerkungen Die allgemeine Formulierung der Verfahrensansprüche 8 und 13 wurde im Hinblick auf das Fax des Mandanten gewählt, das auch die Umsetzung anderer beliebiger Alkylbenzole mit Alken bzw. konjugiertem Dien erwähnt. Da der Katalysator neu und erfinderisch ist auch ein beliebiges Verfahren unter Einsatz des Katalysators erfinderisch bzw. dessen Verwendung (RiLi C-IV 9.5a). Die abhängigen Ansprüche 11, 12 und 14 können als Grundlage dienen, falls eine Beschränkung im Prüfungsverfahren nötig werden sollte. Beispielsweise, weil der Katalysator nicht mehr neu wäre und die Selektivität nur bei Umsetzung von p-xylol mit Buten bzw. 1,3-Butadien auftritt. Ähnliches gilt für Anspruch 16. Die Beschränkung des Anspruchs 8 auf trockene Reaktanden und ein sauerstofffreies Reaktionssystem wurde im Hinblick auf Punkt B 1. Absatz d. Mandantenschreibens (nun Beschreibung) durchgeführt. Evtl. könnte auch noch eine Beschränkung d. Temperaturbereichs im Hinblick auf Punkt B 2. Absatz notwendig sein. Dieser gilt jedoch nur für die Umsetzung von Buten und p-xylol. 7
8 RiLi = Prüfungsrichtlinien EPA Die Patentansprüche sind einheitlich, da sie alle den erfindungsgemäßen Katalysator enthalten als allgemeine erfinderische Idee (Art. 82 EPÜ, R. 30 EPÜ). Ansprüche 8 und 13 bereffen verschiedene Verwendungen eines Erzeugnisses (R. 29 (2) b) EPÜ nämlich des Katalysators. 8
Prüfungsarbeit eines Bewerbers
 Prüfungsarbeit eines Bewerbers Ansprüche Prüfungarbeit eines Bewerbers 0 ACH_DE_A 1. Gallium - oder Galliumlegierungspartikel, wobei der Galliumgehalt der in den Galliumlegierungspartikel eingesetzten
Prüfungsarbeit eines Bewerbers Ansprüche Prüfungarbeit eines Bewerbers 0 ACH_DE_A 1. Gallium - oder Galliumlegierungspartikel, wobei der Galliumgehalt der in den Galliumlegierungspartikel eingesetzten
EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2009/39
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 2 103 604 A1 (43) Veröffentlichungstag: 23.09.2009 Patentblatt 2009/39 (1) Int Cl.: C07D 301/12 (2006.01) (21) Anmeldenummer: 0810263.6 (22) Anmeldetag: 17.03.2008
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 2 103 604 A1 (43) Veröffentlichungstag: 23.09.2009 Patentblatt 2009/39 (1) Int Cl.: C07D 301/12 (2006.01) (21) Anmeldenummer: 0810263.6 (22) Anmeldetag: 17.03.2008
Fossile Rohstoffe. Erdöl
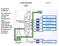 Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
(51) Int Cl. 7 : C08F 10/00, C08F 4/622
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP0017429A1* (11) EP 1 74 29 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 14.09.0 Patentblatt 0/37 (1)
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP0017429A1* (11) EP 1 74 29 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 14.09.0 Patentblatt 0/37 (1)
(51) Int Cl.: C07J 71/00 ( )
 (19) Europäisches Patentamt European Patent Office Office européen des brevets (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 700 862 A1 (43) Veröffentlichungstag: 13.09.2006 Patentblatt 2006/37 (51) Int Cl.:
(19) Europäisches Patentamt European Patent Office Office européen des brevets (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 700 862 A1 (43) Veröffentlichungstag: 13.09.2006 Patentblatt 2006/37 (51) Int Cl.:
@ Erfinder: Grubner, Kurt Birkenhainer Strasse. Vertreter: Munderich, Paul, Dipl.-lng. Frankfurter Strasse 84 D-6466 Grundau-Rothenbergen(DE)
 ä J Europäisches Patentamt European Patent Office Veröffentlichungsnummer: 0 151 662 Office europeen des brevets A1 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 84101486.3 Int. Cl.4: A 23 F 3/30 Anmeldetag:
ä J Europäisches Patentamt European Patent Office Veröffentlichungsnummer: 0 151 662 Office europeen des brevets A1 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 84101486.3 Int. Cl.4: A 23 F 3/30 Anmeldetag:
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Organisch-Chemisches Grundpraktikum Praxisseminar III
 Organisch-Chemisches Grundpraktikum Praxisseminar III Inhalt: Arbeiten mit Gasen Azeotropdestillation Naturstoffextraktion Laboretikette 3. April 21 Dr. Stefan Breitenlechner Lehrstuhl für Organische Chemie
Organisch-Chemisches Grundpraktikum Praxisseminar III Inhalt: Arbeiten mit Gasen Azeotropdestillation Naturstoffextraktion Laboretikette 3. April 21 Dr. Stefan Breitenlechner Lehrstuhl für Organische Chemie
Wertstoffrückgewinnung bei der Biogasreinigung
 Wertstoffrückgewinnung bei der Biogasreinigung Dr. M. Wecks Lutherstadt Wittenberg, 27.10.2006 Fachtagung INNOGAS: Herstellung von Biomethan aus Biogas 1/17 Zielstellung Nutzung der Nebenprodukte bei der
Wertstoffrückgewinnung bei der Biogasreinigung Dr. M. Wecks Lutherstadt Wittenberg, 27.10.2006 Fachtagung INNOGAS: Herstellung von Biomethan aus Biogas 1/17 Zielstellung Nutzung der Nebenprodukte bei der
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Veröffentlichungsnummer: A1 EUROPÄISCHE PATENTANMELDUNG. Anmeldenummer: Int. CI.3: C 07 B 29/00, B 01 J 12/00 ^
 Veröffentlichungsnummer: 0 1 1 0 4 1 1 A1 EUROPÄISCHE PATENTANMELDUNG Anmeldenummer: 83112078.7 Int. CI.3: C 07 B 29/00, B 01 J 12/00 ^ //C07D213/12.C07D231/06, @ Anmeldetag: 01.12.83 C07D233/06, C07D239/06
Veröffentlichungsnummer: 0 1 1 0 4 1 1 A1 EUROPÄISCHE PATENTANMELDUNG Anmeldenummer: 83112078.7 Int. CI.3: C 07 B 29/00, B 01 J 12/00 ^ //C07D213/12.C07D231/06, @ Anmeldetag: 01.12.83 C07D233/06, C07D239/06
*EP A1* EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2003/49
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001366676A1* (11) EP 1 366 676 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 03.12.03 Patentblatt 03/49
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001366676A1* (11) EP 1 366 676 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 03.12.03 Patentblatt 03/49
1 Lehrerversuch Alkalimetalle in Wasser
 1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
7. März 2007 Betreff: Europäische Patentanmeldung Nr. xxx
 2007-B-Chemie_01 An das Europäisches Patentamt D-80298 München 7. März 2007 Betreff: Europäische Patentanmeldung Nr. xxx Auf den Bescheid nach Artikel 96(2) EPÜ. 1. Antrag Es wird beantragt, auf Basis
2007-B-Chemie_01 An das Europäisches Patentamt D-80298 München 7. März 2007 Betreff: Europäische Patentanmeldung Nr. xxx Auf den Bescheid nach Artikel 96(2) EPÜ. 1. Antrag Es wird beantragt, auf Basis
*DE A *
 (19) *DE102017116778A120190131* (10) (12) Offenlegungsschrift (21) Aktenzeichen: 10 2017 116 778.1 (22) Anmeldetag: 25.07.2017 (43) Offenlegungstag: 31.01.2019 (71) Anmelder: Hauni Maschinenbau GmbH, 21033
(19) *DE102017116778A120190131* (10) (12) Offenlegungsschrift (21) Aktenzeichen: 10 2017 116 778.1 (22) Anmeldetag: 25.07.2017 (43) Offenlegungstag: 31.01.2019 (71) Anmelder: Hauni Maschinenbau GmbH, 21033
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Katalyse. Martin Babilon 14/07/2011. Katalyse. Martin Babilon Universität Paderborn. 14 Juli Montag, 18. Juli 2011
 Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
PC I Thermodynamik G. Jeschke FS Lösung zur Übung 12
 PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
*EP A1* EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2005/02
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP00149678A1* (11) EP 1 49 678 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 12.01.200 Patentblatt 200/02
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP00149678A1* (11) EP 1 49 678 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 12.01.200 Patentblatt 200/02
TEPZZ Z64477A_T EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG
 (19) TEPZZ Z64477A_T (11) EP 3 064 477 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 07.09.16 Patentblatt 16/36 (21) Anmeldenummer: 1616612.0 (1) Int Cl.: C02F 1/6 (06.01) C02F 1/68 (06.01)
(19) TEPZZ Z64477A_T (11) EP 3 064 477 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 07.09.16 Patentblatt 16/36 (21) Anmeldenummer: 1616612.0 (1) Int Cl.: C02F 1/6 (06.01) C02F 1/68 (06.01)
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
Europäisches Patentamt. European Patent Veröffentlichungsnummer: Office europeen des brevets A1 EUROPÄISCHE PATENTANMELDUNG
 Europäisches Patentamt European Patent Office @ Veröffentlichungsnummer: 0 023 5 5 6 Office europeen des brevets A1 1 EUROPÄISCHE PATENTANMELDUNG g) Anmeldenummer: 80103394.5 Int. Cl.3: C 07 D 251/32 )
Europäisches Patentamt European Patent Office @ Veröffentlichungsnummer: 0 023 5 5 6 Office europeen des brevets A1 1 EUROPÄISCHE PATENTANMELDUNG g) Anmeldenummer: 80103394.5 Int. Cl.3: C 07 D 251/32 )
Homologe Reihe der unverzweigten Alkane C n H (2n+2)
 Organische hemie I 3.01 Homologe Reihe der unverzweigten Alkane n H (2n+2) (Paraffine) (veraltet: normale Alkane = n-alkane) Name Konstitution Siedepunkt ausführliche Schreibweise Stenographie [ ] Methan
Organische hemie I 3.01 Homologe Reihe der unverzweigten Alkane n H (2n+2) (Paraffine) (veraltet: normale Alkane = n-alkane) Name Konstitution Siedepunkt ausführliche Schreibweise Stenographie [ ] Methan
Übungsaufgaben Physikalische Chemie
 Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Grundlagen der Chemie Chemisches Gleichgewicht
 Chemisches Gleichgewicht Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Das Massenwirkungsgesetz Wenn Substanzen
Chemisches Gleichgewicht Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Das Massenwirkungsgesetz Wenn Substanzen
TEPZZ 7Z9_5_A_T EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG
 (19) TEPZZ 7Z9_5_A_T (11) EP 2 709 151 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 19.03.2014 Patentblatt 2014/12 (21) Anmeldenummer: 13184804.6 (51) Int Cl.: H01L 23/31 (2006.01) H01L
(19) TEPZZ 7Z9_5_A_T (11) EP 2 709 151 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 19.03.2014 Patentblatt 2014/12 (21) Anmeldenummer: 13184804.6 (51) Int Cl.: H01L 23/31 (2006.01) H01L
EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2006/07
 (19) Europäisches Patentamt European Patent Office Office européen des brevets (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 626 264 A1 (43) Veröffentlichungstag: 15.02.2006 Patentblatt 2006/07 (51) Int Cl.:
(19) Europäisches Patentamt European Patent Office Office européen des brevets (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 626 264 A1 (43) Veröffentlichungstag: 15.02.2006 Patentblatt 2006/07 (51) Int Cl.:
EP A2 (19) (11) EP A2 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2000/10
 (19) Europäisches Patentamt European Patent Office Office européen des brevets (11) EP 0 983 984 A2 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 08.03.00 Patentblatt 00/ (21) Anmeldenummer:
(19) Europäisches Patentamt European Patent Office Office européen des brevets (11) EP 0 983 984 A2 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 08.03.00 Patentblatt 00/ (21) Anmeldenummer:
Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether)
 Endersch, Jonas 17./19.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether) Reaktionsgleichung: Einleitung und Theorie
Endersch, Jonas 17./19.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether) Reaktionsgleichung: Einleitung und Theorie
Patentkategorien. Erzeugnispatent (Vorrichtungspatent)
 Patentkategorien Patentschutz kann angestrebt werden für technische Lehren, die entweder ein Erzeugnis oder ein Verfahren betreffen. Welche der beiden Kategorien als Schutzform in Frage kommt, bestimmt
Patentkategorien Patentschutz kann angestrebt werden für technische Lehren, die entweder ein Erzeugnis oder ein Verfahren betreffen. Welche der beiden Kategorien als Schutzform in Frage kommt, bestimmt
Produktkatalog 2015/2016
 Produktkatalog 2015/2016 Holzkohle Holzkohle ist ein Brennstoff, welcher entsteht, wenn lufttrockenes Holz ohne Zufuhr von Sauerstoff auf 350 400 C erhitzt wird. Holzkohle ist ein Gemisch organischer Verbindungen
Produktkatalog 2015/2016 Holzkohle Holzkohle ist ein Brennstoff, welcher entsteht, wenn lufttrockenes Holz ohne Zufuhr von Sauerstoff auf 350 400 C erhitzt wird. Holzkohle ist ein Gemisch organischer Verbindungen
*DE U *
 (19) *DE202014102280U120140731* (10) DE 20 2014 102 280 U1 2014.07.31 (12) Gebrauchsmusterschrift (21) Aktenzeichen: 20 2014 102 280.5 (22) Anmeldetag: 15.05.2014 (47) Eintragungstag: 25.06.2014 (45) Bekanntmachungstag
(19) *DE202014102280U120140731* (10) DE 20 2014 102 280 U1 2014.07.31 (12) Gebrauchsmusterschrift (21) Aktenzeichen: 20 2014 102 280.5 (22) Anmeldetag: 15.05.2014 (47) Eintragungstag: 25.06.2014 (45) Bekanntmachungstag
Ordentliche Bezirksgruppenversammlung VDI-Haus, Hörsaal 1 Düsseldorf, 11. November 2004
 Ordentliche Bezirksgruppenversammlung VDI-Haus, Hörsaal 1 Düsseldorf, 11. November 2004 Patentanspruchsformulierungen: Sind Verwendungen als Verfahren schützbar? Dr. Stefan Féaux de Lacroix feaux@ib-patent.de
Ordentliche Bezirksgruppenversammlung VDI-Haus, Hörsaal 1 Düsseldorf, 11. November 2004 Patentanspruchsformulierungen: Sind Verwendungen als Verfahren schützbar? Dr. Stefan Féaux de Lacroix feaux@ib-patent.de
4.3 Reaktionsgeschwindigkeit und Katalysator
 4.3 Reaktionsgeschwindigkeit und Katalysator - Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Ein- Einstellung des Gleichgewichts,
4.3 Reaktionsgeschwindigkeit und Katalysator - Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Ein- Einstellung des Gleichgewichts,
Int CI.*: C 07 C 119/14 D 06 P 1/24. Anmelder: CIBA-GEIGY AG Postfach CH asel(CH)
 (19) Europäisches Patentamt European Patent Office Office european des brevets Veröffentlichungsnummer: 0 136 981 A2 (12 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 84810478.2 Anmeldetag: 01.10.84 Int CI.*:
(19) Europäisches Patentamt European Patent Office Office european des brevets Veröffentlichungsnummer: 0 136 981 A2 (12 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 84810478.2 Anmeldetag: 01.10.84 Int CI.*:
jyuon rnnung uompany uia.
 Office europeen des brevets A1 EUROPAISCHE PATENTANMELDUNG (21) Anmeldenummer: 79810116.8 0 Int. Cl.3: C 03 C 11/00 (22) Anmeldetag: 05.10.79 0) Prioritat: 06.10.78 CH 10441/78 0 Anmelder: MillcellAG Briinigstrasse
Office europeen des brevets A1 EUROPAISCHE PATENTANMELDUNG (21) Anmeldenummer: 79810116.8 0 Int. Cl.3: C 03 C 11/00 (22) Anmeldetag: 05.10.79 0) Prioritat: 06.10.78 CH 10441/78 0 Anmelder: MillcellAG Briinigstrasse
Ergänzende Hinweise Feste Reaktionsprodukte nicht in den Ausguß schütten! Vorsicht; es entsteht Knallgas!
 Dehydrierung von ** Wassergefährdend! Kupferoxid R-Sätze: 22-50/53 S-Sätze: 22-61 Wasserstoff R-Sätze: 12 S-Sätze: 9-16-33 wird in einem Rundkolben erhitzt. Die Dämpfe werden über erhitzte Kupferspäne
Dehydrierung von ** Wassergefährdend! Kupferoxid R-Sätze: 22-50/53 S-Sätze: 22-61 Wasserstoff R-Sätze: 12 S-Sätze: 9-16-33 wird in einem Rundkolben erhitzt. Die Dämpfe werden über erhitzte Kupferspäne
Europäisches Patentamt 1 1 European Patent Office Office europeen des brevets (11) EP 0 704 960 A1
 (19) (12) Europäisches Patentamt 1 1 European Patent Office Office europeen des brevets (11) EP 0 704 960 A1 EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: igstag: (51) mt. ci.6: H02N 2/04, H01
(19) (12) Europäisches Patentamt 1 1 European Patent Office Office europeen des brevets (11) EP 0 704 960 A1 EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: igstag: (51) mt. ci.6: H02N 2/04, H01
Lehrbuch Chemische Technologie
 C. Herbert Vogel Lehrbuch Chemische Technologie Grundlagen Verfahrenstechnischer Anlagen WILEY- VCH WILEY-VCH Verlag GmbH & Co. KGaA IX Inhaltsverzeichnis 1 Einführung 1 1.1 Das Ziel industrieller Forschung
C. Herbert Vogel Lehrbuch Chemische Technologie Grundlagen Verfahrenstechnischer Anlagen WILEY- VCH WILEY-VCH Verlag GmbH & Co. KGaA IX Inhaltsverzeichnis 1 Einführung 1 1.1 Das Ziel industrieller Forschung
EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2008/50
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 2 000 27 A1 (43) Veröffentlichungstag: 10.12.2008 Patentblatt 2008/0 (1) Int Cl.: C11D 7/0 (2006.01) (21) Anmeldenummer: 08009890.8 (22) Anmeldetag: 30.0.2008
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 2 000 27 A1 (43) Veröffentlichungstag: 10.12.2008 Patentblatt 2008/0 (1) Int Cl.: C11D 7/0 (2006.01) (21) Anmeldenummer: 08009890.8 (22) Anmeldetag: 30.0.2008
Europäisches Patentamt 1 1 European Patent Office Office europeen des brevets (11) EP A1
 (19) (12) Europäisches Patentamt 1 1 European Patent Office Office europeen des brevets (11) EP 0 799 566 A1 EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: igstag: (51) nt. Cl.6: A01 K 9/00 08.10.1997
(19) (12) Europäisches Patentamt 1 1 European Patent Office Office europeen des brevets (11) EP 0 799 566 A1 EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: igstag: (51) nt. Cl.6: A01 K 9/00 08.10.1997
Klausur Technische Chemie SS 2008 Prof. M. Schönhoff // PD Dr. C. Cramer-Kellers Klausur zur Vorlesung
 Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 14.7.2008 10.00 Uhr bis 12.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit
Klausur zur Vorlesung Technische Chemie: Reaktionstechnik 14.7.2008 10.00 Uhr bis 12.00 Uhr Name, Vorname Geburtsdatum Studiengang/Semester Matrikelnummer Hinweis: Alle Ansätze und Rechenwege sind mit
Einleitung Einleitung
 Einleitung 1 1. Einleitung Oxidierte Kohlenwasserstoffe stellen eine wichtige Gruppe der chemischen Verbindungen dar, die durch direkte Nutzung oder weitere Umsetzung ein breites Anwendungsgebiet finden.
Einleitung 1 1. Einleitung Oxidierte Kohlenwasserstoffe stellen eine wichtige Gruppe der chemischen Verbindungen dar, die durch direkte Nutzung oder weitere Umsetzung ein breites Anwendungsgebiet finden.
Dihydridotetrakis(triphenylphosphino)ruthenium(II)
 Illumina-Chemie.de - Artikel Synthesen (RuH2(PPh3)4) Die Synthese des RuH2(PPh3)4 ist weitaus günstiger, als den Komplex zu kaufen, da bei der rechnerisch selben Masse an Ruthenium der Komplex beinahe
Illumina-Chemie.de - Artikel Synthesen (RuH2(PPh3)4) Die Synthese des RuH2(PPh3)4 ist weitaus günstiger, als den Komplex zu kaufen, da bei der rechnerisch selben Masse an Ruthenium der Komplex beinahe
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Salpetersäure. Herstellung und Bedeutung. von
 Salpetersäure Herstellung und Bedeutung von Patrick Götte Stefan Jovanovic Salpetersäure Herstellung und Bedeutung Salpetersäure und deren Eigenschaften Geschichtliches Herstellung Bedeutung / Verwendung
Salpetersäure Herstellung und Bedeutung von Patrick Götte Stefan Jovanovic Salpetersäure Herstellung und Bedeutung Salpetersäure und deren Eigenschaften Geschichtliches Herstellung Bedeutung / Verwendung
Lehrveranstaltung: Chemische Prozesstechnik (CPT)
 Lehrveranstaltung: Chemische Prozesstechnik (CPT) Semester: Projektkurs: 1. Semester (Sommersemester) CEN Vorlesung: 3h ECTS: 5 Dozenten: Unterrichtssprache: Voraussetzungen: 2h Prof. Dr. A. König, Prof.
Lehrveranstaltung: Chemische Prozesstechnik (CPT) Semester: Projektkurs: 1. Semester (Sommersemester) CEN Vorlesung: 3h ECTS: 5 Dozenten: Unterrichtssprache: Voraussetzungen: 2h Prof. Dr. A. König, Prof.
Chloro(salen*)mangan(III)
 Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
*DE U *
 (19) *DE202016100527U120160421* (10) DE 20 2016 100 527 U1 2016.04.21 (12) Gebrauchsmusterschrift (21) Aktenzeichen: 20 2016 100 527.2 (22) Anmeldetag: 03.02.2016 (47) Eintragungstag: 10.03.2016 (45) Bekanntmachungstag
(19) *DE202016100527U120160421* (10) DE 20 2016 100 527 U1 2016.04.21 (12) Gebrauchsmusterschrift (21) Aktenzeichen: 20 2016 100 527.2 (22) Anmeldetag: 03.02.2016 (47) Eintragungstag: 10.03.2016 (45) Bekanntmachungstag
Experiment mit Feinplatin (999,5) und Wasserstoff (H²)
 Experiment mit Feinplatin (999,5) und Wasserstoff (H²) Grundinfo: http://dewikipediaorg/wiki/platin 17062012 ein Auszug daraus: Katalytische Eigenschaften Sowohl Wasserstoff, Sauerstoff als auch andere
Experiment mit Feinplatin (999,5) und Wasserstoff (H²) Grundinfo: http://dewikipediaorg/wiki/platin 17062012 ein Auszug daraus: Katalytische Eigenschaften Sowohl Wasserstoff, Sauerstoff als auch andere
1. Teilprüfung (30 P) - Gruppe A
 Chemisches Grundpraktikum IIB (270062) und Spezielle Synthesechemie (270222) W2016 24.10.2016 1. Teilprüfung (30 P) - Gruppe A NAME: Vorname: Matrikel Nr.: Bitte alle Fragen möglichst an dem dafür vorgesehenen
Chemisches Grundpraktikum IIB (270062) und Spezielle Synthesechemie (270222) W2016 24.10.2016 1. Teilprüfung (30 P) - Gruppe A NAME: Vorname: Matrikel Nr.: Bitte alle Fragen möglichst an dem dafür vorgesehenen
(51) Int Cl.: A23C 1/04 ( ) A23C 9/142 ( ) A23C 21/00 ( ) A23J 1/20 ( ) A23J 3/08 ( )
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 878 349 A1 (43) Veröffentlichungstag: 16.01.2008 Patentblatt 2008/03 (21) Anmeldenummer: 06012916.0 (51) Int Cl.: A23C 1/04 (2006.01) A23C 9/142 (2006.01)
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 878 349 A1 (43) Veröffentlichungstag: 16.01.2008 Patentblatt 2008/03 (21) Anmeldenummer: 06012916.0 (51) Int Cl.: A23C 1/04 (2006.01) A23C 9/142 (2006.01)
4. Zusammenfassung 116
 4. Zusammenfassung 116 =XVDPPHQIDVVXQJ Die vorliegende Arbeit beschreibt die Synthese homoleptischer E(PH 2 ) 4 -Verbindungen (E = Si (), Ge ()). Es konnten außerdem neue Beiträge zur Chemie von Al-P-Verbindungen
4. Zusammenfassung 116 =XVDPPHQIDVVXQJ Die vorliegende Arbeit beschreibt die Synthese homoleptischer E(PH 2 ) 4 -Verbindungen (E = Si (), Ge ()). Es konnten außerdem neue Beiträge zur Chemie von Al-P-Verbindungen
*DE A *
 (19) *DE102015009266A120170119* (10) DE 10 2015 009 266 A1 2017.01.19 (12) Offenlegungsschrift (21) Aktenzeichen: 10 2015 009 266.9 (22) Anmeldetag: 15.07.2015 (43) Offenlegungstag: 19.01.2017 (71) Anmelder:
(19) *DE102015009266A120170119* (10) DE 10 2015 009 266 A1 2017.01.19 (12) Offenlegungsschrift (21) Aktenzeichen: 10 2015 009 266.9 (22) Anmeldetag: 15.07.2015 (43) Offenlegungstag: 19.01.2017 (71) Anmelder:
Europäisches Patentamt European Patent Office Veröffentlichungsnummer: Office europeen des brevets EUROPÄISCHE PATENTANMELDUNG
 Europäisches Patentamt European Patent Office Veröffentlichungsnummer: 0 022 880 Office europeen des brevets A1 EUROPÄISCHE PATENTANMELDUNG Anmeldenummer: 79102545.5 Int. CI.3:C 07 C 99/12 Anmeldetag:
Europäisches Patentamt European Patent Office Veröffentlichungsnummer: 0 022 880 Office europeen des brevets A1 EUROPÄISCHE PATENTANMELDUNG Anmeldenummer: 79102545.5 Int. CI.3:C 07 C 99/12 Anmeldetag:
EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2011/38
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 2 366 294 A1 (43) Veröffentlichungstag: 21.09.2011 Patentblatt 2011/38 (51) Int Cl.: A23L 1/304 (2006.01) A23L 2/52 (2006.01) (21) Anmeldenummer: 10405051.3
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 2 366 294 A1 (43) Veröffentlichungstag: 21.09.2011 Patentblatt 2011/38 (51) Int Cl.: A23L 1/304 (2006.01) A23L 2/52 (2006.01) (21) Anmeldenummer: 10405051.3
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Nr. Aufgabe Pkt. 2.2 Erklären Sie die ungewöhnliche Stabilität aromatischer Systeme gegenüber Additionsversuchen!
 aromatische Kohlenwasserstoffe Jahrgang Index Nr. Aufgabe Pkt 15/IV 1 o-bromtoluol soll aus Benzol, Methan und Brom mit geeigneten Katalysatoren hergestellt werden. Beschreiben Sie unter Verwendung von
aromatische Kohlenwasserstoffe Jahrgang Index Nr. Aufgabe Pkt 15/IV 1 o-bromtoluol soll aus Benzol, Methan und Brom mit geeigneten Katalysatoren hergestellt werden. Beschreiben Sie unter Verwendung von
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol
 Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
V 1 Herstellung von Natriumchlorid
 1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
Darstellung von Malachitgrün Präparat 5
 Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Ammoniaksynthese. Erstellt von Daniel Flanz und Paul Fehren
 Ammoniaksynthese Erstellt von Daniel Flanz und Paul Fehren Inhaltsverzeichnis Geschichte der Ammoniaksynthese Eigenschaften von Ammoniak Herstellungsverfahren Haber-Bosch-Verfahren Alternativen Schwachpunkte
Ammoniaksynthese Erstellt von Daniel Flanz und Paul Fehren Inhaltsverzeichnis Geschichte der Ammoniaksynthese Eigenschaften von Ammoniak Herstellungsverfahren Haber-Bosch-Verfahren Alternativen Schwachpunkte
*DE A *
 (19) *DE102016005739A120170105* (10) (12) Offenlegungsschrift (21) Aktenzeichen: 10 2016 005 739.4 (22) Anmeldetag: 10.05.2016 (43) Offenlegungstag: 05.01.2017 (71) Anmelder: Daimler AG, 70327 Stuttgart,
(19) *DE102016005739A120170105* (10) (12) Offenlegungsschrift (21) Aktenzeichen: 10 2016 005 739.4 (22) Anmeldetag: 10.05.2016 (43) Offenlegungstag: 05.01.2017 (71) Anmelder: Daimler AG, 70327 Stuttgart,
Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2
![Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2](/thumbs/95/126253543.jpg) Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)
 Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... zeigen Vor- und Nachteile ausgewählter Produkte des Alltags (u.a. Aromastoffe, Alkohole) und ihre Anwendung auf, gewichten diese und beziehen
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... zeigen Vor- und Nachteile ausgewählter Produkte des Alltags (u.a. Aromastoffe, Alkohole) und ihre Anwendung auf, gewichten diese und beziehen
TEPZZ 8Z _A_T EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2017/03
 (19) TEPZZ 8Z _A_T (11) EP 3 118 021 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 18.01.17 Patentblatt 17/03 (21) Anmeldenummer: 16177908.7 (1) Int Cl.: B60C /00 (06.01) B60C /04 (06.01)
(19) TEPZZ 8Z _A_T (11) EP 3 118 021 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 18.01.17 Patentblatt 17/03 (21) Anmeldenummer: 16177908.7 (1) Int Cl.: B60C /00 (06.01) B60C /04 (06.01)
Zeolithe. Was sind sie? Wozu werden sie verwendet?
 Folie 1 Zeolithe Was sind sie? Wozu werden sie verwendet? Folie 2... im Feuer vor dem Lötröhrchen wallet und schäumet fast wie Borax". Zeolithe wurden vor zweihundert Jahren entdeckt als ein Mineral, das
Folie 1 Zeolithe Was sind sie? Wozu werden sie verwendet? Folie 2... im Feuer vor dem Lötröhrchen wallet und schäumet fast wie Borax". Zeolithe wurden vor zweihundert Jahren entdeckt als ein Mineral, das
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie
 Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
Darstellung von Silber(I)tetrafluoroborat(III) Ag[BF 4 ]
![Darstellung von Silber(I)tetrafluoroborat(III) Ag[BF 4 ] Darstellung von Silber(I)tetrafluoroborat(III) Ag[BF 4 ]](/thumbs/67/57250696.jpg) Darstellung von Silber(I)tetrafluoroborat(III) Ag[BF 4 ] Andreas J. Wagner, Philipp von den Hoff 26. Juli 2004 1 Theorie Das Tetrafluoroborat-Anion [BF 4 ] gehört zu der Familie der sog. nichtkoordinierenden
Darstellung von Silber(I)tetrafluoroborat(III) Ag[BF 4 ] Andreas J. Wagner, Philipp von den Hoff 26. Juli 2004 1 Theorie Das Tetrafluoroborat-Anion [BF 4 ] gehört zu der Familie der sog. nichtkoordinierenden
Herstellung und Oxidation von 2,4,6-Tri-tert-butylphenol
 2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
(51) Int Cl.: A23L 1/0522 ( ) A23L 1/09 ( ) A23L 1/24 ( ) A23L 2/60 ( ) A23G 3/48 ( ) A23G 3/42 (2006.
 (19) (12) EUROPÄISCHE PATENTANMELDUNG TEPZZ _ 8Z5ZA_T (11) EP 2 138 050 A1 (43) Veröffentlichungstag: 30.12.2009 Patentblatt 2009/53 (21) Anmeldenummer: 09008250.4 (51) Int Cl.: A23L 1/0522 (2006.01) A23L
(19) (12) EUROPÄISCHE PATENTANMELDUNG TEPZZ _ 8Z5ZA_T (11) EP 2 138 050 A1 (43) Veröffentlichungstag: 30.12.2009 Patentblatt 2009/53 (21) Anmeldenummer: 09008250.4 (51) Int Cl.: A23L 1/0522 (2006.01) A23L
*DE A *
 (19) *DE102015114714A120170309* (10) (12) Offenlegungsschrift (21) Aktenzeichen: 10 2015 114 714.9 (22) Anmeldetag: 03.09.2015 (43) Offenlegungstag: 09.03.2017 (71) Anmelder: Hoesch Schwerter Extruded
(19) *DE102015114714A120170309* (10) (12) Offenlegungsschrift (21) Aktenzeichen: 10 2015 114 714.9 (22) Anmeldetag: 03.09.2015 (43) Offenlegungstag: 09.03.2017 (71) Anmelder: Hoesch Schwerter Extruded
4.3 Reaktionsgeschwindigkeit und Katalysator
 4.3 Reaktionsgeschwindigkeit und Katalysator Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Einstellung des Gleichgewichts,
4.3 Reaktionsgeschwindigkeit und Katalysator Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Einstellung des Gleichgewichts,
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Entwicklung eines mikrostrukturierten Membranreaktors zur Direkt- Hydroxylierung von Aromaten mit Gasphase-Sauerstoff
 Entwicklung eines mikrostrukturierten Membranreaktors zur Direkt- Hydroxylierung von Aromaten mit Gasphase-Sauerstoff Laufzeit: 01.04.2007-31.03.2010 Geldgeber: DFG (Deutsche Forschungsgemeinschaft) Bearbeiter:
Entwicklung eines mikrostrukturierten Membranreaktors zur Direkt- Hydroxylierung von Aromaten mit Gasphase-Sauerstoff Laufzeit: 01.04.2007-31.03.2010 Geldgeber: DFG (Deutsche Forschungsgemeinschaft) Bearbeiter:
Dritte Klausur zur Vorlesung Grundlagen der Organischen Chemie
 Prof. Dr. Jens Christoffers 10. März 2008 Universität Oldenburg Dritte Klausur zur Vorlesung Grundlagen der Organischen Chemie (für Studierende der Chemie ist dies die zweite Klausur, für Umweltwissenschaftler
Prof. Dr. Jens Christoffers 10. März 2008 Universität Oldenburg Dritte Klausur zur Vorlesung Grundlagen der Organischen Chemie (für Studierende der Chemie ist dies die zweite Klausur, für Umweltwissenschaftler
(51) Int Cl. 7 : C07C 45/52, C07C 49/12
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP0013476B1* (11) EP 1 3 476 B1 (12) EUROPÄISCHE PATENTSCHRIFT (4) Veröffentlichungstag und Bekanntmachung des Hinweises
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP0013476B1* (11) EP 1 3 476 B1 (12) EUROPÄISCHE PATENTSCHRIFT (4) Veröffentlichungstag und Bekanntmachung des Hinweises
Abschlussklausur Anorganische Chemie für Geowissenschaftler II Modul BGEO2.5.1
 Abschlussklausur Anorganische Chemie für Geowissenschaftler II Modul BGEO2.5.1 Name, Vorname:... MatrikelNr.:... 1. Bei der Anionenanalyse (Analyse 4) gab es eine wichtige Vorprobe, nämlich die Probe darauf,
Abschlussklausur Anorganische Chemie für Geowissenschaftler II Modul BGEO2.5.1 Name, Vorname:... MatrikelNr.:... 1. Bei der Anionenanalyse (Analyse 4) gab es eine wichtige Vorprobe, nämlich die Probe darauf,
(51) Int Cl.: B23K 26/14 ( ) B23K 26/42 ( ) B23K 26/00 ( ) C21D 1/09 ( ) C21D 9/46 ( )
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 842 617 A1 (43) Veröffentlichungstag: 10.10.2007 Patentblatt 2007/41 (21) Anmeldenummer: 07105507.3 (51) Int Cl.: B23K 26/14 (2006.01) B23K 26/42 (2006.01)
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 842 617 A1 (43) Veröffentlichungstag: 10.10.2007 Patentblatt 2007/41 (21) Anmeldenummer: 07105507.3 (51) Int Cl.: B23K 26/14 (2006.01) B23K 26/42 (2006.01)
Europäisches Patentamt European Patent Office Office europeen des brevets. Veröffentlichungsnummer: 0 290 905 A1 EUROPAISCHE PATENTANMELDUNG
 Europäisches Patentamt European Patent Office Office europeen des brevets Veröffentlichungsnummer: 0 290 905 A1 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 88107012.2 Anmeldetag: 02.05.88 int. ci.4: C07C
Europäisches Patentamt European Patent Office Office europeen des brevets Veröffentlichungsnummer: 0 290 905 A1 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 88107012.2 Anmeldetag: 02.05.88 int. ci.4: C07C
EP A2 (19) (11) EP A2 (12) EUROPÄISCHE PATENTANMELDUNG. (51) Int Cl.: C01B 3/36 ( ) C01B 3/38 ( ) C01B 3/48 (2006.
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 84 063 A2 (43) Veröffentlichungstag: 17..07 Patentblatt 07/42 (21) Anmeldenummer: 070069.4 (1) Int Cl.: C01B 3/36 (06.01) C01B 3/38 (06.01) C01B 3/48 (06.01)
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 84 063 A2 (43) Veröffentlichungstag: 17..07 Patentblatt 07/42 (21) Anmeldenummer: 070069.4 (1) Int Cl.: C01B 3/36 (06.01) C01B 3/38 (06.01) C01B 3/48 (06.01)
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
FRAUNHOFER-INSTITUT FÜR. Produkte aus nachwachsenden Rohstoffen
 FRAUNHOFER-INSTITUT FÜR Chemische Technologie ICT Produkte aus nachwachsenden Rohstoffen Produkte aus nachwachsenden Rohstoffen Vor dem Hintergrund einer rasant wachsenden Weltbevölkerung und knapper werdender
FRAUNHOFER-INSTITUT FÜR Chemische Technologie ICT Produkte aus nachwachsenden Rohstoffen Produkte aus nachwachsenden Rohstoffen Vor dem Hintergrund einer rasant wachsenden Weltbevölkerung und knapper werdender
Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on
 Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Sauerstoffzuleitung Widerstandsheizung Quarzrohr Wafer in Carrier. Bubblergefäß mit Wasser (~95 C) Abb. 1.1: Darstellung eines Oxidationsofens
 1 Oxidation 1.1 Erzeugung von Oxidschichten 1.1.1 Thermische Oxidation Bei der thermischen Oxidation werden die Siliciumwafer bei ca. 1000 C in einem Oxidationsofen oxidiert. Dieser Ofen besteht im Wesentlichen
1 Oxidation 1.1 Erzeugung von Oxidschichten 1.1.1 Thermische Oxidation Bei der thermischen Oxidation werden die Siliciumwafer bei ca. 1000 C in einem Oxidationsofen oxidiert. Dieser Ofen besteht im Wesentlichen
*DE A *
 (19) *DE102015208388A120161110* (10) DE 10 2015 208 388 A1 2016.11.10 (12) Offenlegungsschrift (21) Aktenzeichen: 10 2015 208 388.8 (22) Anmeldetag: 06.05.2015 (43) Offenlegungstag: 10.11.2016 (71) Anmelder:
(19) *DE102015208388A120161110* (10) DE 10 2015 208 388 A1 2016.11.10 (12) Offenlegungsschrift (21) Aktenzeichen: 10 2015 208 388.8 (22) Anmeldetag: 06.05.2015 (43) Offenlegungstag: 10.11.2016 (71) Anmelder:
PATENTANMELDUNG. int. Ci.5; C07C 53/08, C07C 53/12, C07C 51/12, C07C 51/56
 Europäisches Patentamt European Patent Office Office europeen des brevets Veröffentlichungsnummer: 0 476 333 A2 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 91113958.2 @ Anmeldetag: 21.08.91 int. Ci.5; C07C
Europäisches Patentamt European Patent Office Office europeen des brevets Veröffentlichungsnummer: 0 476 333 A2 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 91113958.2 @ Anmeldetag: 21.08.91 int. Ci.5; C07C
Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen. c(a) t. v = -
 REAKTIONSKINETIK 1 Reaktionskinetik Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen Anwendung: - Vorgänge in den lebenden Organismen
REAKTIONSKINETIK 1 Reaktionskinetik Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen Anwendung: - Vorgänge in den lebenden Organismen
Anorganische Chemie Martin Schwiertz Helena Wagenleitner
 Müller- Rochow- Synthese Anorganische Chemie Martin Schwiertz Helena Wagenleitner Inhaltsverzeichnis Einleitung Synthese Durchführung Reaktion und Reaktionsprodukte Durchschnittliche Produktverteilung
Müller- Rochow- Synthese Anorganische Chemie Martin Schwiertz Helena Wagenleitner Inhaltsverzeichnis Einleitung Synthese Durchführung Reaktion und Reaktionsprodukte Durchschnittliche Produktverteilung
*DE A *
 (19) *DE102015000566A120160721* (10) (12) Offenlegungsschrift (21) Aktenzeichen: 10 2015 000 566.9 (22) Anmeldetag: 17.01.2015 (43) Offenlegungstag: 21.07.2016 (71) Anmelder: AUDI AG, 85045 Ingolstadt,
(19) *DE102015000566A120160721* (10) (12) Offenlegungsschrift (21) Aktenzeichen: 10 2015 000 566.9 (22) Anmeldetag: 17.01.2015 (43) Offenlegungstag: 21.07.2016 (71) Anmelder: AUDI AG, 85045 Ingolstadt,
Das Chemische Gleichgewicht
 Das Chemische Gleichgewicht 2 Ein chemisches Gleichgewicht herrscht dann, wenn Hin- sowie Rückreaktion gleich schnell ablaufen. Die Reaktionsgeschwindigkeit der Gesamtreaktion erscheint daher gleich null,
Das Chemische Gleichgewicht 2 Ein chemisches Gleichgewicht herrscht dann, wenn Hin- sowie Rückreaktion gleich schnell ablaufen. Die Reaktionsgeschwindigkeit der Gesamtreaktion erscheint daher gleich null,
*EP A1* EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2002/18
 (19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001201165A1* (11) EP 1 201 165 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 02.05.2002 Patentblatt 2002/18
(19) Europäisches Patentamt European Patent Office Office européen des brevets *EP001201165A1* (11) EP 1 201 165 A1 (12) EUROPÄISCHE PATENTANMELDUNG (43) Veröffentlichungstag: 02.05.2002 Patentblatt 2002/18
Lösungen 3. Übungsblatt SS 2002
 Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Organostickstoff- Verbindungen
 rganostickstoff- Verbindungen [1] Chiralität von Aminen [2] -Enantiomere Isomerisieren sehr schnell -E A 20-30 KJ/mol [2] Alkylierung von Ammoniak [2] [2] [2] -geringe Selektivität aufgrund von Mehrfachalkylierung
rganostickstoff- Verbindungen [1] Chiralität von Aminen [2] -Enantiomere Isomerisieren sehr schnell -E A 20-30 KJ/mol [2] Alkylierung von Ammoniak [2] [2] [2] -geringe Selektivität aufgrund von Mehrfachalkylierung
EP A1 (19) (11) EP A1 (12) EUROPÄISCHE PATENTANMELDUNG. (43) Veröffentlichungstag: Patentblatt 2007/01
 (19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 739 251 A1 (43) Veröffentlichungstag: 03.01.2007 Patentblatt 2007/01 (51) Int Cl.: E04F 13/16 (2006.01) E04F 13/02 (2006.01) (21) Anmeldenummer: 05019206.1
(19) (12) EUROPÄISCHE PATENTANMELDUNG (11) EP 1 739 251 A1 (43) Veröffentlichungstag: 03.01.2007 Patentblatt 2007/01 (51) Int Cl.: E04F 13/16 (2006.01) E04F 13/02 (2006.01) (21) Anmeldenummer: 05019206.1
uril Illumina-Chemie.de - Artikel (Cucurbituril, CB6, CB[6])
![uril Illumina-Chemie.de - Artikel (Cucurbituril, CB6, CB[6]) uril Illumina-Chemie.de - Artikel (Cucurbituril, CB6, CB[6])](/thumbs/88/114540367.jpg) Illumina-Chemie.de - Artikel Synthesen uril (, CB6, CB[6]) Cucurbit[6]uril (CB[6]) ist ein makrocyclisches Molekül, das aus 6 Glycoluril-Einheiten aufgebaut ist, die über 12 Methylenbrücken an den Stickstoffatomen
Illumina-Chemie.de - Artikel Synthesen uril (, CB6, CB[6]) Cucurbit[6]uril (CB[6]) ist ein makrocyclisches Molekül, das aus 6 Glycoluril-Einheiten aufgebaut ist, die über 12 Methylenbrücken an den Stickstoffatomen
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13
 Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
