Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert
|
|
|
- Rudolf Armbruster
- vor 7 Jahren
- Abrufe
Transkript
1 Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert A04 Atomspektren (Pr_PhII_A04_Atomspektren_7, ) 1.. Name Matr. Nr. Gruppe Team Protokoll ist ok O Datum Abtestat Folgende Korrekturen nötig O
2 Hinweis Lesen Sie die Versuchsanleitung (inkl. Versuchsdurchführung & Auswertung!) gründlich durch und machen sich mit den Begrifflichkeiten vertraut. Die Teilnahme am Praktikum erfordert das erfolgreiche Beantworten der Zulassungsfragen am Versuchstag (siehe Anleitung) oder alternativ eine kurze Vorstellung eines Themengebietes an der Tafel. 1. Ziel Mit dem Verständnis der Atome und des Lichtes im letzten Jahrhundert wurde nicht nur das Weltbild der Physik und Chemie revolutioniert, sondern es sind entscheidende technologische Entwicklungen gemacht worden, die unser heutiges Leben prägen. In diesem Praktikum wollen wir die damals wesentlichen Erkenntnis-Schritte nachzeichen und uns mit den Grundzügen der Wechselwirkung zwischen Licht und Atomen beschäftigen. Dabei lernen wir einfache Spektrometer kennen, wie sie zur Gasanalyse in der Umwelttechnik oder zur Materialanalyse genutzt werden..theorie.1 Atomspektren Werden Atome z.b. durch Elektronenstoß angeregt, so senden sie Licht aus. Für jedes Element gibt es dabei charakteristische Spektren, die nur bestimmte Wellenlängen besitzen und somit wie ein Fingerabdruck für das entsprechende Element sind. Andererseits absorbiert jedes Atom nur Licht mit elementspezifischen Linien, d.h. diskrete Wellenlängen. Beide Phänomene bilden die Grundlage zur eindeutigen Bestimmung der Atome eines unbekannten Gases oder eines Materials. Die entscheidende Frage ist nun: wie hängen Atomaufbau und Lichtemission / Absorption zusammen?.1.1 Planetenmodell Nach dem Planetenmodell der Atome bewegen sich die Elektronen der Ladung e und der Masse m mit Geschwindigkeit v auf Kreisbahnen (Radius r) um den positiv geladenen Kern. Die Zentrifugalkraft F Z und die elektrostatische Coulombkraft F C halten sich die Waage. Die gesamte Energie E des Elektrons setzt sich aus kinetischer und potenzieller Energie im elektrischen Feld des Kerns zusammen. Dieses Planetenmodell hatte eine große Schwäche: nach ihm dürften Atome gar nicht existieren, denn das rotierende, und damit beschleunigte Elektron müsste elektromagnetische Strahlung emittieren, dadurch Energie verlieren und schließlich in den Kern stürzen. Bei diesem Prozess müsste es ein kontinuierliches Spektrum emittieren. Beides passiert aber nicht!.1. Bohrsches Atommodell Diese Probleme überwand Niels Bohr 1911 indem, er einfach zwei Postulate aufstellte, auch wenn er ihren Ursprung noch nicht erklären konnte: Im Atom gibt es nur diskrete Bahnen, auf denen die Elektronen strahlungsfrei kreisen können. Der Drehimpuls L = mvr kann nur gequantelte Werte mit n = 1,, 3, annehmen, wobei h = 6,6x10-34 Js das Plancksche Wirkungsquantum ist h (1) L n (1. Bohrsches Postulat)
3 Die Werte n heißen Hauptquantenzahlen. Ändert das Elektron seinen Abstand zum Kern, so kann es nicht jede Bahn annehmen, sondern muß die Bedingung (1) erfüllen. Nur beim Wechsel von einer Bahn n zur Bahn m wird Energie ΔE mn benötigt oder frei gesetzt, meist in Form von Lichtteilchen (Photonen) mit der Frequenz f mn : () Emn Em En hf mn (. Bohrsches Postulat) Demnach kann nicht Licht beliebiger Wellenlänge λ mn = c/f mn absorbiert oder emittiert werden, sondern nur bestimmte (diskrete) Werte mit den Quantenzahlen n, m sind möglich..1.3 Atomspektren Aus dem Kräftegleichgewicht und dem Bohrschen Postulat (Gl. 1) lassen sich nun die erlaubten Bahnradien für das Wasserstoffatom berechnen zu (3) h 0 r n n. e m Im nichtangeregten Grundzustand bewegt sich das Elektron auf der Bahn mit der Hauptquantenzahl n = 1 mit dem kleinsten Radius r 1 = 0,53 x m. Die Energie des Elektrons auf der Bahn n berechnet sich damit zu 4 me 1 1 (4) E n 13,6eV 8 h n n 0 Die Energiewerte einer Bahn mit beliebger Quantenzahl n sind negativ (gebundener Zustand) und sie skalieren mit E n ~ 1 n (siehe Abb. 1). Im Grundzustand n 1 beträgt die Bindungsenergie des Eletrons 19 E1 13, 6eV, mit 1eV 1,6 10 J. Mit wachsendem n laufen die Energieniveaus gegen Null und die Energieabstände im Termschema werden immer enger (siehe Abb.). Um das H Atom aus dem Grundzustand in den ersten angeregten Zustand ( n ) zu bringen, muss ein Photon hf E E 13,6eV 1 1 absorbiert werden. Um mit der passenden Energiedifferenz das Atom zu ionisieren, muss das Photon mindestens die Bindungsenergie des Grundzustandes überwinden, also hf hf (5) hf1 E E1 13,6eV 13, 6eV 1. Nun ist das Elektron vollständig aus der Bin-dung gelöst und besitzt positive Energie in Form kinetischer Energie, die nicht mehr quantisiert ist. Man sagt es befindet sich im Kontinuum. Wird das Elektron wieder vom ionisierten H Atom eingefangen, so kann es auf verschiedenen Wegen und Zwischenschrit-ten in den Grundzustand zurückkehren. Dabei wird bei jedem Übergang vom höherener-getischen Niveau m in das tieferenergetische Niveau n die Energiedifferenz in Form eines Photons emittiert (Gl. ) 1 1 (6) hf, m 13,6eV m n n. In der Spektroskopie verwendet man oft die Darstellung in Wellenzahlen 1 Ry1 m n mit der Rydbergkonstante Ry 1, m 1 3 n, m 1. Die Gesamtheit der möglichen Photonenenergien
4 bzw. Wellenlängen nennt man Spektrum. Da die Energieniveaus quantisiert sind, müssen es auch die Photonenenergien sein. Deshalb zeigen Atome kein kontinuierliches, sondern ein Linienspektrum. Es kann auf zwei Wegen experimentell bestimmt werden und zwar in Absorption oder in Emission. Bei der Emissionsmessung werden in einer Entladungslampe die Atome des Wasserstoffgases durch Elektronenstoß angeregt (ionisiert). Bei der Relaxation in den Grundzustand emittieren die Atome Licht, dessen Wellenlänge mittels Monochromator (Spektrometer) gemessen wird. Bei der Absorptionsmessung wird Licht mit einem kontinuierlichen (weißen) Spektrum durch eine Zelle mit Wasserstoffgas geschickt. Mit einem Monochromator hinter der Zelle werden die im Spektrum fehlenden Wellenlängen bestimmt. Die Linien können in beiden Fällen zu Serien zusammengefasst werden, je nachdem, in welchem Zustand die Elektronenübergänge enden. Die Linien der Lyman Serie entspringen Übergängen in den Grundzustand n = 1. Die Linie kleinster Energie wird durch den Übergang m n 1 erzeugt. Die nächste Linie durch m 3 n 1 usw. Beachte: die Spektrallinien selber sind noch nicht die Energiewerte des H Atoms, sondern diese müssen mittels Gl. 8 durch Kombination passender Paare von m, n extrahiert werden. Die Linien der Lyman Serie liegen im UV Bereich. Dagegen liegen die Linien der Balmer Serie ( m n ) im sichtbaren Spektralbereich. Die Linien der Paschen Serie ( m n 3) liegen im Infrarotbereich. Die entsprechende Energieberechnung für Atome mit mehreren Elektronen gestaltet sich deutlich schwieriger, da auch die Wechselwirkung der Elektronen untereinander berücksichtigt werden muss. Vernachlässigen wir diesen Aspekt aber, so ist nur das mit der Ordnungszahl Z steigende Kernpotenzial zu berücksichtigen. Als sehr grobe Näherung erhalten wir für die Energiewerte eines Elementes mit Kernladungszahl Z statt Gl. 5 die Gleichung 13,6eV Z n. Damit besitz jedes Element sein individuelles Termschema, und seine individuelle Rydbergenergie ( Z 13,6eV ), das mit Gl. 6 zu einem individuellen Spektrum führt, ähnlich einem Fingerabdruck. Durch die Spektralanalyse eines unbekannten Gases oder Sterns können so die enthaltenen Elemente eindeutig identifiziert werden.. Spektrometer Abb.1 Wasserstoffspektrum E n 4
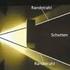
5 Die Untersuchung der atomaren Spektrallinien erfolgt mit dem Gitterspektrometer, das wir in einem früheren Praktikum kennengelernt haben. Unter einem bestimmten Beobachtungswinkel θ sind die Spektrallinien zu erkennen. Emitiert die Lichtquelle ein Kontinuierliches Spektrum (Temperaturstrahler), erscheinen hinter dem Beugungsgitter keine diskreten Linien, sondern eine kontinuierliche Farbverteilung ( Regenbogen )..3 Entladungslampen (Spektrallampen) Die im Praktikum verwendeten intensiven Lichtquellen sind Entladungslampen. Ein mit Gas eines bestimmten Drucks gefülltes Glasrohr besitzt an den äußeren Enden je eine Elektrode. Wird zwischen diese beiden eine Spannung im kv-bereich angelegt, so werden die wenigen, natürlich vorhandenen freien Ladungsträger beschleunigt. Durch Stöße geben die im E-Feld der Entladungsröhre beschleunigten Ladungsträger ihrer kinetischen Energie an die Gasatome ab und regen diese zum Leuchten an. Diese Energieaufnahme erfolgt indem die gebundene Elektronen der Atome in energetisch höher gelegene Schalen angehoben werden. Ist die kinetische Energie groß genug, so können die Gasatome sogar ionisiert werden und tragen zusätzlich zu weiteren Stoßprozessen bei. So bildet sich eine Kaskade von beschleunigten Ladungen. Die ionisierten Atome können danach durch Einfang freier Elektronen und Rekombination dieser in tiefere Schalen Licht emittieren. Die dabei emittierten Spektrallinien folgen aus den charakteristischen Übergänge im Atom und werden im Praktikum untersucht. Fragen zur Zulassung Welche physikalischen Möglichkeiten gibt es, Licht zu erzeugen? Was bedeutet der Begriff monochromatisch? Was ist der Unterschied zwischen einem Atomspektrum und einem Temperaturspektrum? Zeichnen Sie das Termschema von Wasserstoff. Was sind die Spektral-Linien? Wie funktioniert eine Gasentladungslampe? Wie funktioniert eine Glühlampe? Wie funktioniert eine Spektralanalyse? Was ist ein Monochromator und wie funktioniert er? Erklären Sie die Begriffe Absorption und Emission. 5
6 3. Durchführung 3.0 Justieren Sie die Entladungslampe direkt vor dem Eingangsspalt des Goniometers. Suchen Sie die Spektrallinien indem Sie das Fernrohr hinter dem Gitter je auf die pos. und neg. erste Ordnung m = +/-1 schwenken. Damit bestimmen Sie den Nullwinkel (Nullte Ordnung m = 0), auf den die Beugungswinkel der Spektrallinien später bezogen werden. Schätzen Sie den Winkelfehler ab. 3.1 Beleuchten Sie indirekt den Eintritt des Spektrometers mit dem Laser (Papierstück anleuchten, Betreuer fragen!). Messen Sie die Beugungswinkel incl. Genauigkeit und Beugungsordnungen m i und notieren Sie die Laserwellenlänge incl. Genauigkeit, um daraus die Gitterkonstante zu bestimmen. Schauen Sie nie in den Laserstrahl! 3. Beobachten Sie die Spektren der unten aufgelisteten Lichtquellen und Vermessen sie die Beugungswinkel und Beugungsordnung m der auftretenden Spektrallinien und notieren Sie: Farbe, Beugungswinkel, relative Intensität der Spekrallinien Lichtquellen: Na-, Hg-, H-Entladungslampe, Glühlampe, Halogenlampe. Zum Wechsel der Entladungslampe Spannungsquelle auf Null regeln, Betreuer fragen! Nie die Lampe mit Fingern berühren! 3.3 Untersuchen Sie mit dem Handspektrometer qualitativ das Spektrum a) von Leuchtstoffröhren (Deckenbeleuchtung). b) des Sonnenlichtes (nicht direkt in die Sonne schauen!). 3.4 Ermitteln Sie mit dem Gitterspektrometer den Abstand der beiden eng benachbarten D-Linien der Na-Lampe. Zur Steigerung der Auflösung arbeiten Sie in höherer Ordnung. Die D-Linienaufspaltung ist eine Folge der quantenmechanischen Spin-Bahn-Wechselwirkung der Elektronen. 3.5 Untersuchen Sie mit dem Handspektrometer die Flammenfärbung von NaCl und Wunderkerzen gemeinsam mit dem anderen Team (Betreuer fragen). 6
7 4. Auswertung 4.1 Bestimmen Sie aus 3.1 die die Gitterkonstante g incl. Fehler. (Siehe Versuch O06 zur Beugung) 4. Listen Sie für jede Lichtquelle die in 3. beobachteten Spektrallinien wie folgt auf und berechnen Sie die Wellenlängen: Farbe, Beugungswinkel, berechnete Wellenlänge, relative Intensität. Geben Sie den relativen Wellenlängenfehler an. 4.3 Worin und warum unterscheiden sich die Spektren von Leuchtstoffröhre und Sonne? 4.4 Geben Sie die Spin-Bahn-Aufspaltung der D-Linien in Einheiten ev an (Umrechnung E [ev]= 140/λ). 4.5 Beschreiben Sie die spektrale Beobachtung der Flammenfärbung und versuchen Sie mit den Ergebnissen aus 3. und Literaturwerten Elemente in der Flamme zu identifizieren. 4.6 Kennzeichnen Sie die beobachteten Übergänge der Hg-Lampe im unten abgebildeten Hg- Termschemata. Das Diagramm zeigt einen Ausschnitt des Termschemas von Quecksilber. Einige der erlaubten Elektronenübergänge der äußeren Schalen sind eingetragen. Die Symbole in der Kopfzeile (z.b. 3 P 1 ) bezeichnen die sog. Multiplettzustände (nicht mit Orbitalen verwechseln!). Beachte: Quecksilber mit 80 Elektronen besitzt ein komplexeres Termschema als Wasserstoffs mit nur 1 Elektron. 7
Physikalisches Praktikum Bachelor Chemieingenieurwesen, Wirtschaftsingenieurwesen Chemietechnik MSc. M. Gilbert
 Bachelor Chemieingenieurwesen, Wirtschaftsingenieurwesen Chemietechnik MSc. M. Gilbert A01 Hg-Atomspektren Beugung am Gitter (Pr_EX_A01_Hg-Atomspektren_6, 30.8.009) 1. Name Matr. Nr. Gruppe Team. 3. Protokoll
Bachelor Chemieingenieurwesen, Wirtschaftsingenieurwesen Chemietechnik MSc. M. Gilbert A01 Hg-Atomspektren Beugung am Gitter (Pr_EX_A01_Hg-Atomspektren_6, 30.8.009) 1. Name Matr. Nr. Gruppe Team. 3. Protokoll
Physikalisches Praktikum, FH Münster Prof. Dr. H.- CH. Mertins & Dipl.-Ing. M. Gilbert
 Physikalisches Praktikum, FH Münster Prof. Dr. H.- CH. Mertins & Dipl.-Ing. M. Gilbert 7.8.008 A 01: Hg Atomspektren Beugung am Gitter Versuch Nr. (Pr_EX_A01_Hg-Atomspektren) Praktikum: FB 01 Plätze: 3
Physikalisches Praktikum, FH Münster Prof. Dr. H.- CH. Mertins & Dipl.-Ing. M. Gilbert 7.8.008 A 01: Hg Atomspektren Beugung am Gitter Versuch Nr. (Pr_EX_A01_Hg-Atomspektren) Praktikum: FB 01 Plätze: 3
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert
 Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert A02 Photoeffekt (Pr_PhII_A02_Photoeffekt_7, 24.10.2015) 1. 2. Name Matr. Nr. Gruppe Team
Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert A02 Photoeffekt (Pr_PhII_A02_Photoeffekt_7, 24.10.2015) 1. 2. Name Matr. Nr. Gruppe Team
7. Das Bohrsche Modell des Wasserstoff-Atoms. 7.1 Stabile Elektronbahnen im Atom
 phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
phys4.08 Page 1 7. Das Bohrsche Modell des Wasserstoff-Atoms 7.1 Stabile Elektronbahnen im Atom Atommodell: positiv geladene Protonen (p + ) und Neutronen (n) im Kern negative geladene Elektronen (e -
UNIVERSITÄT BIELEFELD
 UNIVERSITÄT BIELEFELD 6. Atom- und Molekülphysik 6.1 - GV Atom- und Molekülspektren Durchgeführt am 22.11.06 Dozent: Praktikanten (Gruppe 1): Dr. Udo Werner Marcus Boettiger Sarah Dirk Marius Schirmer
UNIVERSITÄT BIELEFELD 6. Atom- und Molekülphysik 6.1 - GV Atom- und Molekülspektren Durchgeführt am 22.11.06 Dozent: Praktikanten (Gruppe 1): Dr. Udo Werner Marcus Boettiger Sarah Dirk Marius Schirmer
Hallwachs-Experiment. Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe
 Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
Hallwachs-Experiment Bestrahlung einer geladenen Zinkplatte mit dem Licht einer Quecksilberdampflampe 20.09.2012 Skizziere das Experiment Notiere und Interpretiere die Beobachtungen Photoeffekt Bestrahlt
SS 2015 Supplement to Experimental Physics 2 (LB-Technik) Prof. E. Resconi
 Quantenmechanik des Wasserstoff-Atoms [Kap. 8-10 Haken-Wolf Atom- und Quantenphysik ] - Der Aufbau der Atome Quantenmechanik ==> Atomphysik Niels Bohr, 1913: kritische Entwicklung, die schließlich Plancks
Quantenmechanik des Wasserstoff-Atoms [Kap. 8-10 Haken-Wolf Atom- und Quantenphysik ] - Der Aufbau der Atome Quantenmechanik ==> Atomphysik Niels Bohr, 1913: kritische Entwicklung, die schließlich Plancks
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
PeP Physik erfahren im Forschungs-Praktikum. Das Spektrum Spektrometrie Kontinuumstrahler Das Bohrsche Atommodell Linienstrahler Halbleiterelemente
 Die Entstehung des Lichts Das Spektrum Spektrometrie Kontinuumstrahler Das Bohrsche Atommodell Linienstrahler Halbleiterelemente Das elektromagnetische Spektrum Zur Veranschaulichung Untersuchung von Spektren
Die Entstehung des Lichts Das Spektrum Spektrometrie Kontinuumstrahler Das Bohrsche Atommodell Linienstrahler Halbleiterelemente Das elektromagnetische Spektrum Zur Veranschaulichung Untersuchung von Spektren
Bereich Schwierigkeit Thema Atomphysik X Atommodelle. Dalton, Thomson und Rutherford. Mögliche Lösung
 Atomphysik X Atommodelle Dalton, Thomson und Rutherford a) Formulieren Sie die Daltonsche Atomhypothese. b) Nennen Sie die wesentlichen Merkmale des Atommodells von Thomson. c) Beschreiben Sie die Rutherfordschen
Atomphysik X Atommodelle Dalton, Thomson und Rutherford a) Formulieren Sie die Daltonsche Atomhypothese. b) Nennen Sie die wesentlichen Merkmale des Atommodells von Thomson. c) Beschreiben Sie die Rutherfordschen
Thema heute: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Wiederholung der letzten Vorlesungsstunde: Radioaktive Zerfallsgeschwindigkeit, Altersbestimmungen, Ionisationszähler (Geiger-Müller-Zähler), Szintillationszähler, natürliche radioaktive Zerfallsreihen,
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #25 03/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Physik für Mediziner im 1. Fachsemester #25 03/12/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Abiturprüfung Physik, Grundkurs
 Seite 1 von 6 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer Bedeutung.
Seite 1 von 6 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer Bedeutung.
Das Wasserstoffatom Energiestufen im Atom
 11. 3. Das Wasserstoffatom 11.3.1 Energiestufen im Atom Vorwissen: Hg und Na-Dampflampe liefern ein charakteristisches Spektrum, das entweder mit einem Gitter- oder einem Prismenspektralapparat betrachtet
11. 3. Das Wasserstoffatom 11.3.1 Energiestufen im Atom Vorwissen: Hg und Na-Dampflampe liefern ein charakteristisches Spektrum, das entweder mit einem Gitter- oder einem Prismenspektralapparat betrachtet
Gymnasium / Realschule. Atomphysik 2. Klasse / G8. Aufnahme und Abgabe von Energie (Licht)
 Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Physikalisches Praktikum A 5 Balmer-Spektrum
 Physikalisches Praktikum A 5 Balmer-Spektrum Versuchsziel Es wird das Balmer-Spektrum des Wasserstoffatoms vermessen und die Rydberg- Konstante bestimmt. Für He und Hg werden die Wellenlängen des sichtbaren
Physikalisches Praktikum A 5 Balmer-Spektrum Versuchsziel Es wird das Balmer-Spektrum des Wasserstoffatoms vermessen und die Rydberg- Konstante bestimmt. Für He und Hg werden die Wellenlängen des sichtbaren
Physik für Maschinenbau. Prof. Dr. Stefan Schael RWTH Aachen
 Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Physik für Maschinenbau Prof. Dr. Stefan Schael RWTH Aachen Vorlesung 11 Brechung b α a 1 d 1 x α b x β d 2 a 2 β Totalreflexion Glasfaserkabel sin 1 n 2 sin 2 n 1 c arcsin n 2 n 1 1.0 arcsin
Abiturprüfung Physik, Leistungskurs
 Seite 1 von 8 Abiturprüfung 2010 Physik, Leistungskurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer
Seite 1 von 8 Abiturprüfung 2010 Physik, Leistungskurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer
Beschreibe die wesentlichen Unterschiede zwischen den einzelnen Anregungsmöglichkeiten.
 Erkläre den Begriff Anregung eines Atoms Unter Anregung eines Atoms versteht man die Zufuhr von Energie an ein Atom, welche dieses vom Grundzustand in einen höheren Energiezustand, auf ein höheres Energieniveau,
Erkläre den Begriff Anregung eines Atoms Unter Anregung eines Atoms versteht man die Zufuhr von Energie an ein Atom, welche dieses vom Grundzustand in einen höheren Energiezustand, auf ein höheres Energieniveau,
Atombau, Elektronenkonfiguration und das Orbitalmodell:
 Bohrsches Atommodell: Atombau, Elektronenkonfiguration und das Orbitalmodell: Nachdem Rutherford mit seinem Streuversuch bewiesen hatte, dass sich im Kern die gesamte Masse befindet und der Kern zudem
Bohrsches Atommodell: Atombau, Elektronenkonfiguration und das Orbitalmodell: Nachdem Rutherford mit seinem Streuversuch bewiesen hatte, dass sich im Kern die gesamte Masse befindet und der Kern zudem
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale
 Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Physikalisches Praktikum
 Physikalisches Praktikum MI2AB Prof. Ruckelshausen Versuch 5.6: Bestimmung der Balmerserie Gruppe 2, Mittwoch: Patrick Lipinski, Sebastian Schneider Patrick Lipinski, Sebastian Schneider Seite 1 / 5 1.
Physikalisches Praktikum MI2AB Prof. Ruckelshausen Versuch 5.6: Bestimmung der Balmerserie Gruppe 2, Mittwoch: Patrick Lipinski, Sebastian Schneider Patrick Lipinski, Sebastian Schneider Seite 1 / 5 1.
Abb.15: Experiment zum Rutherford-Modell
 6.Kapitel Atommodelle 6.1 Lernziele Sie kennen die Entwicklung der Atommodelle bis zum linearen Potentialtopf. Sie kennen die Bohrschen Postulate und können sie auch anwenden. Sie wissen, wie man bestimmte
6.Kapitel Atommodelle 6.1 Lernziele Sie kennen die Entwicklung der Atommodelle bis zum linearen Potentialtopf. Sie kennen die Bohrschen Postulate und können sie auch anwenden. Sie wissen, wie man bestimmte
Atommodell führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen.
 Atommodell nach Rutherford 1911 führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen. Beobachtung: Fast alle Teilchen fliegen ungestört durch.
Atommodell nach Rutherford 1911 führte Rutherford den nach ihm benannten Streuversuch durch. Dabei bestrahlte er eine dünne Goldfolie mit α Teilchen. Beobachtung: Fast alle Teilchen fliegen ungestört durch.
SPEKTRALANALYSE. entwickelt um 1860 von: GUSTAV ROBERT KIRCHHOFF ( ; dt. Physiker) + ROBERT WILHELM BUNSEN ( ; dt.
 SPEKTRALANALYSE = Gruppe von Untersuchungsmethoden, bei denen das Energiespektrum einer Probe untersucht wird. Man kann daraus schließen, welche Stoffe am Zustandekommen des Spektrums beteiligt waren.
SPEKTRALANALYSE = Gruppe von Untersuchungsmethoden, bei denen das Energiespektrum einer Probe untersucht wird. Man kann daraus schließen, welche Stoffe am Zustandekommen des Spektrums beteiligt waren.
Spektroskopie. Einleitung
 Spektroskopie Einleitung Schon der Name Quantenphysik drückt aus, dass auf der Ebene der kleinsten physikalischen Objekte (z.b. Atome, Protonen, Neutronen oder Elektronen), bestimmte physikalische Gröÿen
Spektroskopie Einleitung Schon der Name Quantenphysik drückt aus, dass auf der Ebene der kleinsten physikalischen Objekte (z.b. Atome, Protonen, Neutronen oder Elektronen), bestimmte physikalische Gröÿen
14. Atomphysik. Inhalt. 14. Atomphysik
 Inhalt 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Inhalt 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Spektroskopie. Einleitung
 Spektroskopie Einleitung Schon der Name Quantenphysik drückt aus, dass auf der Ebene der kleinsten physikalischen Objekte (z.b. Atome, Protonen, Neutronen oder Elektronen), bestimmte physikalische Gröÿen
Spektroskopie Einleitung Schon der Name Quantenphysik drückt aus, dass auf der Ebene der kleinsten physikalischen Objekte (z.b. Atome, Protonen, Neutronen oder Elektronen), bestimmte physikalische Gröÿen
14. Atomphysik Aufbau der Materie
 14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
c = Ausbreitungsgeschwindigkeit (2, m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 )
 2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
2.3 Struktur der Elektronenhülle Elektromagnetische Strahlung c = λ ν c = Ausbreitungsgeschwindigkeit (2,9979 10 8 m/s) λ = Wellenlänge (m) ν = Frequenz (Hz, s -1 ) Quantentheorie (Max Planck, 1900) Die
10.6. Röntgenstrahlung
 10.6. Röntgenstrahlung Am 8. November 1895 entdeckte Wilhelm Conrad Röntgen in Würzburg die Röntgenstrahlung. Seine Entdeckung zählt zu den wohl bedeutendsten Entdeckungen in der Menschheitsgeschichte.
10.6. Röntgenstrahlung Am 8. November 1895 entdeckte Wilhelm Conrad Röntgen in Würzburg die Röntgenstrahlung. Seine Entdeckung zählt zu den wohl bedeutendsten Entdeckungen in der Menschheitsgeschichte.
12.8 Eigenschaften von elektronischen Übergängen. Übergangsfrequenz
 phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
14. Atomphysik Physik für E-Techniker. 14. Atomphysik
 14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Elemente der Quantenmechanik III 9.1. Schrödingergleichung mit beliebigem Potential 9.2. Harmonischer Oszillator 9.3. Drehimpulsoperator
 VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
VL 8 VL8. VL9. VL10. Das Wasserstoffatom in der klass. Mechanik 8.1. Emissions- und Absorptionsspektren der Atome 8.2. Quantelung der Energie (Frank-Hertz Versuch) 8.3. Bohrsches Atommodell 8.4. Spektren
Übungen Atom- und Molekülphysik für Physiklehrer (Teil 2)
 Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Atommodell. Atommodell nach Bohr und Sommerfeld Für sein neues Atommodell stellte Bohr folgende Postulate auf:
 Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Für sein neues Atommodell stellte Bohr folgende Postulate auf: Elektronen umkreisen den Kern auf bestimmten Bahnen, wobei keine Energieabgabe erfolgt. Jede Elektronenbahn entspricht einem bestimmten Energieniveau
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #26 08/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Physik für Mediziner im 1. Fachsemester #26 08/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Atomphysik Teil 1 Atommodelle, Atomspektren, Röntgenstrahlung Atomphysik Die Atomphysik ist ein
Entstehung des Lichtes und Emissionsspektroskopie
 Entstehung des Lichtes und Emissionsspektroskopie Entstehung des Lichtes Abb. 1 Entstehung des Lichtes Durch Energiezufuhr von Aussen (z.b. Erhitzen) kann die Lage der Elektronen in einem Atom verändert,
Entstehung des Lichtes und Emissionsspektroskopie Entstehung des Lichtes Abb. 1 Entstehung des Lichtes Durch Energiezufuhr von Aussen (z.b. Erhitzen) kann die Lage der Elektronen in einem Atom verändert,
22. Wärmestrahlung. rmestrahlung, Quantenmechanik
 22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
22. Wärmestrahlung rmestrahlung, Quantenmechanik Plancksches Strahlungsgesetz: Planck (1904): der Austausch von Energie zwischen dem strahlenden System und dem Strahlungsfeld kann nur in Einheiten von
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
HOCHSCHULE HARZ Fachbereich Automatisierung und Informatik. Physik. Der Franck-Hertz-Versuch
 Gruppe: HOCHSCHULE HARZ Fachbereich Automatisierung und Informatik Physik Versuch-Nr.: Der Franck-Hertz-Versuch Gliederung: 1. Theoretische Grundlagen 2. Versuchsbeschreibung 3. Versuchsaufbau 4. Messungen
Gruppe: HOCHSCHULE HARZ Fachbereich Automatisierung und Informatik Physik Versuch-Nr.: Der Franck-Hertz-Versuch Gliederung: 1. Theoretische Grundlagen 2. Versuchsbeschreibung 3. Versuchsaufbau 4. Messungen
Festkörperelektronik 2008 Übungsblatt 4
 Lichttechnisches Institut Universität Karlsruhe (TH) Prof. Dr. rer. nat. Uli Lemmer Dipl.-Phys. Alexander Colsmann Engesserstraße 13 76131 Karlsruhe Festkörperelektronik 4. Übungsblatt 12. Juni 2008 Die
Lichttechnisches Institut Universität Karlsruhe (TH) Prof. Dr. rer. nat. Uli Lemmer Dipl.-Phys. Alexander Colsmann Engesserstraße 13 76131 Karlsruhe Festkörperelektronik 4. Übungsblatt 12. Juni 2008 Die
Aufbau von Atomen. Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem
 Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
8.2 Aufbau der Atome. auch bei der Entdeckung der Kathodenstrahlen schienen die Ladungsträger aus den Atomen herauszukommen.
 Dieter Suter - 404 - Physik B3 8.2 Aufbau der Atome 8.2.1 Grundlagen Wenn man Atome als Bausteine der Materie i- dentifiziert hat stellt sich sofort die Frage, woraus denn die Atome bestehen. Dabei besteht
Dieter Suter - 404 - Physik B3 8.2 Aufbau der Atome 8.2.1 Grundlagen Wenn man Atome als Bausteine der Materie i- dentifiziert hat stellt sich sofort die Frage, woraus denn die Atome bestehen. Dabei besteht
[ H, L 2 ]=[ H, L z. ]=[ L 2, L z. U r = Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2. r 1 2. y 2 2. z 2 = 2. r 2 2 r
![[ H, L 2 ]=[ H, L z. ]=[ L 2, L z. U r = Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2. r 1 2. y 2 2. z 2 = 2. r 2 2 r [ H, L 2 ]=[ H, L z. ]=[ L 2, L z. U r = Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2. r 1 2. y 2 2. z 2 = 2. r 2 2 r](/thumbs/71/65107015.jpg) Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2 y 2 2 z 2 = 2 r 2 2 r r 1 2 L r 2 ħ 2 11. Das Wasserstoffatom H = p2 2 U r μ = Masse (statt m, da m später als Quantenzahl verwendet wird) U r = e2
Warum haben wir soviel Zeit mit L 2 verbracht? = x 2 2 y 2 2 z 2 = 2 r 2 2 r r 1 2 L r 2 ħ 2 11. Das Wasserstoffatom H = p2 2 U r μ = Masse (statt m, da m später als Quantenzahl verwendet wird) U r = e2
Abbildung 1. Abbildung 2. R.Goldstein 1
 Wasserstoffatom, Spektrallinien Zusammengestellt von Roman Goldstein A1. Vor 100 Jahren haben Johannes Rydberg und Walter Ritz die Serienformel des Wasserstoffatoms aufgestellt: mit n 2 > n 1 wobei R H
Wasserstoffatom, Spektrallinien Zusammengestellt von Roman Goldstein A1. Vor 100 Jahren haben Johannes Rydberg und Walter Ritz die Serienformel des Wasserstoffatoms aufgestellt: mit n 2 > n 1 wobei R H
Physikalisches Grundpraktikum Abteilung Optik
 O14 Physikalisches Grundpraktikum Abteilung Optik Optische Spektralanalyse 1 Lernziele Entstehung elektromagnetischer Strahlung, Grundbegriffe der Spektroskopie, Auflösungsvermögen optischer Instrumente,
O14 Physikalisches Grundpraktikum Abteilung Optik Optische Spektralanalyse 1 Lernziele Entstehung elektromagnetischer Strahlung, Grundbegriffe der Spektroskopie, Auflösungsvermögen optischer Instrumente,
Licht als Teilchenstrahlung
 Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
Der Photoeffekt: die auf die Materie einfallende Strahlung löst ein Elektron aus. Es gibt eine Grenzfrequenz, welche die Strahlung haben muss, um das Atom gerade zu ionisieren. Licht als Teilchenstrahlung
27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus
 26. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus 28. Atomphysik, Röntgenstrahlung, Bohrsches Atommodell Versuche: Elektronenbeugung Linienspektrum
26. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung, Quantenmechanik (Abschluß: Welle-Teilchen-Dualismus 28. Atomphysik, Röntgenstrahlung, Bohrsches Atommodell Versuche: Elektronenbeugung Linienspektrum
Vorlesung 9: Roter Faden: Wiederholung Quantisierung der Energien in QM. Franck-Hertz Versuch. Emissions- und Absorptionsspektren der Atome
 Vorlesung 9: Roter Faden: Wiederholung Quantisierung der Energien in QM Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem
Vorlesung 9: Roter Faden: Wiederholung Quantisierung der Energien in QM Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem
2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten
 Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Inhalt: 1. Regeln und Normen Modul: Allgemeine Chemie 2. Elementare Stöchiometrie I Definition und Gesetze, Molbegriff, Konzentrationseinheiten 3.Bausteine der Materie Atomkern: Elementarteilchen, Kernkräfte,
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Das Rutherfordsche Atommodelle
 Dieses Lernskript soll nochmals die einzelnen Atommodelle zusammenstellen und die Bedeutung der einzelnen Atommdelle veranschaulichen. Das Rutherfordsche Atommodelle Entstehung des Modells Rutherford beschoss
Dieses Lernskript soll nochmals die einzelnen Atommodelle zusammenstellen und die Bedeutung der einzelnen Atommdelle veranschaulichen. Das Rutherfordsche Atommodelle Entstehung des Modells Rutherford beschoss
Protokoll zum Grundversuch Franck-Hertz Versuch
 Protokoll zum Grundversuch Franck-Hertz Versuch Fabian Schmid-Michels fschmid-michels@uni-bielefeld.de Nils Brüdigam nils.bruedigam@googlemail.com Universität Bielefeld Sommersemester 2007 Grundpraktikum
Protokoll zum Grundversuch Franck-Hertz Versuch Fabian Schmid-Michels fschmid-michels@uni-bielefeld.de Nils Brüdigam nils.bruedigam@googlemail.com Universität Bielefeld Sommersemester 2007 Grundpraktikum
A. Erhaltungsgrößen (17 Punkte) Name: Vorname: Matr. Nr.: Studiengang: ET Diplom ET Bachelor TI WI. Platz Nr.: Tutor:
 Prof. Dr. O. Dopfer Prof. Dr. A. Hese Priv. Doz. Dr. S. Kröger Cand.-Phys. A. Kochan Technische Universität Berlin A. Erhaltungsgrößen (17 Punkte) 1. Unter welcher Bedingung bleiben a) der Impuls b) der
Prof. Dr. O. Dopfer Prof. Dr. A. Hese Priv. Doz. Dr. S. Kröger Cand.-Phys. A. Kochan Technische Universität Berlin A. Erhaltungsgrößen (17 Punkte) 1. Unter welcher Bedingung bleiben a) der Impuls b) der
Wellenlängenmessung mit einem Gitter (O4)
 Wellenlängenmessung mit einem (O4) Ziel des Versuches Die Wellenlängen der intensivsten Linien des Hg-Spektrums und der sichtbaren Linien des H-Spektrums sollen mit einem spektrometer bestimmt werden.
Wellenlängenmessung mit einem (O4) Ziel des Versuches Die Wellenlängen der intensivsten Linien des Hg-Spektrums und der sichtbaren Linien des H-Spektrums sollen mit einem spektrometer bestimmt werden.
10.7 Moderne Atommodelle
 10.7 Moderne Atommodelle Zu Beginn des 20. Jahrhunderts entwickelte Niels Bohr sein berühmtes Bohrsches Atommodell. Mit diesem Modell konnten die Atomhüllen von einfachen Atomen wie dem Wasserstoffatom
10.7 Moderne Atommodelle Zu Beginn des 20. Jahrhunderts entwickelte Niels Bohr sein berühmtes Bohrsches Atommodell. Mit diesem Modell konnten die Atomhüllen von einfachen Atomen wie dem Wasserstoffatom
Aufgaben zum Wasserstoffatom
 Aufgaben zum Wasserstoffatom Hans M. Strauch Kurfürst-Ruprecht-Gymnasium Neustadt/W. Aufgabenarten Darstellung von Zusammenhängen, Abgrenzung von Unterschieden (können u.u. recht offen sein) Beantwortung
Aufgaben zum Wasserstoffatom Hans M. Strauch Kurfürst-Ruprecht-Gymnasium Neustadt/W. Aufgabenarten Darstellung von Zusammenhängen, Abgrenzung von Unterschieden (können u.u. recht offen sein) Beantwortung
10. Das Wasserstoff-Atom Das Spektrum des Wasserstoff-Atoms. im Bohr-Modell:
 phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
phys4.016 Page 1 10. Das Wasserstoff-Atom 10.1.1 Das Spektrum des Wasserstoff-Atoms im Bohr-Modell: Bohr-Modell liefert eine ordentliche erste Beschreibung der grundlegenden Eigenschaften des Spektrums
Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert
 Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert FK02 Röntgenstrahlung & Kristallanalyse (Pr_PhII_FK02_Röntgen_7, 25.10.2015) 1. 2. Name
Physikalisches Praktikum II Bachelor Physikalische Technik: Lasertechnik Prof. Dr. H.-Ch. Mertins, MSc. M. Gilbert FK02 Röntgenstrahlung & Kristallanalyse (Pr_PhII_FK02_Röntgen_7, 25.10.2015) 1. 2. Name
Bohrsches Atommodell / Linienspektren. Experimentalphysik für Biologen und Chemiker, O. Benson & A. Peters, Humboldt-Universität zu Berlin
 Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
Bohrsches Atommodell / Linienspektren Quantenstruktur der Atome: Atomspektren Emissionslinienspektren von Wasserstoffatomen im sichtbaren Bereich Balmer Serie (1885): 1 / λ = K (1/4-1/n 2 ) 656.28 486.13
8 Das Bohrsche Atommodell. 8. Das Bohrsche Atommodell
 1. Einführung 1.1. Quantenmechanik versus klassische Theorien 1.2. Historischer Rückblick 2. Kann man Atome sehen? Größe des Atoms 3. Weitere Eigenschaften von Atomen: Masse, Isotopie 4. Atomkern und Hülle:
1. Einführung 1.1. Quantenmechanik versus klassische Theorien 1.2. Historischer Rückblick 2. Kann man Atome sehen? Größe des Atoms 3. Weitere Eigenschaften von Atomen: Masse, Isotopie 4. Atomkern und Hülle:
Zentralabitur 2008 Physik Schülermaterial Aufgabe II ea Bearbeitungszeit: 300 min
 Thema: Experimente mit Interferometern Im Mittelpunkt der in den Aufgaben 1 und 2 angesprochenen Fragestellungen steht das Michelson-Interferometer. Es werden verschiedene Interferenzversuche mit Mikrowellen
Thema: Experimente mit Interferometern Im Mittelpunkt der in den Aufgaben 1 und 2 angesprochenen Fragestellungen steht das Michelson-Interferometer. Es werden verschiedene Interferenzversuche mit Mikrowellen
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Einführung in die Quantentheorie der Atome und Photonen
 Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Einführung in die Quantentheorie der Atome und Photonen 23.04.2005 Jörg Evers Max-Planck-Institut für Kernphysik, Heidelberg Quantenmechanik Was ist das eigentlich? Physikalische Theorie Hauptsächlich
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Das Bohr sche Atommodell: Strahlenabsorption, -emission, Elektromagentische Strahlung, Wellen, Wellenlänge, Frequenz, Wellenzahl. Postulate: * Elektronen bewegen
Wiederholung der letzten Vorlesungsstunde: Das Bohr sche Atommodell: Strahlenabsorption, -emission, Elektromagentische Strahlung, Wellen, Wellenlänge, Frequenz, Wellenzahl. Postulate: * Elektronen bewegen
Versuch Spektroskopie
 Versuch Spektroskopie Beschafft aus Studiengebühren Vorbereitung: Gitterspektrometer, Atomspektren, Bahndrehimpuls, Spin, Plancksches Strahlungsgesetz, pn-übergang, Leuchtdiode. Literatur: allg. Lehrbücher
Versuch Spektroskopie Beschafft aus Studiengebühren Vorbereitung: Gitterspektrometer, Atomspektren, Bahndrehimpuls, Spin, Plancksches Strahlungsgesetz, pn-übergang, Leuchtdiode. Literatur: allg. Lehrbücher
Vorlesung 24: Roter Faden: Wiederholung Quantisierung der Energien in QM. Emissions- und Absorptionsspektren der Atome
 Vorlesung 24: Roter Faden: Wiederholung Quantisierung der Energien in QM Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Lösung der Schrödingergleichung
Vorlesung 24: Roter Faden: Wiederholung Quantisierung der Energien in QM Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Lösung der Schrödingergleichung
1 Atombau und Periodensystem. 1.1 Struktur der Elektronenhülle. Quantentheorie (Max Planck, 1900)
 1 Atombau und Periodensystem 1.1 Struktur der Elektronenhülle Quantentheorie (Max Planck, 1900) Die Emission oder Absorption von elektromagnetischer Strahlung durch Materie ist nur in Form von Energieportionen
1 Atombau und Periodensystem 1.1 Struktur der Elektronenhülle Quantentheorie (Max Planck, 1900) Die Emission oder Absorption von elektromagnetischer Strahlung durch Materie ist nur in Form von Energieportionen
Einleitung Das Rutherford sche Atommodell Das Bohr sche Atommodell. Atommodelle [HERR] Q34 LK Physik. 25. September 2015
![Einleitung Das Rutherford sche Atommodell Das Bohr sche Atommodell. Atommodelle [HERR] Q34 LK Physik. 25. September 2015 Einleitung Das Rutherford sche Atommodell Das Bohr sche Atommodell. Atommodelle [HERR] Q34 LK Physik. 25. September 2015](/thumbs/49/25189684.jpg) Q34 LK Physik 25. September 2015 Geschichte Antike Vorstellung von Leukipp und Demokrit (5. Jahrh. v. Chr.); Begründung des Atomismus (atomos, griech. unteilbar). Anfang des 19. Jahrh. leitet Dalton aus
Q34 LK Physik 25. September 2015 Geschichte Antike Vorstellung von Leukipp und Demokrit (5. Jahrh. v. Chr.); Begründung des Atomismus (atomos, griech. unteilbar). Anfang des 19. Jahrh. leitet Dalton aus
Physikalisches Praktikum Bachelor Chemieingenieurwesen, Wirtschaftsingenieurwesen Chemietechnik MSc. M. Gilbert
 Physikalisches Praktikum Bachelor Chemieingenieurwesen, Wirtschaftsingenieurwesen Chemietechnik MSc. M. Gilbert O03 Optik: Prismenspektrometer (Pr_EX_O03_Prismenspektrometer_6, 30.8.009). Name Matr. Nr.
Physikalisches Praktikum Bachelor Chemieingenieurwesen, Wirtschaftsingenieurwesen Chemietechnik MSc. M. Gilbert O03 Optik: Prismenspektrometer (Pr_EX_O03_Prismenspektrometer_6, 30.8.009). Name Matr. Nr.
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #27 14/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Das Bohrsche Atommodell Bahnradius im Wasserstoffatom Der Radius der stabilen Elektronenbahnen
Physik für Mediziner im 1. Fachsemester #27 14/12/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Das Bohrsche Atommodell Bahnradius im Wasserstoffatom Der Radius der stabilen Elektronenbahnen
Übungen zur Physik des Lichts
 ) Monochromatisches Licht (λ = 500 nm) wird an einem optischen Gitter (000 Striche pro cm) gebeugt. a) Berechnen Sie die Beugungswinkel der Intensitätsmaxima bis zur 5. Ordnung. b) Jeder einzelne Gitterstrich
) Monochromatisches Licht (λ = 500 nm) wird an einem optischen Gitter (000 Striche pro cm) gebeugt. a) Berechnen Sie die Beugungswinkel der Intensitätsmaxima bis zur 5. Ordnung. b) Jeder einzelne Gitterstrich
Physikalisches Praktikum
 Physikalisches Praktikum MI2AB Prof. Ruckelshausen Versuch 3.2: Wellenlängenbestimmung mit dem Gitter- und Prismenspektrometer Inhaltsverzeichnis 1. Theorie Seite 1 2. Versuchsdurchführung Seite 2 2.1
Physikalisches Praktikum MI2AB Prof. Ruckelshausen Versuch 3.2: Wellenlängenbestimmung mit dem Gitter- und Prismenspektrometer Inhaltsverzeichnis 1. Theorie Seite 1 2. Versuchsdurchführung Seite 2 2.1
Für Geowissenschaftler. EP WS 2009/10 Dünnweber/Faessler
 Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
Für Geowissenschaftler Termin Nachholklausur Vorschlag Mittwoch 14.4.10 25. Vorlesung EP V. STRAHLUNG, ATOME, KERNE 27. Wärmestrahlung und Quantenmechanik Photometrie Plancksches Strahlungsgesetze, Welle/Teilchen
5. Die gelbe Doppellinie der Na-Spektrallampe ist mit dem Gitter (1. und 2. Ordnung) zu messen und mit dem Prisma zu beobachten.
 Universität Potsdam Institut für Physik und Astronomie Grundpraktikum O Gitter/Prisma Geräte, bei denen man von der spektralen Zerlegung des Lichts (durch Gitter bzw. Prismen) Gebrauch macht, heißen (Gitter-
Universität Potsdam Institut für Physik und Astronomie Grundpraktikum O Gitter/Prisma Geräte, bei denen man von der spektralen Zerlegung des Lichts (durch Gitter bzw. Prismen) Gebrauch macht, heißen (Gitter-
Examensaufgaben QUANTENPHYSIK
 Examensaufgaben QUANTENPHYSIK Aufgabe 1 (Juni 2006) Bei einem Versuch wurden folgende Messwerte ermittelt : Wellenlänge des Lichtes (nm) Gegenspannung (V) 436 0,83 578 0,13 a) Berechne aus diesen Werten
Examensaufgaben QUANTENPHYSIK Aufgabe 1 (Juni 2006) Bei einem Versuch wurden folgende Messwerte ermittelt : Wellenlänge des Lichtes (nm) Gegenspannung (V) 436 0,83 578 0,13 a) Berechne aus diesen Werten
Vorlesung 9: Roter Faden: Franck-Hertz Versuch. Emissions- und Absorptionsspektren der Atome. Spektren des Wasserstoffatoms. Bohrsche Atommodell
 Vorlesung 9: Roter Faden: Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
Vorlesung 9: Roter Faden: Franck-Hertz Versuch Emissions- und Absorptionsspektren der Atome Spektren des Wasserstoffatoms Bohrsche Atommodell Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/
FK Experimentalphysik 3, Lösung 4
 1 Sterne als schwarze Strahler FK Experimentalphysik 3, 4 1 Sterne als schwarze Strahler Betrachten sie folgende Sterne: 1. Einen roten Stern mit einer Oberflächentemperatur von 3000 K 2. einen gelben
1 Sterne als schwarze Strahler FK Experimentalphysik 3, 4 1 Sterne als schwarze Strahler Betrachten sie folgende Sterne: 1. Einen roten Stern mit einer Oberflächentemperatur von 3000 K 2. einen gelben
Das Atom Aufbau der Materie (Vereinfachtes Bohrsches Atommodell)
 Das Atom Aufbau der Materie (Vereinfachtes Bohrsches Atommodell) Referat von Anna-Lena Butke und Kristina Lechner Übersicht Niels Bohr (Biographie) Das Bohrsche Atommodell Das Spektrum des Wasserstoffatoms
Das Atom Aufbau der Materie (Vereinfachtes Bohrsches Atommodell) Referat von Anna-Lena Butke und Kristina Lechner Übersicht Niels Bohr (Biographie) Das Bohrsche Atommodell Das Spektrum des Wasserstoffatoms
VL Spin-Bahn-Kopplung Paschen-Back Effekt. VL15. Wasserstoffspektrum Lamb Shift. VL16. Hyperfeinstruktur
 VL 16 VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2. Paschen-Back Effekt VL15. Wasserstoffspektrum 15.1. Lamb Shift VL16. Hyperfeinstruktur 16.1. Hyperfeinstruktur 16.2. Kernspinresonanz
VL 16 VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2. Paschen-Back Effekt VL15. Wasserstoffspektrum 15.1. Lamb Shift VL16. Hyperfeinstruktur 16.1. Hyperfeinstruktur 16.2. Kernspinresonanz
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde. Sommersemester VL #46 am
 Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #46 am 19.07.2007 Vladimir Dyakonov Atome und Strahlung 1 Atomvorstellungen J.J. Thomson 1856-1940
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #46 am 19.07.2007 Vladimir Dyakonov Atome und Strahlung 1 Atomvorstellungen J.J. Thomson 1856-1940
Grundbausteine des Mikrokosmos (6) Vom Planetenmodell der Atome zum Bohrschen Atommodell
 Grundbausteine des Mikrokosmos (6) Vom Planetenmodell der Atome zum Bohrschen Atommodell 1900: Entdeckung einer neuen Naturkonstanten: Plancksches Wirkungsquantum Was sind Naturkonstanten und welche Bedeutung
Grundbausteine des Mikrokosmos (6) Vom Planetenmodell der Atome zum Bohrschen Atommodell 1900: Entdeckung einer neuen Naturkonstanten: Plancksches Wirkungsquantum Was sind Naturkonstanten und welche Bedeutung
Folgendes Röntgenspektrum wurde an einer Röntgenröhre aufgenommen, die mit der Beschleunigungsspannung
 Seite Aufgabe : Röntgenspektrum Folgendes Röntgenspektrum wurde an einer Röntgenröhre aufgenommen, die mit der Beschleunigungsspannung U = 30 kv betrieben wurde.. Berechnen Sie aus dem dargestellten Versuchsergebnis
Seite Aufgabe : Röntgenspektrum Folgendes Röntgenspektrum wurde an einer Röntgenröhre aufgenommen, die mit der Beschleunigungsspannung U = 30 kv betrieben wurde.. Berechnen Sie aus dem dargestellten Versuchsergebnis
Physikalisches Praktikum
 Physikalisches Praktikum MI2AB Prof. Ruckelshausen Versuch 3.6: Beugung am Gitter Inhaltsverzeichnis 1. Theorie Seite 1 2. Versuchsdurchführung Seite 2 2.1 Bestimmung des Gitters mit der kleinsten Gitterkonstanten
Physikalisches Praktikum MI2AB Prof. Ruckelshausen Versuch 3.6: Beugung am Gitter Inhaltsverzeichnis 1. Theorie Seite 1 2. Versuchsdurchführung Seite 2 2.1 Bestimmung des Gitters mit der kleinsten Gitterkonstanten
10. Der Spin des Elektrons
 10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
Übungsblatt 06. PHYS4100 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, oder 3. 6.
 Übungsblatt 06 PHYS400 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, (othmar.marti@uni-ulm.de) 2. 6. 2005 oder 3. 6. 2005 Aufgaben. Schätzen Sie die relativistische Korrektur E
Übungsblatt 06 PHYS400 Grundkurs IV (Physik, Wirtschaftsphysik, Physik Lehramt) Othmar Marti, (othmar.marti@uni-ulm.de) 2. 6. 2005 oder 3. 6. 2005 Aufgaben. Schätzen Sie die relativistische Korrektur E
Lebensmittelphysik. Atomaufbau.
 1 Lebensmittelphysik. Atomaufbau. SS 18. Sem. B.Sc. Lebensmittelwissenschaften Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe unter gleichen Bedingungen
1 Lebensmittelphysik. Atomaufbau. SS 18. Sem. B.Sc. Lebensmittelwissenschaften Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe unter gleichen Bedingungen
8.3 Die Quantenmechanik des Wasserstoffatoms
 Dieter Suter - 409 - Physik B3 8.3 Die Quantenmechanik des Wasserstoffatoms 8.3.1 Grundlagen, Hamiltonoperator Das Wasserstoffatom besteht aus einem Proton (Ladung +e) und einem Elektron (Ladung e). Der
Dieter Suter - 409 - Physik B3 8.3 Die Quantenmechanik des Wasserstoffatoms 8.3.1 Grundlagen, Hamiltonoperator Das Wasserstoffatom besteht aus einem Proton (Ladung +e) und einem Elektron (Ladung e). Der
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Einführung in die Quantenphysik
 Einführung in die Quantenphysik Klassische Optik Der lichtelektrische Effekt Effekte elektromagnetischer Strahlung Kopenhagen-Interpretation Elektronen Quantenphysik und klassische Physik Atomphysik Klassische
Einführung in die Quantenphysik Klassische Optik Der lichtelektrische Effekt Effekte elektromagnetischer Strahlung Kopenhagen-Interpretation Elektronen Quantenphysik und klassische Physik Atomphysik Klassische
Versuch 22: Spektroskopische Bestimmung der Rydbergkonstanten
 Versuch 22: Spektroskopische Bestimmung der Rydbergkonstanten Aus der Balmerserie des Wasserstoffatoms ist mit einem Spektroskop die Rydbergkonstante R H für Wasserstoff zu bestimmen. Vorkenntnisse Historische
Versuch 22: Spektroskopische Bestimmung der Rydbergkonstanten Aus der Balmerserie des Wasserstoffatoms ist mit einem Spektroskop die Rydbergkonstante R H für Wasserstoff zu bestimmen. Vorkenntnisse Historische
Abiturprüfung Physik, Grundkurs
 Seite 1 von 5 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Farbstoffmoleküle In der Spektroskopie unterscheidet man zwei grundsätzliche Typen von Spektren: Emissionsspektren, wie sie
Seite 1 von 5 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Farbstoffmoleküle In der Spektroskopie unterscheidet man zwei grundsätzliche Typen von Spektren: Emissionsspektren, wie sie
Handbuch zu den Schlüsselexperimenten des KLP Physik Grundkurs Qualifikationsphase
 Handbuch zu den Schlüsselexperimenten des KLP Physik Grundkurs Qualifikationsphase Schlüsselexperiment 16: Linienspektren bzw. Spektralanalyse 1. Linienspektren bzw. Spektralanalyse als Schlüsselexperiment
Handbuch zu den Schlüsselexperimenten des KLP Physik Grundkurs Qualifikationsphase Schlüsselexperiment 16: Linienspektren bzw. Spektralanalyse 1. Linienspektren bzw. Spektralanalyse als Schlüsselexperiment
