BREMEN MITTE. Rosten von Eisen. ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht. Lino Dotsikas Kian Ghodoussi
|
|
|
- Gerd Lange
- vor 7 Jahren
- Abrufe
Transkript
1 ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht BREMEN MITTE Rosten von Eisen Lino Dotsikas Kian Ghodoussi Schule: Kippenberg Gymnasium Bremen Jugend forscht 2014
2 Inhaltsverzeichnis Seite 1 Einleitung 2 2 Vorgehensweise Material Durchführung Experiment 1: Rosten von Eisenwolle Experiment 2: Rosten von Eisennägeln Experiment 3: Rosten von galvanisiertem Material 4 3 Beobachtungen, Ergebnisse und Schlussfolgerungen Experiment 1: Rosten von Eisenwolle Experiment 2: Rosten Eisennägeln Experiment 3: Rosten von galvanisiertem Material 7 4 Ergebnisdiskussion 8 5 Zusammenfassung 9 6 Quellen- und Literaturverzeichnis 9 1
3 Rosten von Eisen 1 Einleitung Nachdem uns unsere Jugend forscht -Lehrerin verschiedene Projektvorschläge gemacht hat, haben wir uns für das Thema Rosten von Eisen entschieden. Dieses Thema erschien uns besonders interessant, weil Eisen ein sehr wichtiger Werkstoff ist, aus dem viele Alltagsgegenstände bestehen. Leider rostet Eisen sehr schnell (Korrosion), wenn es nicht geschützt wird. Rost entsteht durch eine chemische Verbindung von Eisen, Sauerstoff und Wasser. Das nennt man auch Eisenoxid. Rost hat eine orange-braune Farbe. Gegenstände aus Eisen, bei denen der Rostschutz besonders wichtig ist, sind z.b. Bahnschienen, Brücken, Autos, Schiffe. Auch kleine, unscheinbare Gegenstände können unbrauchbar werden, wenn sie rosten, beispielsweise Nägel oder Schrauben. Deshalb untersuchen wir die Wirkung verschiedener Stoffe auf das Rostverhalten von Eisen. Dabei suchen wir auch nach einer Substanz, die vor Rost schützen kann. 2 Vorgehensweise Wir haben drei Experimente zum Rosten von Eisen durchgeführt. Dabei haben wir die Auswirkung verschiedener Stoffe auf Eisenwolle, Eisennägel und galvanisierte Nägel bzw. galvanisierte Eisenwolle untersucht. 2.1 Material Als Versuchsmaterial haben wir verwendet: Eisenwolle Eisennägel Zusätzlich haben wir die folgenden Stoffe benötigt: Wasser Brennspiritus Salzwasser Essigessenz Zuckerwasser Olivenöl Zitronensäure Geschirrspülmittel Soda Edding-Stift Haarspray 2
4 Außerdem haben wir für einen Versuch zur elektrolytischen Abscheidung von Zink auf Eisen folgende Materialien gebraucht: Becherglas (100 ml) Elekrolyseeinheit mit Kabelmaterial Kupferdraht 10 g Zinksulfat 50 ml destilliertes Wasser 5 ml Essigsäure (5 %) 2.2 Durchführung Experiment 1: Rosten von Eisenwolle Für unser Experiment 1 haben wir 11 Eisenwollekugeln verwendet. Jeweils eine kleine Eisenwollekugel wurde eingetaucht in bzw. eingesprüht mit: 1. Wasser 2. Brennspiritus 3. Salzwasser 4. Essigessenz 5. Zuckerwasser 6. Olivenöl 7. Zitronensäure 8. Geschirrspülmittel 9. Sodawasser 10. Haarspray Eine zusätzliche Kontrollkugel blieb unbehandelt. Die Eisenwollekugeln wurden anschließend bis an das Ende eines Reagenzglases geschoben. Dieses wurde mit der Öffnung nach unten in ein zur Hälfte mit Wasser gefülltes Becherglas gestellt und sieben Tage stehen gelassen. So waren die Eisenwollekugeln Wasserdampf und Sauerstoff ausgesetzt. Eisenwollekugeln in Reagenzgläsern (Foto: L. Dotsikas, ) 3
5 2.2.2 Experiment 2: Rosten von Eisennägeln Für das Experiment 2 haben wir drei Eisennägel verwendet. Einen Nagel haben wir besprüht bzw. bemalt mit: 1. Haarspray 2. Edding-Stift Der dritte Nagel blieb zur Kontrolle unbehandelt. Alle drei Eisennägel wurden in eine mit Wasser gefüllt Petrischale gelegt und sieben Tage stehen gelassen Experiment 3: Rosten von galvanisiertem Material Für das Experiment 3 haben wir drei Eisennägel und zwei Eisenwollekugeln verwendet. Die drei Eisennägel und eine Eisenwollekugel wurden mithilfe von Zinksulfat galvanisiert 1. Die zweite Eisenwollekugel blieb unbehandelt. Dafür haben wir 10 g Zinksulfat in 50 ml destilliertem Wasser gelöst und 5 ml verdünnte Essigsäure zugegeben. Die Eisennägel und die Eisenwollekugel haben wir nacheinander an einem Kupferdraht in die Lösung gehängt und mit dem Minuspol der Gleichstromquelle verbunden. Als Anode diente ein Graphitstab. Die Spannung wurde so geregelt, dass sich Zink abscheidet, ohne dass die Kathode zu stark gaste. Nachdem die galvanisierten Eisennägel getrocknet waren, wurden sie in eine mit Wasser gefüllte Petrischale gelegt und sieben Tage stehen gelassen. Die getrocknete galvanisierte Eisenwollekugel wurde an das Ende eines Reagenzglases geschoben. Dieses wurde mit der Öffnung nach unten in ein zur Hälfte mit Wasser gefülltes Becherglas gestellt und sieben Tage stehen gelassen. Die unbehandelte Eisenwollekugel wurde ebenfalls an das Ende eines Reagenzglases geschoben. Dieses wurde mit der Öffnung nach unten in ein zur Hälfte mit Wasser gefülltes Becherglas gestellt und sieben Tage stehen gelassen. 3 Beobachtungen, Ergebnisse und Schlussfolgerungen 3.1 Experiment 1: Rosten von Eisenwolle Insgesamt 11 Eisenwollekugeln. Neun Kugeln eingetaucht in Wasser, Brennspiritus, Salzwasser, Essigessenz, Zuckerwasser, Olivenöl, 1 Galvanisieren: Überziehen von Gegenständen mit einem Metall durch Elektrolyse (nach Asselborn, 2009) 4
6 Zitronensäure, Geschirrspülmittel, Sodawasser. Eine Kugel mit Haarspray besprüht. Eine Kugel unbehandelt. Wasser Brennspiritus Salzwasser Essigessenz Zuckerwasser Olivenöl Zitronensäure Geschirrspülmittel Haarspray Sodawasser unbehandelt Auf der Eisenwollekugel haben sich schwarze Flecken gebildet. Die Kugel hinterlässt jetzt auf Papier schwarze Spuren. Die Eisenwollekugel hat sich an sich an einigen kleinen Stellen braun verfärbt. Etwa die Hälfte der Fläche hat sich schwarz verfärbt. Die Eisenwollekugel hat sich an einigen Stellen schwarz verfärbt. Sie hinterlässt auf Papier jedoch gelb-orange-braune Spuren. Auf der Eisenwollekugel haben sich nur einige wenige schwarze Flecken gebildet. Sie hinterlässt aber braune Spuren auf Papier. Diese Spuren waren zunächst hellbraun, nach drei Minuten und 15 Sekunden verfärbten sie sich dunkelbraun. Die Eisenwollekugel hat sich schwarz verfärbt und hinterlässt auf Papier dunkelbraune Spuren. Die Eisenwollekugel ist gut erhalten und glänzt. Sie hinterlässt auf Papier fettige Spuren. Die Eisenwollekugel hat sich schwarz verfärbt. Sie hinterlässt jedoch auf Papier gelbe, grüne und schwarze Spuren. Die Eisenwollekugel hat sich schwarz verfärbt. Sie hinterlässt dunkelgrüne bis schwarze Spuren. Die Eisenwollekugel ist an einer Stelle braun, orange, schwarz. Der Rest ist unverändert. Die Eisenwollekugel ist an einer Stelle schwarz verfärbt. Sie hinterlässt schwarzdunkelgrüne Spuren. Die trockene Eisenwollekugel hat sich an einigen Stellen hellbraun verfärbt. Sie hinterlässt kaum sichtbare braune Spuren. 5
7 Schlussfolgerung zu Experiment 1 Bis auf die mit Olivenöl behandelte Eisenwolle sind bei allen anderen Eisenwolleproben schwarze, braune oder orangene Verfärbungen aufgetreten. Bei orange-braunen Verfärbungen gehen wir davon aus, dass es sich dabei um Rost handelt. Je nach verwendetem Material hinterlassen einige Verfärbungen auf dem Papier nicht nur schwarze, braune und orangene Spuren sondern auch gelbe und grüne Spuren. Allerdings sind wir uns nicht sicher, ob es sich bei den schwarzen Verfärbungen überhaupt um Rost handelt. Unsicher sind wir uns auch mit den gelben und grünen Spuren, die bei der Behandlung mit Salzwasser, Zitronensäure, Geschirrspülmittel und Soda aufgetreten sind. Wir vermuten, dass es eventuell an dem verwendeten Leitungswasser liegen könnte und sich vielleicht Keime wie z.b. Bakterien gebildet haben könnten. Vielleicht enthält das Leitungswasser auch Chlor. Wenn Eisen und Chlor sich verbinden, können gelbe und grüne Lösungen entstehen 2. Da sich alle Eisenwollekugeln, bis auf die in Olivenöl getauchte Kugel verfärbt haben, schließen wir daraus, dass nur das Olivenöl vor Rost geschützt hat. 3.2 Experiment 2: Rosten von Eisennägeln Drei Nägel, mit Haarspray und Edding-Stift behandelt, ein Nagel unbehandelt Haarspray Edding-Stift Der Eisennagel hat sich stark orange-braun verfärbt. Die Rillen, die man vor dem Experiment auf dem Nagel sehen konnte, waren nach dem Experiment nicht mehr sichtbar. Die Seite, auf der der Nagel gelegen hat, blieb unverändert. Beim Herausnehmen aus dem Wasser hat sich der orange-braune Belag zum größten Teil abgelöst und blieb auf dem Boden der Petrischale zurück. Der Nagel war an den Stellen, an denen sich der Belag gelöst hatte, nicht mehr glänzend wie vor dem Experiment, sondern matt. Der Eisennagel hat sich stark orange-braun verfärbt. Die Rillen auf dem Nagel waren nach dem Experiment nicht mehr sichtbar. Die Seite, auf der der Nagel gelegen hat, blieb unverändert. Beim Herausnehmen aus dem Wasser blieb der orange-braune Belag vollständig am Nagel haften. 2 Eisenchlorid (nach Tessloffs Schülerlexikon, 2003) 6
8 Unbehandelt Der Eisennagel hat sich stark orange-braun verfärbt. Die Rillen auf dem Nagel waren nach dem Experiment nicht mehr sichtbar. Die Seite, auf der der Nagel gelegen hat, blieb unverändert. Beim Herausnehmen aus dem Wasser blieb der orange-braune Belag vollständig am Nagel haften. Schlussfolgerung zu Experiment 2 Alle Nägel haben sich stark farblich verändert bzw. haben gerostet. Daraus ziehen wir den Schluss, dass weder Haarspray noch Edding-Stift vor dem Rosten geschützt haben. Auffällig finden wir, dass alle drei Nägel auf der Seite, mit der sie aufgelegen haben, nicht gerostet haben. 3.3 Experiment 3: Rosten von galvanisiertem Material Drei Eisennägel galvanisiert, eine Eisenwollekugel galvanisiert, eine Eisenwollekugel unbehandelt. Galvanisierter Nagel 1 Galvanisierter Nagel 2 Galvanisierter Nagel 3 Galvanisierte Eisenwolle Unbehandelte Eisenwolle Der Nagel hat sich orange-braun verfärbt. Der Nagel hat sich nur an wenigen Stellen orange-braun verfärbt. An einer Stelle ist er weiß geworden. Die Hälfte des Nagels blieb unverändert. Die andere Hälfte ist weiß geworden. Die Eisenwolle hat sehr wenige orangebraune Stellen. Die Eisenwolle hat mehrere orange-braune Stellen. Schlussfolgerung zu Experiment 3 Einer der galvanisierten Nägel hat sich orange-braun verfärbt, d.h. er hat gerostet. Der zweite galvanisierte Nagel hat nur stellenweise gerostet und war an einer Stelle weiß geworden. Der dritte galvanisierte Nagel blieb zur Hälfte unverändert, aber die andere Hälfte war weiß geworden. 7
9 Die galvanisierte Eisenwolle hatte nur sehr wenige orange-braune Stellen. D.h., sie hat nur sehr wenig gerostet. Die unbehandelte Eisenwolle hatte deutlich mehr orange-braune Verfärbungen als die galvanisierte Eisenwolle. D.h. sie hat mehr gerostet. Aus diesen Ergebnissen schließen wir, dass das Galvanisieren vor dem Rosten schützt. Allerdings nehmen wir an, dass die Dauer der Galvanisierung eine wichtige Rolle dabei spielt. Vermutlich haben wir den ersten Eisennagel zu kurz galvanisiert, ebenso die Eisenwolle. Wir wissen aber nicht, worum es sich bei den weißen Verfärbungen der galvanisierten Nägel handelt. Wir nehmen an, dass sich mit dem Zink eine Schutzschicht gebildet hat. 4 Ergebnisdiskussion Aus unseren Ergebnissen schlussfolgern wir, dass nur die Behandlung mit Olivenöl und die Galvanisierung die Eisenwolle bzw. die Eisennägel vor Rost geschützt haben. Es haben sich für uns aber auch einige Fragen ergeben: Um was handelt es sich bei den schwarzen Verfärbungen auf der Eisenwolle bei Experiment 1? Unsere Vermutung ist, dass sich eventuell Keime gebildet haben könnten. Vielleicht haben diese Keime der Eisenoberfläche ebenfalls geschadet. Man könnte den Versuch noch einmal mit abgekochtem Wasser durchführen, um zu sehen, ob dann auch schwarze Verfärbungen auftreten. Wir stellen uns auch die Frage, was passiert wäre, wenn wir die Proben länger in den Reagenzgläsern gelassen hätten. Dieses müsste in einem weiteren Experiment überprüft werden. Warum gibt es im Experiment 2 keine schwarzen Verfärbungen auf den Eisennägeln? Hier haben wir auch Leitungswasser verwendet, in dem die Nägel sieben Tage gelegen haben. Die Nägel hatten keine schwarzen Stellen, waren dafür aber sehr rostig. Wir vermuten, dass das Verhältnis von Wasser und Luft für das Rosten und auch für die Entstehung der schwarzen Flecken eine Rolle gespielt hat. Wie lange genau hätten die Eisennägel und die Eisenwolle in Experiment 3 galvanisiert werden müssen? Wir gehen davon aus, dass wir die drei Nägel unterschiedlich lange galvanisiert haben, weil das Ergebnis so unterschiedlich ausfiel. Leider haben wir die Zeit nicht gemessen. Zukünftig werden wir bei entsprechenden Experimenten die Zeit messen. 8
10 5 Zusammenfassung Wir haben drei verschiedene Experimente durchgeführt, um herauszufinden, wie man Eisen vor dem Rosten schützen kann. Wir haben Eisenwolle und Eisennägel mit verschiedenen Substanzen behandelt bzw. galvanisiert. Dabei haben wir herausgefunden, dass Olivenöl und Galvanisierung Eisen vor dem Rosten schützt. Insgesamt sind aber auch viele neue Fragen aufgekommen. Diese müssten in weiteren Versuchsdurchführungen geklärt werden. 6 Quellen- und Literaturverzeichnis [1] Asselborn, W. Sek.II, Schroedel Verlag, Braunschweig 2009 [2] Tessloffs Schülerlexikon, Tessloff Verlag, Nürnberg (deutsche Ausgabe 2003) Weitere Unterstützung: Hilfe bei der elektronischen Textverarbeitung durch Karin Grzywatz-Dotsikas 9
Schulversuchspraktikum Großtechnische Elektrolyseverfah- ren/galvanisierung Kurzprotokoll
 Schulversuchspraktikum Johanna Osterloh Sommersemester 2015 Klassenstufen 11 & 12 Großtechnische Elektrolyseverfahren/Galvanisierung Kurzprotokoll Auf einen Blick: Das folgende Protokoll enthält einen
Schulversuchspraktikum Johanna Osterloh Sommersemester 2015 Klassenstufen 11 & 12 Großtechnische Elektrolyseverfahren/Galvanisierung Kurzprotokoll Auf einen Blick: Das folgende Protokoll enthält einen
Kopiervorlage 1: Eisen und Aluminium
 Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmenge
Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmenge
Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus:
 Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmasse
Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmasse
Rost und Rostschutz. Korrosion von Metallen: Der Versuch zum Rostvorgang [2-4]
![Rost und Rostschutz. Korrosion von Metallen: Der Versuch zum Rostvorgang [2-4] Rost und Rostschutz. Korrosion von Metallen: Der Versuch zum Rostvorgang [2-4]](/thumbs/53/32999580.jpg) Universität Regensburg Institut für Anorganische Chemie - Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Wintersemester 2011/2012 16.12.2011 Dozentin: Dr. M. Andratschke Referenten: Arthur Hellinger,
Universität Regensburg Institut für Anorganische Chemie - Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Wintersemester 2011/2012 16.12.2011 Dozentin: Dr. M. Andratschke Referenten: Arthur Hellinger,
Korrosion und Korrosionsschutz
 Schulversuchspraktikum Christian Köhler Sommersemester 2016 Klassenstufen 7&8 Korrosion und Korrosionsschutz Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll beinhaltet drei weitere Schülerversuche
Schulversuchspraktikum Christian Köhler Sommersemester 2016 Klassenstufen 7&8 Korrosion und Korrosionsschutz Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll beinhaltet drei weitere Schülerversuche
Warum korrodiert Eisen?
 Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Korrosion und Korrosionsschutz
 Schulversuchspraktikum Name: Alexander König Semester: Sommersemester 2015 Klassenstufen 7 & 8 Korrosion und Korrosionsschutz Kurzprotokoll Auf einen Blick: Dieses Protokoll zeigt in 3 Schülerversuchen
Schulversuchspraktikum Name: Alexander König Semester: Sommersemester 2015 Klassenstufen 7 & 8 Korrosion und Korrosionsschutz Kurzprotokoll Auf einen Blick: Dieses Protokoll zeigt in 3 Schülerversuchen
Rost und Rostschutz. Oxidation: Fe Fe 2+ + 2 e - Reduktion: ½ O 2 + H 2 O + 2 e - 2 OH - Redoxgleichung: Fe + ½ O 2 + H 2 O Fe 2+ + 2 OH -
 Universität Regensburg Institut für Anorganische Chemie - Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Sommersemester 2010 23.06.2010 Dozentin: Dr. M. Andratschke Referenten: Schlichting, Matthias/Will,
Universität Regensburg Institut für Anorganische Chemie - Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Sommersemester 2010 23.06.2010 Dozentin: Dr. M. Andratschke Referenten: Schlichting, Matthias/Will,
Rost und Rostschutz. Definitionen [1, 2] Versuch 1: Rostvorgang [3, 4]
![Rost und Rostschutz. Definitionen [1, 2] Versuch 1: Rostvorgang [3, 4] Rost und Rostschutz. Definitionen [1, 2] Versuch 1: Rostvorgang [3, 4]](/thumbs/55/37862002.jpg) Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Sommersemester 2011 29.06.2011 Dozentin: Dr. M. Andratschke Referenten: Graßold, Birgit
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Sommersemester 2011 29.06.2011 Dozentin: Dr. M. Andratschke Referenten: Graßold, Birgit
KORROSION UND KORROSIONSSCHUTZ VON METALLEN
 11. Einheit: KORROSION UND KORROSIONSSCHUTZ VON METALLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 16 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Korrosion und Korrosionsschutz von Metallen..
11. Einheit: KORROSION UND KORROSIONSSCHUTZ VON METALLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 16 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Korrosion und Korrosionsschutz von Metallen..
Verbrennung einer Kerze
 Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Verbrennung einer Kerze
 Verbrennung einer Kerze Zünde eine Kerze an und notiere deine Beobachtungen: Was passiert eigentlich genau bei der Verbrennung einer Kerze? Diese Frage versuchen wir in diesem Kapitel zu beantworten. Schauen
Verbrennung einer Kerze Zünde eine Kerze an und notiere deine Beobachtungen: Was passiert eigentlich genau bei der Verbrennung einer Kerze? Diese Frage versuchen wir in diesem Kapitel zu beantworten. Schauen
NEUWIED. Änderung der Leitfähigkeit verschiedener Stoffe. ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht.
 ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht NEUWIED Änderung der Leitfähigkeit verschiedener Stoffe Lisa Lindner Schule: Private Realschule der Ursulinen Calvarienberg Jugend forscht
ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht NEUWIED Änderung der Leitfähigkeit verschiedener Stoffe Lisa Lindner Schule: Private Realschule der Ursulinen Calvarienberg Jugend forscht
Rost und Rostschutz. Beobachtung: Nach wenigen Momenten steigt das Wasser im Glasröhrchen an.
 Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Wintersemester 2010/2011 26.11.2010 Dozentin: Dr. M. Andratschke Referenten: Forster, Robert
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Wintersemester 2010/2011 26.11.2010 Dozentin: Dr. M. Andratschke Referenten: Forster, Robert
Licht und Farben. Kurzprotokoll
 Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Nachweis von Eisen-Ionen mit Kaliumthiocyanat
 Name: Datum: Nachweis von Eisen- mit Kaliumthiocyanat Geräte 3 Bechergläser (100 ml), 4 Reagenzgläser, Reagenzglasständer, kleiner Trichter, Faltenfilter, Spatel Materialien Eisennagel, Muscheln (braun
Name: Datum: Nachweis von Eisen- mit Kaliumthiocyanat Geräte 3 Bechergläser (100 ml), 4 Reagenzgläser, Reagenzglasständer, kleiner Trichter, Faltenfilter, Spatel Materialien Eisennagel, Muscheln (braun
Rost und Rostschutz. Chemikalien: Rost, verdünnte Salzsäure HCl, Kaliumhexacyanoferrat(II)-Lösung K 4 [Fe(CN) 6 ]
![Rost und Rostschutz. Chemikalien: Rost, verdünnte Salzsäure HCl, Kaliumhexacyanoferrat(II)-Lösung K 4 [Fe(CN) 6 ] Rost und Rostschutz. Chemikalien: Rost, verdünnte Salzsäure HCl, Kaliumhexacyanoferrat(II)-Lösung K 4 [Fe(CN) 6 ]](/thumbs/28/13018795.jpg) Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsversuche im Sommersemester 2009 24.06.2009 Dozentin: Dr. M. Andratschke Referenten: Mühlbauer, Manuel
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsversuche im Sommersemester 2009 24.06.2009 Dozentin: Dr. M. Andratschke Referenten: Mühlbauer, Manuel
Gefahrenstoffe. P: Zinknitrat-Hexahydrat-Lösung H: P:
 Redoxreihe Der Versuch führt den SuS vor Augen, dass sich nicht jedes Metall von jeder Metallsalz-Lösung oxidieren lässt, sondern dass es viel mehr eine experimentell zu ermittelnde Gesetzmäßigkeit dahintersteckt.
Redoxreihe Der Versuch führt den SuS vor Augen, dass sich nicht jedes Metall von jeder Metallsalz-Lösung oxidieren lässt, sondern dass es viel mehr eine experimentell zu ermittelnde Gesetzmäßigkeit dahintersteckt.
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Schulversuchspraktikum. Anna Hille. Sommersemester Klassenstufen 7 & 8. Korrosion
 Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 7 & 8 Korrosion 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet Versuche zum Thema
Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 7 & 8 Korrosion 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet Versuche zum Thema
SÄUR E. BASE oder LAU GE SAUE R BASI SCH
 SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
Inhalt. Tag Tag Tag Tag Tag
 Inhalt Ziel des Experiments:... 2 Vorbereitung:... 2 In welcher Lösung halten sich Schnittblumen am besten?... 2 Materialien:... 2 Durchführung:... 3 Tag 1... 3 Beobachtung:... 4 Tag 2... 4 Tag 3... 4
Inhalt Ziel des Experiments:... 2 Vorbereitung:... 2 In welcher Lösung halten sich Schnittblumen am besten?... 2 Materialien:... 2 Durchführung:... 3 Tag 1... 3 Beobachtung:... 4 Tag 2... 4 Tag 3... 4
Job 1: Verschmutzung durch Kochsalz
 Was ist zu tun? Bei diesem LernJob bekommt ihr von eurer Lehrerin/eurem Lehrer sauberes Leitungswasser in einem Erlenmeyerkolben. Außerdem bekommt ihr einen Stoff, mit dem ihr das Wasser verschmutzt. Gut
Was ist zu tun? Bei diesem LernJob bekommt ihr von eurer Lehrerin/eurem Lehrer sauberes Leitungswasser in einem Erlenmeyerkolben. Außerdem bekommt ihr einen Stoff, mit dem ihr das Wasser verschmutzt. Gut
Station 1. Glänzend gemacht!! - Das Aussehen von Metallen
 Station 1 Glänzend gemacht!! - Das Aussehen von Metallen Gegenstände: Silber-Löffel, -Draht, Eisen-Platte, Zinn-Rohr, Zink-Blech, Aluminium-Stück, Metall-Politur weißes Küchenpapier Gib 1 Tropfen Metall-Politur
Station 1 Glänzend gemacht!! - Das Aussehen von Metallen Gegenstände: Silber-Löffel, -Draht, Eisen-Platte, Zinn-Rohr, Zink-Blech, Aluminium-Stück, Metall-Politur weißes Küchenpapier Gib 1 Tropfen Metall-Politur
Untersuche das Verhalten von Zitronensäure gegenüber verschiedene Stoffen in Wasser und in Aceton.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P758500).6 Brönstedt Säuren - Aciditätvergleich einer wässrigen und einer acetonischen Citronensäurel Experiment von: Phywe Gedruckt: 5.0.203
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P758500).6 Brönstedt Säuren - Aciditätvergleich einer wässrigen und einer acetonischen Citronensäurel Experiment von: Phywe Gedruckt: 5.0.203
Korrosion von Eisen Kathodischer Schutz. Autoren: Felix Iseli Philip Fankhauser
 Laborbericht Chemie Korrosion von Eisen Kathodischer Schutz Autoren: Felix Iseli iself2@bfh.ch, Philip Fankhauser fankp2@bfh.ch Dozent: Gerhard Tschopp gerhard.tschopp@hti.bfh.ch Berner Fachhochschule
Laborbericht Chemie Korrosion von Eisen Kathodischer Schutz Autoren: Felix Iseli iself2@bfh.ch, Philip Fankhauser fankp2@bfh.ch Dozent: Gerhard Tschopp gerhard.tschopp@hti.bfh.ch Berner Fachhochschule
Stoffeigenschaften auf der Spur
 Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz
 Name: Datum: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz Geräte Becherglas, Spatel, Alu-Teelichtschale, Heizplatte, Pipette, Tiegelzange, Glasstab, Lupe Materialien Kochsalz
Name: Datum: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz Geräte Becherglas, Spatel, Alu-Teelichtschale, Heizplatte, Pipette, Tiegelzange, Glasstab, Lupe Materialien Kochsalz
Arbeitsblatt Ist groß besser als klein?
 Arbeitsblatt Ist groß besser als klein? Aufgabe 1: Führe folgendes Experiment durch und notiere deine Beobachtungen. Materialien: 4 Reagenzgläser, Reagenzglasständer, Spatel Chemikalien: Gefahrenstoffe
Arbeitsblatt Ist groß besser als klein? Aufgabe 1: Führe folgendes Experiment durch und notiere deine Beobachtungen. Materialien: 4 Reagenzgläser, Reagenzglasständer, Spatel Chemikalien: Gefahrenstoffe
Gemische. Zeitangabe: 8 min SCHUTZBRILLE NICHT VERGESSEN! VERSUCH 1 VERSUCH 2
 Gemische Zeitangabe: 8 min SCHUTZBRILLE NICHT VERGESSEN! Materialien: Becherglas, Spatel Chemikalien: Wasser, Tinte VERSUCH 1 Gebt in das Becherglas ca. 2 cm hoch Wasser und gebt dann fünf Tropfen Tinte
Gemische Zeitangabe: 8 min SCHUTZBRILLE NICHT VERGESSEN! Materialien: Becherglas, Spatel Chemikalien: Wasser, Tinte VERSUCH 1 Gebt in das Becherglas ca. 2 cm hoch Wasser und gebt dann fünf Tropfen Tinte
Luft ist nicht Nichts
 Luft ist nicht Nichts Experiment 1 Luft im Glas: Durchführung: Ein offenes Glas wird verkehrt herum in eine Schale voller Wasser getaucht. Luft im Glas Wasser Beobachtung: Das Glas bleibt auch unter Wasser
Luft ist nicht Nichts Experiment 1 Luft im Glas: Durchführung: Ein offenes Glas wird verkehrt herum in eine Schale voller Wasser getaucht. Luft im Glas Wasser Beobachtung: Das Glas bleibt auch unter Wasser
Titel: Faszination Feuer
 Titel: Faszination Feuer 1 Kurzbeschreibung: Das Feuer übt bereits auf junge Kinder eine besonders große Faszination aus und weckt ihr Interesse sich forschend und entdeckend naturwissenschaftlichen Grundeinsichten
Titel: Faszination Feuer 1 Kurzbeschreibung: Das Feuer übt bereits auf junge Kinder eine besonders große Faszination aus und weckt ihr Interesse sich forschend und entdeckend naturwissenschaftlichen Grundeinsichten
Säuren und Basen im Haushalt
 Schulversuchspraktikum Lars Lichtenberg Sommersemester 2015 Klassenstufen 9 & 10 Säuren und Basen im Haushalt Kurzprotokoll Auf einen Blick: Die Unterrichtseinheit,,Säuren und Basen im Haushalt für die
Schulversuchspraktikum Lars Lichtenberg Sommersemester 2015 Klassenstufen 9 & 10 Säuren und Basen im Haushalt Kurzprotokoll Auf einen Blick: Die Unterrichtseinheit,,Säuren und Basen im Haushalt für die
Steckbrief-Test. 1 Überprüfe, ob die Stoff-Steckbriefe richtig sind. Wenn nicht, fertige einen überarbeiteten Steckbrief im Heft an.
 Steckbrief-Test Emma soll für die Schule Stoff-Steckbriefe zu vier verschiedenen Stoffen erstellen. Im Internet hat sie folgende Stoff-Steckbriefe gefunden. Bei manchen Angaben hat sie aber Zweifel, ob
Steckbrief-Test Emma soll für die Schule Stoff-Steckbriefe zu vier verschiedenen Stoffen erstellen. Im Internet hat sie folgende Stoff-Steckbriefe gefunden. Bei manchen Angaben hat sie aber Zweifel, ob
Rezepte: 1. Brause herstellen
 1D Rezepte: 1. Brause herstellen zutaten ½ TL Natron 2 TL Zucker 1 TL Zitronensäure 200 ml Wasser zubereitung Natron, Zucker und Zitronensäure in das Glas geben. Das Wasser hinzufügen. aufgaben Vergleiche
1D Rezepte: 1. Brause herstellen zutaten ½ TL Natron 2 TL Zucker 1 TL Zitronensäure 200 ml Wasser zubereitung Natron, Zucker und Zitronensäure in das Glas geben. Das Wasser hinzufügen. aufgaben Vergleiche
HERFORD. Dichte - Ein spannendes oder langweiliges Thema. ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht.
 ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht HERFORD Dichte - Ein spannendes oder langweiliges Thema Jannik Rönsch Schule: Königin-Mathilde-Gymnasium Vlothoer Straße 1 32049 Herford
ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht HERFORD Dichte - Ein spannendes oder langweiliges Thema Jannik Rönsch Schule: Königin-Mathilde-Gymnasium Vlothoer Straße 1 32049 Herford
INHALTSVERZEICHNIS. 7 Temperatur und Zustandsänderungen 48 V1 Einfaches Flüssigkeitsthermometer 48 V2 Bimetallthermometer 50 Warm und kalt 52
 INHALTSVERZEICHNIS Verhaltensregeln 3 Einführung in das Praxisbuch 4 1 Physik bestimmt unser Leben 6 V1 Längenmessung 6 V2 Messung des Volumens 8 Exp Schwingunsdauer 10 Mein Zeigefinger! 12 2 Alles in
INHALTSVERZEICHNIS Verhaltensregeln 3 Einführung in das Praxisbuch 4 1 Physik bestimmt unser Leben 6 V1 Längenmessung 6 V2 Messung des Volumens 8 Exp Schwingunsdauer 10 Mein Zeigefinger! 12 2 Alles in
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung
 V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
Geht dir ein Licht auf?
 Geht dir ein Licht auf? Im folgenden Experiment wirst du erfahren, wie du mit einfachen Mitteln ein Lämpchen zum Leuchten bringst. Materialien - Glühlämpchen - Flachbatterie Auftrag Die folgenden Abbildungen
Geht dir ein Licht auf? Im folgenden Experiment wirst du erfahren, wie du mit einfachen Mitteln ein Lämpchen zum Leuchten bringst. Materialien - Glühlämpchen - Flachbatterie Auftrag Die folgenden Abbildungen
Kompetenzen und Aufgabenbeispiele Natur und Technik
 Institut für Bildungsevaluation Assoziiertes Institut der Universität Zürich Kompetenzen und Aufgabenbeispiele Natur und Technik Informationen für Lehrpersonen und Eltern 1. Wie sind die Ergebnisse dargestellt?
Institut für Bildungsevaluation Assoziiertes Institut der Universität Zürich Kompetenzen und Aufgabenbeispiele Natur und Technik Informationen für Lehrpersonen und Eltern 1. Wie sind die Ergebnisse dargestellt?
Chemische Reaktionen. Wir erzeugen Wasser
 hemische Reaktionen + Natrium + -> hlor -> Natriumchlorid = Kochsalz Wir erzeugen Wasser Die kleinsten Teilchen des Sauerstoffes und des Wasserstoffes waren im roten Ballon bereits gut durchmischt. Daher
hemische Reaktionen + Natrium + -> hlor -> Natriumchlorid = Kochsalz Wir erzeugen Wasser Die kleinsten Teilchen des Sauerstoffes und des Wasserstoffes waren im roten Ballon bereits gut durchmischt. Daher
Praktikum Umwelt- und technikbedingte Werkstoffkorrosion
 Bauhaus-Universität Weimar Praktikum Umwelt- und technikbedingte Werkstoffkorrosion V2: Metallkorrosion V 2-1: Korrosion von Metallen am Beispiel von Eisen V 2-2: Spannungsrisskorrosionsversuch mit Ammoniak
Bauhaus-Universität Weimar Praktikum Umwelt- und technikbedingte Werkstoffkorrosion V2: Metallkorrosion V 2-1: Korrosion von Metallen am Beispiel von Eisen V 2-2: Spannungsrisskorrosionsversuch mit Ammoniak
Versuch 1: Wie kalt wird es, wenn man Kochsalz mit Eis mischt?
 : Wie kalt wird es, wenn man Kochsalz mit Eis mischt? Man wiege sich in je einem 250 ml-becher aus Kunststoff Kochsalz und Wasser ab und vermische sie innig, indem man das Salz zu dem Eis gibt und gut
: Wie kalt wird es, wenn man Kochsalz mit Eis mischt? Man wiege sich in je einem 250 ml-becher aus Kunststoff Kochsalz und Wasser ab und vermische sie innig, indem man das Salz zu dem Eis gibt und gut
Wie kommt das rohe Ei in die Flasche?
 Wie kommt das rohe Ei in die Flasche? Themenbereich: Wärme/ Kälte Überdruck, Kalk wird aufgelöst Alter der Kinder: Dieses Experiment eignet sich für Kinder ab ca. 5 Jahren. Dabei ist zu beachten, dass
Wie kommt das rohe Ei in die Flasche? Themenbereich: Wärme/ Kälte Überdruck, Kalk wird aufgelöst Alter der Kinder: Dieses Experiment eignet sich für Kinder ab ca. 5 Jahren. Dabei ist zu beachten, dass
Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle
 Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Schwimmen und Sinken
 Schwimmen und Sinken 13.12.2012 Schule: VS Himberg Schulstufe: 4. Klasse Schüleranzahl einer Klasse: ca. 20 Kinder Material: Wannen mit Wasser (Glas; durchsichtig) Wasserbomben Kleine Steine oder Sand
Schwimmen und Sinken 13.12.2012 Schule: VS Himberg Schulstufe: 4. Klasse Schüleranzahl einer Klasse: ca. 20 Kinder Material: Wannen mit Wasser (Glas; durchsichtig) Wasserbomben Kleine Steine oder Sand
Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann.
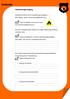 Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Untersuche an einigen Beispielen, welche Grundstoffe am Aufbau unserer Nahrung beteiligt sind.
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802200) 4. Nahrungsmittel und Nährstoffe Experiment von: Phywe Gedruckt: 07.0.203 5:36:8 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802200) 4. Nahrungsmittel und Nährstoffe Experiment von: Phywe Gedruckt: 07.0.203 5:36:8 intertess (Version
Dem Täter auf der Spur
 Dem Täter auf der Spur (Ein Projekt der TU Braunschweig, Prof. Dr. P. Mischnick) Heute werdet Ihr verschiedene chemische Methoden kennenlernen, mit denen z.b. die Polizei Kriminalfälle auflöst. Zuerst
Dem Täter auf der Spur (Ein Projekt der TU Braunschweig, Prof. Dr. P. Mischnick) Heute werdet Ihr verschiedene chemische Methoden kennenlernen, mit denen z.b. die Polizei Kriminalfälle auflöst. Zuerst
GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN
 10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
Korrosion und Korrosionsschutz
 Schulversuchspraktikum Sommersemester 2013 Klassenstufen 11 & 12 Korrosion und Korrosionsschutz 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch
Schulversuchspraktikum Sommersemester 2013 Klassenstufen 11 & 12 Korrosion und Korrosionsschutz 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch
Schülerversuche mit Präsentation rund um die Osmose
 Schülerversuche mit Präsentation rund um die Osmose Mögliche Experimente: Übersicht 1 2 3 Experiment Pflanzenstängel in demineralisiertem Wasser bzw. in Salzlösung Pflanzengewebe in Salzlösungen unterschiedlicher
Schülerversuche mit Präsentation rund um die Osmose Mögliche Experimente: Übersicht 1 2 3 Experiment Pflanzenstängel in demineralisiertem Wasser bzw. in Salzlösung Pflanzengewebe in Salzlösungen unterschiedlicher
Unterrichtsentwurf Physik
 Universität Duisburg-Essen Fachbereich DaZ/DaF Seminar: Sprachförderung im Physikunterricht Unterrichtsentwurf Physik Alice Jarosik Tobias Bezold Marion Matusik Volker Fleck Fach: Physik Thema der Stunde:
Universität Duisburg-Essen Fachbereich DaZ/DaF Seminar: Sprachförderung im Physikunterricht Unterrichtsentwurf Physik Alice Jarosik Tobias Bezold Marion Matusik Volker Fleck Fach: Physik Thema der Stunde:
Elektrizität VARTA. Dieses Skript gehört:
 Elektrizität VARTA Dieses Skript gehört: Versuch 1: Elektrostatik, was ist das? Elektrizität Seite 2 Fleecestoff oder Wollsocke Seidenpapierschnipsel Bleistift Luftballon 1.1 1. Reibe einen aufgeblasenen
Elektrizität VARTA Dieses Skript gehört: Versuch 1: Elektrostatik, was ist das? Elektrizität Seite 2 Fleecestoff oder Wollsocke Seidenpapierschnipsel Bleistift Luftballon 1.1 1. Reibe einen aufgeblasenen
Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden?
 Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden? Beschrifte die Kästchen mit je einem Aggregatzustand. Benenne die Nummern, es handelt sich dabei um Fachbegriffe für die Übergänge
Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden? Beschrifte die Kästchen mit je einem Aggregatzustand. Benenne die Nummern, es handelt sich dabei um Fachbegriffe für die Übergänge
Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz
 Name: Datum: Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz Material: Kochsalz (NaCl), Leitungswasser, Mineralwasser, Becherglas, Spatel, destilliertes Wasser, Alu-Teelichtschalen,
Name: Datum: Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz Material: Kochsalz (NaCl), Leitungswasser, Mineralwasser, Becherglas, Spatel, destilliertes Wasser, Alu-Teelichtschalen,
Schulversuchspraktikum. Miriam Jarrar. Sommersemester Klassenstufen 7 & 8. Korrosion
 Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 7 & 8 Korrosion 1 Kontext und Ziele 1 Auf einen Blick: Dieses Protokoll beinhaltet 2 Lehrerversuche und 4 Schülerversuche für die
Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 7 & 8 Korrosion 1 Kontext und Ziele 1 Auf einen Blick: Dieses Protokoll beinhaltet 2 Lehrerversuche und 4 Schülerversuche für die
Reaktionen von Metallen mit Sauerstoff und mit Luft
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Stoffe und ihre Eigenschaften
 Stoffe und ihre Eigenschaften von PH Vorarlberg Seite 1 Kelterer Stefanie Forscherauftrag Nr. 1 Warum streut man im Winter Salz auf die Straße? 1 Glas Thermometer Eiswürfel Salz 1. Fülle das Glas mit Eiswürfeln.
Stoffe und ihre Eigenschaften von PH Vorarlberg Seite 1 Kelterer Stefanie Forscherauftrag Nr. 1 Warum streut man im Winter Salz auf die Straße? 1 Glas Thermometer Eiswürfel Salz 1. Fülle das Glas mit Eiswürfeln.
Material: Rotkohlblätter, Eiklar, Essigsäurelösung (w=10%), Speiseöl, Spülmittel farblos verdünnt mit Wasser 1:1, Wasser, 9 Reagenzgläser, Messer.
 Bau der Biomembran Experiment mit Rotkohl: Indirekter Nachweis von Membranbestandteilen verändert nach Feldermann, D. (2004). Schwerpunktmaterialien Linder Biologie Band 1. Hannover, Schroedel Fragestellung:
Bau der Biomembran Experiment mit Rotkohl: Indirekter Nachweis von Membranbestandteilen verändert nach Feldermann, D. (2004). Schwerpunktmaterialien Linder Biologie Band 1. Hannover, Schroedel Fragestellung:
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser"
 Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser" a) Identifizierung des entstehenden Gases: Chemikalien: Geräte: Lithium [C] [F], Natrium [C] [F] (jeweils in Benzin mit Siedebereich 90-110
Identifizierung der Produkte der Reaktion "Alkalimetalle + Wasser" a) Identifizierung des entstehenden Gases: Chemikalien: Geräte: Lithium [C] [F], Natrium [C] [F] (jeweils in Benzin mit Siedebereich 90-110
Versuche zur Untersuchung von Fruchtfarbstoffen
 Versuche zur Untersuchung von Fruchtfarbstoffen Durchgeführt und protokolliert von: Annika Bauland, Corinna Brockers, Anne Jonas, Isabelle Schmidt 1.Versuch: Dünnschichtchromatographie Für diesen Versuch
Versuche zur Untersuchung von Fruchtfarbstoffen Durchgeführt und protokolliert von: Annika Bauland, Corinna Brockers, Anne Jonas, Isabelle Schmidt 1.Versuch: Dünnschichtchromatographie Für diesen Versuch
V 1 Herstellung von Natriumchlorid
 1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
VERSTEHEN UND VERARBEITEN EINES LESETEXTES
 VERSTEHEN UND VERARBEITEN EINES LESETEXTES Die Nanotechnologie eine wichtige Technologie des 21. Jahrhunderts 1 2 3 4 5 6 7 8 9 10 11 Vor etwa sechs Jahren wurde in der Wissenschaftswelt ein neuer Begriff
VERSTEHEN UND VERARBEITEN EINES LESETEXTES Die Nanotechnologie eine wichtige Technologie des 21. Jahrhunderts 1 2 3 4 5 6 7 8 9 10 11 Vor etwa sechs Jahren wurde in der Wissenschaftswelt ein neuer Begriff
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
4.9 Funktion des Gallensafts. Aufgabe. Was bewirkt der Gallensaft?
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P803000) 4.9 Funktion des Gallensafts Experiment von: Phywe Gedruckt: 07.0.203 5:54:3 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P803000) 4.9 Funktion des Gallensafts Experiment von: Phywe Gedruckt: 07.0.203 5:54:3 intertess (Version
Gefahrenstoffe. 7 Bechergläser (100 ml), 1 Becherglas (1 L), Spatel, Wasser, Messzylinder, Glaswanne, Kartoffel
 1.1 Zersetzung von H 2O 2 mithilfe verschiedener Katalysatoren [4] Der Zerfall von Wasserstoffperoxid kann mithilfe vieler verschiedener Katalysatoren beschleunigt werden. In diesem Versuch sollen einige
1.1 Zersetzung von H 2O 2 mithilfe verschiedener Katalysatoren [4] Der Zerfall von Wasserstoffperoxid kann mithilfe vieler verschiedener Katalysatoren beschleunigt werden. In diesem Versuch sollen einige
Versuchsanleitung befolgen, Stärkenachweis, wichtigste Stärkepflanzen, Bio-Kunststoffe aus Stärke
 Stations-Info für die Lehrkraft Stärkenachweis Versuchsanleitung befolgen, Stärkenachweis, wichtigste Stärkepflanzen, Bio-Kunststoffe aus Stärke Stationsziel: SuS sollen genau und ordentlich nach der Versuchsanleitung
Stations-Info für die Lehrkraft Stärkenachweis Versuchsanleitung befolgen, Stärkenachweis, wichtigste Stärkepflanzen, Bio-Kunststoffe aus Stärke Stationsziel: SuS sollen genau und ordentlich nach der Versuchsanleitung
Korrosion und Korrosionsschutz
 Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 7 & 8 Korrosion und Korrosionsschutz Auf einen Blick: Diese Unterrichtseinheit für die Klassen 7 & 8 enthält 1 Schülerversuch und
Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 7 & 8 Korrosion und Korrosionsschutz Auf einen Blick: Diese Unterrichtseinheit für die Klassen 7 & 8 enthält 1 Schülerversuch und
Schüler und Schülerinnen im Labor in Rechtenthal. 5 weiße Stoffe. Name:. Klasse: Lehrpersonen: Schule: Ich arbeite in einer Gruppe mit:..
 Schüler und Schülerinnen im Labor in Rechtenthal 5 weiße Stoffe Datum: Name:. Klasse: Lehrpersonen: Schule: Ich arbeite in einer Gruppe mit:.. .. Chemische Laborgeräte (www.seilnacht.com) (Die Laborgeräte,
Schüler und Schülerinnen im Labor in Rechtenthal 5 weiße Stoffe Datum: Name:. Klasse: Lehrpersonen: Schule: Ich arbeite in einer Gruppe mit:.. .. Chemische Laborgeräte (www.seilnacht.com) (Die Laborgeräte,
B E I S P I E L A R B E I T / Aufgaben. Kultusministerium
 B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
Chemie zur Weihnacht. Farbreihe
 Farbreihe Reagenzien: 2 ml Phenolphthalein in 200 ml Wasser verdünnte Natronlauge in Tropfflasche Kaliumpermanganat 2,5 g Eisen(II)-sulfat in 50 ml Wasser 2,5 g Kaliumthiocyanat in 50 ml Wasser 2,5 g Kaliumhexacyanoferrat(II)
Farbreihe Reagenzien: 2 ml Phenolphthalein in 200 ml Wasser verdünnte Natronlauge in Tropfflasche Kaliumpermanganat 2,5 g Eisen(II)-sulfat in 50 ml Wasser 2,5 g Kaliumthiocyanat in 50 ml Wasser 2,5 g Kaliumhexacyanoferrat(II)
Mische einige Stoffe mit Wasser und untersuche die entstandenen Gemischarten.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
JUFOTech. wko.at/tirol/jufotech DATENBLATT. Jugend forscht in der Technik. Titel der Projektarbeit: Fachgebiet:
 Datenblatt (dient als Titelblatt für die Projektarbeit) Seite 1/2 JUFOTech Jugend forscht in der Technik wko.at/tirol/jufotech DATENBLATT Wir nehmen am Wettbewerb Jugend forscht in der Technik Auf den
Datenblatt (dient als Titelblatt für die Projektarbeit) Seite 1/2 JUFOTech Jugend forscht in der Technik wko.at/tirol/jufotech DATENBLATT Wir nehmen am Wettbewerb Jugend forscht in der Technik Auf den
Fortbildung am Schülerlabor in Rechtenthal für die Grundschule. Ideen zu weiterführenden Versuchen in der Klasse:
 Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Carbonat, Hydrogencarbonat
 Chlorid a) Die Lösung die einer Menge Substanz, die etwa 2 mg Chlorid entspricht, in 2 ml Wasser R oder 2 ml der vorgeschrieben Lösung werden verwendet. Diese Lösung wird mit verdünnter Salpetersäure R
Chlorid a) Die Lösung die einer Menge Substanz, die etwa 2 mg Chlorid entspricht, in 2 ml Wasser R oder 2 ml der vorgeschrieben Lösung werden verwendet. Diese Lösung wird mit verdünnter Salpetersäure R
Nährstoffe und Nahrungsmittel
 1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
Forschertagebuch. Auftrieb Wasser. Name: Klasse: PH Vorarlberg Seite 1 Fischer Rebecca
 Forschertagebuch Auftrieb im Wasser Name: Klasse: PH Vorarlberg Seite 1 Fischer Rebecca Datum: Forscherauftrag Nr. 1 Die Kraft im Wasser Du brauchst: 1 kleine Plastikschüssel 1 kleines Holzbrettchen Wasser
Forschertagebuch Auftrieb im Wasser Name: Klasse: PH Vorarlberg Seite 1 Fischer Rebecca Datum: Forscherauftrag Nr. 1 Die Kraft im Wasser Du brauchst: 1 kleine Plastikschüssel 1 kleines Holzbrettchen Wasser
Korrosion und Korrosionsschtz
 Schulversuchspraktikum Christian Köhler Sommersemester 2016 Klassenstufen 7 & 8 Korrosion und Korrosionsschtz 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll stehen
Schulversuchspraktikum Christian Köhler Sommersemester 2016 Klassenstufen 7 & 8 Korrosion und Korrosionsschtz 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll stehen
Nachweis von Mikroorganismen 1
 Vorüberlegungen Nachweis von Mikroorganismen 1 Die Durchführung von mikrobiologischen Versuchen zum Nachweis von Mikroorganismen ist für Schülerinnen und Schüler und Schüler besonders motivierend. Für
Vorüberlegungen Nachweis von Mikroorganismen 1 Die Durchführung von mikrobiologischen Versuchen zum Nachweis von Mikroorganismen ist für Schülerinnen und Schüler und Schüler besonders motivierend. Für
Verlaufsprotokoll. 1. Unterrichtseinheit zum Thema Luft und Luftdruck: Eigenschaften von warmer Luft untersuchen
 Verlaufsprotokoll 1. Unterrichtseinheit zum Thema Luft und Luftdruck: Eigenschaften von warmer Luft untersuchen 1. Doppelstunde: Was passiert mit eingesperrter, warmer Luft? Dritte Klasse anwesend: 19
Verlaufsprotokoll 1. Unterrichtseinheit zum Thema Luft und Luftdruck: Eigenschaften von warmer Luft untersuchen 1. Doppelstunde: Was passiert mit eingesperrter, warmer Luft? Dritte Klasse anwesend: 19
Wirkungsnachweis der Güllebehandlung
 Wirkungsnachweis der Güllebehandlung Einfluss von plocher gülle & jauche auf Flüssigmist von Milchkühen Einleitung Betrieb Yves Mongeau Im Rahmen eines Forschungsprojekts wurden 27 unter dem Patronat des
Wirkungsnachweis der Güllebehandlung Einfluss von plocher gülle & jauche auf Flüssigmist von Milchkühen Einleitung Betrieb Yves Mongeau Im Rahmen eines Forschungsprojekts wurden 27 unter dem Patronat des
1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat
 1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat Geräte/Chemikalien: Mörser mit Pistill, feuerfeste Unterlage, Zucker, Kaliumnitrat, Zünder: Kaliumpermanganat
1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat Geräte/Chemikalien: Mörser mit Pistill, feuerfeste Unterlage, Zucker, Kaliumnitrat, Zünder: Kaliumpermanganat
Klassenarbeitsaufgaben
 Klassenarbeitsaufgaben Untersuchung von Limonade und wasser 1. Erik möchte seine Lieblingslimonade untersuchen. Zuerst muss er das störende Kohlenstoffdioxid ( Kohlensäure ) entfernen. Dazu stehen ihm
Klassenarbeitsaufgaben Untersuchung von Limonade und wasser 1. Erik möchte seine Lieblingslimonade untersuchen. Zuerst muss er das störende Kohlenstoffdioxid ( Kohlensäure ) entfernen. Dazu stehen ihm
Eine unbekannte Flüssigkeit. Darum geht s bei diesem LernJob:
 LernJob BNT, Klasse 5/6 BNT MUSTERLÖSUNG Eine unbekannte Flüssigkeit Euer Lehrer/ eure Lehrerin hat euch eine unbekannte Flüssigkeit gegeben. Auf den ersten Blick spricht einiges dafür, dass es sich hierbei
LernJob BNT, Klasse 5/6 BNT MUSTERLÖSUNG Eine unbekannte Flüssigkeit Euer Lehrer/ eure Lehrerin hat euch eine unbekannte Flüssigkeit gegeben. Auf den ersten Blick spricht einiges dafür, dass es sich hierbei
Korrosion. Salze. Vom Konkreten zum Abstrakten!
 Korrosion Klassenstufe Oberthemen Unterthemen Anforderungsniveau 9-10 Anorganische Chemie, Elektrochemie Salze Durchführung sniveau Vorlauf Vorbereitung Durchführung - ca. 10-30 min. ca. 45min. Rosten
Korrosion Klassenstufe Oberthemen Unterthemen Anforderungsniveau 9-10 Anorganische Chemie, Elektrochemie Salze Durchführung sniveau Vorlauf Vorbereitung Durchführung - ca. 10-30 min. ca. 45min. Rosten
Eine unbekannte Flüssigkeit. Darum geht s bei diesem LernJob:
 LernJob BNT, Klasse 5/6 BNT Eine unbekannte Flüssigkeit Euer Lehrer/ eure Lehrerin hat euch eine unbekannte Flüssigkeit gegeben. Auf den ersten Blick spricht einiges dafür, dass es sich hierbei einfach
LernJob BNT, Klasse 5/6 BNT Eine unbekannte Flüssigkeit Euer Lehrer/ eure Lehrerin hat euch eine unbekannte Flüssigkeit gegeben. Auf den ersten Blick spricht einiges dafür, dass es sich hierbei einfach
Wirksamkeit von Grander-Wasser
 Wirksamkeit von Grander-Wasser Beitrag zum Wettbewerb Schüler experimentieren 2007 von Sebastian Prüfling aus Beutelsbach Gymnasium Vilshofen 1 Inhaltsverzeichnis Seite 2: Seite 3: Seite 6: Inhaltsverzeichnis,
Wirksamkeit von Grander-Wasser Beitrag zum Wettbewerb Schüler experimentieren 2007 von Sebastian Prüfling aus Beutelsbach Gymnasium Vilshofen 1 Inhaltsverzeichnis Seite 2: Seite 3: Seite 6: Inhaltsverzeichnis,
HTBL-PINKAFELD Arbeitsblatt A3/1 1.Station: KOHLENMONOXID. VORSICHT: Ameisensäure und konz. Schwefelsäure sind gefährliche Chemikalien!!
 HTBL-PINKAFELD Arbeitsblatt A3/1 1.Station: KOHLENMONOXID ÜBUNG: KOHLENMONOXID Für diese Versuche brauchst du: Proberöhren Proberöhrenständer Proberöhrenhalter Laborbrenner Ameisensäure konz. Schwefelsäure
HTBL-PINKAFELD Arbeitsblatt A3/1 1.Station: KOHLENMONOXID ÜBUNG: KOHLENMONOXID Für diese Versuche brauchst du: Proberöhren Proberöhrenständer Proberöhrenhalter Laborbrenner Ameisensäure konz. Schwefelsäure
Einfache Elektrolysen und Leitfähigkeit
 Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 9&10 Einfache Elektrolysen und Leitfähigkeit Auf einen Blick: Zum Thema Einfache Elektrolysen und Leitfähigkeit können zahlreiche anschauliche
Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 9&10 Einfache Elektrolysen und Leitfähigkeit Auf einen Blick: Zum Thema Einfache Elektrolysen und Leitfähigkeit können zahlreiche anschauliche
Was passiert mit Zucker, wenn er unsichtbar wird? Lösungen
 Was passiert mit Zucker, wenn er unsichtbar wird? Lösungen Material Demoversuch mit Zucker 10 g Haushaltszucker 20 g Hahnenwasser 2 Plastikbecher (ca. 3 dl) 1 Küchenwaage 1 metallener Esslöffel Material
Was passiert mit Zucker, wenn er unsichtbar wird? Lösungen Material Demoversuch mit Zucker 10 g Haushaltszucker 20 g Hahnenwasser 2 Plastikbecher (ca. 3 dl) 1 Küchenwaage 1 metallener Esslöffel Material
Galvanotechnik. 1. Definition Galvanotechnik (G.): 2. Theoretischer Hintergrund: [2]
![Galvanotechnik. 1. Definition Galvanotechnik (G.): 2. Theoretischer Hintergrund: [2] Galvanotechnik. 1. Definition Galvanotechnik (G.): 2. Theoretischer Hintergrund: [2]](/thumbs/27/11146675.jpg) Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsversuche im Wintersemester 2012/2013 23. November 2012 Betreuung: Frau Dr. M. Andratschke Referenten:
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsversuche im Wintersemester 2012/2013 23. November 2012 Betreuung: Frau Dr. M. Andratschke Referenten:
Was passiert mit Zucker, wenn er unsichtbar wird?
 Was passiert mit Zucker, wenn er unsichtbar wird? Material Demoversuch mit Zucker 10 g Haushaltszucker 20 g Hahnenwasser 2 Plastikbecher (ca. 3 dl) 1 Küchenwaage 1 metallener Esslöffel Material Schülerversuch
Was passiert mit Zucker, wenn er unsichtbar wird? Material Demoversuch mit Zucker 10 g Haushaltszucker 20 g Hahnenwasser 2 Plastikbecher (ca. 3 dl) 1 Küchenwaage 1 metallener Esslöffel Material Schülerversuch
Dokumentation Projekt Entwicklung einer Farbskala PLUS-Kurs SU 4+, GGS Vaalserquartier, Aachen
 Die Arbeitsgruppe Die Gemeinschaftsgrundschule Vaalserquartier ist eine zweizügige Grundschule im westlichsten Stadtteil von Aachen, 400 m von der Grenze zu den Niederlanden gelegen. Sie hat 230 SchülerInnen
Die Arbeitsgruppe Die Gemeinschaftsgrundschule Vaalserquartier ist eine zweizügige Grundschule im westlichsten Stadtteil von Aachen, 400 m von der Grenze zu den Niederlanden gelegen. Sie hat 230 SchülerInnen
Betriebsanweisung nach 20 Gefahrstoffverordnung. Verwendete Chemikalien /37/ Kupfer (Pulver) - -
 Versuche 85-91 3 Problemfeld Stoffkreisläufe Betriebsanweisung nach 20 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeits merkmale Ammoniumdiammintetrathiocyanatochromat(III)
Versuche 85-91 3 Problemfeld Stoffkreisläufe Betriebsanweisung nach 20 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeits merkmale Ammoniumdiammintetrathiocyanatochromat(III)
Film der Einheit Korrosion
 Film der Einheit Korrosion Beispiele von Korrosion an Eisen und Kupfer Elektrochemische Konzentrationskette Nernst - Gleichung Lokalekemente und Einfluss auf die Korrosion Säurekorrosion Sauerstoffkorrosion
Film der Einheit Korrosion Beispiele von Korrosion an Eisen und Kupfer Elektrochemische Konzentrationskette Nernst - Gleichung Lokalekemente und Einfluss auf die Korrosion Säurekorrosion Sauerstoffkorrosion
Herstellung des GST-Elementes (Graphit-Suszeptor-Tiegelsystem-Element)
 Herstellung des GST-Elementes (Graphit-Suszeptor-Tiegelsystem-Element) Suszeptor = Sammler Materialien Graphitspray Ofenmörtel (muss bis 1200 C beständig sein), Porzellantiegel (20 ml) Tonblumentopf (100
Herstellung des GST-Elementes (Graphit-Suszeptor-Tiegelsystem-Element) Suszeptor = Sammler Materialien Graphitspray Ofenmörtel (muss bis 1200 C beständig sein), Porzellantiegel (20 ml) Tonblumentopf (100
