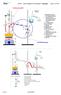
3.1. Physikalische Grundlagen 3.2. Einstufendestillation 3.3. Mehrstufendestillation (Rektifikation) 3.4. Destillation azeotroper Mischungen
|
|
|
- Heidi Schuster
- vor 7 Jahren
- Abrufe
Transkript
1 Einführung in die apparativen Methoden in der Organischen Chemie Ein Tutorial zum Organischen Praktikum als Hypertextsystem Erstellt von P. Kreitmeier, Universität Regensburg, März 2001 basierend auf einem Skript von S. Hünig, G. Märkl, J. Sauer, Universitäten Regensburg, Würzburg Kapitel 3 Destillation 3.1. Physikalische Grundlagen 3.2. Einstufendestillation 3.3. Mehrstufendestillation (Rektifikation) 3.4. Destillation azeotroper Mischungen
2 Die Destillation ist die vielseitigste Methode zur Reinigung von Flüssigkeiten und zur Trennung von Flüssigkeitsgemischen. Voraussetzung ist, daß sich die Substanzen ohne Zersetzung bei Normaldruck oder im Vakuum verdampfen lassen Physikalische Grundlagen Die wesentlichen physikalischen Zusammenhänge wurden bereits im Abschnitt 2.2 bei der Diskussion des Siedepunkts besprochen: Die Moleküle einer Flüssigkeit sind beweglich, ständig entweichen Moleküle durch die Flüssigkeitsoberfläche in den umgebenden Gasraum (Verdampfung) und kehren wieder in die Flüssigkeit zurück (Kondensation). In einem abgeschlossenen System stellt sich ein Gleichgewicht zwischen Verdampfung und Kondensation ein; jede Flüssigkeit besitzt einen charakteristischen, von der Temperatur abhängigen Dampfdruck. Mit steigender Temperatur steigt auch der Dampfdruck einer Verbindung (Abb. 3.1 und Tab. 3.1). Erreicht der Dampfdruck einer Substanz den äußeren Druck des Systems geht sie vollständig in die Gasphase über. Abb. 3.1: Dampfdruckkurven von Diethylether, Ethanol und Wasser Druck [hpa] 1000 Ether log p 3.0 Ether Ethanol 500 Wasser 2.0 Wasser Ethanol Temperatur [ C] T -1 [K -1 ] In einem offenen System kann sich bei einer konstanten Temperatur der entsprechende Dampfdruck nicht einstellen, da die Gasphase "unendlich groß" ist: Es wird ständig Substanz von der flüssigen Phase in die Gasphase gebracht. Die dazu nötige Energie heißt Verdampfungsenthalpie ( H verd ). Die Destillation benutzt die Störung des thermodynamischen Gleichgewichts um Flüssigkeiten zu trennen oder zu reinigen: Durch die apparative Anordnung ist es möglich, die kondensierende Flüssigkeit aus dem System abzutrennen, dadurch wird der Destillationskolben zum offenen System. Die Verdampfungsenthalpie wird durch die Heizung des Destillationskolbens aufgebracht.
3 Tabelle 3.1: Dampfdrucke verschiedener Substanzen. Im Bereich der grau unterlegten Bereiche sind die Substanzen bei Normaldruck gasförmig. Temperatur Dampfdruck (hpa [Torr]) T ( C) Wasser Diethylether Ethanol n-pentan n-heptan [4.58] [185] 16.0 [12] 244 [183] 14.6 [11] [9.21] [292] 32.0 [24] 376 [282] 28 [21] [17.5] 589 [442] 58.6 [44] 560 [420] 48 [36] [31.8] 862 [647] 105 [79] 814 [611] 77 [58] [55.3] 1228 [921] 180 [135] 1164 [873] 123 [92] [92.5] 1702 [1277] 296 [222] 1590 [1193] 188 [141] [149.4] 470 [353] 2139 [1605] 279 [209] [233.7] 722 [542] 2824 [2119] 403 [302] [355.1] 1084 [813] 3645 [2735] 569 [427] [525.8] 1582 [1187] 4662 [3498] 785 [589] [760.0] 5878 [4410] 1060 [795] [1075] 1398 [1049] [1490] 1026 [1367] Sdp. bei (1013 hpa / 760 Torr) 100 C 34.6 C 78.3 C 36.2 C 98.4 C 3.2. Einstufen-Destillation Bei der Destillation wird die zu destillierende Flüssigkeit, das Destillationsgut, in einer geeigneten Destillationsapparatur zum Sieden erhitzt. Der entweichende Dampf wird so kondensiert, daß das Destillat nicht in den Destillationskolben zurückfließt, sondern in einer Vorlage aufgefangen wird. Einstufen-Destillation: Einmaliges Verdampfen und Kondensieren der zu destillierenden Flüssigkeit. Für die Destillation sollte die Siedetemperatur im Bereich von C liegen; bei höherer Temperatur besteht häufig die Gefahr der Zersetzung des Destillationsgutes, bei tieferer Temperatur ist die Kondensation der Dämpfe recht aufwändig. Eine Verbindung mit hohem Siedepunkt z.b. 300 C bei Normaldruck (1013 hpa bzw. 760 Torr), wird man deshalb zweckmäßig bei vermindertem Druck, z.b hpa, Siedepunkt 150 C, destillieren (siehe auch Abschnitt 3.2.3). Zur Verminderung des Drucks in der Destillationsapparatur verwendet man je nach angestrebten Druckbereich verschiedene Vakuumpumpen (siehe 3.2.3): Wasserstrahlpumpenvakuum (Grobvakuum): Ölpumpenvakuum (Feinvakuum): Öldiffusionspumpenvakuum (Hochvakuum): hpa (12-14 Torr) 10-1 bis 10-3 hpa (Torr) 10-4 bis 10-6 hpa (Torr) In Abbildung 3.2 und 3.3 werden die einfachen Standard-Destillationsapparaturen und abgebildet und beschrieben; diese Apparaturen können sowohl für die Destillationen bei Normaldruck als auch bei verminderten Drucken verwendet werden.
4 Aufbau und Inbetriebnahme einfacher Destillationsapparaturen Eine einfache Destillation ist nur bei Flüssigkeiten mit sehr hoch siedenden Verunreinigungen oder zum Abdestillieren von Lösungsmittel aus Lösungen mit hoch siedenden Stoffen sinnvoll. Während der Destillation müssen Siedeverzüge im Destillationskolben unbedingt vermieden werden! Deshalb gibt man von Anfang an entweder Siedesteine oder einen Magnetrührstab in den Destillationskolben. Um eine Massenbilanz erstellen zu können müssen Vorlagekolben und Destillationskolben (am besten mit Magnetrührstab oder Siedesteine) vor dem Einbau gewogen (tariert) werden. Man beginnt beim Aufbau mit dem Anklammern des Destillationskolbens (1); er muß in einer solchen Höhe eingespannt werden, daß Heizquelle und Heizbad rasch und mühelos nach unten entfernt werden können. Dazu verwendet man zweckmäßig eine Laborhebebühne (8), mit der sich die Heizquelle zusammen mit dem Heizbad (6) einfache in der Höhe verstellen und vollständig von der Apparatur entfernen läßt. Anschließend wird der Vorlagekolben (4) an einer zweiten Stativstange geklammert und die Destillationsbrücke (2) mit dem geraden Vorstoß (3) aufgesetzt (s. Abb. 3.2). Die gesamte Destillationsapparatur muß spannungsfrei (Bruchgefahr!) sein. Abb. 3.2: Einfache Destillationsapparatur Apparatesymbol Die Kühlwasserschläuche werden so angeschlossen, dass das frische Kühlwasser von unten in den Liebigkühler einströmt (Gegenstromprinzip) und mit Schlauchklemmen gesichert. Danach auf Dichtigkeit überprüft. Dabei darf das Heizbad nicht unter der Apparatur stehen, um bei einer möglichen Undichtigkeit Wasserspritzer im Ölbad zu verhindern. Erst jetzt wird das abgewogene Destillationsgut mit Hilfe eines Trichters in den Vorlagekolben gefüllt. Zuletzt wird die gerade Schlifföffnung mit einem Glasstopfen verschlossen, das Thermometer (5) aufgesetzt (die Quecksilberkugel muss knapp unterhalb des Ansatzrohrs sitzen, nur dann kann sie vom Dampf vollständig umspült werden, Thermometer mit einer Schliffklammer sichern) und ein Heizbadthermometer (7) zur Messung der Badtemperatur befestigt. Da in jeder Destillationsapparatur eine der Größe der Apparatur entsprechende Menge Destillationsgut zurückgehalten wird (Retentionsvolumen), muß die Größe der Apparatur an die Menge des Destillationsguts angepaßt werden: der Destillationskolben sollte mindestens zur Häfte, maximal zu zwei Drittel gefüllt sein, der Vorlagekolben muss an die zu erwartende Destillatmenge angepasst werden.
5 Die seitliche Oliven- bzw. Schrauböffnung am Vorstoß (3) darf nicht verschlossen werden. Sie dient dem Druckausgleich bzw. dem Anschluss an eine Vakuumleitung (vgl. Kap ). Nie im völlig abgeschlossenen System destillieren! Explosions- und Feuergefahr durch Überdruck in der Apparatur. Vor Beginn der Destillation: Der Kühlwasserfluss wird vorsichtig eingestellt: bei zu starkem Wasserdurchfluss durch den Kühler besteht die Gefahr, daß die Wasserschläuche abplatzen. Bei der Verwendung von Ölbädern als Heizbad kann Wasser in das heiße Öl gelangen, das durch das verdampfende Wasser explosionsartig herausgeschleudert werden kann (Brand- und Verletzungsgefahr!). Der Destillationskolben wird bis zum Schliffansatz in das noch kalte Heizbad eingetaucht. So wird ein maximaler Wärmekontakt gewährleistet. Bei höhersiedenden Flüssigkeiten sollte der Destillationsaufsatz durch Umwickeln mit Aluminiumfolie gegen Wärmeverluste geschützt werden. Dadurch vermeidet man die Kondensation des Destillationsgutes bereits im oberen Teil des Destillationskolbens bzw. im Destillationsaufsatz. Bei der Destillation von hochentzündlichen, giftigen oder aggressiven Substanzen unter Normaldruck wird auf die Olive am Vorstoß ein Schlauch aufgezogen, der hinter die Abzugsprallwand geführt wird. Die Entzündung von nichtkondensierten Dämpfen durch offene Flammen oder heiße Oberflächen wird so vermieden. Bei umweltschädlichen oder reaktiven Substanzen ist die Adsorption der freiwerdenden Stoffe mit jeweils geeigneten Methoden vorzuziehen. Durchführung der Destillation: Das Heizbad wird langsam bis zum Sieden des Destillationsgutes aufgeheizt, dabei muss die Apparatur und die Temperatur des Heizbades ständig überwacht werden. Wenn der erste Tropfen Destillat in den Vorlagekolben fällt beginnt der Destillationsvorgang. Man protokolliert die Ölbadtemperatur, Siedetemperatur und die Zeit. Ab diesem Zeitpunkt sollte die Heizbadtemperatur konstant bis leicht steigend sein und etwa C oberhalb des Siedepunktes liegen, die Destillationsgeschwindigkeit sollte ca. 2-4 Tropfen/Sekunde betragen und der Siedepunkt während der gesamten Destillation innerhalb eines Intervalls von ca. 2 C konstant bleiben. Eine zu niedrige Badtemperatur führt zu falschen Siedetemperaturen, da der Dampf die Thermometerkugel nicht ausreichend umspült. Eine zu hohe Badtemperatur verfälscht den Siedepunkt ebenfalls, da der Dampf überhitzt wird. Bei starker Überhitzung (fehlende Kontrolle der Badtemperatur) besteht die Gefahr des Überschleuderns oder Überschäumens des Destillationsgutes (Brandgefahr!). Der Kühlwasserfluß muss während der Destillation immer wieder kontrolliert werden. Eine unvollständige Kondensation brennbarer Dämpfe (z.b. Diethylether, Petrolether) kann zu schweren Bränden führen. Das Ende der Destillation erkennt man an der abfallenden Siedetemperatur. Jetzt wird nochmals die Siedetemperatur, Badtemperatur und die Zeit protokolliert. Im Normalfall destilliert man aus Sicherheitsgründen nie bis zur Trockne des Destillationskolbens! Es könnten sich im Destillationsrückstand (Sumpf) Substanzen befinden, die sich bei
6 Überhitzung explosionsartig zersetzten. Vor allem Ether bilden beim längeren Stehen durch Autoxidation Peroxide, die thermisch sehr labil sind. Man entfernt das Heizbad und lässt die Apparatur abkühlen. Danach wird die Apparatur abgebaut (von oben nach unten, Thermometer zuerst!). Abschließend wird durch Rückwiegen des Vorlagekolbens bzw. des Destillationskolbens die Masse des Destillats und den Brechungsindex, sowie die Masse des Rückstands bestimmt und protokolliert. Aus der Differenz der Einwaage und der Summe des Destillats und Rückstands wird der Massenverlust der Destillation errechnet. Abschließend werden die Literaturwerte von Siedepunkt und Brechungsindex der destillierten Substanz angegeben. Zu einem vollständigen Protokoll gehören auch Angaben über die verwendete Apparatur (auch die Größe) und Beobachtungen zum Destillationgut und Destillat: Beispiel eines Destillationsprotokolls: Destillation von Ethanol unter Normaldruck in einer NS 14-Destillationsapparatur mit 100 ml Destillations- und Vorlagekolben: Einwaage: 65.2 g verunreinigtes Ethanol, schwach gelblich. Zeit Ölbadtemperatur Siedetemperatur Masse Destillat 20 n D C C 59,8 g Destillationsrückstand: 4.10 g Verlust bei der Destillation: 1.30 g Ausbeute: 59,8 g Ethanol, farblose Flüssigkeit, Sdp C, n D 20 = Lit: Sdp. 78 C, n D 20 = Fraktionierende Einstufendestillation Eine einfache Destillation ist nur in wenigen Fällen sinnvoll. In der Praxis steht man meist vor dem Problem, dass die zu destillierende Substanz mit Stoffen verunreinigt ist, die selbst destillieren können. Weiterhin kommt es vor, dass der Siedepunkt im Verlauf der Destillation nicht konstant bleibt. In diesen Fällen ist es notwendig, die Vorlagekolben während der Destillation zu wechseln, um die einzelnen Fraktionen getrennt zu sammeln und evtl. später weiter zu untersuchen. Sehr einfach gelingt dies durch Verwendung einer sogenannten Spinne zusammen mit einem Vorstoß mit gebogenem Auslauf (Vorstoß nach Bredt): Durch einfaches Drehen können mehrere Vorlagekolben (meist vier) in den Auslauf des Vorstoßes gedreht und so getrennt aufgefangen werden (Abb. 3.4). Der Aufbau der Apparatur erfolgt analog zur einfachen Destillationsapparatur. Statt des Vorlagekolbens wird die Spinne so geklammert, dass sie zwar fest, aber noch drehbar ist. Die tarierten und nummerierten Destillationskolben werden mit Federn oder Schliffklammern an der Spinne befestigt.
7 Abb. 3.4: Destillationsapparatur zur fraktionierenden Destillation Apparatesymbol Die Durchführung der Destillation ist ebenfalls analog zur einfachen Destillation. Im ersten Vorlagekolben sammelt man alles Destillat bis der Siedepunkt konstant ist, dann dreht man auf den 2. Kolben. Ändert sich die Siedetemperatur signifikant (mehr als 2 C), dreht man den nächsten Kolben in den Auslauf und so weiter. Abb. 3.5 zeigt schematisch die beiden häufigsten Destillationsverläufe: Abb. 3.5: Typische Destillationsverläufe. Fraktion 1 Fraktion 2 Fraktion 3 Zeit Fraktion 1 Fraktion 2 Fraktion 3 Fraktion 4 Zeit Das Destillationsprotokoll für eine fraktionierende Destillation entspricht dem der einfachen Destillation, für jede Fraktion wird eine neue Zeile angefügt, die Fraktionen werden durchgehend nummeriert. Die Einteilung der Fraktionen in Vorlauf, Hauptlauf, Nachlauf sind eine Interpretation der erhaltenen Ergebnisse, sie erfolgt erst am Schluss unter Berücksichtigung der Mengen und der sich aus den Brechungsindizes ergebenden Reinheit.
8 Es kann durchaus vorkommen, das sich zwei Fraktionen, die sich im Siedepunkt etwas unterscheiden einen identischen Brechungsindex besitzen und als ein Hauptlauf wieder zusammengegeben werden können. Im Zweifelsfall können weitere analytische Methoden wie z.b. IR-Spektroskopie zur Entscheidung herangezogen werden. Beispiel eines Destillationsprotokolls: Fraktionierende Destillation von Ethanol unter Normaldruck in einer NS 14- Destillationsapparatur mit 100 ml Destillations- und Vorlagekolben: Einwaage: 63.2 g verunreinigtes Toluol, schwach gelblich. Fraktion Zeit Ölbadtemperatur Siedetemperatur Masse Destillat 20 n D C -109 C 2.42 g C C C C C C 1.02 g Destillationsrückstand: 3.10 g Verlust bei der Destillation: 1.12 g Summe g Wegen der fast identischen Brechungsindizes und der sehr ähnlichen Siedepunkte können Fraktion 2 und 3 als Hauptlauf vereinigt werden. Ausbeute: 59,8 g Toluol, farblose Flüssigkeit, Sdp C, n D 20 = Lit: Sdp C, n D 20 = Einstufen-Destillation bei vermindertem Druck Siedepunkte sind - wie im Abschnitt 3.1 ausgeführt - stark abhängig vom Druck. Destillationen sollte man nur bei Siedetemperaturen zwischen 35 C und maximal 170 C durchführen. So wird eine zu hohe thermische Belastung der Substanz die möglicherweise zu Zersetzung führen könnte vermieden. Höhersiedende Flüssigkeiten werden deshalb im Normalfall bei vermindertem Druck durchgeführt. Dabei wird der Druck soweit reduziert, dass der Siedepunkt auf etwa C herabgesetzt wird. Als Faustregel für die Verminderung des Siedepunktes durch Reduzierung des Druckes gilt: Die Reduzierung des Druckes um die Hälfte erniedrigt den Siedepunkt um etwa 15 C!
9 Sehr einfach kann man im erreichbaren Endvakuum verschiedener Pumpen arbeiten: Wasserstrahlpumpen erreichen einen Enddruck von hpa, im selben Druckbereich liegen zweistufige Membranpumpen. Die Wasserstrahlpumpe ist eine sehr einfache und billige Vakuumpumpe, ihr Nachteil ist, dass mitgesaugte Substanzreste (Lösungsmittel) unweigerlich in das Abwasser gelangen. Deshalb werden sie in den letzten Jahren durch die sehr robusten Membranpumpen ersetzt. Nichtsdestotrotz wird der Vakuumbereich um die 20 hpa immer noch als "Wasserstrahlvakuum" bezeichnet. Im Wasserstrahlvakuum kann man mit einer Siedepunkterniedrigung von ca. 100 C rechnen. Ölpumpen (Drehschieberpumpen) decken den Druckbereich von hpa ab. In diesem Bereich sind alle gängigen Lösungsmittel gasförmig und müssen zum Schutz der Pumpe vorher kondensiert werden. Dazu werden sogenannte Kühlfallen verwendet, die mit Trockeneis/Aceton (ca. -78 C) oder flüssigem Stickstoff (ca C) gekühlt werden (Siehe Vorsichtsmaßnahmen beim Arbeiten mit tiefkalten Lösungen oder Flüssigkeiten!). Bei einem Vakuum von hpa ist eine Siedepunkterniedrigung von ca C zu erwarten. Apparatur für die Destillation bei vermindertem Drucken Es kann prinzipiell die Destillationsapparatur für fraktionierende Destillation verwendet werden: Die Apparatur (Abb. 3.5) wird über einen dickwandigen Vakuumschlauch (Innendurchmesser 6-8 mm) an die Vakuumpumpe angeschlossen. Durch zu lange Leitungen bzw. zu kleine lichte Weiten der Schläuche wird das Vakuum in der Apparatur drastisch verschlechtert! Abb. 3.5: Apparaturen zur einfachen Destillation unter vermindertem Druck. Apparatesymbol Apparatur mit Siedekapillare Vakuummeßgerät Belüftungshahn Absperrhahn zur Vakuumpumpe Woulff'sche Flasche
10 Zur Vermeidung von Siedeverzügen (plötzliches, explosionsartiges Verdampfen des überhitzten Destillationsgutes) muß man mit einem Magnetrührstab und Magnetrührer arbeiten. Alternativ kann auch eine Siedekapillare eingesetzt werden, die im Vakuum eine Kette kleiner Luftperlen durchläßt (Abb. 3.5 links). Prinzipiell ist auch die Verwendung hochaktiver, poröser Siedesteinchen möglich, erfahrungsgemäß läßt jedoch die Wirksamkeit der Siedesteinchen bei Vakuumdestillationen sehr rasch nach - besonders wenn das Destillationsgut polymere Bestandteile enthält oder sehr viskos ist. Bei der Destillation sinkt die über die Gasphase transportierte Stoffmenge (und Wärmemenge) mit fallendem Druck stark ab; der Abstand zwischen Oberfläche, Heizbad und absteigendem Kühler muß daher möglichst klein sein. Deshalb sollte dieser Teil der Apparatur gegen Wärmeverluste durch Isolierung mit Alufolie geschützt werden. Vakuumanschluß der Apparatur Die Destillationsapparatur wird über eine sogenannte Sicherheitsflasche (Woulff'sche Flasche) an die Vakuumpumpe angeschlossen, um zu verhindern, dass bei einem eventuellen Überschäumen die Pumpe verunreinigt wird. Beim Einsatz einer Wasserstrahlpumpe verhindert die Woulff'sche Flasche auch, dass bei einem evtl. "Zurückschlagen" der Wasserstrahlpumpe Wasser in die Destillationsapparatur gelangt, was zum Bruch der Apparatur führen kann. Das "Belüften" der Apparatur (Druckausgleich am Ende der Destillation oder bei einer Unterbrechung) erfolgt durch langsames Öffnen des Hahns der Sicherheitsflasche. Zwischen Vakuumpumpe und Woulff'scher Flasche muss sich ein Absperrventil befinden. Bei jeder Destillation unter vermindertem Druck muss der Druck gemessen und mitprotokolliert werden. Druckschwankungen führen zu Änderungen des Siedepunkts während der Destillation! Das Manometer wird dazu über ein T-Stück im Nebenschluß geschaltet. Achtung: Vor dem Anlegen von Vakuum muss die Apparatur auf Sprünge oder schadhafte Glasteile untersucht werden. Schadhafte Glasgeräte können beim evakuieren implodieren! Destillation bei vermindertem Druck Bevor die zu destillierende Substanz in die Destillationsapparatur gefüllt wird sollte auf Dichtigkeit überprüft werden. Dazu wird der Belüftungshahn der Woulff'schen Flasche geschlossen und der Absperrhahn zur Vakuumpumpe langsam geöffnet. Am Manometer kann der Druckabfall in der Apparatur beobachtet werden. Stellt sich der erwartete Druck nicht ein muss die Leckstelle gesucht werden, meistens handelt es sich um lose oder schlecht gefettete Schliffverbindungen. Ist der Enddruck erreicht wird der Absperrhahn zur Pumpe geschlossen. Der Druck in der Apparatur darf danach nicht nennenswert ansteigen. Anschließend wird die Apparatur mit dem Hahn der Sicherheitsflasche vorsichtig belüftet. Nach dem Einfüllen des Destillationsgut kann die Destillation beginnen: Dazu wird das kalte Ölbad an den Destillationskolben gefahren, falls mit Magnetrührstab gearbeitet wird, wird der Rührmotor jetzt eingeschaltet. Anschließend wird die Apparatur vorsichtig evakuiert. Es ist
11 empfehlenswert, die Apparatur hier genau zu beobachten, da beim Evakuieren möglicherweise im Destillationsgut gelöste Luft oder leichtflüchte Bestandteile (Lösungsmittelreste) entweichen, was sich durch mitunter starkes Aufschäumen bemerkbar macht. In diesem Fall ist der Absperrhahn zur Vakuumpumpe sofort wieder zu schließen! Erst wenn der gewünschte Druck anliegt und das Destillationsgut nicht mehr schäumt wird die Heizung eingeschaltet und langsam hochgeregelt. Die weitere Destillation verläuft wie bei der fraktionierenden Destillation unter Normaldruck. Zusätzlich wird bei den Fraktionen der Druck protokolliert. Nach dem Ende der Destillation wird zuerst das Heizbad entfernt. Erst nach Abkühlen der Apparatur wird der Absperrhahn zur Vakuumpumpe geschlossen und die Apparatur langsam belüftet. Weitere Hinweise zur Vakuumdestillation: Siedekapillaren für die Vakuumdestillation Vakuumpumpen und Messgeräte Anwendungsbereiche der Einstufendestillation Beim Vorliegen von Gemischen destillierbarer Verbindungen ist der Dampfdruck der Mischung gleich der Summe der Partialdrucke beider Verbindungen (Gesetz von Raoult). Eine Trennung mehrerer Komponenten mit der einfachen Destillationspparatur ist nur in folgenden Fällen möglich: Die Flüssigkeit enthält nichtflüchtige oder schwerflüchtige Verunreinigungen, z.b. gelöste Salze, fein verteilte (nichtfiltrierbare) feste Partikel, dunkle Zersetzungs- oder Polymerisationsprodukte. Die Flüssigkeit ist ein leichtflüchtiges Lösungsmittel, in dem das schwerflüchtige bzw. nichtflüchtige Reaktionsprodukt gelöst ist (z.b. nach dem Ausschütteln aus einem Reaktionsansatz). Die Flüssigkeit enthält mehrere Komponenten, die sich im Siedepunkt um mindestens C unterscheiden. In diesem Fall lassen sich die Komponenten destillativ trennen. Zwischen den Hauptfraktionen der reinen Produkte liegen Zwischenfraktionen mit entsprechenden Produktgemischen. Destillation unbekannter Produktgemische Bei unbekannten Produktgemischen destilliert man zunächst fraktionierend bei Atmosphärendruck bis zu einer Badtemperatur von etwa C. Der erkaltete Destillationsrückstand wird nun im Wasserstrahlvakuum weiterdestilliert; wenn nötig muß das Destillationsgut zuvor in ein kleineres Kölbchen überführt werden. Man destilliert auch hier bis zu Badtemperaturen von etwa 150 C. Der erkaltete Destillationsrückstand wird anschließend im Ölpumpenvakuum destilliert
12 Wenn Produktgemische bei längerer thermischer Belastung Veränderungen oder Zersetzungen erfahren (z.b. durch katalytisch wirksame, nichtflüchtige Verunreinigungen), wird das gesamte Gemisch in einer einfachen Destillationsapparatur im Vakuum zunächst vollständig - ohne auf eine Trennung zu achten - überdestilliert. Die Vorlage muß mit Aceton/Trockeneis oder mit flüssigem Stickstoff gekühlt werden, damit die leichterflüchtigen Komponenten nicht verlorengehen. Das Destillat kann anschließend normal destillativ aufgereinigt werden Spezielle Apparaturen zur Einstufendestillation Rotationsverdampfer Der Rotationsverdampfer ist besonders geeignet für rasche und schonende Destillation größerer Lösungsmittelmengen (50 ml bis mehrere Liter). In der Regel wird dabei unter vermindertem Druck gearbeitet. Es empfiehlt sich auch hier zwischen Rotationsverdampfer und Vakuumpumpe eine Woulff'sche Flasche zu schalten, um einer Verschmutzung der Pumpe vorzubeugen. Der Destillationskolben rotiert im Heizbad, dadurch bildet sich auf der gesamten Oberfläche des Kolbens ein dünner Flüssigkeitsfilm, der laufend erneuert wird. Diese große Oberfläche erlaubt eine rasche Destillation. Der Dampf steigt durch die Hohlwelle in den Kühler, wo er kondensiert wird und in den Auffangkolben tropft (Abb. 3.6). Abb. 3.6: Schematischer Aufbau eines Rotationsverdampfers. 7 zur Vakuumpumpe Destillationskolben 2 rotierende Hohlwelle (Dampfdurchführungsrohr) 3 Motor mit Antrieb 4 Kühler mit mehren Wendeln 5 Auffangkolben 6 Heizbad 7 Hahn mit Zulaufleitung in den Destillationskolben Die Destillation im Rotationsverdampfer wird in der Regel bei vermindertem Druck durchgeführt, das Heizbad wird konstant auf etwa 60 C gehalten. Über den Druck muss nun ein Siedepunkt von ca. 40 C für die zu destillierende eingestellt werden. Deshalb ist ein Arbeiten am Rotationsverdampfer nur mit geregeltem Vakuum sinnvoll. In Tabelle 3.2 sind die Parameter für die gebräuchlichsten Lösungsmittel aufgeführt.
13 Folgende Punkte sind zu beachten: Durch die hohe Destillationsgeschwindigkeit kann das Lösungsmittel im Kühler möglicherweise nicht mehr vollständig kondensiert werden. Deshalb ist als Vakuumpumpe eine "chemiefeste" Membranpumpe vorzuziehen: Auf der Auspuffseite der Pumpe können Lösungsmittelreste bequem über einen Kühler unter Normaldruck aufgefangen werden. Wenn die Siedepunktdifferenz vom Lösungsmittel zum Produkt kleiner als C ist kann das Produkt bereits mitverdampfen (Ausbeuteverluste!). Der Destillationskolben darf maximal zur Hälfte gefüllt werden, ansonsten kann durch starkes Aufschäumen Lösung überspritzen. Manche Lösungen oder Flüssigkeiten neigen prinzipiell zu starkem Schäumen. In diesen Fällen destilliert man nur kleinere Mengen und füllt den Destillationskolben portionsweise (oder kontinuierlich über den Einlass aus einem Vorratsgefäß) nach. Alternativ kann auch sog. Tropfenfänger zwischen Rotationsverdampfer und Destillationskolben angebracht werden. Sollen niedrig siedende Flüssigkeiten (z.b. n-pentan oder Diethylether) abdestilliert werden, kann unter Normaldruck gearbeitet werden. Dabei muss unbedingt beachtet werden, dass bei ausgeschalteter Druckregelung das Saugleitungsventil zur Vakuumpumpe geschlossen ist, d.h. die Apparatur ist abgeschlossen. Beim Eintauchen des Destillationskolbens in das Heizbad baut sich in der Apparatur ein unzulässiger Überdruck auf. Deshalb ist über ein Belüftungsventil (an der Woulff'schen Flasche oder separates Überdruckventil) unbedingt für Druckausgleich zu sorgen. Tabelle 3.2: Parameter häufig verwendeter Lösungsmittel am Rotationsverdampfer: Lösungsmittel Druck [hpa] für Sdp. bei 40 C Aceton 555 tert-butylmethylether 300 Cyclohexan 235 Diethylether Normaldruck! Essigsäureethylester (Ethylacetat) 240 Ethanol Propanol (Isopropanol) 135 Tetrahydrofuran (THF) 355 Toluol 75 Wasser 70 Feststoffdestillation Selbstverständlich können auch Feststoffe über ihre Schmelze destilliert werden. Das Problem dabei ist, dass das Destillat im Kühler einer normalen Destillationsbrücke bereits wieder erstarrt und den Kühler verstopfen kann. Man verzichtet deshalb auf einen Kühler und schließt den Auffangkolben direkt an den Claisen-Aufsatz. an. Als Auffangkolben ist hier ein Schlenck-Kolben mit seitlichem Kapillarhahn geeignet, der in einem Eisbad gekühlt wird (Abb. 3.7a).
14 Um Siedeverzüge zu vermeiden arbeitet man mit Magnetrührstab oder Siedekapillare (in diesem Fall sollte als Destillationskolben ein Spitzkolben gewählt werden). Kann auf eine Messung der Siedetemperatur verzichtet werden eignet sich auch eine Apparatur mit Krümmer (gebogenes Glasrohr mit 2 Kernschliffen, Abb. 3.7b). Der Vorteil dieser Apparatur ist der kürzere Destillationsweg. Bei allen Feststoffdestillationen besteht die Gefahr, dass das Destillat bereits im Claisenaufsatz bzw. Krümmer erstarrt, deshalb ist für eine gute Isolierung zu sorgen (umwickeln mit Aluminiumfolie). Notfalls kann mit einem Heißluftgebläse zusätzlich erwärmt werden. Abb. 3.7a: Feststoffdestille mit Claisen- Aufsatz. Abb. 3.7b: Feststoffdestille mit Krümmer Vakuumanschluss Vakuumanschluss Eisbad Eisbad Beide Apparaturen sind ebenso zur Destillation hochviskoser Flüssigkeiten geeignet. Weitere Apparaturen zur Einstufendestillation 3.3. Mehrstufendestillation - Rektifikation Bei Siedepunktunterschieden von weniger als C führt eine einfache Destillation nicht mehr zur Auftrennung eines Gemisches in die reinen Komponenten. Durch Mehrstufendestillation (Rektifikation) gelingt meist eine Trennung oder wenigstens eine Anreicherung der Komponenten.
15 Physikalische Grundlagen Am Beispiel des ideal mischbaren Systems n-pentan - n-heptan wird das Prinzip der fraktionierenden Destillation erläutert: Erhitzt man eine Mischung von zwei Flüssigkeiten der Zusammensetzung A langsam, bildet sich am Siedepunkt der Mischung neben der flüssigen Phase eine Gasphase mit der Zusammensetzung B: die leichter flüchtige Komponente reichert sich in der Gasphase an, gleichzeitig erhöht sich der Gehalt der weniger flüchtigen Komponente auf die Zusammensetzung C. Würde die so erhaltene Gasphase von der flüssigen Phase getrennt und vollständig kondensiert hätte man 2 Fraktionen der Mischung mit der Zusammensetzung B und C. Wiederholt man das Experiment mit den beiden Fraktionen könnte man bei der Fraktion B eine weitere Anreicherung der leichtflüchtigen Komponente zu B', bei der schwererflüchtigen Komponente zu C' erreichen usw. (Abb. 3.8). Die untere Kurve eines solchen Siedediagramms bezeichnet man als Siedekurve, sie beschreibt den Übergang von der flüssigen Phase in die Gasphase. Die obere Kurve (Taukurve) beschreibt den Übergang von Gasphase in die flüssige Phase. Zwischen den beiden Kurven liegt ein Zweiphasengebiet (flüssig-gasförmig). Abb. 3.8: Schematisches Siedediagramm des Systems n-pentan - n-heptan 100 Gasphase C' 80 C 60 B 40 B' A Flüssige Phase 0% 100% n-hexan 100% 0% n-pentan Um das ursprüngliche Flüssigkeitsgemisch in die reinen Komponenten zu zerlegen, müßte man eine große Zahl kleiner Fraktionen auffangen und diese noch mehrmals erneut destillieren. Eine solche diskontinuierlich verlaufende fraktionierende Destillation wäre experimentell sehr aufwendig und unrationell. Die Trennung gelingt durch eine kontinuierliche fraktionierende Destillation mit Destillationskolonnen, die eine Mehrstufendestillation (Rektifikation) erlauben. Die Kolonne wird zwischen Destillationskolben und Kühler eingebaut. Eine zusätzliche Verbesserung der Trennleistung wird durch die Verwendung eines Kolonnenkopfs erreicht. Destillationen mit einfacher Destillationsbrücke arbeiten weit entfernt vom thermodynamischen Gleichgewicht, eine optimale Trennung ist aber nur im thermodynamischen Gleichgewicht zu erreichen. Ein Kolonnenkopf ermöglicht durch ein regelbares Ventil die Einstellung eines bestimmten Rücklaufverhältnisses: Nur ein kleiner Teil des Destillats wird entnommen, der Rest fließt in die Kolonne zurück. Dadurch wird die
16 Gleichgewichtseinstellung weniger gestört und die Trennung verbessert. In Abb ist ein einfacher Kolonnenkopf abgebildet. Weitere Informationen zur Mehrstufendestillation Apparaturen zu Mehrstufendestillation Glockenbodenkolonne Das Prinzip der Mehrstufendestillation ist bei der Glockenbodenkolonne sehr anschaulich realisiert (Abb. 3.9): Abb. 3.9: Prinzip der Glockenbodenkolonne. Die Destillationskolonne besteht aus einem Rohr, in dem mehrere Böden eingebaut sind. Dabei handelt es sich um flache Wannen, die von versetzt angeordneten Rohrstücken durchbrochen sind. Die Rohrstücke lassen einerseits frischen Dampf von unten nach oben aufsteigen, andererseits dienen sie als Überlauf für die Böden. Jeder Boden kann so als kleine Destillationsapparatur angesehen werden: Heißer Dampf steigt nach oben, kondensiert und füllt den Boden bis zum Überlaufen. Gleichzeitig wird der Boden durch frischen heißen Dampf geheizt, so dass die leichterflüchtigen Komponenten wieder verdampfen und zum nächsten Boden aufsteigen können. Die Temperatur in einer solchen Glockenbodenkolonne nimmt von unten nach oben ab. Der Nachteil einer solchen Destillationskolonne ist das sehr große Totvolumen: Nach Ende der Destillation bleiben alle Böden gefüllt. Deshalb werden derartige Kolonnen kaum im Laborbetrieb, sondern hauptsächlich in großtechnischen, kontinuierlich betriebenen Anlagen eingesetzt: Hier wird soviel Destillat entnommen wird frisches Destillationsgut in den Destillationskolben zugegeben. Außerdem besteht die Möglichkeit, durch Entnahmeventile an den einzelnen Böden Fraktionen mit unterschiedlicher Zusammensetzung zu entnehmen. Ein Beispiel hierfür ist die Raffination (Destillation) von Erdöl. Vigreux-Kolonne Die Vigreux-Kolonne ist eine einfache und vielseitig einsetzbare Destillationskolonne, vor allem für Anwendungen im Labormaßstab. Sie besteht im wesentlichen aus einem Glasrohr mit nach innen geschmolzenen Zapfen. Aufsteigende Dampf kondensiert auf der Innenseite
17 des Glasrohrs und läuft an den Zapfen zu kleinen Tröpfchen zusammen. Durch nachsteigenden Dampf werden die Tröpfchen wieder erhitzt, die leichterflüchtige Komponente kann weiter verdampfen (Abb. 3.10). Der Temperaturverlust der Kolonne kann durch einen innen verspiegelten Vakuummantel verringert werden, dadurch steigt die Trennleistung an. Seltener findet man auch Vigreux- Kolonnen mit Heizmantel. Die Trennleistung der Kolonne kann durch einen Kolonnenkopf weiter verbessert werden. Es handelt sich dabei um eine Vorrichtung, die es erlaubt nur einen Teil des am oberen ankommenden Destillats zu entnehmen, das restliche Destillat tropft in die Kolonne zurück. Abb. 3.10: Vigreux-Kolonne mit einfachem Kolonnenkopf Das im Kühler (3) kondensierte Destillat wird durch eine Rille an der Innenseite des Kühlers über den Ablauf zu den Hähnen (5) geleitet. Der erste Hahn dient zum Einstellen eines konstanten Rücklaufverhältnisses (meist 10:1 bis 5:1, d.h. nur 1/10 bis 1/5 des Destillats wird entnommen), am zweiten Hahn kann beim Wechseln des Vorlagekolbens abgesperrt werden ohne das Rücklaufverhältnis zu ändern. Der Mehrwegehahn (4) ermöglicht beim Arbeiten im Vakuum ein Belüften und Evakuieren des Vorlagekolbens ohne den Druck in der restlichen Apparatur zu verändern. 1 Destillationskolben 2 Vigreux-Kolonne mit Vakuummantel 3 Rückflusskühler 4 Ventil für Druckaufbau/Druckausgleich beim Arbeiten im Vakuum 5 Hahn zum Einstellen des Rücklaufverhältnisses und Absperrhahn 6 Vorlagekolben Weitere Destillationskolonnen 3.4. Destillation azetroper Mischungen Bei azeotropen Mischungen handelt es sich um Gemische von Flüssigkeiten, die ein nicht ideales Verhalten zeigen. Während bei idealen Mischungen Siedekurve und Taukurve ein linsenförmiges Zweiphasengebiet umschreiben berühren sich bei azeotropen Mischungen die
18 beiden Kurven in einem Extremwert (Azeotrop). Bei den häufigen azeotropen Mischungen eines organischen Lösungsmittels mit Wasser ist der azeotrope Punkt ein Minimum, d.h. er liegt niedriger als die Siedetemperatur der niedrig siedenden Reinkomponente. Abb zeigt das Siedediagramm der azeotropen Mischung Toluol/Wasser, Tabelle 3.3 führt einige wichtige azeotrope Gemische mit Wasser auf. Tabelle 3.3: Azeotrope Gemische einiger organischer Lösungsmittel mit Wasser: Azeotropes Gemisch Wasser / Siedetemperatur der org. Komponente [ C] Siedetemperatur des Azeotrops [ C] Wassergehalt des Azeotrops Mischbarkeit des org. Lösungsmittel mit Wasser bei 20 C Ethanol % unbegrenzt Benzol 80,6 69,2 9% 0.2% Cyclohexan % 0.01% Essigsäureethylester % 2.9% Tetrachlorkohlenstoff % Toluol % Abb. 3.11: Schematisches Siedediagramm der Mischung Wasser/Toluol: 110 Gasphase Azeotrop 80 Flüssige Phase 0% 100% Toluol 100% 0% Wasser Bei "normalen" Destillationen stellt das azeotrope Verhalten ein großes Problem dar, beide Komponenten können prinzipiell durch Destillation nicht vollständig getrennt werden. Je nachdem ob man sich dem azeotropen Punkt von links oder rechts nähert erreicht man bei einer Komponente nur eine Mischung mit der Zusammensetzung des Azeotrops. Dennoch kann die Azeotropbildung wertvoll sein. Weitere Informationen zur azeotropen Destillation
19 Wasserabscheider Die azeotrope Mischung von Wasser und Cyclohexan enthält beispielsweise 9% Wasser. Wird der Dampf dieser Mischung kondensiert, tritt spontane Entmischung der Phasen ein. Die Löslichkeit von Wasser in Cyclohexan beträgt bei Raumtemperatur nur etwa 0.01%! Bei vielen Gleichgewichtsreaktionen (z.b. Veresterung, Acetal- und Ketalbildung, Enaminbildung etc.) entsteht bei der Reaktion Wasser. Die kontinuierliche Entfernung des Wassers aus der Reaktionsmischung kann das Gleichgewicht auf die Produktseite verschieben. Abb. 3.12: Wasserabscheider für spezifisch leichtere Lösungsmittel (Dean-Stark-Falle) Beim Wasserabscheider für spezifisch leichtere Lösungsmittel (Dean-Stark-Falle) (Abb. 3.12) wird die Lösungsmittel/Wasser-Mischung im Reaktionskolben (1) erhitzt. Der Dampf mit azeotroper Zusammensetzung gelangt über das schräge Steigrohr (2) in den Kühler (3) und kondensiert dort unter Entmischung. Das zweiphasige Destillat tropft in das Trennrohr (4) des Wasserabscheiders. Dort setzt sich das Wasser unten ab, das Lösungsmittel fließt oben über das Steigrohr in den Reaktionskolben zurück. Um den Reaktionsverlauf auch quantitativ verfolgen zu können befindet sich am unteren Teil des Trennrohrs eine Graduierung, über einen Hahn kann bei Bedarf Wasser abgelassen werden. 1 Wasserabscheider für spezifisch schwerere Lösungsmittel Wasserdampfdestillation Einige mit Wasser nicht mischbare, sehr hoch siedende Substanzen bilden mit Wasser dennoch Azeotrope mit Siedepunkten unter 100 C. Dieses Verhalten erlaubt oftmals eine einfache und schonende Reinigung der Substanzen.
20 Im einfachsten Fall wird die Suspension der Substanz in Wasser in einer einfachen Destillationsapparatur erhitzt. Aus dem Destillat kann die gereinigte Verbindung durch Filtration (bei Feststoffen) oder Phasentrennung (bei Flüssigkeiten) isoliert werden. Dieses Verfahren wird schon seit langem bei der Gewinnung der sogenannten ätherischen Öle aus pflanzlichem Material verwendet. Die destillierte Menge pro Zeiteinheit lässt sich einfach dadurch steigern, indem eine möglichst große Menge Wasser destilliert wird. Dazu wird in einem speziellen Dampfgenerator überhitzter Wasserdampf erzeugt und über ein Rohr in den Destillationskolben geleitet (Abb. 3.13). Abb. 3.13: Schema einer Wasserdampfdestillation. Wasserdampf Scheidetrichter als Wasserabscheider zur Abtrennung von Kondenswasser 2 Auf etwa 100 C erhitzter Destillationskolben mit dem Destillationsgut in wäßriger Suspension 3 Claisenbrücke 4 Eisbad zur Kühlung der Vorlage Hinweise zur praktischen Durchführung: Bevor man das Dampfeinleitungsrohr in den Destillationskolben einsetzt muss der Kolbeninhalt bis zum Sieden erhitzt werden, sonst kondensiert zu viel Wasser im Destillationskolben. Der Kühlwasserstrom darf nicht zu schwach sein, sonst kann die große Menge Wasserdampf nicht vollständig kondensiert werden. Der Vorlagekolben wird zusätzlich gut mit Eis gekühlt. Das Ende der Destillation erkannt man daran, dass das Destillat nicht mehr trüb ist. Am Ende der Destillation wird zuerst der Ablasshahn des Scheidetrichters geöffnet, erst dann darf der Wasserdampfgenerator abgeschaltet werden. Wird das nicht beachtet, kann beim Abkühlen der heiße Inhalt des Destillationskolbens über das Dampfeinleitungsrohr in den Scheidetrichter und möglicherweise weiter in den Wasserdampfgenerator zurückgesaugt werden. Für die präparative Durchführbarkeit einer Wasserdampfdestillation sollte der Dampfdruck der zu destillierenden Substanz größer als 10 hpa bei 100 C sein. Dampfgeneratoren und Varianten zur Wasserdampfdestillation
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
3. DESTILLATION DESTILLATION BEI NORMALDRUCK
 20 3 DESTILLATION Die Destillation ist die wichtigste Methode zur Reinigung von Flüssigkeiten und zur Trennung von Flüssigkeitsgemischen Voraussetzung ist, dass die Substanzen ohne Zersetzung bei Normaldruck
20 3 DESTILLATION Die Destillation ist die wichtigste Methode zur Reinigung von Flüssigkeiten und zur Trennung von Flüssigkeitsgemischen Voraussetzung ist, dass die Substanzen ohne Zersetzung bei Normaldruck
Praktikumsskript Präparative Anorganische Chemie. Wintersemester 2008/2009
 Skripte zum Praktikum Präparative Anorganische Chemie Wintersemester 2008/2009 FU Berlin/Moritz Kühnel 10/2008 2. Arbeiten mit Vakuumapparaturen (Vacuum-Line) 2.1 Aufbau In der anorganischen Synthesechemie
Skripte zum Praktikum Präparative Anorganische Chemie Wintersemester 2008/2009 FU Berlin/Moritz Kühnel 10/2008 2. Arbeiten mit Vakuumapparaturen (Vacuum-Line) 2.1 Aufbau In der anorganischen Synthesechemie
LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 1 von 12
 LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 1 von 12 LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 2 von 12 a. Nennen Sie eine Bedingung, damit eine Gleichstromdestillation zum Einsatz kommt.
LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 1 von 12 LMPG1 ÜB Grundlagen der Destillation Lösungen Seite 2 von 12 a. Nennen Sie eine Bedingung, damit eine Gleichstromdestillation zum Einsatz kommt.
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 03.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 1.1: Einführung in die Laboratoriumstechnik Einleitung Um die in diesem Praktikum verwendeten Glasgeräte
Endersch, Jonas 03.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 1.1: Einführung in die Laboratoriumstechnik Einleitung Um die in diesem Praktikum verwendeten Glasgeräte
LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 1 von 12
 LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 1 von 12 LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 2 von 12 a. Nennen Sie eine Bedingung, damit eine Gleichstromdestillation zum Einsatz
LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 1 von 12 LMPG1 ÜB3-Lösungen Grundlagen der Destillation Seite 2 von 12 a. Nennen Sie eine Bedingung, damit eine Gleichstromdestillation zum Einsatz
Trennung eines Flüssigkeitsgemisches durch Destillation (Artikelnr.: P )
 Trennung eines Flüssigkeitsgemisches durch Destillation (Artikelnr.: P1132500) Lehrerinformation Einleitung Viele Stoffe liegen in der Natur als Stoffgemisch und nicht als Reinstoff vor. Da viele Stoffe
Trennung eines Flüssigkeitsgemisches durch Destillation (Artikelnr.: P1132500) Lehrerinformation Einleitung Viele Stoffe liegen in der Natur als Stoffgemisch und nicht als Reinstoff vor. Da viele Stoffe
Chemisches Praktikum für TUM-BWL Praxisseminar I Grundoperationen und Reinigungstechniken
 Chemisches Praktikum für TUM-BWL Praxisseminar I Grundoperationen und Reinigungstechniken Inhalt: Aufbauten Umkristallisation Destillation Dr. Andreas Bauer, Dr. Stefan Breitenlechner Lehrstuhl für Organische
Chemisches Praktikum für TUM-BWL Praxisseminar I Grundoperationen und Reinigungstechniken Inhalt: Aufbauten Umkristallisation Destillation Dr. Andreas Bauer, Dr. Stefan Breitenlechner Lehrstuhl für Organische
Chemisches Praktikum für TUM-BWL Praxisseminar II Grundoperationen und Reinigungstechniken
 Chemisches Praktikum für TUM-BWL Praxisseminar II Grundoperationen und Reinigungstechniken Inhalt: Wiederholung Azeotrop-Destillation Extraktion Kontinuierliche Feststoffextraktion Dr. Andreas Bauer, Dr.
Chemisches Praktikum für TUM-BWL Praxisseminar II Grundoperationen und Reinigungstechniken Inhalt: Wiederholung Azeotrop-Destillation Extraktion Kontinuierliche Feststoffextraktion Dr. Andreas Bauer, Dr.
2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid
 2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid H + SCl 2 Cl + HCl + S 2 C 9 H 8 2 (148.2) (119.0) C 9 H 7 Cl (166.6) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid H + SCl 2 Cl + HCl + S 2 C 9 H 8 2 (148.2) (119.0) C 9 H 7 Cl (166.6) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
Soll eine Substanz aus wässriger Lösung extrahiert werden, wählt man das organische Lösungsmittel nach folgenden Kriterien:
 60 8. EXTRAKTION Die Extraktion ist eine wichtige Methode zur Anreicherung, Trennung und Reinigung von festen und flüssigen Substanzen. Grundlage dafür ist die Verteilung der Substanz zwischen zwei nicht
60 8. EXTRAKTION Die Extraktion ist eine wichtige Methode zur Anreicherung, Trennung und Reinigung von festen und flüssigen Substanzen. Grundlage dafür ist die Verteilung der Substanz zwischen zwei nicht
Versuch 6: Rektifikation
 Physikalisch-Chemisches Grundpraktikum Sommersemester 2004 Gruppe B9 Andreas Frintrup / Sven Wolff Versuch 6: Rektifikation Ziel: Die Effizienz zweier verschiedener Trennsäulen, einer fünfbödigen Glockenbodenkolonne
Physikalisch-Chemisches Grundpraktikum Sommersemester 2004 Gruppe B9 Andreas Frintrup / Sven Wolff Versuch 6: Rektifikation Ziel: Die Effizienz zweier verschiedener Trennsäulen, einer fünfbödigen Glockenbodenkolonne
Chemisches Praktikum für TUM-BWL OC-Praxisseminar I Grundoperationen und Reinigungstechniken
 Chemisches Praktikum für TUM-BWL OC-Praxisseminar I Grundoperationen und Reinigungstechniken Inhalt: Umkristallisation Destillation Filtration . Reinigungsschritte bei chemischen Reaktionen Bei fast jeder
Chemisches Praktikum für TUM-BWL OC-Praxisseminar I Grundoperationen und Reinigungstechniken Inhalt: Umkristallisation Destillation Filtration . Reinigungsschritte bei chemischen Reaktionen Bei fast jeder
Ruth Weber. Arbeitstechnik im Chemielabor
 Ruth Weber Arbeitstechnik im Chemielabor 20 Arbeitstechnik im Chemielabor genwärtig und verleiten daher leicht zum übermäßigen Gebrauch von Ethanol und Aceton. Aus ökologischen und ökonomischen Gründen
Ruth Weber Arbeitstechnik im Chemielabor 20 Arbeitstechnik im Chemielabor genwärtig und verleiten daher leicht zum übermäßigen Gebrauch von Ethanol und Aceton. Aus ökologischen und ökonomischen Gründen
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
Destillieren. Apparatur zur Destillation von Alkohol
 Destillieren Die Destillation (von lat. destillare "herabträufeln") war schon bei den alten Ägyptern bekannt. Die einfachste Destillationsappartur bestand aus einem Gefäß mit einem Deckel, an dem sich
Destillieren Die Destillation (von lat. destillare "herabträufeln") war schon bei den alten Ägyptern bekannt. Die einfachste Destillationsappartur bestand aus einem Gefäß mit einem Deckel, an dem sich
Destillation Destillation
 Destillation Die Destillation ist ein in der organischen Chemie häufig eingesetztes Verfahren, um flüssige Substanzen (Stoffgemische und Lösungen) aufgrund der verschiedenen Flüchtigkeiten der Komponente
Destillation Die Destillation ist ein in der organischen Chemie häufig eingesetztes Verfahren, um flüssige Substanzen (Stoffgemische und Lösungen) aufgrund der verschiedenen Flüchtigkeiten der Komponente
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
Einführungspraktikum zu den Arbeitsmethoden in der Organischen Chemie
 Einführungspraktikum zu den Arbeitsmethoden in der Organischen Chemie Versuche und Übungen Kapitel 3: Klassische Methoden zur Charakterisierung organischer Verbindungen Übungen 3.1-3.3 Untersuchungen zum
Einführungspraktikum zu den Arbeitsmethoden in der Organischen Chemie Versuche und Übungen Kapitel 3: Klassische Methoden zur Charakterisierung organischer Verbindungen Übungen 3.1-3.3 Untersuchungen zum
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan
 Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Trennung von Stoffgemischen durch fraktionierte Destillation
 Präparat 1 (B5): Trennung von Stoffgemischen durch fraktionierte Destillation Literatur: Organikum, 23. Auflage, Wiley-VCH, Abschnitt 2.3 Anlagentyp: fraktionierte Destillation mit Vigreux-Kolonne unter
Präparat 1 (B5): Trennung von Stoffgemischen durch fraktionierte Destillation Literatur: Organikum, 23. Auflage, Wiley-VCH, Abschnitt 2.3 Anlagentyp: fraktionierte Destillation mit Vigreux-Kolonne unter
2008 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester
 28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
4. Methoden zur Reinigung der organischen Verbindungen Elementaranalyse. Empirische und Summenformel.
 4. Methoden zur Reinigung der organischen Verbindungen Elementaranalyse. Empirische und Summenformel. Prof. Ivo C. Ivanov 1 Allgemeines Ablauf eines Experiments in der Organischen Chemie: Literaturrecherche
4. Methoden zur Reinigung der organischen Verbindungen Elementaranalyse. Empirische und Summenformel. Prof. Ivo C. Ivanov 1 Allgemeines Ablauf eines Experiments in der Organischen Chemie: Literaturrecherche
170 C C 2 H C C 11 H 10 (174.2) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
4006 Synthese von 2-(3-Oxobutyl)cyclopentanon-2- carbonsäureethylester
 4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
Arbeiten unter Luft- und Feuchtigkeitsausschluss
 Arbeiten unter Luft- und Feuchtigkeitsausschluss Eine Anleitung für Studenten im Praktikum der anorganischen Chemie an der TU Bergakademie Freiberg. Ein Teil der Verbindungen, die im chemischen Laboratorium
Arbeiten unter Luft- und Feuchtigkeitsausschluss Eine Anleitung für Studenten im Praktikum der anorganischen Chemie an der TU Bergakademie Freiberg. Ein Teil der Verbindungen, die im chemischen Laboratorium
Endersch, Jonas 09./
 Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Praktikum Physikalische Chemie II (C-3) Versuch Nr. 12
 Praktikum Physikalische Chemie II (C-3) Versuch Nr. 12 Rektifikation: Bestimmung der theoretischen Trennstufenzahl einer Glockenbodenkolonne bei verschiedenen Rücklaufverhältnissen Grundlagen Die in der
Praktikum Physikalische Chemie II (C-3) Versuch Nr. 12 Rektifikation: Bestimmung der theoretischen Trennstufenzahl einer Glockenbodenkolonne bei verschiedenen Rücklaufverhältnissen Grundlagen Die in der
A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
2002 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan
 22 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan 2 H 5 + H H Montmorillonit K 1 yclohexan 2 H 5 + H 2 6 H 1 3 (13.1) 2 H 6 2 (62.1) 8 H 14 4 (174.2)
22 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan 2 H 5 + H H Montmorillonit K 1 yclohexan 2 H 5 + H 2 6 H 1 3 (13.1) 2 H 6 2 (62.1) 8 H 14 4 (174.2)
DESTILLATION. Aufgabenstellung THEORIE
 DESTILLATION Aufgabenstellung Eine wässrig-alkoholische Lösung (Rotwein) wird durch Destillation in Fraktionen zerlegt. Da Wasser mit Ethanol ein Azeotrop bildet, wird keine der Komponenten rein gewonnen,
DESTILLATION Aufgabenstellung Eine wässrig-alkoholische Lösung (Rotwein) wird durch Destillation in Fraktionen zerlegt. Da Wasser mit Ethanol ein Azeotrop bildet, wird keine der Komponenten rein gewonnen,
Organisch-Chemisches Grundpraktikum Praxisseminar III
 Organisch-Chemisches Grundpraktikum Praxisseminar III Inhalt: Arbeiten mit Gasen Azeotropdestillation Naturstoffextraktion Laboretikette 3. April 21 Dr. Stefan Breitenlechner Lehrstuhl für Organische Chemie
Organisch-Chemisches Grundpraktikum Praxisseminar III Inhalt: Arbeiten mit Gasen Azeotropdestillation Naturstoffextraktion Laboretikette 3. April 21 Dr. Stefan Breitenlechner Lehrstuhl für Organische Chemie
Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung)
 Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Siedediagramm binärer Gemische und Rektifikation
 Versuch Nr. 14: Siedediagramm binärer Gemische und Rektifikation 1. Ziel des Versuchs Ziel des Versuches, ist es die Siedekurve eines Methanol-Wasser-Gemisches aufzunehmen. Im zweiten Versuchsteil soll
Versuch Nr. 14: Siedediagramm binärer Gemische und Rektifikation 1. Ziel des Versuchs Ziel des Versuches, ist es die Siedekurve eines Methanol-Wasser-Gemisches aufzunehmen. Im zweiten Versuchsteil soll
Protokoll Dampfdruck. Punkte: /10
 Protokoll Dampfdruck Gruppe Biologie Assistent: Olivier Evelyn Jähne, Eva Eickmeier, Claudia Keller Kontakt: claudiakeller@teleport.ch Sommersemester 2006 6. Juni 2006 Punkte: /0 . Einleitung Wenn eine
Protokoll Dampfdruck Gruppe Biologie Assistent: Olivier Evelyn Jähne, Eva Eickmeier, Claudia Keller Kontakt: claudiakeller@teleport.ch Sommersemester 2006 6. Juni 2006 Punkte: /0 . Einleitung Wenn eine
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen
 3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus
 NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 3 Dampfdruckkurve einer leichtflüchtigen Flüssigkeit Aufgabe: Es ist die Dampfdruckkurve einer leicht flüchtigen Flüssigkeit zu ermitteln
Praktikumsskript Präparative Anorganische Chemie. Wintersemester 2008/2009
 Skripte zum Praktikum Präparative Anorganische Chemie Wintersemester 2008/2009 FU Berlin/Moritz Kühnel 10/2008 3. Arbeiten unter inerten Bedingungen Viele anorganische Verbindungen sind empfindlich gegenüber
Skripte zum Praktikum Präparative Anorganische Chemie Wintersemester 2008/2009 FU Berlin/Moritz Kühnel 10/2008 3. Arbeiten unter inerten Bedingungen Viele anorganische Verbindungen sind empfindlich gegenüber
1024 Eliminierung von Wasser aus 4-Hydroxy-4-methyl-2- pentanon
 0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
Phasen, Komponenten, Freiheitsgrade
 Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
Phasendiagramme 1 Lernziele: Ø Phasen, Komponenten, Freiheitsgrade Ø Die Phasenregel Ø Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Ø Zweikomponentensysteme: Siedediagramme (die Destillation
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren Brombutanen
 1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
Kapitel 1: Einfache Laborarbeiten
 Kapitel 1: Einfache Laborarbeiten Handhabung von Chemikalien und Geräten Bearbeitung von Glas Pipetten, kleine Reagenzgläser, Gaseinleitungsrohr keine Protokolle notwendig, Durchführung wird nicht testiert
Kapitel 1: Einfache Laborarbeiten Handhabung von Chemikalien und Geräten Bearbeitung von Glas Pipetten, kleine Reagenzgläser, Gaseinleitungsrohr keine Protokolle notwendig, Durchführung wird nicht testiert
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon)
 1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
Synthese von tert-butylchlorid (2-Chloro-2-methylpropan)
 Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol
 4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd
 A1-1 1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd Bereiten Sie folgende Themengebiete vor Zustandsdiagramme von Einkomponentensystemen
A1-1 1. BESTIMMUNG DER DAMPFDRUCKKURVE EINER REINEN FLÜSSIGKEIT ZUR BERECHNUNG DER VER- DAMPFUNGSENTHALPIE DH verd UND -ENTROPIE DS verd Bereiten Sie folgende Themengebiete vor Zustandsdiagramme von Einkomponentensystemen
Praktikum Allgemeine Chemie SS 2013
 Praktikum Allgemeine Chemie SS 2013 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: birlenbach@chemie.uni-siegen.de Kapitel 1: Einfache Laborarbeiten
Praktikum Allgemeine Chemie SS 2013 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: birlenbach@chemie.uni-siegen.de Kapitel 1: Einfache Laborarbeiten
Versuch 1: Destillation Chemieteil, Herbstsemester 2008
 Versuch 1: Destillation Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 12.11.08 Assistent: André Röthlisberger E-Mail: zclaudio@student.ethz.ch 1. Abstract
Versuch 1: Destillation Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 12.11.08 Assistent: André Röthlisberger E-Mail: zclaudio@student.ethz.ch 1. Abstract
Organisch-Chemisches Grundpraktikum Praxisseminar I - Reinigungstechniken
 Organisch-Chemisches Grundpraktikum Praxisseminar I - Reinigungstechniken 19. pril 21 Inhalt: Umkristallisation Destillation Extraktion Dr. Stefan Breitenlechner Lehrstuhl für Organische Chemie I Praxisseminar
Organisch-Chemisches Grundpraktikum Praxisseminar I - Reinigungstechniken 19. pril 21 Inhalt: Umkristallisation Destillation Extraktion Dr. Stefan Breitenlechner Lehrstuhl für Organische Chemie I Praxisseminar
Einführungspraktikum zu den Arbeitsmethoden in der Organischen Chemie
 Einführungspraktikum zu den Arbeitsmethoden in der rganischen Chemie Versuche und Übungen Kapitel 8: Extraktion Extraktion von Crotonsäure oder Malonsäure aus wässrigen Lösungen mit tert-butylmethylether,
Einführungspraktikum zu den Arbeitsmethoden in der rganischen Chemie Versuche und Übungen Kapitel 8: Extraktion Extraktion von Crotonsäure oder Malonsäure aus wässrigen Lösungen mit tert-butylmethylether,
Azeotrope. Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch
 Azeotrope B A Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch zahl- reiche wichtige Systeme weichen davon ab. Ein solches Verhalten kann auftreten, a wenn die Wechselwirkungen
Azeotrope B A Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch zahl- reiche wichtige Systeme weichen davon ab. Ein solches Verhalten kann auftreten, a wenn die Wechselwirkungen
Institut für Technische Chemie Technische Universität Clausthal. Technisch-chemisches Praktikum TCB. Versuch: Rektifikation
 Institut für Technische Chemie Technische Universität Clausthal Technisch-chemisches Praktikum TCB Versuch: Rektifikation Einleitung In einer Vielzahl von chemischen Produktionsanlagen besteht die Notwendigkeit,
Institut für Technische Chemie Technische Universität Clausthal Technisch-chemisches Praktikum TCB Versuch: Rektifikation Einleitung In einer Vielzahl von chemischen Produktionsanlagen besteht die Notwendigkeit,
8.4.5 Wasser sieden bei Zimmertemperatur ******
 8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
Rund ums Vakuum II. Experimente
 Rund ums Vakuum II Experimente Experimente: (1) Demonstration des Vakuums (2) Wasser siedet unterhalb von 100 C (3) Kohlenstoffdioxid-Gehalt von Mineralwasser (4) Mineralwässer und ph-wert (1) Demonstration
Rund ums Vakuum II Experimente Experimente: (1) Demonstration des Vakuums (2) Wasser siedet unterhalb von 100 C (3) Kohlenstoffdioxid-Gehalt von Mineralwasser (4) Mineralwässer und ph-wert (1) Demonstration
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 2- Siedediagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Siedediagramm wird dieses Vorgespräch durch einen Multiple-Choice
PCG-Grundpraktikum Versuch 2- Siedediagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Siedediagramm wird dieses Vorgespräch durch einen Multiple-Choice
Fraktionierte Destillation eines Gemisches
 Fraktionierte Destillation eines Gemisches Die Destillation ist eine physikalische Trennmethode, bei welcher die unterschiedlichen Siedepunkte der Bestandteile (Komponenten) eines Gemisches zur Trennung
Fraktionierte Destillation eines Gemisches Die Destillation ist eine physikalische Trennmethode, bei welcher die unterschiedlichen Siedepunkte der Bestandteile (Komponenten) eines Gemisches zur Trennung
5. Probenaufbereitung
 Analytische Chemie für Biologie, Pharmazie, 75 Teil Chromatographische und 5. Probenaufbereitung Wieso ist eine Probeaufarbeitung für viele Proben notwendig? Störende andere Substanzen sollen entfernt
Analytische Chemie für Biologie, Pharmazie, 75 Teil Chromatographische und 5. Probenaufbereitung Wieso ist eine Probeaufarbeitung für viele Proben notwendig? Störende andere Substanzen sollen entfernt
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
14 Destillation Grundlagen Destillation
 72 4 Destillation 4 Destillation 4. Grundlagen Mit dem wichtigen rennverfahren der Destillation (die entscheidende Modifikation der Destillation stellt dabei die Rektifikation dar) lässt sich aus einem
72 4 Destillation 4 Destillation 4. Grundlagen Mit dem wichtigen rennverfahren der Destillation (die entscheidende Modifikation der Destillation stellt dabei die Rektifikation dar) lässt sich aus einem
Herstellung von Natriumethanolat
 Illumina-Chemie.de - Artikel Synthesen Herstellung von Natriumethanolat Die folgende Anleitung kann zur Orientierung zur Herstellung anderer Natriumalkoholate verwendet werden. Allerdings muss bei der
Illumina-Chemie.de - Artikel Synthesen Herstellung von Natriumethanolat Die folgende Anleitung kann zur Orientierung zur Herstellung anderer Natriumalkoholate verwendet werden. Allerdings muss bei der
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
8 Stevia qualitativ aus der Pflanze extrahieren
 8 Stevia qualitativ aus der Pflanze extrahieren 8.1 Vorwort Stevia ist der mit Abstand am teuersten Zuckerersatzstoff den wir untersucht haben, deshalb beschäftigte uns die Frage, wie der hohe Preis zu
8 Stevia qualitativ aus der Pflanze extrahieren 8.1 Vorwort Stevia ist der mit Abstand am teuersten Zuckerersatzstoff den wir untersucht haben, deshalb beschäftigte uns die Frage, wie der hohe Preis zu
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
Extraktionen von Naturstoffen in Bildern: Eugenol und Eugenolacetat
 Extraktionen von Naturstoffen in Bildern: Eugenol und Eugenolacetat Hier wird die Extraktion von Eugenol und Eugenolacetat aus Gewürznelken dokumentiert. Genaue Extraktionsvorschrift: siehe Lambdasyn.
Extraktionen von Naturstoffen in Bildern: Eugenol und Eugenolacetat Hier wird die Extraktion von Eugenol und Eugenolacetat aus Gewürznelken dokumentiert. Genaue Extraktionsvorschrift: siehe Lambdasyn.
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien
 3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Herstellung von Triphenylphosphin
 Aqua labor Herstellung von Triphenylphosphin Eigenschaften des Produktes: Triphenylphosphin, kurz TPP, ist eine farblose (oder in einem weniger reinem Zustand leicht gelbliche), aus monoklinen Kristallen
Aqua labor Herstellung von Triphenylphosphin Eigenschaften des Produktes: Triphenylphosphin, kurz TPP, ist eine farblose (oder in einem weniger reinem Zustand leicht gelbliche), aus monoklinen Kristallen
Thermische Trennverfahren I Destillation, Rektifikation Shell Eastern Petrochemicals Complex (SEPC), Pulau Bukom, Singapore
 Thermische Trennverfahren I Destillation, Rektifikation Shell Eastern Petrochemicals Complex (SEPC), Pulau Bukom, Singapore Universität Hamburg 133 Atmosphärenrektifikation Aufstellen einer 110 m hohe
Thermische Trennverfahren I Destillation, Rektifikation Shell Eastern Petrochemicals Complex (SEPC), Pulau Bukom, Singapore Universität Hamburg 133 Atmosphärenrektifikation Aufstellen einer 110 m hohe
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol
 3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
Organisch-Chemisches Grundpraktikum. trans-1,2-cyclohexandiol
 rganischhemisches Grundpraktikum Präparat 06: trans1,2yclohexandiol Gliederung: I. Literatur... 1 II. Präparateigenschaften... 1 III. Stöchiometrische Reaktionsgleichung... 1 IV. Reaktionsmechanismus...
rganischhemisches Grundpraktikum Präparat 06: trans1,2yclohexandiol Gliederung: I. Literatur... 1 II. Präparateigenschaften... 1 III. Stöchiometrische Reaktionsgleichung... 1 IV. Reaktionsmechanismus...
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 1- Dampfdruckdiagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Dampfdruckdiagramm wird dieses Vorgespräch durch einen Multiple-Choice
PCG-Grundpraktikum Versuch 1- Dampfdruckdiagramm Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Dampfdruckdiagramm wird dieses Vorgespräch durch einen Multiple-Choice
Lernziele: Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme,
 Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Phasendiagramme Lernziele: ee Phasen, Komponenten, Freiheitsgrade Die Phasenregel Zweikomponentensysteme: Dampfdruckdiagramme, Hebelgesetz Zweikomponentensysteme: Siedediagramme (die Distillation von Mischungen,
Taschenbuch der Verfahrenstechnik Herausgegeben von Karl Schwister
 aschenbuch der Verfahrenstechnik Herausgegeben von Karl Schwister ISBN-: 3-446-458-9 ISBN-3: 978-3-446-458-9 Leseprobe Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-458-9
aschenbuch der Verfahrenstechnik Herausgegeben von Karl Schwister ISBN-: 3-446-458-9 ISBN-3: 978-3-446-458-9 Leseprobe Weitere Informationen oder Bestellungen unter http://www.hanser.de/978-3-446-458-9
S e ite 1. die. Dephlegmator. zu entfalten. wirksam bleibt. Bild 1
 S e ite 1 Obstbrennanlage mit aktivem Kupferhel lm - eingebautem egelbaren bzw. Aromator - Modell Premium Diese Premium-Hybridanlage ist eine leistungsfähige Neuentwicklung bei den Klein-Destillen für
S e ite 1 Obstbrennanlage mit aktivem Kupferhel lm - eingebautem egelbaren bzw. Aromator - Modell Premium Diese Premium-Hybridanlage ist eine leistungsfähige Neuentwicklung bei den Klein-Destillen für
Oxidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) CO 2
 6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Modellversuch
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Modellversuch
ENGLER-BUNTE-INSTITUT Bereich I: Chemische Energieträger - Brennstofftechnologie. Verfahrenstechnisches Praktikum (22999) am Engler-Bunte-Institut
 ENGLER-BUNTE-INSTITUT Bereich I: Chemische Energieträger - Brennstofftechnologie INHALT Verfahrenstechnisches Praktikum (22999) am Engler-Bunte-Institut - Versuch C3-1 STOFFDATEN VON BENZIN UND DIESEL
ENGLER-BUNTE-INSTITUT Bereich I: Chemische Energieträger - Brennstofftechnologie INHALT Verfahrenstechnisches Praktikum (22999) am Engler-Bunte-Institut - Versuch C3-1 STOFFDATEN VON BENZIN UND DIESEL
Versuch 9: Siedepunktserhöhung und Gefrierpunktserniedrigung
 1 Versuch 9: Siedepunktserhöhung und Gefrierpunktserniedrigung 1. Theorie und Aufgabenstellung Theorie und Methode Lösungen bestehen aus einem Lösungsmittel und dem darin gelösten Stoff. Das Lösemittel
1 Versuch 9: Siedepunktserhöhung und Gefrierpunktserniedrigung 1. Theorie und Aufgabenstellung Theorie und Methode Lösungen bestehen aus einem Lösungsmittel und dem darin gelösten Stoff. Das Lösemittel
Versuchsbeschreibung zum Chemisch-Technischen Grundpraktikum
 Universität Karlsruhe Institut für Chemische Technik Prof. Dr. H. Bockhorn Versuchsbeschreibung zum Chemisch-Technischen Grundpraktikum Glockenbodenkolonne 1 Literatur Bockhard/Güntzschel/Poetschukat Grundlagen
Universität Karlsruhe Institut für Chemische Technik Prof. Dr. H. Bockhorn Versuchsbeschreibung zum Chemisch-Technischen Grundpraktikum Glockenbodenkolonne 1 Literatur Bockhard/Güntzschel/Poetschukat Grundlagen
DIE FILES DÜRFEN NUR FÜR DEN EIGENEN GEBRAUCH BENUTZT WERDEN. DAS COPYRIGHT LIEGT BEIM JEWEILIGEN AUTOR.
 Weitere Files findest du auf www.semestra.ch/files DIE FILES DÜRFEN NUR FÜR DEN EIGENEN GEBRAUCH BENUTZT WERDEN. DAS COPYRIGHT LIEGT BEIM JEWEILIGEN AUTOR. Physiklabor 2 Michel Kaltenrieder 9. Februar
Weitere Files findest du auf www.semestra.ch/files DIE FILES DÜRFEN NUR FÜR DEN EIGENEN GEBRAUCH BENUTZT WERDEN. DAS COPYRIGHT LIEGT BEIM JEWEILIGEN AUTOR. Physiklabor 2 Michel Kaltenrieder 9. Februar
3 Kjeldahl-Kolben, 500 ml Weithals-Erlenmeyerkolben, 10 ml Vollpipette,
 Instrumentelle Bestimmungsverfahren 227 Versuch 451: Bestimmung von Stickstoff Arbeitsanleitung Geräteliste: KJELDAHL-Apparatur, 3 Kjeldahl-Kolben, 500 ml Weithals-Erlenmeyerkolben, 20 ml Vollpipette,
Instrumentelle Bestimmungsverfahren 227 Versuch 451: Bestimmung von Stickstoff Arbeitsanleitung Geräteliste: KJELDAHL-Apparatur, 3 Kjeldahl-Kolben, 500 ml Weithals-Erlenmeyerkolben, 20 ml Vollpipette,
1035 Synthese von p-methoxyacetophenon aus Anisol
 NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
LMPG 1 ÜB5 Grundlagen der Dest. Kombinierte Übungen Seite 1 von 10 LÖSUNGEN
 LMG 1 ÜB5 Grundlagen der Dest. Kombinierte Übungen Seite 1 von 10 Substanz A B C tmin tma Formel Name C C H2O Wasser 8.19621 1730.63 233.426 1 100 H3N Ammoniak 7.4854 926.133 240.17 94 12 Antoine- H4N2
LMG 1 ÜB5 Grundlagen der Dest. Kombinierte Übungen Seite 1 von 10 Substanz A B C tmin tma Formel Name C C H2O Wasser 8.19621 1730.63 233.426 1 100 H3N Ammoniak 7.4854 926.133 240.17 94 12 Antoine- H4N2
ENTLÜFTEN UND ENTGASEN
 ENTLÜFTEN UND ENTGASEN Luft ist ein sehr schlechter Wärmeleiter. Gerade bei Wärmetauschern müssen deshalb die Rohrleitungen an der höchsten Stelle der Anlage entlüftet werden. Bei sehr großen Dampfund
ENTLÜFTEN UND ENTGASEN Luft ist ein sehr schlechter Wärmeleiter. Gerade bei Wärmetauschern müssen deshalb die Rohrleitungen an der höchsten Stelle der Anlage entlüftet werden. Bei sehr großen Dampfund
Destillation von Rotwein
 Destillation von Rotwein Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Zerlegung der Verbindung Wasser Titration Herstellung von Natronlauge Öltröpfchen versuch
Destillation von Rotwein Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Zerlegung der Verbindung Wasser Titration Herstellung von Natronlauge Öltröpfchen versuch
Trennmethoden: fest/flüssig
 Kapitel 3: Trenn und Reinigungsmethoden Verschiedene Methoden, je nach Aufgabenstellung dekantieren, filtrieren, abnutschen, zentrifugieren : Wahl der Methode je nach Niederschlag und Ziel Zustand des
Kapitel 3: Trenn und Reinigungsmethoden Verschiedene Methoden, je nach Aufgabenstellung dekantieren, filtrieren, abnutschen, zentrifugieren : Wahl der Methode je nach Niederschlag und Ziel Zustand des
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Liebigkühler. Rundkolben Vorstoß. Becherglas
 Die Destillation 1 1 Allgemeines Bei der Destillation werden Stoffe mit unterschiedlichen Siedetemperaturen durch Erhitzen voneinander getrennt. Aus Rotwein kann auf diese Weise der Alkohol (Ethanol, Sdp.
Die Destillation 1 1 Allgemeines Bei der Destillation werden Stoffe mit unterschiedlichen Siedetemperaturen durch Erhitzen voneinander getrennt. Aus Rotwein kann auf diese Weise der Alkohol (Ethanol, Sdp.
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b).
 2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
Wie verändern sich die Eigenschaften der Alkohole bei Zunahme der Kohlenstoffzahl?
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Versuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten -
 1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion)
 4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
6016 Oxidation von 2,2-Dimethyl-1,3-propandiol zu 2,2- Dimethylmalonsäure
 6016 Oxidation von 2,2-Dimethyl-1,3-propandiol zu 2,2- Dimethylmalonsäure HNO 3 O O C 5 H 12 O 2 HNO 3 C 5 H 8 O 4 (104.2) (63.0) (132.1) Klassifizierung Reaktionstypen und Stoffklassen Oxidation Alkohol,
6016 Oxidation von 2,2-Dimethyl-1,3-propandiol zu 2,2- Dimethylmalonsäure HNO 3 O O C 5 H 12 O 2 HNO 3 C 5 H 8 O 4 (104.2) (63.0) (132.1) Klassifizierung Reaktionstypen und Stoffklassen Oxidation Alkohol,
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
