Einführung in die Biochemie, Aminosäuren. Prof. Dr. Albert Duschl
|
|
|
- Hans Pohl
- vor 7 Jahren
- Abrufe
Transkript
1 Einführung in die Biochemie, Aminosäuren Prof. Dr. Albert Duschl
2 Themen der Vorlesung Einführung in die Biochemie; Aminosäuren Peptide und Proteine Enzyme Proteinfunktionen Kohlenhydrate Lipide Nukleotide und Nukleinsäuren Proteinbiosynthese Bioenergetik Primärstoffwechsel Antikörper Molekulare Medizin
3 Allgemeine Informationen Die Vorlesung findet als Doppelstunde (90 min) an 12 Terminen statt. Diese Präsentation ist als pdf-file über die Homepage meiner Arbeitsgruppe erhältlich: Die Vorlesung wird von einer Multiple Choice Prüfung abgeschlossen. Dabei müssen nur die Lösungsblätter abgegeben werden, so dass alte Klausuren frei erhältlich sind. Bestehen der Prüfung ist Voraussetzung für die Teilnahme an den Molekularbiologischen und Biochemischen Übungen. Es gibt keine Anwesenheitspflicht, aber wenn Sie nicht kommen und nachher durchfallen schieben Sie es bitte nicht auf die Vorlesung. Die pdf-files reichen zur Prüfungsvorbereitung alleine nicht aus, ohne biochemisches Lehrbuch werden Sie also nicht auskommen. Weitere Fragen? Zum Inhalt der Vorlesung: oder lieber gleich nach der Vorlesung Zum Organisatorischen: oder über PLUSonline
4 FAQ Wann ist die nächste Prüfung? In PLUSonline steht noch kein Termin. Dann steht noch keiner fest. Wir können Räume nicht so lang im Voraus buchen. Wann ist aber ungefähr Prüfung? Normal sind zwei Termine direkt nach Ende der Vorlesungsserie, einer Ende des Semesters oder Anfang der Semesterferien, und einer Ende der Semesterferien. Ich habe noch nicht alle Voraussetzungen laut STEOP, kann ich Prüfung schreiben? Das ist leider vom Studienrecht her nicht möglich. Ich hätte gerne eine mündliche Prüfung. Machen Sie sowas? In gut begründeten Ausnahmefällen, etwa bei körperlicher Behinderung. Sonst nicht. Ich muss die Prüfung bestanden haben um die Übungen Molekularbiologie und Biochemie zu machen, richtig? Richtig. Das stand übrigens schon auf der letzten Folie. Ich habe gehört bei Ihnen und manchen anderen Leuten kann man nur arbeiten wenn man Molekularbiologie studiert hat, aber nicht mit Biologie. Stimmt das? Nein, die beiden Studien werden überall gleichwertig behandelt. Entscheidend ist nur was Sie können. Der Zugang zu Modulen, Bachelor- und Masterarbeiten ist gleich.
5 Empfohlene Lehrbücher Umfangreichere Lehrbücher: Löffler/Petrides: Biochemie und Pathobiochemie Stryer: Biochemie Nelson/Cox: Lehninger Biochemie Voet/Voet/Pratt: Lehrbuch der Biochemie Horton et al.: Biochemie Billigere Alternativen: Löffler: Basiswissen Biochemie Walker/McMahon: Biochemistry Demystified Gar nicht schlecht: Biochemie für Dummies Eher ein Nachschlagewerk, aber auch nicht teuer: Koolman/Röhm: Taschenatlas der Biochemie
6 Grundlagen der Biochemie Biochemie untersucht die molekularen Grundlagen des Lebens. Eine Art Gegenpol bildet die Morphologie, die die strukturellen Grundlagen des Lebens untersucht. Die Disziplin ist als selbständiges Fach um 1900 entstanden als Synthese aus der physiologischen Chemie und der Naturstoffchemie. In Salzburg wird die Biochemie am Fachbereich Molekulare Biologie vertreten. So sieht ihr Professor aus "Biowissenschaften und Gesundheit" Gemäldesammlung des Fachbereichs Molekulare Biologie Universität Salzburg
7 Das wichtigste Molekül: Wasser Dipol Hohe spezifische Wärme (Wärmekapazität) Hohe Verdunstungswärme Bildet Wasserstoffbrückenbindungen Bildet Hydrathüllen Gut wasserlösliche Substanzen: Hydrophil Gemischte Löslichkeit: Amphiphil Schlecht wasserlösliche Substanzen: Hydrophob Dissoziiert in OH - (Hydroxyl-Ionen) und H + (Protonen) Die Protonenkonzentration wird durch den ph-wert angegeben: Der ph-wert ist der negative dekadische Logarithmus der H + -Konzentration. Beispiel: [H + ] = 10-7 mol/l ph = 7 Voet/Voet/Pratt: Lehrbuch der Biochemie
8 Dissoziationskonstante Die Reaktion HA + H 2 O A - + H 3 O + wird beschrieben durch v 1 = k 1 [HA] [H 2 O] (Geschwindigkeit der Hinreaktion) und v 2 = k 2 [H 3 O + ] [A - ] (Geschwindigkeit der Rückreaktion) Im Gleichgewicht ist v 1 = v 2, also ist k 1 [HA] [H 2 O] = k 2 [H 3 O + ] [A - ] oder anders ausgedrückt k 1 /k 2 = [H 3 O + ] [A - ] / [HA] [H 2 O] k 1 /k 2 ergibt die Gleichgewichtskonstante K Statt [H 3 O + ] kann man [H + ] schreiben und [H 2 O] ändert sich praktisch nicht, also gilt: K' = [H + ] [A - ] / [HA] K' ist die Dissoziationskonstante einer Säure. Je höher K', desto stärker ist die Säure.
9 ph-wert von Wasser H 2 O zerfällt spontan in H + und OH -. Das Gleichgewicht der Reaktion H 2 O H + + OH - liegt aber stark auf der linken Seite, d.h. Wasser ist überwiegend doch einfach Wasser. So schön ist Biochemie. Die Gleichgewichtskonstante K beträgt bei 25 C 1.8 x Also: K = 1.8 x = [H + ] [OH - ] / [H 2 O] Sie erinnern sich daß 1 mol Wasser g sind? Da 1 l Wasser ca. 1 kg Wasser entspricht, enthält 1 l Wasser 55.5 mol Wasser. Reines H 2 O ist also 55.5-molar. Daher: [H + ] [OH - ] = 1.8 x = Von H + und OH - müssen gleichviel Moleküle vorhanden sein, und das Produkt ihrer Konzentrationen ist Man kann also die Konzentration der beiden Moleküle festlegen auf 10-7, da 10-7 x 10-7 = Die Konzentration von H + wird angegeben durch den ph-wert (analog zu pk), der definiert ist als - log [H + ]. Der ph-wert von Wasser ist bei den angegebenen Bedingungen also 7.
10 Aminosäuren und Proteine Protein vom griechischen proteios, "von herausragender Bedeutung" Jöns J. Berzelius, 1838 Proteine bestehen aus Aminosäuren. Von den unbegrenzt vielen möglichen Aminosäuren kommen 20 normalerweise in Proteinen vor ("proteinogene Aminosäuren ) Proteine können weitere assoziierte Komponenten haben. Zum Beispiel - Glycoproteine (mit kovalent gebundenen Kohlenhydraten) - Lipoproteine (mit kovalent gebundenen Lipiden) - viele Enzyme (mit Coenzymen oder Ionen) Proteine haben normalerweise - eine bestimmte Aminosäuresequenz - definierbare Struktur - spezifische Expression in bestimmten Zellen oder Geweben Nature, 413, 365 (2001)
11 Allgemeine Struktur von Aminosäuren Prüfer: "Können Sie mir sagen was eine Aminosäure ist?" Student: "Nein." Aminosäuren sind Carbonsäuren die eine Aminogruppe enthalten. Sie besitzen also immer die funktionellen Gruppen -COOH und -NH 2. Aminosäuren sind meist ionisiert, liegen also mit NH 3+, COO -, oder beidem vor. Die C-Atome werden nummeriert (incl. COOH-Gruppe, oder mit griechischen Buchstaben bezeichnet (ohne COOH). Nelson/Cox: Lehninger Principles of Biochemistry Deutsch: Lysin Englisch: Lysine Eine Aminosäure kann mehrere Carboxyloder Aminogruppen haben. Nelson/Cox: Lehninger Principles of Biochemistry
12 Chiralität Eine Aminosäure mit 4 verschiedenen Liganden am α-c-atom hat ein chirales Zentrum: Es sind zwei verschiedene Stereoisomere möglich. Chiralität ("Händigkeit") bedeutet Spiegelsymmetrie: Zwei Objekte sind identisch wie Bild und Spiegelbild, können aber nicht miteinander zur Deckung gebracht werden. Stellen Sie sich zwei Handschuhe vor. Spiegelisomere dieses Typs bezeichnet man als Enantiomere. Sie haben biologisch oft ganz unterschiedliche Eigenschaften, z.b. bei Thalidomid oder bei Carvon. Alle Moleküle mit einem chiralem Zentrum sind optisch aktiv, d.h. sie drehen die Schwingungsebene von polarisiertem Licht. John Tenniel BioSite,
13 D- und L-Aminosäuren Aminosäuren werden nach Emil Fischer als D-und L-Formen unterschieden. Die entsprechende zweidimensionale Auftragung heisst Fischer-Projektion. Die Aminosäuren in Proteinen sind L-Stereoisomere. all figures Nelson/Cox: Lehninger Principles of Biochemistry
14 Jäger und Sammler Mehrere Millionen Jahre lang lebten alle Menschen als Mitglieder von Jäger/Sammler-Gesellschaften. Sammler (Sammlerinnen!) bringen mehr Kalorien nach Hause (Van Zinderen Bakker Palaeoecol. Afr. 15:79-99 (1998), see also Reader, Africa - A biography of a continent (1998)). Aber Jäger versorgten die Gesellschaft mit essentiellen Aminosäuren, für die Fleisch die beste Quelle ist. Absolut essentiell sind in Erwachsenen Lysin, Methionin, Threonin, Isoleucin, Valin, Leucin, Phenylalanin, Tryptophan und Histidin. Bedingt essentiell sind Tyrosin (Synthese aus Phenylalanin) und Cystein (Synthese aus Methionin) wenn viel davon benötigt wird. Arginin ist vor allem in Kindern essentiell. Wir produzieren zwar Arginin, der größte Teil davon wird aber bei der Bildung von Harnstoff gespalten. TIME-LIFE: Die ersten Menschen
15 Einspruch! Die!Kung sind ein San-Volk das in der Kalahari lebt. Traditionell lebten sie als Jäger- Sammler in Gruppen von Personen in der Nähe einer Wasserquelle. (Stimmt soweit alles.) ABER: Ein Hauptbestandteil der Nahrung ist die Mongongo-Nuss (Schinziophyton rautanenii), eine Baumfrucht. Diese ist über weite Zeiträume die wesentliche Quelle für Aminosäuren. Kein Fleisch nötig! ucuiyagi.wordpress.com
16 Gegenrede Die Aminosäurezusammensetzung der Mongongo-Nuss ist ungewöhnlich. Normal kann der Aminosäurebedarf aus Pflanzen nur durch eine Mischung von Pflanzen (das ganze Jahr hindurch) erreicht werden. Das funktioniert nur bei einer entwickelten Landwirtschaft, also seit einigen tausend Jahren. Memo: Landwirtschaft ist etwa so natürlich wie Raumfahrt. Allerdings.!Kung Frauen haben nur etwa alle 4 Jahre ein Kind geboren (Hamilton Paloeecol Afr 9:63-97 (1976)). Die Familien hätten gern mehr Kinder gehabt. Es muss noch etwas anderes als Aminosäuren und Wasser geben das die Fruchtbarkeit begrenzt. Davon später. ebay.de: "Luftbild von rechtwinkligen landwirtschaft..." - J. Blair
17 Die 20 proteinogenen Aminosäuren Nelson/Cox: Lehninger Principles of Biochemistry
18 Spezifische Eigenschaften Nelson/Cox: Lehninger Principles of Biochemistry
19 Was sollten Sie wissen? Versuchen Sie sich doch mal an einigen Übungsfragen zu Aminosäuren: Welche drei Aminosäuren sind aromatisch? Was ist die kleinste proteinogene Aminosäure und was die größte? Was haben Arginin, Histidin und Lysin gemeinsam? Welche Aminosäuren enthalten Schwefel? Was unterscheidet Prolin von den andern 19 proteinogenen Aminosäuren? Welche Aminosäuren können phosphoryliert werden? Welche sind sauer? Was ist die häufigste Aminosäure in Proteinen? Und die seltenste? ABCDEFGHI welche Aminosäuren sind das (und welcher Buchstabe davon bezeichnet keine Standard-Aminosäure)? Was ist der Unterschied zwischen Glutamin, Glutamat und Glutaminsäure? Zeichnen Sie die Strukturformel von Alanin! Zeichnen Sie die Strukturformel von Tyrosin!
20 Seltene Aminosäuren In Proteinen kommen außer den 20 normalen Aminosäuren auch noch weitere Aminosäuren vor. Bis auf zwei entstehen sie alle durch posttranslationale Modifikation. Nicht-Standard Aminosäuren werden nach der Translation (Synthese eines Proteins auf Grundlage einer mrna- Sequenz) durch spezifische Enzyme modifiziert. Die Modifikation der Aminosäuren ist für die Funktion der Proteine erforderlich (Bsp.: 4-Hydroxyprolin in Kollagen). Nelson/Cox: Lehninger Principles of Biochemistry Stryer: Biochemistry
21 21. und 22. Aminosäure Normal werden Nicht-Standard Aminosäuren über posttranslationale Modifikation eingefügt. Die einzigen bekannten Ausnahmen sind Selenocystein (Sec, U) und Pyrrolysin (Pyl, O), deren Verwendung schon auf DNA-Ebene festgelegt wird. In diesen Fällen wird ein Stopcodon durch die Nukleinsäuresequenz in der Umgebung umdefiniert, so dass während der Translation eine spezielle trna bindet und dadurch eine seltene Aminosäure eingefügt wird. (Siehe Vorlesung 8.) Beide Aminosäuren sind sehr selten. Nature
22 Nicht-proteinogene Aminosäuren Viele Aminosäuren kommen im Stoffwechsel vor, ohne daß sie in Proteine eingebaut werden. Löffler/Petrides: Biochemie und Pathobiochemie
23 Aminosäuren in Wasser Wir werden noch viel über Aminosäuren hören, aber vergessen Sie das Wasser nicht. Auch bei den Aminosäuren ist das Lösungsverhalten in Wasser ganz entscheidend. Der menschliche Körper besteht zu etwa 70% aus Wasser. Wenn Sie 70 Kilo wiegen sind also ca. 50 Kilo davon Wasser. Minimale Urinproduktion pro Tag: 500 ml. Der Harnstoff muss verdünnt werden. Denken Sie auch an Schweißproduktion. Tägliche Aufnahme 2-2,5 l, bei Hitze deutlich mehr. Ein Verlust von wenigen % der Körpermasse an Wasser ruft schwere Dehydration hervor, ein Verlust von 10% verläuft fast immer tödlich. Wie vor der Erfindung von Einweg-Plastik- Getränkeflaschen Menschen überleben konnten, bleibt ungeklärt. David Hockney: A bigger splash
Einführung in die Biochemie, Aminosäuren. Prof. Dr. Albert Duschl
 Einführung in die Biochemie, Aminosäuren Prof. Dr. Albert Duschl Themen der Vorlesung Einführung in die Biochemie; Aminosäuren Peptide und Proteine Enzyme Proteinfunktionen Kohlenhydrate Lipide Nukleotide
Einführung in die Biochemie, Aminosäuren Prof. Dr. Albert Duschl Themen der Vorlesung Einführung in die Biochemie; Aminosäuren Peptide und Proteine Enzyme Proteinfunktionen Kohlenhydrate Lipide Nukleotide
Einführung in die Biochemie, Aminosäuren. Prof. Dr. Albert Duschl
 Einführung in die Biochemie, Aminosäuren Prof. Dr. Albert Duschl Themen der Vorlesung Einführung in die Biochemie; Aminosäuren Peptide und Proteine Enzyme Proteinfunktionen Kohlenhydrate Lipide Nukleotide
Einführung in die Biochemie, Aminosäuren Prof. Dr. Albert Duschl Themen der Vorlesung Einführung in die Biochemie; Aminosäuren Peptide und Proteine Enzyme Proteinfunktionen Kohlenhydrate Lipide Nukleotide
Pharmazeutische Biologie Grundlagen der Biochemie
 Pharmazeutische Biologie Grundlagen der Biochemie Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Aminosäure... chirale Moleküle
Pharmazeutische Biologie Grundlagen der Biochemie Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Aminosäure... chirale Moleküle
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Aminosäuren - Proteine
 Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Grundlagen der Zellulären Biochemie
 Grundlagen der Zellulären Biochemie Wasser das Medium des Lebens, Aminosäuren Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie,
Grundlagen der Zellulären Biochemie Wasser das Medium des Lebens, Aminosäuren Vorlesung zum Modul BCB P07 im Bachelor-Studiengang Biochemie Hannover Prof. J. Alves, Institut für Biophysikalische Chemie,
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Die hierarchische Organisation biologischer Strukturen
 Das Lehrbuch Die hierarchische Organisation biologischer Strukturen Die drei Etappen der Evolution von Leben Was ist Biochemie? Untersuchung des Lebens auf molekularer Ebene Leben, wie wir es kennen, ist
Das Lehrbuch Die hierarchische Organisation biologischer Strukturen Die drei Etappen der Evolution von Leben Was ist Biochemie? Untersuchung des Lebens auf molekularer Ebene Leben, wie wir es kennen, ist
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Peptide Proteine. 1. Aminosäuren. Alle optisch aktiven proteinogenen Aminosäuren gehören der L-Reihe an: 1.1 Struktur der Aminosäuren
 1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
Aminosäuren und Peptide
 Aminosäuren und Peptide Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Genetischer Code Basentriplets codieren für Aminosäuren Aminosäuren Definition: Aminosäuren (Aminocarbonsäuren)
Aminosäuren und Peptide Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Genetischer Code Basentriplets codieren für Aminosäuren Aminosäuren Definition: Aminosäuren (Aminocarbonsäuren)
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
U. Helmich, Intensivkurs "Proteine" Seite 1
 U. Helmich, Intensivkurs "Proteine" Seite 1 Crashkurs "Proteine" Proteine bestehen aus Aminosäuren, von denen es rund 20 verschiedene gibt. Die meisten Proteine bestehen mehreren hundert oder sogar mehreren
U. Helmich, Intensivkurs "Proteine" Seite 1 Crashkurs "Proteine" Proteine bestehen aus Aminosäuren, von denen es rund 20 verschiedene gibt. Die meisten Proteine bestehen mehreren hundert oder sogar mehreren
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Lösungsblatt zu Aufbau von Aminosäuren
 Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
10 BIOGENE-AMINE 4 NICHT-PROTEINOGENE- AS. 20 PROTEINOGENE AS glucoplastisch/ketoplastisch 8 ESSENTIELLE AS
 Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit
 In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
Foliensatz; Arbeitsblatt; Internet. Je nach chemischem Wissen können die Proteine noch detaillierter besprochen werden.
 03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
Probeklausur zur Vorlesung. Name:... Vorname:... Matr.-Nr... Datum:
 1 Probeklausur zur Vorlesung "Organische Chemie für Mediziner im Sommersemester 2016 Name:... Vorname:... Matr.-Nr.... Datum: 11.07.2016 Studienfach: Medizin Biomedizin Zahnmedizin Technol. d. Funktionswerkstoffe
1 Probeklausur zur Vorlesung "Organische Chemie für Mediziner im Sommersemester 2016 Name:... Vorname:... Matr.-Nr.... Datum: 11.07.2016 Studienfach: Medizin Biomedizin Zahnmedizin Technol. d. Funktionswerkstoffe
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Aminosäuren. Die Mischung macht's. Die Proteinfabrik. ANKUBERO GmbH. Verschiedene Aminosäuren und Proteine
 Aminosäuren ANKUBERO GmbH Lieber Kunde, lieber Interessent, Die Mischung macht's Verschiedene Aminosäuren und Proteine Aufgeteilt in drei Hauptgruppen unterscheidet man essenzielle, semi-essenzielle oder
Aminosäuren ANKUBERO GmbH Lieber Kunde, lieber Interessent, Die Mischung macht's Verschiedene Aminosäuren und Proteine Aufgeteilt in drei Hauptgruppen unterscheidet man essenzielle, semi-essenzielle oder
Bachelorprüfung im Fach Biologie, Teilfach Chemie am
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 14.03.2014 2 Aufgabe 1 a) Skizzieren Sie bitte unten die Strukturformel eines aromatischen Aldehyds mit der Summenformel C 8 H 8 3 b) Zeichnen Sie bitte
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 14.03.2014 2 Aufgabe 1 a) Skizzieren Sie bitte unten die Strukturformel eines aromatischen Aldehyds mit der Summenformel C 8 H 8 3 b) Zeichnen Sie bitte
Organische Chemie der biologischen Stoffwechselwege
 Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Aminosäuren besitzen eine saure und eine basische Gruppe. Sie enthalten mindestens eine Carboxylgruppe und mindestens eine Aminogruppe.
 Aufbau von Aminosäuren Aufgabenstellung Lesen Sie den nachfolgenden Text aufmerksam durch und bearbeiten Sie die Fragen schriftlich. Versuchen Sie die Fragen alle zu beantworten. Arbeitsform Arbeiten Sie
Aufbau von Aminosäuren Aufgabenstellung Lesen Sie den nachfolgenden Text aufmerksam durch und bearbeiten Sie die Fragen schriftlich. Versuchen Sie die Fragen alle zu beantworten. Arbeitsform Arbeiten Sie
Energie aus Aminosäuren - Wundermittel Protein?
 Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
FACHINFORMATIONEN. Vertrieb in Deutschland: OTC SIEBENHANDL GmbH, Lämmerweg 29, D Ulm,
 FACHINFORMATIONEN Vertrieb in Deutschland: OTC SIEBENHANDL GmbH, Lämmerweg 29, D-89079 Ulm, +49 7305 96700 Fotos Montage: Dmitry Naumov / Franz Metelec / Nina Hoff / Maridav / Kzenon fotolia.com Konzept:
FACHINFORMATIONEN Vertrieb in Deutschland: OTC SIEBENHANDL GmbH, Lämmerweg 29, D-89079 Ulm, +49 7305 96700 Fotos Montage: Dmitry Naumov / Franz Metelec / Nina Hoff / Maridav / Kzenon fotolia.com Konzept:
Angelika Stöcklinger. Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate
 Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Rund um das Hühnerei - die Chemie der Proteine
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Rund um das Hühnerei - die Chemie der Proteine Das komplette Material finden Sie hier: School-Scout.de VII/B Organische Verbindungen
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Rund um das Hühnerei - die Chemie der Proteine Das komplette Material finden Sie hier: School-Scout.de VII/B Organische Verbindungen
pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
 Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten.
 Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten. Wie bezeichnet man den Strang der DNA- Doppelhelix, der die
Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten. Wie bezeichnet man den Strang der DNA- Doppelhelix, der die
Chiralität und Leben
 Chiralität und Leben Symmetrie: Ebenmaß Geometrie: Bestimmte Operationen bilden Objekt auf sich selbst ab (dabei bleibt es quasi unverändert) Rotationssymmetrie Achsensymmetrie - Spiegelsymmetrie Punktsymmetrie
Chiralität und Leben Symmetrie: Ebenmaß Geometrie: Bestimmte Operationen bilden Objekt auf sich selbst ab (dabei bleibt es quasi unverändert) Rotationssymmetrie Achsensymmetrie - Spiegelsymmetrie Punktsymmetrie
Aminosäuren und Proteine
 Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
biozym IMC MINCEUR REGULATION & BALANCE DER KÖRPERMASSE KONZENTRIERTE DOSIERUNG 15 Tage Entdecken Sie in diesem Heft alle Vorteile
 biozym IMC MINCEUR KURBELT DIE FETTVERBRENNUNG & DIE ENTSCHLACKUNG AN LÖST DEN SCHLANKHEITSPROZESS AUS WIRKT ANREGEND AUF DEN STOFFWECHSEL REGULIERT DEN KREISLAUF KLÄRT & REMINERALISIERT 16 REGULATION
biozym IMC MINCEUR KURBELT DIE FETTVERBRENNUNG & DIE ENTSCHLACKUNG AN LÖST DEN SCHLANKHEITSPROZESS AUS WIRKT ANREGEND AUF DEN STOFFWECHSEL REGULIERT DEN KREISLAUF KLÄRT & REMINERALISIERT 16 REGULATION
Arbeitsheft. Biochemie. Timo Brandenburger. Fachbeirat Prof. Dr. Klaus-Heinrich Röhm. 2., aktualisierte Auflage
 Arbeitsheft Biochemie Timo Brandenburger Fachbeirat Prof. Dr. Klaus-Heinrich Röhm 2., aktualisierte Auflage Timo Brandenburger Stiftstr. 2 24103 Kiel Fachbeirat: Prof. Dr. Klaus-Heinrich Röhm Universität
Arbeitsheft Biochemie Timo Brandenburger Fachbeirat Prof. Dr. Klaus-Heinrich Röhm 2., aktualisierte Auflage Timo Brandenburger Stiftstr. 2 24103 Kiel Fachbeirat: Prof. Dr. Klaus-Heinrich Röhm Universität
4. Stereochemie. Das wichtigste Kriterium für Chiralität ist, dass sich Objekt und Spiegelbild nicht zur Deckung bringen lassen.
 4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis o- Toluidin positiv, Glu-Oxidase-Peroxidase neg? Begründung!
 TEST1 Schreiben sie 2 saure Aminosäuren an! Was sind essentielle As geben sie 3 Beispiele an! Was versteht man unter Glykopyranose? Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis
TEST1 Schreiben sie 2 saure Aminosäuren an! Was sind essentielle As geben sie 3 Beispiele an! Was versteht man unter Glykopyranose? Unbekannte Probe- entweder D-Glu., L-Glu., beides oder H2O? Testergebnis
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Stoffwechsel - Energiebereitstellung - Biomoleküle
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine
 Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Übungen zur Vorlesung Aminosäuren, Peptide, Proteine Dr. Katja
Übungen zu den Vorlesungen Aminosäuren und Peptide Proteine Dr. Katja Arndt Institut für Biologie III http://www.molbiotech.uni-freiburg.de/ka Übungen zur Vorlesung Aminosäuren, Peptide, Proteine Dr. Katja
Übung zum chemischen Praktikum für Studierende der Biologie und Medizin Übung Nr. 1, /
 Übung zum chemischen Praktikum für Studierende der Biologie und Medizin Übung Nr. 1, 18.04.11 / 19.04.11 Lösung 1. Proteine sind Biopolymere, welche aus langen Ketten von Aminosäuren bestehen. a) Zeichnen
Übung zum chemischen Praktikum für Studierende der Biologie und Medizin Übung Nr. 1, 18.04.11 / 19.04.11 Lösung 1. Proteine sind Biopolymere, welche aus langen Ketten von Aminosäuren bestehen. a) Zeichnen
Zusammensetzung und Struktur der Proteine. Stryer (6. Auflage) Kapitel 2
 Zusammensetzung und Struktur der Proteine Stryer (6. Auflage) Kapitel 2 Vielfalt der Proteine Wie kommt diese Vielfalt an Proteinen zustande? 1. Peptide und Polypeptide sind Ketten aus 20 verschiedenen
Zusammensetzung und Struktur der Proteine Stryer (6. Auflage) Kapitel 2 Vielfalt der Proteine Wie kommt diese Vielfalt an Proteinen zustande? 1. Peptide und Polypeptide sind Ketten aus 20 verschiedenen
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.08.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 26.08.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
15. Aminosäuren, Peptide und Proteine
 Inhalt Index 15. Aminosäuren, Peptide und Proteine Proteine (Polypeptide) erfüllen in biologischen Systemen die unterschiedlichsten Funktionen. So wirken sie z.b. bei vielen chemischen Reaktionen in der
Inhalt Index 15. Aminosäuren, Peptide und Proteine Proteine (Polypeptide) erfüllen in biologischen Systemen die unterschiedlichsten Funktionen. So wirken sie z.b. bei vielen chemischen Reaktionen in der
a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist zu Propansäure oxidierbar. - Die
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist zu Propansäure oxidierbar. - Die
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Erratum zur Diplomarbeit von Andreas Bender. Korrekturverzeichnis: Kapitel 3.2.2, Seiten 39-46
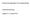 Erratum zur Diplomarbeit von Andreas Bender Korrekturverzeichnis: Kapitel 3.2.2, Seiten 39-46 3.2.2. Einzelne Aminosäuren in N-terminalen Abschnitten In den Abbildungen 16-22 sind die relativen Aminosäurehäufigkeiten
Erratum zur Diplomarbeit von Andreas Bender Korrekturverzeichnis: Kapitel 3.2.2, Seiten 39-46 3.2.2. Einzelne Aminosäuren in N-terminalen Abschnitten In den Abbildungen 16-22 sind die relativen Aminosäurehäufigkeiten
Bildungs- und Wissenszentrum Boxberg Einsatzmöglichkeiten von Körnerleguminosen in der Schweinefütterung
 Bildungs- und Wissenszentrum Boxberg Einsatzmöglichkeiten von Körnerleguminosen in der Schweinefütterung B. Zacharias LSZ Boxberg Einsatz von Sojaschrot als Proteinfuttermittel Dafa x8 Fassung, 2012 Proteinfuttermittel
Bildungs- und Wissenszentrum Boxberg Einsatzmöglichkeiten von Körnerleguminosen in der Schweinefütterung B. Zacharias LSZ Boxberg Einsatz von Sojaschrot als Proteinfuttermittel Dafa x8 Fassung, 2012 Proteinfuttermittel
Kohlenhydrate. Prof. Dr. Albert Duschl
 Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Das Spurenelement Chrom III als Komponente des Glucose Toleranz Faktors
 Das Spurenelement Chrom III als Komponente des Glucose Toleranz Faktors Obwohl nicht mehr als etwa 6 mg Chrom im menschlichen Körper vorkommt, spielt es eine wichtige Rolle im Stoffwechsel der Kohlenhydrate.Die
Das Spurenelement Chrom III als Komponente des Glucose Toleranz Faktors Obwohl nicht mehr als etwa 6 mg Chrom im menschlichen Körper vorkommt, spielt es eine wichtige Rolle im Stoffwechsel der Kohlenhydrate.Die
BIOINF1110 Einführung in die Bioinforma7k. 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on
 BIOINF1110 Einführung in die Bioinforma7k 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Zentrum für Bioinforma7k Tübingen Proteine Zentrales Dogma DNA Transkription mrna
BIOINF1110 Einführung in die Bioinforma7k 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Zentrum für Bioinforma7k Tübingen Proteine Zentrales Dogma DNA Transkription mrna
BIOINF1110 Einführung in die Bioinforma7k. Molekulare Maschinen Proteinstrukturen und ihre Funk/on
 BIOINF1110 Einführung in die Bioinforma7k Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Angewandte Bioinforma0k Zentrum für Bioinforma0k Tübingen Proteine 2 Zentrales Dogma
BIOINF1110 Einführung in die Bioinforma7k Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Angewandte Bioinforma0k Zentrum für Bioinforma0k Tübingen Proteine 2 Zentrales Dogma
Sommersemester 2016 Seminar Stöchiometrie
 Sommersemester 2016 Seminar Stöchiometrie Themenüberblick Kurze Wiederholung der wichtigsten Formeln Neue Themen zur Abschlussklausur: 1. Elektrolytische Dissoziation 2. ph-wert Berechnung 3. Puffer Wiederholung
Sommersemester 2016 Seminar Stöchiometrie Themenüberblick Kurze Wiederholung der wichtigsten Formeln Neue Themen zur Abschlussklausur: 1. Elektrolytische Dissoziation 2. ph-wert Berechnung 3. Puffer Wiederholung
Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Chemische Gleichgewichte, Säuren und
 Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
8. Aminosäuren - (Proteine) Eiweiß
 8. Aminosäuren - (Proteine) Eiweiß Proteine sind aus Aminosäuren aufgebaut. Aminosäuren bilden die Grundlage der belebten Welt. 8.1 Struktur der Aminosäuren Aminosäuren sind organische Moleküle, die mindestens
8. Aminosäuren - (Proteine) Eiweiß Proteine sind aus Aminosäuren aufgebaut. Aminosäuren bilden die Grundlage der belebten Welt. 8.1 Struktur der Aminosäuren Aminosäuren sind organische Moleküle, die mindestens
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Was ist denn NAD / NADP??
 Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Modulabschlussprüfung Chemie für LA-Biologen (o. HF Chemie)
 Modulabschlussprüfung Chemie für LA-Biologen (o. HF Chemie) Nachklausur 18.03.2016 Zeit: 120 min Seite 1 Seite 2 Seite 3 Seite 4 Seite 5 Seite 6 Seite 7 / 18 / 18 / 10 / 10 / 19 / 15 / 10 Gesamt: Note:
Modulabschlussprüfung Chemie für LA-Biologen (o. HF Chemie) Nachklausur 18.03.2016 Zeit: 120 min Seite 1 Seite 2 Seite 3 Seite 4 Seite 5 Seite 6 Seite 7 / 18 / 18 / 10 / 10 / 19 / 15 / 10 Gesamt: Note:
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O 3 ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist vollständig mit Wasser mischbar.
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 8 O 3 ein, die die folgenden Eigenschaften besitzt: - Die Verbindung ist vollständig mit Wasser mischbar.
Kohlenhydrate. Prof. Dr. Albert Duschl
 Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Biochemie I. für Studierende in den Bachelorstudiengängen Biologie und Molekulare Biotechnologie
 Biochemie I für Studierende in den Bachelorstudiengängen Biologie und Molekulare Biotechnologie Anything found to be true of E. coli must also be true of elephants (Jaques Monod) 1 2 Themen Biochemie I
Biochemie I für Studierende in den Bachelorstudiengängen Biologie und Molekulare Biotechnologie Anything found to be true of E. coli must also be true of elephants (Jaques Monod) 1 2 Themen Biochemie I
COOH. Die Aminosäuren tragen laborübliche Abkürzungen, so stehen z. B. Gly für Glycin oder Phe für Phenylalanin.
 Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler
 Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Chiralität in der Natur und synthetisch
 Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
0.1 Eiweißstoffe (Proteine)
 1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
ANWENDUNG Geeignet für ambitionierte AthletInnen. Vorzugsweise vor und nach der Belastung je 1 Shake.
 PRODUKTEBESCHRIEB Eiweiss dient dem Aufbau und Erhalt der Muskelmasse nach harten Trainings. 44/44 PRO Recovery ist ein hochwertiges, natürlich gesüsstes Proteinsupplement mit All-in- One-Charakter. Die
PRODUKTEBESCHRIEB Eiweiss dient dem Aufbau und Erhalt der Muskelmasse nach harten Trainings. 44/44 PRO Recovery ist ein hochwertiges, natürlich gesüsstes Proteinsupplement mit All-in- One-Charakter. Die
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Aminosäure Seitenkette pks. 20 Aminosäuren im genetischen Code verankert. α -Aminosäuren R. Fischer-projektion. COOH H 2 N H R D-Aminosäuren
 20 Aminosäuren im genetischen ode verankert. Gruppe aure Aminosäuren und ihre Amide Aminosäure eitenkette pks Asparaginsäure (D) - 2-3.9 Glutaminsäure (E) -( 2 ) 2-4.2 α -Aminosäuren 2 3 Zwitterion Fischer-projektion
20 Aminosäuren im genetischen ode verankert. Gruppe aure Aminosäuren und ihre Amide Aminosäure eitenkette pks Asparaginsäure (D) - 2-3.9 Glutaminsäure (E) -( 2 ) 2-4.2 α -Aminosäuren 2 3 Zwitterion Fischer-projektion
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Bachelorprüfung im Fach Biologie, Teilfach Chemie am 16.05.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
Bachelorprüfung im Fach Biologie, Teilfach Chemie am 16.05.2014 2 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O 3 ein, die die folgenden Eigenschaften
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
PURE WHEY HEALTH FOOD FOR YOUR BRAND. Sports Nutrition. Auch erhältlich: Molkenprotein-Mix
 PURE WHEY Whey Protein (Molkenprotein) zählt zu den schnelleren, regenerativen Proteinen mit einer hochwertigen Aminosäurenzusammensetzung und einem hohen Anteil an BCAAs. Pure Whey enthält reines Molkenproteinisolat,
PURE WHEY Whey Protein (Molkenprotein) zählt zu den schnelleren, regenerativen Proteinen mit einer hochwertigen Aminosäurenzusammensetzung und einem hohen Anteil an BCAAs. Pure Whey enthält reines Molkenproteinisolat,
Bachelor Studiengang Ernährungswissenschaften Seminar Biochemie der Ernährung (Modul BE2.3) Übersicht Seminarthemen
 Biochemie der Ernährung (Modul BE2.3) Prof. Dr. Stefan Lorkowski 1 Bachelor Studiengang Ernährungswissenschaften Seminar Biochemie der Ernährung (Modul BE2.3) Übersicht Seminarthemen Biosynthese von Aminosäuren
Biochemie der Ernährung (Modul BE2.3) Prof. Dr. Stefan Lorkowski 1 Bachelor Studiengang Ernährungswissenschaften Seminar Biochemie der Ernährung (Modul BE2.3) Übersicht Seminarthemen Biosynthese von Aminosäuren
Intensivkurs Biologie
 Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
Intensivkurs 2016 - Biologie 1. Makromoleküle Lektüre im Cornelsen, Biologie Oberstufe : Chemische Grundlagen: Lipide (S. 40), Proteine (S. 41-42), Kohlenhydrate (S. 92-93) 1.1. Kohlenstoff-Verbindungen
HA + B A - + HB + Säuren und Basen. Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor!
 Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
Säuren und Basen Definition nach Brønsted: Eine Säure ist ein Protonen-Donor, eine Base ein Protonen-Akzeptor! Die Tendenz ein Proton abzuspalten (Säure) bzw. aufzunehmen (Base) bezeichnet man als Säure-
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Nanotechnologie der Biomoleküle. Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie. Aufbau Struktur Funktion
 anotechnologie der Biomoleküle Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie Aufbau Struktur Funktion Zentrum für Mikro- und anotechnologien Das Miller-Urey-Experiment (auch
anotechnologie der Biomoleküle Aminosäuren und Proteine: Bausteine der Biologie und der Bionanotechnologie Aufbau Struktur Funktion Zentrum für Mikro- und anotechnologien Das Miller-Urey-Experiment (auch
ERBOTIN PF. Erbsenproteinisolat. GUSTAV PARMENTIER GmbH
 ( 80% Protein) Geschmacksneutral Hohe Löslichkeit Hohe Emulgierfähigkeit Gute Wasser- und Fettbindefähigkeit Hochwertiger Proteinlieferant Isoliertes Erbsenprotein - ein hochfunktionelles. Das isolierte
( 80% Protein) Geschmacksneutral Hohe Löslichkeit Hohe Emulgierfähigkeit Gute Wasser- und Fettbindefähigkeit Hochwertiger Proteinlieferant Isoliertes Erbsenprotein - ein hochfunktionelles. Das isolierte
Das perfekte Protein für jeden Zeitpunkt!
 DYMATIZE ELITE 100% WHEY Das perfekte Protein für jeden Zeitpunkt Produktbeschreibung Das perfekte Protein für jeden Zeitpunkt! Du bist auf der Suche nach dem perfekten Protein für jeden Zeitpunkt und
DYMATIZE ELITE 100% WHEY Das perfekte Protein für jeden Zeitpunkt Produktbeschreibung Das perfekte Protein für jeden Zeitpunkt! Du bist auf der Suche nach dem perfekten Protein für jeden Zeitpunkt und
Studiengang Bsc Biowissenschaften. Modul-begleitende Prüfung. Organische Chemie
 Studiengang Bsc Biowissenschaften Modul-begleitende Prüfung Organische Chemie 26.07.2016 Name: Vorname: Matrikelnummer: Geboren am: in: Wiederholer/in dieser Klausur: Ja Nein Dauer der Klausur: 90 Minuten
Studiengang Bsc Biowissenschaften Modul-begleitende Prüfung Organische Chemie 26.07.2016 Name: Vorname: Matrikelnummer: Geboren am: in: Wiederholer/in dieser Klausur: Ja Nein Dauer der Klausur: 90 Minuten
7.1 Einleitung... 2. 7.2 Proteine... 2. 7.3 Der chemische Aufbau der Proteine... 4 7.3.1 Peptide... 4. 7.4 Aminosäuren... 5
 Ernährungsberatung Lernheft 7 Eiweiß Teil 1 Chemischer Aufbau der Proteine Inhaltsverzeichnis: 7.1 Einleitung... 2 7.2 Proteine... 2 7.3 Der chemische Aufbau der Proteine... 4 7.3.1 Peptide... 4 7.4 Aminosäuren...
Ernährungsberatung Lernheft 7 Eiweiß Teil 1 Chemischer Aufbau der Proteine Inhaltsverzeichnis: 7.1 Einleitung... 2 7.2 Proteine... 2 7.3 Der chemische Aufbau der Proteine... 4 7.3.1 Peptide... 4 7.4 Aminosäuren...
Organisch-Chemisches Institut Fakultät für Chemie und Geowissenschaften Universität Heidelberg 07. September 2009
 rganisch-chemisches Institut Fakultät für Chemie und Geowissenschaften Universität eidelberg 07. September 2009 Musterlösung zur Wiederholungsklausur zur Experimentalvorlesung rganische Chemie von Prof.
rganisch-chemisches Institut Fakultät für Chemie und Geowissenschaften Universität eidelberg 07. September 2009 Musterlösung zur Wiederholungsklausur zur Experimentalvorlesung rganische Chemie von Prof.
Aufgabe 1: Geben Sie die korrespondierenden Basen zu folgenden Verbindungen an: a) H 3 PO 4 b) H 2 PO 4
 Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Wintersemester 2016 Seminar Stöchiometrie
 Wintersemester 2016 Seminar Stöchiometrie Tutorien Raum Termin Hörsaal OSZ H5 Mo. 19.12., 18-20 Uhr Hörsaal OSZ H5 Fr. 13.1.,16-18 Uhr Hörsaal OSZ H5 Mo. 30.01., 18-20 Uhr Hörsaal OSZ H5 Mo. 06.02., 18-20
Wintersemester 2016 Seminar Stöchiometrie Tutorien Raum Termin Hörsaal OSZ H5 Mo. 19.12., 18-20 Uhr Hörsaal OSZ H5 Fr. 13.1.,16-18 Uhr Hörsaal OSZ H5 Mo. 30.01., 18-20 Uhr Hörsaal OSZ H5 Mo. 06.02., 18-20
Das perfekte Whey für jeden Zeitpunkt!
 DYMATIZE ELITE 100% WHEY Das perfekte Whey für jeden Zeitpunkt Produktbeschreibung Das perfekte Whey für jeden Zeitpunkt! Du bist auf der Suche nach dem perfekten Whey-Protein für jeden Zeitpunkt und zum
DYMATIZE ELITE 100% WHEY Das perfekte Whey für jeden Zeitpunkt Produktbeschreibung Das perfekte Whey für jeden Zeitpunkt! Du bist auf der Suche nach dem perfekten Whey-Protein für jeden Zeitpunkt und zum
Biochemie für Lehramt Biologie
 Biochemie für Lehramt Biologie (11-BIO-0510 / 11-BIO-0554) und Einführung in die Biochemie für B.Sc. Informatik (11-BCH-0530) Wintersemester 2017/18 Institut für Biochemie Prof. Dr. Gunhild Layer 1 Biochemie
Biochemie für Lehramt Biologie (11-BIO-0510 / 11-BIO-0554) und Einführung in die Biochemie für B.Sc. Informatik (11-BCH-0530) Wintersemester 2017/18 Institut für Biochemie Prof. Dr. Gunhild Layer 1 Biochemie
Martin Raiber Chemie Protokoll Nr Gruppe 2 (Schrankseite) Untersuchung von Glycin
 Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
BIOCHEMIE. Teil 2: Aminosäuren, Proteine, Enzyme. Urheberrechtlich geschütztes Material. Lernkarteikarten Veterinärmedizin - BIOCHEMIE
 Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Aminosäuren & Ketosäuren BIOGENE AMINE
 BIOGENE AMINE Von Mohammed Jaber BIOGENE AMINE: Biogene Amine sind AS ohne COOH-Gruppe! Und warum sind sie so wichtig? Von Mohammed Jaber und Proteine BIOGENE AMINE: Durch die Abspaltung der COOH- Gruppe
BIOGENE AMINE Von Mohammed Jaber BIOGENE AMINE: Biogene Amine sind AS ohne COOH-Gruppe! Und warum sind sie so wichtig? Von Mohammed Jaber und Proteine BIOGENE AMINE: Durch die Abspaltung der COOH- Gruppe
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Säuren und Basen. Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O H 3 O + + OH -
 Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O + (aq)-ionen anzugeben. Aus der Gleichung: H 2 O + H 2 O H 3 O + + OH - c(h 3 O + ) c(oh - ) K
Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O + (aq)-ionen anzugeben. Aus der Gleichung: H 2 O + H 2 O H 3 O + + OH - c(h 3 O + ) c(oh - ) K
