Eigenschaften der Brennstoffzelle
|
|
|
- Elke Bayer
- vor 7 Jahren
- Abrufe
Transkript
1 Experimentelle Übungen für Fortgeschrittene Aufgaben im Institut für Materialphysik Aufgabe 2 Eigenschaften der Brennstoffzelle Inhaltsverzeichnis 1 Aufgabe 2 2 Theoretische Voraussetzungen 2 3 Literatur 2 4 Physikalische Grundlagen 3 5 Versuchsdurchführung und Auswertung 11 6 Fragen zum Versuch 15 Stand: SS 2014 Ausgabedatum: 7 April
2 1 Aufgabe Mittels Elektrolyse wird Wasser gespalten. Mithilfe von H 2 - und O 2 -Gasen wird eine Wasserstoff-Brennstoffzelle betrieben. Die Hauptaufgabe des Versuchs liegt in der Messung von Wirkungsgraden und Strom-Spannungs-Kennlinien. Diese zeigen Vorzüge und Nachteile von Brennstoffzellen auf. Der Versuch bietet Grundverständnisse vom Aufbau, Wirkungsprinzip und Eigenschaften von Brennstoffzellen. Die Struktur des Versuchs ist wie folgt: 1) Eine Solarzelle wird benutzt um Strom zu produzieren. 2) Mittels Strom wird im Elektrolyseur Wasser in Gase aufgespalten. 3) Die Gase betreiben eine unterschiedlich belastete Brennstoffzelle. Weitere Brennstoffzellen, darunter eine zerlegbare, ermöglichen Messungen an Systemen mit Parallel- und Reihenschaltungen. 2 Theoretische Voraussetzungen Grundlagen der Thermodynamik Grundlagen zur Festkörperphysik Grundlagen der Elektrochemie 3 Literatur [1] A. Macdonald, M. Berry: Wasserstoff: Energie für morgen, heliocentris Berlin 2000, S [2] J. Larminie, A. Dicks: Fuel Cell Systems Explained, John Wiley & Sons Ltd, West Sussex 2003, Seiten
3 4 Physikalische Grundlagen 4.1 Brennstoffzellen Energie lässt sich nicht erzeugen sondern nur aus einer Form in eine andere überführen. So lässt sich zum Beispiel potentielle Energie in Kinetische Energie umwandeln, wie es bei einem Federpendel passiert. Um gespeicherte Energie freizusetzen gibt es verschiedene Ansätze die von der Form der Speicherung abhängen. In Verbrennungsmotoren wir beispielsweise chemische Energie mittels Oxidation freigesetzt. Typischerweise werden chemische Verbindungen wie Kohlenwasserstoffe verbrannt. Die in der Expansion freiwerdende Energie kann im Motor in Bewegung umgewandelt werden und ist somit als mechanische Energie verfügbar. Verbrennungsmotoren bringen jedoch einige Schwachstellen mit sich. Wie in der Thermodynamikvorlesung erklärt besitzen Verbrennungsmotoren einen begrenzten Wirkungsgrad (Ottomotor: 15-20%). Außerdem entstehen bei der Verbrennung unerwünschte Schadstoffe und viel CO 2. In Brennstoffzellen ist es möglich einen weitaus höheren Wirkungsgrad zu erzielen als in Verbrennungsmotoren. Da eine Brennstoffzelle keine Wärmekraftmaschine ist unterliegt ihr Wirkungsgrad nicht den Beschränkungen des Carnot-Faktors. Brennstoffzellen kommen ohne bewegliche Teile aus und haben somit keine unnötigen Reibungsverluste und auch weniger Verschleißteile. Durch diese Vorteile sind Wirkungsgrade von 60-70% möglich. In einer mit Wasserstoff betriebenen Brennstoffzelle ist Wasser das einzige Abfallprodukt. Einige Brennstoffzellen werden auch mit Kohlenstoffhaltigen Brennstoffen (z.b. Alkohol) betrieben. Diese produzieren auch CO 2, jedoch in einem wesentlich geringeren Maßstab als herkömmliche Verbrennungsmotoren. Die mit Wasserstoff betriebene Brennstoffzelle ist eine der einfachsten Formen. Sie besteht aus zwei Gasflussplatten, eine für Sauerstoff, eine für Wasserstoff (Abbildung 1). Dazwischen finden sich die beiden Elektroden (Anode und Kathode), welche durch eine Polymermembran getrennt sind. Die Elektroden bestehen aus porösen Kohlenstoffgeweben und nehmen das durch die Gasflussplatten gleichmäßig verteilte Gas auf. Der Wasserstoff oxidiert an der Anode durch Abgabe von Elektronen. Diese fließen durch den Stromkreis zur Kathode. Die Polymerelektrolytmembran (PEM; auch Proton Exchange Membrane) lässt keine Gase aber die Protonen passieren. Die Wasserstoffatome können an der Kathodenseite mit dem Sauerstoff zu Wasser reagieren. Die Funktionsweise erinnert so an eine Batterie, jedoch kommt die chemische Energie nicht aus den Elektroden sondern aus dem Brennstoff. Die Reaktionen an Kathode und Anode lauten wie folgt: Anode: Kathode: Gesamtreaktion: 2 2 Die Zersetzung von Wasser bei der Elektrolyse geschieht ab einer Spannung von 1,23 V. Genau diese Spannung liefert eine Wasserstoff-Brennstoffzelle im Maximum. Realistisch sind durch innere Widerstände und weitere Faktoren 0,6-0,9 V. Mehrere Brennstoffzellen in Reihe können aber höhere Spannungen liefern. 3
4 Abbildung 1 Funktionsprinzip einer Wasserstoff-Brennstoffzelle Polymerelektrolytmembran Die Membran-Elektroden-Einheit besteht aus den porösen Kohlenstoffmatten welche die Polymermembran umschließen. Die Elektroden sind sehr fein mit Platin beschichtet. Platin fungiert als Katalysator für die Wasserstoffoxidation und die Sauerstoffreduktion. Darüber hinaus ist Platin sehr edel und chemisch stabil. Die sehr feine Platinverteilung hält den Preis einer Brennstoffzelle niedrig da die Produktionskosten stark von der verwendeten Menge Platin abhängen. Die Elektrolytmembran besteht aus dem Polymer Nafion. Dieses wurde Ende der 1980er Jahre von der Firma DuPont entwickelt. Nafion ist ein auf Teflon basierendes Polymer. Die Rolle dieser Membran ist es Protonen zu leiten ohne Gase passieren zu lassen. Abbildung 4 zeigt die Strukturr von Nafion. Abbildung 2 Strukturformel des Nafion Polymers 4
5 4.1.2 Weiter Brennstoffzellentypen Polymerelektroly tmembran- Brennstoffzelle (PEMFC) C Fahrzeuge, stationäre Kraftwerke, tragbare Stromversorgung C Fahrzeuge, tragbare Stromversorgung Direkt- Methanol- Brennstoffzelle (DMFC) Phosphorsaure Brennstoffzelle (PAFC) 200 C stationäre Kraftwerke Geschmolzene- Carbonat- Brennstoffzelle (MCFC) 650 C stationäre Kraftwerke Festoxid- Brennstoffzelle (SOFC) Protonenleitender Polymerelektrolyt Protonenleitender Polymerelektrolyt Brennstoffzelle Elektrolyt Anoden- Brennstoff Alkalische Kaliumhydroxidlö Brennstoffzelle sung (AFC) Kathodengas Betriebstemperatur Anwendungen Wasserstoff Sauerstoff C Raumfahrt, U- Boote Wasserstoff Sauerstoff aus der Luft Methanol Sauerstoff aus der Luft Phosphorsäure Wasserstoff Sauerstoff aus der Luft Geschmolzene Alkalicarbonate Keramischer Festelektrolyt Wasserstoff, Erdgas oder Kohlegas Wasserstoff, Erdgas oder Kohlegas Sauerstoff der Luft Sauerstoff der Luft aus aus C stationäre Kraftwerke Optimierung des Wirkungsgrades Der Wirkungsgrad einer Maschine ist das Verhältnis aus erzeugter Energie und der im Brennstoff enthaltenen Energie. Im Fall einer Wasserstoff-Brennstoffzelle ist die Energie im verbrauchten Wasserstoff enthalten. Die erzeugte Energie ist die elektrische Energie. Der Wirkungsgrad einer Brennstoffzelle kann durch verschiedene Faktoren beeinflusst werden. 1. Die Gase müssen möglichst über die gesamte Oberfläche der MEE verteilt werden. 2. Elektrolyt und Elektroden müssen möglichst engen Kontakt miteinander haben. 3. Gase dürfen durch die Elektrolytschicht nicht durchgelassen werden. 4. Membran und Elektroden müssen Ladungsträger möglichst gut leiten. 5. Die Oberfläche des Katalysators muss groß gegen die Masse sein, also möglichst kleine Platinpartikel. 6. An der Sauerstoffseite muss das Wasser entfernt werden um den Sauerstoffzufluss nicht zu hindern Die Spannungs-Strom-Kurve einer Brennstoffzelle Abbildung 3 zeigt die Spannungs-Strom-Kurve einer Brennstoffzelle. Für Spannungsverluste zeigen sich verschiedene Effekte verantwortlich. Wie oben erwähnt ist die maximale Spannung einer Brennstoffzelle bei 1,23 V. Die Spannungsdifferenz zwischen der maximalen und der echten Spannung wird als Überspannung bezeichnet. Die Durchtritts-Überspannung entsteht durch steigenden Strom. Die Geschwindigkeit mit der die Elektronen vom Gas in die Katalysatoren gelangen beschränkt den Strom und ist somit Ursache für die Ladungsdurchtrittsüberspannung. 5
6 Bei hohem Strom wird die Überspannung durch die Diffusion der Gase bestimmt. Werden diese am Katalysator schneller verbraucht als sie durch die porösen Elektroden gelangen sinkt die Spannung, was sich auch an der abknickenden Spannungskurve erkennen lässt. Wie jedes elektrisch U D e Bauteil bringt eine Brennstoffzelle einen inneren Widerstand mit. Dies trifft auf die Protonenleiter wie die Elektronenleiter zu. Mit zunehmendem Strom sinkt die Spannung linear. Abbildung 3 Spannungs-Strom-Kurve einer Brennstoffzelle 4.2 Elektrolyse Zum Betrieb der Brennstoffzelle wird Wasserstoff benötigt, der mit Hilfe der Elektrolyse hergestellt wird. Die Elektrolyse ist ein Prozess, bei dem elektrischer Strom benutzt wird um chemische Änderungen in einer Substanz herbeizuführen. Es wird also elektrische Energie in chemische Energie umgewandelt. Taucht man zwei Elektroden in einen Elektrolyten und legt eine hinreichend große Gleichspannung an so fließt ein Strom. Innerhalb des Elektrolyten wird der Strom durch Ionen (im Gegensatz zu Elektronen in metallischen Leitern) übertragen. Somit ist das Vorhandensein von beweglichen Ionen Voraussetzung für die Elektrolyse. Positiv geladene Ionen wandern zur Kathode, nehmen dort Elektronen auf und werden somit neutralisiert, wohingegen negativ geladene Ionen zu Anode wandern und dort Elektronen abgeben. Die nun neutralen Atome oder Moleküle können an den Elektroden ausfallen, als Gas entweichen oder an weiteren Reaktionen teilnehmen. Beispiel: Löst man Kochsalz (NaCl) in Wasser, dissoziiert es in Na + und Cl - Ionen. Die negativ geladenen Cl - Ionen wandern zur positiv geladenen Anode und geben dort ein Elektron ab. Die Na + Ionen wandern zur negativ geladenen Kathode und nehmen dort ein Elektron auf. Es finden also folgende Reaktionen statt: 6
7 Anode: Kathode: Die einzelnen Chloratome verbinden sich zu Cl 2 und steigen als Gas an der Elektrode auf. Das Na hingegen bildet mit OH - Ionen NaOH. Die OH - Ionen stammen aus der immer in gewissen Maßen stattfindenden Autoprotolyse des Wassers: 0 Das übrig bleibende H + bildet H 2. Somit steigt an der Kathode Wasserstoff auf Elektrolyse von Wasser Reines Wasser kann mit Hilfe der konventionellen Elektrolyse nicht aufgespalten werden. Der Grund dafür ist, dass zwar ein Teil des Wassers dissoziiert vorliegt, also als OH - und H + Ionen, aber deren Konzentration so gering ist, sodass Wasser kaum leitfähig ist und somit keine Stromleitung stattfinden kann. Um dennoch Wasserstoff aus Wasser zu gewinnen, kann man verdünnte wässrige Säuren oder Laugen verwenden. Dass bei Verwendung dieser Elektrolyten nur Wasserstoff und Sauerstoff entstehen, liegt daran, dass die meisten Säuren und Laugen zwar Ionen bilden und damit Strom leiten, diese Ionen jedoch selbst chemisch inert sind. Sie reagieren also nicht an mit der Kathode oder Anode. Wichtig bei allen Verwahren der Elektrolyse von Wasser ist den entstehenden Sauerstoff und Wasserstoff räumlich voneinander zu trennen. Dazu wird ein sogenanntes Diaphragma verwendet, welches zwar die Ionen zur Stromleitung hindurchlässt, Sauerstoff und Wasserstoff aber nicht. Eine weitere Methode ist die Verwendung von Polymerelektrolytmembranen (PEM), wie sie auch in diesem Versuch verwendet wird. Abbildung 4 zeigt den Aufbau einer Membran- Elektroden-Einheit. Es finden folgende Reaktionen statt: Anode: Kathode:
8 Abbildung 4: Polymerelektrolytmembran-Elektrolyseur-Aufbau Kennlinie der Elektrolyse Wird die Elektrolyse gestartet und die Spannung langsam erhöht, misst man erst ab einer gewissen Spannung einen Strom. Diejenige Spannung ab der der Strom deutlich ansteigt nennt man Zersetzungsspannung. Sie beträgt theoretisch für Wasser 1,23V. Dieser Wert ergibt sich aus der elektrochemische Spannungsreihe. Abbildung 5: Spannungs-Strom-Kennlinie bei der Elektrolyse Im Experiment werden höhere Zersetzungsspannungen gemessen. Die Differenz zwischen tatsächlicher Zersetzungsspannung und theoretischer Zersetzungsspannung nennt man Über- 8
9 spannung. Sie kann verschiedene Ursachen haben, wie zum Beispiel Art und Konzentration der Ionen, Elektrodenmaterial oder ihre Oberflächenbeschaffenheit Wirkungsgrad Der Faraday-Wirkungsgrad η Faraday ist das Verhältnis zwischen der erzeugten Menge Wasserstoff und der theoretisch zu erwartenden Menge Wasserstoff. Letzteres lässt sich über das Faraday-Gesetz berechnen, welches sagt, dass, um eine Stoffmenge n eines Stoffes elektrolytisch abzuscheiden, man eine Ladung von benötigt. Dabei ist z die Ladungszahl des verwendeten Ions und F die Faraday Konstante. Der energetische Wirkungsgrad η ist das Verhältnis von gewonnener chemischer Energie zur aufgewendeten elektrischen Energie. Die chemische Energie entspricht dem Brennwert des erzeugten Wasserstoffs. 4.3 Solarzelle Die Solarzelle ist ein elektrisches Bauteil, welches aus Licht elektrischen Strom erzeugt. Der zugrunde liegende physikalische Effekt ist der photovoltaische Effekt. Dieser besagt, dass unter bestimmten Voraussetzungen durch die Absorption von Licht in einem Halbleiter eine Spannung aufgebaut wird. Eine Solarzelle besteht im Wesentlichen aus einem pn-übergang, das heißt aus einer p-dotierten und einer n-dotierten Halbleiterschicht. p- bzw. n-dotiert bedeutet, dass im Ausgangsmaterial Atome durch Atome mit weniger Valenzelektronen (p- Dotierung) oder mehr Valenzelektronen (n-dotierung) ersetzt werden. So werden Silizium- Halbleiter (Silizium ist IV-wertig) beispielsweise mit Bor-Atomen (III-wertig) und Phosphor- Atomen (V-wertig) dotiert. In diesem Fall dienen die Bor-Atome als Elektronen-Akzeptoren, das heißt sie nehmen ein Elektron auf, was zu einem Loch im Valenzband führt. Die Phosphor-Atome sind Elektron-Donatoren, sie geben ein Elektron in das Leitungsband ab pn-übergang Bringt man einen n-dotierten und einen p-dotierten Halbleiter in Kontakt, findet aufgrund der unterschiedlichen Konzentrationen eine Diffusion der Ladungsträger statt. Die überschüssigen Elektronen auf der n-dotierten Seite wandern in Richtung der p-dotierung und anders herum. Durch die zurückbleibenden Atomrümpfe bildet sich auf der n-dotierten Seite eine positive Raumladung und auf der p-dotierten Seite eine negative Raumladung aus. Der Bereich des so entstandenen elektrischen Feldes wird Raumladungszone genannt. Das Feld wirkt der weiteren Diffusion entgegen und es stellt sich ein thermodynamisches Gleichgewicht ein. 9
10 4.3.2 Die Solarzelle Wird die Solarzelle beleuchtet so werden durch Absorption von Licht Elektronen aus dem Valenzband in das Leitungsband gehoben und es entstehen Elektron-Loch-Paare. Diese diffundieren durch das Material bis sie die Raumladungszone erreichen. Dort findet aufgrund des elektrischen Feldes eine Ladungstrennung statt. Dadurch entsteht ein zusätzlicher Driftstrom (Photostrom I ph mit I ph > 0) von Elektronen in den Bereich der positiven Raumladung und von Löchern in den Bereich der negativen Raumladung. So werden der p-bereich positiv und der n-bereich negativ aufgeladen. Die daraus resultierende Spannung kann dann über Kontakte abgeführt werden (Abbildung 6 a)). Die Kennlinie (Abbildung 6 b)) einer Solarzelle entspricht im Wesentlichen der einer Diode, wobei der zusätzliche Photostrom I ph berücksichtigt wird. 1 Abbildung 6 a) pn-übergang unter Beleuchtung: Die photogenerierten Minoritätsladungsträger diffundieren zunächst zur Raumladungszone und werden dort durch das elektrische Feld getrennt. b) Strom-Spannungs- Charakteristik einer Solarzelle. Die Kennlinie ergibt sich aus der Summe von Diodenstrom I und Photostrom Iph (negatives Vorzeichen!) Für die Energiegewinnung ist derjenige Bereich von Interesse, in dem die Spannung positiv und der Strom negativ ist, also dem vierten Quadranten (Abbildung 7). Abbildung 7 Der für die Energieproduktion relevante Bereich der Kennlinie liegt im 4. Quadranten. Die maximale Leistung kann der Zelle bei einer Spannung Umpp (MPP = Maximum Power Point) entnommen werden. 10
11 In Abbildung 7 ist die Kennlinie einer Solarzelle gezeigt. Hier steht I sc für den Kurzschluss- zum Photostrom strom und U oc für Leerlaufspannung. Der Kurzschlussstrom ist proportional I ph der Solarzelle. Der Wirkungsgrad der Solarzelle gibt das Verhältnis von zugeführter Strahlungsenergie zur elektrischen Energie: 5 Versuchsdurchführung und Auswertung Spülen der Brennstoffzelle und Speichern des Wasserstoffes Abbildung 8 Aufbau zum Spülen der Brennstoffzelle Abbildung 9 Verschließen der Schläuche mit Verschlussstopfen zum Speichern der Gase Vor einigen Versuchsteilen, in denen die Brennstoffzelle verwendet wird, muss der Aufbau gespült werden und die erzeugten Gase gespeichert werden. Achten Sie darauf, dass der Was- 11
12 serspeicher bis zur 0ml Marke gefüllt ist und stellen Sie den Schalter der Verbrauchermessbox zunächst auf OFFEN. Der Solarstrom am Elektrolyseur sollte mindestens 150mA betragen. Spülen Sie 5min das System mit den erzeugten Gasen und stellen Sie anschließend den Schal- können. Spülen ter an der Verbrauchermessbox auf 3Ω. Nun sollten Sie einen Strom messen Sie wiederum für 3min (Schalter auf OFFEN). Unterbrechen Sie kurzzeitig die Stromversor- gung des Elektrolyseurs und schließen Sie die beiden kurzen Schläuche mit Verschlussstopfen an die Brennstoffzelle an. Stellen Sie die Stromversorgung wieder her und speichern Sie die erzeugten Gase bis auf der Wasserstoffseite die 50ml Marke erreicht ist. Stoppen Sie die Elektrolyse. Aufgaben: 1. Kennlinie Elektrolyseur Abbildung 10 Versuchsaufbau zum Messen der Kennlinie des Elektrolyseurs und dessen Wir- kungsgrads Messen Sie die Kennlinie des Elektrolyseurs. Bauen Sie dazu die Anordnung nach Abbildung 10 auf und füllen Sie den Wasserspeicher des Elektrolyseurs bis zur 0ml Markierung. Stellen Sie den Wahlschalter der Verbrauchermessbox auf Kurzschluss. Variieren Sie nun den Solarmodulstrom und messen die Spannung am Elektrolyseur (10 Messwerte). Zeichnen Sie die Strom-Spannungskennlinie und bestimmen Sie die Zerset- sicher, dass die zungsspannungg des Wassers. 2. Wirkungsgrad des Elektrolyseurs Bauen Sie die Anordnung nach Abbildung 10 auf. Stellen Sie Wassertanks bis zur 0ml Marke gefüllt sind. Verschließen Sie die Wasserstoff- Elektrolyse- seite des Tanks mit einem Verschlussstopfen. Stellen Sie einen strom von ca. 250mA bis 300mA ein. Messen Sie die Spannung und das ent- 12
13 standene Wasserstoffvolumen bei vorgegebener Zeit (180s). Führen Sie diese Messung dreimal durch. Berechnen Sie den Faraday-Wirkungsgrad und den Energiewirkungsgrad des Elektrolyseurs. Berechnen Sie ebenfalls die Avogadro-Konstanten aus Ihren Messungen. 3. Kennlinie der Brennstoffzelle Abbildung 11 Versuchsaufbau zur Messung der Kennlinie der Brennstoffzelle und des Wirkungsgrads Spülen Sie die Brennstoffzelle und speichern Sie 50ml Wasserstoff. Bauen Sie die Anordnung so um, dass sie Abbildung 11 entspricht. Messen Sie nun die Kennlinie der Brennstoffzelle, in dem Sie den Messwiderstand verän- und dern. Nach Beendigung der Messung entfernen Sie die Verschlussstopfen stellen Sie die Messbox auf OFFEN. Zeichnen Sie die U-I-Kennlinie der Brennstoffzelle. 4. Wirkungsgrad einer Brennstoffzelle Spülen Sie die Brennstoffzelle und speichern Sie den Wasserstoff. Wenn Sie 10ml Wasserstoff gespeichert haben, ist eine Nullmessung zur Bestimmung der Leckrate des Systems durchzuführen. Messen Sie dazu den Verlust an Wasser- OFFEN). stoff in 5min ohne Last an der Brennstoffzelle (Schalterstellung Füllen Sie den Wasserstoffspeicher erneut auf 50ml und unterbrechen Sie an- Sie das Voltme- schließend die Stromversorgung des Elektrolyseurs. Schließen ter an die Brennstoffzelle an (entsprechend Abbildung 11)und stellen Sie einen Widerstand von 3Ω ein. Messen Sie das Volumen an Wasserstoff, was die Brennstoffzellee in 180s verbraucht. Messen Sie zusätzlich den Strom und die Spannung. Wiederholen Sie die Messung dreimal. 13
14 Bestimmen sie le. 5. Reihen- und Parallelschaltung von Brennstoffzellen den Faraday- und den Energiewirkungsgrad der Brennstoffzel- Abbildung 12 Aufbau zur Messung der Kennlinie von zwei parallelgeschalteten Brennstoffzellen Abbildung 13 Aufbau zur Messung der Kennlinie von zwei in Reihe geschalteten Brennstoffzellen Spülen Sie die Brennstoffzellen und speichern Sie Wasserstoff. Messen Sie jeweils die Kennlinie der Brennstoffzelle in Parallel- und in Rei- 6. Zerlegbare Brennstoffzelle; Einfluss des Innenwiderstands; Katalysatorbele- gung; Gaszufuhr henschaltung. Zeichnen Sie die Kennlinie und interpretieren Sie die Ergebnisse. Spülen Sie die Brennstoffzelle und speichern Sie Wasserstoff vor jeder Mes- sung. 14
15 Nehmen Sie die Kennlinie der zerlegbaren Brennstoffzelle auf. Gehen Sie dazu wie oben beschrieben vor. Messen Sie außerdem die Kennlinie der Brennstoffzelle mit dem zusätzlichen Widerstand. Um den Einfluss der Gaszufuhr auf die Kennlinie der Brennstoffzelle zu untersuchen, nehmen Sie die Kennlinie bei Betrieb mit Luftsauerstoff einmal mit der Sauerstoffendplatte und einmal mit der Endplatte mit den Luftschlitzen auf. (Warten Sie vor Aufnahme der einzelnen Messpunkte ca. 2min.) Tauschen Sie in der Brennstoffzelle die Membran mit 0,3mg/m³ Katalysatorbelegung durch die Membran mit 0,1mg/m³ Katalysatorbelegung und messen Sie erneut die Kennlinie. (Bei allen Umbauten ist unbedingt die Aufbauanleitung zu beachten!) Zeichen Sie die Kennlinien in ein U-I-Diagramm und diskutieren Sie sie. 6 Fragen (zur Vorbereitung) Welche Probleme entstehen beim Spalten von destilliertem Wasser bei der konventionellen Elektrolyse und wie werden diese umgangen? Wodurch wird der Wirkungsgrad einer Brennstoffzelle beschränkt? Wieso unterliegt der Wirkungsgrad einer Brennstoffzelle nicht denselben Einschränkungen wie der einer Wärmekraftmaschine? Wie ist der Wirkungsgrad eines Systems aus Solarzelle, Elektrolyseur und Brennstoffzelle und welche Faktoren beschränken ihn? 15
Kennlinie der Brennstoffzelle
 E z1 Kennlinie der Material: Zerlegbare mit Membran,3 mg/cm Pt sowie Wasserstoff- und Sauerstoffendplatte montiert nach Aufbauanleitung Komponenten aus Schülerkasten Solar-Wasserstoff-Technologie: Solarmodul
E z1 Kennlinie der Material: Zerlegbare mit Membran,3 mg/cm Pt sowie Wasserstoff- und Sauerstoffendplatte montiert nach Aufbauanleitung Komponenten aus Schülerkasten Solar-Wasserstoff-Technologie: Solarmodul
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Elektrochemie 1 Abbildung 1: I. VERSUCHSZIEL
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 3 Wirkungsgrad der Brennstoffzelle Versuchszweck
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 3 Wirkungsgrad der Brennstoffzelle Versuchszweck
Die Wirkungsweise einer Brennstoffzelle. Ein Vortrag von Bernard Brickwedde
 Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
HappyEvening am Brennstoffzellen zur mobilen Energiebereitstellung
 HappyEvening am 15.10.2008 Brennstoffzellen zur mobilen Energiebereitstellung T. Pröll 15.10.2008 Inhalt Grundlagen Zelltypen und Anwendungen PEM-Brennstoffzelle (Prinzip) Direkt-Methanol-Brennstoffzelle
HappyEvening am 15.10.2008 Brennstoffzellen zur mobilen Energiebereitstellung T. Pröll 15.10.2008 Inhalt Grundlagen Zelltypen und Anwendungen PEM-Brennstoffzelle (Prinzip) Direkt-Methanol-Brennstoffzelle
Strom und Spannungsmessung, Addition von Widerständen, Kirchhoffsche Regeln, Halbleiter, p-n-übergang, Dioden, fotovoltaischer Effekt
 Versuch 27: Solarzellen Seite 1 Aufgaben: Vorkenntnisse: Lehrinhalt: Literatur: Messung von Kurzschlussstrom und Leerlaufspannung von Solarzellen, Messung der I-U-Kennlinien von Solarzellen, Bestimmung
Versuch 27: Solarzellen Seite 1 Aufgaben: Vorkenntnisse: Lehrinhalt: Literatur: Messung von Kurzschlussstrom und Leerlaufspannung von Solarzellen, Messung der I-U-Kennlinien von Solarzellen, Bestimmung
Inhalt. History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ. Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell.
 Brennstoffzellen Inhalt History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell o Stacks o Anwendung o Fazit History Erste BZ vor
Brennstoffzellen Inhalt History Prinzip der Brennstoffzelle Wasserstoff-Sauerstoff-BZ Polymer Elektrolyte Membrane Fuel Cell Direct Methanol Fuel Cell o Stacks o Anwendung o Fazit History Erste BZ vor
Brenstoffzelle (BRZ)
 Seite 1 Themengebiet: Thermodynamik 1 Literatur A. Macdonald, M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris, Berlin, 2007 A.J. Bard, L.R. Faulkner, Electrochemical Methods Fundamentals
Seite 1 Themengebiet: Thermodynamik 1 Literatur A. Macdonald, M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris, Berlin, 2007 A.J. Bard, L.R. Faulkner, Electrochemical Methods Fundamentals
Untersuchung der Abhängigkeit des Photostroms von der Entfernung zur Lichtquelle
 E1 S 3 Untersuchung der Abhängigkeit des Photostroms von der Entfernung zur Lichtquelle Name: Datum: Aufgaben: a) Miss die Höhe des Photostroms in Abhängigkeit von der Entfernung zur Lampe. b) Zeichne
E1 S 3 Untersuchung der Abhängigkeit des Photostroms von der Entfernung zur Lichtquelle Name: Datum: Aufgaben: a) Miss die Höhe des Photostroms in Abhängigkeit von der Entfernung zur Lampe. b) Zeichne
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL SEKUNDARSTUFE II Modul: Versuch: Elektrochemie 1 Abbildung 1:
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg PROTOKOLL SEKUNDARSTUFE II Modul: Versuch: Elektrochemie 1 Abbildung 1:
Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle
 Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Lehrer-/Dozentenblatt Erzeugung elektrischer Energie mit einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusätzliche Informationen Alle Brennstoffzellen bestehen prinzipiell aus zwei
Was ist Elektrochemie? Elektrochemie. Elektrochemie ist die Lehre von der Beziehung
 Was ist Elektrochemie? Elektrochemie Elektrochemie ist die Lehre von der Beziehung zwischen elektrischen und chemischen Prozessen. 131 Stromleitung in einem Metall Wir haben gelernt, dass die Stromleitung
Was ist Elektrochemie? Elektrochemie Elektrochemie ist die Lehre von der Beziehung zwischen elektrischen und chemischen Prozessen. 131 Stromleitung in einem Metall Wir haben gelernt, dass die Stromleitung
Kennlinie der Brennstoffzelle
 E z1 Kennlinie der Material: Zerlegbare mit Membran,3 mg/cm Pt sowie Wasserstoff- und Sauerstoffendplatte montiert nach Aufbauanleitung Komponenten aus Schülerkasten Solar-Wasserstoff-Technologie: Solarmodul
E z1 Kennlinie der Material: Zerlegbare mit Membran,3 mg/cm Pt sowie Wasserstoff- und Sauerstoffendplatte montiert nach Aufbauanleitung Komponenten aus Schülerkasten Solar-Wasserstoff-Technologie: Solarmodul
Brennstoffzelle. Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes. Schüler-Skript und Versuchsanleitung
 Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes Bearbeitet von Markus Beckert, Sheila Sabock Stand 12.09.2013 Inhaltsverzeichnis 1 Einführung... 3 1.1 Vorbereitung, Vorwissen, Vorüberlegungen...
Versuch im Physikalischen Praktikum des Mathematik/Informatik-Gebäudes Bearbeitet von Markus Beckert, Sheila Sabock Stand 12.09.2013 Inhaltsverzeichnis 1 Einführung... 3 1.1 Vorbereitung, Vorwissen, Vorüberlegungen...
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 1 Kennlinie des Elektrolyseurs Versuchszweck Beim
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 1 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 1 Kennlinie des Elektrolyseurs Versuchszweck Beim
Physikalisches Anfängerpraktikum Teil 2 Elektrizitätslehre. Protokollant: Versuch 27 Solarzellen
 Physikalisches Anfängerpraktikum Teil 2 Elektrizitätslehre Protokoll Versuch 27 Solarzellen Harald Meixner Sven Köppel Matr.-Nr. 3794465 Matr.-Nr. 3793686 Physik Bachelor 2. Semester Physik Bachelor 2.
Physikalisches Anfängerpraktikum Teil 2 Elektrizitätslehre Protokoll Versuch 27 Solarzellen Harald Meixner Sven Köppel Matr.-Nr. 3794465 Matr.-Nr. 3793686 Physik Bachelor 2. Semester Physik Bachelor 2.
GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN
 10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
Robert-Bosch-Gymnasium
 Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 2 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 2 Kennlinien der Brennstoffzelle Versuchszweck
Robert-Bosch-Gymnasium NWT Klassenstufe 10 Versuch 2 Regenerative Energien: Brennstoffzelle Albert Pfänder, 22.4.2014 Brennstoffzellen-Praktikum, Versuch 2 Kennlinien der Brennstoffzelle Versuchszweck
Kennlinie der Methanol- Brennstoffzelle
 E m1 Kennlinie der Methanol- Brennstoffzelle Material: Methanol-Brennstoffzelle Flasche mit 1M Methanol-Lösung Spritztülle Verbraucher-Messbox 4 Kabel Verschlussstopfen Tank Zusätzliche Komponenten: Methanol
E m1 Kennlinie der Methanol- Brennstoffzelle Material: Methanol-Brennstoffzelle Flasche mit 1M Methanol-Lösung Spritztülle Verbraucher-Messbox 4 Kabel Verschlussstopfen Tank Zusätzliche Komponenten: Methanol
E5: Faraday-Konstante
 E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
E5: Faraday-Konstante Theoretische Grundlagen: Elektrischer Strom ist ein Fluss von elektrischer Ladung; in Metallen sind Elektronen die Ladungsträger, in Elektrolyten übernehmen Ionen diese Aufgabe. Befinden
diebrennstoffzelle.de
 PEM-Brennstoffzelle PEM-FC? Proton Exchange Membrane Fuel Cell Polymermembran (Methanol)* (Methan)* Temperatur -8 C bis 25kW Wirkungsgrad 6% (H2) 4% (CH4) Anwendungen Stromversorgung Pkw/Bus Hausversorgung
PEM-Brennstoffzelle PEM-FC? Proton Exchange Membrane Fuel Cell Polymermembran (Methanol)* (Methan)* Temperatur -8 C bis 25kW Wirkungsgrad 6% (H2) 4% (CH4) Anwendungen Stromversorgung Pkw/Bus Hausversorgung
Wasserstoff als Energieträger Gliederung:
 Wasserstoff als Energieträger Gliederung: Wasserstoff: Energie speichern und verteilen Die Brennstoffzelle Wasserstoff aus der Ptm6 Alge Wasserstoff als Energiespeicher Der umweltfreundliche Akku: Um Wasserstoff
Wasserstoff als Energieträger Gliederung: Wasserstoff: Energie speichern und verteilen Die Brennstoffzelle Wasserstoff aus der Ptm6 Alge Wasserstoff als Energiespeicher Der umweltfreundliche Akku: Um Wasserstoff
Die Silizium - Solarzelle
 Die Silizium - Solarzelle 1. Prinzip einer Solarzelle Die einer Solarzelle besteht darin, Lichtenergie in elektrische Energie umzuwandeln. Die entscheidende Rolle bei diesem Vorgang spielen Elektronen
Die Silizium - Solarzelle 1. Prinzip einer Solarzelle Die einer Solarzelle besteht darin, Lichtenergie in elektrische Energie umzuwandeln. Die entscheidende Rolle bei diesem Vorgang spielen Elektronen
Die elektrische Energie wird durch Ionen transportiert. Ionen sind elektrisch geladene Atome bzw. Elektrolyt
 Galvanische Elemente Galvanische (Galvani ital.physiker) Elemente wandeln chemische in elektrische um. Sie bestehen aus zwei Elektroden (Anode, Kathode) und einer elektrisch leitenden Flüssigkeit, dem
Galvanische Elemente Galvanische (Galvani ital.physiker) Elemente wandeln chemische in elektrische um. Sie bestehen aus zwei Elektroden (Anode, Kathode) und einer elektrisch leitenden Flüssigkeit, dem
Physikalisches Anfaengerpraktikum. Brennstoffzelle
 Physikalisches Anfaengerpraktikum Brennstoffzelle Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 25. Februar 2005 I. Versuchsaufbau und -beschreibung Die Versuchsapparatur bestand
Physikalisches Anfaengerpraktikum Brennstoffzelle Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 25. Februar 2005 I. Versuchsaufbau und -beschreibung Die Versuchsapparatur bestand
Experimentiertag. Datum: Name: Klasse: Schule:
 Experimentiertag Datum: Name: Klasse: Schule: E1 V 1 Generator, Propeller, Solarmodul Wovon hängt die Spannung ab? 1.) Spannung aus dem Generator: (Taucht in der Spannungsanzeige kein Minuszeichen auf,
Experimentiertag Datum: Name: Klasse: Schule: E1 V 1 Generator, Propeller, Solarmodul Wovon hängt die Spannung ab? 1.) Spannung aus dem Generator: (Taucht in der Spannungsanzeige kein Minuszeichen auf,
Physik 4 Praktikum Auswertung PVM
 Physik 4 Praktikum Auswertung PVM Von J.W, I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Solarzelle......... 2 2.2. PV-Modul......... 2 2.3. Schaltzeichen........ 2 2.4. Zu ermittelnde
Physik 4 Praktikum Auswertung PVM Von J.W, I.G. 2014 Seite 1. Kurzfassung......... 2 2. Theorie.......... 2 2.1. Solarzelle......... 2 2.2. PV-Modul......... 2 2.3. Schaltzeichen........ 2 2.4. Zu ermittelnde
Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle. Inhaltsfeld: Elektrochemie
 Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle Inhaltsfeld: Elektrochemie Inhaltliche Schwerpunkte: Mobile Energiequellen Elektrochemische Gewinnung von Stoffen Zeitbedarf: ca. 5 Std. à 45
Thema/Kontext: Von der Wasserelektrolyse zur Brennstoffzelle Inhaltsfeld: Elektrochemie Inhaltliche Schwerpunkte: Mobile Energiequellen Elektrochemische Gewinnung von Stoffen Zeitbedarf: ca. 5 Std. à 45
Faradayscher und energetischer Wirkungsgrad einer PEM Brennstoffzelle
 Faradayscher und energetischer Wirkungsgrad einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformation Zusatzinformationen Der Wirkungsgrad der Brennstoffzelle ist ein Indikator für die Effizienz
Faradayscher und energetischer Wirkungsgrad einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformation Zusatzinformationen Der Wirkungsgrad der Brennstoffzelle ist ein Indikator für die Effizienz
Google-Ergebnis für
 Solarzellen Friedrich-Schiller-Realschule Böblingen Basiswissen Elektronik - Wissen Schaltzeichen einer Solarzelle Geschichte: Wann wurde die erste Solarzelle entwickelt? Der photovoltaische Effekt wurde
Solarzellen Friedrich-Schiller-Realschule Böblingen Basiswissen Elektronik - Wissen Schaltzeichen einer Solarzelle Geschichte: Wann wurde die erste Solarzelle entwickelt? Der photovoltaische Effekt wurde
Grundlagen: Galvanische Zellen:
 E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
Die alkalische Brennstoffzelle (AFC)
 Die alkalische Brennstoffzelle (AFC) von Mathis Fomferra Fachoberschule Winsen/Luhe Mai 2010 Index Vorwort Wieso die Brennstoffzelle Die Geschichte der Brennstoffzelle Die alkalische Brennstoffzelle Quellenangaben
Die alkalische Brennstoffzelle (AFC) von Mathis Fomferra Fachoberschule Winsen/Luhe Mai 2010 Index Vorwort Wieso die Brennstoffzelle Die Geschichte der Brennstoffzelle Die alkalische Brennstoffzelle Quellenangaben
JUFOTech. wko.at/tirol/jufotech DATENBLATT. Jugend forscht in der Technik. Titel der Projektarbeit: Fachgebiet:
 Datenblatt (dient als Titelblatt für die Projektarbeit) Seite 1/2 JUFOTech Jugend forscht in der Technik wko.at/tirol/jufotech DATENBLATT Wir nehmen am Wettbewerb Jugend forscht in der Technik Auf den
Datenblatt (dient als Titelblatt für die Projektarbeit) Seite 1/2 JUFOTech Jugend forscht in der Technik wko.at/tirol/jufotech DATENBLATT Wir nehmen am Wettbewerb Jugend forscht in der Technik Auf den
Verfahrenstechnisches Tutorium Prof. Dr.-Ing. M. J. Hampe
 Verfahrenstechnisches Tutorium Prof. Dr.-Ing. M. J. Hampe Wintersemester 2012/13 4. Versuch: Brennstoffzelle Dipl.-Ing. Sebastian Lang Learning outcome Nachdem Sie sich mit diesem Versuch auseinandergesetzt
Verfahrenstechnisches Tutorium Prof. Dr.-Ing. M. J. Hampe Wintersemester 2012/13 4. Versuch: Brennstoffzelle Dipl.-Ing. Sebastian Lang Learning outcome Nachdem Sie sich mit diesem Versuch auseinandergesetzt
5. Photoelektrochemische Solarzellen Beispiel: n-halbleiter als Elektrode. Verbiegung des elektrischen Potentials im Halbleiter hin zur Oberfläche
 5. Photoelektrochemische Solarzellen Beispiel: n-halbleiter als Elektrode Ausbildung einer Raumladungszone und einer Bandverbiegung: Verbiegung des elektrischen Potentials im Halbleiter hin zur Oberfläche
5. Photoelektrochemische Solarzellen Beispiel: n-halbleiter als Elektrode Ausbildung einer Raumladungszone und einer Bandverbiegung: Verbiegung des elektrischen Potentials im Halbleiter hin zur Oberfläche
Strom-Spannungs-Kennlinie einer PEM Brennstoffzelle
 Lehrer-/Dozentenblatt Strom-Spannungs-Kennlinie einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusatzinformationen Eine PEM Brennstoffzelle besitzt keine lineare Leistungskurve, sondern
Lehrer-/Dozentenblatt Strom-Spannungs-Kennlinie einer PEM Brennstoffzelle Aufgabe und Material Lehrerinformationen Zusatzinformationen Eine PEM Brennstoffzelle besitzt keine lineare Leistungskurve, sondern
Vorlesung 3: Elektrodynamik
 Vorlesung 3: Elektrodynamik, georg.steinbrueck@desy.de Folien/Material zur Vorlesung auf: www.desy.de/~steinbru/physikzahnmed georg.steinbrueck@desy.de 1 WS 2015/16 Der elektrische Strom Elektrodynamik:
Vorlesung 3: Elektrodynamik, georg.steinbrueck@desy.de Folien/Material zur Vorlesung auf: www.desy.de/~steinbru/physikzahnmed georg.steinbrueck@desy.de 1 WS 2015/16 Der elektrische Strom Elektrodynamik:
Physik für die Sekundarstufe II. Wasserstoff. Energie für morgen. Averil Macdonald. heliocentris
 Physik für die Sekundarstufe II Wasserstoff Energie für morgen Averil Macdonald heliocentris Inhalt Teil 1 Vorbereitete experimentelle Lektionen mit Lehrerinformationen zur Vermittlung von Rahmenplaninhalten
Physik für die Sekundarstufe II Wasserstoff Energie für morgen Averil Macdonald heliocentris Inhalt Teil 1 Vorbereitete experimentelle Lektionen mit Lehrerinformationen zur Vermittlung von Rahmenplaninhalten
Halbleiter. Das Herz unserer multimedialen Welt. Bastian Inselmann - LK Physik
 Halbleiter Das Herz unserer multimedialen Welt Inhalt Bisherig Bekanntes Das Bändermodell Halbleiter und ihre Eigenschaften Dotierung Anwendungsbeispiel: Funktion der Diode Bisher Bekanntes: Leiter Isolatoren
Halbleiter Das Herz unserer multimedialen Welt Inhalt Bisherig Bekanntes Das Bändermodell Halbleiter und ihre Eigenschaften Dotierung Anwendungsbeispiel: Funktion der Diode Bisher Bekanntes: Leiter Isolatoren
Bedienungsanleitung. F109 Fuel Cell Stack 5. F110 Fuel Cell Stack 10
 Bedienungsanleitung F109 Fuel Cell Stack 5 F110 Fuel Cell Stack 10 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com
Bedienungsanleitung F109 Fuel Cell Stack 5 F110 Fuel Cell Stack 10 H-TEC EDUCATION GmbH Maria-Goeppert-Str. 9a 23562 Lübeck Tel.: +49 (0) 451-3 99 41-0 Fax: +49 (0) 451-3 99 41-798 E-mail: info@h-tec-education.com
Brennstoffzellenantriebe für US Militär Hybridauto
 Brennstoffzellenantriebe für US Militär Hybridauto PKW mit antrieb wurden von führenden Fahrzeugherstellern bereits in den 80iger Jahren entwickelt. Die anfänglichen Schwierigkeiten hinsichtlich der Tankgröße,
Brennstoffzellenantriebe für US Militär Hybridauto PKW mit antrieb wurden von führenden Fahrzeugherstellern bereits in den 80iger Jahren entwickelt. Die anfänglichen Schwierigkeiten hinsichtlich der Tankgröße,
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.de 2 von 18 6. Wir bauen eine Zitronenbatterie (Kl. 9/10) Chemische
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.de 2 von 18 6. Wir bauen eine Zitronenbatterie (Kl. 9/10) Chemische
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde. Sommersemester 2007
 Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #35 am 28.06.2007 Vladimir Dyakonov Leitungsmechanismen Ladungstransport in Festkörpern Ladungsträger
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #35 am 28.06.2007 Vladimir Dyakonov Leitungsmechanismen Ladungstransport in Festkörpern Ladungsträger
Power, der die Puste nie ausgeht!
 Fuel Cells Die Brennstoffzelle im Westerwald-Treff Power, der die Puste nie ausgeht! Die Brennstoffzelle im Westerwald-Treff Die Projektpartner Das Brennstoffzellen-Projekt im Hotelpark Westerwald-Treff
Fuel Cells Die Brennstoffzelle im Westerwald-Treff Power, der die Puste nie ausgeht! Die Brennstoffzelle im Westerwald-Treff Die Projektpartner Das Brennstoffzellen-Projekt im Hotelpark Westerwald-Treff
18. Vorlesung III. Elektrizität und Magnetismus
 18. Vorlesung III. Elektrizität und Magnetismus 17. Elektrostatik Zusammenfassung Nachtrag zur Influenz: Faraday-Käfig 18. Elektrischer Strom (in Festkörpern, Flüssigkeiten und Gasen; elektrische Stromkreise)
18. Vorlesung III. Elektrizität und Magnetismus 17. Elektrostatik Zusammenfassung Nachtrag zur Influenz: Faraday-Käfig 18. Elektrischer Strom (in Festkörpern, Flüssigkeiten und Gasen; elektrische Stromkreise)
Seminar zum Quantitativen Anorganischen Praktikum WS 2011/12
 Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Seminar zum Quantitativen Anorganischen Praktikum WS 211/12 Teil des Moduls MN-C-AlC Dr. Matthias Brühmann Dr. Christian Rustige Inhalt Montag, 9.1.212, 8-1 Uhr, HS III Allgemeine Einführung in die Quantitative
Chlor-Alkali-Elektrolyse
 Chlor-Alkali-Elektrolyse 1. Allgemeine Erklärung der Elektrolyse 2. Verfahren 2.1 Diaphragmaverfahren 2.2 Membranverfahren 2.3 Amalgamverfahren 3.Vorteile und Nachteile der Verfahren 4. Überspannung 1.
Chlor-Alkali-Elektrolyse 1. Allgemeine Erklärung der Elektrolyse 2. Verfahren 2.1 Diaphragmaverfahren 2.2 Membranverfahren 2.3 Amalgamverfahren 3.Vorteile und Nachteile der Verfahren 4. Überspannung 1.
Elektrizität. = C J m. Das Coulomb Potential φ ist dabei:
 Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
1. Strom-Spannungs-Kennlinie, Leistungskurve und Wirkungsgrad des Solarmoduls
 1. Strom-Spannungs-Kennlinie, Leistungskurve und Wirkungsgrad des Solarmoduls Hintergrund: Gegeben ist ein Datenblatt eines Solarpanels. Der Schüler soll messtechnisch die Daten eines kleinen Solarmoduls
1. Strom-Spannungs-Kennlinie, Leistungskurve und Wirkungsgrad des Solarmoduls Hintergrund: Gegeben ist ein Datenblatt eines Solarpanels. Der Schüler soll messtechnisch die Daten eines kleinen Solarmoduls
1. Geschichte Im Jahr 1838 fand der Professor Christian Friedrich Schönbein (1799 bis 1868) von der Universität Basel experimentell heraus, dass
 Die Brennstoffzelle 1. Geschichte Im Jahr 1838 fand der Professor Christian Friedrich Schönbein (1799 bis 1868) von der Universität Basel experimentell heraus, dass Elektrizität freigesetzt werden kann,
Die Brennstoffzelle 1. Geschichte Im Jahr 1838 fand der Professor Christian Friedrich Schönbein (1799 bis 1868) von der Universität Basel experimentell heraus, dass Elektrizität freigesetzt werden kann,
Dotierung. = gezieltes Verunreinigen des Si-Kristalls mit bestimmten Fremdatomen. n-dotierung Einbau. von Atomen mit 3 Valenzelektronen
 Halbleiter Dotierung = gezieltes Verunreinigen des Si-Kristalls mit bestimmten Fremdatomen. n-dotierung Einbau von Atomen mit 5 Valenzelektronen = Donatoren Elektronengeber (P, Sb, As) p-dotierung Einbau
Halbleiter Dotierung = gezieltes Verunreinigen des Si-Kristalls mit bestimmten Fremdatomen. n-dotierung Einbau von Atomen mit 5 Valenzelektronen = Donatoren Elektronengeber (P, Sb, As) p-dotierung Einbau
E 3 Brennstoffzelle. 1 Aufgabenstellung
 E 3 Brennstoffzelle 1 Aufgabenstellung 1.1 Ermitteln Sie den Wirkungsgrad eines Elektrolyseurs. 1. Nehmen Sie die Strom-Spannungs-Kennlinie eines Brennstoffzellensystems auf und erläutern Sie den erhaltenen
E 3 Brennstoffzelle 1 Aufgabenstellung 1.1 Ermitteln Sie den Wirkungsgrad eines Elektrolyseurs. 1. Nehmen Sie die Strom-Spannungs-Kennlinie eines Brennstoffzellensystems auf und erläutern Sie den erhaltenen
Auswertung. D07: Photoeffekt
 Auswertung zum Versuch D07: Photoeffekt Alexander Fufaev Partner: Jule Heier Gruppe 434 1 Einleitung In diesem Versuch geht es darum, den Photoeffekt auf verschiedene Weisen zu untersuchen. In Versuchsteil
Auswertung zum Versuch D07: Photoeffekt Alexander Fufaev Partner: Jule Heier Gruppe 434 1 Einleitung In diesem Versuch geht es darum, den Photoeffekt auf verschiedene Weisen zu untersuchen. In Versuchsteil
2 Elektrische Ladung, Strom, Spannung
 2 Elektrische Ladung, Strom, Spannung In diesem Kapitel lernen Sie, ein Grundverständnis der Elektrizität zur Beschäftigung mit Elektronik, welche physikalischen Grundgrößen in der Elektronik verwendet
2 Elektrische Ladung, Strom, Spannung In diesem Kapitel lernen Sie, ein Grundverständnis der Elektrizität zur Beschäftigung mit Elektronik, welche physikalischen Grundgrößen in der Elektronik verwendet
4. Dioden Der pn-übergang
 4.1. Der pn-übergang Die Diode ist ein Halbleiterbauelement mit zwei Anschlüssen: Eine Diode besteht aus einem Halbleiterkristall, der auf der einen Seite p- und auf der anderen Seite n-dotiert ist. Die
4.1. Der pn-übergang Die Diode ist ein Halbleiterbauelement mit zwei Anschlüssen: Eine Diode besteht aus einem Halbleiterkristall, der auf der einen Seite p- und auf der anderen Seite n-dotiert ist. Die
Aufgaben zur Elektrizitätslehre
 Aufgaben zur Elektrizitätslehre Elektrischer Strom, elektrische Ladung 1. In einem Metalldraht bei Zimmertemperatur übernehmen folgende Ladungsträger den Stromtransport (A) nur negative Ionen (B) negative
Aufgaben zur Elektrizitätslehre Elektrischer Strom, elektrische Ladung 1. In einem Metalldraht bei Zimmertemperatur übernehmen folgende Ladungsträger den Stromtransport (A) nur negative Ionen (B) negative
ACHTUNG! Nur zum Gebrauch für Kinder über
 P ROFI FUEL CELL KIT BEDIENUNGSANLEITUNG D ACHTUNG! Nur zum Gebrauch für Kinder über 10 Jahren. Benutzung nur unter der genauen Aufsicht von Erwachsenen, die sich mit den im Experimentierkasten beschriebenen
P ROFI FUEL CELL KIT BEDIENUNGSANLEITUNG D ACHTUNG! Nur zum Gebrauch für Kinder über 10 Jahren. Benutzung nur unter der genauen Aufsicht von Erwachsenen, die sich mit den im Experimentierkasten beschriebenen
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 10. Vorlesung, 27. 6. 2013 Halbleiter, Halbleiter-Bauelemente Diode, Solarzelle,
Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 10. Vorlesung, 27. 6. 2013 Halbleiter, Halbleiter-Bauelemente Diode, Solarzelle,
Photovoltaik-Module mm Länge eines Moduls 4.1A Strom bei max. Leistung
 Photovoltaik-Module Photovoltaik-Module wandeln Sonnenenergie in elektrische Energie um. Dazu nutzen Solarzellen den photoelektrischen Effekt, der mittels Absorption von Sonnenlicht Elektronen in Bewegung
Photovoltaik-Module Photovoltaik-Module wandeln Sonnenenergie in elektrische Energie um. Dazu nutzen Solarzellen den photoelektrischen Effekt, der mittels Absorption von Sonnenlicht Elektronen in Bewegung
6.2.6 Ohmsches Gesetz ******
 6..6 ****** Motivation Das Ohmsche Gesetz wird mithilfe von verschiedenen Anordnungen von leitenden Drähten untersucht. Experiment 6 7 8 9 0 Abbildung : Versuchsaufbau. Die Ziffern bezeichnen die zehn
6..6 ****** Motivation Das Ohmsche Gesetz wird mithilfe von verschiedenen Anordnungen von leitenden Drähten untersucht. Experiment 6 7 8 9 0 Abbildung : Versuchsaufbau. Die Ziffern bezeichnen die zehn
Brennstoffzellen. Schüler: Julia Schürkamp Fach: Technik Thema: Brennstoffzellen Lehrer: Herr Menne
 Brennstoffzellen Schüler: Julia Schürkamp Fach: Technik Thema: Brennstoffzellen Lehrer: Herr Menne Inhaltsangabe Was ist sind Brennstoffzellen? 1 Wie funktionieren Brennstoffzellen? 2-3 Anwendung der verschiedenen
Brennstoffzellen Schüler: Julia Schürkamp Fach: Technik Thema: Brennstoffzellen Lehrer: Herr Menne Inhaltsangabe Was ist sind Brennstoffzellen? 1 Wie funktionieren Brennstoffzellen? 2-3 Anwendung der verschiedenen
ELEKTRISCHE SPANNUNGSQUELLEN
 Physikalisches Grundpraktikum I Versuch: (Versuch durchgeführt am 17.10.2000) ELEKTRISCHE SPANNUNGSQUELLEN Denk Adelheid 9955832 Ernst Dana Eva 9955579 Linz, am 22.10.2000 1 I. PHYSIKALISCHE GRUNDLAGEN
Physikalisches Grundpraktikum I Versuch: (Versuch durchgeführt am 17.10.2000) ELEKTRISCHE SPANNUNGSQUELLEN Denk Adelheid 9955832 Ernst Dana Eva 9955579 Linz, am 22.10.2000 1 I. PHYSIKALISCHE GRUNDLAGEN
Lösungen, Salze, Ionen und Elektrolyte
 Lösungen, Salze, Ionen und Elektrolyte Lösungen Eine Lösung ist in der Chemie ein homogenes Gemisch, das aus zwei oder mehr chemisch reinen Stoffen besteht. Sie enthält einen oder mehrere gelöste Stoffe
Lösungen, Salze, Ionen und Elektrolyte Lösungen Eine Lösung ist in der Chemie ein homogenes Gemisch, das aus zwei oder mehr chemisch reinen Stoffen besteht. Sie enthält einen oder mehrere gelöste Stoffe
4.2 Halbleiter-Dioden und -Solarzellen
 4.2 Halbleiter-Dioden und -Solarzellen Vorausgesetzt werden Kenntnisse über: Grundbegriffe der Halbleiterphysik, pn-übergang, Raumladungszone, Sperrschichtkapazität, Gleichrichterkennlinie, Aufbau und
4.2 Halbleiter-Dioden und -Solarzellen Vorausgesetzt werden Kenntnisse über: Grundbegriffe der Halbleiterphysik, pn-übergang, Raumladungszone, Sperrschichtkapazität, Gleichrichterkennlinie, Aufbau und
1 Schaltungen von Hochleistungs-LEDs
 1 Schaltungen von Hochleistungs-LEDs 1.1 Zwei identische Reihenschaltungen, die parallel an U Gleich geschaltet sind. U R 2 = U gleich 2 = 12 V 6,6 V = 5,4 V R 2 = U R 2 = 5,4 V = 18 Ω ( = R 1) I 2 300
1 Schaltungen von Hochleistungs-LEDs 1.1 Zwei identische Reihenschaltungen, die parallel an U Gleich geschaltet sind. U R 2 = U gleich 2 = 12 V 6,6 V = 5,4 V R 2 = U R 2 = 5,4 V = 18 Ω ( = R 1) I 2 300
Was ist wichtig für die siebte Kursarbeit?
 Was ist wichtig für die siebte Kursarbeit? Redoxreaktion: Oxidation (Elektronen-Donator) und Reduktion (Elektronen-Akzeptor) korrespondierende Redoxpaare. Prinzip der Lösungstension, Betrachtung der Halbzellenreaktion
Was ist wichtig für die siebte Kursarbeit? Redoxreaktion: Oxidation (Elektronen-Donator) und Reduktion (Elektronen-Akzeptor) korrespondierende Redoxpaare. Prinzip der Lösungstension, Betrachtung der Halbzellenreaktion
Basics of Electrical Power Generation Photovoltaik
 Basics of Electrical Power Generation Photovoltaik 1/ 23 GE Global Research Freisinger Landstrasse 50 85748 Garching kontakt@reg-energien.de Inhalte 1. Prinzip 2. Technik 3. Verschattung 2/ 23 1 Prinzip
Basics of Electrical Power Generation Photovoltaik 1/ 23 GE Global Research Freisinger Landstrasse 50 85748 Garching kontakt@reg-energien.de Inhalte 1. Prinzip 2. Technik 3. Verschattung 2/ 23 1 Prinzip
Strom-Spannungs-Kennlinie und Leistung einer PEM Brennstoffzelle
 Strom-Spannungs-Kennlinie und Leistung ENT Schlüsselworte Brennstoffzelle, Protonen-Austausch-Membran, Kennlinie, elektrische Leistung, Innenwiderstand, Wasserstoff Prinzip In reagieren Wasserstoff und
Strom-Spannungs-Kennlinie und Leistung ENT Schlüsselworte Brennstoffzelle, Protonen-Austausch-Membran, Kennlinie, elektrische Leistung, Innenwiderstand, Wasserstoff Prinzip In reagieren Wasserstoff und
Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse
 Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Spannungsquellen. Grundpraktikum I. Mittendorfer Stephan Matr. Nr Übungsdatum: Abgabetermin:
 Grundpraktikum I Spannungsquellen 1/5 Übungsdatum: 7.11. Abgabetermin: 3.1. Grundpraktikum I Spannungsquellen stephan@fundus.org Mittendorfer Stephan Matr. Nr. 9956335 Grundpraktikum I Spannungsquellen
Grundpraktikum I Spannungsquellen 1/5 Übungsdatum: 7.11. Abgabetermin: 3.1. Grundpraktikum I Spannungsquellen stephan@fundus.org Mittendorfer Stephan Matr. Nr. 9956335 Grundpraktikum I Spannungsquellen
Das Brennstoffzellen-Radio
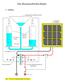 Das Brennstoffzellen-Radio 1. Aufbau Auffangbehälter (Haushaltstrichter) Solarpaneel (KOSMOS) 10 10 20 20 30 30 40 50 destilliertes Wasser Gastanks (Einwegspritzen) 40 50 60 70 80 60 Plexiglas 90 ml 100
Das Brennstoffzellen-Radio 1. Aufbau Auffangbehälter (Haushaltstrichter) Solarpaneel (KOSMOS) 10 10 20 20 30 30 40 50 destilliertes Wasser Gastanks (Einwegspritzen) 40 50 60 70 80 60 Plexiglas 90 ml 100
Galvanoplastik. Elektrochemie B. Lukas Woolley, Rafael Adamek, Peter Krack. 24 Februar ETH Zürich
 Elektrochemie B Lukas Woolley Rafael Adamek Peter Krack ETH Zürich 24 Februar 2017 Programm 1 2 3 4 Garfield Elektrolysezelle + - e e Anode Kathode e Cu CuSO 4 Cu 2+ Cu 2+ e Programm 1 2 3 4 Zelltypen
Elektrochemie B Lukas Woolley Rafael Adamek Peter Krack ETH Zürich 24 Februar 2017 Programm 1 2 3 4 Garfield Elektrolysezelle + - e e Anode Kathode e Cu CuSO 4 Cu 2+ Cu 2+ e Programm 1 2 3 4 Zelltypen
EinFaCh 1. Studienvorbereitung Chemie. Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie.
 Studienvorbereitung Chemie EinFaCh 1 Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie www.tu-freiberg.de http://tu-freiberg.de/fakultaet2/einfach Was ist eine
Studienvorbereitung Chemie EinFaCh 1 Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie www.tu-freiberg.de http://tu-freiberg.de/fakultaet2/einfach Was ist eine
Photovoltaik-Module mm Länge eines Moduls 4.1A Strom bei max. Leistung
 Photovoltaik-Module Photovoltaik-Module wandeln Sonnenenergie in elektrische Energie um. Dazu nutzen Solarzellen den photoelektrischen Effekt, der mittels Absorption von Sonnenlicht Elektronen in Bewegung
Photovoltaik-Module Photovoltaik-Module wandeln Sonnenenergie in elektrische Energie um. Dazu nutzen Solarzellen den photoelektrischen Effekt, der mittels Absorption von Sonnenlicht Elektronen in Bewegung
LEISTUNGSTEST ELEKTROLYSE-STACK
 LEISTUNGSTEST ELEKTROLYSE-STACK Energetischer und Faradayscher Wirkungsgrad Plus, (Thorsten Müller) Bandit, Rubberduck, (Saša Smolčić) 20140225 Dieses Material steht unter der Creative-Commons-Lizenz Namensnennung
LEISTUNGSTEST ELEKTROLYSE-STACK Energetischer und Faradayscher Wirkungsgrad Plus, (Thorsten Müller) Bandit, Rubberduck, (Saša Smolčić) 20140225 Dieses Material steht unter der Creative-Commons-Lizenz Namensnennung
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Elektronen und Löcher 3 2 3 2L 2mkT Eg nn e p exp 2 2 kt n e 3 3/2 2L 2mkT Eg np exp 2 2 2kT Die FermiEnergie liegt in der
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Elektronen und Löcher 3 2 3 2L 2mkT Eg nn e p exp 2 2 kt n e 3 3/2 2L 2mkT Eg np exp 2 2 2kT Die FermiEnergie liegt in der
Schülerexperimente mit Solarzellen
 Elektrodynamik: D. 7. 8 Schülerexperimente mit Solarzellen Die Schüler werden in 4 bzw. 8 Kleingruppen (ca. 3 4 Schüler pro Gruppe) eingeteilt. Jede Kleingruppe wird einem der Experimente zugeteilt, die
Elektrodynamik: D. 7. 8 Schülerexperimente mit Solarzellen Die Schüler werden in 4 bzw. 8 Kleingruppen (ca. 3 4 Schüler pro Gruppe) eingeteilt. Jede Kleingruppe wird einem der Experimente zugeteilt, die
Dipl.-Ing. Alicja Schlange
 Funktionalisierung neuartiger Kohlenstoffmaterialien und deren Einsatz in Direkt-Methanol-Brennstoffzellen Dissertation zur Erlangung des Grades eines Doktors der Ingenieurwissenschaften vorgelegt von
Funktionalisierung neuartiger Kohlenstoffmaterialien und deren Einsatz in Direkt-Methanol-Brennstoffzellen Dissertation zur Erlangung des Grades eines Doktors der Ingenieurwissenschaften vorgelegt von
6.3 Stromerzeugung mit galvanischen Zellen. Aufbauprinzip + Kontakte Abdichtung
 6.3 Stromerzeugung mit galvanischen Zellen Aufbauprinzip + Kontakte Abdichtung Elektrolyt Anode Stromkollektor Kathode Behälter Separator (Diaphragma) Anode: Kathode: Elektrolyt: Separator: Oxidation eines
6.3 Stromerzeugung mit galvanischen Zellen Aufbauprinzip + Kontakte Abdichtung Elektrolyt Anode Stromkollektor Kathode Behälter Separator (Diaphragma) Anode: Kathode: Elektrolyt: Separator: Oxidation eines
Die Brennstoffzelle. Von: Ismail Nasser
 Die Brennstoffzelle Gliederung Was ist eine Brennstoffzelle? Geschichte der Brennstoffzelle Aufbau und Funktionsweise der Brennstoffzelle Unterschiedliche Arten Gesamtwirkungsgrad Kosten Was ist eine Brennstoffzelle?
Die Brennstoffzelle Gliederung Was ist eine Brennstoffzelle? Geschichte der Brennstoffzelle Aufbau und Funktionsweise der Brennstoffzelle Unterschiedliche Arten Gesamtwirkungsgrad Kosten Was ist eine Brennstoffzelle?
E7 Elektrolyse. Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch. Münster, den
 E7 Elektrolyse Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch Münster, den 18.12.2000 INHALTSVERZEICHNIS 1. Einleitung 2. Theoretische Grundlagen 2.1 Elektrolyse 2.2 Die FARADAYschen Gesetze der
E7 Elektrolyse Versuchsprotokoll von Thomas Bauer und Patrick Fritzsch Münster, den 18.12.2000 INHALTSVERZEICHNIS 1. Einleitung 2. Theoretische Grundlagen 2.1 Elektrolyse 2.2 Die FARADAYschen Gesetze der
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde VL # 14,
 Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde VL # 14, 20.05.2009 Vladimir Dyakonov Experimentelle Physik VI dyakonov@physik.uni-wuerzburg.de Professor Dr. Vladimir
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde VL # 14, 20.05.2009 Vladimir Dyakonov Experimentelle Physik VI dyakonov@physik.uni-wuerzburg.de Professor Dr. Vladimir
Gleichstromkreis. 2.2 Messgeräte für Spannung, Stromstärke und Widerstand. Siehe Abschnitt 2.4 beim Versuch E 1 Kennlinien elektronischer Bauelemente
 E 5 1. Aufgaben 1. Die Spannungs-Strom-Kennlinie UKl = f( I) einer Spannungsquelle ist zu ermitteln. Aus der grafischen Darstellung dieser Kennlinie sind Innenwiderstand i, Urspannung U o und Kurzschlussstrom
E 5 1. Aufgaben 1. Die Spannungs-Strom-Kennlinie UKl = f( I) einer Spannungsquelle ist zu ermitteln. Aus der grafischen Darstellung dieser Kennlinie sind Innenwiderstand i, Urspannung U o und Kurzschlussstrom
1.) Skizzierieren Sie den Aufbau einer PEM Brennstoffzelle und erläutern Sie deren Funktionsweise.
 E50 Name: Brennstoffzelle Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Dieser Fragebogen muss von jedem Teilnehmer eigenständig (keine Gruppenlösung!)
E50 Name: Brennstoffzelle Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Dieser Fragebogen muss von jedem Teilnehmer eigenständig (keine Gruppenlösung!)
Leistungsbauelemente
 I (Kurs-Nr. 21645), apl. Prof. Dr. rer. nat. Fakultät für Mathematik und Informatik Fachgebiet Elektrotechnik und Informationstechnik ( ) D-58084 Hagen 1 Gliederung Einleitung Physikalische Grundlagen
I (Kurs-Nr. 21645), apl. Prof. Dr. rer. nat. Fakultät für Mathematik und Informatik Fachgebiet Elektrotechnik und Informationstechnik ( ) D-58084 Hagen 1 Gliederung Einleitung Physikalische Grundlagen
TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in. Reihenschaltung/Parallelschaltung
 TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in V17 Fachgebiet Chemie Reihenschaltung/Parallelschaltung 1. Aufgabe Bauen Sie die Anordnung nach Bild 1 oder Bild 2 auf. Nehmen Sie
TU Ilmenau Chemisches Praktikum Versuch Kennlinie der Brennstoffzelle in V17 Fachgebiet Chemie Reihenschaltung/Parallelschaltung 1. Aufgabe Bauen Sie die Anordnung nach Bild 1 oder Bild 2 auf. Nehmen Sie
Brennstoffzelle. Tim Kösterke Bernd Hasken 15. 06. 2005
 Brennstoffzelle Tim Kösterke Bernd Hasken 15. 06. 2005 Verschiedene Brennstoffzellen Niedertemperaturbereich PEM Brennstoffzelle (PEMFC) Direkt-Methanol Brennstoffzelle (DMFC) Alkalische Brennstoffzelle
Brennstoffzelle Tim Kösterke Bernd Hasken 15. 06. 2005 Verschiedene Brennstoffzellen Niedertemperaturbereich PEM Brennstoffzelle (PEMFC) Direkt-Methanol Brennstoffzelle (DMFC) Alkalische Brennstoffzelle
Technische Universität München. Brennstoffzelle. Roland Fuchsberger
 Brennstoffzelle Roland Fuchsberger Inhalt Elektrochemische Grundlagen Elektrochemische Zelle Faradaysches Gesetz Nernstsche Gleichung Brennstoffzelle Geschichte Verschiedene Typen Marktanalyse Portabel
Brennstoffzelle Roland Fuchsberger Inhalt Elektrochemische Grundlagen Elektrochemische Zelle Faradaysches Gesetz Nernstsche Gleichung Brennstoffzelle Geschichte Verschiedene Typen Marktanalyse Portabel
Originaldokument enthält an dieser Stelle eine Grafik! Original document contains a graphic at this position!
 FUNKTIONSWEISE Thema : HALBLEITERDIODEN Die Eigenschaften des PN-Überganges werden in Halbleiterdioden genutzt. Die p- und n- Schicht befinden sich einem verschlossenen Gehäuse mit zwei Anschlussbeinen.
FUNKTIONSWEISE Thema : HALBLEITERDIODEN Die Eigenschaften des PN-Überganges werden in Halbleiterdioden genutzt. Die p- und n- Schicht befinden sich einem verschlossenen Gehäuse mit zwei Anschlussbeinen.
6.1 Elektrodenpotenzial und elektromotorische Kraft
 6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
Themengebiet: Thermodynamik. Brennstoffzelle, Wirkungsgrad, Durchtrittsüberspannung, Diffusionsüberspannung,
 Seite 1 Themengebiet: Thermodynamik Stichwörter, Wirkungsgrad, Durchtrittsüberspannung, Diffusionsüberspannung, Literatur [1] A. Macdonald and M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris,
Seite 1 Themengebiet: Thermodynamik Stichwörter, Wirkungsgrad, Durchtrittsüberspannung, Diffusionsüberspannung, Literatur [1] A. Macdonald and M. Berry, Wasserstoff: Energie für morgen, Band 4, Heliocentris,
LEISTUNGSTEST ELEKTROLYSE-STACK
 LEISTUNGSTEST ELEKTROLYSE-STACK Energetischer und Faradayscher Wirkungsgrad HHO-Generator HG21 Elektrolyse-Stack von Alexander Weis Travelnova TN-S1 Elektrolyse-Stack von Saša Smolčić Dieses Material steht
LEISTUNGSTEST ELEKTROLYSE-STACK Energetischer und Faradayscher Wirkungsgrad HHO-Generator HG21 Elektrolyse-Stack von Alexander Weis Travelnova TN-S1 Elektrolyse-Stack von Saša Smolčić Dieses Material steht
FUELCELLBOX Wettbewerb 2008 Phase II. Ingeborg-Drewitz- Gesamtschule Gladbeck
 FUELCELLBOX Wettbewerb 2008 Phase II Ingeborg-Drewitz- Gesamtschule Gladbeck Übergabe der FUELCELLBOX 1.a) Kennlinie der Solarzellen MPP R / Ω U / V I / ma P / mw unendlich 4,33 0 0 148,3 4,1 26,6 109,06
FUELCELLBOX Wettbewerb 2008 Phase II Ingeborg-Drewitz- Gesamtschule Gladbeck Übergabe der FUELCELLBOX 1.a) Kennlinie der Solarzellen MPP R / Ω U / V I / ma P / mw unendlich 4,33 0 0 148,3 4,1 26,6 109,06
Zulassungstest zur Physik II für Chemiker
 SoSe 2016 Zulassungstest zur Physik II für Chemiker 03.08.16 Name: Matrikelnummer: T1 T2 T3 T4 T5 T6 T7 T8 T9 T10 T TOT.../4.../4.../4.../4.../4.../4.../4.../4.../4.../4.../40 R1 R2 R3 R4 R TOT.../6.../6.../6.../6.../24
SoSe 2016 Zulassungstest zur Physik II für Chemiker 03.08.16 Name: Matrikelnummer: T1 T2 T3 T4 T5 T6 T7 T8 T9 T10 T TOT.../4.../4.../4.../4.../4.../4.../4.../4.../4.../4.../40 R1 R2 R3 R4 R TOT.../6.../6.../6.../6.../24
Q t U I R = Wiederholung: Stromstärke: Einheit 1 Ampere, C = A s. Elektrischer Widerstand: Einheit 1 Ohm, Ω = V/A
 1 Wiederholung: Stromstärke: I = Q t Einheit 1 Ampere, C = A s Elektrischer Widerstand: R = U I U = R I Einheit 1 Ohm, Ω = V/A Standard Widerstände: 2 Aber auch dies sind Widerstände: Verstellbare Widerstände
1 Wiederholung: Stromstärke: I = Q t Einheit 1 Ampere, C = A s Elektrischer Widerstand: R = U I U = R I Einheit 1 Ohm, Ω = V/A Standard Widerstände: 2 Aber auch dies sind Widerstände: Verstellbare Widerstände
Ich schwitze sagte die Solarzelle. Bei Dir piepst s wohl antwortete der Geigerzähler.
 Ich schwitze sagte die Solarzelle. Bei Dir piepst s wohl antwortete der Geigerzähler. Eine strahlende Reise von der Brennstoffzelle zum Urgestein. Hartmut Abele, Jacqueline Erhart, Christoph Gösselsberger,
Ich schwitze sagte die Solarzelle. Bei Dir piepst s wohl antwortete der Geigerzähler. Eine strahlende Reise von der Brennstoffzelle zum Urgestein. Hartmut Abele, Jacqueline Erhart, Christoph Gösselsberger,
