Eine Runaway-Reaktion
|
|
|
- Lieselotte Grosse
- vor 7 Jahren
- Abrufe
Transkript
1 Eine Runaway-Reaktion Peter Bützer, Markus Roth Inhalt 0H1 1H2 2H3 3H4 8H5 15H6 17H7 18H8 19H9 20H10 Dynamik in der Chemie... 21H1 Schritte der Systemdynamik... 22H2 Ein Katalysator... 23H3 Das Experiment... 24H3 4H4.1 Durchführung... 25H4 5H4.2 Beobachtung... 26H4 6H4.3 Messungen... 27H6 7H4.4 Reaktionsgleichung... 28H6 Simulation... 29H7 9H5.1 Prinzip der Rückkopplung (Typ 2)... 30H7 10H5.2 Die Rückkopplung und der Verbrauch von Edukten (Typ 10)... 31H8 11H5.3 Die Rückkopplung mit der Temperatur mit der RGT-Regel... 32H10 12H5.4 Abschätzung des Temperaturverlaufs mit der Abkühlung... 33H12 13H5.5 Vergleich von Messung und Simulation... 34H14 14H5.6 Interpretation... 35H14 Temperaturverlauf mit der Gleichung von Arrhenius... 36H15 16H6.1 Interpretation... 37H17 Bezug zum Alltag... 38H18 Weitere Möglichkeiten... 39H18 Folgerung... 40H20 Literatur... 41H20 Prof. Dr. Peter Bützer Dipl. Ing. Markus Roth Pädagogische Hochschule St. Gallen
2 Peter Bützer, Markus Roth 2 1 Dynamik in der Chemie Dynamik in der Chemie? Die ist nicht neu. Der sächsische Staatschemiker Wenzel hat die Reaktionsgeschwindigkeit 1777 beim Auflösen von Kupfer- und Zink-Münzen beschrieben0f1. Wir sprechen leider selten darüber, oft nur gerade bei Show-Experimenten und die müssen nicht so genau verstanden werden wie der Trick eines Zauberkünstlers. In den Chemielehrbüchern der Allgemeinen Chemie nehmen Reaktionsgeschwindigkeiten höchstens 5% der Seiten ein, selbst beim chemischen Gleichgewicht wird das Kunststück zustande gebracht, nicht über Geschwindigkeiten sprechen zu müssen. Wenn aber sogar beim Autokatalysator nur Edukte und Produkte erwähnt werden und die Erhöhung der Reaktionsgeschwindigkeit nicht einmal andeutungsweise abgeschätzt wird, dann scheint hier ein grosses Gebiet brach da zu liegen. Dieses Defizit ist nicht zuletzt durch den Umstand erklärbar, dass die mathematischen Ansprüche um dynamische Modelle zu beschreiben, ausser bei den einfachsten Fällen, mehr als Grundlagen verlangten. Das hat sich mit dem Einsatz der Computer mit numerischer Mathematik nun grundlegend geändert. Meist kommt man in den chemischen Anwendungen der Systemdynamik mit den vier Grundoperationen und den Potenzen aus. Diese Simulationen sind wertvoll, zeigen sie doch die Modelle und zudem ermöglichen sie, aktiv Erfahrungen mit einzelnen Parametern zu erhalten. 2 Schritte der Systemdynamik "Wer immer nur das tut, was er schon kann, bleibt immer nur das, was er schon ist." Henry Ford ( ) amerikanischer Automobilhersteller Ein System ist ein geordnetes Zusammenwirken von Elementen. Viele Teile der Welt kann man sich aus Systemen aufgebaut vorstellen, wer diese beschreiben kann, versteht die Welt besser. Abbildung 1: Problemlösen mit dem systemdynamischen Ansatz
3 3F, 4F Peter Bützer, Markus Roth 3 Simulieren bedeutet nachahmen. Eine Simulation ist eine vereinfachte Darstellung realer Vorgänge. Die Simulation baut dabei auf ein Modell einer realen Situation auf. 3 Ein Katalysator Ausserordentlich ist, dass Andreas Libavius ( ) bereits 1597 in seinem Buch Alchymia den die enzymatische Katalyse als Fermentation verwendet1f hat der schwedische Chemiker Jöns Jakob Berzelius ( ) den Begriff Katalysator mit folgenden Worten in der Funktion umschrieben0f3 : Die katalytische Kraft scheint eigentlich darin zu bestehen, dass Körper durch ihre blosse Gegenwart und nicht durch ihre Verwandtschaft die bei dieser Temperatur schlummernden Verwandtschaften zu wecken vermögen, so dass zufolge derselben in einem zusammengesetzten Körper die Elemente sich zu solchen anderen Verhältnissen ordnen, durch welche eine grössere elektrochemische Neutralisierung hervorgebracht wird. Heute ist der Katalysator definiert1f4 : Stoffe, die die Aktivierungsenergie zum Ablauf einer bestimmten Reaktion herabsetzen und dadurch die Reaktionsgeschwindigkeit erhöhen, ohne bei der Reaktion verbraucht zu werden; er geht unverändert aus der Reaktion hervor. Die Katalyse ist wie ein Mysterium: Sie ermöglicht etwas, das vorher nahezu unerreichbar schien, und lässt damit ein Hindernis überwinden. Sie ist verknüpft mit dem Wunder des Verbrauchs und der Erneuerung. 4 Das Experiment Zersetzung von Wasserstoffperoxid mit Eisenchlorid als Katalysator2F H 3 FeCl 2O2 2 H2O O2 Das Experiment zeichnet sich dadurch aus, dass: es sehr einfach durchzuführen ist, einen kleinen experimentellen Aufwand erfordert, sehr anschaulich die Wirkungsweise eines Katalysators zeigt, einfach mit Messungen verfolgt werden kann, billige Ausgangsstoffe verwendet, eine einfache Entsorgung erlaubt. 5 6, 7, 5F8.
4 Peter Bützer, Markus Roth 4 Tabelle 1: Übersicht über die Experimente Verwendete Substanzen Messung 1 Messung 2 Messung 3 Eisen(III)-chlorid-Lösung (0.1 mol/l) 0.8 ml 0.6 ml 0.4 ml Keine Gefahrenklassierung Wasserstoffperoxid (30%) 5 ml 5 ml 5 ml Ätzend (C) R-Sätze: S-Sätze: /37/39-45 dest. Wasser 0.2 ml 0.4 ml 0.6 ml Total Volumen 6 ml 6 ml 6 ml 3 Grosse Reagenzgläser mit je einem Temperatursensor (z.b. Vernier6F9, Stainless Steel, PASCO7F10, Stainless Steel Temperature Probe). 4.1 Durchführung In ein grosses Reagenzglas werden folgende Substanzen vorgelegt: 0.8 ml FeCl mol/l und 0.2 ml Wasser (Varianten: 0.6 ml FeCl 3 und 0.4 ml Wasser, 0.4 ml FeCl 3 und 0.6 ml Wasser) Dann werden mit der Spritze rasch 5 ml 30% H 2 O 2 zugegeben. Der Temperaturverlauf wird mit einer Messfrequenz von mindestens 1 Messung pro Sekunde verfolgt. 4.2 Beobachtung Beim Mischen vom gelben Eisenchlorid mit dem farblosen Wasserstoffperoxid färbt sich die Reaktionsmischung dunkelbraun, was ein Hinweis ist, dass der Katalysator eine chemische Bindung mit dem H 2 O 2 eingegangen ist. Abbildung 2: Experimentelle Anordnung; das Gemisch im Reagenzglas links siedet. Abbildung 3: Reaktionskomplex des Katalysators, wenn er an der "Arbeit" ist. Katalysatorlösung 0.1 mol/l FeCl 3, links: reine Lösung, Mitte: zusammen mit H 2 O 2 beim reagieren, rechts: nach der Reaktion. Die Farbveränderung bei der Zugabe von Wasserstoffperoxid zur Eisenchlorid-Lösung weist darauf hin, dass eine chemische Reaktion stattgefunden hat.
5 Peter Bützer, Markus Roth 5 FeCl 3 als Lösung hellbraun FeCl 3 (OH) 2 als Lösung dunkelbraun FeCl 3 als Lösung hellbraun Abbildung 4: Katalysator entsprechend Abbildung 2 im Ablauf der Reaktion (nicht als Aquakomplexe dargestellt) Die Temperatur erhöht sich, bis die Reaktionsmischung zum Sieden kommt. Nach Abschluss der Reaktion wird die Farbe der Lösung wieder hellgelb, wie sie am Anfang war. Die Reaktion produziert Wärme. Damit wird die Reaktionsmischung erwärmt, die Temperatur steigt. Nach der RGT-Regel nimmt die Reaktionsgeschwindigkeit pro 10 C um einen Faktor 2 3 zu. Somit wird die Reaktion rascher, die Temperatur steigt wieder usw. Das ist ein Beispiel einer positiv rückgekoppelten Reaktion. Die Reaktionslösung nimmt nach der Reaktion wieder die ursprüngliche Farbe an. Wird erneut Wasserstoffperoxid zugegeben, dann verfärbt sich die Lösung erneut zu Braun und die Reaktion läuft am. Der Katalysator wurde bei der Reaktion somit nicht aufgebraucht. Mit dem nicht präzise definierten Begriff Reaktivität bezeichnet man in der Chemie die Eigenschaft von Atomen und Molekülen, eine chemische Reaktion einzugehen. Substanzen, die für die Reaktion nur eine geringe Aktivierungsenergie benötigen, werden als sehr reaktiv bezeichnet, solche mit einer hohen Aktivierungsenergie als inert. Die Reaktionsgeschwindigkeits-Konstante ist ein Mass für die Reaktivität. Da das FeCl 3 den Zerfall von H 2 O 2 stark beschleunigt, ist die Aktivierungsenergie mit diesem Katalysator kleiner oder die Reaktivität von H 2 O 2 grösser.
6 Peter Bützer, Markus Roth Messungen Mit 3 Temperatursonden werden die 3 Ansätze simultan verfolgt Temperatur ( C) Messung 1 Messung 2 Messung Zeit (s) Abbildung 5: Zeitliche Verläufe der Temperaturmessungen von Wasserstoffperoxid (H 2 O 2 ) mit 3 unterschiedlichen Eisen(III)-chlorid-Lösungen (FeCl 3 ) als Katalysator. Die Auswertung der Messdaten zeigt: Die Anstiegs-Geschwindigkeiten der Temperaturen sind proportional der Menge des eingesetzten Katalysators. 4.4 Reaktionsgleichung Reaktion mit dem Katalysator 11 : H 2 O 2 (l) + FeCl 3 (l) [FeCl 3 (OH) 2 ] (l); Formel 1 hellbraun dunkelbraun [FeCl 3 (OH) 2 ] (l) + H 2 O 2 (l) FeCl 3 (l) + 2 H 2 O (l) + O 2 (g); Formel 2 2 H 2 O 2 (l) 2 H 2 O (l) + O 2 (g); Formel 3 Gesamtreaktion H = kj/mol; exotherme Reaktion (setzt Wärme frei) Detaillierter die Fenten-Reaktion 12,13 : Fe 2+ + H 2 O 2 FeOH 2+ + OH Fe 3+ + H 2 O 2 Fe 2+ + H + + HO 2 Fe 3+ + HO 2 Fe 2+ + H + + O 2
7 Peter Bützer, Markus Roth 7 5 Simulation Annahmen: Wasserstoffperoxid wird in einem Reaktionsschritt zersetzt. Die Zersetzung liefert Energie. Die Reaktionsgeschwindigkeit ist abhängig von der Menge Katalysator und der Konzentration von Wasserstoffperoxid. Die Reaktionsenergie heizt das Reaktionsgemisch auf. Die Zunahme der Temperatur führt zu einer Erhöhung der Reaktionsgeschwindigkeit (positive Rückkopplung). Der Einfluss der Temperatur auf die Reaktionsgeschwindigkeit wird mit der RGT- Regel ausgedrückt. Das Reaktionsgefäss kühlt sich durch Wärmeabgabe ab. 5.1 Prinzip der Rückkopplung (Typ 2) 9F kr 14 reagieren Produkt Energie Abbildung 6: Einfachstes Simulationsdiagramm für eine rückgekoppelte Reaktion (Reaktion 1. Ordnung) (Simulation mit Vensim PLE)10F Produkt 0.03 mol Produkt : Current Time (Second) Abbildung 7: Zeitdiagramm für die bei der Bildung des Produkts freigesetzte Energie (Anzahl mole sind proportional der Energie).
8 Peter Bützer, Markus Roth 8 Dokumentation (Gleichungen, Parameter) (1) Edukt= INTEG (-reagieren, 4.32) Units: kj [0,?] Verfügbare Energie des Edukts, 5 ml 30% H2O2 --> 300 g/l, MG = 34 g/mol, 5 ml --> 4.32 kj (2) FINAL TIME = 240 Units: Second The final time for the simulation. (3) INITIAL TIME = 0 Units: Second The initial time for the simulation. (4) kr= 0.05 Units: 1/Second [0,0.1] Reaktionsgeschwindigkeitskonstante (5) Produkt= INTEG (reagieren, 0.001) Units: kj [0,?] Der Anfangswert darf nicht Null sein, weil sonst keine Rückkopplung auftreten kann (Multiplikation mit 0!) (6) reagieren= kr*produkt (entspricht dem üblichen Ansatz: dc/dt = k c) Units: kj/second [0,?] Reaktionsgeschwindigkeit rückgekoppelt (7) SAVEPER = 1 Units: Second [0,?] The frequency with which output is stored. (8) TIME STEP = 0.1 Units: Second [0,?] The time step for the simulation. 5.2 Die Rückkopplung und der Verbrauch von Edukten (Typ 10)11F kr 16 Edukt Energie reagieren Produkt Energie Abbildung 8: Simulationsdiagramm einer positiv rückgekoppelten Reaktion mit Edukt und Produkt (Reaktion 2. Ordnung).
9 Peter Bützer, Markus Roth 9 6 Produkt 4.5 kj Time (Second) Produkt : Current Abbildung 9: Zeitdiagramm für die bei der Bildung des Produkts freigesetzte Energie. Je mehr Energie freigesetzt wird, desto rascher die Reaktion, je weniger Edukt vorhanden ist, desto langsamer die Reaktion. Ist alles Edukt aufgebraucht, kommt die Reaktion zum Stillstand. Dokumentation (Gleichungen, Parameter) (1) Edukt= INTEG (-reagieren, 4.32) Units: kj [0,?] Verfügbare Energie des Edukts, 5 ml 30% H2O2 --> 300 g/l, MG = 34 g/mol, 5 ml --> 4.32 kj (2) FINAL TIME = 240 Units: Second The final time for the simulation. (3) INITIAL TIME = 0 Units: Second The initial time for the simulation. (4) kr= 0.05 Units: 1/(Second*kJ) [0,0.1] Reaktions-Geschwindigkeits-Konstante k = ln(2)/hwz (5) Produkt= INTEG (reagieren, 0.001) Units: kj [0,?] Total freigesetzte Energie = Summe aller bei der Reaktion freigesetzten Energien, Der Anfangswert darf nicht 0 sein! (6) reagieren= kr*edukt*produkt Units: kj/second [0,?] Das ist die Reaktionsgeschwindigkeit der Reaktion (7) SAVEPER = 1 Units: Second [0,?] The frequency with which output is stored. (8) TIME STEP = 0.01 Units: Second [0,?] The time step for the simulation.
10 Peter Bützer, Markus Roth Die Rückkopplung mit der Temperatur mit der RGT-Regel Die RGT-Regel Die Messungen von van t Hoff12F17 haben ihn zum Schluss geführt13f18 : Bei der grössten Zahl der bis jetzt in dieser Richtung untersuchten Fälle, welche sich auf das Temperaturintervall beziehen, ist nun sehr auffallend das Geschwindigkeitsverhältnis für 10 Grad Temperaturerhöhung etwa 2 bis 3 bei gewöhnlicher Temperatur, mit anderen Worten: eine Temperaturerhöhung um 10 Grad verdoppelt resp. verdreifacht die Reaktionsgeschwindigkeit. (Diese Aussagen sind mit 16 ganz unterschiedlichen Reaktionen belegt, wobei die meisten Faktoren über 2,5 liegen). RGT-Regel (Reaktionsgeschwindigkeits-Temperatur Regel): Eine Temperaturerhöhung um 10 Grad verdoppelt bis vervierfacht die Reaktionsgeschwindigkeit (van t Hoff) (Basis = 1.5 4); Diese Basis kann den angegebenen Bereich z.t. weit übersteigen14f19. Q10 Basis Temperaturerhöhung 10 Katalysator kr Basis Q10 T10 Tp Wärme Kapazität Edukt reagieren Produkt Abbildung 10: Simulationsdiagramm einer mit dem Edukt (Reaktion 1. Ordnung) und der Temperatur der Reaktionsmischung rückgekoppelten Reaktion (RGT-Regel). Temperatur: Tp = Energie/Wärmekapazität; Formel 4 Faktor: Q10 = Basis (Temperaturdifferenz/T10) ; T10=10 K; Formel 5
11 Peter Bützer, Markus Roth 11 6 Produkt 4.5 kj Time (Second) Produkt : Current Abbildung 11: Zeitdiagramm Dokumentation (Gleichungen, Parameter) (01) Basis= 3 Units: Dmnl [1,3] Die RG nimmt um einen Faktor 1-3 zu bei einer Erhöhung der Temperatur um 10 K. Das ist diese Basis 1-3. (02) Edukt= INTEG (-reagieren, 4.32) Units: kj [0,?] Verfügbare Energie des Edukts, 5 ml 30% H2O2 --> 300 g/l, MG = 34 g/mol, 5 ml --> 4.32 kj (03) FINAL TIME = 300 Units: Second The final time for the simulation. (04) INITIAL TIME = 0 Units: Second The initial time for the simulation. (05) Katalysator= Units: Dmnl [0.021,0.063,0.021] (06) kr= 0.11 Units: 1/Second [0.001,0.01] Reaktions-Geschwindigkeits-Konstante k = ln(2)/hwz, Wert aus dem Anstieg bei den Messungen, daraus leitet sich der Wert für den Katalysator ab. (07) Produkt= INTEG (reagieren, 0.001) Units: kj [0,?] Total freigesetzte Energie = Summe aller bei der Reaktion freigesetzten Energien; (08) Q10= Basis^(Tp/T10) Units: Dmnl [0,?] RGT-Regel: Faktor um den die Geschwindigkeit bei einer Temperaturzunahme um 10 K steigt. (09) reagieren= kr*q10*edukt*katalysator Units: kj/second [0,?] Reaktionsgeschwindigkeit (10) SAVEPER = TIME STEP Units: Second [0,?]
12 Peter Bützer, Markus Roth 12 The frequency with which output is stored. (11) T10= 10*1 Units: K [0,?] Pro 10 K verdoppelt sich die RG (12) TIME STEP = 0.1 Units: Second [0,?] The time step for the simulation. (13) Tp= Produkt/Wärme Kapazität Units: K [0,?] (14) Wärme Kapazität= 0.07 Units: kj/k [0.01,0.1] Wärmekapazität des Reaktionsgemisches mit dem Gefäss 5.4 Abschätzung des Temperaturverlaufs mit der Abkühlung Katalysator Basis T10 Tz Wärme Kapazität Aussen Temperatur Temperatur Verlauf Einheiten kr Q10 ka Edukt reagieren Produkt abkühlen Abbildung 12: Simulationsdiagramm der über das Edukt (Reaktion 1. Ordnung), die Temperatur und die Abkühlung rückgekoppelten Reaktion. Abkühlung: Die Abkühlrate abkühlen ist proportional der Temperaturdifferenz von Reaktionsgemisch und Aussentemperatur. Formel 6 Die Abkühlkonstante ist abhängig von: Gefässmaterial, Gefässform, Gefässoberfläche, Kühlung (Luft, Tischplatte, Wasser..), sie muss experimentell ermittelt werden. 90 Temperaturverlauf 60 C Time (Second) Temperatur Verlauf : Current Abbildung 13: Zeitdiagramm
13 Peter Bützer, Markus Roth 13 Dokumentation (Gleichungen, Parameter) (01) abkühlen= ka*tz Units: kj/second [0,?] Das ist die Abkühlgeschwindigkeit der Reaktion (02) Aussen Temperatur= 23 Units: C [10,30] Anfangswert der Messung (03) Basis= 3 Units: Dmnl [1,3] Die RG nimmt um einen Faktor 1-3 zu bei einer Erhöhung der Temperatur um 10 K. (04) Edukt= INTEG (-reagieren, 4.32) Units: kj [0,?] Verfügbare Energie des Edukts, 5 ml 30% H2O2 --> 300 g/l, MG = 34 g/mol, 5 ml --> 4.32 kj (05) Einheiten= 1*1 Units: C/K Die Temperaturzunahme in K entspricht der Temperaturzunahme in K (06) FINAL TIME = 240 Units: Second The final time for the simulation. (07) INITIAL TIME = 0 Units: Second The initial time for the simulation. (08) ka= Units: kj/second/k [0.0001,0.001] Abkühlkonstante, wie rasch kühlt sich das Reaktionsgemisch (mit Gefäss) ab. ka hängt von der Grösse, der Form und vom Material des Reaktionsgefässes ab, ebenso vom Material auf dem das Gefäss steht. (09) Katalysator= Units: Dmnl [0.021,0.063,0.021] Katalysator (10) kr= 0.11 Units: 1/Second [0.001,0.01] Reaktions-Geschwindigkeits-Konstante k = ln(2)/hwz, Wert aus dem Anstieg bei den Messungen kr=0.11, daraus leitet sich der Wert für den Katalysator ab. (11) Produkt= INTEG (reagieren-abkühlen, 0.001) Units: kj [0,?] Total freigesetzte Energie = Summe aller bei der Reaktion freigesetzten Energien (12) Q10= Basis^(Tz/T10) Units: Dmnl [0,?] RGT-Regel: Faktor um den die Geschwindigkeit bei einer Temperaturzunahme um 10 K steigt. (13) reagieren= kr*q10*edukt*katalysator Units: kj/second [0,?] Das ist die Reaktionsgeschwindigkeit der Reaktion (14) SAVEPER = 1 Units: Second [0,?] The frequency with which output is stored. (15) T10= 10*1 Units: K [0,?] Pro 10 K verdoppelt sich die RG (16) Temperatur Verlauf= Tz*Einheiten+Aussen Temperatur Units: C [0,?] (17) TIME STEP = 0.1 Units: Second [0,?] The time step for the simulation. (18) Tz= Produkt/Wärme Kapazität Units: K [0,?] Temperaturzunahme der Reaktionsmischung (19) Wärme Kapazität= 0.07 Units: kj/k [0.01,0.1] Wärmekapazität des Reaktionsgemisches mit Gefäss
14 Peter Bützer, Markus Roth Vergleich von Messung und Simulation Eine Aussage ist genau dann wahr, wenn sie mit den Tatsachen übereinstimmt. Karl R. Popper ( ) britischer Erkenntnisphilosoph Nimmt man diese Aussage ernst, dann ist es wichtig, seine Modelle an experimentellen Daten zu überprüfen. Temperatur ( C) Zeit (s) Messung 2 Simulation Abbildung 14: Zeitdiagramm für den Vergleich von Messung und Simulation 5.6 Interpretation Nur mit der Basis 3 bei der RGT-Regel lassen sich die Messdaten einigermassen korrekt nachsimulieren. Am Anfang zeigen Experiment und Simulation eine systematische Abweichung. Das weist darauf hin, dass das Modell noch verbessert werden kann, um die Realität besser zu beschreiben. Das ist möglich, denn bei unserem Modell ist die Katalyse als Gleichgewichtsreaktion von Edukt und Katalysator zum Edukt-Katalysator-Komplex (Formeln 1 und 2) nicht berücksichtigt worden. Dieser Schritt hat jedoch eine Verlangsamung der Anfangsreaktion zur Folge, also genau das, was noch verbessert werden muss. Der Einfluss der Katalysatormenge wird durch die Simulation korrekt wiedergegeben. Die Blasenbildung an der Oberfläche ist ebenfalls abhängig von der Temperatur und das Ausperlen des Sauerstoffs nimmt immer auch etwas Wasser mit, das in die Gasphase geht. Nicht zu vergessen bei all diesen Experimenten ist die Trägheit des Thermometers.
15 Peter Bützer, Markus Roth 15 6 Temperaturverlauf mit der Gleichung von Arrhenius Die von Arrhenius 1889 aufgestellte, quantitative Beziehung zwischen Reaktionsgeschwindigkeitskonstante und Temperatur bei chemischen Reaktionen 20 lautet (Arrhenius Gleichung siehe Atkins-Jones16F21 ): dln(k) ΔH 2 dt R T ( Ea /( R T )) k(t) A e k: Reaktionsgeschwindigkeitskonstante, A: präexponentieller Faktor oder Frequenzfaktor, Ea: Arrhenius'sche Aktivierungsenergie, R: allg. Gaskonstante [ J K -1 mol -1 ] T: absolute Temperatur [Kelvin] Aktivierungsenergie G a und Frequenzfaktor A sind Experimenten mit 3 Temperaturen: 24.7, 34.7, 46.3 C ermittelt. (k ist die Reaktionsgeschwindigkeitskonstante) ln(k) y = x R 2 = /(R x T) Abbildung 15: Bestimmung der Aktivierungsenergie und des Frequenzfaktors mit einem modifizierten Arrhenius-Plot Aktivierungsenergie Ga: Steigung entspricht kj/mol J/mol Frequenzfaktor A: y-achsenabschnitt entspricht ln(a) A=e = 1.33*10 9
16 Peter Bützer, Markus Roth 16 Abkühlkonstante Kühlkonstante Eduktenergie aufheizen Energiefreisetzung abkühlen Aktivierungsenergie Konzentration Frequenzfaktor Volumen Stoffmenge spez Wärmekapazität RG-Konstante Einheit Wärmekapazität Temperaturdiff Temperatur Umgebungstemperatur Temp C Einheiten Abbildung 16: Simulationsdiagramm mit der Arrhenius-Gleichung Dokumentation (Gleichungen, Parameter) (01) abkühlen= Kühlkonstante Units: J/Second [0,?] (02) Abkühlkonstante= Units: 1/Second [0,0.01] (03) Aktivierungsenergie= Units: J [60000,70000] (04) aufheizen= "RG-Konstante"*Eduktenergie Units: J/Second [0,?] (05) Eduktenergie= INTEG (-aufheizen, 20000) Units: J [0,?] (06) Einheit= 1*1 Units: K/J [1,1] (07) Einheiten= 1*1 Units: C/K [1,?] (08) Energiefreisetzung= INTEG (+aufheizen-abkühlen, 0) Units: J [0,?] (09) FINAL TIME = 240 Units: Second The final time for the simulation. (10) Frequenzfaktor= 1.33e+009 Units: 1/Second [0,?] (11) INITIAL TIME = 0 Units: Second The initial time for the simulation. (12) Konzentration= Units: mol/m3 [0,?] mol/m3 (13) Kühlkonstante= Abkühlkonstante*Temperaturdiff*Wärmekapazität Units: J/Second [0,?] (14) "RG-Konstante"=Frequenzfaktor*EXP(-Aktivierungsenergie/(8.314*Temperatur)*Einheit) Units: 1/Second [0,?] (15) SAVEPER = 1 Units: Second [0,?] The frequency with which output is stored. (16) spez Wärmekapazität= 4200 Units: J/mol/K [0,?] (17) Stoffmenge= Konzentration*Volumen Units: mol/m3*m3 n= c*v (18) Temp C= (Temperatur-273)*Einheiten
17 Peter Bützer, Markus Roth 17 Units: C [0,?] (19) Temperatur= Umgebungstemperatur+Energiefreisetzung/Wärmekapazität Units: K [0,?] (20) Temperaturdiff= Temperatur-Umgebungstemperatur Units: K (21) TIME STEP = 0.1 Units: Second [0,?] The time step for the simulation. (22) Umgebungstemperatur= 298 Units: K (23) Volumen= 5e-006 Units: m3 [0,5e-005] m3 (24) Wärmekapazität= spez Wärmekapazität*Stoffmenge Units: J/K Die Abkühlkonstante kann aus dem Experiment direkt bestimmt werden (exponentieller Abfall der Temperatur nach beenden der Reaktion). Der einzige freie Parameter ist die effektive spezifische Verdampfungswärme (c p ), die bei dem kleinen Wasservolumen und dem grossen Anteil an Gefässmasse nicht aus Tabellen erhalten werden kann. 6.1 Interpretation Die Simulation berücksichtigt viele reale Parameter nicht. So z.b. die Verdampfung gegen Schluss der Reaktion, das Aufheizen des Reagenzglases, das keinen Beitrag zur Beschleunigung der Reaktion liefert. Die Katalysatormenge ist in der Aktivierungsenergie enthalten, es fehlt das vorgelagerte Gleichgewicht Temperatur ( C) Messung Temp C Zeit (s) Abbildung 17: Vergleich von Messung und Simulation (mit Arrhenius-Gleichung) Der Vergleich von Messung und Simulation ist deshalb nicht besonders gut, weil viele realen Parameter nicht berücksichtigt sind so z.b. das Verdampfen der Flüssigkeit (Abkühlung), die
18 Peter Bützer, Markus Roth 18 Isolation des Gefässes, die Form des Gefässes, der Einfluss der relativ grossen Temperatursonde. Die Wärmekapazität der Flüssigkeit ist zudem temperaturabhängig, was im Modell auch nicht enthalten ist. Entscheidend ist sicher auch, dass nur die Summen-Reaktionsgleichung eingesetzt wurde aber die wesentlichen gemessenen Parameter der detaillierten Kinetik waren nicht verfügbar. Der Brite Henry John Horstman Fenton ( ) verwendete 1893 erstmals Gemisch von Wasserstoffperoxid und Eisen(II)-Salzen zur Oxidation von Hydroxy-Verbindungen (Fenton- Reagenz) Bezug zum Alltag Exotherme Reaktionen sind wegen dieser Rückkopplung industriell immer kritisch der Name Runaway-Reaktion 22,23 weist darauf hin. Die grössten bekannten Chemieunfälle z.b. in Seveso (10. Juli 1976) und Bhopal (3. Dezember 1984) hatten die Ursache in exothermen Reaktionen. 8 Weitere Möglichkeiten Dieses Beispiel eignet sich sehr gut, um: auf die Risiken von exothermen Reaktionen hinzuweisen (Runaway, Unfälle ), die Effektivität der Biokatalysatoren zu zeigen (Vergleich mit Catalase), die Thermodynamik aufzuzeigen, die Entgiftung von H 2 O 2 zu demonstrieren, Für diese und ähnliche Anwendungen mit H 2 O 2 sind folgend einige Angaben zusammengestellt. Tabelle 2: Thermodynamische Daten Substanz H 0 f [kj/mol] S 0 [J/mol/K] G 0 f [kj/mol] O 2 (g) H 2 O (l) H 2 O 2 (l) Tabelle 3: Wasserstoffperoxid ist extrem stabil bei üblichen Temperaturen, zerfällt jedoch bei höheren Temperaturen rascher18f24 : Temperatur C Anteil, der zerfallen ist: < 1% pro Jahr 1% pro Woche 2% pro Tag Eine normale Lösung von H 2 O 2 ist ziemlich stabil und hat bei Raumtemperatur eine HWZ von ca. 7 Jahren. In alkalischen Lösungen ist H 2 O 2 nicht stabil19f25.
19 Peter Bützer, Markus Roth 19 Tabelle 4: Katalyse von Wasserstoffperoxid Molekül Molmasse [g/mol] k [298 K] Aktivierungsenergie20F26 [kj/mol] Ohne Katalysator (H 2 O) E-14 a 75.4 Fe 3+ aq (dieses Exp.) E Fe 3+ aq 164 6E-10 b 52.6 b I E-10 a 56.5 Pt E-9 a 49 Häm 364 1E-8 b 44 b Catalase E-2 a 8.4 a Ea : berechnet nach: ln k lna ; A als Frequenzfaktor ist temperaturunabhängig; A ist R T für diese Reaktion ca. 2E-5 (= 2*10 5 = 200'000) b : abgeschätzt Interpretation Zerfall von Wasserstoffperoxid: 2 H 2 O 2 Katalysator 2 H 2 O + O 2 Der Eisenkatalysator beschleunigt die Reaktion um einen Faktor '000. Die Biochemie ist hier weit überlegen, sie beschleunigt mit Catalase um einen Faktor 10 12!!
20 Peter Bützer, Markus Roth 20 9 Folgerung Der Einsatz der Systemdynamik in Chemie und Biochemie ermöglicht einfache Modelle mit minimalem mathematischem Aufwand für die Erklärung heranzuziehen. Die Vergleiche von Messdaten, der Realität, und den Simulationen sind dann oft eine Herausforderung, die Modelle zu verbessern und zu verfeinern. Katalysatoren können systemdynamisch gut verstanden werden, weil die Modelle ganz einfach und die Veränderungen in den Auswirkungen sofort sichtbar sind. There is no truth, only progress. Karl R. Popper, ( ) britischer Erkenntnisphilosoph 10 Literatur 1 Wenzel K. F., Lehr von der Verwandtschaft der Körper, Dresden, 1777, 3.Ausgabe, herausg. V. D. H. Gründel, (Dresden 1800) zitiert in: Winkler Hans-Georg, Das Massenwirkungsgesetz, Aulis-Verlag Deubner, Köln, 2.Aufl., 1975, 83 2 Libavius Andreas, Die Alchemie des Andreas Libavius, Ein Lehrbuch aus dem Jahre 1597, Verlag Chemie, Weinheim, 1964, S Zitiert nach Ostwald Wilhelm, Leitlinien der Chemie, Leipzig, Katalysator, Thieme Römpp Online, Georg Thieme Verlag KG, Stuttgart, Bützer P., Coray R., Eine thermische Runaway-Reaktion: Ein Demonstrationsexperiment, Praxis der Naturwissenschaften, 8/40, 1991, 38 6 Bützer P., Ein Katalysator sichtbar an der Arbeit (Ein einfaches Demonstrationsexperiment), Spektrum, 2, 1992, 34 7 Bützer P., in Byland Th., Gloor P.(Hrsg.), ICT, einfach-praktisch, Wie Farben verschwinden und Zinsen wachsen, Bildung Sauerländer, Sauerländer Verlage, Aarau, 2002, 86 8 Bützer P., Roth M., Chemische Reaktionen als dynamische Systeme, T^3-Schweiz, August, 2002, Vernier Software & Technology, 10 PASCO, Steudel R., Chemie der Nichtmetalle (Reaktionen von H 2 O 2 ), Walter de Gruyter, 1998, Frost A.A., Pearson R.G., Kinetics and Mechanism, John Wiley & Sons, Inc., New York/London, 1961, Kremer M.L., Mechanism of the Fenton reaction. Evidence for a new intermediate, Phys. Chem. Chem. Phys., 1999, 1, Bützer P., Roth M., Die Zeit im Griff, Systemdynamik in Chemie und Biochemie, verlag pestalozzianum, Zürich 2006, 43ff 15 Vensim PLE, Simulationssoftware, Ventana Systems Inc., Bützer P., Roth M., Die Zeit im Griff, Systemdynamik in Chemie und Biochemie,verlag pestalozzianum, Zürich 2006, 98ff
21 Peter Bützer, Markus Roth van 't Hoff J. H. (Nobelpreis 1901) : "in recognition of the extraordinary services he has rendered by the discovery of the laws of chemical dynamics and osmotic pressure in solutions", Cohen E., Studien zur chemischen Dynamik, nach van t Hoff J.H., Etudes de dynamique chimique, Frederik Muller & Co, Amsterdam, Wilhelm Engelmann, Leipzig, 1896, Für physikalische Prozesse (Diffusion, Leitfähigkeit) Basis <1.5, für chemische/biochemische Prozesse Basis 2-3, für Proteindenaturierung (Coagulation) Basis Svante A.A. (Nobelpreis 1903):Im Presentation Speech heisst es unter anderem: One of the most important consequences of Arrhenius's theory was the completion of the great generalizations for which the first Nobel Prize for Chemistry was awarded to Van't Hoff. 21 Atkins P., Jones L., Chemical Principles, W.H. Freeman and Co., New York, 1999, 595ff 22 Urban P.G. (ed.), Bretherick s Handbook of Reactive Chemical Hazards, Oxford, Vol. 2, 2007, p Bützer P., Rückkopplung im Experiment: Eine Runaway- Reaktion; Erfahrung mit einer entscheidenden Funktion in vernetzten Systemen, Spektrum, 2, 1990, Hydrogen Peroxide (H 2 O 2 ), TECHNICAL INFORMATION, Stevens B., Chemical Kinetics, Chapman & Hall, London 1961, p.7 26 Chung Ch., Cyberspace Chemistry (CaCt), Catalysts and Energy of Activation, Ea,
Systemdynamik der Katalyse H 2 O 2 /FeCl 3
 1 Systemdynamik der Katalyse H 2 O 2 /FeCl 3 Inhalt 1 Dynamik in der Chemie... 1 2 Schritte der Systemdynamik... 2 3 Ein Katalysator... 2 4 Das Experiment... 3 4.1 Durchführung... 3 4.2 Beobachtung...
1 Systemdynamik der Katalyse H 2 O 2 /FeCl 3 Inhalt 1 Dynamik in der Chemie... 1 2 Schritte der Systemdynamik... 2 3 Ein Katalysator... 2 4 Das Experiment... 3 4.1 Durchführung... 3 4.2 Beobachtung...
Kohlenmonoxid aus Ethanal, CH 3 -CHO
 Kohlenmonoxid aus Ethanal, CH 3 -CHO Peter Bützer Chemiker haben viele nette Reaktionen! Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung... 2 2.1 Beobachtungen/Messungen, Datenbasis... 2 2.2 Reaktionsgleichungen/Berechnungen...
Kohlenmonoxid aus Ethanal, CH 3 -CHO Peter Bützer Chemiker haben viele nette Reaktionen! Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung... 2 2.1 Beobachtungen/Messungen, Datenbasis... 2 2.2 Reaktionsgleichungen/Berechnungen...
Michaelis-Menten-Kinetik
 Michaelis-Menten-Kinetik Peter Bützer Inhalt 1 Einführung... 1 2 Modell... 2 2.1 Modellannahmen... 2 2.2 Drei Fälle... 2. Simulationsdiagramm (Typ ), Systemdynamik... 2.4 Dokumentation (Gleichungen, Parameter)...
Michaelis-Menten-Kinetik Peter Bützer Inhalt 1 Einführung... 1 2 Modell... 2 2.1 Modellannahmen... 2 2.2 Drei Fälle... 2. Simulationsdiagramm (Typ ), Systemdynamik... 2.4 Dokumentation (Gleichungen, Parameter)...
Gipshärtung Energiefreisetzung, Systemdynamik
 Gipshärtung Energiefreisetzung, Systemdynamik Inhalt 1 Reaktion... 1 2 Experiment... 2 3 Simulation... 3 3.1 Simulationsdiagramm... 3 3.2 Dokumentation (Gleichungen, Parameter)... 3 3.3 Zeitdiagramm...
Gipshärtung Energiefreisetzung, Systemdynamik Inhalt 1 Reaktion... 1 2 Experiment... 2 3 Simulation... 3 3.1 Simulationsdiagramm... 3 3.2 Dokumentation (Gleichungen, Parameter)... 3 3.3 Zeitdiagramm...
Ethanolbildung in Bananen
 Ethanolbildung in Bananen Peter Bützer Inhalt 1 Einführung... 1 2 Modell... 2 2.1 Annahmen:... 2 2.2 Simulation(Typ 1)... 2 2.3 Dokumentation (Gleichungen, Parameter)... 3 2.4 Vergleich der Simulation
Ethanolbildung in Bananen Peter Bützer Inhalt 1 Einführung... 1 2 Modell... 2 2.1 Annahmen:... 2 2.2 Simulation(Typ 1)... 2 2.3 Dokumentation (Gleichungen, Parameter)... 3 2.4 Vergleich der Simulation
Titration einer Säure mit einer Base
 Titration einer Säure mit einer Base Peter Bützer Inhalt 1 Einleitung... 1 2 Modellannahmen (Systemdynamik)... 2 3 Simulationsdiagramm (Typ 1)... 2 4 Dokumentation (Gleichungen, Parameter)... 3 5 Simulation...
Titration einer Säure mit einer Base Peter Bützer Inhalt 1 Einleitung... 1 2 Modellannahmen (Systemdynamik)... 2 3 Simulationsdiagramm (Typ 1)... 2 4 Dokumentation (Gleichungen, Parameter)... 3 5 Simulation...
4.3 Reaktionsgeschwindigkeit und Katalysator
 4.3 Reaktionsgeschwindigkeit und Katalysator - Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Ein- Einstellung des Gleichgewichts,
4.3 Reaktionsgeschwindigkeit und Katalysator - Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Ein- Einstellung des Gleichgewichts,
Atmung, Dissimilation
 Atmung, Dissimilation Peter Bützer Abbildung 1: Atmung Inhalt 1 Physiologisches... 1 2 Atmung, eine Reaktion 0. Ordnung... 2 3 Simulation... 2 4 Interpretation... 4 5 Mikroökologie im Zimmer... 4 6 Interpretation...
Atmung, Dissimilation Peter Bützer Abbildung 1: Atmung Inhalt 1 Physiologisches... 1 2 Atmung, eine Reaktion 0. Ordnung... 2 3 Simulation... 2 4 Interpretation... 4 5 Mikroökologie im Zimmer... 4 6 Interpretation...
Daisyworld. Peter Bützer. 1 Eine kurze Theorie. Inhalt
 Daisyworld Peter Bützer Inhalt 1 Eine kurze Theorie... 1 2 Aufgabe... 2 3 Simulation, Lösung (Typ 3), Systemdynamik... 3 3.1 Annahmen... 3 3.2 Simulationsdiagramm... 3 3.3 Zeitdiagramm... 4 3.4 Dokumentation
Daisyworld Peter Bützer Inhalt 1 Eine kurze Theorie... 1 2 Aufgabe... 2 3 Simulation, Lösung (Typ 3), Systemdynamik... 3 3.1 Annahmen... 3 3.2 Simulationsdiagramm... 3 3.3 Zeitdiagramm... 4 3.4 Dokumentation
Hefewachstum. Peter Bützer
 Hefewachstum Peter Bützer Inhalt 1 Hefe... 1 2 Das System als Black Box... 2 3 Messung des... 2 4 Modell... 3 5 Simulation (Typ 9)... 3 5.1 Simulationsdiagramm... 4 5.2 Messung... 4 5.3 Dokumentation (Gleichungen,
Hefewachstum Peter Bützer Inhalt 1 Hefe... 1 2 Das System als Black Box... 2 3 Messung des... 2 4 Modell... 3 5 Simulation (Typ 9)... 3 5.1 Simulationsdiagramm... 4 5.2 Messung... 4 5.3 Dokumentation (Gleichungen,
Monod-Kinetik. Peter Bützer
 Monod-Kinetik Peter Bützer Inhalt 1 Einleitung... 1 1.1 Modell... 1 1.2 Modellannahmen... 2 1. Gleichung... 2 1.4 Drei Fälle... 2 Simulation, Systemdynamik... 2.1 Simulationsdiagramm (Typ 1)... 2.2 Dokumentation
Monod-Kinetik Peter Bützer Inhalt 1 Einleitung... 1 1.1 Modell... 1 1.2 Modellannahmen... 2 1. Gleichung... 2 1.4 Drei Fälle... 2 Simulation, Systemdynamik... 2.1 Simulationsdiagramm (Typ 1)... 2.2 Dokumentation
Kohlendioxidfreisetzung aus Champagner. 1 Einleitung/Theorie. Peter Bützer. Inhalt
 Kohlendioxidfreisetzung aus Champagner Inhalt 1 Einleitung/Theorie... 1 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 2 2.4 Reaktionsgleichungen/Berechnungen...
Kohlendioxidfreisetzung aus Champagner Inhalt 1 Einleitung/Theorie... 1 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 2 2.4 Reaktionsgleichungen/Berechnungen...
Systemdynamik: Iodwasserstoff-Gleichgewicht
 1 Systemdynamik: Iodwasserstoff-Gleichgewicht Inhalt 1 Einleitung... 1 2 Reaktionsgleichung, Substanzdaten... 2 3 Simulation... 3 3.1 Simulationsdiagramm (Reaktions Typ 3)... 3 3.2 Zeitdiagramme... 3 3.3
1 Systemdynamik: Iodwasserstoff-Gleichgewicht Inhalt 1 Einleitung... 1 2 Reaktionsgleichung, Substanzdaten... 2 3 Simulation... 3 3.1 Simulationsdiagramm (Reaktions Typ 3)... 3 3.2 Zeitdiagramme... 3 3.3
Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse
 Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Säureangriff auf die Zähne
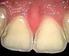 Säureangriff auf die Zähne Eine erfolgreiche Reduktion ist vielleicht die erfolgreichste Form aller wissenschaftlichen Erklärungen, die man sich vorstellen kann. 1 Karl R. Popper, (1902-199) britischer
Säureangriff auf die Zähne Eine erfolgreiche Reduktion ist vielleicht die erfolgreichste Form aller wissenschaftlichen Erklärungen, die man sich vorstellen kann. 1 Karl R. Popper, (1902-199) britischer
Phototrope Gläser. Dr. Peter Bützer. Inhalt
 1 Phototrope Gläser Inhalt 1 Einleitung/Theorie... 2 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 3 2.4 Reaktionsgleichungen/Berechnungen... 3 3 Simulation,
1 Phototrope Gläser Inhalt 1 Einleitung/Theorie... 2 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 3 2.4 Reaktionsgleichungen/Berechnungen... 3 3 Simulation,
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
3.4 Energieumsatz bei Reaktionen
 3.4 Energieumsatz bei Reaktionen Versuch: Verbrennen eines Stückes Holz Beobachtung: Energie wird freigesetzt in Form von Wärme. Jede Reaktion ist mit einem Energieumsatz gekoppelt. Reaktionen, bei denen
3.4 Energieumsatz bei Reaktionen Versuch: Verbrennen eines Stückes Holz Beobachtung: Energie wird freigesetzt in Form von Wärme. Jede Reaktion ist mit einem Energieumsatz gekoppelt. Reaktionen, bei denen
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2
 Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 10. Temperaturabhängigkeit der Reaktionsgeschwindigkeit: Arrhenius-Beziehung Thema In diesem Versuch
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 10. Temperaturabhängigkeit der Reaktionsgeschwindigkeit: Arrhenius-Beziehung Thema In diesem Versuch
Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus)
 Kinetik Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus) Klassifizierung chem. Reaktionen nach kinetischen Aspekten a) Reaktionsmolekularität: wie viele Teilchen
Kinetik Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus) Klassifizierung chem. Reaktionen nach kinetischen Aspekten a) Reaktionsmolekularität: wie viele Teilchen
Chemie Protokoll. Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung. Stuttgart, Sommersemester 2012
 Chemie Protokoll Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung Stuttgart, Sommersemester 202 Gruppe 0 Jan Schnabel Maximilian Möckel Henri Menke Assistent: Durmus 20. Mai 202 Inhaltsverzeichnis Theorie
Chemie Protokoll Versuch 2 3 (RKV) Reaktionskinetik Esterverseifung Stuttgart, Sommersemester 202 Gruppe 0 Jan Schnabel Maximilian Möckel Henri Menke Assistent: Durmus 20. Mai 202 Inhaltsverzeichnis Theorie
4.3 Reaktionsgeschwindigkeit und Katalysator
 4.3 Reaktionsgeschwindigkeit und Katalysator Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Einstellung des Gleichgewichts,
4.3 Reaktionsgeschwindigkeit und Katalysator Neben der thermodynamischen Lage des chemischen Gleichgewichts ist der zeitliche Ablauf der Reaktion, also die Geschwindigkeit der Einstellung des Gleichgewichts,
endotherme Reaktionen
 Exotherme/endotherme endotherme Reaktionen Edukte - H Produkte Exotherme Reaktion Edukte Produkte + H Endotherme Reaktion 101 Das Massenwirkungsgesetz Das Massenwirkungsgesetz Gleichgewicht chemischer
Exotherme/endotherme endotherme Reaktionen Edukte - H Produkte Exotherme Reaktion Edukte Produkte + H Endotherme Reaktion 101 Das Massenwirkungsgesetz Das Massenwirkungsgesetz Gleichgewicht chemischer
0.1 Geschwindigkeit bei Reaktionen
 1 0.1 Geschwindigkeit bei Reaktionen Salzsäure reagiert mit Magnesium Erklärung 2HCl + Mg MgCl 2 + H 2 Das M g-pulver reagiert schneller mit der Salzsäure als die Mg-Späne. Definition: Reaktionsgeschwindigkeit
1 0.1 Geschwindigkeit bei Reaktionen Salzsäure reagiert mit Magnesium Erklärung 2HCl + Mg MgCl 2 + H 2 Das M g-pulver reagiert schneller mit der Salzsäure als die Mg-Späne. Definition: Reaktionsgeschwindigkeit
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie
 Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
Richtung von spontanem Prozeßablauf und Veränderung der G in Abhängigkeit vom Vorzeichen der Enthalpie und der Entropie H S G= H-T S Prozeß 1. (-) (+) (-) immer exergonisch, erfolgt spontan bei allen Temperaturen
= Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s]
![= Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s] = Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s]](/thumbs/94/122358469.jpg) Ache2 Kapitel 14: Chemische Kinetik (Geschwindigkeit) Reaktionsgeschwindigkeit Beeinflussung: 1. Aggregatszustände der Reaktanten: Je öfters Moleküle zusammenstossen, desto schneller reagieren sie. (Oberflächenvergrösserung
Ache2 Kapitel 14: Chemische Kinetik (Geschwindigkeit) Reaktionsgeschwindigkeit Beeinflussung: 1. Aggregatszustände der Reaktanten: Je öfters Moleküle zusammenstossen, desto schneller reagieren sie. (Oberflächenvergrösserung
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion:
 Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Fragen zum Versuch 11a Kinetik Rohrzuckerinversion: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen
Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
 Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Coulomb-Gesetz, Ionen- (Kristall-)strukturen, NaCl, CsCl, ZnS, Elementarzelle, 7 Kristallsysteme Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Coulomb-Gesetz, Ionen- (Kristall-)strukturen, NaCl, CsCl, ZnS, Elementarzelle, 7 Kristallsysteme Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
EinFaCh 2. Studienvorbereitung Chemie. Einstieg in Freibergs anschauliches Chemiewissen Teil 2: Chemische Reaktionskinetik. tu-freiberg.
 Studienvorbereitung Chemie EinFaCh 2 Einstieg in Freibergs anschauliches Chemiewissen Teil 2: Chemische Reaktionskinetik tu-freiberg.de tu-freiberg.de/fakultaet2/einfach Was bedeutet Chemische Reaktionskinetik?
Studienvorbereitung Chemie EinFaCh 2 Einstieg in Freibergs anschauliches Chemiewissen Teil 2: Chemische Reaktionskinetik tu-freiberg.de tu-freiberg.de/fakultaet2/einfach Was bedeutet Chemische Reaktionskinetik?
Richtung chemischer Reaktionen, chemisches Gleichgewicht. Massenwirkungsgesetz
 Richtung chemischer Reaktionen, chemisches Gleichgewicht a A + b B K [C] [A] c a [D] [B] c C + d D d b K = Gleichgewichtskonstante Massenwirkungsgesetz [ ] = in Lösung: Konzentration (in mol L -1 ), für
Richtung chemischer Reaktionen, chemisches Gleichgewicht a A + b B K [C] [A] c a [D] [B] c C + d D d b K = Gleichgewichtskonstante Massenwirkungsgesetz [ ] = in Lösung: Konzentration (in mol L -1 ), für
2 NO 2 N 2 O 4, ein einfaches Gleichgewicht
 2 NO 2 N 2 O 4, ein einfaches Gleichgewicht Peter Bützer Inhalt 1 Einführung... 1 2 Grundlagen zur Reaktion... 1 3 Simulation (Typ 3), Systemdynamik... 4 3.1 Das einfache Gleichgewicht... 4 3.2 Das Prinzip
2 NO 2 N 2 O 4, ein einfaches Gleichgewicht Peter Bützer Inhalt 1 Einführung... 1 2 Grundlagen zur Reaktion... 1 3 Simulation (Typ 3), Systemdynamik... 4 3.1 Das einfache Gleichgewicht... 4 3.2 Das Prinzip
Energetik und Kinetik chemischer Reaktionen
 Energetik und Kinetik chemischer Reaktionen Reaktionsenergetik als Teil der Thermodynamik - wann läuft eine chemische Reaktion freiwillig ab? - in welchem Umfang läuft eine Reaktion ab? - wie viel Energie
Energetik und Kinetik chemischer Reaktionen Reaktionsenergetik als Teil der Thermodynamik - wann läuft eine chemische Reaktion freiwillig ab? - in welchem Umfang läuft eine Reaktion ab? - wie viel Energie
Versuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten -
 1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
1 ersuch 14: Dampfdruckkurve - Messung der Dampfdruckkurven leicht verdampfbarer Flüssigkeiten - 1. Theorie Befindet sich eine Flüssigkeit in einem abgeschlossenen Gefäß, so stellt sich zwischen der Gasphase
Fragen zum Thema chemische Reaktionen Klasse 4 1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion
 1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion vorliegen? 3. Wie nennt man die Stoffe, die nach der Reaktion vorliegen? 4. Womit wird die Richtung
1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion vorliegen? 3. Wie nennt man die Stoffe, die nach der Reaktion vorliegen? 4. Womit wird die Richtung
Thermodynamik. Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen.
 Thermodynamik Was ist das? Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen. Gesetze der Thermodynamik Erlauben die Voraussage, ob eine bestimmte
Thermodynamik Was ist das? Thermodynamik ist die Lehre von den Energieänderungen im Verlauf von physikalischen und chemischen Vorgängen. Gesetze der Thermodynamik Erlauben die Voraussage, ob eine bestimmte
Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen. c(a) t. v = -
 REAKTIONSKINETIK 1 Reaktionskinetik Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen Anwendung: - Vorgänge in den lebenden Organismen
REAKTIONSKINETIK 1 Reaktionskinetik Reaktionskinetik: - Geschwindigkeit chemischer Reaktionen - Untersuchung (bzw. Bestimmung) der Reaktionsmechanismen Anwendung: - Vorgänge in den lebenden Organismen
Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10
 Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: birlenbach@chemie.uni-siegen.de Lars
Vorlesung Allgemeine Chemie Teil Physikalische Chemie WS 2009/10 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: birlenbach@chemie.uni-siegen.de Lars
Grundlagen der Kinetik
 Kapitel 1 Grundlagen der Kinetik In diesem Kapitel werden die folgenden Themen kurz wiederholt: Die differenziellen und integralen Geschwindigkeitsgesetze von irreversiblen Reaktionen., 1., und. Ordnung
Kapitel 1 Grundlagen der Kinetik In diesem Kapitel werden die folgenden Themen kurz wiederholt: Die differenziellen und integralen Geschwindigkeitsgesetze von irreversiblen Reaktionen., 1., und. Ordnung
Fragen zum Versuch Kinetik:
 Fragen zum Versuch Kinetik: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen von Rohrzucker im Wasser
Fragen zum Versuch Kinetik: 1. Die Inversion von Rohrzucker ist: a. Die Umwandlung von Rohrzucker in Saccharose b. Die katalytische Spaltung in Glucose und Fructose c. Das Auflösen von Rohrzucker im Wasser
Richtung chemischer Reaktionen, Chemisches Gleichgewicht. Massenwirkungsgesetz
 Richtung chemischer Reaktionen, Chemisches Gleichgewicht a A + b B K = [C] [A] c a [D] [B] c C + d D d b Massenwirkungsgesetz K = Gleichgewichtskonstante [ ] = in Lösung: Konzentration (in mol L -1 ),
Richtung chemischer Reaktionen, Chemisches Gleichgewicht a A + b B K = [C] [A] c a [D] [B] c C + d D d b Massenwirkungsgesetz K = Gleichgewichtskonstante [ ] = in Lösung: Konzentration (in mol L -1 ),
Aufgabe: Man bestimme die Geschwindigkeitskonstante für den Zerfall des Diacetonalkohols bei 293 und 303 K.
 A 31 Zersetzung von Diacetonalkohol Aufgabe: Man bestimme die Geschwindigkeitskonstante für den Zerfall des Diacetonalkohols bei 293 und 303 K. Grundlagen: Diacetonalkohol (ρ (20 C) = 0,931 g/cm 3 ) zerfällt
A 31 Zersetzung von Diacetonalkohol Aufgabe: Man bestimme die Geschwindigkeitskonstante für den Zerfall des Diacetonalkohols bei 293 und 303 K. Grundlagen: Diacetonalkohol (ρ (20 C) = 0,931 g/cm 3 ) zerfällt
Zink, ein wichtiges Spurenelement
 Zink, ein wichtiges Spurenelement Peter Bützer Inhalt 1 Einleitung... 1 2 Aufgaben... 2 3 Lösungen... 3 3.1 Simulationsdiagramm (Typ 1)... 3 3.2 Dokumentation (Gleichungen, Parameter)... 3 3.3 Zeitdiagramm...
Zink, ein wichtiges Spurenelement Peter Bützer Inhalt 1 Einleitung... 1 2 Aufgaben... 2 3 Lösungen... 3 3.1 Simulationsdiagramm (Typ 1)... 3 3.2 Dokumentation (Gleichungen, Parameter)... 3 3.3 Zeitdiagramm...
Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung
 Versuchsprotokoll: Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung Gruppe 10 29.06.2013 Patrik Wolfram TId:20 Alina Heidbüchel TId:19 1 Inhaltsverzeichnis 1 Einleitung... 3 2 Theorie...
Versuchsprotokoll: Bestimmung der Geschwindigkeitskonstanten einer Esterverseifung Gruppe 10 29.06.2013 Patrik Wolfram TId:20 Alina Heidbüchel TId:19 1 Inhaltsverzeichnis 1 Einleitung... 3 2 Theorie...
Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate
 Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate Zeitbedarf für die Versuchsdurchführung: ca. 10 Min. Geräte: Magnetrührer mit Magnetrührstäbchen Thermometer (min. 0,5 C Genauigkeit)
Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate Zeitbedarf für die Versuchsdurchführung: ca. 10 Min. Geräte: Magnetrührer mit Magnetrührstäbchen Thermometer (min. 0,5 C Genauigkeit)
Verseifungsgeschwindigkeit eines Esters
 A 32 Verseifungsgeschwindigkeit eines Esters Aufgabe: Man bestimme die Geschwindigkeitskonstante k der Methylacetatverseifung bei 2 verschiedenen Temperaturen und berechne daraus den Vorfaktor sowie die
A 32 Verseifungsgeschwindigkeit eines Esters Aufgabe: Man bestimme die Geschwindigkeitskonstante k der Methylacetatverseifung bei 2 verschiedenen Temperaturen und berechne daraus den Vorfaktor sowie die
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Lösungen 10 (Kinetik)
 Chemie I WS 2003/2004 Lösungen 10 (Kinetik) Aufgabe 1 Verschiedenes 1.1 Als Reaktionsgeschwindigkeit v c wird die Ableitung der Konzentration eines Reaktanden A nach der Zeit t, dividiert durch dessen
Chemie I WS 2003/2004 Lösungen 10 (Kinetik) Aufgabe 1 Verschiedenes 1.1 Als Reaktionsgeschwindigkeit v c wird die Ableitung der Konzentration eines Reaktanden A nach der Zeit t, dividiert durch dessen
Gegenstand der letzten Vorlesung
 Gegenstand der letzten Vorlesung Reaktionsgeschwindigkeit Reaktionsordnung Molekularität Reaktion 0., 1.,. Ordnung Reaktion pseudo-erster Ordnung Aktivierungsenergie Temperaturabhängigkeit der Geschwindigkeitskonstanten
Gegenstand der letzten Vorlesung Reaktionsgeschwindigkeit Reaktionsordnung Molekularität Reaktion 0., 1.,. Ordnung Reaktion pseudo-erster Ordnung Aktivierungsenergie Temperaturabhängigkeit der Geschwindigkeitskonstanten
Posten 1a. Antworten: a) Newton b) Sievert c) Joule d) Watt. (=> Posten 2a) (=> Posten 3d) (=> Posten 4j) (=> Posten 5s) Bor
 Posten 1a Welche Einheit hat die Arbeit? a) Newton b) Sievert c) Joule d) Watt (=> Posten 2a) (=> Posten 3d) (=> Posten 4j) (=> Posten 5s) Posten 1f Welche Eigenschaft gehört nicht zu den drei wichtigen
Posten 1a Welche Einheit hat die Arbeit? a) Newton b) Sievert c) Joule d) Watt (=> Posten 2a) (=> Posten 3d) (=> Posten 4j) (=> Posten 5s) Posten 1f Welche Eigenschaft gehört nicht zu den drei wichtigen
Reaktionskinetik. Geschwindigkeitsgesetze
 Reaktionskinetik Geschwindigkeitsgesetze Lernziele: Thermodynamische Beschreibung chemischer Reaktionen Berechnen und Beschreiben von Reaktionsordnungen Kinetische Beschreibung von Reaktionsmechanismen
Reaktionskinetik Geschwindigkeitsgesetze Lernziele: Thermodynamische Beschreibung chemischer Reaktionen Berechnen und Beschreiben von Reaktionsordnungen Kinetische Beschreibung von Reaktionsmechanismen
Indigokarmin, Indigotin - Metabolismus
 Indigokarmin, Indigotin - Metabolismus Inhalt 1.1 Chemische Charakterisierung,... 1 1.2 Verwendung und physiologische Eigenschaften... 3 1.3 Simulation des Metabolismus (Simulations-Typ 4), Systemdynamik...
Indigokarmin, Indigotin - Metabolismus Inhalt 1.1 Chemische Charakterisierung,... 1 1.2 Verwendung und physiologische Eigenschaften... 3 1.3 Simulation des Metabolismus (Simulations-Typ 4), Systemdynamik...
Wilhelm Ostwald -100 Jahre Nobelpreis-
 Wilhelm Ostwald -100 Jahre Nobelpreis- 2. Jahrestreffen der Senior Expert Chemists (SEC) Hanau 7. bis 9.5. 2009 Nobelpreisurkunde für seine Leistungen über Katalyse und seine grundlegenden Untersuchungen
Wilhelm Ostwald -100 Jahre Nobelpreis- 2. Jahrestreffen der Senior Expert Chemists (SEC) Hanau 7. bis 9.5. 2009 Nobelpreisurkunde für seine Leistungen über Katalyse und seine grundlegenden Untersuchungen
Sauerstoffbindung im Blut
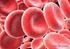 Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Sauerstoffbindung im Blut Die Fähigkeit uns zu wundern, ist das Einzige, was wir brauchen, um gute Philosophen zu werden. Gaarder Jostein, Sofies Welt 1 Inhalt 1 Einleitung/Theorie... 1 2 Aufgabenstellung...
Helvetia setzt Energien frei Eine heterogene Katalyse
 Helvetia setzt Energien frei Eine heterogene Katalyse Peter Bützer Der Unterschied zwischen einem Zauberer und einem Chemiker ist der: Der Zauberer täuscht dich mit einem raffinierten Trick. Der Chemiker
Helvetia setzt Energien frei Eine heterogene Katalyse Peter Bützer Der Unterschied zwischen einem Zauberer und einem Chemiker ist der: Der Zauberer täuscht dich mit einem raffinierten Trick. Der Chemiker
Gefahrenstoffe. 7 Bechergläser (100 ml), 1 Becherglas (1 L), Spatel, Wasser, Messzylinder, Glaswanne, Kartoffel
 1.1 Zersetzung von H 2O 2 mithilfe verschiedener Katalysatoren [4] Der Zerfall von Wasserstoffperoxid kann mithilfe vieler verschiedener Katalysatoren beschleunigt werden. In diesem Versuch sollen einige
1.1 Zersetzung von H 2O 2 mithilfe verschiedener Katalysatoren [4] Der Zerfall von Wasserstoffperoxid kann mithilfe vieler verschiedener Katalysatoren beschleunigt werden. In diesem Versuch sollen einige
5 Teilchen treffen Teilchen: Reaktionskinetik
 5 Teilchen treffen Teilchen: Reaktionskinetik 5.1 Elementarreaktionen und Mehrschritt-Reaktionen Wassergasreaktion: H 2 O + CO CO 2 + H 2 Dies ist lediglich der makroskopisch sichtbare Ablauf der Reaktion.
5 Teilchen treffen Teilchen: Reaktionskinetik 5.1 Elementarreaktionen und Mehrschritt-Reaktionen Wassergasreaktion: H 2 O + CO CO 2 + H 2 Dies ist lediglich der makroskopisch sichtbare Ablauf der Reaktion.
Chemisches Gleichgewicht in homogenen Systemen I Seminarvortrag SoSe 08
 Chemisches Gleichgewicht in homogenen Systemen I Seminarvortrag SoSe 08 Sebastian Meiss 14. Mai 2008 1 Historischer Einstieg Erstmals wurde das Massenwirkungsgesetz 1867 von dem norwegischen Mathematiker
Chemisches Gleichgewicht in homogenen Systemen I Seminarvortrag SoSe 08 Sebastian Meiss 14. Mai 2008 1 Historischer Einstieg Erstmals wurde das Massenwirkungsgesetz 1867 von dem norwegischen Mathematiker
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Universität Ulm Grundpraktikum Physikalische Chemie Versuch Nr. 24 Temperaturabhängigkeit von Gleichgewichts- und Geschwindigkeitskonstanten
 Universität Ulm Grundpraktikum Physikalische Chemie Versuch Nr. 24 Temperaturabhängigkeit von Gleichgewichts- und Geschwindigkeitskonstanten 1. Grundlagen 1.1. Vorkenntnisse Informieren Sie sich vor Durchführung
Universität Ulm Grundpraktikum Physikalische Chemie Versuch Nr. 24 Temperaturabhängigkeit von Gleichgewichts- und Geschwindigkeitskonstanten 1. Grundlagen 1.1. Vorkenntnisse Informieren Sie sich vor Durchführung
Die Geschwindigkeit zum Gleichgewicht
 2F 3F 6F 7F 8F Inhalt Die Geschwindigkeit zum Gleichgewicht Peter Bützer 0H1 1H2 2H3 8H4 15H5 Einleitung... 17H1 Reaktionsgleichung, Substanzdaten... 18H2 Simulation... 19H3 3H3.1 Simulationsdiagramm (Reaktions-Typ
2F 3F 6F 7F 8F Inhalt Die Geschwindigkeit zum Gleichgewicht Peter Bützer 0H1 1H2 2H3 8H4 15H5 Einleitung... 17H1 Reaktionsgleichung, Substanzdaten... 18H2 Simulation... 19H3 3H3.1 Simulationsdiagramm (Reaktions-Typ
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Chemische Oszillationen
 Ludwig Pohlmann Thermodynamik offener Systeme und Selbstorganisationsphänomene SS 007 Chemische Oszillationen. Chemische (Formal-)Kinetik Die chemische Kinetik untersucht die Geschwindigkeit und den Mechanismus
Ludwig Pohlmann Thermodynamik offener Systeme und Selbstorganisationsphänomene SS 007 Chemische Oszillationen. Chemische (Formal-)Kinetik Die chemische Kinetik untersucht die Geschwindigkeit und den Mechanismus
Verbrennungsrechnung als kinetischer Simulationsansatz
 Verbrennungsrechnung als kinetischer Simulationsansatz Simulationsansatz mit CHEMCAD Die Daten für Flammpunkt, Zündtemperatur, Explosionsgrenzen diverser Stoffe sind weitestgehend bekannt. Methoden zur
Verbrennungsrechnung als kinetischer Simulationsansatz Simulationsansatz mit CHEMCAD Die Daten für Flammpunkt, Zündtemperatur, Explosionsgrenzen diverser Stoffe sind weitestgehend bekannt. Methoden zur
Thermodynamik. Thermodynamik
 Geschlossenes System: Energieaustausch, aber kein Materieaustausch mit der Umgebung. Innere Energie: Jeder Stoff hat in sich Energie in irgendeiner Form gespeichert: die innere Energie U. U 1 = innere
Geschlossenes System: Energieaustausch, aber kein Materieaustausch mit der Umgebung. Innere Energie: Jeder Stoff hat in sich Energie in irgendeiner Form gespeichert: die innere Energie U. U 1 = innere
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
Thermodynamik & Kinetik
 Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Thermodynamik & Kinetik Inhaltsverzeichnis Ihr versteht die Begriffe offenes System, geschlossenes System, isoliertes System, Enthalpie, exotherm und endotherm... 3 Ihr kennt die Funktionsweise eines Kalorimeters
Name: Punktzahl: von 57 Note:
 Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
weniger Gasteilchen enthält. In diesem Fall also auf die Produktseite.
 A ÜB Prinzip Le HATELIER Seite 1 von 5 1. a) Formulieren Sie für die folgenden Reaktionen jeweils und entscheiden Sie gemäss dem Prinzip Le hatelier in welche Richtung sich die jeweiligen Gleichgewichte
A ÜB Prinzip Le HATELIER Seite 1 von 5 1. a) Formulieren Sie für die folgenden Reaktionen jeweils und entscheiden Sie gemäss dem Prinzip Le hatelier in welche Richtung sich die jeweiligen Gleichgewichte
Lösung 11. Allgemeine Chemie I Herbstsemester d[a] t. = k (1) Trennung der Variablen und Integration in den Randbedingungen führt auf: [A]
![Lösung 11. Allgemeine Chemie I Herbstsemester d[a] t. = k (1) Trennung der Variablen und Integration in den Randbedingungen führt auf: [A] Lösung 11. Allgemeine Chemie I Herbstsemester d[a] t. = k (1) Trennung der Variablen und Integration in den Randbedingungen führt auf: [A]](/thumbs/78/76746487.jpg) Lösung Allgemeine Chemie I Herbstsemester 20. Aufgabe Die Geschwindigkeitsgesetze finden Sie im Skript der Vorlesung und im Mortimer, p. 26-27. Für eine Reaktion, die Species A verbraucht, gilt bei einer
Lösung Allgemeine Chemie I Herbstsemester 20. Aufgabe Die Geschwindigkeitsgesetze finden Sie im Skript der Vorlesung und im Mortimer, p. 26-27. Für eine Reaktion, die Species A verbraucht, gilt bei einer
Herleitung des Massenwirkungsgesetzes für das chemische Gleichgewicht zwischen Iod, Wasserstoff und Iodwasserstoff
 Lernaufgabe zum Thema Herleitung des Massenwirkungsgesetzes für das chemische Gleichgewicht zwischen Iod, Wasserstoff und Iodwasserstoff Unterrichtsfach Schultyp Zielgruppe Chemie Gymnasium, alle Typen
Lernaufgabe zum Thema Herleitung des Massenwirkungsgesetzes für das chemische Gleichgewicht zwischen Iod, Wasserstoff und Iodwasserstoff Unterrichtsfach Schultyp Zielgruppe Chemie Gymnasium, alle Typen
... U I t = c m ΔT ( ΔT = T 2 - T 1 )
 nergie - Wärmespeicherung und Wärmeumsatz 1.) Spezifische Wärmekapazität von Wasser F Unter der spezifischen Wärmekapazität c eines Stoffes versteht man die nergie, die man zuführen muß, um 1 kg dieses
nergie - Wärmespeicherung und Wärmeumsatz 1.) Spezifische Wärmekapazität von Wasser F Unter der spezifischen Wärmekapazität c eines Stoffes versteht man die nergie, die man zuführen muß, um 1 kg dieses
Versuch 41: Viskosität durchgeführt am
 Physikalisch-chemisches Grundpraktikum Gruppe 6 Philipp von den Hoff Andreas J. Wagner Versuch 4: Viskosität durchgeführt am 26.05.2004 Zielsetzung: Ziel des Versuches ist es, die Viskosität von n-butan-2-ol
Physikalisch-chemisches Grundpraktikum Gruppe 6 Philipp von den Hoff Andreas J. Wagner Versuch 4: Viskosität durchgeführt am 26.05.2004 Zielsetzung: Ziel des Versuches ist es, die Viskosität von n-butan-2-ol
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 12. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 12. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 12. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 12. 07. 2007 Klausur Die Klausur
Atome. Chemie. Zusammenfassungen. Prüfung Mittwoch, 14. Dezember Dalton-Modell. Reaktionsgrundgesetze. Chemische Formeln.
 Chemie Atome Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Dalton-Modell Reaktionsgrundgesetze Chemische Formeln Avogadro Relative Massen Quantitative Beziehungen Stöchiometrie Steffi, Tom, Marvin
Chemie Atome Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Dalton-Modell Reaktionsgrundgesetze Chemische Formeln Avogadro Relative Massen Quantitative Beziehungen Stöchiometrie Steffi, Tom, Marvin
Physikalische Chemie 1
 Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung
 V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
Kerncurriculum Chemie Eichsfeld-Gymnasium Duderstadt Juni 2012
 Kerncurriculum Chemie Eichsfeld-Gymnasium Duderstadt Juni 2012 Jahrgänge 7 und 8 Jeweils 1 Jahreswochenstunde pro Schuljahr (epochal, entspricht 40 Stunden pro Schuljahr). Basiskonzepte: BK1: Stoff-Teilchen;
Kerncurriculum Chemie Eichsfeld-Gymnasium Duderstadt Juni 2012 Jahrgänge 7 und 8 Jeweils 1 Jahreswochenstunde pro Schuljahr (epochal, entspricht 40 Stunden pro Schuljahr). Basiskonzepte: BK1: Stoff-Teilchen;
PC I Thermodynamik G. Jeschke FS Lösung zur Übung 12
 PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
PC I Thermodynamik G. Jeschke FS 2015 Lösung zur Übung 12 12.1 Die Hydrierung von Ethen zu Ethan a) Die Reaktionsenthalpie ist direkt aus den in der Aufgabenstellung tabellierten Standardbildungsenthalpien
Das chemische Gleichgewicht
 Das chemische Gleichgewicht Modell: Geschlossenes Gefäß mit Flüssigkeit, die verdampft ( T=const ) Moleküle treten über in die Dampfphase H 2 O (l) H 2 O (g) H 2 O (g) Dampfdruck p H 2 O (l) T = const.
Das chemische Gleichgewicht Modell: Geschlossenes Gefäß mit Flüssigkeit, die verdampft ( T=const ) Moleküle treten über in die Dampfphase H 2 O (l) H 2 O (g) H 2 O (g) Dampfdruck p H 2 O (l) T = const.
Die Innere Energie U
 Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Die Innere Energie U U ist die Summe aller einem System innewohnenden Energien. Es ist unmöglich, diese zu berechnen. U kann nicht absolut angegeben werden! Differenzen in U ( U) können gemessen werden.
Die Freie Aktivierungsenthalpie
 Die Freie Aktivierungsenthalpie E A G k Ae RT e = = RT G: Freie Aktivierungsenthalpie G = H T S e G RT = e S R e H RT e S R A H E A Katalyse: der aktivierte Übergangskomplex H E A Katalysatoren beeinflussen
Die Freie Aktivierungsenthalpie E A G k Ae RT e = = RT G: Freie Aktivierungsenthalpie G = H T S e G RT = e S R e H RT e S R A H E A Katalyse: der aktivierte Übergangskomplex H E A Katalysatoren beeinflussen
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 5 Verhalten von Lösungen Konzentrationen Solvatation und Solvatationsenthalpie Kolligative Eigenschaften Kryoskopie/Ebullioskopie
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 5 Verhalten von Lösungen Konzentrationen Solvatation und Solvatationsenthalpie Kolligative Eigenschaften Kryoskopie/Ebullioskopie
Mischen von Flüssigkeiten mit verschiedener Temperatur
 V13 Thema: Wärme 1. Einleitung Ob bei der Regelung der Körpertemperatur, dem Heizen des Zimmers oder zahlreichen technischen Prozessen: Der Austausch von Wärme spielt eine wichtige Rolle. In diesem Versuch
V13 Thema: Wärme 1. Einleitung Ob bei der Regelung der Körpertemperatur, dem Heizen des Zimmers oder zahlreichen technischen Prozessen: Der Austausch von Wärme spielt eine wichtige Rolle. In diesem Versuch
Angezeigte Messgröße: Leitwert Kanal (LF) Für Grafik 0-10 ms Bei Zeitintervall: 5 s Gesamtzeit (für Grafik) : 1500 s
 Computer im Chemieunterricht von Ethansäureethylester Seite 1 / 5 Prinzip: Bei der alkalischen Verseifung von Ethansäureethylester werden Hydroxidionen durch AcetatiIonen ersetzt. Daher kann die Reaktion
Computer im Chemieunterricht von Ethansäureethylester Seite 1 / 5 Prinzip: Bei der alkalischen Verseifung von Ethansäureethylester werden Hydroxidionen durch AcetatiIonen ersetzt. Daher kann die Reaktion
PC I Thermodynamik und Transportprozesse. Kapitel 7. Kinetik. PC I-Kap :27 1
 20.07.2006 11:27 1 PC I Thermodynamik und Transportprozesse Kapitel 7 Kinetik Reaktionsgeschwindigkeit 20.07.2006 11:27 2 Messung der Reaktionsgeschwindigkeit. Die Konzentration des Edukts A ist als Funktion
20.07.2006 11:27 1 PC I Thermodynamik und Transportprozesse Kapitel 7 Kinetik Reaktionsgeschwindigkeit 20.07.2006 11:27 2 Messung der Reaktionsgeschwindigkeit. Die Konzentration des Edukts A ist als Funktion
8.4.5 Wasser sieden bei Zimmertemperatur ******
 8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
Katalyse. Martin Babilon 14/07/2011. Katalyse. Martin Babilon Universität Paderborn. 14 Juli Montag, 18. Juli 2011
 Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
Katalyse Universität Paderborn 14 Juli 2011 1 Übersicht Motivation & Einleitung Katalyse-Zyklus homogene Katalyse heterogene Katalyse 2 Motivation 3 Geschichte der Katalyse 6000 v. Christus: Alkoholvergärung
Grundlagen: Die Zersetzung von Ameisensäure in konzentrierter Schwefelsäure verläuft nach folgendem Mechanismus:
 A 35: Zersetzung von Ameisensäure Aufgabe: Für die Zersetzung von Ameisensäure in konzentrierter Schwefelsäure sind die Geschwindigkeitskonstante bei 30 und 40 C sowie der präexponentielle Faktor und die
A 35: Zersetzung von Ameisensäure Aufgabe: Für die Zersetzung von Ameisensäure in konzentrierter Schwefelsäure sind die Geschwindigkeitskonstante bei 30 und 40 C sowie der präexponentielle Faktor und die
Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen.
 1) DEFINITIONEN DIE CHEMISCHE REAKTION Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen. Der Massenerhalt: Die Masse ändert sich im Laufe einer Reaktion
1) DEFINITIONEN DIE CHEMISCHE REAKTION Eine chemische Reaktion läuft ab, wenn reaktionsfähige Teilchen mit genügend Energie zusammenstoßen. Der Massenerhalt: Die Masse ändert sich im Laufe einer Reaktion
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2016 Wie zählen wir Mengen in der Chemie? Stefan
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2016 Wie zählen wir Mengen in der Chemie? Stefan
Auswertung. B04: Spezifische Wärme
 Auswertung zum Versuch B04: Spezifische Wärme Alexander FufaeV Partner: Jule Heier Gruppe 254 Inhaltsverzeichnis 2. Bestimmung der Wärmekapazität C1 des blauen Dewargefäßes... 3 3. Bestimmung der Schmelzwärme
Auswertung zum Versuch B04: Spezifische Wärme Alexander FufaeV Partner: Jule Heier Gruppe 254 Inhaltsverzeichnis 2. Bestimmung der Wärmekapazität C1 des blauen Dewargefäßes... 3 3. Bestimmung der Schmelzwärme
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie
 1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum 0. Übungsblatt zur Vorlesung hysikalische Chemie I SS 04 rof. Dr. Bartsch 0. L Die freie Standardreaktionsenthalpie der
Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum 0. Übungsblatt zur Vorlesung hysikalische Chemie I SS 04 rof. Dr. Bartsch 0. L Die freie Standardreaktionsenthalpie der
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludwigs-Uniersität Freiburg Lösungen zum 11. Übungsblatt zur Vorlesung Physikalische Chemie I SS 214 Prof. Dr. Bartsch 11.1 L a) Die Bildungsgeschwindigkeit on
Institut für Physikalische Chemie Albert-Ludwigs-Uniersität Freiburg Lösungen zum 11. Übungsblatt zur Vorlesung Physikalische Chemie I SS 214 Prof. Dr. Bartsch 11.1 L a) Die Bildungsgeschwindigkeit on
-Reaktionsordnung- Referat zur Vorlesung Reaktionsdynamik. 31. Oktober 2012 Nils Wilharm Reaktionsordnung Seite 1
 -Reaktionsordnung- Referat zur Vorlesung Reaktionsdynamik 31. Oktober 2012 Nils Wilharm Reaktionsordnung Seite 1 Reaktionsordnung Allgemeines Reaktionsgeschwindigkeit/-ordnung 0. Ordnung 1. Ordnung 2.
-Reaktionsordnung- Referat zur Vorlesung Reaktionsdynamik 31. Oktober 2012 Nils Wilharm Reaktionsordnung Seite 1 Reaktionsordnung Allgemeines Reaktionsgeschwindigkeit/-ordnung 0. Ordnung 1. Ordnung 2.
Stoffwechsel bei Mehlkäferlarven
 Stoffwechsel bei Mehlkäferlarven Franziskus Graber, Peter Bützer 1 Inhalt 1 Einleitung... 1 2 Warum gerade der Mehlwurm als Versuchstier?... 2 3 Das Experiment... 2 3.1 Einige Bilder von Mehlkäferlarven...
Stoffwechsel bei Mehlkäferlarven Franziskus Graber, Peter Bützer 1 Inhalt 1 Einleitung... 1 2 Warum gerade der Mehlwurm als Versuchstier?... 2 3 Das Experiment... 2 3.1 Einige Bilder von Mehlkäferlarven...
