II. Wämelehre. II.1 Temperatur Temperaturabhängigkeit von Stoffeigenschaften. Physik für Mediziner 1
|
|
|
- Hinrich Reuter
- vor 7 Jahren
- Abrufe
Transkript
1 II. Wämelehre II.1 Temperatur Temperaturabhängigkeit von Stoffeigenschaften Physik für Mediziner 1
2 Temperatur Temperatur ist ein alltäglicher Begriff; Wahrnehmung über die Haut als warm oder kalt physikalisch gesehen ist Temperatur eine makroskopische Zustandsgröße. Auf mikroskopischer Skala nur mittels Statistik für ein Ensemble von Teilchen definierbar. Brownsche Bewegung Beispiel: Brownsche Bewegung: ein Staubpartikel unter dem Mikroskop bewegt sich aufgrund von Stößen mit Atomen des umgebenden Mediums Die mittlere kinetische Energie der Atome / Moleküle definiert die Temperatur m k T Physik für Mediziner 2 E kin = 1 2 Boltzmann-Konstante v 2 = 3 2 k=1, J/K
3 Maxwellsche Geschwindigkeitsverteilung f(v) = 2 π m k T 3 2 v 2 e 2 m v 2 k T m = Masse T = Temperatur v = Geschwindigkeit k = Boltzmann-Konstante v W = 2 k T m wahrscheinlichste Geschwindigkeit v w Die Maxwellsche Geschwindigkeitsverteilung gibt die relativen Häufigkeiten für die verschiedenen Geschwindigkeiten an mittlere Geschwindigkeit: 8 k T v = W π m > v Physik für Mediziner 3
4 Die Existenz des absoluten Temperatur-Nullpunkts E kin = 1 m 2 v 2 k T die mittlere kinetische Energie der Atome / Moleküle kann nicht kleiner als Null werden. Wäre sie Null, dann würden alle Teilchen des Ensembles ruhen: absoluter Temperatur-Nullpunkt der absolute Temperatur-Nullpunkt liegt bei T= 0 K bzw. T=-273,15 0 C = K (Kelvin) bzw. Grad Celsius (0 0 C) sind die SI- Einheiten der Temperatur 3 2 in der Praxis wird die Temperatur mit Thermometern gemessen, die auf dem reproduzierbaren Temperaturverhalten von Stoffen beruhen. Phasenübergänge definieren Fixpunkte zur Temperatureichung Physik für Mediziner 4
5 Temperaturskalen Nach G. Fahrenheit (*1686, ) 0 0 F = Kältemischung (Salmiak/Wasser) F = Körpertemperatur benutzt in USA T[K] = T[ 0 C] Physik für Mediziner 5
6 Thermische Ausdehnung im Allgemeinen dehnen sich Stoffe (Festkörper, Flüssigkeiten und Gase) bei Erwärmung aus; die Längenänderung ΔL ist proportional zur ursprünglichen Länge L und zur Temperaturdifferenz ΔT: ΔL = α L Δ T α = Längenausdehnungskoeffizient Temp: T Temp: T+ΔT L 0 z.b. α Fe /K ΔL Längenänderung α Al = ΔL L Δ T = 3 0,9 10 m 5 = 2, ,5m 80 Physik für Mediziner 6
7 Längenausdehnung als technisches Problem Dehnungsfugen bei Brücken Eisenbahnschienen Öl-Pipeline Schon Temperaturschwankungen zwischen Sommer und Winter müssen bei technischen Anwendungen berücksichtigt werden Physik für Mediziner 7
8 Temperatureffekte Temperatureffekte, die zur Temperaturmessung eingesetzt werden die Dichte (fast) aller Stoffe nimmt mit der Temperatur ab, Ausnutzen der Längen oder Volumenänderung der elektrische Widerstand von Metallen nimmt mit der Temperatur zu Widerstandsthermometer der elektrische Widerstand Temperatur ab von Halbleitern nimmt mit der Auftreten von Thermospannungen Thermoelemente Wärmestrahlung Pyrometer Physik für Mediziner 8
9 Thermometerbauformen die thermische Ausdehnung lässt sich zur Konstruktion von Thermometern verwenden: Bi-Metall- Streifen Beispiele: Bi-Metall-Thermometer (2 Metalle mit unterschiedlichen Ausdehnungskoeffizienten) Quecksilber (Hg) - Thermometer Fieberthermometer (Ausdehnung einer Quecksilbersäule) Physik für Mediziner 9
10 Weitere Thermometer-Bauformen Thermoelement: verbindet man zwei verschiedene Metalldrähte miteinander, so entsteht eine Thermospannung, wenn die beiden Verbindungsstellen unterschiedliche Temperaturen haben. Die Spannung U ist der Temperaturdifferenz proportional Pyrometer: Thermoelement Jeder Gegenstand emittiert Infrarot- Strahlung, deren Intensität von der 4. Potenz seiner Temperatur abhängt: U T 1 ΔT = T 1 -T 2 T 2 Gesamtstrahlungsleistung P T 4 Physik für Mediziner 10
11 Anomalie des Wassers Dichte von Wasser ist bei 4 0 C am größten Eis hat eine kleinere Dichte als Wasser beides wichtig für Wasserfauna und -flora Physik für Mediziner 11
12 Temperaturverhalten von Gasen ein ideales Gas besteht aus punktförmigen Gasteilchen (Atomen, Molekülen), die elastisch miteinander und mit der Gefäßwand stoßen, aber sonst keine Kräfte untereinander ausüben beim Auftreffen eines Atoms/ Moleküls auf die Gefäßwand wird ein Impuls von 2 m v übertragen Kraftwirkung (zeitliche Impulsänderung) Druck = Kraft/ Fläche Modellgas Zurückführung der Wärmelehre (Thermodynamik) auf die Mechanik kinetische Gastheorie Physik für Mediziner 12
13 Ideale Gasgleichung eine Erhöhung der Temperatur entspricht einer Erhöhung der mittleren kinetischen Energie der Teilchen höhere Molekülgeschwindigkeit größerer Impulsübertrag auf Gefäßwand höherer Druck bei Temperaturerhöhung in einem konstanten Volumen steigt der Druck p V T ideale Gasgleichung: p V = n R T n ist die Stoffmenge, d.h. Zahl der Mole 1 Mol = Stoffmenge eines Elements oder einer chemischen Verbindung, die aus ebensoviel Teilchen besteht, wie Atome in 12g 12 C enthalten sind, nämlich N A =6, Teilchen ( N A = Avogadro-Zahl) 1 Mol entspricht der Stoffmenge von A g (A = atomare Masseneinheiten) R = 8,314 J mol -1 K -1 allgemeine Gaskonstante Physik für Mediziner 13
14 Das Gesetz von Boyle-Mariotte aus der idealen Gasgleichung folgt für konstante Temperatur T Gesetz von Boyle-Mariotte p V = n R T p V = const für T = const Das Produkt aus Druck p und Volumen V einer abgeschlossenen Gasmenge ist bei gleichbleibender Temperatur konstant p V=const Darstellung in einem p-v-diagramm p 1 V (mathematisch: Hyperbel) Physik für Mediziner 14
15 Ideale Gasgleichung weitere Schlussfolgerungen aus der idealen Gasgleichung n R p = T V p T für V = const p V = n R T n R V = p T V T für p =const Anwendung: Gasthermometer: durch Druckmessung kann bei konstantem Volumen die absolute Temperatur bestimmt werden ohne Eichpunkte wie siedendes oder gefrierendes Wasser; d.h. unabhängig von Materialeigenschaften!! Gesetz von Gay-Lussac Gasthermometer Physik für Mediziner 15
16 Wärme als Energieform werden 2 Körper mit unterschiedlicher Temperatur in Kontakt gebracht, so erfolgt ein Temperaturausgleich das System strebt ein thermisches Gleichgewicht an dabei erwärmt sich der kältere Körper und der wärme kühlt sich ab dies entspricht einer Erhöhung der mittleren kinetischen Energie der Moleküle des kälteren Körpers bei gleichzeitiger Absenkung der mittleren kinetischen Energie der Moleküle des wärmeren Körpers Energietransport vom wärmeren zum kälteren Körper: diese Form der Energie nennt man Wärmeenergie Physik für Mediziner 16
17 Äquivalenz von mechanischer und Wärmeenergie mechanische Energie lässt sich in Wärmeenergie umsetzen James Joule ( ) Wärmeäquivalent Robert Mayer ( ) Wärme als Energie lässt sich in andere Energieformen umwandeln: z.b. Dampfmaschine, Verbrennungsmotor (später) Vergleich: Erwärmung von 1 l Wasser (1kg) um 1 K erfordert 4186 J Heben von 1 kg um 1 m erfordert nur 9,81 J Physik für Mediziner 17
18 Unterschiede zwischen mechanischer und Wärmeenergie Arbeit entspricht einer gerichteten kinetischen Energie: bei Heben einer Last bewegen sich alle Moleküle in einer Richtung Wärmeenergie ist ungeordnete kinetische Energie der Moleküle statistische Beschreibung; anstatt mikroskopische Bewegungsgleichungen für jedes einzelne Molekül einer Substanz zu lösen, beschreibt man ihre makroskopischen Eigenschaften durch Zustandsgrößen wie Druck, Temperatur, Volumen entsprechend ihrem statistischen Charakter hat Wärmeenergie andere Eigenschaften als die bisher bekannten Energieformen obwohl Energieerhaltung strikt gilt, kann man nicht ohne weiteres Wärmeenergie vollkommen in mechanische Energie umwandeln: Beispiel: Stein fällt auf Boden und erwärmt sich bei Aufprall; kinetische Energie wird in Wärmeenergie umgewandelt. Der umgekehrte Prozess wird in der Natur nicht beobachtet: warmer Stein liegt auf Boden; springt plötzlich hoch und kühlt sich dabei ab Physik für Mediziner 18
19 Wärmekapazität und spezifische Wärme wird einer Substanz Wärmeenergie zugeführt, so steigt i.a. die Temperatur die für die Temperaturerhöhung ΔT notwendige Wärmenge Q ist proportional zu ΔT und zur Masse m der Substanz Q = c m Δ T c = spezifische Wärmekapazität Einheit: [c] = J kg-1 K-1 entsprechend wird die molare Wärmekapazität definiert: Q = cm n Δ T c m = molare Wärmekapazität (n = Zahl der Mole) Einheit: [c m ] = J mol-1 K-1 um 1 Gramm Wasser um 1 Grad zu erwärmen, benötigt man eine Wärmeenergie von 4,184 J historische Einheit für die Wärmemenge: Kalorie: 1 cal = 4,184 J (heute noch benutzt, um Verbrennungswerte bei Nahrungsmitteln anzugeben, meistens in kcal) Physik für Mediziner 19
20 Beispiel für spezifische Wärmen Wasser Stoff Wasser Wasser C [J/(kg C)] (flüssig) 4186 (Eis) 2100 (Dampf) 2010 Äthylalkohol 2400 Holz 1700 Aluminium 900 Marmor 860 Glas 840 Eisen 450 Kupfer 390 Silber 230 Beispiel: welche Wärmemenge ist notwendig, um 3 kg Kupfer um 20 Grad zu erwärmen? 1 1 Q = c m Δ T = 390 Jkg K 3kg 20K = J = 23,4 kj da nur die Temperaturdifferenz eingeht, spielt es keine Rolle, ob wir die Temperatur in Kelvin oder Celsius einsetzen Physik für Mediziner 20
21 Wärmekapazität von Gasen Druck p, Volumen V und Temperatur T eines Gases sind über die ideale Gasgleichung: p V = n R T verknüpft; d.h. bei Erwärmen des Gases (Zunahme von T) müssen V und/oder p zunehmen man unterscheidet deshalb 2 molare Wärmekapazitäten: ΔQ = cmp n Δ T; p = const c mp = molare Wärmekapazität des Gases bei konstantem Druck ΔQ = cm n Δ T; V = const V c mv = molare Wärmekapazität des Gases bei konstantem Volumen für ideale Gase gilt c mp > c mv, da bei konstantem Druck das Volumen größer werden muss; dazu muss Arbeit geleistet werden: c mp =c mv + R Physik für Mediziner 21
22 Wärmekapazität von Festkörpern bei Festkörpern (z.b. Kristallen) wird die zugeführte Wärmeenergie in Schwingungsenergie gespeichert bei hohen Temperaturen, d.h. wenn alle Gitterschwingungen thermisch angeregt werden können, ist die molare Wärmekapazität für die meisten Festkörper gleich: c m Physik für Mediziner 22 = 3R 25J mol 1 K Regel von Dulong-Petit 1 mikroskopische Erklärung: Atome sind im Gitter eingebunden; jedes Atom kann drei unabhängige Schwingungsmoden (entlang der x-, y-, z-achse) gegen die Nachbaratome ausüben; jede Schwingungsmode speichert die Energie von R T
23 Kalorimetrie Messung von Wärmekapazitäten bzw. Wärmemengen mit einem Kalorimeter Körper K der Masse M K und der Temperatur T K aber unbekannter Wärmekapazität c K wird in Wasser der Masse M W im Dewar D bei einer Temperatur T W geworfen: T W < T K ; Wärmekapazitäten c D und c W sind bekannt. es findet ein Temperaturausgleich statt (thermisches Gleichgewicht): es stellt sich eine Mischtemperatur T M ein: T W <T M < T K Körper K, Dewar D und Wasser bilden ein abgeschlossenes System: Energieerhaltung bei Wärmeaustausch ΔQK + ΔQW + ΔQD = von K abgegebene Wärmemenge 0 von Wasser und Dewar aufgenommene Wärme ( T T ) + c M ( T T ) + c M ( T T ) 0 ck MK K M W W W M D D W M = ( cw MW + cd MD ) ( TM TW ) M ( T T ) Physik für Mediziner 23 c K = K Kalorimeter K M
24 Reale Gase: Van der Waals Gleichung das Verhalten realer Gase weicht von dem idealer Gase bei tiefen Temperaturen und hohen Drucken ab; z.b. reale Gase lassen sich verflüssigen Ursachen: bisher vernachlässigt: Anziehungskräfte zwischen den Molekülen; Eigenvolumen der Moleküle 1.) anziehende Kräfte zwischen den Gasmolekülen verringern den Druck p, der nach außen wirkt; a p p + im Gas ist der Druck höher 2 V a beschreibt die Stärke der Anziehungskräfte 2.) das Eigenvolumen b der Moleküle verringert das zur Verfügung stehende Volumen: V V N b Die ideale Gasgleichung p V = n R T geht über in die van der Waals-Gleichung für reale Gase (für 1 Mol:) p + a V 2 A ( V N b) = R T A Physik für Mediziner 24
25 Reale Gase im p-v-diagramm oberhalb der kritischen Temperatur T kr lassen sich auch reale Gase nicht verflüssigen; n R T p = Isotherme wie bei idealen Gasen: V Kritische Daten: Van der Waals-Gleichung a p + 2 A V ( V N b) = R T unterhalb der kritischen Temperatur T kr: Verflüssigung für T<T kr : bei Volumenverkleinerung zunächst Kondensation: Mischphase flüssig + gasförming; bei weiterer Kompression: rein flüssige Phase; extremer Druckanstieg wegen Inkompressibilität der Flüssigkeit Physik für Mediziner 25
26 Phasenumwandlungen Zur Umwandlung zwischen Aggregatzuständen (fest, flüssig, gasförmig) muss der Materie Energie zugeführt oder entzogen werden um eine Flüssigkeit in ein Gas umzuwandeln, muss Energie aufgewendet werden, um die Kohäsionskräfte zwischen den Flüssigkeitsmolekülen zu überwinden; während des Phasenübergangs ändert sich die Temperatur nicht; die Energie wird benötigt, um die Trennung der Moleküle zu bewirken. Man spricht von latenter Wärme, weil die Wärmemenge nicht der Temperaturänderung dient sondern nur die innere Struktur ändert Physik für Mediziner 26
27 Kalorische Kurve von Wasser Phasenübergang: fest flüssig; schmelzen; zum Schmelzen von Wasser wird ohne dass sich dabei die Temperatur erhöht - eine Schmelzwärme von 333,5 kj/kg benötigt (1 atm Druck) Phasenübergang: flüssig gasförmig; verdampfen zum Verdampfen von Wasser wird ohne dass sich dabei die Temperatur erhöht - eine Verdampfungswärme von 2,26 MJ/kg benötigt (1 atm Druck) kalorische Kurve Wasser Physik für Mediziner 27
28 Koexistenzlinie: Sättigungsdampfdruck Thermodynamisches Gleichgewicht im geschlossenen System der leere Raum oberhalb der Flüssigkeit füllt sich mit Dampf im Gleichgewicht verdampfen genauso viele Moleküle aus der Flüssigkeit wie aus dem Dampf kondensieren Dampfdruck im Gleichgewicht = Sättigungsdampfdruck Der Sättigungsdampfdruck ist abhängig von der Temperatur Dampfdruck-Kurve Wasser Physik für Mediziner 28
29 Sieden und Verdunsten Sieden und Siedepunkt Der Siedevorgang findet bei einer Temperatur T s statt, bei der der Sättigungsdampfdruck gleich dem von außen auf der Flüssigkeit lastenden Luftdruck ist Sieden unter vermindertem Druck Verdunstung = Verdampfen einer Flüssigkeit, ohne dass der Sättigungsdampfdruck erreicht ist. Die zur Verdunstung notwendige Energie wird der Umgebung entzogen: Verdunstungskälte Verdunstungskälte Luftfeuchtigkeit = Verhältnis aus tatsächlichem Dampfdruck und dem Sättigungsdampfdruck Taupunkt = Temperatur, bei der sich bei plötzlicher Temperaturerniedrigung Kondensat in der Luft bildet (Nebel) Physik für Mediziner 29
30 Phasendiagramm eines Ein-Stoffsystems entlang der Phasengrenzen sind je 2 Phasen im Gleichgewicht am Tripelpunkt koexistieren alle 3 Phasen Physik für Mediziner 30
31 Sublimation Phasenübergang: gasförmig fest; sublimieren Entspannen eines Flüssigkeits-/Gas- Gemisches: CO 2 CO 2 -Schnee Physik für Mediziner 31
32 Wärmetransport Wärmeleitung: Wärmetransport vom wärmeren zum kälteren Körper durch Kontakt ohne Materialtransport Konvektion: Wärmetransport durch Materietransport Wärmestrahlung: alle Körper strahlen Wärmeenergie als elektromagnetische Strahlung ab (ohne Materietransport, auch im Vakuum) Physik für Mediziner 32
33 Wärmeleitung Wärmeleitung = Energietransport über einen Stab der Länge L, der im Kontakt mit zwei Wärmebädern auf unterschiedlichen Temperaturen T 1 und T 2 steht Wärmeleitungsgleichung: In der Zeit Δt transportierte Wärmemenge ΔQ =Wärmestrom ΔQ/Δt ΔQ Δ t = λ A L λ = materialspezifischer Wärmeleitungskoeffizient ( ) T 1 T 2 Geometrie Wärmeleitung Physik für Mediziner 33
34 Wärmekonvektion strömendes Gas oder strömende Flüssigkeit kann Wärme an einer Stelle aufnehmen und an einer anderen Stelle abgeben: Wärmetransport verbunden mit Materietransport Energietransport abhängig von Art, Geschwindigkeit und Wärmekapazität des strömenden Mediums Beispiele: Wind, Ventilator, Fön, Warmwasserheizung Wärmekonvektion Physik für Mediziner 34
35 Wärmestrahlung Alle Körper geben Energie in Form von Wärmestrahlung ab (elektromagnetische Wellen) Spektrale Verteilung: Plancksche Strahlungsgesetz: (Ursprung der Quantenphysik) integriert über alle Wellenlängen: Gesamtstrahlungsintensität: P = σ A T 4 (Stefan-Boltzmann Gesetz) Beispiele: Sonnenstrahlung, Pyrometer, Thermographie Wärmestrahlung Physik für Mediziner 35
36 Zusammenfassung Temperatur entspricht der kinetischen Energie der Atome/ Moleküle Temperaturmessung nutzt verschiedene thermische Effekte aus: thermische Ausdehnung, Änderung des elektrischen Widerstands, Wärmestrahlung ideale Gasgleichung: p V = n R T van der Waals Gleichung für reale Gase (Berücksichtigung der Wechselwirkung zwischen den Atomen und deren Eigenvolumen) a p + ( V NA b) = R T 2 V Zustandsänderungen von Stoffen bei Erwärmung: - Temperaturänderung proportional zur zugeführten Wärmemenge Proportionalitätskonstante: Wärmekapazität - bei Phasenübergängen wird zusätzliche Wärmemenge benötigt oder frei, da sich die Bindungen zwischen den Atomen ändern (latente Wärme) Wärmetransport durch Wärmeleitung, Konvektion, Wärmestrahlung Physik für Mediziner 36
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen!
 1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Temperatur. Temperaturmessung. Grundgleichung der Kalorik. 2 ² 3 2 T - absolute Temperatur / ºC T / K
 Temperatur Temperatur ist ein Maß für die mittlere kinetische Energie der Teilchen 2 ² 3 2 T - absolute Temperatur [ T ] = 1 K = 1 Kelvin k- Boltzmann-Konst. k = 1,38 10-23 J/K Kelvin- und Celsiusskala
Temperatur Temperatur ist ein Maß für die mittlere kinetische Energie der Teilchen 2 ² 3 2 T - absolute Temperatur [ T ] = 1 K = 1 Kelvin k- Boltzmann-Konst. k = 1,38 10-23 J/K Kelvin- und Celsiusskala
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
Vorlesung Physik für Pharmazeuten PPh Wärmelehre
 Vorlesung Physik für Pharmazeuten PPh - 07 Wärmelehre Aggregatzustände der Materie im atomistischen Bild Beispiel Wasser Eis Wasser Wasserdampf Dynamik an der Wasser-Luft Grenzfläche im atomistischen Bild
Vorlesung Physik für Pharmazeuten PPh - 07 Wärmelehre Aggregatzustände der Materie im atomistischen Bild Beispiel Wasser Eis Wasser Wasserdampf Dynamik an der Wasser-Luft Grenzfläche im atomistischen Bild
1. Wärmelehre 1.1. Temperatur Wiederholung
 1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
9. Thermodynamik. 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala. 9.4 Wärmekapazität
 9. Thermodynamik 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala 93 9.3 Thermische h Ausdehnung 9.4 Wärmekapazität 9. Thermodynamik Aufgabe: - Temperaturverhalten von Gasen,
9. Thermodynamik 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala 93 9.3 Thermische h Ausdehnung 9.4 Wärmekapazität 9. Thermodynamik Aufgabe: - Temperaturverhalten von Gasen,
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen
 Ferienkurs Experimentalphysik II Thermodynamik Grundlagen Lennart Schmidt 08.09.2011 Inhaltsverzeichnis 1 Grundlagen 3 1.1 Temperatur und Wärme............................ 3 1.2 0. und 1. Hauptsatz..............................
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen Lennart Schmidt 08.09.2011 Inhaltsverzeichnis 1 Grundlagen 3 1.1 Temperatur und Wärme............................ 3 1.2 0. und 1. Hauptsatz..............................
(VIII) Wärmlehre. Wärmelehre Karim Kouz WS 2014/ Semester Biophysik
 Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Physik I Mechanik und Thermodynamik
 Physik I Mechanik und hermodynamik 1 Einführung: 1.1 Was ist Physik? 1.2 Experiment - Modell - heorie 1.3 Geschichte der Physik 1.4 Physik und andere Wissenschaften 1.5 Maßsysteme 1.6 Messfehler und Messgenauigkeit
Physik I Mechanik und hermodynamik 1 Einführung: 1.1 Was ist Physik? 1.2 Experiment - Modell - heorie 1.3 Geschichte der Physik 1.4 Physik und andere Wissenschaften 1.5 Maßsysteme 1.6 Messfehler und Messgenauigkeit
Versuch 2. Physik für (Zahn-)Mediziner. c Claus Pegel 13. November 2007
 Versuch 2 Physik für (Zahn-)Mediziner c Claus Pegel 13. November 2007 1 Wärmemenge 1 Wärme oder Wärmemenge ist eine makroskopische Größe zur Beschreibung der ungeordneten Bewegung von Molekülen ( Schwingungen,
Versuch 2 Physik für (Zahn-)Mediziner c Claus Pegel 13. November 2007 1 Wärmemenge 1 Wärme oder Wärmemenge ist eine makroskopische Größe zur Beschreibung der ungeordneten Bewegung von Molekülen ( Schwingungen,
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Temperatur Der nullte Hauptsatz der Thermodynamik: Thermoskop und Thermometer Kelvin, Celsius- und der Fahrenheit-Skala Wärmeausdehnung
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Temperatur Der nullte Hauptsatz der Thermodynamik: Thermoskop und Thermometer Kelvin, Celsius- und der Fahrenheit-Skala Wärmeausdehnung
Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m
 GRATIS-Übungsdokument Gymnasium Klasse 8 Physik Thema: Mechanik, Wärmelehre, Elektrizitätslehre CATLUX de Energie Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m Energie ist gespeicherte
GRATIS-Übungsdokument Gymnasium Klasse 8 Physik Thema: Mechanik, Wärmelehre, Elektrizitätslehre CATLUX de Energie Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m Energie ist gespeicherte
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #10 30/10/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Thermisches Gleichgewicht Soll die Temperatur geändert werden, so muss dem System Wärme (kinetische
Physik für Mediziner im 1. Fachsemester #10 30/10/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Thermisches Gleichgewicht Soll die Temperatur geändert werden, so muss dem System Wärme (kinetische
Grund- und Angleichungsvorlesung Physik der Wärme.
 2 Grund- und Angleichungsvorlesung Physik. Physik der Wärme. WS 17/18 1. Sem. B.Sc. LM-Wissenschaften Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe
2 Grund- und Angleichungsvorlesung Physik. Physik der Wärme. WS 17/18 1. Sem. B.Sc. LM-Wissenschaften Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe
d) Das ideale Gas makroskopisch
 d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
Flüssigkeitsthermometer Bimetallthermometer Gasthermometer Celsius Fahrenheit
 Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
4.6.5 Dritter Hauptsatz der Thermodynamik
 4.6 Hauptsätze der Thermodynamik Entropie S: ds = dq rev T (4.97) Zustandsgröße, die den Grad der Irreversibilität eines Vorgangs angibt. Sie ist ein Maß für die Unordnung eines Systems. Vorgänge finden
4.6 Hauptsätze der Thermodynamik Entropie S: ds = dq rev T (4.97) Zustandsgröße, die den Grad der Irreversibilität eines Vorgangs angibt. Sie ist ein Maß für die Unordnung eines Systems. Vorgänge finden
Teilchenmodell: * Alle Stoffe bestehen aus Teilchen (Atomen, Molekülen). * Die Teilchen befinden sich in ständiger Bewegung.
 Teilchenmodell Teilchenmodell: * Alle Stoffe bestehen aus Teilchen (Atomen, Molekülen). * Die Teilchen befinden sich in ständiger Bewegung. *Zwischen den Teilchen wirken anziehende bzw. abstoßende Kräfte.
Teilchenmodell Teilchenmodell: * Alle Stoffe bestehen aus Teilchen (Atomen, Molekülen). * Die Teilchen befinden sich in ständiger Bewegung. *Zwischen den Teilchen wirken anziehende bzw. abstoßende Kräfte.
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen!
 1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
Grundlagen der Wärmelehre
 Ausgabe 2007-09 Grundlagen der Wärmelehre (Erläuterungen) Die Wärmelehre ist das Teilgebiet der Physik, in dem Zustandsänderungen von Körpern infolge Zufuhr oder Abgabe von Wärmeenergie und in dem Energieumwandlungen,
Ausgabe 2007-09 Grundlagen der Wärmelehre (Erläuterungen) Die Wärmelehre ist das Teilgebiet der Physik, in dem Zustandsänderungen von Körpern infolge Zufuhr oder Abgabe von Wärmeenergie und in dem Energieumwandlungen,
Ferienkurs Experimentalphysik 2
 Ferienkurs Experimentalphysik 2 Vorlesung 1 Thermodynamik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 13.09.2010 1 Allgemeines und Grundbegriffe Grundlegend für das nun folgende Kapitel Thermodynamik
Ferienkurs Experimentalphysik 2 Vorlesung 1 Thermodynamik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 13.09.2010 1 Allgemeines und Grundbegriffe Grundlegend für das nun folgende Kapitel Thermodynamik
ELEMENTE DER WÄRMELEHRE
 ELEMENTE DER WÄRMELEHRE 3. Elemente der Wärmelehre 3.1 Grundlagen 3.2 Die kinetische Gastheorie 3.3 Energieumwandlungen 3.4 Hauptsätze der Thermodynamik 2 t =? 85 ºC t =? 61.7 ºC Warum wird der Kaffe eigentlich
ELEMENTE DER WÄRMELEHRE 3. Elemente der Wärmelehre 3.1 Grundlagen 3.2 Die kinetische Gastheorie 3.3 Energieumwandlungen 3.4 Hauptsätze der Thermodynamik 2 t =? 85 ºC t =? 61.7 ºC Warum wird der Kaffe eigentlich
Energie und Energieerhaltung. Mechanische Energieformen. Arbeit. Die goldene Regel der Mechanik. Leistung
 - Formelzeichen: E - Einheit: [ E ] = 1 J (Joule) = 1 Nm = 1 Energie und Energieerhaltung Die verschiedenen Energieformen (mechanische Energie, innere Energie, elektrische Energie und Lichtenergie) lassen
- Formelzeichen: E - Einheit: [ E ] = 1 J (Joule) = 1 Nm = 1 Energie und Energieerhaltung Die verschiedenen Energieformen (mechanische Energie, innere Energie, elektrische Energie und Lichtenergie) lassen
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung
 Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Zwei neue Basisgrössen in der Physik
 Nachtrag zur orlesung am vergangenen Montag Zwei neue Basisgrössen in der Physik 9. Wärmelehre, kinetische Gastheorie Temperatur T: Wärme ist verknüpft mit ungeordneter Bewegung der Atome oder Moleküle.
Nachtrag zur orlesung am vergangenen Montag Zwei neue Basisgrössen in der Physik 9. Wärmelehre, kinetische Gastheorie Temperatur T: Wärme ist verknüpft mit ungeordneter Bewegung der Atome oder Moleküle.
Der Magnus-Effekt. Rotierender Körper in äußerer Strömung: Anwendungen:
 Der Magnus-Effekt Rotierender Körper in äußerer Strömung: Ohne Strömung: Körper führt umgebendes Medium an seinen Oberflächen mit Keine resultierende Gesamtkraft. ω Mit Strömung: Geschwindigkeiten der
Der Magnus-Effekt Rotierender Körper in äußerer Strömung: Ohne Strömung: Körper führt umgebendes Medium an seinen Oberflächen mit Keine resultierende Gesamtkraft. ω Mit Strömung: Geschwindigkeiten der
NTB Druckdatum: DWW
 WÄRMELEHRE Der Begriff der Thermisches Gleichgewicht und - Mass für den Wärmezustand eines Körpers - Bewegung der Atome starke Schwingung schwache Schwingung gleichgewicht (Thermisches Gleichgewicht) -
WÄRMELEHRE Der Begriff der Thermisches Gleichgewicht und - Mass für den Wärmezustand eines Körpers - Bewegung der Atome starke Schwingung schwache Schwingung gleichgewicht (Thermisches Gleichgewicht) -
Einführung in die Physik
 Einführung in die Physik für Pharmazeuten und Biologen (PPh) Mechanik, Elektrizitätslehre, Optik Übung : Vorlesung: Tutorials: Montags 13:15 bis 14 Uhr, Liebig-HS Montags 14:15 bis 15:45, Liebig HS Montags
Einführung in die Physik für Pharmazeuten und Biologen (PPh) Mechanik, Elektrizitätslehre, Optik Übung : Vorlesung: Tutorials: Montags 13:15 bis 14 Uhr, Liebig-HS Montags 14:15 bis 15:45, Liebig HS Montags
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Wärmelehre Wärme als Energie-Form
 Wärmelehre Wärme als Energie-Form Joule's Vorrichtung zur Messung des mechanischen Wärme-Äquivalents alte Einheit: 1 cal = 4.184 J 1 kcal Wärme erwärmt 1 kg H 2 O um 1 K Wird einem Körper mit der Masse
Wärmelehre Wärme als Energie-Form Joule's Vorrichtung zur Messung des mechanischen Wärme-Äquivalents alte Einheit: 1 cal = 4.184 J 1 kcal Wärme erwärmt 1 kg H 2 O um 1 K Wird einem Körper mit der Masse
II. Der nullte Hauptsatz
 II. Der nullte Hauptsatz Hauptsätze... - sind thermodyn. Gesetzmäßigkeiten, die als Axiome (Erfahrungssätze) formuliert wurden - sind mathematisch nicht beweisbar, basieren auf Beobachtungen und Erfahrungen
II. Der nullte Hauptsatz Hauptsätze... - sind thermodyn. Gesetzmäßigkeiten, die als Axiome (Erfahrungssätze) formuliert wurden - sind mathematisch nicht beweisbar, basieren auf Beobachtungen und Erfahrungen
2 Wärmelehre. Reibungswärme Reaktionswärme Stromwärme
 2 Wärmelehre Die Thermodynamik ist ein Musterbeispiel an axiomatisch aufgebauten Wissenschaft. Im Gegensatz zur klassischen Mechanik hat sie die Quantenrevolution überstanden, ohne in ihren Grundlagen
2 Wärmelehre Die Thermodynamik ist ein Musterbeispiel an axiomatisch aufgebauten Wissenschaft. Im Gegensatz zur klassischen Mechanik hat sie die Quantenrevolution überstanden, ohne in ihren Grundlagen
Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti.
 (c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 10. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
(c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 10. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
Tutorium Physik 1. Wärme
 1 Tutorium Physik 1. Wärme WS 15/16 1.Semester BSc. Oec. und BSc. CH 2 Themen 1. Einführung, Umrechnen von Einheiten / Umformen von Formeln 2. Kinematik, Dynamik 3. Arbeit, Energie, Leistung 4. Impuls
1 Tutorium Physik 1. Wärme WS 15/16 1.Semester BSc. Oec. und BSc. CH 2 Themen 1. Einführung, Umrechnen von Einheiten / Umformen von Formeln 2. Kinematik, Dynamik 3. Arbeit, Energie, Leistung 4. Impuls
Festkörper - System steht unter Atmosphärendruck gemessenen Wärmen erhalten Index p : - isoliert
 Kalorimetrie Mit Hilfe der Kalorimetrie können die spezifischen Wärmekapazitäten für Festkörper, Flüssigkeiten und Gase bestimmt werden. Kalorische Grundgleichung: ΔQ = c m ΔT Festkörper - System steht
Kalorimetrie Mit Hilfe der Kalorimetrie können die spezifischen Wärmekapazitäten für Festkörper, Flüssigkeiten und Gase bestimmt werden. Kalorische Grundgleichung: ΔQ = c m ΔT Festkörper - System steht
Tutorium Physik 1. Wärme.
 Tutorium Physik 1. Wärme. WS 18/19 1. Sem. B.Sc. Catering und Hospitality Services Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nicht-kommerziell Weitergabe unter gleichen
Tutorium Physik 1. Wärme. WS 18/19 1. Sem. B.Sc. Catering und Hospitality Services Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nicht-kommerziell Weitergabe unter gleichen
Physik für Nicht-Physikerinnen und Nicht-Physiker
 RUHR-UNIVERSITÄT BOCHUM FAKULTÄT FÜR PHYSIK UND ASTRONOMIE Physik für Nicht-Physikerinnen und Nicht-Physiker Prof. W. Meyer 5. Juni 2014 Wärmelehre Lernziele Alle Körper haben eine Temperatur Die Temperatur
RUHR-UNIVERSITÄT BOCHUM FAKULTÄT FÜR PHYSIK UND ASTRONOMIE Physik für Nicht-Physikerinnen und Nicht-Physiker Prof. W. Meyer 5. Juni 2014 Wärmelehre Lernziele Alle Körper haben eine Temperatur Die Temperatur
3.4 Änderung des Aggregatzustandes
 34 Änderung des Aggregatzustandes Man unterscheidet 3 Aggregatzustände: Fest Flüssig Gasförmig Temperatur: niedrig mittel hoch Molekülbindung: Gitter lose Bindung keine Bindung schmelzen sieden erstarren
34 Änderung des Aggregatzustandes Man unterscheidet 3 Aggregatzustände: Fest Flüssig Gasförmig Temperatur: niedrig mittel hoch Molekülbindung: Gitter lose Bindung keine Bindung schmelzen sieden erstarren
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases. f=5 Translation + Rotation. f=7 Translation + Rotation +Vibration. Wiederholung
 1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
Hydrodynamik: bewegte Flüssigkeiten
 Hydrodynamik: bewegte Flüssigkeiten Wir betrachten eine stationäre Strömung, d.h. die Geschwindigkeit der Strömung an einem gegebenen Punkt bleibt konstant im Laufe der Zeit. Außerdem betrachten wir zunächst
Hydrodynamik: bewegte Flüssigkeiten Wir betrachten eine stationäre Strömung, d.h. die Geschwindigkeit der Strömung an einem gegebenen Punkt bleibt konstant im Laufe der Zeit. Außerdem betrachten wir zunächst
Versuch Nr.53. Messung kalorischer Größen (Spezifische Wärmen)
 Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
Die 4 Phasen des Carnot-Prozesses
 Die 4 Phasen des Carnot-Prozesses isotherme Expansion: A B V V T k N Q ln 1 1 isotherme Kompression: adiabatische Kompression: adiabatische Expansion: 0 Q Q 0 C D V V T k N Q ln 2 2 S Q 1 1 /T1 T 1 T 2
Die 4 Phasen des Carnot-Prozesses isotherme Expansion: A B V V T k N Q ln 1 1 isotherme Kompression: adiabatische Kompression: adiabatische Expansion: 0 Q Q 0 C D V V T k N Q ln 2 2 S Q 1 1 /T1 T 1 T 2
Versuche: Brownsche Bewegung pneumatisches Feuerzeug Wärmekapazität gleicher Massen von verschiedenen Metallen
 14. Vorlesung EP II. Wärmelehre 1. Temperatur und Stoffmenge 11. Ideale Gasgleichung 1. Gaskinetik 13. Wärmekapazität Versuche: Brownsche Bewegung pneumatisches Feuerzeug Wärmekapazität gleicher Massen
14. Vorlesung EP II. Wärmelehre 1. Temperatur und Stoffmenge 11. Ideale Gasgleichung 1. Gaskinetik 13. Wärmekapazität Versuche: Brownsche Bewegung pneumatisches Feuerzeug Wärmekapazität gleicher Massen
8.4.5 Wasser sieden bei Zimmertemperatur ******
 8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
Experimentalphysik. Vorlesungsergänzung (VE), Wintersemester 2017 Modulnummer PTI 301
 Experimentalphysik Vorlesungsergänzung (VE), Wintersemester 2017 Modulnummer PTI 301 Experimentalphysik, Inhalt VE 2.1: Temperatur und Wärmeausdehnung VE 2.2: Zustandsgleichung idealer Gase VE 2.3: Erster
Experimentalphysik Vorlesungsergänzung (VE), Wintersemester 2017 Modulnummer PTI 301 Experimentalphysik, Inhalt VE 2.1: Temperatur und Wärmeausdehnung VE 2.2: Zustandsgleichung idealer Gase VE 2.3: Erster
Planungsblatt Physik für die 3B
 Planungsblatt Physik für die 3B Woche 20 (von 15.01 bis 19.01) Hausaufgaben 1 Bis Montag 22.01: Lerne die Notizen von Woche 20! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
Planungsblatt Physik für die 3B Woche 20 (von 15.01 bis 19.01) Hausaufgaben 1 Bis Montag 22.01: Lerne die Notizen von Woche 20! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
13.Wärmekapazität. EP Vorlesung 14. II) Wärmelehre
 13.Wärmekapazität EP Vorlesung 14 II) Wärmelehre 10. Temperatur und Stoffmenge 11. Ideale Gasgleichung 12. Gaskinetik 13. Wärmekapazität 14. Hauptsätze der Wärmelehre Versuche: Mechanisches Wärmeäquivalent
13.Wärmekapazität EP Vorlesung 14 II) Wärmelehre 10. Temperatur und Stoffmenge 11. Ideale Gasgleichung 12. Gaskinetik 13. Wärmekapazität 14. Hauptsätze der Wärmelehre Versuche: Mechanisches Wärmeäquivalent
Thermodynamik. Wechselwirkung mit anderen Systemen Wärme, Arbeit, Teilchen
 18a Temperatur 1 Thermodynamik Thermodynamik ist eine phänomenologische Wissenschaft Sie beschreibt die Wechselwirkung von Systemen mit ihrer Umgebung Aus der Erfahrung und durch zahllose Beobachtungen
18a Temperatur 1 Thermodynamik Thermodynamik ist eine phänomenologische Wissenschaft Sie beschreibt die Wechselwirkung von Systemen mit ihrer Umgebung Aus der Erfahrung und durch zahllose Beobachtungen
Musterlösung Thermodynamik 3 Besprechung in der Woche vom bis
 E2-E2p: Experimentalphysik 2 Prof. J. Lipfert SS 2018 Musterlösung 3 Musterlösung Thermodynamik 3 Besprechung in der Woche vom 30.04.18 bis 04.05.18 Anmerkung: Es wird jede Aufgabe bepunktet, nicht jede
E2-E2p: Experimentalphysik 2 Prof. J. Lipfert SS 2018 Musterlösung 3 Musterlösung Thermodynamik 3 Besprechung in der Woche vom 30.04.18 bis 04.05.18 Anmerkung: Es wird jede Aufgabe bepunktet, nicht jede
TEMPERATUR UND WÄRMEKAPAZITÄT... 2 KALORIMETRIE I... 3 KALORIMETRIE II... 5 PHASENUMWANDLUNGEN... 6
 E-Mail: Homepage: info@schroeder-doms.de schroeder-doms.de München den 11. Mai 2009 W1 Kalorimetrie (Skript zur Vorbereitung) TEMPERATUR UND WÄRMEKAPAZITÄT... 2 Wärme und Temperatur, Kelvin-Skala:... 2
E-Mail: Homepage: info@schroeder-doms.de schroeder-doms.de München den 11. Mai 2009 W1 Kalorimetrie (Skript zur Vorbereitung) TEMPERATUR UND WÄRMEKAPAZITÄT... 2 Wärme und Temperatur, Kelvin-Skala:... 2
Thermodynamik der Atmosphäre II
 Einführung in die Meteorologie Teil I Thermodynamik der Atmosphäre II Der erste Hauptsatz der Thermodynamik Die Gesamtenergie in einem geschlossenen System bleibt erhalten. geschlossen steht hier für thermisch
Einführung in die Meteorologie Teil I Thermodynamik der Atmosphäre II Der erste Hauptsatz der Thermodynamik Die Gesamtenergie in einem geschlossenen System bleibt erhalten. geschlossen steht hier für thermisch
Allgemeines Gasgesetz. PV = K o T
 Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
E2: Wärmelehre und Elektromagnetismus 6. Vorlesung 26.04.2018 Heute: - Kondensationskerne - Van der Waals-Gas - 2. Hauptsatz https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 26.04.2018 Prof.
Mechanik Akustik Wärme
 Mechanik Akustik Wärme Autoren Klaus Lüders Gebhard von Oppen 12., völlig neu bearbeitete Auflage W DE G Walter de Gruyter Berlin-New York 2008 Inhalt Einleitung 1 Teil I: Mechanik
Mechanik Akustik Wärme Autoren Klaus Lüders Gebhard von Oppen 12., völlig neu bearbeitete Auflage W DE G Walter de Gruyter Berlin-New York 2008 Inhalt Einleitung 1 Teil I: Mechanik
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas. Thermodynamik
 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - van der Waals-Gas https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert
E2: Wärmelehre und Elektromagnetismus 5. Vorlesung 23.04.2018 Heute: - Phasenübergänge - van der Waals-Gas https://xkcd.com/1561/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 23.04.2018 Prof. Dr. Jan Lipfert
Tutorium der Grund- und Angleichungsvorlesung Physik. Wärme.
 1 Tutorium der Grund- und Angleichungsvorlesung Physik. Wärme. WS 17/18 1. Sem. B.Sc. LM-Wissenschaften Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe
1 Tutorium der Grund- und Angleichungsvorlesung Physik. Wärme. WS 17/18 1. Sem. B.Sc. LM-Wissenschaften Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nichtkommerziell Weitergabe
Tutorium Physik 1. Wärme.
 1 Tutorium Physik 1. Wärme. WS 17/18 1. Sem. B.Sc. Catering und Hospitality Services Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nicht-kommerziell Weitergabe unter gleichen
1 Tutorium Physik 1. Wärme. WS 17/18 1. Sem. B.Sc. Catering und Hospitality Services Diese Präsentation ist lizenziert unter einer Creative Commons Namensnennung Nicht-kommerziell Weitergabe unter gleichen
Physikalische Chemie 1
 Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
Physikalische Chemie 1 Christian Lehmann 31. Januar 2004 Inhaltsverzeichnis 1 Einführung 2 1.1 Teilgebiete der Physikalischen Chemie............... 2 1.1.1 Thermodynamik (Wärmelehre)............... 2 1.1.2
Thermodynamik I. Sommersemester 2012 Kapitel 2, Teil 1. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 1: Übersicht 2 Zustandsgrößen 2.1 Thermische Zustandsgrößen 2.1.1 Masse und Molzahl 2.1.2 Spezifisches
Thermodynamik I Sommersemester 2012 Kapitel 2, Teil 1 Prof. Dr. Ing. Heinz Pitsch Kapitel 2, Teil 1: Übersicht 2 Zustandsgrößen 2.1 Thermische Zustandsgrößen 2.1.1 Masse und Molzahl 2.1.2 Spezifisches
Gesetz von Boyle. Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V.
 Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Kapitel IV Wärmelehre und Thermodynamik
 Kapitel IV Wärmelehre und Thermodynamik a) Definitionen b) Wärme und Wärmekapazität c) Das ideale Gas - makroskopisch d) Das reale Gas / Phasenübergänge e) Das ideale Gas mikroskopisch f) Hauptsätze und
Kapitel IV Wärmelehre und Thermodynamik a) Definitionen b) Wärme und Wärmekapazität c) Das ideale Gas - makroskopisch d) Das reale Gas / Phasenübergänge e) Das ideale Gas mikroskopisch f) Hauptsätze und
Physikalisches Praktikum I
 Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Fachbereich Physik Physikalisches Praktikum I W21 Name: Verdampfungswärme von Wasser Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Folgende Fragen
Thermodynamik (Wärmelehre) I Die Temperatur
 Physik A VL24 (04.12.2012) hermodynamik (Wärmelehre) I Die emperatur emperatur thermische Ausdehnung Festkörper und Flüssigkeiten Gase Das ideale Gas 1 Die emperatur Der Wärmezustand ist nicht mit bisherigen
Physik A VL24 (04.12.2012) hermodynamik (Wärmelehre) I Die emperatur emperatur thermische Ausdehnung Festkörper und Flüssigkeiten Gase Das ideale Gas 1 Die emperatur Der Wärmezustand ist nicht mit bisherigen
Physik für Biologen und Zahnmediziner
 Physik für Biologen und Zahnmediziner Kapitel 11: Wärmelehre Dr. Daniel Bick 13. Dezember 2017 Daniel Bick Physik für Biologen und Zahnmediziner 13. Dezember 2017 1 / 36 Übersicht 1 Wellen 2 Wärmelehre
Physik für Biologen und Zahnmediziner Kapitel 11: Wärmelehre Dr. Daniel Bick 13. Dezember 2017 Daniel Bick Physik für Biologen und Zahnmediziner 13. Dezember 2017 1 / 36 Übersicht 1 Wellen 2 Wärmelehre
Ideale Gase. Abb.1: Versuchsanordnung von Torricelli
 Ideale Gase 1 Empirische Gasgesetze, Einblick in die Geschichte der Naturwissenschaften. Wie hängt das Volumen eines Gases von Druck, Temperatur und Stoffmenge ab? Definition Volumen V: Das Volumen V ist
Ideale Gase 1 Empirische Gasgesetze, Einblick in die Geschichte der Naturwissenschaften. Wie hängt das Volumen eines Gases von Druck, Temperatur und Stoffmenge ab? Definition Volumen V: Das Volumen V ist
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #12 am 26.01.2007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #12 am 26.01.2007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
Planungsblatt Physik für die 3B
 Planungsblatt Physik für die 3B Woche 24 (von 12.02 bis 16.02) Hausaufgaben 1 Bis Montag 19.02: Lerne die Notizen von Woche 24! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
Planungsblatt Physik für die 3B Woche 24 (von 12.02 bis 16.02) Hausaufgaben 1 Bis Montag 19.02: Lerne die Notizen von Woche 24! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
Physik für Biologen und Zahnmediziner
 Physik für Biologen und Zahnmediziner Kapitel 12: Wärmelehre Dr. Daniel Bick 09. Dezember 2016 Daniel Bick Physik für Biologen und Zahnmediziner 09. Dezember 2016 1 / 35 Übersicht 1 Wellen 2 Wärmelehre
Physik für Biologen und Zahnmediziner Kapitel 12: Wärmelehre Dr. Daniel Bick 09. Dezember 2016 Daniel Bick Physik für Biologen und Zahnmediziner 09. Dezember 2016 1 / 35 Übersicht 1 Wellen 2 Wärmelehre
oder 10 = 1bar = = 10 Pa Für viele Zwecke wird die Umrechnung 1bar = 10 verwendet.
 R. Brinkmann http://brinkmann-du.de Seite 1 5.11.013 HF14S Arbeitsblatt Wärme als Energieform Die Celsius-Skala ist durch folgende Fixpunkte definiert: 0 0 C: Schmelzpunkt des Eises bei einem Druck von
R. Brinkmann http://brinkmann-du.de Seite 1 5.11.013 HF14S Arbeitsblatt Wärme als Energieform Die Celsius-Skala ist durch folgende Fixpunkte definiert: 0 0 C: Schmelzpunkt des Eises bei einem Druck von
11. Wärmetransport. und Stoffmischung. Q t. b) Wärmeleitung (ohne Materietransport)
 11. Wärmetransport und Stoffmischung b) Wärmeleitung (ohne Materietransport) Wärme(energie) Q wird durch einen Wärmeleiter (Metall) der Querschnittsfläche A vom wärmeren zum kälteren transportiert, also
11. Wärmetransport und Stoffmischung b) Wärmeleitung (ohne Materietransport) Wärme(energie) Q wird durch einen Wärmeleiter (Metall) der Querschnittsfläche A vom wärmeren zum kälteren transportiert, also
Einleitung in die Wärmelehre
 Einleitung in die Wärmelehre Im ersten Teil der Experimentalphysik, Mechanik, haben wir die Grundlagen geschaffen, Bewegung von einzelnen Massepunkten und später von starren Körpern zu berechnen. Wir hatten
Einleitung in die Wärmelehre Im ersten Teil der Experimentalphysik, Mechanik, haben wir die Grundlagen geschaffen, Bewegung von einzelnen Massepunkten und später von starren Körpern zu berechnen. Wir hatten
Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol
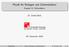
![Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol Molzahl: n = N/N A [n] = mol N ist die Anzahl der Atome oder Moleküle des Stoffes. Molmasse oder Molekularmasse: M [M ]= kg/kmol](/thumbs/50/26795947.jpg) 2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
2. Zustandsgrößen 2.1 Die thermischen Zustandsgrößen 2.1.1. Masse und Molzahl Reine Stoffe: Ein Mol eines reinen Stoffes enthält N A = 6,02214. 10 23 Atome oder Moleküle, N A heißt Avogadro-Zahl. Molzahl:
Modelle zur Beschreibung von Gasen und deren Eigenschaften
 Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
15. Wärmetransport. Q t. b) Wärmeleitung (ohne Materietransport)
 16. Vorlesung EP II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenü (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
16. Vorlesung EP II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenü (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Physik I TU Dortmund WS2017/18 Gudrun Hiller Shaukat Khan Kapitel 6
 Physik I TU Dortmund WS07/8 Gudrun Hiller Shaukat Khan Kapitel 6 Zustandsdiagramm Zustandsgrößen eines Gases sind z.b. Druck p, Temperatur T, Volumen V und Molzahl n (Stoffmenge). Thermodynamische Prozesse
Physik I TU Dortmund WS07/8 Gudrun Hiller Shaukat Khan Kapitel 6 Zustandsdiagramm Zustandsgrößen eines Gases sind z.b. Druck p, Temperatur T, Volumen V und Molzahl n (Stoffmenge). Thermodynamische Prozesse
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang lektrotechnik - kinetische Gastheorie - Prof. Dr. Ulrich Hahn WS 008/09 Molekularbewegung kleine sichtbare Teilchen in Flüssigkeiten oder Gasen: unregelmäß äßige Zitterbewegung
Physik III im Studiengang lektrotechnik - kinetische Gastheorie - Prof. Dr. Ulrich Hahn WS 008/09 Molekularbewegung kleine sichtbare Teilchen in Flüssigkeiten oder Gasen: unregelmäß äßige Zitterbewegung
( ) ( ) J =920. c Al. m s c. Ü 8.1 Freier Fall
 Ü 8. Freier Fall Ein Stück Aluminium fällt aus einer Höhe von z = 000 m auf den Erdboden (z = 0). Die Luftreibung wird vernachlässigt und es findet auch kein Energieaustausch mit der Umgebung statt. Beim
Ü 8. Freier Fall Ein Stück Aluminium fällt aus einer Höhe von z = 000 m auf den Erdboden (z = 0). Die Luftreibung wird vernachlässigt und es findet auch kein Energieaustausch mit der Umgebung statt. Beim
Thermodynamik Thermodynamische Systeme
 Thermodynamik Thermodynamische Systeme p... Druck V... Volumen T... Temperatur (in Kelvin) U... innere Energie Q... Wärme W... Arbeit Idealisierung; für die Betrachtung spielt die Temperatur eine entscheidende
Thermodynamik Thermodynamische Systeme p... Druck V... Volumen T... Temperatur (in Kelvin) U... innere Energie Q... Wärme W... Arbeit Idealisierung; für die Betrachtung spielt die Temperatur eine entscheidende
Thermodynamik (Wärmelehre) III kinetische Gastheorie
 Physik A VL6 (07.1.01) Thermodynamik (Wärmelehre) III kinetische Gastheorie Thermische Bewegung Die kinetische Gastheorie Mikroskopische Betrachtung des Druckes Mawell sche Geschwindigkeitserteilung gdes
Physik A VL6 (07.1.01) Thermodynamik (Wärmelehre) III kinetische Gastheorie Thermische Bewegung Die kinetische Gastheorie Mikroskopische Betrachtung des Druckes Mawell sche Geschwindigkeitserteilung gdes
Physik 1 für Chemiker und Biologen 13. Vorlesung
 Physik 1 für Chemiker und Biologen 13. Vorlesung 30.01.2017 Diese Woche (30.1.-3.2.): Vorlesung heute: o Thermodynamik & statistische Physik o Kurzer Ausblick: Spezielle Relativitätstheorie Übungen: Besprechung
Physik 1 für Chemiker und Biologen 13. Vorlesung 30.01.2017 Diese Woche (30.1.-3.2.): Vorlesung heute: o Thermodynamik & statistische Physik o Kurzer Ausblick: Spezielle Relativitätstheorie Übungen: Besprechung
Carnotscher Kreisprozess
 Carnotscher Kreisprozess (idealisierter Kreisprozess) 2 p 1, V 1, T 1 p(v) dv > 0 p 2, V 2, T 1 Expansionsarbeit wird geleistet dq fließt aus Wärmebad zu dq > 0 p 2, V 2, T 1 p(v) dv > 0 p 3, V 3, T 2
Carnotscher Kreisprozess (idealisierter Kreisprozess) 2 p 1, V 1, T 1 p(v) dv > 0 p 2, V 2, T 1 Expansionsarbeit wird geleistet dq fließt aus Wärmebad zu dq > 0 p 2, V 2, T 1 p(v) dv > 0 p 3, V 3, T 2
E2: Wärmelehre und Elektromagnetismus 3. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 3. Vorlesung 16.04.2018 https://xkcd.com/1978/ Heute: - Gleichverteilungssatz - 1. Hauptsatz - Volumenarbeit - Wärmekapazität - Wärmekapazität des idealen Gases -
E2: Wärmelehre und Elektromagnetismus 3. Vorlesung 16.04.2018 https://xkcd.com/1978/ Heute: - Gleichverteilungssatz - 1. Hauptsatz - Volumenarbeit - Wärmekapazität - Wärmekapazität des idealen Gases -
Beispiel für ein thermodynamisches System: ideales Gas (Edelgas)
 10. Hauptsätze tze der Wärmelehre Thermodynamik: zunächst: Klassische Mechanik punktförmiger Teilchen, starrer und deformierbarer Körper aber: Bewegungsgleichungen für N=10 23 Teilchen mit 6N ariablen
10. Hauptsätze tze der Wärmelehre Thermodynamik: zunächst: Klassische Mechanik punktförmiger Teilchen, starrer und deformierbarer Körper aber: Bewegungsgleichungen für N=10 23 Teilchen mit 6N ariablen
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik -. Hauptsatz der Thermodynamik - Prof. Dr. Ulrich Hahn WS 2008/09 Energieerhaltung Erweiterung des Energieerhaltungssatzes der Mechanik Erfahrung: verschiedene
Physik III im Studiengang Elektrotechnik -. Hauptsatz der Thermodynamik - Prof. Dr. Ulrich Hahn WS 2008/09 Energieerhaltung Erweiterung des Energieerhaltungssatzes der Mechanik Erfahrung: verschiedene
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
Physik für Pharmazeuten WÄRME I. Wärmeenergie und Temperatur Beschreibung des Zustands von Gasen Wärmekapazität
 Physik für Pharmazeuten WÄRME I Wärmeenergie und Temperatur Beschreibung des Zustands von Gasen Wärmekapazität wozu Wärmelehre? Temperatur bin ich mittags größer als am morgen? wieso wird Sodaflasche kalt,
Physik für Pharmazeuten WÄRME I Wärmeenergie und Temperatur Beschreibung des Zustands von Gasen Wärmekapazität wozu Wärmelehre? Temperatur bin ich mittags größer als am morgen? wieso wird Sodaflasche kalt,
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #4 am 3.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E43, Tel. 888-5875,
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #4 am 3.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E43, Tel. 888-5875,
