Kernmagnetische Resonanz
|
|
|
- Johannes Friedrich
- vor 7 Jahren
- Abrufe
Transkript
1 Strahlung Kernmagnetische Resonanz Die verschiedenen Arten der Spektroskopie nutzen die Adsorption, Emission oder Streuung von Strahlen an Atomen oder Molekülen. Die Kernresonanzspektroskopie im speziellen nutzt die Möglichkeit Kernspins mit Hilfe von Radiowellen zu Übergängen anzuregen, also ihre Orientierung umzukehren. λ km m cm mm mm nm nm pm lg ν in Hz Radiowellen Mikro wellen Fern IR Nah IR UV VIS Vak UV Röntgen- und Gammastrahlen Kernspin-Übergänge Rotationen, Schwingungen Elektronenspinübergänge Elektronenübergänge Photoelektronen Mit Hilfe der Kernresonanzspektroskopie lassen sich Aussagen über die Umgebung und die Struktur von einzelnen Atomgruppen in einem Molekül machen. Das Prinzip, auf dem alle spektroskopischen Methode beruhen, ist dass Strahlung nur in diskreten Portionen, den Quanten, absorbiert oder emittiert werden kann. Die dazu notwendige Energie E, die Frequenz ν der Strahlung sowie deren Wellenlänge λ hängen mit dem Planckschen Wirkungsquantum h und der Lichtgeschwindigkeit c wie folgt zusammen: E = h ν = h c λ 1 = h c ν Die Wellenzahl ν ist als Kehrwert der Wellenlänge λ definiert. Die Energie der Strahlung nimmt mit steigender Frequenz und Wellenzahl zu, dabei sinkt jedoch die Wellenlänge. Durch die Absorption eines Strahlungsquants wird dem Molekül Energie zugeführt und vom Grundzustand E 0 in einen zeitlich begrenzten, angeregten Zustand E 1 versetzt. Ein Spektrometer misst diese Absorption, indem es den aus der Probe austretenden Strahl mit einem Referenzstrahl vergleicht und die Abweichung als Peak in einem Diagramm darstellt. Download von 1 by Benjamin Bulheller & Frank Bock
2 Kernresonanz und Zeeman-Effekt Verfügt ein Atomkern über eine gerade Anzahl an Protonen und eine gerade Anzahl an Neutronen, so besitzt er kein magnetisches Moment (z.b. 12 C, 16 O) und ist NMR-inaktiv. Ist jedoch eine dieser Zahlen ungerade, besitzt er eine halbzahlige Kernspinquantenzahl I und damit ein magnetisches Moment µ (z.b. 1 H, 13 C, 15 N, 19 F). Sind sowohl Protonenzahl als auch Neutronenzahl gerade, so ist I ganzzahlig (z.b. 2 H, 6 Li, 14 N) und der Kern ist wiederum NMR-inaktiv. Das magnetisches Moment µ eines Kerns lässt sich über folgende Formel berechnen: I I K ( ) µ = g µ I I+ 1 Hierbei ist I die Kernspinquantenzahl und g I der Kern-g-Faktor (eine stoffspezifische Konstante). Das Kernmagneton µ K ist eine Konstante die sich über die Elementarladung, das Plancksche Wirkungsquantum h und die Masse eines Protons errechnen lässt: h µ K = em P = em P 2 π Ein Atomkern mit einem magnetischen Moment µ verhält sich so, als hätte er einen Eigendrehimpuls p oder auch Kernspin. Man kann ihn als kleinen Stabmagneten ansehen, der sich in einem angelegten Magnetfeld in zwei mögliche Orientierungen ausrichten kann, parallel oder antiparallel. Bringt man einen Kern mit Eigendrehimpuls in ein homogenes, statisches Magnetfeld B 0, so erfolgt also eine Richtungsquantelung des Drehimpulses. Die Atome präzessieren mit der Larmorfrequenz ω um die Achse des Magnetfeldes, die Größe des Winkels α (und damit diejenige der Präzession) hängt von der Kernspinquantenzahl des Atoms und vom angelegten Magnetfeld ab. Die potentielle Energie des magnetischen Momentes ist bei der parallelen Ausrichtung am geringsten. Wird ein solcher Kern mit einer bestimmten Energie E = h ν bestrahlt, so kann er durch deren Absorption vom energieärmeren Zustand in den angeregten Zustand übergehen, seine Orientierung in die antiparallele Ausrichtung ändern. Diese Absorption ist die Kernspinresonanz. Sie tritt dann ein, wenn die eingestrahlte Frequenz mit der Frequenz der Präzessionsbewegung übereinstimmt, dann erfolgt eine Umorientierung der Kerne. 1 H präzessiert in einem Magnetfeld von 1.45 Tesla beispielsweise mit 60 MHz. Für eine bestimmte Kernsorte mit dem spezifischen magnetogyrischen Verhältnis γ I lautet die Resonanzbedingung im statischen Magnetfeld B 0 : γ ν = B 2π I 0 0 Download von 2 by Benjamin Bulheller & Frank Bock
3 Der Drehimpulsvektor p der magnetischen Kernmomente (rote Pfeile) nimmt einen bestimmten Winkel α zur Richtung des Magnetfeldes B ein (Richtungsquantelung). Für die Komponente des Vektors p in Feldrichtung gilt quantitativ: p Z = m I m I ist die magnetische Kernspinquantenzahl oder auch Orientierungsquantenzahl. Sie kann folgende Werte annehmen: mi = I, I 1,..., (I 1), I Energetisch gesehen, bedeutet die Ausrichtung des Kernes eine Aufspaltung in Energieniveaus. Diese Aufspaltung ist der Zeeman-Effekt. Es ergeben sich (2 I + 1) Kern-Zeeman-Niveaus. Für die Energie der einzelnen Niveaus gilt: E = g µ m B mi I I K I 0 Die Resonanzbedingung für Übergänge zwischen Energieniveaus lautet aufgrund der Auswahlregel m I = ±1 (es sind nur Übergänge zu benachbarten Zuständen erlaubt): E= h ν 0 = gi µ K B0 Die Energiedifferenz ist also unabhängig von der magnetischen Kernspinquantenzahl. Aus dieser Beziehung lassen sich die Resonanzfrequenz ν 0 und die Larmorfrequenz ω 0 bestimmen: g ν = 0 µ B h I K 0 ν ω = =γ B 2π 0 0 I 0 mit γ I als magnetogyrisches Verhältnis, eine stoffspezifische Konstante. Download von 3 by Benjamin Bulheller & Frank Bock
4 Chemische Verschiebung Aus den vorangegangenen Berechnungen ließe sich schließen, dass alle gleichen Kerne nur ein NMR Signal ergeben. Dies ist aber nicht der Fall, da jeder Kern durch die Elektronenhüllen seiner Umgebung ein anderes Magnetfeld erfährt. Am Kernort gilt demnach die effektive Magnetfeldstärke B loc, die sich von dem äußeren Magnetfeld B 0 aufgrund von Abschirmungseffekten unterscheidet. Die Elektronenhüllen, die den Kern umgeben, induzieren das Magnetfeld B ind, das aufgrund der Lenz schen Regel dem äußeren Magnetfeld entgegengerichtet ist. Der Proportionalitätsfaktor ist die Abschirmungskonstante σ: Bloc = B0 Bind = B0 σ B0 = B 0 (1 σ ) Für die Resonanzbedingung gilt nun: γi ν 0 = B0 1 σ 2π ( ) Es gilt also für jede Kernsorte eine separate effektive Magnetfelddichte. Der Begriff Kernsorte umfasst gleiche Atome mit gleicher Umgebung, Protonen in Nachbarschaft einer Hydroxylgruppe verhalten sich anders, als solche in der Nähe einer Methylgruppe. Je stärker ein Kern durch benachbarte Elektronenhüllen abgeschirmt ist (also je größer σ ist), desto kleiner wird sein lokales Magnetfeld B loc und desto größer muss daher das angelegte Feld B 0 sein um den Kern zur Resonanz zu bringen. Da die Flussdichte im Diagramm nach rechts ansteigt, stehen die am besten abgeschirmten Kerne rechts. Je mehr elektronenziehende (also entschirmende) Gruppen in ihrer Nähe sind, desto weiter wandern die Peaks nach links. Damit man Spektren unabhängig von der Messfrequenz und der Magnetfeldstärke vergleichen kann, verwendet man die chemische Verschiebung δ, zu deren Bestimmung man sich auf ein Referenzsignal bezieht: ν ν Probe Referenz δ= νmessfrequenz 10 6 Die Referenzsubstanz erhält definitionsgemäß δ = 0. Meist wird TMS (Tetramethylsilan) verwendet. Die 12 Wasserstoffatome des Moleküls besitzen alle exakt die gleiche Nachbarschaft, es resultiert also nur ein Peak. Da die Resonanzfrequenz mit der angelegten Magnetfeldstärke variiert, dividiert man durch die Spektrometerfrequenz. Diese ist zur Feldstärke proportional, man erhält also unabhängig vom angelegten Feld und der Messfrequenz vergleichbare Werte. Abschirmung σ magnetische Flussdichte B Frequenz in Hz chemische Verschiebung δ Download von 4 by Benjamin Bulheller & Frank Bock
5 Spin Spin Kopplung Ein weiterer zur Strukturaufklärung genutzter Effekt ist die Spin-Spin-Kopplung. In den Spektren treten Feinstrukturen, sogenannte Multipletts, auf. Ursache dieser Aufspaltung ist die Wechselwirkung mit Nachbarkernen, die ebenfalls ein magnetisches Moment besitzen. Die Kerne koppeln miteinander, d.h. ihre Spinorientierungen beeinflussen gegenseitig ihre lokalen Magnetfelder. Zur quantitativen Beschreibung der Spin-Spin- Kopplung dient die Kopplungskonstante J, die unabhängig von der äußeren Magnetfeldstärke ist. Die Anzahl der Signale eines Multipletts wird durch die Multiplizität M beschrieben: M = 2 n I+ 1 Die Intensitätsverteilung entspricht den Koeffizienten der Binominalreihe (Pascalsches Dreieck). In der Tabelle ist n die Anzahl der Nachbarn und n + 1 die relativen Intensitäten der Aufspaltungen: n Linienzahl n Singulett 1 1 Dublett Triplett Quartett Quintett Sind beispielweise 3 koppelnde Nachbarkerne vorhanden spaltet das Signal in ein Quartett auf mit den Verhältnissen 1 : 3 : 3 : 1. Dieses Verhältnis lässt sich auch aus den möglichen Spinanordnungen ablesen: 1 : 3 : 3 : 1 Die Abstände zwischen den Peaks entsprechen der Kopplungskonstante J. Sie ist ein Maß für die Energieaufspaltung. Die Fläche unter der Absorptionskurve macht eine Aussage über die Anzahl der absorbierenden Protonen. Diese kann durch Integration ermittelt werden, welche vom NMR-Spektrometer in Form einer Stufenkurve geliefert wird. Da die Peaks sehr schmal sind kann man näherungsweise die Höhe als Maß für die Protonenanzahl ansehen. Die Peakgruppe von vier Protonen eines Moleküls ist im Verhältnis in etwa doppelt so hoch wie die Peakgruppe von zwei Protonen im selben Molekül. Download von 5 by Benjamin Bulheller & Frank Bock
6 Fourier-Transformation Es gibt prinzipiell zwei Möglichkeiten ein NMR Spektrum aufzunehmen: Continuous Wave (CW): Hier wird entweder der mögliche Magnetfeldbereich (field sweep) oder das Frequenzspektrum (frequency sweep) durchlaufen. Die Auftragung der Intensität I gegen die Frequenz ν nennt man Frequenz Domäne. Fourier Transformation (FT): Hierbei werden alle Frequenzen gleichzeitig in einem Schuss gemessen. Das geht wesentlich schneller und liefert ein Interferogramm der Frequenzen. Die Auftragung der Intensität I gegen die Zeit t nennt man Zeit Domäne. Um von der wenig aussagekräftigen Zeit-Domäne zur Frequenz Domäne zu gelangen, muss die Fourier Transformation durchgeführt werden: + iωt FT : f ( ν ) = f (t) e dt Diese Rechnung wird heutzutage vom Computer übernommen, so dass nach einer Messung in der Zeit Domäne das Spektrum sofort in der gewohnten Auftragung der Intensität gegen die Frequenz erhalten werden kann. Download von 6 by Benjamin Bulheller & Frank Bock
7 NMR Spektren NMR Spektren Wie bereits erwähnt, erfolgt üblicherweise die Auftragung der Stärke der Resonanz gegen die chemische Verschiebung in ppm. Das 1 H-Spektrum der Essigsäure zeigt recht anschaulich den Einfluss der chemischen Umgebung auf die Resonanzfrequenz eines Kerns. Das Proton der Carboxylgruppe ist durch die hohe Elektronegativität der Sauerstoffatome, welche die Elektronenwolken in ihrem Umkreis anziehen, stark entschirmt. Daher tritt es bereits bei einer geringen Magnetfeldstärke in Resonanz und es ergibt sich eine größere chemische Verschiebung bei einer höheren Frequenz. Der Peak erscheint also relativ weit links im Spektrum. Die Protonen der Methylgruppe sind weit weniger gut abgeschirmt und verursachen daher eine geringere Verschiebung von nur 2 im Verhältnis zu 11.5 des Carboxylprotons. Da in der Methylgruppe 3 Protonen in Resonanz treten ist der Peak entsprechend größer als derjenige der Säuregruppe. Die Sauerstoffatome wirken außerdem als Puffer, so dass es zu keiner Kopplung zwischen den Wasserstoffatomen kommt. Das Spektrum des Diethylethers zeigt deutlich die Auswirkung der Spin-Spin-Kopplung in einem Molekül. Die beiden Methylgruppen sind chemisch äquivalent, ebenso wie die CH 2 -Gruppen, da sie sich durch Symmetrieoperationen (hier eine einfach Spiegelung am Sauerstoffatom) ineinander überführen lassen, bzw. einfacher ausgedrückt, die gleich Nachbarschaft haben. Chemisch äquivalente Atome treten bei der selben Frequenz in Resonanz. Die Methylgruppe hat zwei Nachbaratome (die Protonen der Methylengruppe), es erfolgt also eine Aufspaltung in ein Triplett mit den Verhältnissen 1 : 2 : 1. Die Methylengruppe selbst koppelt mit den 3 Protonen der Methylgruppe, wodurch eine Signalaufspaltung in ein Quartett mit den Verhältnissen 1 : 3 : 3 : 1 erfolgt. Das die Methylengruppen durch das zentrale Sauerstoffatom entschirmt werden, erscheint der Peak bei einer geringeren Feldstärke als derjenige der Methylgruppe. Die Größe der Peakgruppen gibt einen Hinweis auf die Anzahl der koppelnden Protonen und besitzt in etwa das Verhältnis 2 : 3 (bzw. 4 : 6 oder 8 : 12). Die Höhe der Peaks mit derselben Größe ist durch den sogenannten Dacheffekt leicht in Richtung der koppelnden Gruppe hin abgeschrägt. Download von 7 by Benjamin Bulheller & Frank Bock
8 Auswertung Auswertung Aufgabe 1 Zeichnen Sie die bei geringer Auflösung (das heißt ohne Aufspaltungen) zu erwartenden NMR-Spektren der folgenden Verbindungen. Berücksichtigen Sie alle NMR-aktiven Kerne. Die Stärke des externen Magnetfeldes betrage T. a) Chloroform CHCl 3 : b) Freon 11 CFCl 3 : c) Halothan CF 3 CHClBr: Würde man die Spektren bei 8.46 T aufnehmen, wären alle Frequenzen um den Faktor 4 größer, der 1 H-Kern würde erst bei 360 MHz in Resonanz treten. Download von 8 by Benjamin Bulheller & Frank Bock
9 Fehlerbetrachtung Aufgabe 2 Wie würden die Spektren a bis c aussehen, wenn ein hochauflösendes Spektrum aufgenommen werden würde? Es verändert sich lediglich das Spektrum von Halothan, da es zwei unterschiedliche Kohlenstoffatome enthält und dadurch zwei 13 C-Peaks direkt nebeneinander auftreten würden. Fehlerbetrachtung Da die Universität Würzburg im Hinblick auf die immer knappen Finanzen davon abgesehen hat, unwissende und minder begabte Studenten an Geräte heranzulassen, deren Gesamtwert empfindlich im sechsstelligen Bereich und damit jenseits des Jahreseinkommens eines Normalsterblichen liegt, erfolgte die Messung anhand der Aufgabenstellung des Vollhardts. Messfehler und Ungenauigkeiten beim Einfüllen der Probe sind daher weitestgehend ausgeschlossen. Als gravierendste Fehlerquelle sind der Autor des Arbeitsbuches, Neil E. Shore, sowie der Korrekturleser des Manuskripts zu nennen. Ein weiteres Problem stellen die Übersetzer der Werkes, Eduard Krahé und Nicole Kindler dar, ein Vergleich mit der eiligst hinzugezogenen Originalausgabe des Werkes zeigte jedoch eine hundertprozentige Übereinstimmung, so dass die letztgenannten Personen aus der Fehlerkette herausgenommen werden können. Gesamtdiskussion Eine sehr nützliche und informative Vorlesung, die uns noch lange Zeit in guter Erinnerung bleiben wird. Dieses Protokoll wurde selbstständig erstellt. Frank Bock Benjamin Bulheller Download von 9 by Benjamin Bulheller & Frank Bock
NMR - Seite 1. NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie
 NMR - Seite 1 NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie Protonen besitzen ebenso wie Elektronen einen eigenen Spin (Drehung um die eigene Achse).Allerdings gibt es mehrere Möglichkeiten als
NMR - Seite 1 NMR (Kernresonanzspektroskopie) Allgemeines zur Theorie Protonen besitzen ebenso wie Elektronen einen eigenen Spin (Drehung um die eigene Achse).Allerdings gibt es mehrere Möglichkeiten als
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ
 Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Merke: Zwei Oszillatoren koppeln am stärksten, wenn sie die gleiche Eigenfrequenz besitzen. RESONANZ Viele Kerne besitzen einen Spindrehimpuls. Ein Kern mit der Spinquantenzahl I hat einen Drehimpuls (L)
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden
 Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
Kernmagnetische Resonanzspektroskopie (NMR) Spektroskopische Methoden Grundlagen Die meisten Atomkerne führen eine Drehbewegung um die eigene Achse aus ("Spin"). Da sie geladene Teilchen (Protonen) enthalten,
NMR Spektroskopie. 1nm Frequenz X-ray UV/VIS Infrared Microwave Radio
 NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
NMR Spektroskopie 1nm 10 10 2 10 3 10 4 10 5 10 6 10 7 Frequenz X-ray UV/VIS Infrared Microwave Radio Anregungsmodus electronic Vibration Rotation Nuclear Spektroskopie X-ray UV/VIS Infrared/Raman NMR
Vorbereitung. µ z = mγ h (1) γ = gq 2m wobei q die Ladung und m die Masse des Teilchens beschreiben.
 Physikalisches Fortgeschrittenenpraktikum NMR-Spektroskopie Vorbereitung Armin Burgmeier Robert Schittny 1. Theoretische Grundlagen 1.1. Kerndrehimpuls und magnetisches Moment Nach der Quantentheorie besitzt
Physikalisches Fortgeschrittenenpraktikum NMR-Spektroskopie Vorbereitung Armin Burgmeier Robert Schittny 1. Theoretische Grundlagen 1.1. Kerndrehimpuls und magnetisches Moment Nach der Quantentheorie besitzt
Kernmagnetische Resonanzspektroskopie. N Nuclear M Magnetic R Resonance Beobachtung magnetisch aktiver Kerne in einem äußeren Magnetfeld
 NMR- SPEKTROSKOPIE Prüfungsfrage Radiospektroskopische Methode: NMR. Das Spin und magnetische Moment, die Bedingung der Resonanz, Spektralspaltung, chemische Verschiebung. Kernmagnetische Resonanzspektroskopie
NMR- SPEKTROSKOPIE Prüfungsfrage Radiospektroskopische Methode: NMR. Das Spin und magnetische Moment, die Bedingung der Resonanz, Spektralspaltung, chemische Verschiebung. Kernmagnetische Resonanzspektroskopie
Kernmagnetismus und Magnetfelder
 Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Kernmagnetismus und Magnetfelder. Kernspin Die meisten Kerne besitzen einen Eigendrehimpuls oder P ist gequantelt P = h I(I + ) h = h und h: das Plancksche Wirkungsquantum. π I: Kernspinquantenzahl (kurz:
Übungsaufgaben zur NMR-Spektrometrie
 Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4.1 Allgemeines Spektroskopische Methode zur Untersuchung von Atomen: elektronische Umgebung Wechselwirkung
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4.1 Allgemeines Spektroskopische Methode zur Untersuchung von Atomen: elektronische Umgebung Wechselwirkung
Spektroskopische Methoden in der Organischen Chemie (OC IV) NMR Spektroskopie 1. Physikalische Grundlagen
 NMR Spektroskopie 1. Physikalische Grundlagen Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR Spektroskopie 1. Physikalische Grundlagen Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
Kernresonanzspektroskopie
 Gleich geht s los! Kernresonanzspektroskopie 1. Geschichtliche Entwicklung 2. Physikalische Grundlagen 3. Das NMR-Spektrometer 4. Anwendung der 1 H-NMR-Spektren zur Analyse der Konstitution von Molekülen
Gleich geht s los! Kernresonanzspektroskopie 1. Geschichtliche Entwicklung 2. Physikalische Grundlagen 3. Das NMR-Spektrometer 4. Anwendung der 1 H-NMR-Spektren zur Analyse der Konstitution von Molekülen
Zentralabstand b, Spaltbreite a. Dreifachspalt Zentralabstand b, Spaltbreite a. Beugungsgitter (N Spalte, N<10 4, Abstand a)
 Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
Doppelspalt (ideal) Doppelspalt (real) Zentralabstand b, Spaltbreite a Dreifachspalt Zentralabstand b, Spaltbreite a Beugungsgitter (N Spalte, N
Kernmagnetische Resonanz NMR
 Kernmagnetische Resonanz: NMR F. Bloch E.M. Purcell: NMR 195 Physik Standard-Technik zur Strukturanalyse in der Organischen Chemie Kernmagnetische Resonanz NMR Kern: Eigenschaft der Atomkerne wird Kernspin
Kernmagnetische Resonanz: NMR F. Bloch E.M. Purcell: NMR 195 Physik Standard-Technik zur Strukturanalyse in der Organischen Chemie Kernmagnetische Resonanz NMR Kern: Eigenschaft der Atomkerne wird Kernspin
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
Die chemische Verschiebung - 1
 Die chemische Verschiebung - 1 Die Messfrequenz ν einer Kernsorte, hier: 1 H (Protonen), hängt bei einem isolierten Kern ausschließlich vom äußeren Magnetfeld (B 0 ) und ihrem magnetogyrischen Verhältnis
Die chemische Verschiebung - 1 Die Messfrequenz ν einer Kernsorte, hier: 1 H (Protonen), hängt bei einem isolierten Kern ausschließlich vom äußeren Magnetfeld (B 0 ) und ihrem magnetogyrischen Verhältnis
NMR Spektroskopie I = 0 : C, 16 O (sogenannte gg-kerne haben immer I=0!) I = 1/2: 1 H, 13 C, 15 N, 19 F, 31 P,... I = 1: 2. H=D, 6 Li, 14 N I = 3/2: 7
 NMR Spektroskopie folie00 Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR Spektroskopie folie00 Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p=ħ I, der ganz oder halbzahlige Werte von ħ betragen kann. I bezeichnet die Kernspin-Quantenzahl.
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
18. Strukturaufklärung in der Organischen Chemie
 Inhalt Index 18. Strukturaufklärung in der Organischen Chemie Die Kenntnis der zahlreichen organischen Reaktionen und funktionellen Gruppen, die in den vorangegangenen Kapiteln vorgestellt wurden, sollten
Inhalt Index 18. Strukturaufklärung in der Organischen Chemie Die Kenntnis der zahlreichen organischen Reaktionen und funktionellen Gruppen, die in den vorangegangenen Kapiteln vorgestellt wurden, sollten
III. Strukturbestimmung organischer Moleküle
 III. Strukturbestimmung organischer Moleküle Röntgenstrukturbestimmung g Spektroskopie UV-VIS IR NMR Massenspektrometrie (MS) Röntgenstruktur eines bakteriellen Kohlenhydrats O O O O O O O C3 Röntgenstruktur
III. Strukturbestimmung organischer Moleküle Röntgenstrukturbestimmung g Spektroskopie UV-VIS IR NMR Massenspektrometrie (MS) Röntgenstruktur eines bakteriellen Kohlenhydrats O O O O O O O C3 Röntgenstruktur
Methodische Ansätze zur Strukturaufklärung: Rnt. - Kernmagnetische Resonanzspektroskopie (NMR)
 ? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
? Methodische Ansäte ur Strukturaufklärung: - Rastersondenmikroskopie (AFM, SPM) SPM - Röntgenbeugung Rnt. - Elektronenspektroskopie (UV-vis) UV-vis - Schwingungsspektroskopie (IR) IR - Massenspektroskopie
NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz)
 NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz) Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p = ħ I, der ganz - oder halbzahlige Werte von ħ betragen
NMR Spektroskopie (Nuclear Magnetic Resonance Kern-Magnetische Resonanz) Viele Atomkerne besitzen einen von Null verschiedenen Eigendrehimpuls (Spin) p = ħ I, der ganz - oder halbzahlige Werte von ħ betragen
UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische Chemie Prof. Dr. B. Dick
 UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische hemie Prof. Dr. B. Dick PHYSIKALISH-HEMISHES PRAKTIKUM (Teil Ic) (Spektroskopie) Versuch NMR Protonenresonanz 0 http://www-dick.chemie.uni-regensburg.de/studium/praktikum1c.html
UNIVERSITÄT REGENSBURG Institut für Physikalische und Theoretische hemie Prof. Dr. B. Dick PHYSIKALISH-HEMISHES PRAKTIKUM (Teil Ic) (Spektroskopie) Versuch NMR Protonenresonanz 0 http://www-dick.chemie.uni-regensburg.de/studium/praktikum1c.html
Chemisches Grundpraktikum II (270002) Kernresonanzspektroskopie. NMR-Spektroskopie
 hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
hemisches Grundpraktikum II (270002) Kernresonanzspektroskopie NMR-Spektroskopie (Nuclear Magnetic Resonance). Kählig, SS 2010 Von der Substanz zur Struktur Substanz NMR - Spektren Struktur N N 1 Spektroskopie
Bestimmung der Struktur einer (un)bekannten Verbindung
 Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektrometrie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie H 3 C H 3
Bestimmung der Struktur einer (un)bekannten Verbindung Elementaranalyse Massenspektrometrie andere spektroskopische Methoden Röntgen- Strukturanalyse Kernmagnetische Resonanz - Spektroskopie H 3 C H 3
Ferienkurs Experimentalphysik Übung 2 - Musterlösung
 Ferienkurs Experimentalphysik 4 00 Übung - Musterlösung Kopplung von Drehimpulsen und spektroskopische Notation (*) Vervollständigen Sie untenstehende Tabelle mit den fehlenden Werten der Quantenzahlen.
Ferienkurs Experimentalphysik 4 00 Übung - Musterlösung Kopplung von Drehimpulsen und spektroskopische Notation (*) Vervollständigen Sie untenstehende Tabelle mit den fehlenden Werten der Quantenzahlen.
Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen
 Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen Seminar 5. 0. 200 Teil : NMR Spektroskopie. Einführung und Physikalische Grundlagen.2 H NMR Parameter: a) Chemische
Analytische Methoden in Org. Chemie und optische Eigenschaften von chiralen Molekülen Seminar 5. 0. 200 Teil : NMR Spektroskopie. Einführung und Physikalische Grundlagen.2 H NMR Parameter: a) Chemische
Einführung in die NMR-Spektroskopie. NMR-Spektroskopie. Teil 1: Einführung und Grundlagen der 1 H NMR. Das NMR Spektrometer
 NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
NMR-Spektroskopie Einführung in die NMR-Spektroskopie m I = - /2 (β) Teil : Einführung und Grundlagen der NMR E E. Physikalische und apparative Grundlagen m I = + /2 (α).2 Das D NMR Experiment.3 Die chemische
VL Spin-Bahn-Kopplung Paschen-Back Effekt. VL15. Wasserstoffspektrum Lamb Shift. VL16. Hyperfeinstruktur
 VL 16 VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2. Paschen-Back Effekt VL15. Wasserstoffspektrum 15.1. Lamb Shift VL16. Hyperfeinstruktur 16.1. Hyperfeinstruktur 16.2. Kernspinresonanz
VL 16 VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2. Paschen-Back Effekt VL15. Wasserstoffspektrum 15.1. Lamb Shift VL16. Hyperfeinstruktur 16.1. Hyperfeinstruktur 16.2. Kernspinresonanz
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
Versuchsprotokoll: Magnetische Kernresonanz (NMR)
 Versuchsprotokoll: Magnetische Kernresonanz (NMR) Christian Buntin, Jingfan Ye Gruppe 221 Karlsruhe, 22. November 2010 Inhaltsverzeichnis 1 Theoretische Grundlagen 2 1.1 Kernspin und magnetisches Moment.............................
Versuchsprotokoll: Magnetische Kernresonanz (NMR) Christian Buntin, Jingfan Ye Gruppe 221 Karlsruhe, 22. November 2010 Inhaltsverzeichnis 1 Theoretische Grundlagen 2 1.1 Kernspin und magnetisches Moment.............................
NMR-Lösungsmittel. 1 H-NMR. Bei der Verwendung der normalen, nichtdeuterierten Lösungsmittel. Spektroskopie in der Organischen Chemie
 NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
NMR-Lösungsmittel In der werden i.a. deuterierte Lösungsmittel verwendet. ie Substitution der leichten durch die schweren Wasserstoffatome hat zwei Vorteile: - euterium als Spin-1-Kern hat ebenfalls ein
PN 2 Einführung in die Experimentalphysik für Chemiker
 PN 2 Einführung in die Experimentalphysik für Chemiker 9. Vorlesung 13.6.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 2 Einführung in die Experimentalphysik für Chemiker 9. Vorlesung 13.6.08 Evelyn Plötz, Thomas Schmierer, Gunnar Spieß, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
Eigenschaften einiger für die NMR-Spektrometrie organischer Verbindungen wichtiger Kerne
 Der Zusammenhang zwischen dem magnetischen Moment eines Atomkerns und seines mechanischen Drehimpulses lautet: μ=γ J, wobei γ das gyromagnetische Verhältnis ist. Der mechanische Drehimpuls ist durch die
Der Zusammenhang zwischen dem magnetischen Moment eines Atomkerns und seines mechanischen Drehimpulses lautet: μ=γ J, wobei γ das gyromagnetische Verhältnis ist. Der mechanische Drehimpuls ist durch die
Mößbauer-Spektroskopie Vortrag zum apparativen Praktikum SS 05. Hella Berlemann Nora Obermann
 Mößbauer-Spektroskopie Vortrag zum apparativen Praktikum SS 05 Hella Berlemann Nora Obermann Übersicht: Mößbauer (1958): rückstoßfreie Kernresonanzabsorption von γ-strahlen γ-strahlung: kurzwellige, hochenergetische,
Mößbauer-Spektroskopie Vortrag zum apparativen Praktikum SS 05 Hella Berlemann Nora Obermann Übersicht: Mößbauer (1958): rückstoßfreie Kernresonanzabsorption von γ-strahlen γ-strahlung: kurzwellige, hochenergetische,
Thema heute: Aufbau der Materie: Das Bohr sche Atommodell
 Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Wiederholung der letzten Vorlesungsstunde: Erste Atommodelle, Dalton Thomson, Rutherford, Atombau, Coulomb-Gesetz, Proton, Elektron, Neutron, weitere Elementarteilchen, atomare Masseneinheit u, 118 bekannte
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Übungen Atom- und Molekülphysik für Physiklehrer (Teil 2)
 Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Einführung: NMR, was ist das? NMR = Nuclear Magnetic Resonance oder zu deutsch: Kernspinresonanz
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Einführung: NMR, was ist das? NMR = Nuclear Magnetic Resonance oder zu deutsch: Kernspinresonanz
Vorbemerkung. [disclaimer]
![Vorbemerkung. [disclaimer] Vorbemerkung. [disclaimer]](/thumbs/91/105086168.jpg) Vorbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik4. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
Vorbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik4. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie
 Fragenkatalog AC III NMR Teil 3 (Fröhlich) Die Boltzmann-Verteilung lautet: 1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie bezeichnet die Anzahl der Teilchen
Fragenkatalog AC III NMR Teil 3 (Fröhlich) Die Boltzmann-Verteilung lautet: 1) Diskutieren Sie die Boltzmann-Verteilung und deren Bedeutung für die NMR- Spektroskopie bezeichnet die Anzahl der Teilchen
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
Teil 1 Schwingungsspektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Kerne haben magn. Moment, dass sich entlang der Magnetfeldlinien eines statischen
Grundlagen der NMR-Spektroskopie
 Westfälische Wilhelms-Universität Münster Institut für Pharmazeutische und Medizinische Chemie 8. Semester Übersicht: Einleitung Physikalische Grundlagen Magnetische Kerne Resonanz Spektrometer 1 Chem.
Westfälische Wilhelms-Universität Münster Institut für Pharmazeutische und Medizinische Chemie 8. Semester Übersicht: Einleitung Physikalische Grundlagen Magnetische Kerne Resonanz Spektrometer 1 Chem.
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Chemische Verschiebung Chemische Umgebung Funktionelle Gruppen Signalintensitäten
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Chemische Verschiebung Chemische Umgebung Funktionelle Gruppen Signalintensitäten
P105. Konstitution. Massenspektrum 100 % m/z
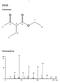 1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
10. Der Spin des Elektrons
 10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
10. Elektronspin Page 1 10. Der Spin des Elektrons Beobachtung: Aufspaltung von Spektrallinien in nahe beieinander liegende Doppellinien z.b. die erste Linie der Balmer-Serie (n=3 -> n=2) des Wasserstoff-Atoms
Spektroskopiemodul II. H-NMR und 13 C-NMR
 Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? 1.1. 1 H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen
Spektroskopiemodul II 1 H-NMR und 13 C-NMR 1 1. Was gehört zu einer vollständigen Spektreninterpretation zur Strukturaufklärung? 1.1. 1 H-NMR-Spektren Man muss die chemische Verschiebung jedes einzelnen
Magnetische Kernresonanz NMR
 Physikalisches Praktikum für Fortgeschrittene (P3) Magnetische Kernresonanz NMR Betreuer: Dirk Waibel Michael Lohse, Matthias Ernst Gruppe 11 Karlsruhe, 6.12.2010 Verbessertes Protokoll Inhaltsverzeichnis
Physikalisches Praktikum für Fortgeschrittene (P3) Magnetische Kernresonanz NMR Betreuer: Dirk Waibel Michael Lohse, Matthias Ernst Gruppe 11 Karlsruhe, 6.12.2010 Verbessertes Protokoll Inhaltsverzeichnis
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
Das NMR-Experiment Eine kurze Einführung
 Multipuls-NMR in der Organischen Chemie Das NMR-Experiment Eine kurze Einführung Spektroskopie bedeutet Wechselwirkung von elektromagnetischer Strahlung (Photonen) mit Materie; meist Absorption, aber auch
Multipuls-NMR in der Organischen Chemie Das NMR-Experiment Eine kurze Einführung Spektroskopie bedeutet Wechselwirkung von elektromagnetischer Strahlung (Photonen) mit Materie; meist Absorption, aber auch
Ferienkurs der TU München- - Experimentalphysik 4 Wasserstoffatom, Feinstruktur und Atome im Magnetfeld. Jonas J. Funke
 Ferienkurs der TU München- - Experimentalphysik 4 Wasserstoffatom, Feinstruktur und Atome im Magnetfeld Lösung Jonas J. Funke 0.08.00-0.09.00 Aufgabe (Drehimpulsaddition). : Gegeben seien zwei Drehimpulse
Ferienkurs der TU München- - Experimentalphysik 4 Wasserstoffatom, Feinstruktur und Atome im Magnetfeld Lösung Jonas J. Funke 0.08.00-0.09.00 Aufgabe (Drehimpulsaddition). : Gegeben seien zwei Drehimpulse
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2016 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 2. Vorlesung, 17. 3. 2016 Wasserstoffspektren, Zeemaneffekt, Spin, Feinstruktur,
Atom-, Molekül- und Festkörperphysik für LAK, SS 2016 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 2. Vorlesung, 17. 3. 2016 Wasserstoffspektren, Zeemaneffekt, Spin, Feinstruktur,
Spektroskopie-Seminar WS 17/18 5 NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
WS 17/18 1 -NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 1 5.1 1 -NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung δ(in
Vorbemerkung. [disclaimer]
![Vorbemerkung. [disclaimer] Vorbemerkung. [disclaimer]](/thumbs/75/72955190.jpg) Vorbemerkung Dies ist ein korrigierter Übungszettel aus dem Modul physik4. Dieser Übungszettel wurde von einem Tutor korrigiert. Dies bedeutet jedoch nicht, dass es sich um eine Musterlösung handelt. Weder
Vorbemerkung Dies ist ein korrigierter Übungszettel aus dem Modul physik4. Dieser Übungszettel wurde von einem Tutor korrigiert. Dies bedeutet jedoch nicht, dass es sich um eine Musterlösung handelt. Weder
NMR-Spektroskopie Nuclear Magnetic Resonance - Spektroskopie H2N HO2C CH3
 NMR-Spektroskopie Nuclear Magnetic Resonance - Spektroskopie anwendbar auf Atomkerne mit magnetischem Moment z.b. 1 H, 13 C, und andere Kerne O H 2 N NH HO 2 C Si CH 3 6. 5. 4. 3. 2. 1.. ppm Folie 1 Bedeutung
NMR-Spektroskopie Nuclear Magnetic Resonance - Spektroskopie anwendbar auf Atomkerne mit magnetischem Moment z.b. 1 H, 13 C, und andere Kerne O H 2 N NH HO 2 C Si CH 3 6. 5. 4. 3. 2. 1.. ppm Folie 1 Bedeutung
1 Grundbegriffe, Meßgrößen, Meßverfahren in Kürze
 Grundbegriffe, Meßgrößen, Meßverfahren in Kürze. hemische Verschiebung Als chemische Verschiebung bezeichnet man die Abängigkeit der Larmorfrequenz eines Kernspins von seiner chemischen Umgebung. Der Kernspin
Grundbegriffe, Meßgrößen, Meßverfahren in Kürze. hemische Verschiebung Als chemische Verschiebung bezeichnet man die Abängigkeit der Larmorfrequenz eines Kernspins von seiner chemischen Umgebung. Der Kernspin
1. Allgemeine Grundlagen Quantenmechanik
 1. Allgemeine Grundlagen 1.3. Quantenmechanik Klassische Mechanik vs Quantenmechanik Klassische (Newton sche) Mechanik klassischer harmonischer Oszillator Quantenmechanik quantenmechanischer harmonischer
1. Allgemeine Grundlagen 1.3. Quantenmechanik Klassische Mechanik vs Quantenmechanik Klassische (Newton sche) Mechanik klassischer harmonischer Oszillator Quantenmechanik quantenmechanischer harmonischer
4.57 ppm 1.45 ppm = 3.12 ppm 3.12 ppm * MHz = Hz Hz = rad/sec
 (1) Zwei Signale liegen im Protonenspektrum bei 1.45 und 4.57 ppm, das Spektrometer hat eine Frequenz von 400.13 MHz. Wieweit liegen die Signale in Hz bzw. in rad/sec auseinander? 4.57 ppm 1.45 ppm = 3.12
(1) Zwei Signale liegen im Protonenspektrum bei 1.45 und 4.57 ppm, das Spektrometer hat eine Frequenz von 400.13 MHz. Wieweit liegen die Signale in Hz bzw. in rad/sec auseinander? 4.57 ppm 1.45 ppm = 3.12
Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen. Wann: Mi Fr Wo: P1 - O1-306
 Laserspektroskopie Was: Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen Wann: Mi 13 15-14 00 Fr 10 15-12 00 Wo: P1 - O1-306 Wer: Dieter Suter Raum P1-O1-216 Tel. 3512 Dieter.Suter@uni-dortmund.de
Laserspektroskopie Was: Optische Spektroskopie mit Lasern: Grundlagen und Anwendungen Wann: Mi 13 15-14 00 Fr 10 15-12 00 Wo: P1 - O1-306 Wer: Dieter Suter Raum P1-O1-216 Tel. 3512 Dieter.Suter@uni-dortmund.de
2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment
 Prof. Dieter Suter / Prof. Roland Böhmer Magnetische Resonanz SS 03 2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment 2.1.1 Felder und Dipole; Einheiten Wir beginnen mit einer
Prof. Dieter Suter / Prof. Roland Böhmer Magnetische Resonanz SS 03 2. Grundlagen und Wechselwirkungen 2.1 Magnetismus und magnetisches Moment 2.1.1 Felder und Dipole; Einheiten Wir beginnen mit einer
Ferienkurs Experimentalphysik 4
 Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Ferienkurs Experimentalphysik 4 Probeklausur Markus Perner, Markus Kotulla, Jonas Funke Aufgabe 1 (Allgemeine Fragen). : (a) Welche Relation muss ein Operator erfüllen damit die dazugehörige Observable
Elektromagnetische Wellen
 Elektromagnetische Wellen Im Gegensatz zu Schallwellen sind elektromagnetische Wellen nicht an ein materielles Medium gebunden -- sie können sich auch in einem perfekten Vakuum ausbreiten. Sie sind auch
Elektromagnetische Wellen Im Gegensatz zu Schallwellen sind elektromagnetische Wellen nicht an ein materielles Medium gebunden -- sie können sich auch in einem perfekten Vakuum ausbreiten. Sie sind auch
Multipuls-NMR in der Organischen Chemie. Puls und FID
 Puls und FID Obwohl der Puls eine bestimmte, am NMR-Spektrometer vorab eingestellte Sendefrequenz ν 1 hat, ist er in der Lage, über einen relativ weiten Frequenzbereich von mehreren khz, den gesamten Resonanzbereich
Puls und FID Obwohl der Puls eine bestimmte, am NMR-Spektrometer vorab eingestellte Sendefrequenz ν 1 hat, ist er in der Lage, über einen relativ weiten Frequenzbereich von mehreren khz, den gesamten Resonanzbereich
Übungsaufgaben NMR-Spektroskopie (1)
 Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Ferienkurs Experimentalphysik Lösung zur Übung 2
 Ferienkurs Experimentalphysik 4 01 Lösung zur Übung 1. Ermitteln Sie für l = 1 a) den Betrag des Drehimpulses L b) die möglichen Werte von m l c) Zeichnen Sie ein maßstabsgerechtes Vektordiagramm, aus
Ferienkurs Experimentalphysik 4 01 Lösung zur Übung 1. Ermitteln Sie für l = 1 a) den Betrag des Drehimpulses L b) die möglichen Werte von m l c) Zeichnen Sie ein maßstabsgerechtes Vektordiagramm, aus
Spektroskopische Methoden in der Organischen Chemie (OC IV) C NMR Spektroskopie
 6. 3 C NMR Spektroskopie Die Empfindlichkeit des NMR Experiments hängt von folgenden physikalischen Parametern (optimale Abstimmung des Spektrometers vorausgesetzt) ab: Feldstärke B o, Temperatur T, gyromagnetisches
6. 3 C NMR Spektroskopie Die Empfindlichkeit des NMR Experiments hängt von folgenden physikalischen Parametern (optimale Abstimmung des Spektrometers vorausgesetzt) ab: Feldstärke B o, Temperatur T, gyromagnetisches
VL Landé-Faktor (Einstein-deHaas Effekt) Berechnung des Landé-Faktors Anomaler Zeeman-Effekt
 VL 14 VL13. Spin-Bahn-Kopplung (II) 13.1. Landé-Faktor (Einstein-deHaas Effekt) 13.2. Berechnung des Landé-Faktors 13.3. Anomaler Zeeman-Effekt VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2.
VL 14 VL13. Spin-Bahn-Kopplung (II) 13.1. Landé-Faktor (Einstein-deHaas Effekt) 13.2. Berechnung des Landé-Faktors 13.3. Anomaler Zeeman-Effekt VL14. Spin-Bahn-Kopplung (III) 14.1. Spin-Bahn-Kopplung 14.2.
NMR Vortag im Rahmen des Fortgeschrittenen-Praktikums
 NMR Vortag im Rahmen des Fortgeschrittenen-Praktikums Martin Fuchs 1 Motivation Die Nuclear Magnetic Resonance, oder zu deutsch Kernspinresonanz ist vor allem durch die aus der Medizin nicht mehr wegzudenkende
NMR Vortag im Rahmen des Fortgeschrittenen-Praktikums Martin Fuchs 1 Motivation Die Nuclear Magnetic Resonance, oder zu deutsch Kernspinresonanz ist vor allem durch die aus der Medizin nicht mehr wegzudenkende
Magnetische Resonanzmethoden
 Nuclear Magnetic Resonance (NMR) und Electron Spin Resonance (ESR) Kernspinresonanz und Elektronenspinresonanz Wichtige Technik in der organischen Chemie Zahlreiche Anwendungen in der Chemie, Medizin,
Nuclear Magnetic Resonance (NMR) und Electron Spin Resonance (ESR) Kernspinresonanz und Elektronenspinresonanz Wichtige Technik in der organischen Chemie Zahlreiche Anwendungen in der Chemie, Medizin,
Einführung in die NMR-Spektroskopie im Rahmen des Praktikums OC-II
 Einführung in die NMR-Spektroskopie im Rahmen des Praktikums O-II Till Opatz Kerne im statischen Magnetfeld Zeeman-Aufspaltung -1-3/2 Energie -1/2 +1/2 0 +1-1/2 +1/2-3/2 I = 1/2 I = 1 I = 3/2 Insgesamt
Einführung in die NMR-Spektroskopie im Rahmen des Praktikums O-II Till Opatz Kerne im statischen Magnetfeld Zeeman-Aufspaltung -1-3/2 Energie -1/2 +1/2 0 +1-1/2 +1/2-3/2 I = 1/2 I = 1 I = 3/2 Insgesamt
Der Kern-Overhauser-Effekt (Nuclear Overhauser Effect, NOE)
 Der Kern-verhauser-Effekt (Nuclear verhauser Effect, NE) Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten 1 H-Kerns S für eine
Der Kern-verhauser-Effekt (Nuclear verhauser Effect, NE) Die Intensität eines 1 H-Signals kann durch ein Entkopplungsexperiment verändert werden. Wird der Übergang eines ausgewählten 1 H-Kerns S für eine
Optisches Pumpen an Rubidium
 Optisches Pumpen an Rubidium Inhaltsverzeichnis Theorie... Optisches Pumpen... Kernspinbestimmung... Versuchsaufbau... Kernspinbestimmung... Auswertung... Bestimmung der Relaxationszeit:... Bestimmung
Optisches Pumpen an Rubidium Inhaltsverzeichnis Theorie... Optisches Pumpen... Kernspinbestimmung... Versuchsaufbau... Kernspinbestimmung... Auswertung... Bestimmung der Relaxationszeit:... Bestimmung
Die Strukturabhängigkeit der chemischen Verschiebung
 Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
Die Strukturabhängigkeit der chemischen Verschiebung. Abschirmung in einem Atom (wie bisher geschildert) Die Elektronenverteilung in einem Wasserstoffatom ist sphärisch. B 0 0 0000000 000000000 000000000
9. Moleküle. 9.1 Wasserstoff-Molekül Ion H Wasserstoff-Molekül H Schwerere Moleküle 9.4 Angeregte Moleküle. Physik IV SS
 9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
Seminar WiSe 2015/2016. PD Dr. Markus Nett. Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: jena.
 Kernresonanzspektroskopie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: markus.nett@hki jena.de NMR = nuclear
Kernresonanzspektroskopie Seminar WiSe 2015/2016 PD Dr. Markus Nett Nachwuchsgruppenleiter Leibniz Institut für Naturstoff Forschung und Infektionsbiologie E mail: markus.nett@hki jena.de NMR = nuclear
J(J + 1) + S(S + 1) L(L + 1) = g J m J µ B B 0 mit g J = 1 +. (A.2) 2J(J + 1) g J 2
 A. Atomdaten A.. Fein- und Hyperfeinstruktur im Magnetfeld A... Feinstruktur-Aufspaltung Aus der Spin-Bahn-Kopplung eines Zustandes ( J = L + S) ergibt sich die Zusatzenergie E LS = a {J (J + ) L(L + )
A. Atomdaten A.. Fein- und Hyperfeinstruktur im Magnetfeld A... Feinstruktur-Aufspaltung Aus der Spin-Bahn-Kopplung eines Zustandes ( J = L + S) ergibt sich die Zusatzenergie E LS = a {J (J + ) L(L + )
Aufbau von Atomen. Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem
 Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Aufbau von Atomen Atommodelle Spektrum des Wasserstoffs Quantenzahlen Orbitalbesetzung Periodensystem Wiederholung Im Kern: Protonen + Neutronen In der Hülle: Elektronen Rutherfords Streuversuch (90) Goldatome
Spinsysteme. AX 3 -Spinsystem
 Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
Spinsysteme Eine Gruppe aus zwei oder mehreren Kernspins, die miteinander eine magnetische Wechselwirkung eingehen, bezeichnet man als ein Spinsystem. Die Struktur eines hochaufgelösten NMR-Spektrums und
Theoretical Biophysics - Quantum Theory and Molecular Dynamics. 9. Vorlesung. Pawel Romanczuk WS 2017/18
 Theoretical Biophysics - Quantum Theory and Molecular Dynamics 9. Vorlesung Pawel Romanczuk WS 2017/18 http://lab.romanczuk.de/teaching 1 Zusammenfassung letzte VL Wasserstoffatom Quantenmechanisches Zweikörperproblem
Theoretical Biophysics - Quantum Theory and Molecular Dynamics 9. Vorlesung Pawel Romanczuk WS 2017/18 http://lab.romanczuk.de/teaching 1 Zusammenfassung letzte VL Wasserstoffatom Quantenmechanisches Zweikörperproblem
Übungen zur Vorlesung Physikalische Chemie 2 (B. Sc.) Lösungsvorschlag zu Blatt 12
 Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Teil 3 2D-NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
gleicher Magnetfeldstärke die Resonanzfrequenz entsprechend kleiner; z.b: 400 MHz 1 H, aber MHz 13 C.
 Der 13 C-Kern ist in seinen wichtigsten Kerneigenschaften dem 1 H ähnlich. Er ist ebenso ein Spin-½-Kern, weist also im äußeren Magnetfeld B 0 nur zwei praktisch gleich populierte Energiezustande auf.
Der 13 C-Kern ist in seinen wichtigsten Kerneigenschaften dem 1 H ähnlich. Er ist ebenso ein Spin-½-Kern, weist also im äußeren Magnetfeld B 0 nur zwei praktisch gleich populierte Energiezustande auf.
2. Magnetresonanztomographie (MRT, MRI) 2.3. Spin und Magnetisierung
 2. Magnetresonanztomographie (MRT, MRI) 2.3. Spin und Magnetisierung Übergang zwischen den beiden Energieniveaus ω l = γb 0 γ/2π Larmor-Frequenz ν L 500 400 300 200 100 ν L = (γ/2π)b 0 [MHz/T] 1 H 42.57
2. Magnetresonanztomographie (MRT, MRI) 2.3. Spin und Magnetisierung Übergang zwischen den beiden Energieniveaus ω l = γb 0 γ/2π Larmor-Frequenz ν L 500 400 300 200 100 ν L = (γ/2π)b 0 [MHz/T] 1 H 42.57
14. Atomphysik. Inhalt. 14. Atomphysik
 Inhalt 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Inhalt 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Molekulare Biophysik. NMR-Spektroskopie (Teil 1)
 Molekulare Biophysik NMR-Spektroskopie (Teil 1) Das Vorlesungs-Programm 2/94 Vorlesung Molekulare Biophysik : NMR-Spektroskopie Tag 1 Theoretische Grundlagen der NMR-Spektroskopie (1) Tag 2 Theoretische
Molekulare Biophysik NMR-Spektroskopie (Teil 1) Das Vorlesungs-Programm 2/94 Vorlesung Molekulare Biophysik : NMR-Spektroskopie Tag 1 Theoretische Grundlagen der NMR-Spektroskopie (1) Tag 2 Theoretische
Musterlösung 02/09/2014
 Musterlösung 0/09/014 1 Streuexperimente (a) Betrachten Sie die Streuung von punktförmigen Teilchen an einer harten Kugel vom Radius R. Bestimmen Sie die Ablenkfunktion θ(b) unter der Annahme, dass die
Musterlösung 0/09/014 1 Streuexperimente (a) Betrachten Sie die Streuung von punktförmigen Teilchen an einer harten Kugel vom Radius R. Bestimmen Sie die Ablenkfunktion θ(b) unter der Annahme, dass die
14. Atomphysik Physik für E-Techniker. 14. Atomphysik
 14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
14. Atomphysik 14.1 Aufbau der Materie 14.2 Der Atomaufbau 14.2.1 Die Hauptquantenzahl n 14.2.2 Die Nebenquantenzahl l 14.2.3 Die Magnetquantenzahl m l 14.2.4 Der Zeemann Effekt 14.2.5 Das Stern-Gerlach-Experiment
Kurs "Spektroskopische Methoden in der Anorganischen und Organischen Chemie" Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt 1)
 Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt ) Zum Lösungsmittel: Das Kohlenstoffspektrum zeigt bei 77 ppm drei gleich große äquidistante Signale. Diese stammen von CDC 3. Chemische Verschiebungen
Kernresonanzspektroskopie - Übungen Lösung zu NMR-6 (Blatt ) Zum Lösungsmittel: Das Kohlenstoffspektrum zeigt bei 77 ppm drei gleich große äquidistante Signale. Diese stammen von CDC 3. Chemische Verschiebungen
Spektroskopie-Seminar SS NMR-Spektroskopie. C-NMR-Spektroskopie und 2D-Spektroskopie
 13 C-NMR-Spektroskopie und 2D-Spektroskopie 6.1 Allgemeines Kernresonanz: Wechselwirkungen zwischen dem magnetischen Moment von Atomkernen mit einem magnetischen Wechselfeld Nur solche Isotope können untersucht
13 C-NMR-Spektroskopie und 2D-Spektroskopie 6.1 Allgemeines Kernresonanz: Wechselwirkungen zwischen dem magnetischen Moment von Atomkernen mit einem magnetischen Wechselfeld Nur solche Isotope können untersucht
 Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
Die Lage der Emissionsbanden der charakteristischen Röntgenstrahlung (anderer Name: Eigenstrahlung) wird bestimmt durch durch das Material der Kathode durch das Material der Anode die Größe der Anodenspannung
