Kapitel 4 - Baustoffe der Erde: Minerale und Gesteine
|
|
|
- Bärbel Albert
- vor 7 Jahren
- Abrufe
Transkript
1 Kapitel 4 - Baustoffe der Erde: Minerale und Gesteine 1) Was sind Minerale? - Baustoffe der Gesteine -> Ein M. ist ein homogener, natürlich vorkommender, kristalliner, im Allgemeinen anorganischer Festkörper bestimmter ch. Zusammensetzung. Natürliches Vorkommen: Entsteht nur in der Natur, nicht im Labor Kristalliner Festkörper: Atome bilden in allen 3 Raumrichtungen eine geordnete Struktur (Gegenteil von amorphen oder glasigen Materialien, die richtungslos sind) Allgemein anorganisch: Schließt organische Substanzen aus Pflanzen und Tieren aus Bestimmter ch. Zusammensetzung: Das Besondere an einem Mineral ist seine ch. Zusammensetzung in Verbindung mit der Anordnung der Atome in einer Kristallstruktur: Bsp.: Quarz: Immer ein festes Verhältnis von 2 Sauerstoffatomen zu einem Siliciumatom. 2) Was sind Gesteine? Eine natürlich vorkommende, verfestigte Mischung von Mineralen und mineralähnlichen Stoffen. 3) Was sind mono- und polymineralische Gesteine? G. nur aus einem M.: Monomineralisch: Kalkstein aus Kalzit G. aus mehreren M.: Polymineralisch: Granit; aus Feldspat, Quarz und Glimmer 4) Was sind Atome? Kleinste, chemisch(!) nicht weiter zerlegbare Teilchen eines Elements, das alle phy. und ch. Eigenschaften seines Elements in sich trägt und mit anderen Elementen reagieren und ch. Bindungen eingehen kann. Man kann sich ein Atom als eine feste Kugel vorstellen, mit einem Durchmesser von 1 angstrom = meters. Elektronen umkreisen den Atomkern in einer Elektronenwolke. Diese Wolke ist etwa x größer, als der Atomkern. Die Abstände, mit denen sich die Elektronen auf den unterschiedlichen Orbitalen (Energieniveaus) um den Kern bewegen, bestimmen somit auch die Größe des gesamten Atoms. 5) Was macht praktisch die gesamte Atommasse aus? Was ist zu vernachlässigen? Summe von Protonen und Neutronen im Kern. Dabei kann die Anzahl der Neutronen variieren (dann versch. Isotope eines Elements), die Protonen sind aber konstant. Somit erhalten alle Kohlenstoffatome 6 Protonen. Die Masse der Elektronen ist zu vernachlässigen, also sehr gering: Die Masse eines Protons ist 1800x größer als die eines Elektrons Die Massen eines Neutrons ist 1800x größer als die eines Elektrons 6) Wo bewegen sich Elektronen? Auf Orbitalbahnen um den Atomkern (Modellvorstellung) 7) Was gibt die Ordnungs- oder Kernladungszahl an? Anzahl der Protonen im Atomkern. Alle Atome eines Elements haben die gleiche Anzahl an Protonen, dh. die gleiche Ordnungs- und Kernladungszahl. 8) Was bestimmt das ch. Verhalten eines Elementes? Anzahl der Protonen 9) Was sind Isotope? Nuklide, dh. Atomkernsorten, deren Atomkerne eine gleiche Anzahl an Protonen (gleiche Ordnungszahl bzw. Kernladungszahl), aber unterschiedliche Anzahl von Neutronen haben, was zu ungleichen Massenzahlen, aber weitgehend identischem ch. Verhalten der Isotope des selben Elements führt. Die 3 existierenden Isotope des Kohlenstoffs C, die alle 6 Protonen haben, können 6,7, oder 8 Neutronen besitzen und daher die Atommassen 12, 13 und 14. Isotope finden besonders in der (Paläo)-Klimatologie eine hohe wissenschaftliche Resonanz. 10) Was ist eine ch. Reaktion? Beispielreaktion? Ch. R. entstehen dadurch, dass die beiden miteinander reagierenden Atome gemeinsame Elektronen besitzen (kovalente Bindung), oder dass die Atome Elektronen ab- und aufnehmen können Stichwort Elektronentransfer
2 Natrium + Chlor = Natriumchlorid 11) Was sind Ionen? Atomkerne, die durch ch. Reaktionen und Elektronentransfers positiv (Kation) oder negativ (Anion) geladen sind. 12) Welche ch. Bindungsarten gibt es? - Elektronische Ionenbindung: Kräfte zwischen Ionen unterschiedlicher Ladung. Die Kraft ist umso stärker, je näher die Atomkerne beisammen sind und je mehr sich die el. Ladung erhöht. Bindungstyp macht 90 % aller mineralischen Bindungen aus. (Bei Mineralen oft sichtbar durch Glasglanz) Kovalente Bindung: Atome teilen sich Elektronen. Bindung ist im Allgemeinen stärker, als die Ionenbindung, z. B. Diamant. Diamant besteht aus Kohlenstoff (C). C hat 4 Valenzelektronen (Elektronen auf dem äußeren Orbit). Jedes C ist von 4 andern C umgeben, die einen gleichseitigen Tetraeder bilden. In dieser Konfiguration teilt sich jedes C mit jedem seiner 4 Nachbarn ein Elektron, woraus sich eine sehr stabile kovalente Bindung ergibt. Metallische Bindung Bei den Metallen haben Atome eine starke Tendenz, Elektronen abzugeben und in Form von Kationen ein Gitter zu bilden, während die Elektronen frei im Raum sind und von allen Ionen geteilt werden. Sie verteilen sich zwischen den Ionen in Form eines Elektronengases. Van der Vaals Bindung Schwache Anziehungskräfte, die im Gegensatz zu den anderen Kräften vernachlässigbar sind. 13) Wie entstehen Kristalle? Es gibt 3 Möglichkeiten: 1. Kristallisation aus einem Magma 2. Kristallwachstum im festen Zustand 3. Fällung aus einer Lösung Durch den Prozess der Kristallisation, bilden sich aus einer gasförmigen oder fluiden Phase ein Festkörper (Kristall), wenn seine atomaren Bestandteile im richtigen ch. Verhältnis in die Kristallstruktur eingebaut werden können. (Häufig Kristallisation aus einem Magma.) Kationen sind dabei kleiner als Anionen, was zur Folge hat, dass die Kristallstruktur davon bestimmt wird, wie die Anionen angeordnet sind und wie die Kationen dazwischen passen. Die Kristallisation beginnt mit der Bildung von winzigen Kristallisationskeimen, kleinste, geordnete 3D-Strukturen, in denen die Atome in einem Raumgitter angeordnet sind. Die Begrenzung der Kristalle besteht aus den Kristallflächen, welche natürlich sind. Kristalle mit gut ausgebildeten Flächen entstehen durch langsames und stetiges Wachstum, wenn sie genügend Raum haben -> In Klüften und Drusen (Hohlräume im Gestein) 14) Nennen Sie Beispiele für 1.kleine Kationen und 2. größere Anionen! Was haben die unterschiedlichen Größen für eine Folge? 1: Kalium(+), Natrium (+), Calcium (2+), Magnesium(2+), Eisen (3+), Al (3+), Si(4+); KNaCaMg FeAlSi 2: Chlorid (-), Sulfid (2-), Sauerstoff (2-) Die Struktur eines Kristalls wird im Wesentlichen durch die Anordnung der großen Anionen bestimmt, und wie die kleinen Kationen dazwischen passen. 15) Welche Kationen werden bei der Hydrolisierung besonders gut ausgetauscht und warum? Wie in der oberen Aufgabe beschrieben, von links nach rechts weniger gut. Kalium wird daher gut, Silicium sehr schlecht ausgetauscht. Der Grund ist die stärkere positive Ladung, die einen einfachen Austausch verhindert. Im Zusammenhang mit der ch. Verwitterung der Hydrolyse, bestimmt die Ladung der Kationen im Kristallgitter daher auch, wie stark ein Mineral für die Hydrolyse anfällig ist. 16) Was versteht man unter Diadochie? - Kationenersatz: Dabei bleibt die Kristallstruktur gleich, die ch. Zusammensetzung ändert sich. -> Kationen mit ähnlichen ch. Eigenschaften und ähnlicher Größe, können sich im Kristallgitter gegenseitig ersetzen. Kationenersatz ist bei den Silicaten weit verbreitet, wie z. B. Beim Olivin, einem Inselsilicat. Ein weiteres Beispiel sind die Minerale der Glimmerfamilie. Alle Varietäten haben die gleiche Kristallstruktur mit wechselnden Anteilen der Kationen Na, K, Al, Fe, Mg in der Silicatverbindung.
3 17) Ordnen Sie die 1. generell kleineren Kationen und 2. generell größeren Anionen nach der Größe, beginnend mit der kleinsten Größe! 1: Si4+, Al3+, Fe3+, Mg2+, Fe2+, Na+, Ca2+, K+ 2: O2-, Cl-, S2-18) Wann kristallisieren Kristalle? - bei T unter Schmelzpunkt - Bei Überschreitung des Sättigungspunktes einer Lösung (NaCl und Wasser -> Große Salzseen) 19) Was versteht man unter Polymorphie? Bsp.! Minerale mit gleicher ch. Zusammensetzung aber unterschiedlichen kristallinen Phasen Diamant & Graphit. Andalusit, Disthen und Sillimanit Die Wirkung von T und P führt zu unterschiedlichen kristallinen Phasen eines Elements oder einer Verbindung. Welche Struktur sich bildet, hängt von T und P ab. Bsp.: Diamant und Graphit: Bestehen beide aus C, weisen aber aufgrund ihres Bildungsmilieus unterschiedliche Kristallstrukturen auf. Diamant: Dicht gepackte C-Atome, hohe kovalente Bindung -> hartes Mineral. Graphit: vice versa. 20) Wie viele unterschiedliche Minerale sind auf der Erde bekannt? Welche 5 Mineralgruppen sind die wichtigsten gesteinsbildenden Minerale? - bekannt sind ca die wichtigsten g. Minerale sind: Silikate: Silizium-Sauerstoff-Tetraeder bilden die Basis der Silikate. 4 Sauerstoffionen um ein Siliziumion bilden einen Tetraeder. Kombinationen dieser Tetraeder bilden das Gerüst der Silikate. Verschiedene Kombinationen bilden verschieden Strukturen: - Ring: Turmalin - Gruppen: Melilith - Insel: Olivin - Ketten: Pyroxene - 2-Schicht: Kaolinit, Serpentin - 3-Schicht: Illit, Montmorillonit, Glimmer, Muskovit - Gerüst: Feldspat - Doppelketten (Bänder): Amphibole, Hornblende Carbonate Zweithäufigste Mineralgruppe der Erdkruste; Hauptkomponenten von Kalksteinen; Mit verdünnter Salzsäure lässt sich prüfen, ob das Gestein carbonathaltig ist; die 3 wichtigsten sind: - Calcit - Aragonit - Dolomit - Siderit Oxide - Hämatit - Magnetit - Korund - Spinell - Quarz - Bauxit Sulfide - Pyrit Sulfate - Gips - Anhydrit Phosphate Apatit 21) Beschreiben Sie, wie und womit physikalische Eigenschaften der Minerale bestimmt werden! - Säuretest mit verdünnter Salzsäure:
4 Einige Tropfen verdünnte Salzsäure auf das Aggregat geben: Gasbläßchen zeigen, dass Co² freigesetzt wird, was mit großer Sicherheit auf Calcit, ein Carbonatmineral oder Carbonatgestein hinweist. - Ritzhärte: Härtebestimmung mit der Mohs` schen Härteskala von 1 bis 10 (Talk-Diamant) 1: Talk 2: Gips Halit; noch ritzbar mit Fingernagel 3: Calcit; noch ritzbar mit Kupfermünze 4: Fluorit (Flussspat) 5: Apatit, Mangan noch ritzbar mit Messer 6: Orthoklas (Feldspat) noch ritzbar mit Fensterglas 7: Quarz noch ritzbar mit Stahlfeile 8: Topas 9: Korund 10: Diamant - Spaltbarkeit Anzahl und Richtungen der Spaltflächen -> M. mit Ionenbindung zeigten durch schwache Kräfte meist sehr gute Spaltbarkeiten -> M. mit Kovalenter Bindung zeigen durch starke Kräfte meist keine oder schlechte Spaltbarkeit -> Glimmer, als 3-Schichttonmineral, zeigt zwischen den TOT-Schichten eine sehr gute Spaltbarkeit entlang der Zwischenschicht durch Kaliumionen Spaltbarkeit nach Richtung der Spaltflächen: Pyroxene: Spaltflächen stehen im Winkel von 93 und 87 Grad zueinander: Querschnitt führt zu einem Quadrat. Amphibole: 2 Spaltrichtungen: 54 und 124 Grad: Querschnitt führ zu einem rautenförmigen Muster. Muskovit: Nur 1 Spaltfläche Calcit, Dolomit: 3 Spaltflächen, daher ergibt sich eine rhomboedrische Spaltbarkeit Spaltbarkeit nach Qualität: Bestimmt als vollkommen, gut oder unvollkommen. Sowie die Insel- als auch die Gerüstsilikate zeigen normalerweise keine Spaltbarkeit. Muskovit, ein Glimmer, lässt sich hingegen vollkommen spalten. - Bruch Brucharten: Faserig, muschelig, splittrig, blättrig, körnig, -> Unter dem Bruch versteht man die Beschaffenheit von Bruchflächen, die bei mechanischer Beanspruchung entlang unregelmäßiger Flächen entstehen. Alle Minerale zeigen i.d.r. ein Bruchverhalten entweder quer zu den Spaltflächen oder richtungslos. - Glanz - Metallglanz: starke Reflexion durch opake Substanzen - Fettglanz: wie mit Öl oder Fett überzogen - Perlmuttglanz: weißlich irisierend, wie bei Perlmutt - Porzellanglanz: typisch ist Trübung - Seidenglanz: Schimmer feinfaseriger Kristalle wie Seide - Diamantglanz: hell strahlend wie Diamant oder andere durchsichtige Minerale - Glasglanz: heller Glanz, wie Glas Kovalente Bindung: Oft Diamantglanz Ionenbindung: Oft Glasglanz Reines Gold, viele Sulfidminerale und andere opake M.: Metallglanz Perlmuttglanz ist das Ergebnis von mehrfach reflektierenden Schichten innerhalb eines durchsichtigen M. - Farbe z. Bsp. Hämatit: Hinterlässt beim Streichen über eine weiße Porzellanplatte einen rotbraunen Strich Entsteht durch - die Art der Ionen, die im reinen Material enthalten sind - Spuren von Verunreinigungen - Spurenelemente Die Farbe muss man mit Vorsicht genießen, da einige M. ihre Farbe nur an frischen Bruchflächen oder verwitterten Oberflächen zeigen. Bsp: Ein eisenhaltiger Olivin reflektiert nur grün, während ein eisenfreier Olivin farblos ist. Ursache für die Blaufärbung von Saphir sind Eisen und Titan. Ideochromatische Färbung: mit Strichfarbe Allochromatische Färbung: ohne Strichfarbe 22) Wie ist die Dichte definiert und wovon ist sie abhängig? Masse/Volumen
5 Abhängig von - Atomgewicht und Kompression der Atome im Kristallgitter - Bestandteile des Minerals 23) Was ist das Standartmaß für die Dichte? Spezifisches Gewicht: Gewicht eines Minerals in Luft dividiert durch das Gewicht der gleichen Volumenmenge reinen Wassers bei 4 Grad. 24) Auf was hat die Zunahme der Dichte einen Effekt? Lichtdurchlässigkeit (Transmission), Wärmeleitung und die Ausbreitungsgeschwindigkeit von Erdbebenwellen, Gewicht 25) Was versteht man unter Habitus? Kristallform: Gibt an, wie schnell und in welche Richtung ein Kristall gewachsen ist: Ein tafeliger Kristall wächst ein eine Richtung langsam, in der orthogonalen Richtung schnell. 26) Nennen Sie ein Beispiel für eine Silikatgruppe mit faserigem Habitus! Asbest gesundheitsgefährdend, wenn winzige Kristalle in die Lunge gelangen 27) Was sind Gesteine? Beispiele? Natürlich vorkommende, feste Gemenge aus Mineralen, Bruchstücken von M., mineralähnlichen Soffen, oder anderen Gesteinen, von Organismenresten, oder in einigen Fällen auch aus nicht m. Substanz wie etwa die vulkanischen Gläser wie Bimsstein oder Obsidian sowie Kohle, die aus Pflanzenrückständen entstanden sind. G. können poly- oder monomineralsich sein. G. dienen dem Geologen als Proxidaten für Prozesse, die unseren Planeten betreffen. Man benötigt z. B. Kenntnisse, zum Finden von neuen Energieressourcen wie Erdgas, Kohle und Erze. Sie dienen als Informationsquelle. -> Marmor, Granit, Sandstein, Kalkstein, 28) Was beeinflusst die Gestalt der G.? - Mineralogie: Relative Anteile der Minerale - Gefüge: Größe, Form und Ausdehnung der m. Bestandteile - G. können grob- oder feinkörnig sein - o.g. Punkte sind abhängig vom Entstehungsprozess des Gesteins 29) Welche 3 Gesteinsgruppen gibt es? Magmatische G. Sedimentgesteine, Metamorphe G. 30) Wie entstehen magmatische G.? Durch Kristallisation einer Gesteinsschmelze eines Magmas. Eine solche Schmelze entsteht in großen Tiefen im oberen Mantel oder in der Erdkruste bei ca. 700 Grad der Temperatur, die zum Aufschmelzen der meisten Gesteine notwendig ist. Kühlen Schmelzen langsam ab, wie z. B. bei Intrusivgesteinen, so ist genug Zeit, um viele grobkörnige M. auszubilden (Granit). Wird die Schmelze aber eruptiv aus einem Vulkan geschleudert, kühlt sie so rasch ab, dass nur sehr kleine Kristalle wachsen können -> feinkörniges magmatisches Gestein. Kühlt Magma auf dem Meeresboden aus, entstehen nicht mal winzige Kristalle: Das Gestein ist glasig und wird zu einer Gesteinsmasse abgeschreckt. 31) Einteilung der magmatischen Gesteine was sind (1) Intrusiv- und (2) Effusivgesteine? 1) Werden auch Plutonite genannt, entstehen in der Erdkruste, wenn Magma tief in der Erdkruste in andere Gesteine eingedrungen ist (Intrusionen, z. Bsp.: Granit). Intrusivgesteine sind daher an großen Mineralen erkennbar. 2) Werden auch Vulkanite genannt, entstehen nach der Eruption aus einem Vulkan an Land oder im Meer. Erkennbar an ihrer feinkörnigen oder glasigen Grundmasse: z. Bsp.: Basalt oder vulkanische Gläser 32) Nennen Sie die häufigsten M. der 1. magmatischen 2. metamorphen und 3. Sedimentgesteine! 1: Quarz, Feldspat, Glimmer, Pyroxen, Amphibol, Olivin (QfeGLIMpyAMol) 2: Quarz, Feldspat, Glimmer, Pyroxen, Granulit, Granat, Staurolith, Disthen (QfeGLIMpyGRAstauDIS) 3: Quarz, Tonminerale, Feldspäte, Gips, Kalzit, Dolomit, Steinsalz 33) Nach welcher Prozesssequenz entstehen Sedimentgesteine? Welche Arten gibt es? Prozesssequenz: Verwitterung (zunächst eher physikalisch, dann zunehmend chemisch), Abtragung, Transport, Sedimentation, Versenkung, Diagenese Siliciklastische S.: mechanisch abgelagerte Sedimentpartikel, die vom Wind, Wasser und Eis transportiert wurden und Schichten aus Kies, Sand, Silt (Schluff) oder Ton bilden. Chemisch-Biogenen S.: Entstehen mit der Ausfällung, sofern bei der Verwitterung der Gesteine einige ihrer
6 Bestandteile in Lösung gehen und mit dem Flusswasser in das Meer verfrachtet werden, in dem es zur Ausfällung kommen kann. Bsp.: Mineralische Lagen aus Steinsalz oder Calcit. Calciumcarbonat wird häufig in Form von Schalen gefunden. Sedimentgesteine sind oft das einzige Archiv für geologische Ereignisse & Prozesse Bedecken fast 100% des Meeresbodens, 75% der Landflächen aber nur 5% der Erdkruste 34) Diagenese und Lithifizierung: Was versteht man unter (1) Kompaktion und (2) Zementation? Welche Minerale wirken zementierend bzw. verkittend? 1) überlagerndes Gewicht drückt Sedimente zusammen 2) Durch Ausfällung neu gebildeter Minerale in den Räumen zwischen den abgelagerten Komponenten, werden diese verkittet und fester. Kompaktion und Zementation setzt erst bei Überlagerung von anderen Sedimenten ein. Daher sind Sandsteine das Ergebnis der Diagenese von Sandkörnern und Kalksteine die Folge der Diagenese von Sedimentpartikeln aus Calciumcarbonat. Zementierend: Quarz, Kalzit,.. 35) Was versteht man unter geschichteten Sedimenten? S., die geschichtet sind. - Schichtung nach Mineralogie: Tonsteine wechseln mit Kalksteinen ab - Schichtung nach Gefüge: Grobkörnig wechselt mit feinkörnig ab - Schichtung kann: horizontal oder schräg sein. Keine Schichtung ist auch ein Merkmal. - Schichtung kann eine Gradierung sein: normal (unten grob, oben fein), invers, oder nicht gradiert 36) Was sind die meisten auftretenden Gesteine auf der Erdoberfläche? Sedimentgesteine. Verglichen mit den metamorphen bzw. magmatischen G., sind ihre Mächtigkeit und Volumina aber sehr gering. 37) Nennen Sie häufige Minerale der siliciklastischen Sedimente! Silicate: Sie kommen gehäuft in den Gesteinen vor, die später zur Bildung von Sedimenten beitragen: Quarz, Feldspate, Glimmer, usw. 38) Nennen Sie Sedimentationsräume! - Delta, See, Meer, Kontinentalhang, Schelf, Sümpfe, Korallenriffe, 39) Was sind häufigste Minerale der chemisch-biogenen Sedimente? Carbonatgesteine wie Calcit, dem Hauptbestandteil der Kalksteine, oder Dolomit, ein Calcium-Magnesium Carbonat. Gips und Steinsalz sind das Ergebnis rein chemischer Ausfällung durch Verdunstung. 40) Wie entstehen metamorphe Gesteine? (Metamorphite) - durch Änderung des Mineralbestandes, der ch. Zusammensetzung und des Gefüges im festen Zustand unter dem Einfluss hoher T und P-Werte tief im Erdinneren ohne den Vorgang des Schmelzens. Sie entstehen aus allen Gesteinsarten. Der Vorgang der Metamorphose findet schon bei T über 250 Grad statt. 41) Welche 5 Hauptarten der Metamorphose gibt es? Was sind Leitmetamorphite für bestimmte Metamorphosen? - Kontaktm.: An den Rändern von Magmenintrusionen werden bei hohen T die Gesteine unmittelbar am Kontakt mit der heißen Magma und in der angrenzenden Zone verändert. Hornfels - Regionalm.: Bei Plattenkollisionen, wenn sich in ausgedehnten Bereichen hohe T und P- Bedingungen einstellen. Glimmerschiefer - Ultrahochdruckm.: Beschränkt auf die tiefen Bereiche der kontinentalen Lithosphäre und der ozeanischen Kruste. Eklogit - Hochdruck-Niedrigtemperaturm.: kommt vor, wo ozeanische Kruste unter dem Rand einer kontinentalen Platte subduziert wird. Glaukophanschiefer - Impactmetamorphose: durch Einschlag eines Meteoriten: Extrem hohe Drücke und Temperaturen: Leitmineral: Coesit 42) Was sind gute Leitminerale für eine vorliegende Metamorphose? Granat, Staurolith, Disthen 43) Beschreiben Sie den Kreislauf der Gesteine bildhaft! 44) Inwieweit steht das System Klima mit dem Gesteinskreislauf im Zusammenhang? Je mehr durch Regen und Wind erodiert wird, desto schneller heben sich Gebirge durch Druckentlasung. Ändert sich also der Niederschlag oder der Wind, hat das Auswirkungen auf die Hebungsrate von Gebirgen. Ebenso können schnelle Hebungsraten wieder die globale Zirkulation beeinflussen -> Bsp: Rocky Mountains als Initialauslöse für unsere 3 bis 5 Rossbywellen, inkl. Tiefdruckbahnen und Druckverteilungen.
7 45) Was sind Erze? Minerale, die Metalle enthalten. Dazu gehören Sulfide, Oxide und Silicate, dh. Verbindungen von metallischen Elementen mit Sauerstoff, Schwefel und Silicium. 46) Was sind 1. Gang, 2. Imprägnations, 3. Magmatische und 3. Sedimentäre Lagerstätten? 1: Durch hydrothermale Lösungen im zerklüfteten Gestein, kommt es zur Abscheidung von Erzmineralen. In den Spalten können die Lösungen schnell eindringen, was eine rasche Abkühlung der Lösung und Ausscheidung der Erzminerale begünstigt. Die Ganglagerstätten sind häufig platten- oder schichtförmig auf Spalten oder Klüften. Hydrothermale Gänge zählen zu den wichtigsten Lagerstätten von Metallen, wie z. Bsp. Gold. 2: Lagerstätten, in denen die Erze über größere Ausbreitung fein verteilt sind. Solche L. bilden sich oft in geologischen Räumen, in denen es häufig zu Intrusionen kommt, die meist große Intrusivkörper bilden. 3: Sie treten in Form von gravitativer Entmischung von Erzmineralen in den bodennahen Bereichen der Intrusionen auf. Diese L. entstehen, wenn Minerale mit niedriger Schmelztemperatur bereits zu einem frühen Zeitpunkt aus dem Magma auskristallisieren und sich am Boden der Magenkammer anreichern. 4: Viele wichtige wirtschaftliche L. reichen sich durch sedimentäre Prozesse an. Sie bilden wichtige Vorkommen von Kupfer, Eisen und anderen Metallen. Seifenlagerstätten sind Erzlagerstätten, die in Flüssen oder vereinzelt auch an Stränden durch mechanische Sortierungsvorgänge von Strömungen angereichert werden.
Einführung in die Geologie
 Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke International Geothermal Centre Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und
Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke International Geothermal Centre Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und
Einführung in die Geologie. Mark Feldmann Dr.sc.nat. ETH
 Geologie & Tourismus Einführung in die Geologie Mark Feldmann Dr.sc.nat. ETH Ihr Profi für geo-kulturelle Führungen und Exkursionen Buchholzstrasse 58 8750 Glarus 078 660 01 96 www.geo-life.ch Inhalt Aufbau
Geologie & Tourismus Einführung in die Geologie Mark Feldmann Dr.sc.nat. ETH Ihr Profi für geo-kulturelle Führungen und Exkursionen Buchholzstrasse 58 8750 Glarus 078 660 01 96 www.geo-life.ch Inhalt Aufbau
Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine
 Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke FH Bochum GeothermieZentrum Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und Kristalle
Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke FH Bochum GeothermieZentrum Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und Kristalle
Übungen zur Allgemeinen Geologie, Nebenfach. Erta Ale, Afrika
 Übungen zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Minerale anorganisch, (natürlich) Festkörper definierte chemische Zusammensetzung homogen definiert durch chemische Formel kristallin Physikalische
Übungen zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Minerale anorganisch, (natürlich) Festkörper definierte chemische Zusammensetzung homogen definiert durch chemische Formel kristallin Physikalische
Gesteinskunde Einführung
 Gesteinskunde Einführung Christopher Giehl, Uni Tübingen 13.10.2011 Christopher Giehl (Universität Tübingen) 13.10.2011 1 / 23 1 Organisatorisches 2 Kursinhalte und -ziele 3 Grundbegriffe und Definitionen
Gesteinskunde Einführung Christopher Giehl, Uni Tübingen 13.10.2011 Christopher Giehl (Universität Tübingen) 13.10.2011 1 / 23 1 Organisatorisches 2 Kursinhalte und -ziele 3 Grundbegriffe und Definitionen
Entstehung der Gesteine
 Entstehung der Gesteine Entstehung der Gesteine In der Natur unterliegen die Gesteine verschiedenen, in enger Beziehung zueinander stehenden geologischen Prozessen wie Kristallisation, Hebung, Verwitterung,
Entstehung der Gesteine Entstehung der Gesteine In der Natur unterliegen die Gesteine verschiedenen, in enger Beziehung zueinander stehenden geologischen Prozessen wie Kristallisation, Hebung, Verwitterung,
FOS: Radioaktivität und Strahlenschutz. Chemische Elemente und ihre kleinsten Teilchen
 R. Brinkmann http://brinkmann-du.de Seite 5..03 Chemische Elemente FOS: Radioaktivität und Strahlenschutz Chemische Elemente und ihre kleinsten Teilchen Der Planet Erde besteht aus 9 natürlich vorkommenden
R. Brinkmann http://brinkmann-du.de Seite 5..03 Chemische Elemente FOS: Radioaktivität und Strahlenschutz Chemische Elemente und ihre kleinsten Teilchen Der Planet Erde besteht aus 9 natürlich vorkommenden
Unterrichtsmaterial zur Stoff-Separation einer heterogenen Mischung am Beispiel von Granit
 Unterrichtsmaterial zur Stoff-Separation einer heterogenen Mischung am Beispiel von Granit Inhalt (je 6x) Granit Schraubdeckelgläser mit Granitsplitter Quarz Alkalifeldspat Plagioklas Schraubdeckelgläser
Unterrichtsmaterial zur Stoff-Separation einer heterogenen Mischung am Beispiel von Granit Inhalt (je 6x) Granit Schraubdeckelgläser mit Granitsplitter Quarz Alkalifeldspat Plagioklas Schraubdeckelgläser
Gesteinskunde. Bestimmung magmatischer Minerale. Christopher Giehl, Uni Tübingen 20.10.2011
 Gesteinskunde Bestimmung magmatischer Minerale Christopher Giehl, Uni Tübingen 20.10.2011 Christopher Giehl (Universität Tübingen) 20.10.2011 1 / 18 1 Wiederholung 2 Klassifikation magmatischer Gesteine
Gesteinskunde Bestimmung magmatischer Minerale Christopher Giehl, Uni Tübingen 20.10.2011 Christopher Giehl (Universität Tübingen) 20.10.2011 1 / 18 1 Wiederholung 2 Klassifikation magmatischer Gesteine
Bohrsches Atommodell
 Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
Beispielklausur Geochemie I Mineralogie (Anteil Schertl)
 Beispielklausur Geochemie I Mineralogie (Anteil Schertl) 1. Wichtig zum Verständnis der Kristallchemie von Mineralen sind Wertigkeiten und Ionenradien von Elementen. a. Geben Sie die Wertigkeiten folgender
Beispielklausur Geochemie I Mineralogie (Anteil Schertl) 1. Wichtig zum Verständnis der Kristallchemie von Mineralen sind Wertigkeiten und Ionenradien von Elementen. a. Geben Sie die Wertigkeiten folgender
Einführung in die Geowissenschaften I Geomaterialien Teil II WS 2016/2017
 Einführung in die Geowissenschaften I Geomaterialien Teil II WS 2016/2017 13. Dez. Kristallchemie der Silikate Was ist ein Mineral? Was ist ein Gestein? Gesteinsbildende Minerale 20. Dez Das System Erde:
Einführung in die Geowissenschaften I Geomaterialien Teil II WS 2016/2017 13. Dez. Kristallchemie der Silikate Was ist ein Mineral? Was ist ein Gestein? Gesteinsbildende Minerale 20. Dez Das System Erde:
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Experimente zum Kreis-Lauf der Gesteine. Aufbau der Erde
 Experimente zum Kreis-Lauf der Gesteine Aufbau der Erde Foto Nasa Male das Schnitt-Bild auf das Papier 1 Erdapfel Du hast 1 Apfel-Hälfte, Becher mit Wasser, Pinsel und 1 Tusch-Kasten Bemale dein Apfel-Kern
Experimente zum Kreis-Lauf der Gesteine Aufbau der Erde Foto Nasa Male das Schnitt-Bild auf das Papier 1 Erdapfel Du hast 1 Apfel-Hälfte, Becher mit Wasser, Pinsel und 1 Tusch-Kasten Bemale dein Apfel-Kern
Ökopedologie I + II. Einführung in die Mineralogie und Gesteinskunde
 Ökopedologie I + II Einführung in die Mineralogie und Gesteinskunde Minerale - Definition Minerale sind stofflich einheitliche (physikalisch und chemisch homogene), feste, anorganische, meist natürlich
Ökopedologie I + II Einführung in die Mineralogie und Gesteinskunde Minerale - Definition Minerale sind stofflich einheitliche (physikalisch und chemisch homogene), feste, anorganische, meist natürlich
Der Granit 200 Jahre nach Goethe
 Sonderdrucke aus der Albert-Ludwigs-Universität Freiburg WOLFHARD WIMMENAUER Der Granit 200 Jahre nach Goethe Originalbeitrag erschienen in: Jahrbuch der Heidelberger Akademie der Wissenschaften (1992),
Sonderdrucke aus der Albert-Ludwigs-Universität Freiburg WOLFHARD WIMMENAUER Der Granit 200 Jahre nach Goethe Originalbeitrag erschienen in: Jahrbuch der Heidelberger Akademie der Wissenschaften (1992),
Atomaufbau. Elektronen e (-) Atomhülle
 Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
Atomaufbau Institut für Elementarteilchen Nukleonen Protonen p (+) Neutronen n (o) Elektronen e (-) Atomkern Atomhülle Atom WIBA-NET 2005 Prof. Setzer 1 Elementarteilchen Institut für Name Symbol Masse
Bauchemie 1. 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle?
 Bauchemie 1 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle? a) Der Atomkern besteht aus Neutronen und Protonen, die zusammen auch Nukleonen genannt werden. Er befindet sich
Bauchemie 1 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle? a) Der Atomkern besteht aus Neutronen und Protonen, die zusammen auch Nukleonen genannt werden. Er befindet sich
Die Bestimmung gesteinsbildender Minerale
 7 2 Die Bestimmung gesteinsbildender Minerale 2.1 Definition 8 2.2 Mineralgliederung 8 2.3 Mineraleigenschaften 8 2.4 Gesteinsbildende Minerale 9 U. Sebastian, Gesteinskunde, DOI 10.1007/978-3-642-41757-3_2,
7 2 Die Bestimmung gesteinsbildender Minerale 2.1 Definition 8 2.2 Mineralgliederung 8 2.3 Mineraleigenschaften 8 2.4 Gesteinsbildende Minerale 9 U. Sebastian, Gesteinskunde, DOI 10.1007/978-3-642-41757-3_2,
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Strahlung
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Strahlung Das komplette Material finden Sie hier: Download bei School-Scout.de SCHOOL-SCOUT
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Strahlung Das komplette Material finden Sie hier: Download bei School-Scout.de SCHOOL-SCOUT
Geographie 207: Petrographie
 Geographie 207: Petrographie Sphäre Tiefe Temp. Dichte Aggregatszustand unterteilt in Kruste -70 km -1'000 C 2,8 g/cm 3 fest ozeanisch kontinental Mantel -2900 km 3'700 C 4,6 g/cm 3 viskos / zähplastisch
Geographie 207: Petrographie Sphäre Tiefe Temp. Dichte Aggregatszustand unterteilt in Kruste -70 km -1'000 C 2,8 g/cm 3 fest ozeanisch kontinental Mantel -2900 km 3'700 C 4,6 g/cm 3 viskos / zähplastisch
1. Die Entstehung eines Planeten
 1. Die Entstehung eines Planeten 1.1 Die Entstehung eines Sonnensystems Die Wolke, aus der unser Sonnensystem entstand, wird als solarer Urnebel bezeichnet (Abb. 1.4 S.7) Dieser wurde von der Schwerkraft
1. Die Entstehung eines Planeten 1.1 Die Entstehung eines Sonnensystems Die Wolke, aus der unser Sonnensystem entstand, wird als solarer Urnebel bezeichnet (Abb. 1.4 S.7) Dieser wurde von der Schwerkraft
Der Kreislauf der Gesteine
 2 Der Kreislauf der Gesteine All die faszinierenden Mineralien und Fossilien, die Sie im Folgenden noch kennenlernen werden, entstehen über viele Millionen Jahre durch geologische Prozesse. Unsere Erdkugel
2 Der Kreislauf der Gesteine All die faszinierenden Mineralien und Fossilien, die Sie im Folgenden noch kennenlernen werden, entstehen über viele Millionen Jahre durch geologische Prozesse. Unsere Erdkugel
Grundwissen Chemie 9. Klasse SG
 Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Talk Apatit Feldspat Topas. Granat Halit Magnetit Turmalin Härte (Mohs): Härte (Mohs):
 Talk Apatit Feldspat Topas mittlere Volumen Lichtbrechung: Elementarzelle:.-. Talk ist das weichste Mineral, man kann es sogar mit dem Fingernagel ritzen. Zähne und Knochen des Körpers bestehen zu einem
Talk Apatit Feldspat Topas mittlere Volumen Lichtbrechung: Elementarzelle:.-. Talk ist das weichste Mineral, man kann es sogar mit dem Fingernagel ritzen. Zähne und Knochen des Körpers bestehen zu einem
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
Naturstein Lexikon Informationen und Wissenswertes rund um das Thema Naturstein
 Naturstein Lexikon Informationen und Wissenswertes rund um das Thema Naturstein Unser Naturstein Lexikon bietet Informationen und Wissenswertes rund um das Thema Naturstein. Steinsorten, Handelsnamen,
Naturstein Lexikon Informationen und Wissenswertes rund um das Thema Naturstein Unser Naturstein Lexikon bietet Informationen und Wissenswertes rund um das Thema Naturstein. Steinsorten, Handelsnamen,
Bodengeographie. Bodenbildung und Bodenfruchtbarkeit. 1.) Bodenbildung
 Bodengeographie Bodenbildung und Bodenfruchtbarkeit 1.) Bodenbildung B o d e n e n t s t e h u n g B o d e n b e s t a n d t e i l e V e g e t a t i o n T i e r w e l t B O Organische Substanz a.) Humus:
Bodengeographie Bodenbildung und Bodenfruchtbarkeit 1.) Bodenbildung B o d e n e n t s t e h u n g B o d e n b e s t a n d t e i l e V e g e t a t i o n T i e r w e l t B O Organische Substanz a.) Humus:
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie
 Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Robert-Koch-Gymnasium Deggendorf. Grundwissen Chemie. 8. Jahrgangsstufe
 Robert-Koch-Gymnasium Deggendorf Grundwissen Chemie 8. Jahrgangsstufe Teilchenmodell und Stoffeigenschaften Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, vereinfacht dargestellt als Kugeln.
Robert-Koch-Gymnasium Deggendorf Grundwissen Chemie 8. Jahrgangsstufe Teilchenmodell und Stoffeigenschaften Teilchenmodell: Alle Stoffe bestehen aus kleinsten Teilchen, vereinfacht dargestellt als Kugeln.
Grundwissenskatalog Chemie G8 8. Klasse nt
 Grundwissenskatalog Chemie G8 8. Klasse nt 1. Wissenschaft Chemie: Chemie ist die Lehre von den Stoffen. Chemischer Vorgang: Stoffänderung Physikalischer Vorgang: Zustandsänderung 2. Unterteilung Stoffe:
Grundwissenskatalog Chemie G8 8. Klasse nt 1. Wissenschaft Chemie: Chemie ist die Lehre von den Stoffen. Chemischer Vorgang: Stoffänderung Physikalischer Vorgang: Zustandsänderung 2. Unterteilung Stoffe:
Wasservorräte auf der Erde Arbeitsblatt 1
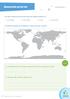 Wasservorräte auf der Erde Arbeitsblatt 1 1. Wo gibt es Süßwasser auf der Erde? Kreuze die richtigen Antworten an. In den Wolken In der Erdkruste Im Meer Im Gletschereis 2. Schraffiere die Gebiete auf
Wasservorräte auf der Erde Arbeitsblatt 1 1. Wo gibt es Süßwasser auf der Erde? Kreuze die richtigen Antworten an. In den Wolken In der Erdkruste Im Meer Im Gletschereis 2. Schraffiere die Gebiete auf
Atombau. Chemie. Zusammenfassungen. Prüfung Mittwoch, 14. Dezember Elektrische Ladung. Elementarteilchen. Kern und Hülle
 Chemie Atombau Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Elektrische Ladung Elementarteilchen Kern und Hülle Atomsorten, Nuklide, Isotope Energieniveaus und Schalenmodell Steffi Alle saliorel
Chemie Atombau Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Elektrische Ladung Elementarteilchen Kern und Hülle Atomsorten, Nuklide, Isotope Energieniveaus und Schalenmodell Steffi Alle saliorel
Grundwissen Chemie 8. Klasse NTG
 Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
STEOP: System Erde (LV ) Unterstützendes Handoutmaterial zum Themenkomplex 4: Magmatite:
 STEOP: System Erde (LV 280001) Unterstützendes Handoutmaterial zum Themenkomplex 4: Magmatite: Gesteine und Minerale entstanden aus Schmelzen und ihren Folgeprodukten Dieses Handoutmaterial ergänzt die
STEOP: System Erde (LV 280001) Unterstützendes Handoutmaterial zum Themenkomplex 4: Magmatite: Gesteine und Minerale entstanden aus Schmelzen und ihren Folgeprodukten Dieses Handoutmaterial ergänzt die
Chemische Bindung. Chemische Bindung
 Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Sammlung 24 Gesteine (U72015)
 Sammlung 24 Gesteine 1018443 (U72015) Nach der Entstehungsart werden Gesteine in drei Gruppen unterschieden: Magmatite entstehen durch die Erstarrung von Magma in (Plutonite) oder auf (Vulkanite) der Erdkruste.
Sammlung 24 Gesteine 1018443 (U72015) Nach der Entstehungsart werden Gesteine in drei Gruppen unterschieden: Magmatite entstehen durch die Erstarrung von Magma in (Plutonite) oder auf (Vulkanite) der Erdkruste.
Anorganische Chemie! der unbelebten Natur keine Kohlenstoffverbindung (Kohlenstoffatome C) Metall Nichtmetallverbindungen Ionenbindung
 3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
LB1 Stoffe. LB1 Stoffe. LB1 Stoffe. Womit beschäftigt sich die Chemie?
 Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Grundwissen Chemie 9. Jahrgangsstufe Sprachlicher Zweig
 Grundwissen Chemie 9. Jahrgangsstufe Sprachlicher Zweig 1. Stoffeigenschaften und modell a) modell Alle Stoffe bestehen aus kleinsten Die eines Stoffes sind untereinander gleich. Die verschiedener Stoffe
Grundwissen Chemie 9. Jahrgangsstufe Sprachlicher Zweig 1. Stoffeigenschaften und modell a) modell Alle Stoffe bestehen aus kleinsten Die eines Stoffes sind untereinander gleich. Die verschiedener Stoffe
Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm Klasse 9 Themen Das Kern-Hülle-Modell Modell des Atomkerns Die Atomhülle im Energiestufenmodell Elektrische Ladung im Atom Das Kern-Hülle-Modell
Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm Klasse 9 Themen Das Kern-Hülle-Modell Modell des Atomkerns Die Atomhülle im Energiestufenmodell Elektrische Ladung im Atom Das Kern-Hülle-Modell
Einführung in die Geologie. Mark Feldmann Dr.sc.nat. ETH
 Geologie & Tourismus Einführung in die Geologie Mark Feldmann Dr.sc.nat. ETH Ihr Profi für geo-kulturelle Führungen und Exkursionen Buchholzstrasse 58 8750 Glarus 078 660 01 96 www.geo-life.ch Inhalt Aufbau
Geologie & Tourismus Einführung in die Geologie Mark Feldmann Dr.sc.nat. ETH Ihr Profi für geo-kulturelle Führungen und Exkursionen Buchholzstrasse 58 8750 Glarus 078 660 01 96 www.geo-life.ch Inhalt Aufbau
Definiere den Begriff Chemischer Vorgang! Definiere den Begriff Physikalischer Vorgang!
 Chemischer Vorgang! Stoffänderung, keine Zustandsänderung, mit Energiebeteiligung Physikalischer Vorgang! Zustandsänderung, keine Stoffänderung (z.b. Lösen, Aggregatzustände,...) Erkläre die Begriffe heterogenes
Chemischer Vorgang! Stoffänderung, keine Zustandsänderung, mit Energiebeteiligung Physikalischer Vorgang! Zustandsänderung, keine Stoffänderung (z.b. Lösen, Aggregatzustände,...) Erkläre die Begriffe heterogenes
Wasser à. Nachweis: Wasser ist
 Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
0.6 Einfache Modelle der chemischen Bindung
 0.6 Einfache Modelle der chemischen Bindung Ionenbindung Ionenbindungen entstehen durch Reaktion von ausgeprägt metallischen Elementen (Alkalimetalle und Erdalkalimetalle mit geringer Ionisierungsenergie)
0.6 Einfache Modelle der chemischen Bindung Ionenbindung Ionenbindungen entstehen durch Reaktion von ausgeprägt metallischen Elementen (Alkalimetalle und Erdalkalimetalle mit geringer Ionisierungsenergie)
Elektronenpaarbindung (oder Atombindung) Nichtmetallatom + Nichtmetallatom Metallatom + Nichtmetallatom 7. Welche Bindungsart besteht jeweils?
 LÖSUNGEN Probetest 1 Kap. 03 Theorie Name: 1. C = Kohlenstoff Ag = Silber Br = Brom Schwefel = S Lithium = Li Uran = U 2. Aluminium - Finde die richtigen Zahlen mit Hilfe deines PSE: Massenzahl: 27 Ordnungszahl:
LÖSUNGEN Probetest 1 Kap. 03 Theorie Name: 1. C = Kohlenstoff Ag = Silber Br = Brom Schwefel = S Lithium = Li Uran = U 2. Aluminium - Finde die richtigen Zahlen mit Hilfe deines PSE: Massenzahl: 27 Ordnungszahl:
Magische Kristalle Prof. Dr. R. Glaum
 Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
1. Die Entstehung eines Planeten
 1. Die Entstehung eines Planeten 1.1 Die Entstehung des Sonnensystems Vor etwa 15 bis 20 Milliarden Jahren entstand unser Universum mit einer kosmischen Explosion (Urknall). Vor diesem Zeitpunkt war die
1. Die Entstehung eines Planeten 1.1 Die Entstehung des Sonnensystems Vor etwa 15 bis 20 Milliarden Jahren entstand unser Universum mit einer kosmischen Explosion (Urknall). Vor diesem Zeitpunkt war die
Kochsalz-Kristalle (Halit) Wichtige Stoffgruppen Atomverband Stoffgruppe Metall Metall: Metallische Stoffe Salzartige Stoffe Metall Nichtmetall:
 Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
K-Feldspat + Wasser + Kohlensäure Kaolinit + gelöstes Hydrogencarbonat + gelöstes Kalium + gelöste Kieselsäure
 Hydrolyse 20 K-Feldspat + Wasser + Kohlensäure Kaolinit + gelöstes Hydrogencarbonat + gelöstes Kalium + gelöste Kieselsäure 2KAlSi 3 O 8 + H 2 O + 2H 2 CO 3 Al 2 Si 2 O 5 (OH) 4 + 2HCO 3 - + 2K + + 4SiO
Hydrolyse 20 K-Feldspat + Wasser + Kohlensäure Kaolinit + gelöstes Hydrogencarbonat + gelöstes Kalium + gelöste Kieselsäure 2KAlSi 3 O 8 + H 2 O + 2H 2 CO 3 Al 2 Si 2 O 5 (OH) 4 + 2HCO 3 - + 2K + + 4SiO
Unterrichtsmaterial zum Modul Symmetrie
 Unterrichtsmaterial zum Modul Symmetrie Inhalt (je 4x) Alkalifeldspat (Prisma - monoklin) Kalkspat/Calcit (Rhomboeder - trigonal) Apatit (Prisma & Pyramide - hexagonal) Quarz (Prisma & Pyramide - trigonal)
Unterrichtsmaterial zum Modul Symmetrie Inhalt (je 4x) Alkalifeldspat (Prisma - monoklin) Kalkspat/Calcit (Rhomboeder - trigonal) Apatit (Prisma & Pyramide - hexagonal) Quarz (Prisma & Pyramide - trigonal)
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Atombau und PSE. Das komplette Material finden Sie hier: School-Scout.
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Atombau und PSE Das komplette Material finden Sie hier: School-Scout.de Chemiekonzept Pro Unterrichtsreihen Sekundarstufe I Band 11
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Atombau und PSE Das komplette Material finden Sie hier: School-Scout.de Chemiekonzept Pro Unterrichtsreihen Sekundarstufe I Band 11
1 Chemische Elemente und chemische Grundgesetze
 1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
Gebrauchsanweisung für Lehrkräfte
 Materialien entwickelt und zusammengestellt von Claudia Holtermann, Geographielehrerin am Friedrich-Dessauer- Gymnasium in Aschaffenburg Gebrauchsanweisung für Lehrkräfte 1. Vor der Untersuchung der Gesteine
Materialien entwickelt und zusammengestellt von Claudia Holtermann, Geographielehrerin am Friedrich-Dessauer- Gymnasium in Aschaffenburg Gebrauchsanweisung für Lehrkräfte 1. Vor der Untersuchung der Gesteine
Kerncurriculum und Schulcurriculum (2 Wochenstunden) Themen und Inhalte. Bezug zu den Standards. Kerncurriculum / Schulcurriculum
 Chemie: Klasse 9 Kerncurriculum und Schulcurriculum (2 Wochenstunden) Zeit Themen und Inhalte Umsetzung Bezug zu den Standards Kerncurriculum / Schulcurriculum 10 Atombau und Periodensystem - Das Kern-Hülle-Modell
Chemie: Klasse 9 Kerncurriculum und Schulcurriculum (2 Wochenstunden) Zeit Themen und Inhalte Umsetzung Bezug zu den Standards Kerncurriculum / Schulcurriculum 10 Atombau und Periodensystem - Das Kern-Hülle-Modell
Werkstoffkunde Chemische Bindungsarten
 Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
MAGNESIUM. 1. Bei Verbrennungsreaktionen entstehen in der Regel (kreuze richtig an):
 MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Grundlagen der Chemie Metalle
 Metalle Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Metalle 75% aller chemischen Elemente sind Metalle. Typische
Metalle Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Metalle 75% aller chemischen Elemente sind Metalle. Typische
Übungen zur Allgemeinen Geologie, Nebenfach
 zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Übungstermine und Themen Termine Einführungsstunde Übung 26.10.2010 Einführung + Mineral- Eigenschaften Gruppeneinteilung 02.11. 2010 Minerale 1 Eigenschaften
zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Übungstermine und Themen Termine Einführungsstunde Übung 26.10.2010 Einführung + Mineral- Eigenschaften Gruppeneinteilung 02.11. 2010 Minerale 1 Eigenschaften
Vom Ton zum Porzellan
 Vom Ton zum Porzellan Ein Streifzug vom Rohstoff zum Produkt Matthias Göbbels Historischer Überblick I Fasern 9000 Lehmziegel 0 Irdengut - Keramik 7000 Hanf 5000 Töpferscheibe 3500 Glasuren 3000 Seide,
Vom Ton zum Porzellan Ein Streifzug vom Rohstoff zum Produkt Matthias Göbbels Historischer Überblick I Fasern 9000 Lehmziegel 0 Irdengut - Keramik 7000 Hanf 5000 Töpferscheibe 3500 Glasuren 3000 Seide,
Grundwissenkarten Hans-Carossa-Gymnasium. 9. Klasse. Chemie SG
 Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Teilchenmodell. Aggregatzustände. Diffusion. Spezifische Eigenschaften = Stoffeigenschaften
 Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser Bewegung (Brownsche Bewegung),
Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser Bewegung (Brownsche Bewegung),
2 Bindung, Struktur und Eigenschaften von Stoffen. 2.1 Ionenbindung und Ionenkristall s Modell der Ionenbindung
 2 Bindung, Struktur und Eigenschaften von Stoffen 2.1 Ionenbindung und Ionenkristall s. 0.6 Modell der Ionenbindung 8 - Bindung zwischen typischen Metallen und Nichtmetallen, EN > 1,7 - stabile Edelgaskonfiguration
2 Bindung, Struktur und Eigenschaften von Stoffen 2.1 Ionenbindung und Ionenkristall s. 0.6 Modell der Ionenbindung 8 - Bindung zwischen typischen Metallen und Nichtmetallen, EN > 1,7 - stabile Edelgaskonfiguration
6-10 LEBENSRAUM GESTEINSARTEN SACH INFORMATION MAGMATISCHES GESTEIN SEDIMENTGESTEIN
 SACH INFORMATION Jede/r kann spontan einige Gesteinsarten aufzählen, diese lassen sich in drei Großgruppen einteilen. Der/die GeologIn unterscheidet zwischen magmatischem, Sediment- und metamorphem Gestein.
SACH INFORMATION Jede/r kann spontan einige Gesteinsarten aufzählen, diese lassen sich in drei Großgruppen einteilen. Der/die GeologIn unterscheidet zwischen magmatischem, Sediment- und metamorphem Gestein.
Alle Stoffe bestehen aus kleinen Teilchen, die sich bewegen. Je mehr Energie sie besitzen, desto mehr bewegen sie sich.
 Grundwissen 8. Klasse 1. Stoffe und Teilchen Teilchenmodell: Atome Ionen Alle Stoffe bestehen aus kleinen Teilchen, die sich bewegen. Je mehr Energie sie besitzen, desto mehr bewegen sie sich. von atomos
Grundwissen 8. Klasse 1. Stoffe und Teilchen Teilchenmodell: Atome Ionen Alle Stoffe bestehen aus kleinen Teilchen, die sich bewegen. Je mehr Energie sie besitzen, desto mehr bewegen sie sich. von atomos
Chemie Zusammenfassung III
 Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann und dessen Teilchen(Atome oder Moleküle) aus einer einzigen Atomart (d.h. Teilchen mit gleicher Ordnungszahl) besteht. Verbindung Reinstoff,
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann und dessen Teilchen(Atome oder Moleküle) aus einer einzigen Atomart (d.h. Teilchen mit gleicher Ordnungszahl) besteht. Verbindung Reinstoff,
Ionenbindungen. Chemie. Library
 Chemie Ionenbindungen Library IONENBINDUNGEN Begriffserklärung 1 Formeltabelle 1 Ladungsermittlung 2 Formale Ladung 3 Hydrogen-Ionen 3 Verhältnisformeln 4 Nomenklatur 4 Gitterenthalpie 4 Eigenschaften
Chemie Ionenbindungen Library IONENBINDUNGEN Begriffserklärung 1 Formeltabelle 1 Ladungsermittlung 2 Formale Ladung 3 Hydrogen-Ionen 3 Verhältnisformeln 4 Nomenklatur 4 Gitterenthalpie 4 Eigenschaften
Aufgreifen von Schülervorstellungen im Sachunterricht am Beispiel Steine
 Aufgreifen von Schülervorstellungen im Sachunterricht am Beispiel Steine Rodgau, 24. September 2010 Birgit Harder, IPN Kiel http://www.ipn.uni-kiel.de http://www.nawi5-6.de Übersicht (Schüler-) Vorstellungen
Aufgreifen von Schülervorstellungen im Sachunterricht am Beispiel Steine Rodgau, 24. September 2010 Birgit Harder, IPN Kiel http://www.ipn.uni-kiel.de http://www.nawi5-6.de Übersicht (Schüler-) Vorstellungen
Grundlagen. Maximilian Ernestus Waldorfschule Saarbrücken
 Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Grundlagen Chemie. Dipl.-Lab. Chem. Stephan Klotz. Freiwill ige Feuerwehr Rosenheim
 Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Erläutere den CO 2 -Nachweis. Definiere den Begriff exotherme Reaktion und zeichne ein passendes Energiediagramm. Grundwissenskatalog Chemie 8 NTG
 Erläutere den CO 2 -Nachweis. Wird das Gas in Kalkwasser (Ca(OH) 2 ) eingeleitet bildet sich ein schwerlöslicher Niederschlag von Calciumcarbonat (CaCO 3 ). Abgabe von innerer Energie (Wärme, Knall,...)
Erläutere den CO 2 -Nachweis. Wird das Gas in Kalkwasser (Ca(OH) 2 ) eingeleitet bildet sich ein schwerlöslicher Niederschlag von Calciumcarbonat (CaCO 3 ). Abgabe von innerer Energie (Wärme, Knall,...)
Chemie Grundwissen der neunten Jahrgangsstufe (SG)
 hemie Grundwissen der neunten Jahrgangsstufe (SG) hemie ist die Lehre von den Stoffen und den Stoffänderungen Alle Materie besteht aus kleinsten Teilchen. Sie können sich in ihrer Masse bzw. Größe unterscheiden
hemie Grundwissen der neunten Jahrgangsstufe (SG) hemie ist die Lehre von den Stoffen und den Stoffänderungen Alle Materie besteht aus kleinsten Teilchen. Sie können sich in ihrer Masse bzw. Größe unterscheiden
Atomphysik Klasse 9. Aufgabe: Fülle die freien Felder aus!
 1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
Grundwissen Chemie 8I
 1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen
 Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu?
Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu?
Freie Elektronen bilden ein Elektronengas. Feste positive Aluminiumionen. Abb. 1.1: Metallbindung: Feste Atomrümpfe und freie Valenzelektronen
 1 Grundlagen 1.1 Leiter Nichtleiter Halbleiter 1.1.1 Leiter Leiter sind generell Stoffe, die die Eigenschaft haben verschiedene arten weiterzuleiten. Im Folgenden steht dabei die Leitfähigkeit des elektrischen
1 Grundlagen 1.1 Leiter Nichtleiter Halbleiter 1.1.1 Leiter Leiter sind generell Stoffe, die die Eigenschaft haben verschiedene arten weiterzuleiten. Im Folgenden steht dabei die Leitfähigkeit des elektrischen
11. Kernphysik. [55] Ianus Münze
![11. Kernphysik. [55] Ianus Münze 11. Kernphysik. [55] Ianus Münze](/thumbs/52/29657300.jpg) 11. Kernphysik Der griechische Gott Ianus ist einer der ältesten römischen Gottheiten. Er gehört zur rein römischen Mythologie, das heißt es gibt in der griechischen Götterwelt keine vergleichbare Gestalt.
11. Kernphysik Der griechische Gott Ianus ist einer der ältesten römischen Gottheiten. Er gehört zur rein römischen Mythologie, das heißt es gibt in der griechischen Götterwelt keine vergleichbare Gestalt.
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
EDUKTE PRODUKTE. Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Reagiert zu
 L2 1 Chemische Reaktion, Energetik Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Ausgangsstoff e EDUKTE Reagiert zu Endstoffe
L2 1 Chemische Reaktion, Energetik Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Ausgangsstoff e EDUKTE Reagiert zu Endstoffe
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
1. Endogene Dynamik. 2. Minerale und Gesteine
 Fragenkatalog zur Geologie (Endversion Juli 2015) 1 1. Endogene Dynamik 1.) Die Erde ist nur näherungsweise eine Kugel. a. Wodurch werden die unterschiedlichen Radien an Pol und Äquator verursacht? b.
Fragenkatalog zur Geologie (Endversion Juli 2015) 1 1. Endogene Dynamik 1.) Die Erde ist nur näherungsweise eine Kugel. a. Wodurch werden die unterschiedlichen Radien an Pol und Äquator verursacht? b.
Diese Unterlagen dienen gemäß 53, 54 URG ausschließlich der Ausbildung an der Hochschule Bremen.
 WERK Werkstofftechnik Grundlagen Diese Unterlagen dienen gemäß 53, 54 URG ausschließlich der Ausbildung an der Hochschule Bremen. M + ENTEC -Vorlesung im SS - Klausur am Ende des SS - Klausurteilnahme
WERK Werkstofftechnik Grundlagen Diese Unterlagen dienen gemäß 53, 54 URG ausschließlich der Ausbildung an der Hochschule Bremen. M + ENTEC -Vorlesung im SS - Klausur am Ende des SS - Klausurteilnahme
Atomverbände. In stabilen Verbindungen, die auf der Erde existieren besitzen die Elemente meist die Elektronenkonfiguration
 Atomverbände Möglichkeit 1: Abgabe von Elektronen bei gleichzeitiger Aufnahme durch einen Reaktionspartner --> SALZE In stabilen Verbindungen, die auf der Erde existieren besitzen die Elemente meist die
Atomverbände Möglichkeit 1: Abgabe von Elektronen bei gleichzeitiger Aufnahme durch einen Reaktionspartner --> SALZE In stabilen Verbindungen, die auf der Erde existieren besitzen die Elemente meist die
Auf der rechten Seite sind Beispiele für kovalente Bindungen.
 Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Grundwissen 8. Klasse Chemie (NTG) Stoffebene. Teilchenebene. Reinstoffe. Kenneigenschaften von Reinstoffen
 Grundwissen 8. Klasse Chemie (NTG) Stoffebene Teilchenebene = Makroskopische (sichtbare) Ebene Betrachtung einer Stoffportion mit den erkennbaren und messbaren Eigenschaften Sie ermöglicht Aussagen über
Grundwissen 8. Klasse Chemie (NTG) Stoffebene Teilchenebene = Makroskopische (sichtbare) Ebene Betrachtung einer Stoffportion mit den erkennbaren und messbaren Eigenschaften Sie ermöglicht Aussagen über
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Element. Verbindung. Reinstoff. Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
bestimmte mehratomige Anionen mit Sauerstoff werden mit dem lateinischen Namen benannt und enden auf at.
 DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
Grundwissen 9. Klasse Chemie
 Grundwissen 9. Klasse Chemie 1. Formelzeichen und Einheiten 2. Was versteht man unter der Stoffmenge und der Avogadro- Konstante N A? Eine Stoffportion hat die Stoffmenge n = 1 mol, wenn sie 6 * 10 23
Grundwissen 9. Klasse Chemie 1. Formelzeichen und Einheiten 2. Was versteht man unter der Stoffmenge und der Avogadro- Konstante N A? Eine Stoffportion hat die Stoffmenge n = 1 mol, wenn sie 6 * 10 23
4 Boden. 4.1 Grundlagen. Boden mit charakteristischen Bodenhorizonten Bodenprofil Bodentyp. Aufbau und Zusammensetzung
 4 Boden 4.1 Grundlagen Aufbau und Zusammensetzung Lithosphäre - feste Gesteinshülle, ca. 100 km dick (griech. lithos, Stein; lat. sphaira, Kugel) Pedosphäre - Bodenhülle, wenige Dezimeter bis einige Meter
4 Boden 4.1 Grundlagen Aufbau und Zusammensetzung Lithosphäre - feste Gesteinshülle, ca. 100 km dick (griech. lithos, Stein; lat. sphaira, Kugel) Pedosphäre - Bodenhülle, wenige Dezimeter bis einige Meter
Atomverband mit festem Atomzahlverhältnis. Anzahl der Atome veränderlich? (bei festem Atomzahlverhältnis) Elektrisch Leitend?
 L3 1 Atomverband mit festem Atomzahlverhältnis. Ja Anzahl der Atome veränderlich? (bei festem Atomzahlverhältnis) Nein Ja Elektrisch Leitend? Nur in der Schmelze? Nein Ionenkristall Beliebig erweiterbar
L3 1 Atomverband mit festem Atomzahlverhältnis. Ja Anzahl der Atome veränderlich? (bei festem Atomzahlverhältnis) Nein Ja Elektrisch Leitend? Nur in der Schmelze? Nein Ionenkristall Beliebig erweiterbar
Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1. Grundwissen 9.Klasse SG 2 Grundwissen 9.Klasse SG 2. Stoffebene.
 Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp.,
Grundwissen 9.Klasse SG 1 Grundwissen 9.Klasse SG 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp.,
Grundwissen 8.Klasse 1 Grundwissen 8.Klasse 1. Grundwissen 8.Klasse 2 Grundwissen 8.Klasse 2. Stoffebene. Teilchen -ebene
 Grundwissen 8.Klasse 1 Grundwissen 8.Klasse 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp., Löslichkeit,
Grundwissen 8.Klasse 1 Grundwissen 8.Klasse 1 Stoff Reinstoff mischen Gemisch Einteilung der Stoffe Bei gleichen Bedingungen (Temp., Druck) immer gleiche Eigenschaften (z.b. Schmelz- /Siedetemp., Löslichkeit,
Unterschied zwischen Physik und Chemie:
 Unterschied zwischen Physik und Chemie: Der Begriff Physik bezeichnet die Lehre über Zustände und Zustandsänderungen die Chemie hingegen beschäftigt sich mit Stoffen und stofflichen Veränderungen. Unterteilung
Unterschied zwischen Physik und Chemie: Der Begriff Physik bezeichnet die Lehre über Zustände und Zustandsänderungen die Chemie hingegen beschäftigt sich mit Stoffen und stofflichen Veränderungen. Unterteilung
1. H 2 O Grundlagen Thermodynamik 2. Lösung / Fällung Silicium, Aluminium 3. Natrium, Kalium Ionenaustausch
 Institut für Geologie Lehrstuhl für Hydrogeologie Vorlesung Grundwasserbeschaffenheit 1. H 2 O Grundlagen Thermodynamik 2. Lösung / Fällung Silicium, Aluminium 3. trium, Kalium Ionenaustausch Prof. B.
Institut für Geologie Lehrstuhl für Hydrogeologie Vorlesung Grundwasserbeschaffenheit 1. H 2 O Grundlagen Thermodynamik 2. Lösung / Fällung Silicium, Aluminium 3. trium, Kalium Ionenaustausch Prof. B.
