Stoffklassen in der Organischen Chemie. Nomenklaturfragen. Isomerie und sterischer Bau
|
|
|
- Anneliese Schmitt
- vor 7 Jahren
- Abrufe
Transkript
1 Stoffklassen in der Organischen Chemie Nomenklaturfragen Isomerie und sterischer Bau 1
2 Stoffklassen in der organischen Chemie Kohlenwasserstoffe Kohlenwasserstoffe mit Substituenten Y (eteroatom oder funktionelle Gruppe) heterocyclische Verbindungen 2
3 Vielfalt in der Organischen Chemie Kohlenwasserstoffe kettenförmig ringförmig unverzweigt verzweigt nicht benzoid benzoid gesättigt ungesättigt mit Doppelbindung mit Dreifachbindung 3
4 Vielfalt in der Organischen Chemie Kohlenwasserstoffe kettenförmig ringförmig unverzweigt verzweigt nicht aromatisch aromatisch gesättigt ungesättigt mit Doppelbindung mit Dreifachbindung 4
5 Was sind Aromaten? Ernst ückel ursprünglich: wohlriechende (latein.: aroma = Wohlgeruch) Stoffe, die aus Balsamen, arzen u.a. Naturstoffen gewonnen wurden Nach der ückel- Regel ist auch das Cyclopropeniumkation ein aromatisches System. Cl Cl Cl später: Benzen und alle Benzen- Derivate, d.h. auf alle isocycl. Kohlenstoff-Verb. mit der besonders stabilen symmetrischen Elektronenanordnung des Benzens heute: Ringsystem mit (4n+2) π- Elektronen, planar gebaut (ückel- Regel) 5
6 Verbindungen mit funktionellen Gruppen Einführung von eteroatomen alogenkohlenwasserstoffe Alkohole Phenole Ether Aldehyde (Ox.prod. eines prim. Alkohols) Ketone (Ox.prod. eines sek. Alkohols) Carbonsäuren und deren Derivate R-al R-O Ar-O R-O-R R-CO R-CO-R R-COO RCOOR 6
7 alogenkohlenwasserstoffe O O 2 N C C C 2 O N Chloramphenicol D(-)-threo-2-Dichloracetamido-1-(4- nitrophenyl)-propan-1,3-diol wurde aus Mikroorganismen 1946 isoliert, hemmt die Proteinsynthese, Nitro- und Dichloracetylgruppe sind für biogene Stoffe ungewöhnlich Cl C C Cl O 7
8 Alkohole und Phenole sekundärer Alkohol O O 2 N C C C 2 O N primärer Alkohol Phenol C O 3 CO O Cl C 3 C C C 3 C 3 Cl Butylhydroxyanisol (Radikalfänger) 8
9 Ether 3 C O O 3 C C C 3 C 3 9
10 Aldehyde und Ketone O C C O O C O C C O C 2 O D-Galactose C 2 O C O O C C O C O C 2 O D-Fructose 10
11 Carbonsäuren und Carbonsäurederivate 4-Thia-1-azabicyclo[3.2.0]heptan-7-on R C N O Carbonsäureamid O N 4 1 S C C 3 COO Cyclisches Carbonsäureamid (β-lactamring) Carbonsäure 11
12 Verbindungen mit funktionellen Gruppen Thiole R-S- Thioether/Sulfide R-S-R Sulfonsäuren (Ox.prod. von Thiol) R-SO 3 - Peroxide R-O-O-R Amine R-N 2 Nitroverb. (Ox.prod. von Amin) R-NO 2 12
13 Thiole und Thioether COO 2 N C C 2 S Cystein COO 2 N C C 2 C 2 S C 3 Methionin 13
14 Sulfonsäuren und Peroxide 2 N C RO C O O C OR C 2 O S O O Etherperoxid Taurin im Stierharn nachgewiesen und in Red Bull 14
15 Amine und Nitroverbindungen O O 2 N C C C 2 O Nitrogruppe N C O Aminogruppe? Carbonsäureamid! Cl C Cl 15
16 Amine und Nitroverbindungen COO 2 N C Alle Aminosäuren sind natürlich Amine! C 2 Im Tyrosin findet man auch eine Carboxylgruppe eine Phenylgruppe. O Tyrosin 16
17 eterocyclen Pyran Thiopyran Thiophen Furan O S S O Pyridin Thiophen Furan Pyrrol Pyrimidin N N S N O N 17
18 Nomenklatur Alkane - Alkene - Alkine Anzahl der Kohlenstoffatome in der auptkette bestimmt den Stamm: Meth-, Eth-, Prop-, But-, Pent-, ex-, ept-, Okt- Nur Einfachbindungen: Endung -an Doppelbindung: Endung -en (bzw. -dien, -trien) Dreifachbindung: Endung -in (bzw. -diin etc.) 18
19 Nomenklatur verzweigter Kohlenwasserstoffe auptkette hat die größte Zahl der Kohlenstoffatome Nummerierung muss so erfolgen, dass die Lokanten für die Substituenten möglichst klein werden Bezeichnung der Substituenten leitet sich von der Anzahl der Kohlenstoffatome ab, Endung -yl 7 C 3 C C 5 6 C 3 3 C 1 3 C 3 C 3 C 3 C C 2 C C C C 3 2,3,6-Trimethyl-heptan (und nicht 2,5,6- Trimethyl-heptan) C 3 19
20 Nomenklatur C 3 C 3 3 C C 2 C 2 C C 3 C 3 3 C C C 3 C 2 C 2 C C C2 C 3 C3 2,2-Dimethyl-pentan 2,5,6-Trimethyl-octan C 3 C 3 C 3 C C 3 C 3 C C 3 C 3 C C 3 C 3 C C 3 quartäres C-Atom tertiäres C-Atom sekundäres C-Atom primäres C-Atom 20
21 Trivialnamen für Kohlenwasserstoffgruppen 3 C 3 C 3 C C 3 C C C 2 C 3 3 C C 2 C Isopropyl- 1-Methyl-ethyl- Isobutyl- 2-Methyl-propyl- sec-butyl- 1-Methyl-propyl- tert.-butyl- 1,1-Dimethyl-ethyl C 3 3 C C C 3 Vinyl- Ethenyl- 2 C C 21
22 Nomenklatur von Verbindungen mit funktionellen Gruppen funkt. Gruppe Präfix Suffix -(C)OO - -säure -(C)O Oxo- -al >(C)=O Oxo- -on -O ydroxy- -ol -S Mercapto-/Sulfanyl- -thiol -N 2 Amino- -amin -OR Alkoxy- -NO 2 Nitro- -Cl Chlor- 22
23 Kohlenwasserstoffe und Isomerie Summenformel C 5 12 C 3 3 C C 2 C 2 C 2 C 3 3 C C C 2 C 3 C 3 3 C C C 3 C 3 n-pentan 2-Methyl-butan 2,2-Dimethyl-propan Gleiche Summenformel - unterschiedliche Strukturen KONSTITUTIONSISOMERIE 23
24 Konformationsisomerie Folge der Rotationen um s-bindungen: räumlich unterschiedlichen Strukturen, die sich in ihrem Energieinhalt unterscheiden Es werden keine Bindungen gelöst oder neu geknüpft. 24
25 Strukturdarstellung 3 C C 3 C C 2 C C 2 C 3 C 3 3 C 3 C C 2 C 3 C 2 C 3 Sägebock-Projektion (engl. sawhorse) 3 C 3 C 2 C 3 C C 2 C 3 Keil-Strich-Projektion 3 C 3 C 2 C C 3 C 2 C 3 Newman-Projektion Torsions- oder Diederwinkel A B 25
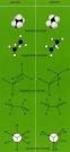
26 Butan ekliptisch oder synperiplanar gauche oder synclinal ekliptisch oder anticlinal 26 gestaffelt oder antiperiplanar
27 Konformation und Konstitution Konformationsisomere (Konformere) sind keine Konstitutionsisomere! Begriffe schließen sich aus! Konstitutionsisomere sind nur durch Bindungsspaltung ineinander überführbar. Konformationsisomere können durch Rotation um Einfachbindungen ineinander überführt werden. Konformere sind Stereoisomere! 27
28 Wie unterscheide ich Konstitutions- und Stereoisomere? Sind es wirklich Isomere? aben sie die gleiche Summenformel und das gleiche Verknüpfungsmuster der Atome? NEIN: Konstitutionsisomere JA: Stereoisomere Welche Arten von Stereoisomeren gibt es? Sind die Stereoisomere durch Rotation um Einfachbindungen ineinander überführbar? JA: NEIN: Konformationsisomere Konfigurationsisomere 28
29 Konstitution, Konformation und Konfiguration bei cyclischen Kohlenwasserstoffen 29
30 Dreiringsysteme Ringschluss einer Kette erfordert einen bestimmten Betrag an Energie (Spannung). auptfaktoren der Ringspannung: Baeyer-Spannung (Bindungswinkel-Spannung) Pitzer-Spannung (Konformationsspannung zwischen benachbarten Bindungen). Prelog-Spannung (Wechselwirkungen der -Atome) 30
31 Vierringsysteme ca. 5 kj mol -1 Knick-Winkel ca. 35 a a ca. 5 kj mol -1 e e e e a a 31
32 Fünfringsysteme Cyclopentan: Bindungswinkel nahe dem Optimum (108 statt Tetraederwinkel) Bayer-Spannung wird minimal. Konformative Änderungen zur Verminderung der Pitzer-Spannung. twist envelope 32
33 Sechsringsysteme Cyclohexan Bevorzugte Konformation ist die Sesselform. Baeyer- und Pitzer-Spannung durch Bindungswinkel von 111 und Diederwinkel von 56 ausbalanciert. Unterscheidung zwischen axial und äquatorial stehenden Substituenten. a e a e e a a e e a e a 33
34 Sessel- und Wannenform (chair - boat) Sesselform: alle Substituenten stehen auf Lücke (gestaffelt) Wannenform: Substituenten an C1, C2, C4 und C5 sind verdeckt angeordnet 34
35 Sechsringsysteme Man unterscheidet zwei Sesselformen. Ein in der Sesselform A axial angeordneter Substituent steht in der Sesselform B äquatorial. e e a a a e a e a a e e 44 kj mol -1 e e a a e a a e a a e e 35
36 Konformationen des Cyclohexans Quelle: 36
37 Substituierte Cyclohexane Unterschiede bezüglich der axialen oder äquatorialen Stellung der Substituenten machen sich erst bemerkbar, wenn Wasserstoff substituiert wird. Generell ist die äquatoriale Stellung energetisch begünstigt, da der Substituent am weitesten von anderen Teilen des Ringes entfernt ist. Ist der Substituent axial angeordnet, kommt es zu WW mit den axial stehenden Wasserstoff-Atomen, außerdem ist der Substituent in gauche- und nicht in anti-stellung zu zwei C-C-Bindungen. struktur/cyclische_verbindungen/carbocyclisch/cycloalkane/cyclohexan_struktur.vscml.html 37
38 Substituierte Cyclohexane Beispiel: 1,2-Dimethyl-cyclohexan C 3 3 C C 3 C 3 Konformer I: Substituenten a,a Konformer II: Substituenten e,e 38
39 Konformere und Konfigurationsisomere 1,2-Dimethyl-cyclohexan trans C 3 Konformere 3 C C 3 C 3 Konfigurationsisomere Konfigurationsisomere cis C 3 C 3 Konformere 3 C C 3 39
40 Konformere und Konfigurationsisomere 1,3-Dimethyl-cyclohexan 3 C C 3 C 3 cis C 3 C 3 trans C 3 3 C 3 C 40
41 Konformere und Konfigurationsisomere 1,4-Dimethyl-cyclohexan C 3 trans 3 C C 3 3 C 3 C C 3 cis C 3 3 C 41
42 Nochmals Konstitutionsisomerie Die Konstitution eines Moleküls gibt bei gegebener Summenformel die Aufeinanderfolge von Atomen und Bindungen an. 1,3-Dimethyl-cyclohexan C 3 C 3 3 C 1,2-Dimethyl-cyclohexan C 3 3 C C 3 1,4-Dimethyl-cyclohexan
43 Konfigurationsisomerie Moleküle mit gleicher Summenformel und gleicher Konstitution können unterschiedliche räumliche Strukturen aufweisen. Das sind Stereoisomere! Ursache: räumlich unterschiedliche Positionierung der Substituenten trans C 3 C 3 cis 3 C 3 C 1,3-Dimethyl-cyclohexan 43
44 Alkene und Isomerie Alkene sind nicht frei drehbar! Isomerie ist dann möglich, wenn an C1 und an C2 jeweils zwei unterschiedliche Substituenten sind! Sonst handelt es sich um omomere. 44
45 Alkene und Isomerie Diese Isomerie ist eine Form der Stereoisomerie. Es handelt sich um Konfigurationsisomere! C 1 2 C 1 2 C C Cl Cl Cl Cl Z früher cis E früher trans Substituenten an C1 unterscheiden sich und die Substituenten an C2 unterscheiden sich. Nur dann gibt es Isomere. 45
46 Alkene und Isomerie Das sind keine Isomere, sondern omomere! Cl C 1 2 C Cl C 1 2 C Substituenten an C1 unterscheiden sich zwar, die Substituenten an C2 sind jedoch gleich. 46
47 E oder Z Eine eindeutige Bestimmung ist nach der E/Z-Nomenklatur möglich. Dazu sortiert man die jeweils unmittelbar an C1 und an C2 gebundenen Atome der Ordnungszahl nach (CIP-Regeln). 3 C a C b a C b COO C 3 3 C C a b a C b COO C 3 Z: zusammen (Z)-2-Methyl-but-2-ensäure E: entgegen (E)-2-Methyl-but-2-ensäure 47
48 CIP -Regeln von R.S. Cahn, Sir C. Ingold und V. Prelog aufgestellt die unmittelbar am sp 2 -C-Atom gebundenen Atome (bzw. am stereogenen Zentrum) werden nach ihrer Ordnungszahl geordnet wenn keine Entscheidung möglich, werden Atome der zweiten oder weiterer Sphären verglichen, bis ein Unterschied gefunden wurde (bei Verzweigungen verfolgt man die Äste, die Atome höherer Ordnungszahlen enthalten), Atome mit Doppelbindungen werden doppelt, die mit Dreifachbindungen dreifach gewertet -I > -Br > -Cl > -O-Ar > -O-C 3 > -O > -N 2 > -COO > -CON 2 > -CO > -C 2 O > -C 2 -C 2 -C 3 > -C 2 -C 3 > -CD 3 > -C 3 > -D > - 48
49 Weitere Beispiele exakt ist (Z)-3-Chlor-hex-3-en 3 C 2 C b b 3 C C a C a C C 3 C C Cl a a C 2 C 3 b b exakt ist (Z)-4-Phenyl-pent-2-en 49
50 cis - trans oder E - Z? trans 2-Methyl-but-2-ensäure cis 3 C C C COO C 3 cis oder trans? 3 C C C COO C 3 Angelikasäure Tiglinsäure Bezugspunkt Methylgruppen muss explizit vereinbart werden! 50
51 Neue Aspekte Stereoisomere können auch nach ihren Symmetrieeigenschaften systematisiert werden! Verhalten sich die Isomere wie Bild und Spiegelbild? NEIN: JA: DIASTEREOMERE (Beispiel: E, Z-Isomerie an Doppelbindung) Cl C C C C Cl Cl Cl ENANTIOMERE 51
52 Enantiomere Stereoisomere Moleküle verhalten sich wie Bild und Spiegelbild und können nicht zur Deckung gebracht werden. Beispiel: COO COO C N 2 2 N C C C 52
53 lichtung manche meinen Lechts und rinks Kann man nicht velwechsern. werch ein illtum! Ernst Jandl (aus Laut und Luise 1966) 53
54 Eigenschaften der Enantiomere Stereoisomere Moleküle, die sich wie Bild und Spiegelbild verhalten und nicht zur Deckung gebracht werden können, (also: Enantiomere oder optische Antipoden) zeigen nicht nur Unterschiede in der Drehung des linear polarisierten Lichts. Es gibt Unterschiede in allen Reaktionen mit analog gebauten Reagenzien. erkömmliche Eigenschaften stimmen überein. Von einem Molekül gibt es nur dann zwei enantiomere Formen, wenn das Molekül chiral ist. 54
55 Voraussetzung für Chiralität (Auftreten von nicht deckungsgleichen Spiegelbildern) Fehlen einer Symmetrieebene, Fehlen eines Inversionszentrums, Fehlen einer Drehspiegelachse führen zu Chiralität Chiral: Schrauben, Schneckenhäuser, Korkenzieher, andschuh, Kohlenstoffatome mit vier verschiedenen Substituenten Achiral: Methan, 1,2-Dichlor-ethen, Citronensäure, Tischtennisball 55
56 Chiralität ohne asymmetrisch substituierte C-Atome elikale Strukturen P M M P P Betrachtet man eine rechtsgängige elix (right-handed) längs ihrer Achse in Richtung von vorn nach hinten, so beschreibt sie eine Rechtsdrehung und wird mit P (plus) bezeichnet. Eine linksgängige elix (left-handed) wird mit M (minus) bezeichnet. 56
57 Spiralen links oder rechts? 57
58 Dach oder immel? 58
59 Treppen Burg Warwick Vatikanisches Museum 59
60 Schnecken Cubanische Baumschnecken Turboschnecken Weinbergschnecke Turmschnecken 60
61 Optische Aktivität Das Natrium-Ammonium-Salz der Weinsäure kristallisiert in zwei spiegelbildlichen Formen aus. A B Kristalle sind asymmetrisch. Louis Pasteur trennte 1848 die Kristalle: Lösung der Kristalle des Typs A ist optisch aktiv, Lösung der Kristalle des Typs B ist optisch aktiv (Ablenkung des linear polarisierten Lichtes um den gleichen Betrag, aber mit entgegen gesetzten Vorzeichen). Das 1:1- Gemisch (Racemat) beider Kristalle ist in Lösung optisch nicht aktiv erkannte Pasteur, dass Penicillium glaucum bei Einwirkung auf racemische Weinsäure (Traubensäure) nur die rechtsdrehende Form abbaut. 61
62 Optische Aktivtät Ein Molekül, von dem es zwei enantiomere Formen (zwei optische Antipoden) gibt, ist optisch aktiv. Untersuchung im linear polarisierten Licht 62
63 Worin sich Enantiomere unterscheiden asymmetrisch subst. C-Atom asymmetrisch subst. C-Atom 2 N O O * O 2 N * O N 2 O N 2 L-Asparagin D-Asparagin bitter süß O Geschmack 63
64 Worin sich Enantiomere unterscheiden * * (S)-Limonen Zitronenduft (R)-Limonen Orangenduft Geruch 64
65 Worin sich Enantiomere unterscheiden O O * * * * * * * O O (+)-Östron (-)-Östron ormonwirkung Keine ormonwirkung Biochemische Wirkung 65
66 Worin sich Enantiomere unterscheiden O O N * O N * N N O O O O O (R)-Thalidomid (S)-Thalidomid Schlafmittel Racemat: Contergan stark teratogene Wirkung Teratos, Gen. von teras = Zeichen, Vorzeichen, Schreckensbild Thalidomid heute gegen Lepra, Multiples Myelom, Myelodysplastisches Syndrom, Morbus Crohn, unter strenger Kontrolle zugelassen in EU, USA, Australien, Neuseeland, Türkei 66
67 Enantiomere und Diastereomere Ein Molekül ist chiral. Folge: Bild und Spiegelbild sind nicht deckungsgleich. Molekülbild und Molekülspiegelbild sind ein Enantiomerenpaar, es handelt sich um optische Antipoden. Zwei Stereoisomere können sich nicht gleichzeitig wie ein Enantiomeren- und ein Diastereomerenpaar verhalten! Enantiomere drehen das linear polarisierte Licht um den gleichen Betrag, aber mit entgegen gesetzten Vorzeichen. [(+) oder (-)]. 67
68 Enantiomere und Diastereomere Äquimolare Mengen von zwei Enantiomeren einer Verbindung bilden ein Racemat. Lösungen des Racemats sind optisch inaktiv. Ungerichtete physikalische und chemische Eigenschaften sind bei den Enantiomeren einer Verbindung gleich, während diasteromere Verbindungen sich in ihren Energieinhalten und in ihren chemischen und physikalischen Eigenschaften unterscheiden. 68
69 Relative Nomenklatur 1 2 CO O CO O relativ: Bezug zum D-Glyceraldehyd 3 C 2 O C 2 O Voraussetzung: Darstellung des Moleküls in Fischer-Projektion längste Kohlenstoffkette vertikal C-Atom mit dem kleinsten Lokanten steht oben vertikale Bindungen zeigen vom Betrachter weg horizontale Bindungen zeigen zum Betrachter hin Konsequenz: Drehung um 90 in der Zeichenebene verboten Substituententausch erzeugt das Spiegelbild 69
70 Relative Nomenklatur II O- oder N 2 -Gruppe wie im D-Glyceraldehyd auf der rechten Seite führt zu D (dexter) O- oder N 2 -Gruppe wie im L-Glyceraldehyd auf der linken Seite führt zu L (laevus) COO CO CO C 3 2 N C C 3 O C C O C C O O C O C 2 C 3 L-Alanin L-Glyceraldehyd D-Glyceraldehyd D-Butan-2-ol 70
71 Relative Nomenklatur Was macht man bei vielen O- Gruppen? Festlegung: die O-Gruppe des stereogenen Zentrums, das am weitesten von der höchst oxidierten Gruppe (C Atom mit dem kleinsten Lokanten) entfernt ist, bestimmt die Konfiguration Beispiel: D- und L-Glucose 71
72 Enantiomere und Diastereomere Enantiomere können auftreten, wenn ein Kohlenstoffatom vier verschiedene Substituenten hat (stereogenes Zentrum). Alle vier Substituenten eines Kohlenstoffatoms müssen jeweils in ihrer Gesamtheit untersucht werden. n stereogene Zentren führen zu 2 n chiralen Stereoisomeren (wenn jeweils mind. 2 unterschiedliche Substituenten) Beispiele: Erythrose, Threose, Stereoisomere zu C 6 12 O 6 72
73 Innere Racemate Mehrere stereogene Zentren führen nicht immer zu Chiralität, wenn sich die Zentren in ihren Substituenten gleichen. D(-)-Weinsäure L(+)-Weinsäure Mesoweinsäure Fp. in C α ( ml/g dm) pks 1 2,93 2,93 3,11 2,96 Löslichkeit g/100 ml bei 20 C (?) Dichte g/cm 3 1,76 1,76 1,67 1,68 Vorkommen im westafrikanischen Baum Bankinia reticulata in vielen Früchten, besonders in Weintrauben nicht in der Natur Traubensäure nicht in der Natur 73
74 Absolute Konfiguration R-Konfiguration lat. rectus, rechts S-Konfiguration lat. sinister, links 74
75 CIP-Regeln Die Priorität der jeweils unmittelbar mit dem stereogenen Zentrum verbundenen ersten Atome wird nach der Ordnungszahl bestimmt (Ordnung nach abnehmender Ordnungszahl). Bei identischen Atomen werden die Ordnungszahlen der mit ihnen verbundenen zweiten Atome bestimmt. Notfalls zieht man auch die dritten Atome heran. Ist ein Atom mit einer Doppel- oder Dreifachbindung mit dem nächsten verknüpft, zählt es doppelt bzw. dreifach. 75
76 Absolute Konfiguration Das Molekül ist so im Raum zu orientieren, dass das Atom mit der niedrigsten Priorität nach hinten zeigt. (räumliche Betrachtung). Geht man vom Substituenten 1 über 2 nach 3 im Uhrzeigersinn, handelt es sich um R-Konfiguration. Geht man vom Substituenten 1 über 2 nach 3 gegen den Uhrzeigersinn, handelt es sich um S-Konfiguration. 76
77 Absolute Konfiguration FISCER-Projektion: Das Molekül ist so zu orientieren, dass das Atom niedrigster Priorität nach unten oder oben zeigt (Projektion in die Papierebene). Wenn dazu ein Tausch von Substituenten notwendig ist, erzeugt der Tausch benachbarter Substituenten genau das Spiegelbild. 77
78 CO 2 CO 2 CO 2 CO 2 Moleküle mit gleicher Summenformel O CO 2 O O CO 2 O O CO 2 O O CO 2 O C 4 6 O 6 deckungsgleich? ja omomer (identisch) Enantiomer ja nein Isomer gleiche Konstitution? ja Stereoisomer Bild- Spiegelbild- Beziehung? CO 2 CO 2 nein nein CO 2 CO 2 O O O CO 2 O C 2 CO 2 Konstitutionsisomer Diasteromer O CO 2 78 O O O CO 2
79 CO 2 CO 2 COO Moleküle mit gleicher Summenformel C 4 6 O 6 O CO 2 O O CO 2 O O O COO COO O O COO ja omomer (identisch) deckungsgleich? Konformationsisomere nein ja Isomer gleiche Konstitution? ja Stereoisomer Rotation um Einfachbindung möglich? O CO 2 O O CO 2 CO 2 O C 2 CO 2 nein Konstitutionsisomer nein Konfigurationsisomere D-, L- und Meso- Weinsäure 79
4. Stereochemie. Das wichtigste Kriterium für Chiralität ist, dass sich Objekt und Spiegelbild nicht zur Deckung bringen lassen.
 4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
4. Stereochemie Auch die cis-trans-isomerie zählt zur Stereoisomerie: 4.1 Chirale Moleküle Chirale Moleküle besitzen ein asymmetrisches C- Atom = Chiralitätszentrum. Das wichtigste Kriterium für Chiralität
Konfigurationsisomerie
 Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Konfigurationsisomerie Enatiomerie, Diastereomerie (σ undπ). Prof.Dr. Ivo C. Ivanov 1 Optische Aktivität Zur Bestimmung des Drehwertes bedient man sich eines Polarimeters, dessen Aufbau nachfolgend schematisch
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 10 Stereochemie (Thema 11.1 11.4) Aufgabe 1: a) Zeichnen Sie den Isomeren-Stammbaum auf. b) Erklären Sie folgende Isomerie-Arten: i) Konstitutionsisomere Konstitutionsisomere
Chemie für Biologen, 2017 Übung 10 Stereochemie (Thema 11.1 11.4) Aufgabe 1: a) Zeichnen Sie den Isomeren-Stammbaum auf. b) Erklären Sie folgende Isomerie-Arten: i) Konstitutionsisomere Konstitutionsisomere
Stereoisomerie. C 2 H 4 O 2 Schmelzpunkt 17 Grad Celcius
 3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
3. Stereochemie Stereoisomerie Definition Isomerie: Als Isomere bezeichnet man Moleküle mit gleicher Summenformel, die sich jedoch in der Sequenz der Atome (Konstitutionsisomere) oder deren räumlichen
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
L.9 Organische Chemie I
 L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind!
 4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism ball de.svg OC I Lehramt F. H. Schacher 1 Stereoisomerie andere
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism ball de.svg OC I Lehramt F. H. Schacher 1 Stereoisomerie andere
4. Stereoisomerie. ! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! Organische Chemie I LA / J. C.
 4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism-ball-de.svg Organische Chemie I LA / J. C. Brendel 1 Stereoisomerie
4. Stereoisomerie! Diastereomer hier: allg. alle Stereosiomere, die keine Enantiomere sind! http://de.wikipedia.org/wiki/datei:isomerism-ball-de.svg Organische Chemie I LA / J. C. Brendel 1 Stereoisomerie
Übung 9: Aufbau und Struktur organischer Verbindungen Übung für Medizinische Biologen - Jun.-Prof. Dr. Michael Giese.
 Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Zusammenfassung Aufbau und Struktur organischer Verbindungen Kohlenstoff besitzt eine Sonderstellung unter den Elementen ybridisierungsmodell beschreibt die Bindungsverhältnisse in Kohlenstoffverbindungen
Chiralität in der Natur und synthetisch
 Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Weiterführende Fragen und Knobeleien zur Vorlesung Organische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach.
 Weiterführende Fragen und Knobeleien zur Vorlesung rganische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach Teil II Mit diesem Blatt will ich Sie anregen, weiter über das Thema Chiralität
Weiterführende Fragen und Knobeleien zur Vorlesung rganische Chemie für chemieinteressierte Studierende mit Chemie als Nebenfach Teil II Mit diesem Blatt will ich Sie anregen, weiter über das Thema Chiralität
Einführung in die Nomenklatur der organischen Chemie. Einteilung der Kohlenwasserstoffe
 organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
organischen hemie Klasse 8 Einteilung der Kohlenwasserstoffe Alkane Alkene Alkine Kettenverbindungen Organische hemie socyclen ycloalkane ycloalkene ycloalkine Aromate Ringverbindungen eterocyclen Fünfringe
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Isomerie organischer Verbindungen
 15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
Übungen zur VL Chemie für Biologen und Humanbiologen Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur:
 Übungen zur VL Chemie für Biologen und Humanbiologen 21.01.2011 1. Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur: a) 3-Methyl-4-propylhexan Erklärung: Es liegt keine funktionelle Gruppe
Übungen zur VL Chemie für Biologen und Humanbiologen 21.01.2011 1. Benennen Sie die folgenden Verbindungen nach IUPAC-Nomenklatur: a) 3-Methyl-4-propylhexan Erklärung: Es liegt keine funktionelle Gruppe
III. Cycloalkane (Stereochemie II)
 49 III. Cycloalkane (Stereochemie II) (C 2 ) n-2 2 C C 2 (C 2 ) n-2 2 C C 2 C n 2n+2 Cn 2n Nomenklatur: Alkan Cycloalkan für n = 5 n-pentan Cyclopentan Bruttoformel allgemein C n 2n oder (C 2 ) n Cycloalkane
49 III. Cycloalkane (Stereochemie II) (C 2 ) n-2 2 C C 2 (C 2 ) n-2 2 C C 2 C n 2n+2 Cn 2n Nomenklatur: Alkan Cycloalkan für n = 5 n-pentan Cyclopentan Bruttoformel allgemein C n 2n oder (C 2 ) n Cycloalkane
Grundlagen zum Verständnis chemischer Reaktionen = Handwerkszeug
 Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Kohlenwasserstoffe. sp 3 -Orbitale. Alkane. Alkene. sp 2 - Orbitale p z - Orbital. sp -Orbitale p y, p z - Orbitale. Alkine
 Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
Kohlenwasserstoffe sp 3 -Orbitale Alkane sp 2 - Orbitale p z - Orbital Alkene sp -Orbitale p y, p z - Orbitale Alkine Offenkettige Alkane 4 4 than "Erdgas" 2 6 3 3 Ethan 3 8 3 2 3 Propan Bei Raumtemperatur
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
- Punktsymmetriegruppe Gesamtheit aller Symmetrieelemente: Gruppentheorie
 195 14. Stereochemie Bereits am Anfang der Vorlesung einige Grundbegriffe: Konformation, Enantio- und Diastereomerie Jetzt nochmals systematisch und genauer a) Symmetrie und hiralität α) Symmetrieelemente
195 14. Stereochemie Bereits am Anfang der Vorlesung einige Grundbegriffe: Konformation, Enantio- und Diastereomerie Jetzt nochmals systematisch und genauer a) Symmetrie und hiralität α) Symmetrieelemente
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
weiteres Beispiel für Stereoisomere: Enantiomere Spiegelebene
 Stereoisomere - Isomerie I: Konstitutionsisomere (siehe oben) - Isomerie II: Konformationsisomere (Konformere, siehe oben) - Isomerie III: Stereoisomere; Stereoisomere weisen eine identische Konstitution
Stereoisomere - Isomerie I: Konstitutionsisomere (siehe oben) - Isomerie II: Konformationsisomere (Konformere, siehe oben) - Isomerie III: Stereoisomere; Stereoisomere weisen eine identische Konstitution
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Cycloalkane
 3. Cycloalkane Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Einteilung: Cycloalkane Cycloaliphaten (Alicyclen, Carbocyclen) Polycyclen Cycloaliphaten (Alicyclen, Carbocyclen):
3. Cycloalkane Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Einteilung: Cycloalkane Cycloaliphaten (Alicyclen, Carbocyclen) Polycyclen Cycloaliphaten (Alicyclen, Carbocyclen):
VII INHALTSVERZEICHNIS
 VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
VII INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 3.2 Chemische Reaktionstypen 12 3.3 Stereochemie 30 3.4 Alkane, Cycloalkane 46 3.5 Alkene, Alkine 47 3.6 Aromatische
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
Energie. 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital
 sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
7. Stereochemie. Isomere. Alkene. Cycloalkane
 7. Stereochemie 56 In den vorhergehenden Kapiteln haben wir zwei Arten von Isomerie kennengelernt (z.b. Seiten 12, 20 und 23), die Konstitutionsisomerie, und die Stereoisomerie : Isomere Konstitutionsisomerie
7. Stereochemie 56 In den vorhergehenden Kapiteln haben wir zwei Arten von Isomerie kennengelernt (z.b. Seiten 12, 20 und 23), die Konstitutionsisomerie, und die Stereoisomerie : Isomere Konstitutionsisomerie
Organische Chemie für MST 6. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
4.1. Gesättigte Kohlenwasserstoffe (Alkane)
 4. Stoffgruppen 4.1. Gesättigte Kohlenwasserstoffe (Alkane) ffenkettige Alkane à für n C-Atome ergibt sich: C n 2n+2 Methan Ethan Propan Butan C 4 C 2 6 C 3 8 C 3 C C 3 3 C C 3 C 4 10 3 C C 3 à Es gibt
4. Stoffgruppen 4.1. Gesättigte Kohlenwasserstoffe (Alkane) ffenkettige Alkane à für n C-Atome ergibt sich: C n 2n+2 Methan Ethan Propan Butan C 4 C 2 6 C 3 8 C 3 C C 3 3 C C 3 C 4 10 3 C C 3 à Es gibt
Prof. Dr. Thomas Heinze Institut für Organische Chemie und Makromolekulare Chemie Humboldtstraße Jena
 Vorlesung/Seminare Organische Chemie für Materialwissenschaften Prof. Dr. Thomas Heinze Institut für Organische Chemie und Makromolekulare Chemie Humboldtstraße 10 07743 Jena 03641/9 48270 03641/9 48271
Vorlesung/Seminare Organische Chemie für Materialwissenschaften Prof. Dr. Thomas Heinze Institut für Organische Chemie und Makromolekulare Chemie Humboldtstraße 10 07743 Jena 03641/9 48270 03641/9 48271
EINFÜHRUNG IN DIE ORGANISCHE CHEMIE
 rganische Chemie Lehrgang CEMIE FÜR BILGIELERKRÄFTE EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs
rganische Chemie Lehrgang CEMIE FÜR BILGIELERKRÄFTE EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs
Prof. Dr. Stephen Hashmi, Sommersemester Organische Chemie für Technische Biologen, Organische Chemie für Lehramtskandidaten, Teil 5
 Prof. Dr. ashmi, Sommersemester 2005 45 Mechanismus der 1,2-Isomerisierung: Start: [o III ] Kette: reversible omolyse nur 65 kj/mol Metall--Bindung Organometall-Verbindung X + [o II ] + -Abstraktion das
Prof. Dr. ashmi, Sommersemester 2005 45 Mechanismus der 1,2-Isomerisierung: Start: [o III ] Kette: reversible omolyse nur 65 kj/mol Metall--Bindung Organometall-Verbindung X + [o II ] + -Abstraktion das
Z 8 EINFÜHRUNG IN DIE ORGANISCHE CHEMIE 1) DEFINITIONEN 2) ELEMENTE UND BINDUNGEN. Organische Chemie. Kunstoffe. Farbstoffe
 EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Thema: Komplexverbindungen, die koordinative Bindung. Koordinationszahl, 18-Elektronen-Schale, ein- mehrzähnige Liganden, EDTA,
 Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Wiederholung der letzten Vorlesungsstunde: Thema: Komplexverbindungen, die koordinative Bindung Koordinationschemie nach A. Werner, Zentralteilchen, Liganden, Koordinationszahl, 18-Elektronen-Schale, ein-
Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Cycloalkane
 3. Cycloalkane Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Einteilung: Cycloalkane Cycloaliphaten (Alicyclen, Carbocyclen) Polycyclen Cycloaliphaten (Alicyclen, Carbocyclen):
3. Cycloalkane Cycloalkane enthalten eine oder mehrere gesättigte, ringförmige Kohlenstoffketten. Einteilung: Cycloalkane Cycloaliphaten (Alicyclen, Carbocyclen) Polycyclen Cycloaliphaten (Alicyclen, Carbocyclen):
IUPAC Nomenklatur. Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten. Feld 2: Stammname der Verbindung
 Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten Feld 2: Stammname der Verbindung Feld 3: Grad der Ungesättigtheit Feld 4: funktionelle Gruppe mit höchster
Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten Feld 2: Stammname der Verbindung Feld 3: Grad der Ungesättigtheit Feld 4: funktionelle Gruppe mit höchster
2. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
 2. AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybridisierungskonzepts verstehen und anschaulich darstellen (siehe
2. AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybridisierungskonzepts verstehen und anschaulich darstellen (siehe
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Spezielle Methoden der pharmazeutischen Chemie 2
 Spezielle thoden der pharmazeutischen Chemie 2 Asymmetrische Synthese (für Diplomanden und Dissertanten im Fach Pharmazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Symmetrie, Asymmetrie, Chiralität
Spezielle thoden der pharmazeutischen Chemie 2 Asymmetrische Synthese (für Diplomanden und Dissertanten im Fach Pharmazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Symmetrie, Asymmetrie, Chiralität
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Verzeichnis der Wortabkürzungen... Verzeichnis der Zeichen und Symbole...XVII
 VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
Organische Chemie. Einstieg. Chemie-Formeldarstellungen. Formeldarstellungen der Chemie: Bei Ionenverbindungen: Verhältnisformeln. , AlF 3. etc.
 Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Die Verwendung von Rot- und Bleistift sowie Tipp-Ex ist untersagt!!!
 Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Chemisches Praktikum für Studierende der Biologie (Bachelor) Universität zu Köln Department für Chemie Prof. Dr..-G. Schmalz Prof. Dr. A. G. Griesbeck M.Sc. P. Thomopoulou Greinstr. 4 50939 Köln Modul:
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Inhaltsverzeichnis. 3 Organische Chemie. Vorwort Chemische Bindung Chemische Reaktionstypen Bindungen...
 VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
Cyclohexan und Dekalin
 Cyclohexan und Dekalin Die wohl wichtigste ringförmige Struktur in der organischen Chemie ist der Sechsring, im gesättigten Fall Cyclohexan. Dies gilt schon deshalb, weil dieser Ring zentraler Bestandteil
Cyclohexan und Dekalin Die wohl wichtigste ringförmige Struktur in der organischen Chemie ist der Sechsring, im gesättigten Fall Cyclohexan. Dies gilt schon deshalb, weil dieser Ring zentraler Bestandteil
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 0-2, S04 T0 A02 Paul Rademacher Institut für rganische hemie der Universität Duisburg-Essen (Teil 2: 2.0.2005) MILESS: hemie für Biologen 28 Konstitutionsisomere:
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 0-2, S04 T0 A02 Paul Rademacher Institut für rganische hemie der Universität Duisburg-Essen (Teil 2: 2.0.2005) MILESS: hemie für Biologen 28 Konstitutionsisomere:
IUPAC-Nomenklaturregeln als Grundlage für Q11 Chemie
 Nomenklatur 1 IUPA-Nomenklaturregeln als Grundlage für Q11 hemie 1 Kohlenwasserstoffe und Derivate 1.1 Regeln zur Benennung von unverzweigten Alkanen (n-alkane) Der Name der n-alkane enthält die folgenden
Nomenklatur 1 IUPA-Nomenklaturregeln als Grundlage für Q11 hemie 1 Kohlenwasserstoffe und Derivate 1.1 Regeln zur Benennung von unverzweigten Alkanen (n-alkane) Der Name der n-alkane enthält die folgenden
Wiederholung Grundlagen OC
 Wiederholung Grundlagen C 28.04.2017 Auswertung Stichprobe Frage 1: Die oben abgebildete Strukturformel zeigt 25 20 15 10 5 0 Ether Ester Acetal Keton Ester+Weiteres Frage 2: Die absolute Konfiguration
Wiederholung Grundlagen C 28.04.2017 Auswertung Stichprobe Frage 1: Die oben abgebildete Strukturformel zeigt 25 20 15 10 5 0 Ether Ester Acetal Keton Ester+Weiteres Frage 2: Die absolute Konfiguration
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
I. Alkane Homologe Reihe, Nomenklatur
 Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
3. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
 3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
Organische Chemie. 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8. Lehrstuhl für Organische Chemie
 Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
Organische Chemie 3. Semester, SWS: V-3, Ü-1, P-3; insgesamt: V-45, Ü-15, P-45; ECTS 8 Lehrstuhl für Organische Chemie (ivanov43@gmail.com) Prof. Dr. Ivo C. Ivanov 1 1. Gegenstand der Organischen Chemie,
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Isomerie I. Konstitutionsisomerie. Identifizieren Sie alle Konstitutionsisomere. a b c. a b c d
 Isomerie I Konstitutionsisomerie Identifizieren Sie alle Konstitutionsisomere. 1. a) Br b) a b c) a b c 2. a b I a b c d e f 3. a b c d e f g R,S-omenklatur Bestimmen der absoluten Konfiguration am Chiralitätszentrum:
Isomerie I Konstitutionsisomerie Identifizieren Sie alle Konstitutionsisomere. 1. a) Br b) a b c) a b c 2. a b I a b c d e f 3. a b c d e f g R,S-omenklatur Bestimmen der absoluten Konfiguration am Chiralitätszentrum:
Decan Homologe Reihe der Alkane, unterschiedlich lange C-Ketten mit C- C (sp 3 /sp 3 ) und C-H (sp 3 /s)-bindungen (σ-bindungen) Beispiele: Butan
 1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
ORGANISCHE CHEMIE. Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen
 ORGANISE EMIE Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen hemische Formeln Summenformeln Strukturformeln (Konstitutionsformeln) Ausführliche Strukturformeln Vereinfachte
ORGANISE EMIE Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen hemische Formeln Summenformeln Strukturformeln (Konstitutionsformeln) Ausführliche Strukturformeln Vereinfachte
Bundesrealgymnasium Imst. Chemie Klasse 8. Aliphate
 Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Stereochemie. mit Vitamin C. Süßstoff Aspartam (QWKlOWÃHLQHÃ3KHQ\ODODQLQTXHOOH. L(+)-Milchsäure. Zuckeraustauschstoff Sorbit
 Stereochemie mit Vitamin Süßstoff Aspartam (QWKlWÃLQÃ3KQ\DDQLQTX L(+)-Milchsäure Zuckeraustauschstoff Sorbit hemie für Mediziner Isomerie organischer Verbindungen Isomere Konstitutionsisomere Stereoisomere
Stereochemie mit Vitamin Süßstoff Aspartam (QWKlWÃLQÃ3KQ\DDQLQTX L(+)-Milchsäure Zuckeraustauschstoff Sorbit hemie für Mediziner Isomerie organischer Verbindungen Isomere Konstitutionsisomere Stereoisomere
Organische Chemie. Kohlenstoff. Kohlenstoffkreislauf. Erdölverarbeitung. Kohlenwasserstoffe
 rganische hemie Teilgebiet der hemie, welches sich mit Aufbau, erstellung und Eigenschaften der Verbindungen des Kohlenstoffs beschäftigt. NTG 10.1 Kohlenstoff - 4. auptgruppe 4 Valenzelektronen 4 Bindungen
rganische hemie Teilgebiet der hemie, welches sich mit Aufbau, erstellung und Eigenschaften der Verbindungen des Kohlenstoffs beschäftigt. NTG 10.1 Kohlenstoff - 4. auptgruppe 4 Valenzelektronen 4 Bindungen
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane: Moleküle ohne funktionelle Gruppen
E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane: Moleküle ohne funktionelle Gruppen
CHE 172.1: Organische Chemie für die Life Sciences
 1 E 172.1: rganische hemie für die Life Sciences Prof Dr. J. A. Robinson 2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle
1 E 172.1: rganische hemie für die Life Sciences Prof Dr. J. A. Robinson 2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle
Stereochemie. Grundbegriffe. Bearbeitet von K.-H Hellwich
 Stereochemie Grundbegriffe Bearbeitet von K.-H Hellwich Neuausgabe 2007. Taschenbuch. xii, 120 S. Paperback ISBN 978 3 540 71707 2 Format (B x L): 14 x 21,6 cm Gewicht: 181 g Weitere Fachgebiete > Chemie,
Stereochemie Grundbegriffe Bearbeitet von K.-H Hellwich Neuausgabe 2007. Taschenbuch. xii, 120 S. Paperback ISBN 978 3 540 71707 2 Format (B x L): 14 x 21,6 cm Gewicht: 181 g Weitere Fachgebiete > Chemie,
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Einführung in die Organische Chemie. Benjamin Grimm
 Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Vokabular zur Stereochemie
 Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Bachelorprüfung im Fach Biologie, Teilfach Chemie am a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel
 Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
Aufgabe 1 a) Zeichnen Sie bitte unten die Strukturformel einer Verbindung der Summenformel C 3 H 6 O ein, die die folgenden Eigenschaften besitzt: - Die Verbindung bildet mit einem primären Amin ein Imin.
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen
 2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 11 2.1 Funktionellen Gruppen Es gibt heute ungefähr neun Millionen bekannter organischer Substanzen.
2. rganische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 11 2.1 Funktionellen Gruppen Es gibt heute ungefähr neun Millionen bekannter organischer Substanzen.
Inhaltsverzeichnis. 3 Gesättigte Kohlenwasserstoffe (Alkane) 3.1 Offenkettige Alkane 3.2 Cyclische Alkane
 Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Inhaltsverzeichnis 1 Chemische Bindung in organischen Verbindungen 1.1 Einleitung 1.2 Grundlagen der chemischen Bindung 1.3 Die Atombindung (kovalente oder homöopolare Bindung) 1.4 Bindungslängen und Bindungsenergien
Tetraeder mit gleichen und verschiedenen Ecken (1, 2, 3, 4)
 Prof. Dr..-U. Reißig rganische hemie 7. Tetraeder mit gleichen und verschiedenen Ecken (,,, ) Diese drei Tetraeder sind mit ihrem Spiegelbild deckbar, d. h. es ist achiral. gleiche Ecken "chemisches Beispiel"
Prof. Dr..-U. Reißig rganische hemie 7. Tetraeder mit gleichen und verschiedenen Ecken (,,, ) Diese drei Tetraeder sind mit ihrem Spiegelbild deckbar, d. h. es ist achiral. gleiche Ecken "chemisches Beispiel"
Gruppenunterricht zum Thema Stereoisomerie
 Gruppenunterricht zum Thema Stereoisomerie Unterlagen Fach: Institution: Adressaten: Kurs: Gruppenarbeitsform: Dauer: Autor: Betreuer: Erprobungsstatus: Chemie Gymnasium Maturanden im letzten Jahr des
Gruppenunterricht zum Thema Stereoisomerie Unterlagen Fach: Institution: Adressaten: Kurs: Gruppenarbeitsform: Dauer: Autor: Betreuer: Erprobungsstatus: Chemie Gymnasium Maturanden im letzten Jahr des
Aktuelle Beispiele aus der Forschung
 Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Vorlesung: Allgemeine Chemie Organische Chemie 05.12.; 08.12.; Prof. Dr. C. Meier Eine Einführung in die Organische Chemie Themen: Elektronenstruktur, kovalente Bindung, Säure-Basen-Eigenschaften in Abhängigkeit
Chemie für Biologen WS 2005/6. Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen WS 2005/6 Arne Lützen Institut für Organische hemie der Universität Duisburg-Essen (Teil 10: Organische hemie gesättigte Kohlenwasserstoffe) Sonderstellung des Elements Elektronegativität
hemie für Biologen WS 2005/6 Arne Lützen Institut für Organische hemie der Universität Duisburg-Essen (Teil 10: Organische hemie gesättigte Kohlenwasserstoffe) Sonderstellung des Elements Elektronegativität
IUPAC Nomenklatur. Der Name eines Moleküls wird in 3 Felder aufgeteilt: Feld 1: Name und Position von Substituenten (Präfixe)
 Der Name eines Moleküls wird in 3 Felder aufgeteilt: Feld 1: Name und Position von Substituenten (Präfixe) Feld 2: Stammkern der Verbindung Feld 3: funktionelle Gruppe mit höchster Priorität (Suffix) Substituenten/
Der Name eines Moleküls wird in 3 Felder aufgeteilt: Feld 1: Name und Position von Substituenten (Präfixe) Feld 2: Stammkern der Verbindung Feld 3: funktionelle Gruppe mit höchster Priorität (Suffix) Substituenten/
Prof. Dr. Th. K. Lindhorst, SS 2003, Übungsklausur. Übungsklausur. zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, OC I
 Übungsklausur zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, C I Diese Auswahl von Aufgaben wurde auf Anfrage zusammengestellt; die Klausur könnte also beispielsweise wie folgt lauten
Übungsklausur zur Vorlesung Allgemeine Chemie II, SS 2003 Experimentalvorlesung, C I Diese Auswahl von Aufgaben wurde auf Anfrage zusammengestellt; die Klausur könnte also beispielsweise wie folgt lauten
Moleküle mit mehr als einem Chiralitätselement
 Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Übersicht: Organische Experimentalchemie für Mediziner und Zahnmediziner (122101) WS 2010/11. 7.Aufl., Kap. 11)
 Übersicht: Organische Experimentalchemie für Mediziner und Zahnmediziner (122101) Prof. Dr. Ernst-Ulrich Würthwein,, Organisch-Chemisches Institut, WWU Münster WS 2010/11 10/11,, Mo.-Fr. 8-98 Uhr A. Einführung:
Übersicht: Organische Experimentalchemie für Mediziner und Zahnmediziner (122101) Prof. Dr. Ernst-Ulrich Würthwein,, Organisch-Chemisches Institut, WWU Münster WS 2010/11 10/11,, Mo.-Fr. 8-98 Uhr A. Einführung:
Beispielklausur Allgemeine Chemie II (Organische Chemie)
 Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Beispielklausur Allgemeine hemie II (rganische hemie) für Studierende mit hemie als Nebenfach zum Üben LÖSUNGEN (Teilweise gibt es viele mögliche richtige Antworten, dann sind lediglich Beispiele angegeben.)
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Isomerie. Ethanol. Stereoisomere: gleiche Summenformel, gleiche Verknüpfung der Atome, aber in unterschiedlicher Raumrichtung. trans- oder E-2-Buten
 Isomerie Folie271 Konstitutions- zw. Strukturisomere: gleiche Summenformel, unterschiedliche Verknüpfung der Atome: Beispiele: 2 6 : 3 3 3 2 Dimethylether Ethanol 4 10 : 3 2 2 3 3 3 n-butan 3 Isoutan Stereoisomere:
Isomerie Folie271 Konstitutions- zw. Strukturisomere: gleiche Summenformel, unterschiedliche Verknüpfung der Atome: Beispiele: 2 6 : 3 3 3 2 Dimethylether Ethanol 4 10 : 3 2 2 3 3 3 n-butan 3 Isoutan Stereoisomere:
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
Organische Chemie im Überblick
 Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
Evelyne Chelain Nadeqe Lubin-Germain Jacques Uziel Organische Chemie im Überblick Grundwissen in Lerneinheiten Aus dem Französischen übersetzt von Karin Beifuss ~ Springer Spektrum Inhaltsverzeichnis 1
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Inhaltsverzeichnis VII. Vorwort... V
 VII Vorwort... V 1 Einleitung... 1 1.1 Der Begriff der Organischen Chemie... 1 1.2 Vielfalt organischer Verbindungen... 1 1.3 Ordnung in der Vielfalt... 2 2 Grundlegendes... 3 2.1 Kohlenstoff hat vier
VII Vorwort... V 1 Einleitung... 1 1.1 Der Begriff der Organischen Chemie... 1 1.2 Vielfalt organischer Verbindungen... 1 1.3 Ordnung in der Vielfalt... 2 2 Grundlegendes... 3 2.1 Kohlenstoff hat vier
8. Stereochemie organischer Moleküle 8.1
 8. Stereochemie organischer Moleküle 8.1 Stereochemie organischer Moleküle Zur Darstellung der Struktur organischer Moleküle werden oft Formeln verwendet, welche den räumlichen Bau nicht zum Ausdruck bringen.
8. Stereochemie organischer Moleküle 8.1 Stereochemie organischer Moleküle Zur Darstellung der Struktur organischer Moleküle werden oft Formeln verwendet, welche den räumlichen Bau nicht zum Ausdruck bringen.
s- und p-orbitale MO-Schema des Wasserstoffmoleküls H 2 y z z x p x p y p z antibindendes MO bindendes MO
 s- und p-rbitale y y z z x x s p x p y p z M-Schema des Wasserstoffmoleküls 2 antibindendes M 1s 1s bindendes M Merkmale wichtiger ybridorbitale sp 3 -ybridisierung: Tetraedrische Ausrichtung der ybridorbitale,
s- und p-rbitale y y z z x x s p x p y p z M-Schema des Wasserstoffmoleküls 2 antibindendes M 1s 1s bindendes M Merkmale wichtiger ybridorbitale sp 3 -ybridisierung: Tetraedrische Ausrichtung der ybridorbitale,
Kohlenhydrate Einleitung
 Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
