Gruppe 10 vorgegebener Versuch. Die Wirkung der Carboanhydrase
|
|
|
- Chantal Gerhardt
- vor 7 Jahren
- Abrufe
Transkript
1 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: SS 09 Gruppe 10 vorgegebener Versuch Die Wirkung der Carboanhydrase Reaktion: C2 2 C 2 3 C3 Zeitbedarf: Vorbereitung: Versuchsdurchführung: Nachbereitung 30 min 60 min 30 min Chemikalien: Chemikalien Frisches Rinder- oder Schweineblut Ethanol- Wasser- Lösung (4:6) Kochsalz- Lösung (w = 0,9 %) Trichlormeth an (Chloroform) Phenolrot Summenformel C 5 - ca. 100 ml Menge R-Sätze S-Sätze Gefahrensymbole Schuleinsatz (essgiss) S 1 2 aq 2,5 ml F S 1 NaCl aq 4 ml S 1 CCl 1 ml C 5 48/20/22 36/37 Xn Keine Schülerexperimente erlaubt S 1,25 mg 36/37/ Xi S 1 (*) 1
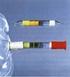
2 Natrium- Dinatriumhy hydrogencar- bonat drogenphosphat Kohlensäure haltigesmine ralwasser NaC 2,2 g /25 - S 1 3 Na 2 P " 3 C " aq 5,3 g S ml S 1 (*) Ersatzstoffprüfung ist besonders wichtig. Geräte und Materialien: 5 x Bechergläser (ca. 100 ml) 2 x Reagenzgläser 2 x Zentrifugengläschen 2 x Gummistopfen (passend zu den Zentrifugengläschen) 5 x Spritzen (2 x 2 ml, 1 x 5 ml, 2 x 10 ml) mit Kanüle Zentrifuge Luftdichtes Aufbewahrungsgefäß für das Blut (ca. 100 ml) Versuchsaufbau: Abb. 1: Vorbereitetes Schweineblut sowie die Komponenten der Pufferlösung, die Phenolrot-Lösung, die Ethanol-Wasser-Lösung, die physiologische Kochsalzlösung, Trichlormethan und zwei Zentrifugengläschen. Versuchsdurchführung: 2
3 a) Enzymisolation aus Erythrocyten 6 ml Blut werden zentrifugiert und der Überstand verworfen. Die Erythrocyten im Zentrifugat werden in 4 ml physiologischer Kochsalzlösung erneut aufgeschwemmt und wieder zentrifugiert. Der Überstand wird abermals verworfen. Zu den Erythrocyten im Zentrifugat werden 2,5 ml der wässrigen Methanol-Lösung (4:6) und 1 ml Chloroform gegeben. Dann wird kräftig geschüttelt. Danach wird erneut zentrifugiert. Die Carboanhydrase befindet sich dann im Überstand, der mehrere Tage im Kühlschrank aufbewahrt werden kann. b) Lösungen für den Enzymtest Für die Indikatorlösung werden 1,25 mg Phenolrot und 21,8 mg Natriumhydrogencarbonat in 100 ml entionisiertem Wasser gelöst. Für den Puffer werden zunächst in einem Becherglas 2,2 g NaC 3 in 24 ml entionisiertem Wasser gelöst (Lösung A). Anschließend werden in einem weiteren Becherglas 5,5 g Na 2P in 40 ml entionisiertem Wasser gelöst (Lösung B). Der Puffer wird nun durch Zusammengießen von 20,6 ml der Lösung A und 30 ml der Lösung B hergestellt. Die so entstehende Lösung wird mit entionisiertem Wasser auf ml aufgefüllt. c) Enzymtest In zwei Reagenzgläser wird jeweils 1) 1 ml Phenolrot-Lösung, 0,5 ml Puffer und 1 ml Enzymlösung 2) 1 ml Phenolrot-Lösung, 0,5 ml Puffer und 1 ml entionisiertes Wasser gegeben. Dann werden möglichst gleichzeitig und gleichmäßig je 5 ml kaltes kohlensäurehaltiges Mineralwasser dazugegeben. Beobachtungen: a) Enzymisolation aus Erythrocyten Nach der Zugabe der wässrigen Methanol-Lösung verklumpten die Erythrocyten und klebten am Boden des Zentrifugenglases fest. Die Lösung, die das Enzym enthielt war leicht gelbbraun gefärbt und trübe. c) Enzymtest 3
4 Nachdem die Phenolrot-Lösung und die Pufferlösung zusammengeben wurden, färbte sich das Gemisch violett. Es lag eine klare Lösung vor. 1) Nach Zugabe des isolierten Enzyms in das Reagenzglas 1) färbte sich diese Lösung leicht rosa. Zudem wurde sie durch die Enzymprobe etwas getrübt. 2) Auch nach Zugabe des Wassers in das Reagenzglas 2) blieb die Lösung violett gefärbt und klar. Nach der gleichzeitigen, tropfenweisen Zugabe von je 5 ml gekühlten, kohlensäurehaltigen Mineralswassers konnten folgende Beobachtungen gemacht werden. 1) Sobald die ersten Tropfen in das Reagenzglas gelangten färbte sich die gesamte Lösung gelblich. 2) Beim Zutropfen des Mineralwassers verfärbte sich die Lösung ganz allmählich von violett nach gelb. Am Reagenzglasboden war die Lösung auch 2 min nach den ersten Wassertropfen noch violett gefärbt. Schließlich färbte sich auch diese Lösung vollständig gelb. Insgesamt geschah der Farbwechsel von rosa bzw. violett nach gelb im Reagenzglas 1) binnen Sekunden, während er sich im Reagenzglas 2) innerhalb von Minuten vollzog. Abb. 2: Vorbereitete Lösungen vor Zugabe des Mineralwassers. Abb. 3: Lösungen nach Zugabe des Minealwassers. Die Lösung im Bodenbereich von Reagenzglas 2 ist noch leicht violett gefärbt, während Lösung 1 bereits gelb gefärbt ist. Entsorgung: 4
5 Alle Lösungen wurden neutral in den Sammelbehälter für organische Lösungsmittelabfälle gegeben, da sie entweder in Kontakt mit dem Chloroform standen oder die Indikatorlösung enthielten. Das nicht benötigte Blut wurde mit Wasser verdünnt und in den Ausguss entsorgt. Fachliche Analyse: Um den menschlichen Körper mit Energie zu versorgen, bedarf es biochemischer Prozesse, die grob unter dem Begriff der Zellatmung zusammengefasst werden können. Für die Zellatmung wird neben einem Energieträger, meist Glucose, auch elementarer Sauerstoff benötigt. Der Sauerstoff wird der Luft in den Lungenbläschen entzogen und in den Körper aufgenommen. Als Transportmedium dient das Blut. Der Sauerstoff bindet dabei an die äm-gruppe des ämoglobins und wird damit im Blut gelöst. Jetzt kann über den Blutkreislauf jede Zelle des Körpers mit dem Sauerstoff erreicht werden. Für die Energiegewinnungsprozesse der Zellen dient das 2 als xidationsmittel. Ein auptprodukt der Zellatmung ist das Kohlenstoffdioxid. Für den Körper hat es keinen weiteren Nutzen und wird als Abfallprodukt wieder ausgeschieden. Um erneut zu den Lungen zu gelangen, wo es als Gas ausgeatmet wird, muss es abermals über das Blut transportiert werden. Aufgrund der neuen Molekülstruktur und veränderter chemischer Eigenschaften kann es nicht an der äm-gruppe des ämoglobins binden. Da das Blut zu einem großen Anteil aus Wasser besteht, kann ein Teil des Kohlenstoffdioxids aufgrund seiner Polarität direkt in Lösung gehen. Dennoch lässt sich das C 2 (g) in einem wässrigen Medium besser in Form seines ydrates ( C 3 (aq) (aq) ) transportieren. Kohlenstoffdioxid reagiert dabei mit einem Wassermolekül zur Kohlensäure. In Anwesendheit weiterer Wassermoleküle, zerfällt diese jedoch sofort zu einem Proton und einem ydrogencarbonat-ion. In wässriger Lösung ist das Kohlensäure-Molekül nur zu 0,2 % enthalten. C 2 C C3 (I) Das Kohlenstoffdioxid-Kohlensäure-Gleichgewicht (I) liegt unter Normalbedingungen zu 99 % auf der Linken Seite. Zudem läuft die Kohlensäurebildung nur sehr langsam ab. Um also das im Körper gebildete C 2 (g) effizient im Blut zu lösen und damit den Abtransport dieses Abfallproduktes zu gewährleisten, bedarf es eines Katalysators. Diese Aufgabe wird von einem Enzym, der Carboanhydrase, übernommen. Es ist hauptsächlich in den Erythrocyten, den roten Blutkörperchen, enthalten und ist einer der effizientesten, bekannten Biokatalysatoren. Die Katalysegeschwindigkeit ist mit 36 Millionen Umsetzungen 5
6 pro Enzym-Molekül und Minute enorm hoch. Um es zu isolieren, werden die Erythrocyten in der Zentrifuge vom Blutplasma getrennt und mit einer physiologischen Kochsalzlösung gewaschen. Dabei können sämtliche wasserlöslichen Bestandteile des Blutes ausgewaschen werden. Nach erneutem Zentrifugieren wird ein Wasser-Ethanol-Gemisch sowie Trichlormethan zu den Erythrocyten gegeben. Durch das Konzentrationsgefälle an Salzen und anderen wasserlöslichen Stoffen zwischen dem Inneren der Erythrocyten und der äußeren Lösung, baut sich ein osmotischer Druck auf. Die gelösten Stoffe im Inneren der roten Blutkörperchen sind nicht in der Lage die semipermeable Biomembran nach außen zu durchdringen. Dagegen ist diese Membran wasserdurchlässig, so dass Wassermoleküle, in dem Bestreben einen Konzentrationsausgleich herbeizuführen, ins Innere der Zelle eindringen können. Gleichzeitig sind das Ethanol und das Trichlormethan durch ihren unpolaren, lipophilen Charakter dazu in der Lage die Biomembran zu lösen und stückweise abzutragen. Es kommt zum Platzen der Zellen, so dass der Zellsaft, der auch die Carboanhydrase enthält mit der Wasser-Methanol- Trichlormethan-Lösung vereinigt wird. Die unerwünschten Zellbestandteile können nun mittels Zentrifuge vom flüssigen Überstand getrennt werden. Das Enzym ist dann in diesem Überstand halten. Die Lage des Gleichgewichtes in (I) wird über den p-wert gesteuert. Liegt der p-wert im basischen Bereich, so wird das Gleichgewicht zu Gunsten der Kohlensäurebildung verschoben. Im leicht sauren Milieu dagegen wird die Bildung von Kohlenstoffdioxid und Wasser begünstigt. Menschliches Blut hat einen p-wert im Bereich von p = 7,3 bis p = 7,5. Werden Natriumhydrogencarbonat und Dinatriumhydrogenphosphat in Wasser gelöst, so entsteht eine basische Pufferlösung. Neben den Eigenschaften als Säure-Base-Puffer wirkt das ydrogenphosphat als Stabilisator für das Enzym. Wird nun der Indikator Phenolrot zugesetzt, so zeigt er den basischen Charakter der Lösung durch eine rot-violett Färbung (für p-werte > 7,3) an. Bei Zugabe des Enzyms Carboanhydrase zu dieser Pufferlösung und anschließendem Zutropfen des kohlensäurehaltigen Mineralwassers, katalysiert das Enzym die Bildung des Kohlenstoffdioxid-ydrates. Da die Lösung alkalisch ist, werden die Kohlenstoffdioxid-Moleküle, die in großer Menge im Mineralwasser gelöst sind, schnell umgesetzt. Um den Mechanismus dieser Umsetzung verstehen zu können ist es hilfreich ein stark vereinfachtes Modell der Carboanhydrase zu betrachten. Das aktive Zentrum des Enzyms bildet ein Zn(II)-Kation, das über drei tidin-reste fixiert ist. 6
7 Zn 2 Carboanhydrase Durch den stark nucleophilen Charakter des Zn(II)-Kations bindet an die vierte Koordinationsstelle des Zinks ein Wassermolekül mit einem freien Elektronenpaar des Sauerstoffatoms. Um die positive Ladung am -Atom des Zwischenprodukts (1) zu stabilisieren, wird nun eines der Protonen abgespalten. Das Enzym enthält in seiner Aminosäurekette basische tidin-reste. Dieser tidin-rest ist unter Anderem aus einem aromatischen 5-Ring aufgebaut. Das freie Elektronenpaar des unbesetzten N-Atoms fängt das freigesetzte Proton sofort ab und bildet ein weiteres Zwischenprodukt (2). N N Zn 2 Zn - N R N Zn Carboanhydrase (1) R (2) Dieses Zwischenprodukt ist auf zweifache Weise Aktiviert und reagiert rasch mit einem C2 -Molekül zu einem komplexierten ydrogencarbonat-molekül weiter. Einerseits agiert das Zinkkation als Lewis-Säure und zieht am freien Elektronenpaar des -Atoms eines C2 - Moleküls. Andererseits wirkt der koordinierte ydroxid-rest mit einem seiner freien Elektronenpaare als Lewis-Base und drückt ein Elektronenpaar an das partial positiv geladene C-Atom des Kohlenstoffdioxids. Durch den elektronenziehenden und schiebenden Effekt wird dieser Mechanismus auch als push-pull-mechanismus bezeichnet. Die zweifache Aktivierung des Enzymzentrums erklärt die hohe Reaktionsgeschwindigkeit dieses Katalysators. Schließlich tritt das vorgebildete ydrogencarbonat-molekül aus dem Komplex aus, so dass die Carboanhydrase wieder regeneriert wird. Zn "pull"-effekt Zn Zn 2 - C "push"-effekt δ (2) δ δ (3) Carboanhydrase ydrogencarbonat 7
8 Das vom tidin-rest abgefangene Proton wird nach kurzer Zeit ebenfalls wieder abgespalten. N N N N R R Zunächst werden die so gebildeten Protonen durch die 2 P4 -Ionen der Pufferlösung abgefangen. 2 ( aq) P4 (aq) 2P4 Ist das ydrogenphosphat auf diese Weise vollständig zu Dihydrogenphosphat umgesetzt, so können die Protonen nicht weiter abgefangen werden. Die Lösung wird allmählich saurer, so dass der Indikator Phenolrot das Gemisch gelb (1 < p-wert < 7,3) färbt. Es wird so lange Kohlensäure gebildet, bis sich ein neues Gleichgewicht (I) eingestellt hat. Wird dieses Experiment ohne die Carboanhydrase durchgeführt, so dauert es sehr viel länger, bis sich das Gleichgewicht (I) zu Gunsten der Kohlensäurebildung verschoben hat. Dennoch wird die Lösung auch ohne den Katalysator allmählich saurer. ierbei sorgt das Prinzip von Le Chatelier für eine Verschiebung des Gleichgewichts auf die Produktseite. Durch die hohe Konzentration an gelöstem C 2 im Mineralwasser wird das Gleichgewicht auf die Produktseite gedrückt. Analog zur oben beschriebenen Reaktion wird auch diese Lösung langsam gelb gefärbt. Allerdings dauert die Reaktion sehr viel länger. Der langsame Reaktionsverlauf sorgt auch dafür, dass es innerhalb des Reaktionsgemisches zu unterschiedlichen p-werten kommt. So färbt sich zuerst der obere Bereich der Lösung gelb, da hier als erstes das kohlenstoffdioxidhaltige Wasser vorhanden ist und die Bildung von Kohlensäure bereits stattfindet. Gleichzeitig ist der untere Bereich der Lösung nach wie vor alkalisch und damit violett gefärbt. Nur langsam durchmischt sich die Lösung, so dass der untere Bereich vergleichsweise spät gelb gefärbt wird. 8
9 Methodisch-didaktische Analyse: 1. Einordnung Der Versuch kann wie folgt in die Themengebiete des hessischen Lehrplans (G8) eingebettet werden. Jahrgangsstufe u. Unterrichtseinheit Themengebiet 9G.2 Eigenschaften von Säuren: Saure Lösungen (verdünnte Säuren) in aushalt und Industrie vergleichen; Gefahren im Umgang mit Säuren darstellen; Beispiele: Salzsäure (Schweflige Säure; Schwefelsäure, Kohlensäure). 11G.2 Aminosäuren, Peptide, Polypeptide: Struktur und Eigenschaften natürlicher Aminosäuren; Peptidbindung; Strukturen und Strukturaufklärung von Eiweißen; Vorkommen und Bedeutung; Nachweisreaktionen für Aminosäuren und Eiweiße. 11G.2 Fakultativ: Enzyme: Aufbau und Bedeutung in Stoffwechselprozessen (Modellvorstellung der Enzymkatalyse). 12G.1 Geschwindigkeit chemischer Reaktionen: Reaktionszeit; Reaktionsgeschwindigkeit (Definition und experimentelle Ermittlung; c / t Diagramme); Anwendung analytischer Verfahren zur Messung der Änderung des Reaktionsverlaufs (z.b. Fotometrie, Maßanalyse, Leitfähigkeitsmessungen); Einfluss verschiedener Faktoren (z.b. Stoff, Konzentration, Temperatur, Zerteilungsgrad, Druck); Aktivierungsenergie und Katalyse/ Katalysatoren. 12G.1 Fakultativ: Enzymkinetik: Bedeutung im Stoffwechsel. 2. Aufwand Mit Ausnahme einer Zentrifuge und dazugehörigen Zentrifugengläschen zählen alle verwendeten Geräte zur Standardausrüstung einer Chemiesammlung. Diese ist jedoch wichtig für das Gelingen dieses Versuches. hne die Verwendung einer Zentrifuge können die Erythrocyten nicht ohne weiteres aus dem Blut abgetrennt werden. Der Versuch kann damit nicht ohne die Verwendung einer Zentrifuge durchgeführt werden. Zudem kann sich die Beschaffung von frischem Schweine- bzw. Rinderblut schwierig gestalten, da es wenig Betriebe gibt, in denen noch selbst geschlachtet wird. Die Möglichkeiten der Beschaffung frischen Schweine- bzw. Rinderblutes sind damit ortsabhängig. Alle verwendeten Chemikalien werden nur in kleinen Mengen benötigt und verursachen damit keine hohen Kosten. Durch das Ansetzen zahlreicher Lösungen ist der Versuch sehr zeitintensiv in der Vorbereitung. Auch das Isolieren der Carboanhydrase ist zeitaufwendig. Der gesamte Versuch kann nicht innerhalb einer Doppelstunde durchgeführt werden. Die Isolation des Enzyms und der Enzymtest sind innerhalb einer Doppelstunde durchführbar. Die Nachbereitung erfordert ebenfalls viel Zeit, da die 9
10 Erythrocyten im Zentrifugenglas verklumpen und fest in diesem kleben. Die Reinigung der verwendeten Zentrifugengläser ist sehr aufwendig. Insgesamt ist der Versuch nur bedingt für den Einsatz in der Schule geeignet. Sollte eine Zentrifuge an der Schule vorhanden sein, so eignen sich bei guter Vorbereitung die Isolation des Enzyms und die Durchführung des Enzymtests für den Unterricht. Alle anderen Arbeiten sollten außerhalb des Unterrichts geschehen und nehmen viel Zeit in Anspruch. 3. Durchführung Die gewünschten Effekte sind gut aus der Nähe erkennbar. Die Schüler sollten unbedingt im Bereich des Versuchsgeschehens stehen, um zum einen das Verklumpen der Erythrocyten und zum anderen die Farbumschläge der Versuchslösungen gut beobachten zu können. Alle verwendeten Chemikalien mit Ausnahme des Chloroforms sind nach essgiss für Schülerexperimente ab der Sekundarstufe I freigegeben. Die Verwendung von Chloroform in Schülerversuchen ist nicht erlaubt. Eine Ersatzstoffprüfung für diesen Stoff ist besonders wichtig. Damit darf dieses Experiment nicht als Schülerversuch durchgeführt werden. Literatur: Versuchsvorschrift aus: Naturwissenschaften im Unterricht, 2/06, eft 92, S. 30. K. P. C. Vollhardt, N. E. Schore, rganische Chemie, Dritte Auflage, Wiley-VC Verlag Gmb, Weinheim, A. F. olleman, E. Wiberg, N. Wiberg, Lehrbuch der Anorganischen Chemie, 102. Auflage, Walter de Gruyter & Co., Berlin, Charles E. Mortimer, Ulrich Müller, Chemie, das Basiswissen der Chemie, Georg Thieme Verlag, Stuttgart, Kaim, W.; Schwederski, B., Bioanorganische Chemie Zur Funktion chemischer Elemente in Lebensprozessen, Teubner Studienbücher Chemie, essgiss-datenbank, V / GESTIS-Stoffdatenbank, 2009, Zugriff: Lehrplan Chemie, Gymnasialer Bildungsgang, Jahrgangsstufen 7G bis 12G, essisches Kultusministerium
Gruppe 8 eigener Versuch. Hydrolyse der Seife
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 eigener Versuch ydrolyse der Seife Reaktion:
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 eigener Versuch ydrolyse der Seife Reaktion:
Gruppe 5 eigener Versuch. Hydrolyse von 2-Chlor-2-methylpropan
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 27.05.09 SS 09 Gruppe 5 eigener Versuch ydrolyse von 2-Chlor-2-methylpropan
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 27.05.09 SS 09 Gruppe 5 eigener Versuch ydrolyse von 2-Chlor-2-methylpropan
Gruppe 13 vorgegebener Versuch. Polyelektrolyte im Haargel
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 17.06.09 SS 09 Gruppe 13 vorgegebener Versuch Polyelektrolyte
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 17.06.09 SS 09 Gruppe 13 vorgegebener Versuch Polyelektrolyte
Gruppe 10 eigener Versuch. Maillard-Reaktion
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.07.09 SS 09 Gruppe 10 eigener Versuch Maillard-Reaktion Reaktion:
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.07.09 SS 09 Gruppe 10 eigener Versuch Maillard-Reaktion Reaktion:
Gruppe 9 eigener Versuch. Reaktion von Saccharose und Schwefelsäure
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 3.06.09 SS 09 Gruppe 9 eigener Versuch Reaktion von Saccharose
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 3.06.09 SS 09 Gruppe 9 eigener Versuch Reaktion von Saccharose
Gruppe 7 Pflichtversuch. Darstellung von Essigsäurepentylester aus 1-Pentanol und Essigsäure
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 12.06.09 SS 09 Gruppe 7 Pflichtversuch Darstellung von Essigsäurepentylester
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 12.06.09 SS 09 Gruppe 7 Pflichtversuch Darstellung von Essigsäurepentylester
Gruppe 6 eigener Versuch. Reaktion von Methanol mit Calciumchlorid
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 02.06.09 SS 09 Gruppe 6 eigener Versuch Reaktion von Methanol mit
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 02.06.09 SS 09 Gruppe 6 eigener Versuch Reaktion von Methanol mit
Gruppe 2 eigener Versuch. Veränderung einer Kerzenflamme in Feuerzeuggas
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 20.05.09 SS 09 Gruppe 2 eigener Versuch Veränderung einer Kerzenflamme
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 20.05.09 SS 09 Gruppe 2 eigener Versuch Veränderung einer Kerzenflamme
Gruppe 6 Pflichtversuch. Abnahme der Wasserlöslichkeit der Alkanole mit zunehmender Molekülgröße
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.06.09 SS 09 Gruppe 6 Pflichtversuch Abnahme der Wasserlöslichkeit
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.06.09 SS 09 Gruppe 6 Pflichtversuch Abnahme der Wasserlöslichkeit
Gruppe 9 Pflichtversuch. Unterscheidung von Glucose und Fructose
 Philipps- Universität Marburg FB 1 hemie rganisch-hemisches Grundpraktikum für das Lehramt hristian Lego Leitung: err Dr. Reiß Datum:.06.09 SS 09 Gruppe 9 Pflichtversuch Unterscheidung von Glucose und
Philipps- Universität Marburg FB 1 hemie rganisch-hemisches Grundpraktikum für das Lehramt hristian Lego Leitung: err Dr. Reiß Datum:.06.09 SS 09 Gruppe 9 Pflichtversuch Unterscheidung von Glucose und
Versuch: Molischprobe mit Gelatine H 2 SO 4. O - 2 H e H 2. Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
 Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Molischprobe
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Molischprobe
Gruppe 1 Pflichtversuch. Qualitative Analyse: Nachweis von Kohlenstoff als Kohlendioxid
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 19.05.09 SS 09 Gruppe 1 Pflichtversuch Qualitative Analyse: Nachweis
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 19.05.09 SS 09 Gruppe 1 Pflichtversuch Qualitative Analyse: Nachweis
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Gruppe 7 eigener Versuch. Tollens-Nachweis von Aldehyden (Silberspiegel) , Η 2. Aldehyd Silberspiegel Carbonsäure
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 12.06.09 SS 09 Gruppe 7 eigener Versuch Tollens-Nachweis von Aldehyden
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 12.06.09 SS 09 Gruppe 7 eigener Versuch Tollens-Nachweis von Aldehyden
Gruppe 2 vorgegebener Versuch Darstellung und Bromierung von Ethen
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 15.05.09 SS 09 Gruppe 2 vorgegebener Versuch Darstellung und omierung
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 15.05.09 SS 09 Gruppe 2 vorgegebener Versuch Darstellung und omierung
Gruppe 8 vorgegebener Versuch. Synthese eines Fettalkoholsulfats (FAS)/ Aniontensid
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 02.07.09 09 Gruppe 8 vorgegebener Versuch ynthese eines Fettalkoholsulfats
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 02.07.09 09 Gruppe 8 vorgegebener Versuch ynthese eines Fettalkoholsulfats
Gruppe 4 eigener Versuch. Reduktion von Anthrachinon
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 eigener Versuch Reduktion von Anthrachinon
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 eigener Versuch Reduktion von Anthrachinon
Gruppe 3 Pflichtversuch. Umsetzung von Cyclohexan und Cyclohexen mit Bromwasser. Menge R-Sätze S-Sätze Gefahrensymbole. 300 ml /38
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 3 Pflichtversuch Umsetzung von Cyclohexan
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 3 Pflichtversuch Umsetzung von Cyclohexan
Gruppe 9 vorgegebener Versuch. Verbrennung eines Gummibärchens in der Kaliumchlorat-Schmelze
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 9 vorgegebener Versuch Verbrennung eines
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 9 vorgegebener Versuch Verbrennung eines
Gruppe 8 Pflichtversuch. Verseifung: Spaltung von Estern mit Lauge
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 Pflichtversuch Verseifung: Spaltung von
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 Pflichtversuch Verseifung: Spaltung von
Versuch: Hydrolyse von Stärke mit Speichel
 Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Versuchsprotokoll: Fehling- Spaltung von Saccharose
 Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure
 Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Sublimation & Resublimation
 Reaktionsgleichung I 2 (s) I2 (g) I 2 (s) Zeitbedarf Vorbereitung: 15 min. Durchführung: 7 Std. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel R-Sätze S-Sätze Gefahrensymbole Schuleinsatz
Reaktionsgleichung I 2 (s) I2 (g) I 2 (s) Zeitbedarf Vorbereitung: 15 min. Durchführung: 7 Std. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel R-Sätze S-Sätze Gefahrensymbole Schuleinsatz
Gruppe 11 eigener Versuch. Extraktion von Coffein
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 14.07.09 SS 09 Gruppe 11 eigener Versuch Extraktion von Strukturformeln:
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 14.07.09 SS 09 Gruppe 11 eigener Versuch Extraktion von Strukturformeln:
Versuch: Fehling- und Biuretprobe mit Gummibärchen
 Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Fehling- und Biuretprobe mit
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Fehling- und Biuretprobe mit
+ HBr. Gruppe 2 Pflichtversuch. Fotochemische Halogenierung des Toluols. Reaktion: h ν. Zeitbedarf: Versuchsdurchführung: Nachbereitung
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe Pflichtversuch Fotochemische Halogenierung
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe Pflichtversuch Fotochemische Halogenierung
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Versuch: Maillardreaktion
 Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Maillardreaktion
Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Maillardreaktion
Versuch: Reaktivität von primären, sekundären und tertiären Alkylbromiden gegenüber ethanolischer Silbernitratlösung. keine Reaktion.
 Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Gruppe 05: Alkylchloride gegenüber AgNO 3
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Gruppe 10 Pflichtversuch. Dünnschichtchromatographie Trennung von Aminosäuren
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.07.09 SS 09 Gruppe 10 Pflichtversuch Dünnschichtchromatographie
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.07.09 SS 09 Gruppe 10 Pflichtversuch Dünnschichtchromatographie
Versuch: Isolierung von Citronensäure aus Zitronen
 Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 11, Naturstoffe und Lebensmittel Versuch: Isolierung
Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 11, Naturstoffe und Lebensmittel Versuch: Isolierung
Reaktion zwischen Aluminiumpulver und Iod
 Reaktionsgleichung 2 Al (s) + 3 2 (s) Al 2 6 (s) Zeitbedarf Vorbereitung: 5 min. Durchführung: 15 min. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel Menge R-Sätze S-Sätze Gefahrensymbole
Reaktionsgleichung 2 Al (s) + 3 2 (s) Al 2 6 (s) Zeitbedarf Vorbereitung: 5 min. Durchführung: 15 min. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel Menge R-Sätze S-Sätze Gefahrensymbole
Philipps-Universität Marburg Organisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß Assistentin: Beate Abé
 Philipps-Universität Marburg 14.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 4/Assistentenversuch):
Philipps-Universität Marburg 14.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 4/Assistentenversuch):
Schulversuch (Gruppe 6/Assistentenversuch): Vergleich aliphatischer Alkohole und Phenole
 Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 17.12.2010 Gruppe 8: Ester, Fette, Seifen und
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 17.12.2010 Gruppe 8: Ester, Fette, Seifen und
Schuleinsatz Calciumfluorid CaF 2 (s) 22-24/ S1 Schwefelsäure, (konz., w = 96 %)
 Reaktionsgleichungen F + (aq ) + H (aq ) HF (g) 4 HF (g) + SiO 2 (s) SiF 4 g + 2 H 2 O (l) Zeitbedarf Vorbereitung: 5min. Durchführung: 5 min. Nachbereitung: 5 min. Chemikalienliste Edukte Chemikalien
Reaktionsgleichungen F + (aq ) + H (aq ) HF (g) 4 HF (g) + SiO 2 (s) SiF 4 g + 2 H 2 O (l) Zeitbedarf Vorbereitung: 5min. Durchführung: 5 min. Nachbereitung: 5 min. Chemikalienliste Edukte Chemikalien
+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose
![+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose + 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose](/thumbs/54/33374656.jpg) Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 12.11.2008 Gruppe 3: Alkene, Alkine Versuch: erstellung und
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 12.11.2008 Gruppe 3: Alkene, Alkine Versuch: erstellung und
Gruppe 13 eigener Versuch. Recycling von Polystyrol
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 10.06.09 SS 09 Gruppe 13 eigener Versuch Recycling von Polystyrol
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 10.06.09 SS 09 Gruppe 13 eigener Versuch Recycling von Polystyrol
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Gruppe 4 Pflichtversuch. Bromierung des Kerns von Toluol 40 % Menge R-Sätze S-Sätze Gefahrensymbole. 2 ml /
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 Pflichtversuch omierung des Kerns von Toluol
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 Pflichtversuch omierung des Kerns von Toluol
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch: Reaktivität
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch: Reaktivität
Gruppe 5 Pflichtversuch. Reaktivität von Halogenalkanen
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 27.05.09 SS 09 Gruppe 5 Pflichtversuch Reaktivität von Halogenalkanen
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 27.05.09 SS 09 Gruppe 5 Pflichtversuch Reaktivität von Halogenalkanen
Von Arrhenius zu Brönsted
 Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration
 SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration Der Versuch sollte mindestens zu zweit oder in einer Gruppe durchgeführt werden, damit die Messung so genau wie möglich erfolgt. Als
SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration Der Versuch sollte mindestens zu zweit oder in einer Gruppe durchgeführt werden, damit die Messung so genau wie möglich erfolgt. Als
Experiment Isolierung, Aktivität und Hemmung der Carboanhydrase
 Experiment Isolierung, Aktivität und emmung der Carboanhydrase 1 Aufgabe: Partnerarbeit Bilden ie selbständig Zweiergruppen. tudieren ie zuerst die Einleitung. Legen ie das Material bereit. Bereiten ie
Experiment Isolierung, Aktivität und emmung der Carboanhydrase 1 Aufgabe: Partnerarbeit Bilden ie selbständig Zweiergruppen. tudieren ie zuerst die Einleitung. Legen ie das Material bereit. Bereiten ie
Versuchsprotokoll: Fehling-Glucose
 Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 10 Minuten Abbau/Entsorgung: 5 Minuten (bei angesetzten Lösungen) Chemikalien: Chemikalie R-Sätze S-Sätze Gefahrensymbol Pentahydrat CuS 4 *5 2 22-36/38-50/53
Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 10 Minuten Abbau/Entsorgung: 5 Minuten (bei angesetzten Lösungen) Chemikalien: Chemikalie R-Sätze S-Sätze Gefahrensymbol Pentahydrat CuS 4 *5 2 22-36/38-50/53
Schulversuch-Protokoll Jan gr. Austing
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 5: alogenalkane Versuch: Reaktivität von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 5: alogenalkane Versuch: Reaktivität von
Versuch: Fäden spinnen Polymer aus Citronensäure und Glycerin
 Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Versuch: Blitze unter Wasser
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Blitze unter Wasser
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Blitze unter Wasser
Gruppe 11 vorgegebener Versuch. Isolierung der Citronensäure
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 14.07.09 SS 09 Gruppe 11 vorgegebener Versuch Isolierung der Citronensäure
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 14.07.09 SS 09 Gruppe 11 vorgegebener Versuch Isolierung der Citronensäure
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 17.12.2010 Gruppe 9: Kohlenhydrate Versuch (Nachweis):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 17.12.2010 Gruppe 9: Kohlenhydrate Versuch (Nachweis):
Versuchsprotokoll. Synthese von Aromastoffen. Gruppe 7, Typ: Pflichtversuch O OH H 3 C C C C C CH 3 H H 3 C C C C C O C C OH
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese von Aromastoffen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese von Aromastoffen Gruppe
Versuchsprotokoll. Reaktivität von Alkylbromiden. Gruppe 5, Typ: Pflichtversuch. AgBr + HNO 3 + H 3 C C C C. AgBr + HNO 3 +
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Reaktivität von Alkylbromiden Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Reaktivität von Alkylbromiden Gruppe
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
+ Na. Gruppe 4 vorgegebener Versuch. Reaktion aromatischer Ketone mit elementarem Natrium. Reaktion: Zeitbedarf: Versuchsdurchführung:
 Philipps- Universität Marburg FB 15 hemie rganisch-hemisches Grundpraktikum für das Lehramt hristian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 vorgegebener Versuch Reaktion aromatischer
Philipps- Universität Marburg FB 15 hemie rganisch-hemisches Grundpraktikum für das Lehramt hristian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 vorgegebener Versuch Reaktion aromatischer
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 14.12.2010 Gruppe 9: Kohlenhydrate Versuch (Assi):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 14.12.2010 Gruppe 9: Kohlenhydrate Versuch (Assi):
Versuchsprotokoll. Mischbarkeit von Alkoholen
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Versuch: Bromierung von n-hexan. Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Bemerkung
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Versuch: Alkoholtest mit Dichromat. Chemikalien: Menge: R-Sätze: S-Sätze: Gefahrensymbol: Schuleinsatz:
 Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Versuchsprotokoll. Züchtung von Kandiszucker-Kristallen
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Gruppe 06: pulsierende Amöben
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: pulsierende Amöben Reaktion: Chemikalien: Eingesetzte Stoffe Gefahrensymbole
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: pulsierende Amöben Reaktion: Chemikalien: Eingesetzte Stoffe Gefahrensymbole
Versuchsprotokoll: Mutarotation von Glucose
 Versuchsprotokoll: Mutarotation von Glucose Zeitaufwand: Aufbau: 10 Minuten Durchführung: 24 Stunden Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Glucose
Versuchsprotokoll: Mutarotation von Glucose Zeitaufwand: Aufbau: 10 Minuten Durchführung: 24 Stunden Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Glucose
+ H 2 O. Versuch: Zersetzung von Milchsäure
 Philipps-Universität Marburg 25.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 7, Aldehyde und Carbonsäuren Versuch: Zersetzung von Milchsäure
Philipps-Universität Marburg 25.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 7, Aldehyde und Carbonsäuren Versuch: Zersetzung von Milchsäure
Chemisches Gleichgewicht
 Schulversuchspraktikum Lars Lichtenberg Sommersemester 2015 Klassenstufen 11 & 12 Chemisches Gleichgewicht Kurzprotokoll Auf einen Blick: Die Unterrichtseinheit,,Chemisches Gleichgewicht für die Klassenstufen
Schulversuchspraktikum Lars Lichtenberg Sommersemester 2015 Klassenstufen 11 & 12 Chemisches Gleichgewicht Kurzprotokoll Auf einen Blick: Die Unterrichtseinheit,,Chemisches Gleichgewicht für die Klassenstufen
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Zeitbedarf Gruppe 6: Alkohole Versuch: Mischungsexperimente
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Zeitbedarf Gruppe 6: Alkohole Versuch: Mischungsexperimente
Gruppe 6 Pflichtversuch. Alkoholtest mit Schwefelsäure und Kaliumdichromat
 Philipps- Universität Marburg FB 15 hemie rganisch-hemisches Grundpraktikum für das Lehramt hristian Lego Leitung: err Dr. Reiß Datum: 0.06.09 SS 09 Gruppe 6 Pflichtversuch Alkoholtest mit Schwefelsäure
Philipps- Universität Marburg FB 15 hemie rganisch-hemisches Grundpraktikum für das Lehramt hristian Lego Leitung: err Dr. Reiß Datum: 0.06.09 SS 09 Gruppe 6 Pflichtversuch Alkoholtest mit Schwefelsäure
Versuchsprotokoll. Gummibärchen-Indikator
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Gummibärchen-Indikator Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Gummibärchen-Indikator Gruppe
Versuch: Qualitativer Nachweis von Kohlenstoff und Wasserstoff
 Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 24.11.2010 Gruppe 4: Aromaten Versuch (selbst):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 24.11.2010 Gruppe 4: Aromaten Versuch (selbst):
Versuchsprotokoll. Nitrierung von Phenol. Gruppe 4, Typ: Pflichtversuch O O - N
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Darstellen eines flüssigen Elements
 Reaktionsgleichungen 2 KBr (s) + H 2 SO 4 (l) K 2 SO 4 (solv ) + 2 HBr (g) 2 HBr (g) + H 2 O 2 (aq ) Br 2 (g) + 2 H 2 O (l) Zeitbedarf Vorbereitung: 30 min. Durchführung: 10 min. Nachbereitung: 10 min.
Reaktionsgleichungen 2 KBr (s) + H 2 SO 4 (l) K 2 SO 4 (solv ) + 2 HBr (g) 2 HBr (g) + H 2 O 2 (aq ) Br 2 (g) + 2 H 2 O (l) Zeitbedarf Vorbereitung: 30 min. Durchführung: 10 min. Nachbereitung: 10 min.
Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose
 Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Organisch Chemisches Grundpraktikum Lehramt WS 2007/08. Gruppe 9 Herstellung von Kupferkunstseide
 rganisch Chemisches Grundpraktikum Lehramt WS 2007/08 Name: Jan Schäfer Datum: 19.1.08 Reaktionsgleichungen: Gruppe 9 erstellung von Kupferkunstseide (aq) + 4 N 3(aq) + 2 - (aq) [Cu(N 3 ) 4 () 2 ] (aq)
rganisch Chemisches Grundpraktikum Lehramt WS 2007/08 Name: Jan Schäfer Datum: 19.1.08 Reaktionsgleichungen: Gruppe 9 erstellung von Kupferkunstseide (aq) + 4 N 3(aq) + 2 - (aq) [Cu(N 3 ) 4 () 2 ] (aq)
Gruppe 3 vorgegebener Versuch. Vergleich von PE-Pyrolysegas und Feuerzeuggas im Lowcost-GC
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 14.05.09 SS 09 Gruppe 3 vorgegebener Versuch Vergleich von PE-Pyrolysegas
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 14.05.09 SS 09 Gruppe 3 vorgegebener Versuch Vergleich von PE-Pyrolysegas
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 2: Alkane Versuch: alogenierung von Alkanen
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 2: Alkane Versuch: alogenierung von Alkanen
Schulversuch-Protokoll Jan gr. Austing
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von Nitroglycerin
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von Nitroglycerin
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Arbeitsblatt Bestimmung der Reaktionsgeschwindigkeit
 Arbeitsblatt Bestimmung der Reaktionsgeschwindigkeit Aufgabe 1: Definieren Sie die folgenden Begriffe: a)reaktionsgeschwindigkeit:. b) Reaktionsordnung: :. Aufgabe 2: Nennen Sie mindestens zwei Beispiele
Arbeitsblatt Bestimmung der Reaktionsgeschwindigkeit Aufgabe 1: Definieren Sie die folgenden Begriffe: a)reaktionsgeschwindigkeit:. b) Reaktionsordnung: :. Aufgabe 2: Nennen Sie mindestens zwei Beispiele
Versuchsprotokoll. Kernbromierung und Seitenkettenbromierung von Xylol. Gruppe 4, Typ: Assiversuch KKK SSS
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Kernbromierung und Seitenkettenbromierung
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Kernbromierung und Seitenkettenbromierung
Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß. Schulversuch-Protokoll Jan gr.
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
Versuch: Emulgierende und dispergierende Wirkung von Tensiden
 Philipps-Universität Marburg 18.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Emulgierende
Philipps-Universität Marburg 18.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Emulgierende
Schulversuchspraktikum. Constanze Koch. Sommersemester Klassenstufen 5 & 6. Wasser als Lösungsmittel. Kurzprotokoll
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Versuch: Seifenherstellung aus Kokosfett
 Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Das Chemische Gleichgewicht
 Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge im Sommersemester 27.07.2011 Betreuung: Dr. M. Andratschke Referent: Hofmann, Martin Das Chemische
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge im Sommersemester 27.07.2011 Betreuung: Dr. M. Andratschke Referent: Hofmann, Martin Das Chemische
Säuren und Basen. 18 UE Präsenz - Selbststudium 1,3 ECTS
 Säuren und Basen 18 UE Präsenz - Selbststudium 1,3 ECTS Überblick 1. Schülervorstellungen Phänomenologische Begriffsbestimmung 2. Verschiedene Definitionen der Begriffe 3. Stärke von Säuren und Basen 4.
Säuren und Basen 18 UE Präsenz - Selbststudium 1,3 ECTS Überblick 1. Schülervorstellungen Phänomenologische Begriffsbestimmung 2. Verschiedene Definitionen der Begriffe 3. Stärke von Säuren und Basen 4.
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, Natriumsalz) - Azofarbstoff -
 Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Versuchsprotokoll. Nachweis von Tensiden in Kernseife, Spülmittel und Waschmittel
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 5.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Nachweis von Tensiden in
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 5.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Nachweis von Tensiden in
Schülercode Erste zwei Buchstaben Letzte zwei Buchstaben des Vornamens deiner Geburtstag (TT) deines Vornamens Mutter Kontext Experiment Aufgabe
 Schülercode Letzte zwei Buchstaben deines Vornamens Erste zwei Buchstaben des Vornamens deiner Mutter Geburtstag (TT) Kontext Experiment Aufgabe Erklärung Box 1 Kontext Kohlensäure im Mineralwasser Heute
Schülercode Letzte zwei Buchstaben deines Vornamens Erste zwei Buchstaben des Vornamens deiner Mutter Geburtstag (TT) Kontext Experiment Aufgabe Erklärung Box 1 Kontext Kohlensäure im Mineralwasser Heute
Bleitiegelprobe (Wassertropfenprobe)
 Reaktionsgleichungen Na 2 SiO 3 + 2 CaF 2 + 3 H 2 SO 4 SiF 4 + 3 H 2 O + 2 CaSO 4 + Na 2 SO 4 SiF 4 + 3 H 2 O H 2 SiO 3 + 4 HF Zeitbedarf Vorbereitung: 20 min. Durchführung: 20 min. Nachbereitung: 10 min.
Reaktionsgleichungen Na 2 SiO 3 + 2 CaF 2 + 3 H 2 SO 4 SiF 4 + 3 H 2 O + 2 CaSO 4 + Na 2 SO 4 SiF 4 + 3 H 2 O H 2 SiO 3 + 4 HF Zeitbedarf Vorbereitung: 20 min. Durchführung: 20 min. Nachbereitung: 10 min.
Versuch: Elektrophile Addition von Brom an Ethen
 Philipps-Universität Marburg 03.12.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 3, Alkene / Alkine Versuch: Elektrophile Addition von
Philipps-Universität Marburg 03.12.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 3, Alkene / Alkine Versuch: Elektrophile Addition von
