Organische Chemie für Bioinformatiker. Dozentin: Dr. Stefanie Kellner 3. Stock BioSysM: Raum 03.
|
|
|
- Felix Althaus
- vor 7 Jahren
- Abrufe
Transkript
1 Organische Chemie für Bioinformatiker Dozentin: Dr. Stefanie Kellner 3. Stock BioSysM: Raum F 1
2 BioSysM 2
3 Vorlesungsplan Reaktionen in der organischen Chemie Elektrophile Addition Nukleophile Substitution Eliminierung Wichtige Stoffklassen Oxidation und Reduktion Aromaten eterocyclen 3
4 Lehrbücher 4
5 Gliederung der Organischen Chemie in vier Reaktionstypen ADDITION (A) ELIMINIERUNG (E) inzufügen weiterer Atome / Atomgruppen; nur an ungesättigten funktionellen Gruppen möglich Abspaltung von Molekülen es entstehen ungesättigte Strukturelemente SUBSTITUTION (S) Austausch eines Atoms / einer Atomgruppe Addition + Eliminierung = Substitution UMLAGERUNG Verschieben von Atomen / Atomgruppen innerhalb des Kohlenstoffgerüstes 5
6 Kohlenwasserstoffe (griech: aleiphar = fettig) aliphatisch aromatisch acyclisch cyclisch gesättigt ungesättigt gesättigt ungesättigt 6
7 A L K A N E gesättigte Kohlenwasserstoffe oder Paraffine Kennzeichen: C C-Einfachbindung parum affinis = wenig reaktionsfähig Endung: -an allgemeine Summenformel: C n 2n+2 keine polaren Gruppen vorhanden unlöslich in Wasser: lipophil oder hydrophob Beispiele: Petrolether (niedrig siedende Benzin-Fraktion, hauptsächlich Gemisch aus Pentan und exan) Vaseline (Wasser und griech. elaion = Öl) halbfestes Paraffin, Schmelzbereich ~ C, komplexes Kohlenwasserstoff-Gemisch 8
8 A L K E N E ungesättigte Kohlenwasserstoffe oder Olefine (gaz oléfiant = Öl bildendes Gas) Kennzeichen: Endung: allgemeine Summenformel: C=C-Doppelbindung -en C n 2n Beispiele C C Ethen C 1 2 C C 3 C 1 2 C 3 C C 2 C 3 Propen 1-Buten 2-Buten 2 C C C 3 3 Konstitutionsisomere 9
9 Alkene: zur zentralen s-bindung gesellt sich ein zusätzliche p-bindung Bruice: Org. Chemie, Pearson-Verlag C -Bindungen: s-bindungen durch C-sp 2 -s-überlappung der C-Atome innere, stabile C C-Bindung: s-bindung durch zentrale sp 2 -sp 2 -Überlappung der C-Atome äußere, weniger stabile C C-Bindung: p-bindung durch seitliche p-p-überlappung der C-Atome keine freie Drehbarkeit um Doppelbindung 10
10 11
11 Elektrophile Addition Entfärbung von Bromwasser Bromoniumion, ein gespannter Dreiring p-komplex 12
12 13
13 Pfeile der organischen Chemie 14
14 Elektrophile Addition Addition von alogenwasserstoff 2 C C C C 2 + Br 2 C C 2 Br Addition von Wasser 3 C C 3 C + 3 C 3 C C C 2 C 2 C 3 3 C C tertiäres Carbenium-Ion + 2 O - C 3 2 C C O C 3 tert. -Butanol C 2 primäres Carbenium-Ion stabiler als 15
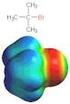
15 Stabilisierung von Carbeniumionen durch Alkylgruppen. Je mehr Alkylgruppen an ein positiv geladenes C-Atom gebunden sind, umso stabiler ist das Kation, da Alkylgruppen elektronenschiebende Eigenschaften aufweisen. Die Elektronenlücke im Methylkation (starke Blaufärbung) ist daher größer als im tert-butylkation (geringere Blaufärbung). (aus Schmuck, Schirmeister: Chemie für Mediziner ) 16
16 ORIENTIERUNG der elektrophilen Addition! MARKOWNIKOW - Produkt Anti-MARKOWNIKOW - Produkt MARKOWNIKOW -Produkt: Das + -Ion bzw. das Elektrophil addiert an das wasserstoffreichere C-Atom regiospezifisch gilt für elektrophile Additionen (A E -Rkt.) nicht für nucleophile oder radikalische Reaktionen 17
17 Propen sek. Carbenium-Ion stabiler wegen des positiv induktiver Effektes der Alkylgruppen 2-Chlorpropan 1-Chlorpropan entsteht nicht! Acrylsäure sek. Carbenium-Ion Carboxylgruppe ist elektronenziehend macht pos. Ladung noch positiver energetisch ungünstig anti - MARKOWNIKOW hier: prim. Carbenium-Ion stabiler 3-Chlorpropionsäure 18
18 2 C C CF C C CF 3 Trifluor-2-propen + Br 2 C C CF 3 Br O 2 C C C Acrolein + 2 C C O + Br 2 C C Br O Ausnahme 2 C C Cl + 2 C C Cl Vinylchlorid + Br 2 C C Cl Br MARKOWNIKOW- Produkt Chlor: I, aber auch +M-Effekt; 2 C C Cl stabilisiert durch freies 19 Elektronenpaar
19 Stereochemie syn anti Nicht verwechseln mit anti-markownikow (Begriff aus der Regiochemie) 20
20 ALKYLALOGENIDE / ALOGENALKANE Substitution (Austausch) eines oder mehrerer Wasserstoffatome durch alogen (Fluor, Chlor, Brom, Iod) Unterscheidung nach Alkylierungsgrad des halogenierten C-Atoms primär 3 C C 2 Br Beispiele: Ethylbromid Eigenschaften wasserunlöslich: lipophil/hydrophob Siede-oder Kochpunkte (KP): > Alkane < Alkohole sekundär 3 C C 3 C Cl Isopropylchlorid tertiär 3 C 5 C 2 C 3 7 C I 3-Iod-3-methylhexan 21
21 Siedepunkte und Kochpunkte Ethylchlorid Ethanol Cl 12 C Bei Raumtemperatur Campus Großhadern gas gas gas gas flüssig gas gas gas flüssig flüssig 22
22 wird nucleophil angegriffen Folge: heterolytische C X-Bindungsspaltung 23
23 Nucleophile Substitutionen am gesättigten, sp 3 -hybridisierten C-Atom! Nucleophil Substitution = Austausch Nu oder Nu Neutralmolekül (z.b. N 3 ) oder Anion (z.b. O ) kernliebendes Teilchen weist eine erhöhte Elektronendichte auf besitzt freies/nichtbindendes Elektronenpaar - diese haben eine hohe Energie - oder leicht verschiebbare p-bindung reagiert mit Teilchen, die selbst ein Elektronendefizit besitzen polare Reaktion Bindungen werden heterolytisch gebildet und gespalten d Abgangsgruppe Nucleophil 24
24 Nucleophilie Definition: Fähigkeit, Elektronenpaar für die Bindung an ein positiv polarisiertes Atom (zumeist Kohlenstoff/C) bereitzustellen; charakterisierbar durch den Vergleich verschiedener Reaktionsgeschwindigkeiten kinetischer Vorgang bestimmt durch: Basizität: Reaktion mit einem Proton, Gleichgewichtskonstante mit Wasser thermodynamischer Vorgang Polarisierbarkeit: Deformierbarkeit der Elektronenhülle vereinfacht: Basenstärke Nucleophilie 25
25 Beispiele C 2 5 O O C 6 5 O 3 CCOO 2 O NO 3 I Br Cl F O basischer als S ; S aber nucleophiler RS ArS I CN O N 3 Br ArO Cl AcO 2 O Phenolat O S Thiophenolat 26
26 (Bruice: Organische 27 Chemie, Pearson-Verlag)
27 Lösungsmittel Beim Lösen eines Stoffes: intermolekulare (bei Salzen interionische) Kräfte, die ihn zusammenhalten, werden durch intermolekulare Wechselwirkungen zwischen den Molekülen und dem Lösungsmittel ersetzt. Wir sprechen von Solvatation. ülle von Solvensmolekülen schirmen ab kleines Fluorid wird gut solvatisiert Vollhardt: Organsiche Chemie, Wiley-VC großes Iodid wird schlecht solvatisiert Je besser ein Ion solvatisiert wird, um so schwächer ist seine Nucleophilie 28
28 protische Lösungsmittel 2 O 3 C C 3 3 C C 3 C C 78 O 20 O Wasser Methanol 33 Ethanol 25 3 C O Ameisensäure COO 58 Formamid 109 *Dielektrizitätskonstante e r ( ) 5 C 2 O 3 C 3 C S O 3 C 3 C 3 C C N 3 C C N 3 C C N C 3 dipolar-aprotische Lösungsmittel O S O 3 C C N C 3 O O 2 N C 3 N C 3 O O Aceton Dimethylsulfoxid (DMSO) 47 Acetonitril 37 Dimethylformamid (DMF) 37 Nitromethan 29 [ unpolare Lösungsmittel sind z.b. n-exan (1.9) Toluol (2.4) Diethylether (4.2) Chloroform 37
29 zunehmende Größe zunehmende Basizität zunehmende Nucleophilie in einem aprotischen LM zunehmende Nucleophilie in einem protischen LM Die Nucleophilie ist vom Lösungsmittel abhängig! Aprotische Lösungsmittel verringern den Solvatationseffekt die Reaktivität des Nucleophils steigt Lösungsmittel Geschwindigkeitskonstante Methanol k = 1 Aceton k = 500 Die Nucleophilie kleiner Anionen nimmt beim Wechsel von einem protischen zu einem aprotischen Lösungsmittel stärker zu als die der großen Anionen. 30
30 Konjugierte Säure pk a Abgangsgruppe Eignung als Abgangsgruppe I -10 I gut Br -9 Br gut Cl -8 Cl gut 3 C SO 3 (Methansulfonsäure) Abgangsgruppe (oder Nucleofug) C SO 3 (Mesylat) gut F 3.2 F schlecht 3 C CO C CO 2 schlecht 3 C O C O (Methylat, Methanolat, Methoxid) schlecht 2 O 15.7 O schlecht schwache Basen sind gute Abgangsgruppen starke Basen sind schlechte Abgangsgruppen 31
31 äufig vorkommende sind: Iodid, Bromid, Tosylat, Mesylat, Chlorid schlecht Substituierbarkeit F Cl Br I gut hoch alogen-kohlenstoff-bindungsenergie Basizität niedrig pk a -Wert: quantifiziert die Stabilität des Anions relativ zu seiner Säure niedriger/negativer pk a -Wert bedeutet starke Säure bzw. stabiles Anion und schlechte Abgangsgruppe schwächere Basen sind gute Abgangsgruppen Iodid und Bromid sind gute Abgangsgruppen, Chlorid ist weniger gut und Fluorid ist schlecht gute Abgangsgruppe, wenn geringe C al-bindungsenergie niedriger/negativer pk a -Wert der korrespondierenden Säure, was geringe Basizität des Anions bedeutet 32
32 Ambidente Nucleophile zwei reaktive Zentren ambi: zweifach dent: Zahn Bsp. Nitrit O: höhere Elektronendichte, weil größere Elektronegativität harte Base N: höhere Nucleophilie, geringere Elektronendichte weiche Base Angriff des elektronegativeren Sauerstoffs S N 1 sek-butylnitrit S N 2 2-Nitrobutan Angriff des nucleophileren Stickstoffs 33
33 S N 1 - Reaktion! 3 C C 3 C Br C 3 - Br 3 C Carbenium-Ion C 3 C C3 als Zwischenprodukt 3 C C 3 C O C 3 O Energiediagramm einer exothermen S N 1-Reaktion 34
34 Substitution nucleophil mono(1)molekular Reaktionsgeschwindigkeit nur vom Ausgangsstoff abhängig, nicht vom Nucleophil O : NUCLEOPIL Br : ABGANGSGRUPPE (Nucleofug) (dicht gepackte bzw. solvatisierte) Ionenpaare Carbenium-Ion Nebenreaktion: durch Konzentrationszunahme der Abgangsgruppe (hier Br ) gegen Ende der Reaktion Rückreaktion in Abhängigkeit von der Stabilität des Carbenium-Ions Racemisierung: Angriff von beiden Seiten möglich 35
35 36
36 EINFLUSSFAKTOREN S N 1 - Reaktionen begünstigt durch polare Lösungsmittel: Wasser, Methanol, Ethanol LEWIS-SÄUREN (AlCl 3, BF 3, Ag + ) koordinieren Anion erleichtern Dissoziation Stabilität des Carbenium-Ions tertiär sekundär primär Methyl 37
37 (R) -Enantiomer C 6 5 C 6 5 C Cl C C 3 - Cl C 3 O O O C 6 5 C C 3 C 6 5 C C 3 O 3 C 5 C 6 O O C 6 5 C 3 (S) -Enantiomer nur bei ausreichender Stabilität des Carbenium-Ions ist vollständige Racemisierung zu erwarten 38
38 S N 2 - Reaktion! Energiediagramm einer exothermen S N 2-Reaktion C Br + O O C Br - Br O C 39
39 Substitution nucleophil bi(2)molekular Reaktionsgeschwindigkeit abhängig von Ausgangsstoff und Nucleophil Für das praktische Arbeiten gilt demzufolge: Beide Reaktanden im Reaktionsansatz in möglichst Konzentration vorliegen hoher über planares bzw. pentakoordiniertes C-Atom ein Reaktionsschritt konzertiert stereospezifische Konfigurationsumkehr / WALDEN-Umkehr / Inversion an asymmetrisch substituierten C-Atomen 40
40 41
41 2-Brombutan S-konfiguriert Konfigurationsinversion sek.-butanol R-konfiguriert + Nucleophil + Abgangsgruppe Bruice: Organische Chemie, Pearson-Verlag = 5! 42
42 S N 2-Reaktionen - Einflußfaktoren Reste im aktivierten Komplex: Wechselwirkungen der Reste mit Nucleophil und Abgangsgruppe: 90 R R R R R C X Y C R X 90 3 C 3 C 3 C X 5 C 2 X C X 3 C C X 3 C 3 C große Reste stören S N 2 sterische inderung Kleine Reste begünstigen S N 2 43
43 raumerfüllende Substituenten Substituenten im Carbenium-Ion 120 anstelle 109 Große Reste begünstigen S N 1-Reaktionen sterische Beschleunigung tri-tert- Butylchlormethan Reaktionsgeschwindigkeitskonstante mal höher als bei tert- Butylchlorid tert- Butanol 44
44 S N - Reaktionen können reversibel sein (Cl ), Br und I sind sowohl gute Nucleophile als auch gute Abgangsgruppen S N 2 bei primären alogenalkanen Gleichgewicht auf Seite der Chloralkane (infolge der relativen Bindungsstärken von Ausgangsmaterial und Produkt) Löslichkeit in Aceton: Lithiumhalogenide allesamt gut Natriumhalogenide: NaI NaBr NaCl FINKELSTEIN-REAKTION Nucleophil Abgangsgruppe 45
45 Zusammenfassung S N 1 S N 2 zweistufig über Carbenium-Ion sterische Beschleunigung an tertiären C-Atomen Racemisierung polare Lösungsmittel monomolekular: Reaktionsgeschwindigkeit vom Edukt abhängig einstufig/konzertiert sterische inderung an primären C-Atomen Konfigurationsinversion dipolar-aprotische Lösungsmittel bimolekular: Reaktionsgeschwindigkeit von Edukt und Nucleophil abhängig 46
46 Bspe. nucleophiler Substitutionen am gesättigten Kohlenstoffatom Veresterung von Alkoholen mit alogenwasserstoffsäuren R O + Br R Br + 2 O ydrolyse von Alkylhalogeniden saure Veretherung R I + R O R O R + I Etherspaltung Synthese von Thiolen R Br + S - R S + Br - Synthese von Sulfiden R Br + RS - R S R + Br - 47
47 Nucleophile Substitutionen Einfluss des Elektrophils: SN1 oder SN2? Einfluss des Nukleophils: SN1 oder SN2? Einfluss des Nukleofugs: Bennen/Markieren Sie die Abgangsgruppe? 48
48 Nucleophile Substitutionen SN1 oder SN2? 49
49 Elektrophile Addition Welches Reaktionsprodukt wird gebildet bei Addition von Cl Welches Reaktionsprodukt wird gebildet bei Addition von Br Welches Reaktionsprodukt wird gebildet bei Addition von Cl Zeichnen Sie alle möglichen Produkte bei Addition von Brom 50
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Kapitel 3. Nucleophile Substitution
 Kapitel 3. Nucleophile Substitution Reaktionsmechanismen - S N 1-Reaktion: Reaktionskoordinate-Energie-Diagramm; Kinetik, Struktur-Reaktivitätsbeziehungen (stabiles Carbokation, schwaches Nucleophil, gute
Kapitel 3. Nucleophile Substitution Reaktionsmechanismen - S N 1-Reaktion: Reaktionskoordinate-Energie-Diagramm; Kinetik, Struktur-Reaktivitätsbeziehungen (stabiles Carbokation, schwaches Nucleophil, gute
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Vorlesung "Organische Chemie 1" Übungsblatt 4
 Vorlesung "Organische hemie 1" Übungsblatt 4 Ü1: Beim Steamcracken wird eine komplexe Mischung von Kohlenwasserstoffen durch kurzzeitiges Erhitzen in Gegenwart von Wasserdampf in eine Mischung von leichter
Vorlesung "Organische hemie 1" Übungsblatt 4 Ü1: Beim Steamcracken wird eine komplexe Mischung von Kohlenwasserstoffen durch kurzzeitiges Erhitzen in Gegenwart von Wasserdampf in eine Mischung von leichter
4. Alkene und Alkine : Reaktionen und Darstellung
 Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Die verschiedenen Mechanismen der Nucleophilen Substitution
 Die verschiedenen Mechanismen der Nucleophilen Substitution Dinah Shafry 21. Juni 2010 Inhalt Vom Alkan zum Alkohol...2 Struktur der Alkane...2 Die Lösung des Problems...2 Die nucleophile Substitution...2
Die verschiedenen Mechanismen der Nucleophilen Substitution Dinah Shafry 21. Juni 2010 Inhalt Vom Alkan zum Alkohol...2 Struktur der Alkane...2 Die Lösung des Problems...2 Die nucleophile Substitution...2
N H H. Carbanionen Lewis-Basen Olefine (Alkane) Die Stärke der Nucleophilie wird von versch. Faktoren beeinflußt z.b.
 Organische hemie Nucleophil = kernliebend Nucleophil = Teilchen oder Gruppe, die Lewis-basische Eigenschaften aufweist (also mind. ein freies Elektronenpaar besitzt), es gibt neutrale Nucleophile sowie
Organische hemie Nucleophil = kernliebend Nucleophil = Teilchen oder Gruppe, die Lewis-basische Eigenschaften aufweist (also mind. ein freies Elektronenpaar besitzt), es gibt neutrale Nucleophile sowie
4. Alkene und Alkine : Reaktionen und Darstellung
 Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Halogenalkane. Radikalische Halogenierung von Alkanen. Addition von Halogenwasserstoffen an Alkene. H 3 C + HBr H C C C H.
 alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
5. Halogenalkane. Alkylierungsgrad. Halogenalkane Halogenierungsgrad
 5. Halogenalkane Halogenalkane gehören zur Gruppe der Halogenkohlenwasserstoffe (neben Halogenalkenen und Halogenaromaten). In Halogenkohlenwasserstoffen ist mindenstens ein Wasserstoffatom durch ein Halogenatom
5. Halogenalkane Halogenalkane gehören zur Gruppe der Halogenkohlenwasserstoffe (neben Halogenalkenen und Halogenaromaten). In Halogenkohlenwasserstoffen ist mindenstens ein Wasserstoffatom durch ein Halogenatom
kj/mol kj/mol 500 I Halogenmethan
 250 200 150 100 50 0 Vorlesung 11. alogenalkane CalogenBindungsstärke nimmt mit zunehmender Größe des alogens ab CalogenBindungslänge nimmt in derselben Richtung zu (Vollhardt,. Aufl., S. 206, Tab. 61,
250 200 150 100 50 0 Vorlesung 11. alogenalkane CalogenBindungsstärke nimmt mit zunehmender Größe des alogens ab CalogenBindungslänge nimmt in derselben Richtung zu (Vollhardt,. Aufl., S. 206, Tab. 61,
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Versuch: Reaktivität von primären, sekundären und tertiären Alkylbromiden gegenüber ethanolischer Silbernitratlösung. keine Reaktion.
 Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Übungen Kapitel 1 Alkane- Radikalische Substitution
 Übungen Kapitel 1 Alkane- Radikalische Substitution 1. Ein Gemisch aus Halogen und Alkan reagiert bei Bestrahlung mit UV- Licht oder höheren Temperaturen (Bsp. die Gase Methan und Chlor erst bei 250-400
Übungen Kapitel 1 Alkane- Radikalische Substitution 1. Ein Gemisch aus Halogen und Alkan reagiert bei Bestrahlung mit UV- Licht oder höheren Temperaturen (Bsp. die Gase Methan und Chlor erst bei 250-400
ORGANISCHE CHEMIE. Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen
 ORGANISE EMIE Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen hemische Formeln Summenformeln Strukturformeln (Konstitutionsformeln) Ausführliche Strukturformeln Vereinfachte
ORGANISE EMIE Struktur organischer Verbindungen: Formeln, Nomenklatur und Reaktionsmechanismen hemische Formeln Summenformeln Strukturformeln (Konstitutionsformeln) Ausführliche Strukturformeln Vereinfachte
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
II. Halogenalkane, radikalische und nukleophile Substitution
 II. alogenalkane, radikalische und nukleophile Substitution Experimentelle Beobachtung: 36 n-c 6 14 RT n-c 6 13 Br + Br Allgemein formuliert: R- Br 2 -Br R-Br Wie geht das? 37 Mechanismus am besten mit
II. alogenalkane, radikalische und nukleophile Substitution Experimentelle Beobachtung: 36 n-c 6 14 RT n-c 6 13 Br + Br Allgemein formuliert: R- Br 2 -Br R-Br Wie geht das? 37 Mechanismus am besten mit
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
CCl 3. 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan
 V. alogenalkane 2 l 2, l 3, l 4 : wichtige Lösungsmittel l l 1,2-Dichlorethan Insektizid DDT l l 2 1 l 3 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan - Insektizid (P. Müller,
V. alogenalkane 2 l 2, l 3, l 4 : wichtige Lösungsmittel l l 1,2-Dichlorethan Insektizid DDT l l 2 1 l 3 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan - Insektizid (P. Müller,
S N 2, S N 1 E1, E2 S N 2, S N 1, E1, E2
 S N vs. E S N 2, S N 1 - B: E1, E2 H E1, E2 C C - : Nu L S N 2, S N 1, E1, E2 Die vier durch Pfeile angedeutenden Reaktionsmöglichkeiten laufen mit unterschiedlichen Geschwindigkeiten ab. Wichtigste Einflussfaktoren:
S N vs. E S N 2, S N 1 - B: E1, E2 H E1, E2 C C - : Nu L S N 2, S N 1, E1, E2 Die vier durch Pfeile angedeutenden Reaktionsmöglichkeiten laufen mit unterschiedlichen Geschwindigkeiten ab. Wichtigste Einflussfaktoren:
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und Herstellung
 6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
6. Kohlenwasserstoffe Alkane, Alkene, Alkine, Arene Molekülbau, Reaktionen und erstellung Moleküle, die nur Kohlenstoff und Wasserstoff enthalten, werden Kohlenwasserstoffe genannt Prof. Dr. Ivo C. Ivanov
Radikalische Substitution von Alkanen
 adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
Summenformel. Strukturformel. Halbstrukturformel. Fossile Energieträger. ( 10. Klasse NTG 1 / 47 ) ( 10. Klasse NTG 2 / 47 ) ( 10. Klasse NTG 3 / 47 )
 Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Summenformel ( 10. Klasse NTG 1 / 47 ) Angabe der Atomsorten und deren Anzahl innerhalb eines Moleküls z.b. Ethanol C 2 6 O Strukturformel ( 10. Klasse NTG 2 / 47 ) Darstellung der bindenden und freien
Kapitel 3: Nucleophile Substitution am gesättigten (sp 3 ) C-Atom
 Kapitel 3: ucleophile Substitution am gesättigten (sp 3 ) -Atom 3.1. Allgemeines Reaktionsschema und Grundlagen δ δ Solvens X YI Y Substrat ucleophil Substitutionsprodukt XI nucleofuge Abgangsgruppe (engl.
Kapitel 3: ucleophile Substitution am gesättigten (sp 3 ) -Atom 3.1. Allgemeines Reaktionsschema und Grundlagen δ δ Solvens X YI Y Substrat ucleophil Substitutionsprodukt XI nucleofuge Abgangsgruppe (engl.
Ether sind organische Verbindungen mit einer Sauerstoffbrücke (als funktionelle Gruppe) zwischen zwei Alkyl-, Aryl- oder Alkenylresten.
 10. Ether Ether sind organische Verbindungen mit einer Sauerstoffbrücke (als funktionelle Gruppe) zwischen zwei Alkyl-, Aryl- oder Alkenylresten. Ether besitzen die allgemeine Summenformel: C n H 2n+2
10. Ether Ether sind organische Verbindungen mit einer Sauerstoffbrücke (als funktionelle Gruppe) zwischen zwei Alkyl-, Aryl- oder Alkenylresten. Ether besitzen die allgemeine Summenformel: C n H 2n+2
Alkene / Additions-, Eliminierungsreaktionen
 2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
1. Klausur zum Praktikum Organische Chemie I für Studierende der Chemie und der Biochemie im SS 2000
 Prof. Dr. B. König Prof. Dr. Th. Troll 1. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Dienstag, dem 30. Mai 2000 Name: Mustermann...Vorname: Max...
Prof. Dr. B. König Prof. Dr. Th. Troll 1. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Dienstag, dem 30. Mai 2000 Name: Mustermann...Vorname: Max...
9. Alkohole. Alkohole können als Derivate des Wassers betrachtet werden, bei denen ein Wasserstoff durch einen Alkylrest ausgetauscht wurde: IOMC
 9. Alkohole Als ALKOHOLE (Alkanole) bezeichnet man organische Verbindungen, die mindestens eine Hydroxygruppe (-OH) (als Gruppe höchster Priorität) besitzen. Bei den Resten R handelt es sich um ALKYLGRUPPEN!
9. Alkohole Als ALKOHOLE (Alkanole) bezeichnet man organische Verbindungen, die mindestens eine Hydroxygruppe (-OH) (als Gruppe höchster Priorität) besitzen. Bei den Resten R handelt es sich um ALKYLGRUPPEN!
Aufgaben zur Chemie der Alkohole und Ether (incl. deren Herstellung)
 Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Organische Chemie, Reaktionsmechanismen
 , Reaktionen, Teil 3-1 - hemieskript Dr. R. Steiger rganische hemie, Reaktionsmechanismen Das Lernziel dieser Unterrichtseinheit beinhaltet folgende Punkte: Wie können funktionelle Gruppen ineinander überführt
, Reaktionen, Teil 3-1 - hemieskript Dr. R. Steiger rganische hemie, Reaktionsmechanismen Das Lernziel dieser Unterrichtseinheit beinhaltet folgende Punkte: Wie können funktionelle Gruppen ineinander überführt
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
CHE 172.1: Organische Chemie für die Life Sciences
 1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 8. alogenalkane : Nucleophile Substitutions- und Eliminationsreaktionen alogenalkane sind in der organischen
E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 8. alogenalkane : Nucleophile Substitutions- und Eliminationsreaktionen alogenalkane sind in der organischen
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Aliphatische Substitutionen
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aliphatische Substitutionen Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aliphatische Substitutionen Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
Kapitel 4: Eliminierung - Übersicht
 » Reaktionstypen - 1,1-, 1,2-, 1,3-, 1,4-Eliminierung (α-, β-, γ-, δ- Eliminierung), thermische Fragmentierung, cis-eliminierung» Regel - Eliminierung wird begünstigt durch hohe Temperatur, starke Basen,
» Reaktionstypen - 1,1-, 1,2-, 1,3-, 1,4-Eliminierung (α-, β-, γ-, δ- Eliminierung), thermische Fragmentierung, cis-eliminierung» Regel - Eliminierung wird begünstigt durch hohe Temperatur, starke Basen,
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 5: alogenalkane Versuch: Reaktivität von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 5: alogenalkane Versuch: Reaktivität von
Energie. 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital
 sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
S N 2, S N 1 E1, E2 S N 2, S N 1, E1, E2
 S N vs. E S N 2, S N 1 - B: E1, E2 H E1, E2 C C - : Nu L S N 2, S N 1, E1, E2 Die vier durch Pfeile angedeutenden Reaktionsmöglichkeiten laufen mit unterschiedlichen Geschwindigkeiten ab. Wichtigste Einflussfaktoren:
S N vs. E S N 2, S N 1 - B: E1, E2 H E1, E2 C C - : Nu L S N 2, S N 1, E1, E2 Die vier durch Pfeile angedeutenden Reaktionsmöglichkeiten laufen mit unterschiedlichen Geschwindigkeiten ab. Wichtigste Einflussfaktoren:
Organische Experimentalchemie
 PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und
PD Dr. Alexander Breder (abreder@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der umanmedizin, Zahnmedizin und
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Ein kurzer Hinweis vorab:
 Ein kurzer Hinweis vorab: Die Folien 1 18 sind lediglich eine lockere Einführung in die Materie. Konzentriert lesen und mitdenken sollten Sie ab Folie 19, auf der die Überschrift ucleophile Substitution:
Ein kurzer Hinweis vorab: Die Folien 1 18 sind lediglich eine lockere Einführung in die Materie. Konzentriert lesen und mitdenken sollten Sie ab Folie 19, auf der die Überschrift ucleophile Substitution:
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen.
 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
Verzeichnis der Wortabkürzungen... Verzeichnis der Zeichen und Symbole...XVII
 VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
VII Verzeichnis der Wortabkürzungen... XIII Verzeichnis der Zeichen und Symbole...XVII Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung... 3 3.1.2 Einfachbindungen...
Organische Chemie I. OC I Lehramt F. H. Schacher 1
 Organische Chemie I OC I Lehramt F. H. Schacher 1 Organisatorisches Kontakt: Felix H. Schacher IOMC, Lessingstr. 8, Raum 122 Email: felix.schacher@uni jena.de Termine: Vorlesung: Freitag 12 14 Uhr Hörsaal,
Organische Chemie I OC I Lehramt F. H. Schacher 1 Organisatorisches Kontakt: Felix H. Schacher IOMC, Lessingstr. 8, Raum 122 Email: felix.schacher@uni jena.de Termine: Vorlesung: Freitag 12 14 Uhr Hörsaal,
Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff
 Vorlesung 16 Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff Bimolekulare nucleophile Substitutionen (S N 2-Reaktionen) In Vorlesung 11 hatten wir bereits die nucleophile Substitution
Vorlesung 16 Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff Bimolekulare nucleophile Substitutionen (S N 2-Reaktionen) In Vorlesung 11 hatten wir bereits die nucleophile Substitution
Inhaltsverzeichnis. 3 Organische Chemie. Vorwort Chemische Bindung Chemische Reaktionstypen Bindungen...
 VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
VII Inhaltsverzeichnis Vorwort... V 3 Organische Chemie 3.1 Chemische Bindung... 3 3.1.1 Orbitale, deren Hybridisierung und Überlappung....................... 3 3.1.2 Einfachbindungen... 12 3.1.3 Doppelbindungen...
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Arzneistoff der Woche. Alkohole. Eliminierungen. Organische Chemie Agenda. Johann Wolfgang Goethe -Universität Frankfurt am Main
 Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Michael Pieper Universität-Oldenburg - SoSe 2003
 1. Klassifizierung (von : eliminare = aus dem Haus treiben). Allgemeinen Reaktionen bei denen zwei Gruppen (Atome, Ionen, Moleküle) aus einem Substrat abgespalten werden. Die Klassifizierung in α-, β-
1. Klassifizierung (von : eliminare = aus dem Haus treiben). Allgemeinen Reaktionen bei denen zwei Gruppen (Atome, Ionen, Moleküle) aus einem Substrat abgespalten werden. Die Klassifizierung in α-, β-
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
Reaktionsmechanismen nach dem gleichnahmigen Buch von R. Brückner
 eaktionsmechanismen nach dem gleichnahmigen Buch von. Brückner Kap. 2 cleophile Substitution Dr. ermann A. Wegner hermann.wegner@unibas.ch 1 Darauf wird aufgebaut... Atom-rbital & Molekül-rbital Theorie
eaktionsmechanismen nach dem gleichnahmigen Buch von. Brückner Kap. 2 cleophile Substitution Dr. ermann A. Wegner hermann.wegner@unibas.ch 1 Darauf wird aufgebaut... Atom-rbital & Molekül-rbital Theorie
Dipolmomente + - a ohne Feld b mit Feld. δ + δ- δ + δ - δ + δ - δ + δ - δ + δ - δ + Dipolmoment: µ = q * d
 CI_folie29 Dipolmomente δ- + - a ohne Feld b mit Feld + + + + + + - - - - - - Effekt eines elektrostatischen Feldes auf die rientierung polarer Moleküle. Dipolmoment: µ = q * d d: Abstand zwischen den
CI_folie29 Dipolmomente δ- + - a ohne Feld b mit Feld + + + + + + - - - - - - Effekt eines elektrostatischen Feldes auf die rientierung polarer Moleküle. Dipolmoment: µ = q * d d: Abstand zwischen den
Organische Chemie 1 Teil 2
 Inhalte der 7. Vorlesung: 2.4. Bildung & Reaktion von Enolen und Enolaten 2.5 Chemie des Enolatanions 2.6 Enolat-Analoga 2.8 1,3-Dicarbonylverbindungen/ß-Dicarbonylverbindungen 2.9 α,β-ungesättigte Carbonylverbindungen
Inhalte der 7. Vorlesung: 2.4. Bildung & Reaktion von Enolen und Enolaten 2.5 Chemie des Enolatanions 2.6 Enolat-Analoga 2.8 1,3-Dicarbonylverbindungen/ß-Dicarbonylverbindungen 2.9 α,β-ungesättigte Carbonylverbindungen
Ether sind organische Verbindungen mit einer Sauerstoffbrücke (als funktionelle Gruppe) zwischen zwei Alkyl, Aryl oder Alkenylresten.
 10. Ether Ether sind organische Verbindungen mit einer Sauerstoffbrücke (als funktionelle Gruppe) zwischen zwei Alkyl, Aryl oder Alkenylresten. Ether besitzen die allgemeine Summenformel: C n H 2n+2 O
10. Ether Ether sind organische Verbindungen mit einer Sauerstoffbrücke (als funktionelle Gruppe) zwischen zwei Alkyl, Aryl oder Alkenylresten. Ether besitzen die allgemeine Summenformel: C n H 2n+2 O
Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-OC-II Prof. R. Peters
 Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-C- Prof. R. Peters 1. Ergänzen Sie das folgende Schema durch Angabe der fehlenden Produkte oder Reagenzien! Bitte achten Sie auf die korrekte Darstellung
Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-C- Prof. R. Peters 1. Ergänzen Sie das folgende Schema durch Angabe der fehlenden Produkte oder Reagenzien! Bitte achten Sie auf die korrekte Darstellung
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Organische Chemie für MST 5. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie I Molekül der Woche - Azulen
 I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser Reaktion: Chemikalien:
13. Amine und ihre Derivate
 Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen
 KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen Ketone werden nicht weiter oxidiert Ether R1 - O - R2 R-O- ersetzt H bei einem Alkan Ether: MTBE (Antiklopfmittel) Tertiäre Alkohole
KATA LOGO Organische Chemie - Zusammenhänge wichtiger funktioneller Gruppen Ketone werden nicht weiter oxidiert Ether R1 - O - R2 R-O- ersetzt H bei einem Alkan Ether: MTBE (Antiklopfmittel) Tertiäre Alkohole
2. Elektroneneffekte in den organischen Molekülen
 2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Bundesrealgymnasium Imst. Chemie Klasse 8. Reaktionsmechanismen der Aliphate
 Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Bundesrealgymnasium Imst Chemie 2010-11 Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet
Organische Chemie I SS 2018
 Organische Chemie I SS 2018 Organische Chemie I LA / J. C. Brendel 1 Organisatorisches Kontakt: Johannes C. Brendel ZAF, Philosophenweg 7, Raum 103 Email: johannes.brendel@uni-jena.de Felix H. Schacher,
Organische Chemie I SS 2018 Organische Chemie I LA / J. C. Brendel 1 Organisatorisches Kontakt: Johannes C. Brendel ZAF, Philosophenweg 7, Raum 103 Email: johannes.brendel@uni-jena.de Felix H. Schacher,
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
2 Nucleophile Substitutionen am gesättigten Kohlenstoff
 2 ucleophile Substitutionen am gesättigten Kohlenstoff 21 Allgemeiner eaktionsablauf X Y: Y X: allgemeiner: Substrat ucleophil Produkt ucleofug Elektrophil ucleophil Elektrophil ucleophil ucleophile: Anionen
2 ucleophile Substitutionen am gesättigten Kohlenstoff 21 Allgemeiner eaktionsablauf X Y: Y X: allgemeiner: Substrat ucleophil Produkt ucleofug Elektrophil ucleophil Elektrophil ucleophil ucleophile: Anionen
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
REAKTIONEN DER ORGANISCHEN CHEMIE
 REAKTIONEN DER ORGANISCHEN CHEMIE 1) ÜBERSICHT VON DEN REAKTIONEN AUSGEHEND: Die Reaktion der OC lassen sich auf 4 Grundtypen zurückführen: Grundtyp Addition Substitution Eliminierung Umlagerung allg A
REAKTIONEN DER ORGANISCHEN CHEMIE 1) ÜBERSICHT VON DEN REAKTIONEN AUSGEHEND: Die Reaktion der OC lassen sich auf 4 Grundtypen zurückführen: Grundtyp Addition Substitution Eliminierung Umlagerung allg A
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
 INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
INHALTSVERZEICHNIS MC-FRAGEN 3. ORGANISCHE CHEMIE 1 3.1 Grundzüge der chemischen Bindung 1 Säuren und Basen der organischen Chemie 5 3.2 Chemische Reaktionstypen 15 3.3 Stereochemie 39 3.4 Alkane, Cycloalkane
