Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009
|
|
|
- Käthe Beyer
- vor 7 Jahren
- Abrufe
Transkript
1 Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: Assistent: Esther Amstad
2 1. Zusammenfassung Azofarbstoffe gehören zu den bedeutsamsten Farbstoffen der Industrie. In diesem Versuch wurde der Azofarbstoff Orange II in zwei Reaktionsschritten aus den Bestandteilen Sulfanilsäure, Natriumnitrit, Salzsäure und 2-Naphtol synthetisiert. Die Ausbeute betrug 69% bezogen auf die maximal mögliche Ausbeute an Orange II. Weiter konnte mittels UV/VIS-Spektroskopie festgestellt werden, dass die maximale Absorption bei einer Wellenlänge von 485 nm stattfindet, was exakt dem Literaturwert entspricht. Beim Anfärben von Seide und Wollfaden konnte gezeigt werden, dass sich Orange II besonders gut zum Anfärben von Textilien (Wolle, Seide und Nylon) eignet, da diese Aminendgruppen besitzen, welche sich an die Sulfonatanionen des Orange II anlagern. 2. Einführung 2.1. Ziele Ziel dieses Versuchs ist die Herstellung eines Farbstoffs, in unserem Fall Orange II und das Kennenlernen der Methoden zur Einfärbung eines polymeren Materials Theorie Farbstoffe Der Mensch nimmt nur Wellenlängen im Bereich von nm als sichtbares Licht wahr. Wellenlängen, die über oder unter diesem Bereich liegen, bleiben dem menschlichen Auge verwehrt. Werden Elektronen durch absorbieren oder reflektieren von elektromagnetischer Strahlung im sichtbaren Bereich angeregt, so erscheinen uns diese Stoffe farbig. Bei Farbstoff-Molekülen werden die Elektronen durch sichtbares Licht angeregt, was bedeutet, dass sie in höhere Energieniveaus angehoben werden. Da die Moleküle nach geringster Energie streben, fallen diese Elektronen wieder in ihren Grundzustand und emittieren die Energiedifferenz in Form von elektromagnetischer Strahlung. Entspricht die Wellenlänge der elektromagnetischen Strahlung dem Bereich des sichtbaren Lichts so bezeichnen wir diese Moleküle als Farbstoffe. Zu beachten gilt die Tatsache, dass die Farbe des Farbstoffes die Komplementärfarbe des absorbierten Lichtes ist (Tab. 1). Tab.1: Wellenlängen der absorbierten Farben mit den dazugehörigen Komplementärfarben [1] Ungefähre Wellen-länge λ Absorbierte Farbe Beobachtete Farbe (nm) 400 violett gelb 450 blau orange 500 blaugrün orange-rot 550 grün rot 1 / 9
3 600 gelb violett 650 orange blau 700 orange-rot blau-grün 750 rot grün Die Energie eines Teilchens und dessen Wellenlänge stehen im folgenden Zusammenhang: E: Energie h: Planksches Wirkungsquantum ( ) : Frequenz : Wellenlänge c: Lichtgeschwindigkeit ( ) =h =h ( ) (1) Mit Hilfe dieser Formel kann aufgrund der Farbe des emittierten Lichts auf die Energiedifferenz von zwei benachbarten Schalen geschlossen werden. Die wichtigste Klasse industrieller Farbstoffe sind die sogenannten Azofarbstoffe. Charakteristisch für die Azofarbstoffe ist ihre Strukturformel, welche immer folgende Zusammensetzung hat: = R: Reste (R und R können identisch oder verschieden sein) Vertreter der Azofarbstoffe sind beispielsweise Orange II, welches als Textilfarbstoff genutzt wird oder auch Methylorange, welches als ph-indikator zum Einsatz kommt. UV/VIS-Spektroskopie Bei der UV/VIS-Spektroskopie geht es um die Anregung von Elektronensystemen durch elektromagnetische Strahlung. Sind die Wellenlängen der elektromagnetischen Strahlung zwischen ca. 200 bis 400 nm, so spricht man von der UV-Spektroskopie, liegen sie zwischen ca. 400 bis 750 nm, so wird dies als VIS- Spektroskopie bezeichnet. Damit ein Elektron angeregt wird, also die Strahlung absorbiert, muss der einfallende Strahl genau der Energiedifferenz der zwei Energieniveaus entsprechen. Nach kurzer Zeit fallen die Elektronen wieder in ihren Grundzustand zurück und emittieren die zuvor aufgenommene Energie in Form von Wärme und/oder Licht. In einem Molekül gibt es sowohl bindende Valenzelektronen (σ und π) als auch nicht bindende Valenzelektronen. Die Energien zur Anregung von bindenden Valenzelektronen sind deutlich höher als jene für die nicht bindenden. Durch die Absorption kann ein Spektrum erstellt werden mit charakteristischen 2 / 9
4 Absorptionslinien, welche den unterschiedlichen Anregungszuständen entsprechen. Meistens sind es π-elektronen und freie Elektronenpaare, die die Strahlung absorbieren. Chromatographie Als Chromatographie bezeichnet man Trennungsmethoden, bei denen zwei nicht mischbare Phasen in ihre Komponenten zerlegt werden. Der Vorteil dieser Trennungsmethode liegt in seiner schonenden Art sowie der schnellen Durchführbarkeit. Dabei fliesst die eine Phase (mobile Phase) an der anderen, unbeweglichen Phase (stationäre Phase) vorbei. Die stationäre Phase kann sowohl fest als auch flüssig sein, die mobile Phase, die auch als Fliessmittel oder Eluiermittel bezeichnet wird, ist flüssig oder gasförmig. Es existieren unterschiedliche Arten von Chromatographien, wie beispielsweise Dünnschichtchromatographie (DC), Säulenchromatographie oder auch Flüssigkeitschromatographie. In unserem Versuch wurde die Trennung mittels DC- Technik durchgeführt. Dabei bewegt sich die mobile Phase inklusive dem aufzutrennenden Gemisch nur durch Kapillarkräfte durch die stationäre Phase. Synthese von Orange II Die Synthese des Azofarbstoffs Orange II erfolgt in 2 Reaktionsschritten: Der Diazotierung von Sulfanilsäure mit Natriumnitrit und der Azokupplung. Abb. 1: Diazotierung von Sulfanilsäure mit Natriumnitrit [2] Bei der Diazotierung erfolgt im Wesentlichen ein elektrophiler Angriff auf die Aminogruppe der Sulfanilsäure. Zuvor wird Natriumnitrit (NaNO 2 ) in wässriger 3 / 9
5 Lösung zu Natrium (Na + ) - und Nitritionen (NO 2 - ) gespalten. Aus NO 2 - werden über ein Zwischenprodukt (salpetrige Säure) Nitrosoniumionen (NO + ) und Wasser gebildet. Diese Nitrosoniumionen greifen die NH 2 -Gruppe der Sulfanilsäure an und bilden das Diazoniumion und im Nebenprodukt Wasser (siehe Abb.1). Abb. 2: Azokupplung von 2-Naphtol mit dem Diazonium Ion [3] Auch die Azokopplung erfolgt über einen elektrophilen Angriff. Dabei wird das 2- Naphtol unter basischen Bedingungen deprotoniert und erhält beim ersten C-Atom eine negative Ladung. Nun kann eine Kupplungsreaktion erfolgen bei der das Orange II Anion entsteht. 4 / 9
6 3. Materialien und Methoden 3.1. Synthese von Orange II Es wurden 0.95 g Sulfanilsäure ( 99.0 %, Fluka), zusammen mit 10 ml einer 2.5%igen Soda-Lösung in einen 100 ml Erlenmeyerkolben gegeben. Anschliessend wurde gerührt bis sich alles gelöst hat und stellte die Lösung in ein Eisbad. Dann wurde die Lösung auf einen Magnetrührer gestellt um unter Rühren 0.37 g Natriumnitrit hinzuzufügen. Die Lösung wurde anschliessend zusammen mit 5 g Eis und 1 ml konzentrierter Salzsäure (37 vol-%, Fluka) in ein Becherglas gegeben, worauf der Ausfall des Diazoniumions als Chlorsalz zu beobachten war. In ein separates Becherglas wurden 0.7 g 2-Naphtol und 5 ml 10%ige NaOH gegeben. Diese Lösung wurde mit Hilfe einer Pasteurpipette in die Diazoniumsalzaufschlämmung, welche sich im Eisbad befand, überführt. Anschliessend wurde die Lösung im Wasserbad auf 90 C erhitzt und während ca. 10 min stehen gelassen. Dann wurden 3 g NaCl hinzugegeben und die Lösung für 20 Minuten ins Eisbad gestellt. Anschliessend wurde abgenutscht und ca. 2 Mal mit eiskaltem Wasser nachgespült. Das Orange II wurde in ein Pillenglas gegeben und zum Trocknen in den Trockenschrank gestellt Anfärben von polymeren Materialien Zum Anfärben wurde ein Stück Seide (0.25 g) und Wolfaden (0.25 g) verwendet. Dann wurden 50 ml Wasser und 1 g des zuvor hergestellten Farbstoffs Orange II in ein Becherglas gegeben. Ausserdem wurden 0.75 ml H 2 SO 4 (95-97 %, Fluka) und 7.5 g Natriumchlorid zur Lösung hinzugefügt. Nachdem die Lösung im Wasserbad auf 90 C erhitzt wurde, gab man das zu färbende Mat erial hinzu und liess dieses während etwas mehr als einer Stunde bei 90 C in der Lösung. Anschliessend wurde das Material mit kaltem Wasser gewaschen und getrocknet Dünnschichtchromatographie Für die Dünnschichtchromatographie wurde eine Aluplatte mit Kieselgelbeschichtung verwendet. Diese wurde passend zugeschnitten und ca. 1 cm oberhalb des unteren Randes ein Strich gezogen, welcher die Startlinie symbolisierte. Anschliessend wurden die drei Proben (Orange II, Azulen und ein Gemisch der beiden) mit Hilfe von Kapillaren auf die Startlinie aufgetragen. Dann wurde gerade so viel Eluiermittel in ein Becherglas gegeben, damit die Startlinie nicht berührt wurde und die DC- Platte ins Becherglas hineingesetzt. Es wurde solange gewartet bis die Lösemittelfront ca. 1 cm unter dem Rand war, um anschliessend die DC-Platte zu entfernen. Die Dünnschichtchromatographie wurde mit drei unterschiedlichen Eluiermittel durchgeführt, um das geeignete Eluiermittel für das Gemisch zu finden. Die drei eingesetzten Eluiermittel waren Ethanol, Ethylacetat und eine 1:2 Mischung aus Ethanol und Ethylacetat. 5 / 9
7 4. Resultate 4.1. Synthese von Orange II und Anfärben von Materialien Die Ausbeute von Orange II (Molmasse: M = g/mol [4] ) nach dem Trocknen belief sich auf g. Die maximale Ausbeute kann berechnet werden, indem man die hinzugefügte Menge an 2-Naphtol ausrechnet, da diese Komponente beschränkend wirkt. Die 0.7 g 2-Naphtol entsprechen bei einer Molmasse von g/mol einer Stoffmenge von n = mol. Vergleicht man dieses Resultat mit den g, was einer Stoffmenge von mol entspricht, kann die relative Ausbeute zu 69 % berechnet werden. Abb. 3: UV/VIS-Spektrum von Orange II 6 / 9
8 Abb. 3 zeigt das UV/VIS-Spektrum des von uns synthetisierten Orange II. Es ist deutlich bei allen vier Konzentrationen ein Pik bei 485 nm zu erkennen. Zu beachten ist, dass die Kurve für 100 µm um ca. 20 nm nach rechts verschoben ist. Zum Anfärben der Materialien gibt es zu sagen, dass die Seide die Farbe recht gut aufgenommen hat, wobei allerdings ein Teil des Stücks zersetzt wurde. Der Faden nahm die Farbe ebenfalls recht gut auf, verklebte jedoch recht stark Dünnschichtchromatographie Durch Ausprobieren wurde das passende Eluiermittel gesucht. Im Falle des 1:2 Gemischs aus Ethanol und Ethylacetat flossen sowohl Azulen als auch Orange II. Beim reinen Ethylacetat hingegen floss lediglich Azulen und beim reinen Ethanol als Eluiermittel floss nur Orange II. Somit ist das passende Eluiermittel das 1:2 Gemisch, da bei den beiden anderen Fliessmitteln jeweils eine Komponente nicht mitfloss, was zu keinem eindeutigen Trennergebnis führt. 5. Diskussion Die Ausbeute von 69 % ist eher mittelmässig und ist dadurch zu erklären, dass bei den einzelnen Schritten Rückstände in den Behältern geblieben sind. Besonders vor dem Abnutschen war es schwierig den kompletten Inhalt aus dem Becherglas zu bekommen. Allerdings ist die Substanz rein, was beim UV/VIS-Spektrum daran zu erkennen ist, dass es jeweils nur einen Pik gibt. Dieser Pik liegt jeweils ca. bei 485 nm, was exakt mit dem Literaturwert übereinstimmt. Dies kann auch mit den Werten aus Tabelle 1 erklärt werden. Da die Farbe von Orange II zwischen orange und orange-rot liegt muss die Wellenlänge zwischen 450 und 500 nm liegen. Der Faden und das Seidenstück haben die Farbe recht gut aufgenommen, da sie beide über eine Aminendgruppe verfügen. Diese wandelt sich in saurer Umgebung (in unserem Experiment war konzentrierte Salzsäure vorhanden) zu Ammoniumgruppen (-NH 3 + ) um, welche sich mit dem SO 3 - des Orange II verkuppeln. Das Zersetzen von Teilen des Seidenstücks ist damit zu erklären, dass der Anteil der Säure in der Lösung womöglich zu hoch war. Es könnte auch damit zusammenhängen, dass sich die Materialien über eine Stunde in der Lösung bei 90 C befanden. 7 / 9
9 6. Referenzen [1] Skript Versuch 5: Diazotierung und Azokupplung, S.3 [2] Skript Versuch 5: Diazotierung und Azokupplung, S.8 [3] Skript Versuch 5: Diazotierung und Azokupplung, S.10 [4] (Stand: März 2009) 7. Anhang Beantwortung der Fragen Frage 5.1.: Welcher Energie (in kj/mol) entspricht einer Lichtabsorption bei 500 nm? Man verwendet die Formel (1) und setzt ein: = ( )= Multipliziert man nun das Resultat mit N A (= ) so erhält man die Energie für 1 Mol: = = / Frage 5.2.: Weshalb können Methylorange und Kongorot als ph-indikatoren verwendet werden? Wo findet eine Protonierung/Deprotonierung statt? Überlegen Sie sich, ob die aufgeführten Azofarbstoffe wasserlöslich sind! Wie lauten die korrekten Lewisformeln von Methylorange und Orange II? Kongorot und Methylorange können als ph-indikatoren benutzt werden, da sie ihre Farbe ändern je nach ph-wert. Die Protonierung bzw. Deprotonierung findet jeweils dort statt, wo das Natrium angelagert ist, also an den Sulfonatanionen SO 3 -. Im Falle von Methylorange wäre dies (roter Kreis): 8 / 9
10 Frage 5.3.: Bei der Diazotierung muss konz. HCl (aq.) zu Eis zugegeben werden. Warum? Was passiert bei der Verdünnung von konz. HCl? Berechnen Sie die Standard-Reaktionsenthalpien für das Lösen von HCl (g) und H 2 SO 4 (g) in Wasser! Vergleichen Sie die Werte! Weshalb besteht bei der Isolierung des Diazoniumsalzes Explosionsgefahr? Durch die Kühlung mit dem Eis wird die exotherme Reaktion gedämpft. Gibt man das Wasser zur Säure kann die Säure hinaus spritzen und Verätzungen hervorrufen. Die Explosionsgefahr des Diazoniumsalzes rührt daher, da sich die N 2 + -Endgruppe des Diazonium Ions vom Molekül trennt, sobald es mit Luft in Kontakt kommt, was sehr explosiv ist. Berechnung der Standard-Reaktionsenthalpien für das Lösen von HCl und H 2 SO 4 : HCl: + + = = ( ) = 75 H 2 SO 4 : = =( ) = 94 Frage 5.4.: Literatursuchaufgabe: Suchen Sie mit Hilfe des Clicaps die folgende Literaturstelle: P. Griess, Chem. Ber. 11 (1878), 2192 und geben Sie die ihr Geburtsmonat geteilt durch drei (Kommastellen wegstreichen) -te Arbeit im Literaturverzeichnis dieser Arbeit (S. 2199) an. 1) Aus der aus Naphtylamin entstehenden Amidonaphtalinsulfosäure gewonnen. (Clève, Jahresber. 1876, 676) 9 / 9
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53
 Endersch, Jonas 13.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.5: Dünnschicht und Säulenchromatographie Einleitung und Theorie In diesem Versuch wurden
Endersch, Jonas 13.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.5: Dünnschicht und Säulenchromatographie Einleitung und Theorie In diesem Versuch wurden
Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, Natriumsalz) - Azofarbstoff -
 Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008
 Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: zclaudio@student.ethz.ch 1. Abstract
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: zclaudio@student.ethz.ch 1. Abstract
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Synthese des Azofarbstoff Orange II
 ynthese des Azofarbstoff range II a + - rganische Chemie Praktikum 1 Zürich, 05.12.2006 W 2006 / 07 Maresa Afthinos Assistenz: Michael chär Versuchsdurchführung: 27. ovember 2006-1 - CP1 ynthese 2 Maresa
ynthese des Azofarbstoff range II a + - rganische Chemie Praktikum 1 Zürich, 05.12.2006 W 2006 / 07 Maresa Afthinos Assistenz: Michael chär Versuchsdurchführung: 27. ovember 2006-1 - CP1 ynthese 2 Maresa
Essigsäure färbt ph-papier rot. Natronlauge färbt ph-papier blau
 5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
5. SÄUREN UND BASEN ARBEITSBLATT 5.1 WAS SIND INDIKATOREN? DER PH-WERT SÄUREN und BASEN sind Stoffe die sich gegenseitig in ihrer Wirkung aufheben. INDIKATOREN sind Farbstoffe, die über Farbänderungen
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2
 Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 9. Spektralphotometrische Bestimmung einer Gleichgewichtskonstanten: Lambert-Beer und Massenwirkungsgesetz
Institut für Physikalische und Theoretische Chemie Physikalisch-Chemisches Praktikum für Studenten L2 9. Spektralphotometrische Bestimmung einer Gleichgewichtskonstanten: Lambert-Beer und Massenwirkungsgesetz
Protokoll zum Versuch 50: Photometrie vom Thema: Photometrische Fe 2+ -Konzentrationsbestimmung mit Phenanthrolin
 Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
Herstellung von Azofarbstoffen und Färben von Textilien
 Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Herstellung von Azofarbstoffen und Färben von Textilien Einleitung ach ihrer chemischen Struktur teilt man die organischen Farbstoffe in eine Reihe verschiedener Gruppen ein. Die bedeutendste ist die der
Protokoll Tag 4, Teil 1
 Protokoll Tag 4, Teil 1 D. Titrationsverfahren D.1. Einführung in die quantitative Analyse; D.2. Acidimetrie (Bestimmung der Konzentration einer Säure) Am heutigen letzten Tag des Praktikums geht es um
Protokoll Tag 4, Teil 1 D. Titrationsverfahren D.1. Einführung in die quantitative Analyse; D.2. Acidimetrie (Bestimmung der Konzentration einer Säure) Am heutigen letzten Tag des Praktikums geht es um
Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on
 Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
5 Elektronenübergänge im Festkörper
 5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
Tris(acetylacetonato)eisen(III)
 Praktikum rg. und Anorg. Chemie II DCHAB Wintersemester 04/05 Zürich, den 15. November 2004 Tris(acetylacetonato)eisen(III) [Fe(acac) 3 ] Fe 1 1. SYNTHESE 1.1 Methode [1] Eisen(III)chlorid wird mit Ammoniak
Praktikum rg. und Anorg. Chemie II DCHAB Wintersemester 04/05 Zürich, den 15. November 2004 Tris(acetylacetonato)eisen(III) [Fe(acac) 3 ] Fe 1 1. SYNTHESE 1.1 Methode [1] Eisen(III)chlorid wird mit Ammoniak
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Chloro(triphenylphosphin)gold(I)
 raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe.
 2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 09. April 2018 Inhalt: Volumetrische Messgeräte Analysenwaagen Fest-Flüssig-Trennverfahren Flüssig-Flüssig-Trennverfahren Wasserlöslichkeit
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 09. April 2018 Inhalt: Volumetrische Messgeräte Analysenwaagen Fest-Flüssig-Trennverfahren Flüssig-Flüssig-Trennverfahren Wasserlöslichkeit
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Schweizerische Maturitätsprüfung Gruppe / Kandidat/in Nr:... Winter 2010, Zürich Name/Vorname:...
 Gruppe / Kandidat/in Nr:... Name/Vorname:... Grundlagenfach Bereich Teil: NATURWISSENSCHAFTEN Chemie Verfasser: Richtzeit: Hilfsmittel: Hinweise: R. Guenin, J. Lipscher, S. Steiner 80 Minuten (von total
Gruppe / Kandidat/in Nr:... Name/Vorname:... Grundlagenfach Bereich Teil: NATURWISSENSCHAFTEN Chemie Verfasser: Richtzeit: Hilfsmittel: Hinweise: R. Guenin, J. Lipscher, S. Steiner 80 Minuten (von total
Säure-Base Titrationen
 Chemie Praktikum Säure-Base Titrationen WS 2006/2007 Verfasser: Lorenz Germann, Lukas Bischoff Versuchsteilnehmer: Lorenz Germann, Lukas Bischoff Datum: 29.11.2006 Assistent: Lera Tomasic E-mail: lukas-bischoff@student.ethz.ch
Chemie Praktikum Säure-Base Titrationen WS 2006/2007 Verfasser: Lorenz Germann, Lukas Bischoff Versuchsteilnehmer: Lorenz Germann, Lukas Bischoff Datum: 29.11.2006 Assistent: Lera Tomasic E-mail: lukas-bischoff@student.ethz.ch
Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie
 Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13
 Kantonsschule Kreuzlingen, Klaus Hensler Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13 Grundregeln für stöchiometrische Berechnungen Wenn es um Reaktionen geht zuerst die chem. Gleichung aufstellen
Kantonsschule Kreuzlingen, Klaus Hensler Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13 Grundregeln für stöchiometrische Berechnungen Wenn es um Reaktionen geht zuerst die chem. Gleichung aufstellen
Anorganische Chemie. Versuch 16 Titration einer schwachen Säure gegen eine starke Base. Versuchsteil 16.1 Potentiometrische Titration
 Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Anorganische Chemie Versuch 16 Titration einer schwachen Säure gegen eine starke Base Versuchsteil 16.1 Potentiometrische Titration
Georg-August-Universität Göttingen Fakultät für Biologie und Psychologie Anorganische Chemie Versuch 16 Titration einer schwachen Säure gegen eine starke Base Versuchsteil 16.1 Potentiometrische Titration
Chloro(salen*)mangan(III)
 Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Phasendiagramm. Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 6; Verfasser: Philippe Knüsel
 Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 6; 19.11.2008 Phasendiagramm Verfasser: Philippe Knüsel (pknuesel@student.ethz.ch) Versuchsdurchführung: Claudio Zihlmann und Philippe Knüsel Assistenz:
Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 6; 19.11.2008 Phasendiagramm Verfasser: Philippe Knüsel (pknuesel@student.ethz.ch) Versuchsdurchführung: Claudio Zihlmann und Philippe Knüsel Assistenz:
Organisches Praktikum I - SS 2006 Assistentin: Gabi Marti. Synthese von. Isobutylacetat. Zürich, Balzers & Eschen, Mai 2005
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
Name: Punktzahl: von 57 Note:
 Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Rosa Geheimschrift. Durchführung
 Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Name: Datum: Materialien verschiedene Papiersorten (auch Filterpapier), Pinsel, Wattestäbchen, Fön, Lösung F (Phenolphthalein-Lösung: 0,1 g/100 ml Ethanol), Lösung G (Natriumcarbonat-Lösung: 1 g/100 ml)
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Quantenphysik in der Sekundarstufe I Atome und Atomhülle Quantenphysik in der Sek I, Folie 1 Inhalt Voraussetzungen 1. Der Aufbau der Atome 2. Größe und Dichte der Atomhülle 3. Die verschiedenen Zustände
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 21/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 11.2.211 Gruppe 12: Farb-, Spreng- und Wirkstoffe
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 21/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 11.2.211 Gruppe 12: Farb-, Spreng- und Wirkstoffe
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
A 2.6 Wie ist die Zusammensetzung der Flüssigkeit und des Dampfes eines Stickstoff-Sauerstoff-Gemischs
 A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2
![Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2](/thumbs/95/126253543.jpg) Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Farbstoffe Zusammenfassung Klausur K2
 Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale
 Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Periodensystem, elektromagnetische Spektren, Atombau, Orbitale Als Mendelejew sein Periodensystem aufstellte waren die Edelgase sowie einige andere Elemente noch nicht entdeck (gelb unterlegt). Trotzdem
Synthese von 1-Amino-2-naphthol
 Illumina-Chemie.de - Artikel Synthesen Synthese von Der wohl bekannteste Weg zu einer Aminogruppe ist die Nitrierung eines Kohlenwasserstoffes und anschließende Reduktion. Reaktive Aromaten wie Phenole
Illumina-Chemie.de - Artikel Synthesen Synthese von Der wohl bekannteste Weg zu einer Aminogruppe ist die Nitrierung eines Kohlenwasserstoffes und anschließende Reduktion. Reaktive Aromaten wie Phenole
P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger
 P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger Warum Spektroskopie auf dem Mars? Befindet sich Wasser auf dem Mars? Gibt es eine Atmosphäre? Aus welchen Elemente besteht sie? Gibt es Leben?
P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger Warum Spektroskopie auf dem Mars? Befindet sich Wasser auf dem Mars? Gibt es eine Atmosphäre? Aus welchen Elemente besteht sie? Gibt es Leben?
Lehrerinformation Brillantblau
 Lehrerinformation: Allgemeines zu Triarylmethylfarbstoffen Viele Gegenstände, mit denen wir tagtäglich in Berührung kommen, sind farbig. Letztlich ist aber all diese Farbenpracht auf die chemischen Verbindungen
Lehrerinformation: Allgemeines zu Triarylmethylfarbstoffen Viele Gegenstände, mit denen wir tagtäglich in Berührung kommen, sind farbig. Letztlich ist aber all diese Farbenpracht auf die chemischen Verbindungen
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung)
 Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Kapitel 4: Lebensmittelfarbstoffe
 Kapitel 4: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität
Kapitel 4: Lebensmittelfarbstoffe Zusatzstoffe Zusatzstoffe werden Lebensmitteln bei der Verarbeitung zugesetzt, um deren Beschaffenheit zu beeinflussen oder bestimmte Eigenschaften wie Haltbarkeit, Stabilität
Die Natriumlinie. und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz
 Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
Von Arrhenius zu Brönsted
 Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Darstellung von Malachitgrün Präparat 5
 Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Probe- und Vergleichslösungen: Trennschicht (stationäre Phase): Kieselgel. Fließmittel (mobile Phase):
 , der Allrounder aus dem Supermarkt Welche Zucker sind in enthalten? Nachweis mittels Dünnschichtchromatografie (DC) [6] 27.06.03 / 04.07.03 Jessica Bornemann Grundlagen: Für die DC verwendet man Kunststofffolien,
, der Allrounder aus dem Supermarkt Welche Zucker sind in enthalten? Nachweis mittels Dünnschichtchromatografie (DC) [6] 27.06.03 / 04.07.03 Jessica Bornemann Grundlagen: Für die DC verwendet man Kunststofffolien,
Quantenphysik in der Sekundarstufe I
 Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Quantenphysik in der Sekundarstufe I Atomphysik Dr. Holger Hauptmann Europa-Gymnasium Wörth holger.hauptmann@gmx.de Quantenphysik in der Sek I, Folie 1 Inhalt 1. Der Aufbau der Atome 2. Größe und Dichte
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Welcher Indikator ist für die Titration von Essigsäure (pks =4.76) mit Natronlauge am besten geeignet?
 1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
1. Aufgaben zu Versuchstag 1: Säure-Base-Titration Aufgabe 1.1 Welche der folgenden Aussagen ist falsch? A) Säuren erhöhen durch Abgabe eines Protons an Wasser die H3O + -Konzentration einer Lösung. B)
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Synthese von Diphenylmethanol
 FS 2008 ET Zürich 23.06.2009 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von Diphenylmethanol Dietikon, 18. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 FS 2008
FS 2008 ET Zürich 23.06.2009 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von Diphenylmethanol Dietikon, 18. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 FS 2008
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
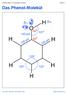 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Arbeitsblatt Wie entstehen Farben?
 Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Anorganische Peroxide und Radikale. von Benjamin Scharbert
 Anorganische Peroxide und Radikale von Benjamin Scharbert Inhalt: 1. Anorganische Peroxide: 2. Radikale: 1.1 Grundsätzliches 1.2 Na 2 O 2 1.3 BaO 2 1.4 H 2 O 2 2.1 Grundsätzliches 2.2 Sauerstoff 2.3 Stickstoffmonoxid
Anorganische Peroxide und Radikale von Benjamin Scharbert Inhalt: 1. Anorganische Peroxide: 2. Radikale: 1.1 Grundsätzliches 1.2 Na 2 O 2 1.3 BaO 2 1.4 H 2 O 2 2.1 Grundsätzliches 2.2 Sauerstoff 2.3 Stickstoffmonoxid
Trisacetylacetonatoferrat(III) Fe(acac) 3
 Trisacetylacetonatoferrat(III) Fe(acac) 3 Mols, 21. 11. 2004 Marco Lendi, AC II 1. Synthese 1.1 Methode Wasserfreies Eisen(III)chlorid wird in wässriger, basischer Lösung durch Erhitzen in Eisen(III)hydroxid
Trisacetylacetonatoferrat(III) Fe(acac) 3 Mols, 21. 11. 2004 Marco Lendi, AC II 1. Synthese 1.1 Methode Wasserfreies Eisen(III)chlorid wird in wässriger, basischer Lösung durch Erhitzen in Eisen(III)hydroxid
Lernmaterial Lernfeld 1 Grundlagen Physik und Chemie. Chemische Grundlagen, Bindungsarten. Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms
 Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Synthese von Adipinsäure Infrarotspektroskopie Nylonsynthese
 Praktikum II, Teil Chemie FS 2009 Versuch 6; 27.02.2009 Synthese von Adipinsäure Infrarotspektroskopie Nylonsynthese Verfasser: Philippe Knüsel (pknuesel@student.ethz.ch) Versuchsdurchführung: Claudio
Praktikum II, Teil Chemie FS 2009 Versuch 6; 27.02.2009 Synthese von Adipinsäure Infrarotspektroskopie Nylonsynthese Verfasser: Philippe Knüsel (pknuesel@student.ethz.ch) Versuchsdurchführung: Claudio
Dünnschichtchromatographie
 PB III/Seminar DC Dünnschichtchromatographie Dr. Johanna Liebl Chromatographie - Prinzip physikalisch-chemische Trennmethoden Prinzip: Verteilung von Substanzen zwischen einer ruhenden (stationären) und
PB III/Seminar DC Dünnschichtchromatographie Dr. Johanna Liebl Chromatographie - Prinzip physikalisch-chemische Trennmethoden Prinzip: Verteilung von Substanzen zwischen einer ruhenden (stationären) und
Farbigkeit bei Molekülen Fluoreszenz Phosphoreszenz
 Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen
 Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen Einleitung Um die Anfangssequenz aus drei Aminosäuren eines Proteins zu bestimmen, benutzen wir eine Methode, bei der schrittweise vom N-terminalen
Versuchsprotokoll 1.3. Sequenzbestimmung von Proteinen Einleitung Um die Anfangssequenz aus drei Aminosäuren eines Proteins zu bestimmen, benutzen wir eine Methode, bei der schrittweise vom N-terminalen
Schulversuchspraktikum. Isabel Großhennig. Sommersemester Klassenstufen 11 & 12. Farbstoffe. Kurzprotokoll
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 11 & 12 Farbstoffe Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen 11 und 12 zum Thema Farbstoffe enthält
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 11 & 12 Farbstoffe Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen 11 und 12 zum Thema Farbstoffe enthält
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau
 Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Gymnasium / Realschule. Atomphysik 2. Klasse / G8. Aufnahme und Abgabe von Energie (Licht)
 Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Gefahrenstoffe. 2 Bechergläser (230 ml), Bürette, Magnetrührer, Trichter, Rührschwein, Pipette, Stativ, Muffe, ph-meter
 1.1 V1 Titration von Cola In diesem Versuch wird die in Cola enthaltene Phosphorsäure mittels Säure-Base-Titration titriert und bestimmt. Ebenfalls wird mit den erhaltenen Werten gerechnet um das chemische
1.1 V1 Titration von Cola In diesem Versuch wird die in Cola enthaltene Phosphorsäure mittels Säure-Base-Titration titriert und bestimmt. Ebenfalls wird mit den erhaltenen Werten gerechnet um das chemische
Bilder Ton Zeit [s] Vorspann
![Bilder Ton Zeit [s] Vorspann Bilder Ton Zeit [s] Vorspann](/thumbs/62/47191146.jpg) Bilder Ton Zeit [s] Vorspann 4 Intro Man kennt es aus dem Alltag: 5 Gegenstände die unter Schwarzlicht leuchten. Aber welche Eigenschaften muss ein Stoff haben, um in Schwarzlicht leuchten zu können? 6
Bilder Ton Zeit [s] Vorspann 4 Intro Man kennt es aus dem Alltag: 5 Gegenstände die unter Schwarzlicht leuchten. Aber welche Eigenschaften muss ein Stoff haben, um in Schwarzlicht leuchten zu können? 6
Wie Heavy Metal ist der Boden?
 Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
Wie Heavy Metal ist der Boden? Inhaltsverzeichnis 1. Entstehung und Ausbreitung von Schwermetallen im Boden 2. Analytische Aufschlussverfahren 3. Grundlagen der UV-VIS- und AAS-Spektroskopie 2 Schwermetalle
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan
 Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Schmelz- und Siedepunkte von typischen reinen Stoffen. Symbolik der Elektronenpaarbindung
 Prof. Dr..-U. Reißig 2.01 Schmelz- und Siedepunkte von typischen reinen Stoffen Salzartig Diamantartig Flüchtige Stoffe Ionengitter Atomgitter diskrete Moleküle (Nal) (af 2 ) (Al 2 O 3 ) 4 6 6 l 4 O 2
Prof. Dr..-U. Reißig 2.01 Schmelz- und Siedepunkte von typischen reinen Stoffen Salzartig Diamantartig Flüchtige Stoffe Ionengitter Atomgitter diskrete Moleküle (Nal) (af 2 ) (Al 2 O 3 ) 4 6 6 l 4 O 2
Dünnschichtchromatographie (DC) und Säulenchromatographie Kurzanleitung
 Dünnschichtchromatographie (DC) und Säulenchromatographie Kurzanleitung Sebastian Meiss 24. Oktober 2008 1 1 Dünnschichtchromatographie Vorbereitung Gemisch fest Gemisch in möglichst wenig Lösungsmittel
Dünnschichtchromatographie (DC) und Säulenchromatographie Kurzanleitung Sebastian Meiss 24. Oktober 2008 1 1 Dünnschichtchromatographie Vorbereitung Gemisch fest Gemisch in möglichst wenig Lösungsmittel
Coffein-Natriumbenzoat Coffeinum-natrii benzoas Synonym: Coffeinum-Natrium benzoicum
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
Einfluß von Substituenten am Benzol auf Geschwindigkeit und Richtung der elektrophilen Substitution
 14.01 Einfluß von Substituenten am Benzol auf Geschwindigkeit und Richtung der elektrophilen Substitution Substitutenten Geschwindigkeit (Reaktivität) Richtung (Regioselektivität) Interpretation 1. 2,,
14.01 Einfluß von Substituenten am Benzol auf Geschwindigkeit und Richtung der elektrophilen Substitution Substitutenten Geschwindigkeit (Reaktivität) Richtung (Regioselektivität) Interpretation 1. 2,,
Qualitative Analyse. - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch,
 - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
- Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Synthese von tert-butylchlorid (2-Chloro-2-methylpropan)
 Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Experiment: Synthese von Gold-Nanopartikeln (Klasse 9)
 Experiment: Synthese von Gold-Nanopartikeln (Klasse 9) Chemikalien Gold(III)-chlorid-Lösung c = 0,000 44 mol/l Natriumcitrat-Lösung c = 1 % Geräte siedendes Wasserbad, Reagenzgläser, Messpipette 10 ml,
Experiment: Synthese von Gold-Nanopartikeln (Klasse 9) Chemikalien Gold(III)-chlorid-Lösung c = 0,000 44 mol/l Natriumcitrat-Lösung c = 1 % Geräte siedendes Wasserbad, Reagenzgläser, Messpipette 10 ml,
(±)-4-Methyl-3- heptanon
 Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Atomabsorptionsspektrometrie (AAS)
 Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 17.11.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Photometrische Analyse der Reduktion von Methylenblau mit Ascorbinsäure, Salzsäure und Lösungsmittel Einfluss
 Kinetik Physikalische Chemie Praktikum Photometrische Analyse der Reduktion von Methylenblau mit Ascorbinsäure, Salzsäure und Lösungsmittel Einfluss Author: Mark Hardmeier markh@student.ethz.ch D-BIOL
Kinetik Physikalische Chemie Praktikum Photometrische Analyse der Reduktion von Methylenblau mit Ascorbinsäure, Salzsäure und Lösungsmittel Einfluss Author: Mark Hardmeier markh@student.ethz.ch D-BIOL
Dichlorobis(triphenylphosphin)nickel(II)
 Praktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 8. November 2004 Dichlorobis(triphenylphosphin)nickel(II) [Ni 2 ( ) 2 ] Ni 1 1. SYNTHESE 1.1 Methode [1] Nickel(II)chlorid reagiert
Praktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 8. November 2004 Dichlorobis(triphenylphosphin)nickel(II) [Ni 2 ( ) 2 ] Ni 1 1. SYNTHESE 1.1 Methode [1] Nickel(II)chlorid reagiert
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 8. Klasse NTG 1 / 48 ) ( 8. Klasse NTG 2 / 48 ) ( 8. Klasse NTG 3 / 48 )
 Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Rf-Werte für einige Saccharide: Arabinose 0,54 Fructose 0,51 Galactose 0,44
 Chromatographie 1996/IV/1 1 Bei der chromatographischen Analyse spielt der Verteilungskoeffizient K eine große Rolle für die Qualität der Auftrennung von Substanzgemischen. Er ist definiert als Quotient
Chromatographie 1996/IV/1 1 Bei der chromatographischen Analyse spielt der Verteilungskoeffizient K eine große Rolle für die Qualität der Auftrennung von Substanzgemischen. Er ist definiert als Quotient
Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure
 Illumina-Chemie.de - Artikel Synthesen Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure Geräte: Erlenmeyerkolben, Becherglas, Scheidetrichter, Pipetten, Trichter und Faltenfilter Chemikalien: Kaliumhexacyanoferrat(III)
Illumina-Chemie.de - Artikel Synthesen Ammoniumhexacyanoferrat(III) / Hexacyanoeisen(III)-säure Geräte: Erlenmeyerkolben, Becherglas, Scheidetrichter, Pipetten, Trichter und Faltenfilter Chemikalien: Kaliumhexacyanoferrat(III)
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13
 Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Kaliumdioxalatocuprat(II)- dihydrat
 Kaliumdioxalatocuprat(II)- dihydrat K[Cu(C4)]H Zürich, 17. November 004 Raphael Aardoom, ACP 300 o C 00 50 150 50 ml 100 A N AUS AN AUS 1000 50 ml 0 U/min 1500 50 750 500 1 Synthese 1.1 Methode [1] Kupfer(II)sulfat-pentahydrat
Kaliumdioxalatocuprat(II)- dihydrat K[Cu(C4)]H Zürich, 17. November 004 Raphael Aardoom, ACP 300 o C 00 50 150 50 ml 100 A N AUS AN AUS 1000 50 ml 0 U/min 1500 50 750 500 1 Synthese 1.1 Methode [1] Kupfer(II)sulfat-pentahydrat
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Betreuer Andreas Branding - 1 - Theorie Zur Erläuterung
Synthese von Acetylsalicylsäure (Aspirin)
 1 Grundlagen 1.1 Einleitung Synthese von Acetylsalicylsäure (Aspirin) von HRISTPH KÖLBL Acetylsalicylsäure, ist eines der weit verbreiteten Schmerz- und Entzündungshemmenden Mittel. Bekannt wurde Acetylsalicylsäure
1 Grundlagen 1.1 Einleitung Synthese von Acetylsalicylsäure (Aspirin) von HRISTPH KÖLBL Acetylsalicylsäure, ist eines der weit verbreiteten Schmerz- und Entzündungshemmenden Mittel. Bekannt wurde Acetylsalicylsäure
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
