Regeln zur Durchführung und Dokumentation von klinischen Studien
|
|
|
- Hetty Schmitz
- vor 8 Jahren
- Abrufe
Transkript
1 Medizinische Universitätsklinik Bonn Allgemeine Innere Medizin Schwerpunkt Hämatologie-Onkologie Regeln zur Durchführung und Dokumentation von klinischen Studien A. Glasmacher, C. Hahn, I.G.H. Schmidt-Wolf Stand: 1. April 1999 (Version 2) Gültig ab: 1. Mai 1999 Nach einigen Fällen von Datenfälschung auswärtiger Arbeitsgruppen und einem deutlich gewachsenen Mißtrauen gegenüber den Ergebnissen klinischer Forschung haben wir diese Regeln zur Dokumentation und Durchführung klinischer Studien zusammengestellt, die helfen sollen, die Glaubwürdigkeit und Qualität unserer Studien zu verbessern. Diese Studien haben einen sehr großen Einfluß auf das Schicksal von Patienten und können nicht ohne große und unnötige Belastung der Patienten wiederholt werden. Wir halten es daher für sehr wichtig, die Ergebnisse und den Ablauf klinischer Studien so zu dokumentieren, daß jederzeit eine externe Nachprüfung von Ergebnissen möglich ist und die Regeln der Good Clinical Practice (GCP) auch für Therapieoptimierungen verwirklicht werden. Grundlagen und Definitionen 1 Diese Regeln gelten für klinische Prüfungen, deren Studienleitung bei Mitarbeitern des Schwerpunktes Hämatologie-Onkologie der Medizinischen Klinik und Poliklinik, Allgemeine Innere Medizin, der Universität Bonn liegt und die mit bereits zugelassenen Arzneimitteln durchgeführt werden (Therapieoptimierungen). Für diese Studien gibt es keinen Sponsor im Sinne des Arzneimittelgesetzes. Bei klinischen Prüfungen, die zur Zulassung eines Arzneimittels dienen und die durch die pharmazeutische Industrie ( Sponsor ) koordiniert werden, gelten in Ergänzung zu diesen Regeln die Anleitungen zur Good Clinical Practice nach der International Conference on Harmonization (ICH-GCP) sowie die entsprechenden gesetzlichen Vorschriften. 2 Diese Regeln gelten im Rahmen der klinischen Prüfung für Studienleitung und kooperierende Zentren gleichermaßen. In Zweifelsfällen gelten die Regeln der Good Clinical Practice (z.b. Langenbahn HH, Hutchinson DR. Ordnungsgemäße klinische Prüfung (Good Clinical Practice): Eine praxisnahe Anleitung für Prüfärzte. Brookwood Medical Publications: Brookwood 1995). 3 Eine Therapieoptimierungsstudie kann erst beginnen, wenn ein vollständiges Studienprotokoll (Prüfplan), ein zustimmendes Votum der Ethik-Kommission des Studienleiters und - falls
2 Med. Univ. Klinik Bonn, Regeln zur Dokumentation klinischer Studien, Seite 2 notwendig - eine Probandenversicherung vorliegt. Die Prüfärzte der kooperierenden Zentren müssen der Studienleitung ihre Teilnahme schriftlich erklären und vor Beginn der Studie abklären, ob eine nochmalige Beratung durch die für sie zuständige Ethik-Kommission notwendig ist und ggf. einen entsprechenden Antrag einreichen. 4 Während der Studie müssen alle Änderungen des Prüfplans, die den Schutz der Patienten oder die Qualität der Studie betreffen (gilt auch für Patienteninformation und einverständniserklärung), erneut der Ethik-Kommission vorgelegt werden. Aufgaben der Studienleitung 5 Die Studienleitung legt für jede Studie einen Studienordner ( Trial Master File ) an, in dem alle Versionen des Studienprotokolles (ab dem ersten Votum der Ethik-Kommission) und der Dokumentationsbögen abgelegt werden, ebenso wie die Korrespondenz mit den kooperierenden Zentren, Korrespondenz und Voten der Ethik-Kommission, Teilnahmeerklärungen der kooperierenden Zentren, Patientenmeldungen, Meldungen schwerer unerwarteter Ereignisse, sowie ggf. die Versicherungspolice und die -bedingungen. 6 Die Studienleitung übersendet jedem kooperierendem Zentrum einen Studienordner ( Trial Center File ), der alle wichtigen Unterlagen für die Durchführung der Studie enthält: Das aktuelle Studienprotokoll, Voten der Ethik-Kommission, Kopie der Versicherungspolice und der Versicherungsbedingungen, Vorlagen der Dokumentationsbögen, diese Regeln zur Dokumentation, gesetzliche Bestimmungen (soweit sie nicht Bestandteil des Protokolles sind), Korrespondenz zwischen Zentrum und Studienleitung und die Fachinformationen wichtiger Arzneimittel (Prüfmedikamente und wichtige Begleitmedikamente). Im kooperierenden Zentrum wird der Studienordner vom Prüfarzt weitergeführt. Alle weiteren wichtigen Unterlagen für den Verlauf der Studie, werden dort abgelegt (Patienteneinverständniserklärungen, Patientenliste, Liste der dokumentierenden Mitarbeiter, Meldungen schwerer unerwarteter Ereignisse). Kopien bzw. Durchschläge der Dokumentationsbögen werden ebenfalls vom Prüfarzt aufbewahrt. Der Studienordner verbleibt im kooperierenden Zentrum und wird nach Abschluß der Studie für 15 Jahre aufbewahrt. Aufnahme von Patienten in die Studie 7 Die Aufklärung des Patienten erfolgt mündlich und schriftlich durch den behandelnden Arzt und das Patienteninformationsblatt. Die Einverständniserklärung muß vom Patienten vor der Durchführung irgendeiner studienspezifischen Maßnahme unterschrieben und eigenhändig datiert werden. Dabei werden die gesetzlichen Vorschriften und die Regeln der durchführenden Institution angewandt. Eine mündliche Einverständniserklärung ist nur in seltenen Ausnahmefällen möglich, die einer besonders sorgfältigen Dokumentation bedürfen. Dieses Vorgehen wird jedoch ausdrücklich nicht empfohlen. Die Einverständniserklärungen
3 Med. Univ. Klinik Bonn, Regeln zur Dokumentation klinischer Studien, Seite 3 werden im Studienordner aufbewahrt und bleiben für eine spätere Einsicht zugänglich. Von der oft üblichen Aufbewahrung der Einverständniserklärung in der Krankenakte wird ausdrücklich abgeraten. Eine Kopie der Einverständniserklärung verbleibt beim Patienten. 8 Die Aufnahme eines Patienten in die Studie erfolgt nach Durchführung folgender Schritte: (1.) Überprüfung der Einschluß- und Ausschlußkriterien, (2.) der Aufklärung und schriftlichen Erklärung des Einverständnisses durch den Patienten und (3.) Absenden (z.b. durch Fax) des Meldebogens an die Studienzentrale. Die Einhaltung dieser Schritte, insbesondere die Meldung an die Studienzentrale ist auch in Bezug auf die Probandenversicherung sehr wichtig, da nach unserer Auffassung nur gemeldete Studienpatienten versichert sind. Regeln zur Dokumentation 9 Jedes kooperierende Zentrum benennt einen für die Studie zuständigen Mitarbeiter (Mitarbeiterin), der auch Ansprechpartner der Studienleitung für die Koordination bzw. Durchführung der Dokumentation ist ( Prüfarzt ). Die Dokumentation selbst kann auch von anderen Mitarbeitern (z.b. einer Dokumentationsstelle im jeweiligen Zentrum) durchgeführt werden, wenn diese Mitarbeiter eingewiesen sind. 10 Jeder, der Einträge in Dokumentationsbögen vornimmt, muß auf der Liste der dokumentierenden Mitarbeiter, die sich im Trial Center File befindet, eingetragen sein. Er muß das jeweilige Studienprotokoll kennen, sein voller Name, seine Berufsbezeichnung, seine Unterschrift und seine Initialen bzw. sein Kürzel müssen in dieser Liste verzeichnet sein und vom Prüfarzt schriftlich bestätigt werden. Diese Mitarbeiter können während der Laufzeit der Studie wechseln, Beginn und Ende der Studienteilnahme der Mitarbeiter müssen jedoch auf der Liste eingetragen werden. Die Studienleitung erhält am Ende der Studie eine Kopie der Liste. 11 Die primäre Aufzeichnung von Patientendaten im Rahmen der Studie ist nur auf den dazu vorgesehenen Dokumentationsbögen möglich. Eine direkte Erfassung in EDV-Systeme ist derzeit nicht möglich, da keine Programme zur Verfügung stehen, die nachträgliche Änderungen erkennbar und nachvollziehbar machen. 12 Jeder Dokumentationsbogen muß zum Abschluß datiert und vom Prüfarzt unterzeichnet werden. Wird nur ein Teil des Dokumentationsbogens an die Studienleitung versendet, so muß dieser Teil ebenfalls vom Prüfarzt datiert und unterschrieben werden. 13 Jede Änderung auf dem Dokumentationsbogen muß so durchgeführt werden, daß der geänderte Text lesbar bleibt, und mit Datum und Initialen/Kürzel versehen werden.
4 Med. Univ. Klinik Bonn, Regeln zur Dokumentation klinischer Studien, Seite 4 14 Vor dem Versand der Dokumentationsbögen von einem Zentrum an die Studienleitung sollten die Bögen vom Prüfarzt durchgesehen und die wesentlichen Angaben (verabreichte Therapie, Ansprechen, Toxizität) auf Plausibilität geprüft werden. Eine Kopie der Bögen sollte im Zentrum verbleiben. Eine Überprüfung der Dokumentationsbögen muß jederzeit möglich sein. Externes Monitoring 15 Wie in den GCP-Regeln festgelegt, muß jedes kooperierende Zentrum und die Studienleitung einem (zumindest teilweisen) externen Monitoring der Daten zustimmen und die Krankenakten dazu zur Verfügung stellen. Ein Gespräch über den Verlauf der Studie mit dem Prüfarzt ist Teil des Monitoring. Das Monitoring im Bereich der Studienleitung kann nicht von einem Mitarbeiter der gleichen Klinik erfolgen. Der Monitor verfaßt einen Bericht, in dem die Ergebnisse (u.a. Studienordner/Trial Center File, Anzahl und Identifikation der geprüften Unterlagen, relevante Abweichungen, Hinweise des besuchten Zentrums zum Verlauf der Studie und zur Dokumentation) aufgeführt werden. Dokumentation im Bereich der Studienleitung 16 Die Studienleitung legt für jede Studie ein Protokollbuch an, in dem alle für die Dokumentation (d.h. Umgang mit Dokumentationsbögen) und Auswertung (d.h. Umgang mit der aufgrund der Bögen erstellten Datenbank) relevanten Tatsachen verzeichnet werden. 17 Die Studienleitung dokumentiert den Eingang des Dokumentationsbogens (Eingangsstempel und Logbuch). 18 Rückfragen der Studienleitung an die Zentren und deren Beantwortung werden beim Dokumentationsbogen auf einem entsprechenden Vordruck vermerkt. 19 Nachträgliche Korrekturen oder Ergänzungen von Dokumentationsbögen sind auch durch die Studienleitung möglich, wenn folgende Angaben erkennbar sind: 19.1 Wer hat die Änderungen durchgeführt? 19.2 Aufgrund welcher Angaben wurden diese Änderungen durchgeführt (z.b. telefonische Rücksprache mit einem zu benennenden Mitarbeiter)? 19.3 Wann wurden diese Änderungen durchgeführt (Datumsangabe)? 19.4 Änderungen der Daten nach Erfassung des Dokumentationsbogen müssen sowohl im Dokumentationsbogen als auch im Protokollbuch vermerkt werden. Unerwünschte Ereignisse
5 Med. Univ. Klinik Bonn, Regeln zur Dokumentation klinischer Studien, Seite 5 20 Schwere unerwünschte Ereignisse (GCP: Serious Adverse Events, (SAE) s. auch unser Informationsblatt zu Adverse Events und Serious Adverse Events in der Anlage) während der Studienbehandlung müssen der Studienleitung sofort (innerhalb von 24 h) telefonisch oder besser per Telefax auf einem dazu vorgesehenen Meldeformular mitgeteilt werden. Prüfarzt und Studienleiter bewerten das unerwünschte Ereignis hinsichtlich des Zusammenhanges mit dem zu prüfenden Arzneimittel (sicherer, wahrscheinlicher, möglicher, kein Zusammenhang). Die sorgfältige Aufzeichnung aller unerwünschten Ereignisse während der klinischen Prüfung ist eine wichtige Aufgabe des Prüfarztes und des Studienleiters. 21 Die Ethik-Kommission am Sitz der Studienleitung wird über alle schwerwiegenden oder unerwarteten (d.h. Nebenwirkungen, die nicht in der Fachinformation aufgeführt sind) unerwünschten Ereignisse, die während der Studie auftreten und die Sicherheit der Studienteilnehmer oder die Durchführung der Studie beeinträchtigen könnten, zeitnah unterrichtet. Über andere SAEs wird jährlich berichtet. 22 Die Prüfärzte werden regelmäßig (z.b. durch Rundschreiben oder Studientreffen) über unerwünschte Ereignisse informiert. Über schwere oder unerwartete unerwünschte Ereignisse, die die Sicherheit der Studienteilnehmer oder die Durchführung der Studie beeinträchtigen könnten, werden die Prüfärzte sofort informiert. Die Prüfärzte werden darauf hingewiesen, diese Meldungen an ihre zuständige Ethik-Kommission weiterzuleiten, soweit diese es wünscht. Auf Anforderung durch den Prüfarzt kann die Studienleitung diese Aufgabe übernehmen. 23 Bei schweren unerwünschten Ereignissen mit sicherem oder wahrscheinlichen Zusammenhang mit dem Prüfarzneimittel wird unverzüglich (im Todesfall innerhalb von 48 Stunden) ebenfalls die für die Studie zuständige Versicherungsgesellschaft informiert. Primär zuständig sind Patient und der Prüfarzt. Nach Absprache kann die Meldung auch durch die Studienleitung erfolgen, wenn die gesetzten Fristen eingehalten werden können. Die Anschrift und Telefonnummer des Versicherungsunternehmens wird in der Einverständniserklärung angegeben. 24 Soweit das unerwünschte Ereignis sicher oder wahrscheinlich durch das zu prüfende Arzneimittel bedingt ist und diese Nebenwirkung nicht bereits aus der Fachinformation bekannt ist, erfolgt eine Unterrichtung der Arzneimittelkommission der Deutschen Ärzteschaft, des Bundesinstitutes für Arzneimittel und Medizinprodukte (BfArM) und des pharmazeutischen Unternehmens durch die Studienleitung. Abschluß und Auswertung der Studie 25 Nach Ende der Studie geben Prüfärzte und Studienleiter einen Bericht über die Sicherheit und Wirksamkeit des geprüften Arzneimittels aufgrund ihrer in der Studie gewonnenen Erfahrungen ab. Diese Berichte werden Teil der Dokumentation der Studienleitung und stehen jedem Studienteilnehmer zur Verfügung.
6 Med. Univ. Klinik Bonn, Regeln zur Dokumentation klinischer Studien, Seite 6 26 Die Erfassung des Dokumentationsbogens in der Datenbank wird auf dem Bogen vermerkt (Datum, Initialen des Erfassenden). Die Daten zur Patientenidentifikation, zu unerwünschten Nebenwirkungen und zu den Therapieergebnissen werden zu 100% und alle anderen Daten zu 20% überprüft. Finden sich in den überprüften Daten mehr als 2% Abweichungen, so wird der gesamte Datensatz abgeglichen. 27 Zur Sicherung der Anonymität werden Patientennamen nicht in der Datenbank erfaßt. Es wird eine Patientenidentifikationsliste angelegt, in der Name und Nummer des Patienten erkennbar sind. Datenlisten mit Patientennamen werden, falls überhaupt elektronisch gespeichert, nur auf dem Server der Med. Univ. Klinik und nicht auf einem peripheren Rechner gespeichert (Diebstahl- und Zugangsschutz). Kooperierende Zentren halten ähnliche Sicherheitsvorkehrungen ein. 28 Die Versionen der Datenbank werden fortlaufend numeriert. Jede Änderung macht eine neue Version notwendig und wird im Protokollbuch unter Angabe des Namens des Ändernden vermerkt. Änderungen in einer Sitzung können zusammengefaßt werden Die verwendete Software muß einschließlich der Versionsnummer so dokumentiert werden, daß jede Auswertung der verwendeten Software zugeordnet werden kann. Dazu wird die Software und ihre Nutzungsdauer im Protokollbuch vermerkt. Das Datum eines Versionswechsels muß festgehalten werden Die Berechnung neuer Variablen bzw. die Umkodierung alter Variablen muß im Protokollbuch einschließlich der verwendeten Formel/Rechenfunktion so detailliert vermerkt werden, daß der Rechenprozeß nachvollziehbar ist. 29 Der nachträgliche Ausschluß von Patienten, die im Rahmen der Studie behandelt wurden, durch das Zentrum oder die Studienleitung muß nach folgenden Regeln dokumentiert werden: 29.1 Identifikation des Patienten und die wesentlichen klinischen Daten (z.b. Diagnose, Alter etc.) 29.2 Informative Darstellung des Problemes (z.b. Art der Protokollverletzung, Fehlen der Einschlußkriterien, Vorliegen von Ausschlußkriterien) 29.3 Art der Entscheidung: Ausschluß und keine weitere Dokumentation; Ausschluß und weitere Dokumentation (z.b. zur Beurteilung der Toxizität), vorübergehender Ausschluß (z.b. bis zur Klärung eines Sachverhaltes) 29.4 Angabe des Entscheidungsträgers und Bestätigung des Studienleiters (mit Datum) 29.5 Ausgeschlossene Patienten werden in der Regel nicht in die Datenbank übernommen bzw. dort als ausgeschlossen markiert. Die Dokumentationsbögen werden aufbewahrt Wird die Entscheidung zum Ausschluß eines Patienten in einem Zentrum getroffen, so übersendet der dort für die Studie zuständige Mitarbeiter die o.a. Unterlagen dem Studienleiter Bei der Auswertung der Studie werden alle ausgeschlossenen Patienten erfaßt und die Gründe für den Ausschluß angegeben.
7 Med. Univ. Klinik Bonn, Regeln zur Dokumentation klinischer Studien, Seite 7 30 Jede Auswertung der Datenbank, die zu den Ergebnissen der Studie beiträgt, muß folgende Angaben enthalten: 30.1 Mit welchem Programm wurde die Auswertung durchgeführt? 30.2 Welche Version der Datenbank lag der Auswertung zugrunde? 30.3 Welche Patienten wurden von der Auswertung ausgeschlossen? 31 Die in diesen Regeln genannten Unterlagen werden einschließlich von Kopien der Datenträger nach Abschluß der Studie für 15 Jahre aufbewahrt. Diese Frist gilt ab dem Ende der Patientenrekrutierung. Scheidet der Studienleiter nach Ende der Studie aus der Med. Univ. Klinik aus, so wird eine schriftliche Vereinbarung über den Verbleib der Studienunterlagen zwischen dem Studienleiter und dem Direktor der Klinik getroffen. Anlagen: Informationsblatt zu Adverse Events und Serious Adverse Events
8 Med. Univ. Klinik Bonn, Regeln zur Dokumentation klinischer Studien, Seite 8 Informationsblatt zu Adverse Events und Serious Adverse Events Was ist ein Adverse Event (AE)? Nach den Regeln zur Ordnungsgemäßen Durchführung klinischer Studien wird als AE jedes unerwünschte klinische Ereignis verstanden, das einen Patienten während einer klinischen Studie betrifft, ungeachtet der Kausalität. Ereignisse, wie unerwünschte Reaktionen auf die gegebenen Medikamente, Krankheiten, die während der Studie auftreten oder sich während der Studie verschlechtern, müssen aufgezeichnet werden. Dazu gehört auch jede Veränderung von Allgemeinzustand oder Laborwerten eines Patienten, die eine Gefährdung von Gesundheit oder Wohlbefinden des Patienten bedeutet oder bedeuten könnte. Was ist ein Serious Adverse Event (SAE)? Jedes Ereignis, das die kurzfristige oder dauernde Gefährdung der Gesundheit des Patienten zur Folge hat, ungeachtet der Kausalität. Ein SAE ist jedes Ereignis, das zum Tode führt (während der Studie oder bis zu 4 Wochen nach Studienende) lebensbedrohlich ist zu einer anhaltenden oder signifikanten Behinderung/Beeinträchtigung führt zu einer Klinikeinweisung führt (> 24 Stunden) oder einen bestehenden Klinikaufenthalt verlängert eine angeborene Anomalie oder ein Geburtsfehler ist (bei Nachkommen von Patienten) Krebs ist Folge einer Überdosierung (versehentlich oder absichtlich) ist Andere bedeutsame medizinische Ereignisse, die möglicherweise nicht zum Tod führen, nicht lebensbedrohlich sind oder keinen Klinikaufenthalt erforderlich machen, können als schwerwiegend angesehen werden, wenn sie den Patienten gefährden und eine medizinische oder chirurgische Intervention erforderlich machen können (z.b. allergische Bronchospasmen, Blutdyskrasien, Krämpfe oder Fieberanfälle) Ausnahmen: erwartete oder bekannte Progression der Grunderkrankung ohne grundlegende Veränderung der Symptomatik ( = nur AE) oder aus der Fachinformation bekannte Zytostatikaeffekte z.b. Neutropenie ( = nur AE) Was tun bei Serious Adverse Events? - innerhalb von 24 Stunden: Studienleitung informieren (SAE Formular ausfüllen und per FAX schicken, FAX-Nr.: 0228/ ) - Ethikkommission informieren (nur bei wahrscheinlichem oder sicherem Zusammenhang)
9 Med. Univ. Klinik Bonn, Regeln zur Dokumentation klinischer Studien, Seite 9 - Probandenversicherung informieren (nur bei wahrscheinlichem oder sicherem Zusammenhang)
IHR PATIENTENDOSSIER IHRE RECHTE
 IHR PATIENTENDOSSIER IHRE RECHTE Im Spital, in der Klinik bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer informiert werden darf Information Patientendossier
IHR PATIENTENDOSSIER IHRE RECHTE Im Spital, in der Klinik bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer informiert werden darf Information Patientendossier
Monitoring. Lucia Kacina. CTU Bern
 Monitoring Lucia Kacina CTU Bern Themen Einverständniserklärung Protokoll & Dokumentation (e)crf-einträge: Dos & Don ts Monitoringvisiten: Teilnehmer & Ablauf Monitoring: Aufgaben des Zentrums Monitoring
Monitoring Lucia Kacina CTU Bern Themen Einverständniserklärung Protokoll & Dokumentation (e)crf-einträge: Dos & Don ts Monitoringvisiten: Teilnehmer & Ablauf Monitoring: Aufgaben des Zentrums Monitoring
Betroffenes Produkt: PRI Femureinschlägerkopf, 00-5901-032-00 (vollständige Liste der betroffenen Chargen siehe Anhang 1)
 22. Mai 2015 An: Betrifft: Risikomanager und Chirurgen DRINGENDER CHARGENSPEZIFISCHER RÜCKRUF EINES MEDIZINPRODUKTES Betroffenes Produkt: PRI Femureinschlägerkopf, 00-5901-032-00 (vollständige Liste der
22. Mai 2015 An: Betrifft: Risikomanager und Chirurgen DRINGENDER CHARGENSPEZIFISCHER RÜCKRUF EINES MEDIZINPRODUKTES Betroffenes Produkt: PRI Femureinschlägerkopf, 00-5901-032-00 (vollständige Liste der
Hinweis zur Ergänzung im Fall schwerer Erkrankung. Anpassung der PATIENTENVERFÜGUNG für den Fall schwerer Krankheit
 40 Hinweis zur Ergänzung im Fall schwerer Erkrankung Liegt bereits eine schwere Erkrankung vor, bedarf es einer hieran angepassten Patientenverfügung. Diese kann nur in engem Zusammenwirken mit dem behandelnden
40 Hinweis zur Ergänzung im Fall schwerer Erkrankung Liegt bereits eine schwere Erkrankung vor, bedarf es einer hieran angepassten Patientenverfügung. Diese kann nur in engem Zusammenwirken mit dem behandelnden
Ihr Patientendossier. Ihre Rechte
 Ihr Patientendossier Ihre Rechte Im Spital bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer auch informiert werden darf Auskunftsrecht und Informationsweitergabe
Ihr Patientendossier Ihre Rechte Im Spital bestimmen Sie, wie Sie über Ihre Krankheit und deren Behandlung informiert werden wollen und wer auch informiert werden darf Auskunftsrecht und Informationsweitergabe
Codex Newsletter. Allgemeines. Codex Newsletter
 Newsletter Newsletter Dezember 05 Seite 1 Allgemeines Newsletter Mit diesem Rundschreiben (Newsletter) wollen wir Sie in ca. zweimonatigen Abständen per Mail über Neuerungen in unseren Programmen informieren.
Newsletter Newsletter Dezember 05 Seite 1 Allgemeines Newsletter Mit diesem Rundschreiben (Newsletter) wollen wir Sie in ca. zweimonatigen Abständen per Mail über Neuerungen in unseren Programmen informieren.
Eine doppelte bzw. mehrfache Erfassung eines Kunden ist unbedingt zu vermeiden.
 Arbeitsanweisungen 1 Prüfung und Erfassung eines Kunden Für die langfristige Kundenbindung sollen möglichst alle Kunden in der Kundenverwaltung gespeichert werden. Termine im Kalender können nur gespeichert
Arbeitsanweisungen 1 Prüfung und Erfassung eines Kunden Für die langfristige Kundenbindung sollen möglichst alle Kunden in der Kundenverwaltung gespeichert werden. Termine im Kalender können nur gespeichert
Für die MitarbeiterInnen kann das auch eine Verbesserung ihrer Arbeitsbedingungen
 Direkte Beteiligung der Beschäftigten 65 Für die MitarbeiterInnen kann das auch eine Verbesserung ihrer Arbeitsbedingungen bedeuten. 3.5 Direkte Beteiligung der Beschäftigten Einzelne Vereinbarungen führen
Direkte Beteiligung der Beschäftigten 65 Für die MitarbeiterInnen kann das auch eine Verbesserung ihrer Arbeitsbedingungen bedeuten. 3.5 Direkte Beteiligung der Beschäftigten Einzelne Vereinbarungen führen
Datenübernahme von HKO 5.9 zur. Advolux Kanzleisoftware
 Datenübernahme von HKO 5.9 zur Advolux Kanzleisoftware Die Datenübernahme (DÜ) von HKO 5.9 zu Advolux Kanzleisoftware ist aufgrund der von Update zu Update veränderten Datenbank (DB)-Strukturen in HKO
Datenübernahme von HKO 5.9 zur Advolux Kanzleisoftware Die Datenübernahme (DÜ) von HKO 5.9 zu Advolux Kanzleisoftware ist aufgrund der von Update zu Update veränderten Datenbank (DB)-Strukturen in HKO
Gemeinsame Ausführungsordnung zum Madrider Abkommen 1 über die internationale Registrierung von Marken und zum Protokoll 2 zu diesem Abkommen
 BGBl. III - Ausgegeben am 9. März 2015 - Nr. 32 1 von 7 (Übersetzung) Gemeinsame Ausführungsordnung zum Madrider Abkommen 1 über die internationale Registrierung von Marken und zum Protokoll 2 zu diesem
BGBl. III - Ausgegeben am 9. März 2015 - Nr. 32 1 von 7 (Übersetzung) Gemeinsame Ausführungsordnung zum Madrider Abkommen 1 über die internationale Registrierung von Marken und zum Protokoll 2 zu diesem
DR. MARC CHRISTOPH BAUMGART
 DR. MARC CHRISTOPH BAUMGART RECHTSANWALT FACHANWALT FÜR MEDIZINRECHT RA Dr. Baumgart, Meierottostraße 7, 10719 Berlin Meierottostraße 7 10719 Berlin Telefon: 030 / 88 62 49 00 Telefax: 030 / 88 62 49 02
DR. MARC CHRISTOPH BAUMGART RECHTSANWALT FACHANWALT FÜR MEDIZINRECHT RA Dr. Baumgart, Meierottostraße 7, 10719 Berlin Meierottostraße 7 10719 Berlin Telefon: 030 / 88 62 49 00 Telefax: 030 / 88 62 49 02
SEPA Lastschriften. Ergänzung zur Dokumentation vom 27.01.2014. Workshop Software GmbH Siemensstr. 21 47533 Kleve 02821 / 731 20 02821 / 731 299
 SEPA Lastschriften Ergänzung zur Dokumentation vom 27.01.2014 Workshop Software GmbH Siemensstr. 21 47533 Kleve 02821 / 731 20 02821 / 731 299 www.workshop-software.de Verfasser: SK info@workshop-software.de
SEPA Lastschriften Ergänzung zur Dokumentation vom 27.01.2014 Workshop Software GmbH Siemensstr. 21 47533 Kleve 02821 / 731 20 02821 / 731 299 www.workshop-software.de Verfasser: SK info@workshop-software.de
Inhaltsübersicht Produktinformationsblatt zur Jahres-Reiserücktritts-Versicherung der Europäische Reiseversicherung AG
 Inhaltsübersicht Produktinformationsblatt zur Jahres-Reiserücktritts-Versicherung der Europäische Reiseversicherung AG 1. Produktinformationsblatt zur Jahres-Reiserücktritts-Versicherung mit Selbstbeteiligung
Inhaltsübersicht Produktinformationsblatt zur Jahres-Reiserücktritts-Versicherung der Europäische Reiseversicherung AG 1. Produktinformationsblatt zur Jahres-Reiserücktritts-Versicherung mit Selbstbeteiligung
Evaluation eines stichprobenartigen Monitorings bei Therapieoptimierungsstudien Ulrike Zettelmeyer
 internet: www.lymphome.de email: lymphome@medizin.uni-koeln.de Evaluation eines stichprobenartigen Monitorings bei Therapieoptimierungsstudien Ulrike Zettelmeyer Gliederung Deutsche Hodgkin Studiengruppe
internet: www.lymphome.de email: lymphome@medizin.uni-koeln.de Evaluation eines stichprobenartigen Monitorings bei Therapieoptimierungsstudien Ulrike Zettelmeyer Gliederung Deutsche Hodgkin Studiengruppe
CoCStom. Inhalt. 1. Monitoring und Query-Prozess. 2. SAE-Meldeweg. 3. Vorstellung des Investigator Site File (ISF) 21./22.11.
 Prospective randomized multicentre investigator initiated study: Randomised trial comparing completeness of adjuvant chemotherapy after early versus late diverting stoma closure in low anterior resection
Prospective randomized multicentre investigator initiated study: Randomised trial comparing completeness of adjuvant chemotherapy after early versus late diverting stoma closure in low anterior resection
Auftrag zum Fondswechsel
 Lebensversicherung von 1871 a.g. München Postfach 80326 München Auftrag zum Fondswechsel Versicherungsnummer Versicherungsnehmer Änderung zum: Bei fehlender Eintragung, findet die Änderung für den Switch
Lebensversicherung von 1871 a.g. München Postfach 80326 München Auftrag zum Fondswechsel Versicherungsnummer Versicherungsnehmer Änderung zum: Bei fehlender Eintragung, findet die Änderung für den Switch
Dokumentation für die software für zahnärzte der procedia GmbH Onlinedokumentation
 Dokumentation für die software für zahnärzte der procedia GmbH Onlinedokumentation (Bei Abweichungen, die bspw. durch technischen Fortschritt entstehen können, ziehen Sie bitte immer das aktuelle Handbuch
Dokumentation für die software für zahnärzte der procedia GmbH Onlinedokumentation (Bei Abweichungen, die bspw. durch technischen Fortschritt entstehen können, ziehen Sie bitte immer das aktuelle Handbuch
Sie haben das Recht, binnen vierzehn Tagen ohne Angabe von Gründen diesen Vertrag zu widerrufen.
 Widerrufsbelehrung Nutzt der Kunde die Leistungen als Verbraucher und hat seinen Auftrag unter Nutzung von sog. Fernkommunikationsmitteln (z. B. Telefon, Telefax, E-Mail, Online-Web-Formular) übermittelt,
Widerrufsbelehrung Nutzt der Kunde die Leistungen als Verbraucher und hat seinen Auftrag unter Nutzung von sog. Fernkommunikationsmitteln (z. B. Telefon, Telefax, E-Mail, Online-Web-Formular) übermittelt,
Dok.-Nr.: Seite 1 von 6
 Logo Apotheke Planung, Durchführung und Dokumentation von QM-Audits Standardarbeitsanweisung (SOP) Standort des Originals: Dok.-Nr.: Seite 1 von 6 Nummer der vorliegenden Verfaßt durch Freigabe durch Apothekenleitung
Logo Apotheke Planung, Durchführung und Dokumentation von QM-Audits Standardarbeitsanweisung (SOP) Standort des Originals: Dok.-Nr.: Seite 1 von 6 Nummer der vorliegenden Verfaßt durch Freigabe durch Apothekenleitung
Anwenderdokumentation Prüfung nach dem Heilmittelkatalog
 Ausgabe August 2008 Anwenderdokumentation Prüfung nach dem Heilmittelkatalog 1 Einleitung... 2 2 Stammdateneinstellungen... 3 2.1 Zuordnung der Heilmittel... 3 3 Prüfung einer Verordnung... 7 3.1 Vorgehensweise
Ausgabe August 2008 Anwenderdokumentation Prüfung nach dem Heilmittelkatalog 1 Einleitung... 2 2 Stammdateneinstellungen... 3 2.1 Zuordnung der Heilmittel... 3 3 Prüfung einer Verordnung... 7 3.1 Vorgehensweise
Kapitel I: Registrierung im Portal
 Kapitel I: Registrierung im Portal Um zu unserem Portal zu gelangen, rufen Sie bitte die folgende Internetseite auf: www.arag-forderungsmanagement.de Bei Ihrem ersten Besuch des ARAG Portals ist es notwendig,
Kapitel I: Registrierung im Portal Um zu unserem Portal zu gelangen, rufen Sie bitte die folgende Internetseite auf: www.arag-forderungsmanagement.de Bei Ihrem ersten Besuch des ARAG Portals ist es notwendig,
ARAkoll 2013 Dokumentation. Datum: 21.11.2012
 ARAkoll 2013 Dokumentation Datum: 21.11.2012 INHALT Allgemeines... 3 Funktionsübersicht... 3 Allgemeine Funktionen... 3 ARAmatic Symbolleiste... 3 Monatsprotokoll erzeugen... 4 Jahresprotokoll erzeugen
ARAkoll 2013 Dokumentation Datum: 21.11.2012 INHALT Allgemeines... 3 Funktionsübersicht... 3 Allgemeine Funktionen... 3 ARAmatic Symbolleiste... 3 Monatsprotokoll erzeugen... 4 Jahresprotokoll erzeugen
Häufig wiederkehrende Fragen zur mündlichen Ergänzungsprüfung im Einzelnen:
 Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Mündliche Ergänzungsprüfung bei gewerblich-technischen und kaufmännischen Ausbildungsordnungen bis zum 31.12.2006 und für alle Ausbildungsordnungen ab 01.01.2007 Am 13. Dezember 2006 verabschiedete der
Vereinbarung über privatzahnärztliche Leistungen bei der kieferorthopädischen Behandlung
 Vereinbarung über privatzahnärztliche Leistungen bei der kieferorthopädischen Behandlung Zwischen Zahlungspflichtige/-r und Zahnärztin I Zahnarzt für Patient (falls abweichend vom Zahlungspflichtigen)
Vereinbarung über privatzahnärztliche Leistungen bei der kieferorthopädischen Behandlung Zwischen Zahlungspflichtige/-r und Zahnärztin I Zahnarzt für Patient (falls abweichend vom Zahlungspflichtigen)
4. Sie müssen jede Vorschlagsliste innerhalb von zwei Tagen nach Eingang auf Gültigkeit überprüfen ( 7 Abs. 2 WO).
 Wird eine Vorschlagsliste eingereicht, gehen Sie wie folgt vor: 1. Stempeln mit Eingangsdatum. 2. Bestätigen Sie den Eingang der Vorschlagsliste sofort (Muster-Formular 120b). 3. Wenn die Liste kein Kennwort
Wird eine Vorschlagsliste eingereicht, gehen Sie wie folgt vor: 1. Stempeln mit Eingangsdatum. 2. Bestätigen Sie den Eingang der Vorschlagsliste sofort (Muster-Formular 120b). 3. Wenn die Liste kein Kennwort
Das Persönliche Budget in verständlicher Sprache
 Das Persönliche Budget in verständlicher Sprache Das Persönliche Budget mehr Selbstbestimmung, mehr Selbstständigkeit, mehr Selbstbewusstsein! Dieser Text soll den behinderten Menschen in Westfalen-Lippe,
Das Persönliche Budget in verständlicher Sprache Das Persönliche Budget mehr Selbstbestimmung, mehr Selbstständigkeit, mehr Selbstbewusstsein! Dieser Text soll den behinderten Menschen in Westfalen-Lippe,
Forschungs- und Entwicklungsprojekt Erstversorgung von Patienten mit Schädel-Hirn-Trauma Zwischenbericht 2010
 An das Bundesministerium für Gesundheit, Familie und Jugend Sektion IV/1 Radetzkystrasse 2 A 1030 WIEN Wien, 16. Nov. 2010 Forschungs- und Entwicklungsprojekt Erstversorgung von Patienten mit Schädel-Hirn-Trauma
An das Bundesministerium für Gesundheit, Familie und Jugend Sektion IV/1 Radetzkystrasse 2 A 1030 WIEN Wien, 16. Nov. 2010 Forschungs- und Entwicklungsprojekt Erstversorgung von Patienten mit Schädel-Hirn-Trauma
GVService - Der GerichtsVollzieherService. Anleitung für das Onlinebanking mit dem GVService
 GVService - Der GerichtsVollzieherService Anleitung für das Onlinebanking mit dem GVService Hausanschrift Baqué & Lauter GmbH Falkenweg 3 53881 Euskirchen Telefon (Sammelleitung) 02255 / 950-300 Telefax
GVService - Der GerichtsVollzieherService Anleitung für das Onlinebanking mit dem GVService Hausanschrift Baqué & Lauter GmbH Falkenweg 3 53881 Euskirchen Telefon (Sammelleitung) 02255 / 950-300 Telefax
So nutzen Sie VOICEMEETING. Vereinbaren Sie mit allen Konferenzteilnehmern den genauen Zeitpunkt, zu dem die Konferenz stattfinden soll.
 Schnellstart / Kompakt Seite 1 Während der Konferenz So nutzen Sie VOICEMEETING Vereinbaren Sie mit allen Konferenzteilnehmern den genauen Zeitpunkt, zu dem die Konferenz stattfinden soll. Ausserdem teilen
Schnellstart / Kompakt Seite 1 Während der Konferenz So nutzen Sie VOICEMEETING Vereinbaren Sie mit allen Konferenzteilnehmern den genauen Zeitpunkt, zu dem die Konferenz stattfinden soll. Ausserdem teilen
Darlehensvertrag zwischen der Energie-Genossenschaft Darmstadt eg im Folgenden Darlehensnehmerin genannt, und. Name. Anschrift
 Darlehensvertrag zwischen der Energie-Genossenschaft Darmstadt eg im Folgenden Darlehensnehmerin genannt, und Name Anschrift 1 Zweck Zweck des Darlehens ist die Finanzierung von Photovoltaikanlagen in
Darlehensvertrag zwischen der Energie-Genossenschaft Darmstadt eg im Folgenden Darlehensnehmerin genannt, und Name Anschrift 1 Zweck Zweck des Darlehens ist die Finanzierung von Photovoltaikanlagen in
Datenschutz im Alters- und Pflegeheim
 Urs Belser, Fürsprecher Safe+Legal, AG für Datenschutz und Management-Consulting Schwarztorstrasse 87, 3007 Bern Tel. 031 382 74 74 E-Mail urs.belser@safelegal.ch Datenschutz im Alters- und Pflegeheim
Urs Belser, Fürsprecher Safe+Legal, AG für Datenschutz und Management-Consulting Schwarztorstrasse 87, 3007 Bern Tel. 031 382 74 74 E-Mail urs.belser@safelegal.ch Datenschutz im Alters- und Pflegeheim
Wir empfehlen Ihnen eine zeitnahe Bewerbung, da in jedem Halbjahr nur eine limitierte Anzahl an Bündnissen bewilligt werden können.
 Ich bin ein LeseHeld Bewerbungsformular zur Teilnahme am Leselernförderprojekt des Borromäusverein e.v. im Rahmen des Programms Kultur macht stark. Bündnisse für Bildung des Bundesministeriums für Bildung
Ich bin ein LeseHeld Bewerbungsformular zur Teilnahme am Leselernförderprojekt des Borromäusverein e.v. im Rahmen des Programms Kultur macht stark. Bündnisse für Bildung des Bundesministeriums für Bildung
Name Funktion Datum Unterschrift
 Bericht über die Kassenprüfung der Teilgliederung Kreisverband Mittelhaardt der Piratenpartei Deutschland für das laufende Geschäftsjahr 2010 (12.12.2009 01.11.2010) Name Funktion Datum Unterschrift Markus
Bericht über die Kassenprüfung der Teilgliederung Kreisverband Mittelhaardt der Piratenpartei Deutschland für das laufende Geschäftsjahr 2010 (12.12.2009 01.11.2010) Name Funktion Datum Unterschrift Markus
Ust.-VA ab 01.01.2013. Release 1.0.0
 Ust.-VA ab 01.01.2013 Release 1.0.0 2012 myfactory International GmbH Seite 1 von 9 Ohne ausdrückliche schriftliche Erlaubnis dürfen weder das Handbuch noch Auszüge daraus mit mechanischen oder elektronischen
Ust.-VA ab 01.01.2013 Release 1.0.0 2012 myfactory International GmbH Seite 1 von 9 Ohne ausdrückliche schriftliche Erlaubnis dürfen weder das Handbuch noch Auszüge daraus mit mechanischen oder elektronischen
Widerrufsbelehrung der Free-Linked GmbH. Stand: Juni 2014
 Widerrufsbelehrung der Stand: Juni 2014 www.free-linked.de www.buddy-watcher.de Inhaltsverzeichnis Widerrufsbelehrung Verträge für die Lieferung von Waren... 3 Muster-Widerrufsformular... 5 2 Widerrufsbelehrung
Widerrufsbelehrung der Stand: Juni 2014 www.free-linked.de www.buddy-watcher.de Inhaltsverzeichnis Widerrufsbelehrung Verträge für die Lieferung von Waren... 3 Muster-Widerrufsformular... 5 2 Widerrufsbelehrung
GOST - NORMEN IN ÜBERSETZUNG RUSSIAN STANDARDS IN TRANSLATION
 GOST - NORMEN IN ÜBERSETZUNG RUSSIAN STANDARDS IN TRANSLATION Zusammengestellt und herausgegeben von Tatiana Czepurnyi in Zusammenarbeit mit Monika Lemke VORWORT In der vorliegenden Liste sind Übersetzungen
GOST - NORMEN IN ÜBERSETZUNG RUSSIAN STANDARDS IN TRANSLATION Zusammengestellt und herausgegeben von Tatiana Czepurnyi in Zusammenarbeit mit Monika Lemke VORWORT In der vorliegenden Liste sind Übersetzungen
Patientenleitfaden für das Gespräch mit dem Arzt. Liebe Patientin, lieber Patient!
 Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
Patientenleitfaden für das Gespräch mit dem Arzt Liebe Patientin, lieber Patient! Je besser Sie sich auf das Gespräch mit Ihrem Arzt vorbereiten, desto leichter wird es für sie/ihn sein, eine Diagnose
DAS GRÜNE REZEPT. Für eine sichere Medikation mit rezeptfreien Arzneimitteln
 DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
DAS GRÜNE REZEPT Für eine sichere Medikation mit rezeptfreien Arzneimitteln Was ist das Grüne Rezept? Obwohl das Grüne Rezept schon seit Jahren in Arztpraxen verwendet wird, ist es vielen Patienten und
Verfahrensordnung für die Durchführung der Compliance-Zertifizierung der ICG
 Verfahrensordnung für die Durchführung der Compliance-Zertifizierung der ICG 1 Allgemeines (Stand 17.04.2015) (1) Der Vorstand führt die Geschäfte der ICG nach Maßgabe der Gesetze, der Satzung und der
Verfahrensordnung für die Durchführung der Compliance-Zertifizierung der ICG 1 Allgemeines (Stand 17.04.2015) (1) Der Vorstand führt die Geschäfte der ICG nach Maßgabe der Gesetze, der Satzung und der
Verschreibungsfreie Arzneimittel wieder in der Erstattung
 Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
Satzungsleistungen Verschreibungsfreie Arzneimittel wieder in der Erstattung Was sind Satzungsleistungen? Der Rahmen für die Leistungen der gesetzlichen Krankenversicherung wird im Fünften Sozialgesetzbuch
tegos Support 1 Kontakt... 2 2 tegos Support Ticketing System... 2 3 Support Knowledge Database... 6 4 Fehlerklassen... 6 5 Fehlermanagement...
 Seite 1 von 9 tegos Support Inhalt 1 Kontakt... 2 2 tegos Support Ticketing System... 2 3 Support Knowledge Database... 6 4 Fehlerklassen... 6 5 Fehlermanagement... 7 6 Servicelevel... 8 7 Eskalation...
Seite 1 von 9 tegos Support Inhalt 1 Kontakt... 2 2 tegos Support Ticketing System... 2 3 Support Knowledge Database... 6 4 Fehlerklassen... 6 5 Fehlermanagement... 7 6 Servicelevel... 8 7 Eskalation...
How to do? Projekte - Zeiterfassung
 How to do? Projekte - Zeiterfassung Stand: Version 4.0.1, 18.03.2009 1. EINLEITUNG...3 2. PROJEKTE UND STAMMDATEN...4 2.1 Projekte... 4 2.2 Projektmitarbeiter... 5 2.3 Tätigkeiten... 6 2.4 Unterprojekte...
How to do? Projekte - Zeiterfassung Stand: Version 4.0.1, 18.03.2009 1. EINLEITUNG...3 2. PROJEKTE UND STAMMDATEN...4 2.1 Projekte... 4 2.2 Projektmitarbeiter... 5 2.3 Tätigkeiten... 6 2.4 Unterprojekte...
DRINGEND SICHERHEITSMITTEILUNG Rückruf bei HeartStart HS1
 Sicherheitsmitteilung Emergency Care and Resuscitation -1/2- FSN86100130 7. März 2014 DRINGEND SICHERHEITSMITTEILUNG Rückruf bei HeartStart HS1 Sehr geehrte Kundin, sehr geehrter Kunde, Verunreinigung
Sicherheitsmitteilung Emergency Care and Resuscitation -1/2- FSN86100130 7. März 2014 DRINGEND SICHERHEITSMITTEILUNG Rückruf bei HeartStart HS1 Sehr geehrte Kundin, sehr geehrter Kunde, Verunreinigung
AUF LETZTER SEITE DIESER ANLEITUNG!!!
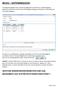 BELEG DATENABGLEICH: Der Beleg-Datenabgleich wird innerhalb des geöffneten Steuerfalls über ELSTER-Belegdaten abgleichen gestartet. Es werden Ihnen alle verfügbaren Belege zum Steuerfall im ersten Bildschirm
BELEG DATENABGLEICH: Der Beleg-Datenabgleich wird innerhalb des geöffneten Steuerfalls über ELSTER-Belegdaten abgleichen gestartet. Es werden Ihnen alle verfügbaren Belege zum Steuerfall im ersten Bildschirm
Handlungshilfe Medikamentengabe im Kindergarten
 Handlungshilfe Medikamentengabe im Kindergarten Stand: November 2010 2 Medikamentengabe im Kindergarten 1. Einleitung In Kindergärten kommt es immer wieder zu Diskussionen über die Frage, ob und wie ErzieherInnen
Handlungshilfe Medikamentengabe im Kindergarten Stand: November 2010 2 Medikamentengabe im Kindergarten 1. Einleitung In Kindergärten kommt es immer wieder zu Diskussionen über die Frage, ob und wie ErzieherInnen
Abweichungen. Anforderungen / Zitate aus den Rechtsvorschriften
 Abweichungen Anforderungen / Zitate aus den Rechtsvorschriften AMWHV [...] Alle Abweichungen im Prozess und von der Festlegung der Spezifikation sind zu dokumentieren und gründlich zu untersuchen. [...]
Abweichungen Anforderungen / Zitate aus den Rechtsvorschriften AMWHV [...] Alle Abweichungen im Prozess und von der Festlegung der Spezifikation sind zu dokumentieren und gründlich zu untersuchen. [...]
Beschreibung E-Mail Regeln z.b. Abwesenheitsmeldung und Weiterleitung
 Outlook Weiterleitungen & Abwesenheitsmeldungen Seite 1 von 6 Beschreibung E-Mail Regeln z.b. Abwesenheitsmeldung und Weiterleitung Erstellt: Quelle: 3.12.09/MM \\rsiag-s3aad\install\vnc\email Weiterleitung
Outlook Weiterleitungen & Abwesenheitsmeldungen Seite 1 von 6 Beschreibung E-Mail Regeln z.b. Abwesenheitsmeldung und Weiterleitung Erstellt: Quelle: 3.12.09/MM \\rsiag-s3aad\install\vnc\email Weiterleitung
FAKULTÄT FÜR HUMAN- UND SOZIALWISSENSCHAFTEN. Projektplan
 Projektplan zur Einreichung bei der Ethikkommission der Fakultät für Human und Sozialwissenschaften der Technischen Universität Chemnitz PROJEKTBEZEICHNUNG Datum des Projektplans: Professur: Studienleitung:
Projektplan zur Einreichung bei der Ethikkommission der Fakultät für Human und Sozialwissenschaften der Technischen Universität Chemnitz PROJEKTBEZEICHNUNG Datum des Projektplans: Professur: Studienleitung:
Sehr geehrter Herr Pfarrer, sehr geehrte pastorale Mitarbeiterin, sehr geehrter pastoraler Mitarbeiter!
 Sehr geehrter Herr Pfarrer, sehr geehrte pastorale Mitarbeiterin, sehr geehrter pastoraler Mitarbeiter! Wir möchten Sie an Ihr jährliches Mitarbeitergespräch erinnern. Es dient dazu, das Betriebs- und
Sehr geehrter Herr Pfarrer, sehr geehrte pastorale Mitarbeiterin, sehr geehrter pastoraler Mitarbeiter! Wir möchten Sie an Ihr jährliches Mitarbeitergespräch erinnern. Es dient dazu, das Betriebs- und
AKH-DER-P-5.3. Gültig ab:01.10.2008 Version:1.0.1 Seite 1 von 5
 Gültig ab:01.10.2008 Version:1.0.1 Seite 1 von 5 1. Ziel und Geltungsbereich Diese Prozessbeschreibung regelt die Vorgangsweise zur Beseitigung der Ursachen von bereits aufgetretenen Fehlern bzw. Mängeln
Gültig ab:01.10.2008 Version:1.0.1 Seite 1 von 5 1. Ziel und Geltungsbereich Diese Prozessbeschreibung regelt die Vorgangsweise zur Beseitigung der Ursachen von bereits aufgetretenen Fehlern bzw. Mängeln
Richtlinie. des Gemeinsamen Bundesausschusses. zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie )
 Richtlinie des Gemeinsamen Bundesausschusses zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie ) in der Fassung vom 22. Januar 2004 veröffentlicht im Bundesanzeiger
Richtlinie des Gemeinsamen Bundesausschusses zur Umsetzung der Regelungen in 62 für schwerwiegend chronisch Erkrankte ( Chroniker-Richtlinie ) in der Fassung vom 22. Januar 2004 veröffentlicht im Bundesanzeiger
Gut essen als Dialysepatient Grundlagen der Ernährung. Claire Drube Dr. Sebastian Drube
 Gut essen als Dialysepatient Grundlagen der Ernährung Claire Drube Dr. Sebastian Drube Liebe Leserinnen und Leser, Nierenerkrankungen bringen Veränderungen mit sich, die in unterschiedlichem Maße praktisch
Gut essen als Dialysepatient Grundlagen der Ernährung Claire Drube Dr. Sebastian Drube Liebe Leserinnen und Leser, Nierenerkrankungen bringen Veränderungen mit sich, die in unterschiedlichem Maße praktisch
Lexware eservice personal - Nutzung ab Januar 2014
 Lexware eservice personal - Nutzung ab Januar 2014 Sie möchten sich von den vielen Vorteilen überzeugen und Lexware eservice personal ab 2014 nutzen. Wie können Sie sich registrieren und welche Funktionen
Lexware eservice personal - Nutzung ab Januar 2014 Sie möchten sich von den vielen Vorteilen überzeugen und Lexware eservice personal ab 2014 nutzen. Wie können Sie sich registrieren und welche Funktionen
Zimmertypen. Zimmertypen anlegen
 Zimmertypen anlegen Hier legen Sie Ihre Zimmer an, damit sie auf der Homepage dargestellt werden und online buchbar gemacht werden können. Wobei wir ausdrücklich darauf hinweisen möchten, dass es ganz
Zimmertypen anlegen Hier legen Sie Ihre Zimmer an, damit sie auf der Homepage dargestellt werden und online buchbar gemacht werden können. Wobei wir ausdrücklich darauf hinweisen möchten, dass es ganz
CHECKLISTE für KRANKENANSTALTEN
 CHECKLISTE für KRANKENANSTALTEN 12 Schritte zur nutritionday Teilnahme (nd.h) 6 Monate bis 1 Woche vor nutritionday 1 2 3 4 5 6 7 8 9 10 11 12 Registrieren und Kodes bestellen Beachten Sie nationale Richtlinien
CHECKLISTE für KRANKENANSTALTEN 12 Schritte zur nutritionday Teilnahme (nd.h) 6 Monate bis 1 Woche vor nutritionday 1 2 3 4 5 6 7 8 9 10 11 12 Registrieren und Kodes bestellen Beachten Sie nationale Richtlinien
Maintenance & Re-Zertifizierung
 Zertifizierung nach Technischen Richtlinien Maintenance & Re-Zertifizierung Version 1.2 vom 15.06.2009 Bundesamt für Sicherheit in der Informationstechnik Postfach 20 03 63 53133 Bonn Tel.: +49 22899 9582-0
Zertifizierung nach Technischen Richtlinien Maintenance & Re-Zertifizierung Version 1.2 vom 15.06.2009 Bundesamt für Sicherheit in der Informationstechnik Postfach 20 03 63 53133 Bonn Tel.: +49 22899 9582-0
Antrag für ein Schlichtungs-Verfahren
 Eingangsstempel Antrag für ein Schlichtungs-Verfahren Dieser Antrag ist in Leichter Sprache geschrieben. Das sieht man auch am gelben, runden Zeichen. Im Text finden Sie immer wieder unterstrichene Wörter.
Eingangsstempel Antrag für ein Schlichtungs-Verfahren Dieser Antrag ist in Leichter Sprache geschrieben. Das sieht man auch am gelben, runden Zeichen. Im Text finden Sie immer wieder unterstrichene Wörter.
Muster. Ort, Datum Unterschrift Patientin / Patient / Betreuungsperson Ort, Datum Stempel / Unterschrift des Klinikmitarbeiters
 Einwilligungserklärung zur Teilnahme am Deutschen Aortenklappenregister Exemplar für die Registerstelle - Seite 1 Exemplar für die Registerstelle Kanzlerstraße 4 40472 Düsseldorf RegisterID 201601301 Ich
Einwilligungserklärung zur Teilnahme am Deutschen Aortenklappenregister Exemplar für die Registerstelle - Seite 1 Exemplar für die Registerstelle Kanzlerstraße 4 40472 Düsseldorf RegisterID 201601301 Ich
Ihre Rechte und Vorteile bei der CH- Versichertenkarte. Information zur Versichertenkarte aus Sicht der Patienten
 Ihre Rechte und Vorteile bei der CH- Versichertenkarte Information zur Versichertenkarte aus Sicht der Patienten Sie haben das Recht......dass Ihre Versichertenkarte als Zugangs-Schlüssel zu medizinischen
Ihre Rechte und Vorteile bei der CH- Versichertenkarte Information zur Versichertenkarte aus Sicht der Patienten Sie haben das Recht......dass Ihre Versichertenkarte als Zugangs-Schlüssel zu medizinischen
Nachricht der Kundenbetreuung
 Cisco WebEx: Service-Pack vom [[DATE]] für [[WEBEXURL]] Sehr geehrter Cisco WebEx-Kunde, Cisco WebEx sendet diese Mitteilung an wichtige Geschäftskontakte unter https://[[webexurl]]. Ab Samstag, 1. November
Cisco WebEx: Service-Pack vom [[DATE]] für [[WEBEXURL]] Sehr geehrter Cisco WebEx-Kunde, Cisco WebEx sendet diese Mitteilung an wichtige Geschäftskontakte unter https://[[webexurl]]. Ab Samstag, 1. November
Telekommunikation Ihre Datenschutzrechte im Überblick
 Telekommunikation Ihre Datenschutzrechte im Überblick Inhalt Bestands- und Verkehrsdaten 5 Vertragsschluss 6 Bonitätsabfrage 7 Telefonbuch und Auskunft 8 Rechnung und Einzelverbindungsnachweis 9 Auskunftsrecht
Telekommunikation Ihre Datenschutzrechte im Überblick Inhalt Bestands- und Verkehrsdaten 5 Vertragsschluss 6 Bonitätsabfrage 7 Telefonbuch und Auskunft 8 Rechnung und Einzelverbindungsnachweis 9 Auskunftsrecht
Ihr Mandant möchte einen neuen Gesellschafter aufnehmen. In welcher Höhe wäre eine Vergütung inklusive Tantieme steuerrechtlich zulässig?
 Ihr Mandant möchte einen neuen Gesellschafter aufnehmen. In welcher Höhe wäre eine Vergütung inklusive Tantieme steuerrechtlich zulässig? Oft wirft die Aufnahme neuer Gesellschafter oder auch die Einstellung
Ihr Mandant möchte einen neuen Gesellschafter aufnehmen. In welcher Höhe wäre eine Vergütung inklusive Tantieme steuerrechtlich zulässig? Oft wirft die Aufnahme neuer Gesellschafter oder auch die Einstellung
Verarbeitung der E-Mail-Adressen
 Verarbeitung der E-Mail-Adressen A) Auswertung aus dem Infotyp 0105 - Kommunikation zur Feststellung, welche E-Mail-Adressen gespeichert sind Aufruf über direkte Eingabe der Transaktion (notfalls Transaktionsfenster
Verarbeitung der E-Mail-Adressen A) Auswertung aus dem Infotyp 0105 - Kommunikation zur Feststellung, welche E-Mail-Adressen gespeichert sind Aufruf über direkte Eingabe der Transaktion (notfalls Transaktionsfenster
Zur Bestätigung wird je nach Anmeldung (Benutzer oder Administrator) eine Meldung angezeigt:
 K U R Z A N L E I T U N G D A S R Z L WE B - P O R T A L D E R R Z L N E W S L E T T E R ( I N F O - M A I L ) RZL Software GmbH Riedauer Straße 15 4910 Ried im Innkreis Version: 11. Juni 2012 / mw Bitte
K U R Z A N L E I T U N G D A S R Z L WE B - P O R T A L D E R R Z L N E W S L E T T E R ( I N F O - M A I L ) RZL Software GmbH Riedauer Straße 15 4910 Ried im Innkreis Version: 11. Juni 2012 / mw Bitte
Einrichtung des Cisco VPN Clients (IPSEC) in Windows7
 Einrichtung des Cisco VPN Clients (IPSEC) in Windows7 Diese Verbindung muss einmalig eingerichtet werden und wird benötigt, um den Zugriff vom privaten Rechner oder der Workstation im Home Office über
Einrichtung des Cisco VPN Clients (IPSEC) in Windows7 Diese Verbindung muss einmalig eingerichtet werden und wird benötigt, um den Zugriff vom privaten Rechner oder der Workstation im Home Office über
Lenkung von Dokumenten und Aufzeichnungen. Studienabteilung
 gültig ab: 08.08.2011 Version 1.3 Lenkung von Dokumenten und Aufzeichnungen Studienabteilung Spitalgasse 23 1090 Wien Funktion Name Datum Unterschrift erstellt Stellv. Mag. Julia Feinig- 27.07.2011 Leiterin
gültig ab: 08.08.2011 Version 1.3 Lenkung von Dokumenten und Aufzeichnungen Studienabteilung Spitalgasse 23 1090 Wien Funktion Name Datum Unterschrift erstellt Stellv. Mag. Julia Feinig- 27.07.2011 Leiterin
Einrichten einer Festplatte mit FDISK unter Windows 95/98/98SE/Me
 Einrichten einer Festplatte mit FDISK unter Windows 95/98/98SE/Me Bevor Sie die Platte zum ersten Mal benutzen können, muss sie noch partitioniert und formatiert werden! Vorher zeigt sich die Festplatte
Einrichten einer Festplatte mit FDISK unter Windows 95/98/98SE/Me Bevor Sie die Platte zum ersten Mal benutzen können, muss sie noch partitioniert und formatiert werden! Vorher zeigt sich die Festplatte
Mitarbeiterbefragung als PE- und OE-Instrument
 Mitarbeiterbefragung als PE- und OE-Instrument 1. Was nützt die Mitarbeiterbefragung? Eine Mitarbeiterbefragung hat den Sinn, die Sichtweisen der im Unternehmen tätigen Menschen zu erkennen und für die
Mitarbeiterbefragung als PE- und OE-Instrument 1. Was nützt die Mitarbeiterbefragung? Eine Mitarbeiterbefragung hat den Sinn, die Sichtweisen der im Unternehmen tätigen Menschen zu erkennen und für die
Struktur der Transplantationen in Deutschland in den Jahren 2004 und 2005
 FORSCHUNGSBERICHTE DES INSTITUTS FÜR GESUNDHEITSÖKONOMIE UND KLINI- SCHE EPIDEMIOLOGIE DER UNIVERSITÄT ZU KÖLN STUDIEN ZU GESUNDHEIT, MEDIZIN UND GESELLSCHAFT NR. 10/ 2007 VOM 13.12.2007 *** ISSN 1862-7412
FORSCHUNGSBERICHTE DES INSTITUTS FÜR GESUNDHEITSÖKONOMIE UND KLINI- SCHE EPIDEMIOLOGIE DER UNIVERSITÄT ZU KÖLN STUDIEN ZU GESUNDHEIT, MEDIZIN UND GESELLSCHAFT NR. 10/ 2007 VOM 13.12.2007 *** ISSN 1862-7412
Tutorial. Wie kann ich meinen Kontostand von meinen Tauschpartnern in. übernehmen? Zoe.works - Ihre neue Ladungsträgerverwaltung
 Wie kann ich meinen Kontostand von meinen Tauschpartnern in Tutorial übernehmen? 1. Schritt : Legen Sie ein Startdatum fest Im ersten Schritt legen Sie für Ihr Unternehmen ein Startdatum fest, an dem Sie
Wie kann ich meinen Kontostand von meinen Tauschpartnern in Tutorial übernehmen? 1. Schritt : Legen Sie ein Startdatum fest Im ersten Schritt legen Sie für Ihr Unternehmen ein Startdatum fest, an dem Sie
zum Vertrag zur Integrierten Versorgung von Patienten mit der Diagnose Osteoporose im Rheinland gemäß 3 Abs. 5 Buchst. e
 Der Prozess der Ausschreibung eines Versicherten aus diesem Vertrag kann von zwei Akteuren vorgenommen werden. Zum einen vom Vertragsarzt zum anderen von der Krankenkasse. In beiden Fällen muss eine Mitteilung
Der Prozess der Ausschreibung eines Versicherten aus diesem Vertrag kann von zwei Akteuren vorgenommen werden. Zum einen vom Vertragsarzt zum anderen von der Krankenkasse. In beiden Fällen muss eine Mitteilung
Systemisches Arbeiten
 Blatt 1 Zertifikatsbedingungen Das Weiterbildungsprogramm ", wird vom Institut seit 17 Jahren regelmäßig bundesweit durchgeführt. Es entspricht in Inhalt und Form den Standards der Deutschen Gesellschaft
Blatt 1 Zertifikatsbedingungen Das Weiterbildungsprogramm ", wird vom Institut seit 17 Jahren regelmäßig bundesweit durchgeführt. Es entspricht in Inhalt und Form den Standards der Deutschen Gesellschaft
Einleitende Bemerkungen
 Einleitende Bemerkungen EU-FORMBLATT LENKFREIE TAGE / KONTROLLGERÄT MANUELLER NACHTRAG ENTSCHEIDUNGSHILFE FÜR FAHRPERSONAL VON VERORDNUNGS-FAHRZEUGEN 1 BEI TÄTIGKEITEN IM INNERSTAATLICHEN VERKEHR Zur Frage,
Einleitende Bemerkungen EU-FORMBLATT LENKFREIE TAGE / KONTROLLGERÄT MANUELLER NACHTRAG ENTSCHEIDUNGSHILFE FÜR FAHRPERSONAL VON VERORDNUNGS-FAHRZEUGEN 1 BEI TÄTIGKEITEN IM INNERSTAATLICHEN VERKEHR Zur Frage,
Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt?
 DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
DGSV-Kongress 2009 Wann ist eine Software in Medizinprodukte- Aufbereitungsabteilungen ein Medizinprodukt? Sybille Andrée Betriebswirtin für und Sozialmanagement (FH-SRH) Prokuristin HSD Händschke Software
Urlaubsregel in David
 Urlaubsregel in David Inhaltsverzeichnis KlickDown Beitrag von Tobit...3 Präambel...3 Benachrichtigung externer Absender...3 Erstellen oder Anpassen des Anworttextes...3 Erstellen oder Anpassen der Auto-Reply-Regel...5
Urlaubsregel in David Inhaltsverzeichnis KlickDown Beitrag von Tobit...3 Präambel...3 Benachrichtigung externer Absender...3 Erstellen oder Anpassen des Anworttextes...3 Erstellen oder Anpassen der Auto-Reply-Regel...5
Ein Gesuch erfassen und einreichen
 Eidgenössisches Departement des Innern EDI Bundesamt für Kultur BAK Förderplattform (FPF) - Anleitung Ein Gesuch erfassen und einreichen Seit Mitte September 2014, bietet das BAK für die Eingabe von Gesuchen
Eidgenössisches Departement des Innern EDI Bundesamt für Kultur BAK Förderplattform (FPF) - Anleitung Ein Gesuch erfassen und einreichen Seit Mitte September 2014, bietet das BAK für die Eingabe von Gesuchen
Datenübernahme easyjob 3.0 zu easyjob 4.0
 Datenübernahme easyjob 3.0 zu easyjob 4.0 Einführung...3 Systemanforderung easyjob 4.0...3 Vorgehensweise zur Umstellung zu easyjob 4.0...4 Installation easyjob 4.0 auf dem Server und Arbeitsstationen...4
Datenübernahme easyjob 3.0 zu easyjob 4.0 Einführung...3 Systemanforderung easyjob 4.0...3 Vorgehensweise zur Umstellung zu easyjob 4.0...4 Installation easyjob 4.0 auf dem Server und Arbeitsstationen...4
WAS finde ich WO im Beipackzettel
 WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
WAS finde ich WO im Beipackzettel Sie haben eine Frage zu Ihrem? Meist finden Sie die Antwort im Beipackzettel (offiziell "Gebrauchsinformation" genannt). Der Aufbau der Beipackzettel ist von den Behörden
Die Bundes-Zentrale für politische Bildung stellt sich vor
 Die Bundes-Zentrale für politische Bildung stellt sich vor Die Bundes-Zentrale für politische Bildung stellt sich vor Deutschland ist ein demokratisches Land. Das heißt: Die Menschen in Deutschland können
Die Bundes-Zentrale für politische Bildung stellt sich vor Die Bundes-Zentrale für politische Bildung stellt sich vor Deutschland ist ein demokratisches Land. Das heißt: Die Menschen in Deutschland können
Zypern. Mehrwertsteuererstattungen nach der 13. MwSt-Richtlinie (86/560/EWG)
 Zypern Mehrwertsteuererstattungen nach der 13. MwSt-Richtlinie (86/560/EWG) I. GEGENSEITIGKEITSABKOMMEN Artikel 2 Absatz 2 1. Hat Ihr Land Gegenseitigkeitsabkommen abgeschlossen? Ja, Zypern hat zwei Gegenseitigkeitsabkommen
Zypern Mehrwertsteuererstattungen nach der 13. MwSt-Richtlinie (86/560/EWG) I. GEGENSEITIGKEITSABKOMMEN Artikel 2 Absatz 2 1. Hat Ihr Land Gegenseitigkeitsabkommen abgeschlossen? Ja, Zypern hat zwei Gegenseitigkeitsabkommen
Kommunikationsdaten Spielberechtigungsliste. Speicherpfad/Dokument: 140617_DFBnet_Kommunikationsdaten_Spielberechtigungsliste_Freigabemitteilung_4.
 Freigabemitteilung System: DFBnet Version: R4.96 Kommunikationsdaten Spielberechtigungsliste Speicherpfad/Dokument: 140617_DFBnet_Kommunikationsdaten_Spielberechtigungsliste_Freigabemitteilung_4.96 Erstellt:
Freigabemitteilung System: DFBnet Version: R4.96 Kommunikationsdaten Spielberechtigungsliste Speicherpfad/Dokument: 140617_DFBnet_Kommunikationsdaten_Spielberechtigungsliste_Freigabemitteilung_4.96 Erstellt:
Träger : Kath. Kirchengemeinde St. Laurentius Bretten
 Träger : Kath. Kirchengemeinde St. Laurentius Bretten Wir sind Mitglied im Verband katholischer Tageseinrichtungen für Kinder (KTK) - Bundesverband e.v. - BESCHWERDEMANAGEMENT BESCHWERDEMANAGEMENT SEITE
Träger : Kath. Kirchengemeinde St. Laurentius Bretten Wir sind Mitglied im Verband katholischer Tageseinrichtungen für Kinder (KTK) - Bundesverband e.v. - BESCHWERDEMANAGEMENT BESCHWERDEMANAGEMENT SEITE
Allgemeine Geschäftsbedingungen. Onlineshop. Datenblatt. Stand 2015
 Stand 2015 Datenblatt des s der X-CEN-TEK GmbH & Co. KG (XCT) Stand: 2015/10 1 Allgemeines Alle Leistungen, die aufgrund einer Bestellung über den von der X-CEN-TEK GmbH & Co. KG (XCT) für den Kunden erbracht
Stand 2015 Datenblatt des s der X-CEN-TEK GmbH & Co. KG (XCT) Stand: 2015/10 1 Allgemeines Alle Leistungen, die aufgrund einer Bestellung über den von der X-CEN-TEK GmbH & Co. KG (XCT) für den Kunden erbracht
0. Wo finde ich detaillierte Informationen zum Fach Chemie für Human- und Zahnmediziner?
 FAQ -Übersicht 0. Wo finde ich detaillierte Informationen zum Fach Chemie für Human- und Zahnmediziner? 1. Warum wird meine Email nicht beantwortet? 2. Ich kann zu den Sprechzeiten nicht vorbeikommen,
FAQ -Übersicht 0. Wo finde ich detaillierte Informationen zum Fach Chemie für Human- und Zahnmediziner? 1. Warum wird meine Email nicht beantwortet? 2. Ich kann zu den Sprechzeiten nicht vorbeikommen,
Handbuch. NAFI Online-Spezial. Kunden- / Datenverwaltung. 1. Auflage. (Stand: 24.09.2014)
 Handbuch NAFI Online-Spezial 1. Auflage (Stand: 24.09.2014) Copyright 2016 by NAFI GmbH Unerlaubte Vervielfältigungen sind untersagt! Inhaltsangabe Einleitung... 3 Kundenauswahl... 3 Kunde hinzufügen...
Handbuch NAFI Online-Spezial 1. Auflage (Stand: 24.09.2014) Copyright 2016 by NAFI GmbH Unerlaubte Vervielfältigungen sind untersagt! Inhaltsangabe Einleitung... 3 Kundenauswahl... 3 Kunde hinzufügen...
Anlage eines neuen Geschäftsjahres in der Office Line
 Leitfaden Anlage eines neuen Geschäftsjahres in der Office Line Version: 2016 Stand: 04.11.2015 Nelkenweg 6a 86641 Rain am Lech Stand: 04.11.2015 Inhalt 1 Zielgruppe... 3 2 Zeitpunkt... 3 3 Fragen... 3
Leitfaden Anlage eines neuen Geschäftsjahres in der Office Line Version: 2016 Stand: 04.11.2015 Nelkenweg 6a 86641 Rain am Lech Stand: 04.11.2015 Inhalt 1 Zielgruppe... 3 2 Zeitpunkt... 3 3 Fragen... 3
EVANGELISCHES SCHULZENTRUM LEIPZIG in Trägerschaft des Evangelisch-Lutherischen Kirchenbezirks Leipzig
 Bewerbung um einen Diakonischen Einsatz Sehr geehrte Damen und Herren, die Schülerin/der Schüler.. wohnhaft in.. besucht zurzeit die 10. Klasse unseres Gymnasiums. Vom 26. Januar bis 05. Februar 2015 werden
Bewerbung um einen Diakonischen Einsatz Sehr geehrte Damen und Herren, die Schülerin/der Schüler.. wohnhaft in.. besucht zurzeit die 10. Klasse unseres Gymnasiums. Vom 26. Januar bis 05. Februar 2015 werden
InVo. Information zu Verordnungen in der GKV. Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen. Stand: Februar 2010
 Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
Nr. 1 2010 InVo Information zu Verordnungen in der GKV Stand: Februar 2010 Herstellung von Arzneimitteln durch Ärzte Anzeigepflicht bei Bezirksregierungen Bisher konnten Sie als Arzt Arzneimittel (z. B.
ARBEITSBOGEN 18: ARZNEIMITTELBERATUNG INTERAKTIONS-CHECK
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten über Interaktionen. Überprüfen Sie die Arzneimitteltherapie eines Patienten, der aktuell mindestens drei Arzneimittel
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten über Interaktionen. Überprüfen Sie die Arzneimitteltherapie eines Patienten, der aktuell mindestens drei Arzneimittel
Vertragsnummer: Deutsche Krankenhaus TrustCenter und Informationsverarbeitung GmbH im folgenden "DKTIG"
 Talstraße 30 D-66119 Saarbrücken Tel.: (0681) 588161-0 Fax: (0681) 58 96 909 Internet: www.dktig.de e-mail: mail@dktig.de Vertragsnummer: TrrusttCentterr--Verrttrrag zwischen der im folgenden "DKTIG" und
Talstraße 30 D-66119 Saarbrücken Tel.: (0681) 588161-0 Fax: (0681) 58 96 909 Internet: www.dktig.de e-mail: mail@dktig.de Vertragsnummer: TrrusttCentterr--Verrttrrag zwischen der im folgenden "DKTIG" und
Der Datenschutzbeauftragte
 Die Zulässigkeit von Videoüberwachungsmaßnahmen am Arbeitsplatz unterliegt sehr strengen gesetzlichen Anforderungen und erfordert immer eine ausführliche Abwägung der betroffenen Interessen des Kameraverwenders
Die Zulässigkeit von Videoüberwachungsmaßnahmen am Arbeitsplatz unterliegt sehr strengen gesetzlichen Anforderungen und erfordert immer eine ausführliche Abwägung der betroffenen Interessen des Kameraverwenders
7.6.8 Ermittlung des tatsächlichen privaten Nutzungswerts (Fahrtenbuchmethode)
 Seite 17.8 Ermittlung des tatsächlichen privaten Nutzungswerts (Fahrtenbuchmethode) Der Unternehmer hat bei einem Fahrzeug, welches zu über 50 % betrieblich genutzt wird, die Wahlmöglichkeit, den privaten
Seite 17.8 Ermittlung des tatsächlichen privaten Nutzungswerts (Fahrtenbuchmethode) Der Unternehmer hat bei einem Fahrzeug, welches zu über 50 % betrieblich genutzt wird, die Wahlmöglichkeit, den privaten
In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können.
 Tutorial: Wie erfasse ich einen Termin? In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können. Neben den allgemeinen Angaben zu einem
Tutorial: Wie erfasse ich einen Termin? In diesem Tutorial lernen Sie, wie Sie einen Termin erfassen und verschiedene Einstellungen zu einem Termin vornehmen können. Neben den allgemeinen Angaben zu einem
Investigator Initiated Trials
 Investigator Initiated Trials Die Universität in der Rolle des Sponsors nach AMG - Rechtliche Aspekte - Alexander May, LL.M. Seite 1 Überblick Rechtliche Rahmenbedingungen 12. AMG-Novelle Der Sponsor und
Investigator Initiated Trials Die Universität in der Rolle des Sponsors nach AMG - Rechtliche Aspekte - Alexander May, LL.M. Seite 1 Überblick Rechtliche Rahmenbedingungen 12. AMG-Novelle Der Sponsor und
Prüfungsrichtlinie für die Anerkennung von Prüfingenieuren/Prüfsachverständigen für Brandschutz
 Prüfungsrichtlinie für die Anerkennung von Prüfingenieuren/Prüfsachverständigen für Brandschutz Vom 10. April 2008 Az.: C/5B III.3.2.1 163/08 El I. Verfahren Der Prüfungsausschuss (im Folgenden: Ausschuss)
Prüfungsrichtlinie für die Anerkennung von Prüfingenieuren/Prüfsachverständigen für Brandschutz Vom 10. April 2008 Az.: C/5B III.3.2.1 163/08 El I. Verfahren Der Prüfungsausschuss (im Folgenden: Ausschuss)
Wir sind für Sie da. Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression
 Wir sind für Sie da Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression Wir nehmen uns Zeit für Sie und helfen Ihnen Depressionen lassen sich heute meist gut behandeln. Häufig ist es
Wir sind für Sie da Unser Gesundheitsangebot: Unterstützung im Umgang mit Ihrer Depression Wir nehmen uns Zeit für Sie und helfen Ihnen Depressionen lassen sich heute meist gut behandeln. Häufig ist es
Projektmanagement in Outlook integriert
 y Projektmanagement in Outlook integriert InLoox 6.x Update auf InLoox 6.7.x Ein InLoox Whitepaper Veröffentlicht: März 2011 Copyright: 2011 InLoox GmbH. Aktuelle Informationen finden Sie unter http://www.inloox.de
y Projektmanagement in Outlook integriert InLoox 6.x Update auf InLoox 6.7.x Ein InLoox Whitepaper Veröffentlicht: März 2011 Copyright: 2011 InLoox GmbH. Aktuelle Informationen finden Sie unter http://www.inloox.de
Schritte zum Systempartner Stufe Großhandel
 Schritte zum Systempartner Stufe Großhandel Schritt 1: Anmeldung in der Software-Plattform https://qs-platform.info/ Falls Sie bislang noch kein QS- Systempartner sind, gehen Sie bitte auf die Startseite
Schritte zum Systempartner Stufe Großhandel Schritt 1: Anmeldung in der Software-Plattform https://qs-platform.info/ Falls Sie bislang noch kein QS- Systempartner sind, gehen Sie bitte auf die Startseite
Anmeldung zum Weiterbildungskurs «Führung an Hochschulen»
 Eingang Bestätigung Zulassung Anmeldung zum Weiterbildungskurs «Führung an Hochschulen» Bitte schicken Sie das ausgefüllte Anmeldeformular unterschrieben per Post an Patricia Tremel, Universität Bern,
Eingang Bestätigung Zulassung Anmeldung zum Weiterbildungskurs «Führung an Hochschulen» Bitte schicken Sie das ausgefüllte Anmeldeformular unterschrieben per Post an Patricia Tremel, Universität Bern,
