SUCCESS-Studie. Kurzprotokoll Co-Studien-Direktoren: Prof. Dr. M. W. Beckmann Universitätsfrauenklinik Erlangen
|
|
|
- Dorothea Kaiser
- vor 7 Jahren
- Abrufe
Transkript
1 SUCCESS-Studie Multizentrische prospektiv randomisierte Phase III Studie zum Vergleich von FEC-Doc- Chemotherapie versus FEC-DocG-Chemotherapie, sowie 2 versus 5 Jahre Zoledronattherapie in der adjuvanten Therapie von Patientinnen mit Brustkrebs in Kooperation mit : empfohlen von: Studienleitung: Prof. Dr. H. Sommer (Sponsor) PD. Dr. W. J. Janni (LKP) I. Universitätsfrauenklinik Klinikum Innenstadt der LMU Studienzentrum Onkologie Maistraße 11 D München Tel: Studiensekretariat Zentrale Fax: { HYPERLINK "mailto:success@med.uni-muenchen.de" } Web: Randomisation und CRO: Alcedis GmbH, Winchesterstr. 2 D Gießen Tel: Fax: success-cro@alcedis.de Kurzprotokoll Co-Studien-Direktoren: Prof. Dr. M. W. Beckmann Universitätsfrauenklinik Erlangen Prof. Dr. W. Lichtenegger Universitätsfrauenklinik Charité Berlin Chair Advisory Board: Prof. Dr. A. Schneider Universitätsklinik Benjamin-Franklin Berlin Statistik: Estimate GmbH, Konrad-Adenauer-Allee 1 D Augsburg Tel: Fax: { HYPERLINK "mailto:info@estimate.de" } Version 1.2 { PAGE 1 }
2 Zielsetzung der Studie Hauptzielkriterium: Primäres Studienziel ist der Vergleich der rezidivfreien Überlebenszeit nach Randomisierung von Patientinnen, die adjuvant 3 Zyklen 5-Fluorouracil-Epirubicin-Cyclophosphamid (FEC)- Chemotherapie, gefolgt von 3 Zyklen Docetaxel (D)-Chemotherapie versus 3 Zyklen FEC- Chemotherapie, gefolgt von 3 Zyklen Gemcitabin-Docetaxel (DG)-Chemotherapie erhalten, sowie der Vergleich der rezidivfreien Überlebenszeit nach Randomisierung von Patientinnen, die 2 Jahre versus 5 Jahre mit Zoledronat behandelt werden. Sekundäre Zielkriterien: Gesamtüberleben nach Randomisation Fernmetastasenfreies Überleben Toxizität Lebensqualität Prädiktiver und prognostischer Wert von Minimal Residual Disease im peripheren Blut Skelettbezogene Ereignisse Häufigkeit von Zweitkarzinomen Einschlusskriterien Primäres epitheliales invasives Mammakarzinom pt1-4, pm0 Histologischer Nachweis axillärer Lymphknotenmetastasen pn1-3 oder nodal negative highrisk Patientinnen No/x, definiert als pt 2 oder histopathologisches Grading 3 oder Alter 35 oder negativer Hormonrezeptorstatus R0-Resektion des Primärtumors (Resektionsränder frei von invasiven Karzinomanteilen, insitu-anteile jedoch erlaubt), maximal 6 Wochen vor Randomisation Frauen älter als 18 Jahre Allgemeinzustand 2 auf der ECOG-Skala Adäquate Knochenmarksreserve: Leukozyten 3.0 x 10 9 /l und Thrombozyten 100 x 10 9 /l Bilirubin innerhalb Normalwert, GOT, GPT, Alkalische Phosphatase innerhalb 1,5-fachem Normalwert des jeweiligen Referenzlabors Gewährleistung regelmäßiger Nachsorge während der Studiendauer Verständnis des Studienkonzepts und schriftliche Einverständniserklärung 2
3 Ausschlusskriterien Inflammatorisches Mammakarzinom (bilaterales Mamma-Ca ist kein Ausschlusskriterium) Vorangegangene oder gleichzeitige Therapie mit anderen zytotoxischen oder antineoplastischen Medikamenten, die nicht innerhalb des Protokolls vorgesehen sind Vorgeschichte von Erkrankungen mit Einfluss auf den Knochenstoffwechsel wie z.b. M. Paget und primärer Hyperparathyreoidismus Vorausgegangene Behandlung mit Bisphosphonaten innerhalb der letzten 6 Monate Eingeschränkte Nierenfunktion: Creatinin-Clearance 30 ml/min nach der Cockcroft-Gault- Formel: 140 Alter(Jahre) * Gewicht(kg )* 0,85 CrCl= 72 * Serum Kreatinin(mg/dl) Zweitkarzinom (außer In-situ-Karzinom der Cervix uteri oder adäquat behandeltes Basaliom) Manifeste kardiale Vorschädigung (Kardiomyopathie mit verminderter Ventrikelfunktion (NYHA > II), therapiebedürftige Arrhythmien mit Einfluss auf die LVEF, Z. n. Myokardinfarkt oder Angina pectoris innerhalb der letzten 6 Monate, medikamentös nicht eingestellter arterieller Hypertonus) Jede bekannte Überempfindlichkeit gegenüber Docetaxel, Epirubicin, 5-Fluorouracil, Cyclophosphamid, Gemcitabin, Zoledronat oder sonstigen Studienmedikamenten Behandlung mit einem zu untersuchenden Medikament in den letzten 3 Wochen vor Studieneintritt Bestehende dentale Beschwerden, Kiefer- und Zahnentzündungen oder akute oder vorbestehende Kiefernekrosen, von exponierten Knochen in der Mundhöhle, oder von langsam heilenden Wunden nach Zahnbehandlungen Kürzlich durchgeführte (6 Wochen) oder geplante Zahn- oder Kieferoperationen (Extraktionen, Implantate) Patientinnen in Schwangerschaft oder Stillzeit (bei prämenopausalen Frauen muss eine sichere Kontrazeption gewährleistet werden: Intrauterinpessare, operative Sterilisation oder, nur bei hormonrezeptornegativen Mammakarzinompatientinnen, orale, subkutane oder transvaginale, nicht östrogenhaltige Kontrazeptiva) 3
4 Studiendesign R R Endokrine Therapie: MRD-Überwachung im peripheren Blut Nachweis von zirkulierenden Tumorzellen und Tumormarkern im peripheren Blut vor der Chemotherapie, nach der Chemotherapie, 2 Jahre nach Abschluss der Chemotherapie, 5 Jahre nach Abschluss der Chemotherapie 5- FU 500 mg/m², Epirubicin 100 mg/m², Cyclophosphamid 500 mg/m² q3w Docetaxel 100 mg/m² q3w Docetaxel 75mg/m², Gemcitabine mg/m² d1,8 q3w Zoledronat 4mg x 2a vs 5a (q3mx24m, vs. q3mx24m gefolgt von q6mx36m) Tamoxifen 20 mg qid p.o.x 2 a (plus Goserelin 3.6 mg Depot x 2 a bei prämenopausalen Frauen) Anastrozol 1 mg qid p.o.x 3 a bei postmenop. Pat. (Tam bei prämenop. Pat.) Randomisation A: AA: 5-Fluorouracil 500 mg/m² und Epirubicin 100 mg/m² und Cyclophosphamid 500 mg/m² i.v. q3w x 3 (alle nur an Tag 1 verabreicht) gefolgt von Docetaxel 75 mg/m² (nur an Tag 1) und Gemcitabin 1000 mg/m² i.v. (an Tag 1 und 8 verabreicht, 30 min Infusion) q3w x3 AB: 5-Fluorouracil 500 mg/m² und Epirubicin 100 mg/m² und Cyclophosphamid 500 mg/m² i.v. q3w x 3 gefolgt von Docetaxel 100 mg/m² i.v. q3w x 3 (alle nur an Tag 1 verabreicht) Randomisation B: BA: Zoledronat 4 mg i.v. q3m x 24m gefolgt von Zoledronat 4 mg i.v. q6m x 36m BB: Zoledronat 4 mg i.v. q3m x 24m Weitere Weitere Hinweise Hinweise zur Studientherapie zur Studientherapie und FAQs unter und { FAQs HYPERLINK unter " } 4
5 Bestrahlung: Patientinnen nach brusterhaltender Therapie erhalten obligat eine Strahlentherapie. Patientinnen nach Mastektomie erhalten eine adjuvante Radiatio, wenn mindestens einer der im Studienprotokoll genannten zusätzlichen Risikofaktoren vorliegt. Therapie mit Trastuzumab (Herceptin ): Bei Patientinnen mit einem eindeutig HER2-neu überexprimierenden Tumor (IHC+++ oder FISH+) wird die Therapie mit Trastuzumab nach Abschluss der Chemotherapie über ein Jahr empfohlen. Diese sollte nach Beendigung der Strahlentherapie beginnen. Dosierung: 8 mg/kg KG loading dose, gefolgt von 6 mg/kg KG, q3w, für 1 Jahr Endokrine Anschlussbehandlung bei positivem Hormonrezeptorstatus (Östrogen- u/o Progesteronrezeptor ab 10 %) (nach Abschluss der Chemotherapie): Ausgangssituation Prämenopausale Patientinnen Behandlung Tamoxifen 20 mg p.o. für 5 Jahre Falls Patientin < 40 Jahre oder Menstruation innerhalb von 6 Monaten nach Ende der Chemotherapie oder LH < 20 mie/ml, FSH < 20 mie/ml und E2 > 20 pg/ml (unabhängig vom Lymphknotenstatus) Postmenopausale Patientinnen Zusätzlich Goserelin (Zoladex ) 3,6 mg/monat s.c. q4w für 2 Jahre Tamoxifen 20 mg p.o. für 2 Jahre nachfolgend Anastrozol (Arimidex ) 1mg p.o. für weitere 3 Jahre Bei Kontraindikationen oder Unverträglichkeit gegen Tamoxifen Anastrozol (Arimidex ) 1mg p.o. für 5 Jahre 5
6 Behandlungsplan Arm AA: Zyklus 1 bis 3 Präparat Dosierung Applikationsart Tag 5-Fluorouracil 500 mg/m² i.v., Min. Kurzinfusion Tag 1 Epirubicin 100 mg/m 2 i.v., 15 Min. Kurzinfusion Tag 1 Cyclophosphamid 500 mg/m 2 i.v., 60 Min. Infusion Tag 1 Zyklus 4 bis 6 Docetaxel (Taxotere ) 75 mg/m 2 i.v., 60 Min. Infusion Tag 1 Gemcitabin 1000 mg/m² i.v., 30 Min. Infusion Tag 1, 8 Begleitmedikation Arm AA: Zyklus 1 bis 3 Präparat Dosierung Applikationsart Tag Dexamethason 8 mg 0 0 i.v. 15 Min. vor der Infusion Mesna (Uromitexan ) 20% d. Cycloph.-Gesamtdosis bzw. nach 1 i.v. Gabe 40% d. Cycloph.-Gesamtdosis i.v. p.o h nach Infusion 2 + 6h nach Infusion Wiederholung des Zyklus am Tag 22 Zyklus 4 bis 6 Dexamethason 8 mg 0 8 mg p.o. Morgens und abends am Tag vor der Infusion Dexamethason 8 mg 0 0 i.v. 15 Min. vor der Infusion Dexamethason mg p.o. Abends nach der Infusion Dexamethason 8 mg 0 8 mg p.o. Morgens und abends am Tag nach der Infusion Arm AB: Zyklus 1 bis 3 Präparat Dosierung Applikationsart Tag 5-Fluorouracil 500 mg/m² i.v., Min. Kurzinfusion Tag 1 Epirubicin 100 mg/m 2 i.v., 15 Min. Kurzinfusion Tag 1 Cyclophosphamid 500 mg/m 2 i.v., 60 Min. Infusion Tag 1 Zyklus 4 bis 6 Docetaxel (Taxotere ) 100 mg/m² i.v., 60 min. Infusion Tag 1 Wiederholung des Zyklus am Tag 22 Begleitmedikation Arm AB: Zyklus 1 bis 3 Präparat Dosierung Applikationsart Tag Dexamethason 8 mg 0 0 i.v. 15 Min. vor der Infusion Mesna (Uromitexan ) 20% d. Cycloph.-Gesamtdosis bzw. nach 1 i.v. Gabe 40% d. Cycloph.-Gesamtdosis i.v. p.o h nach Infusion 2 + 6h nach Infusion Zyklus 4 bis 6 Dexamethason 8 mg 0 8 mg p.o. Morgens u. abends am Tag vor der Infusion Dexamethason 8 mg 0 0 i.v. 15 Min. vor der Infusion Dexamethason mg p.o. Abends nach der Infusion Dexamethason 8 mg 0 8 mg p.o. Morgens und abends am Tag nach der Infusion Weitere Hinweise zur Studientherapie und FAQs unter Weitere Hinweise zur Studientherapie und FAQs unter { HYPERLINK " } 6
7 Allgemeine Empfehlungen zur Therapiedurchführung In beiden Therapiearmen sollte eine adäquate Behandlung mit Antiemetika (z.b. 5-HT-3 Antagonisten 15 min vor Infusion) durchgeführt werden. Weitere Gaben sollten nach Bedarf auch an den folgenden Tagen durchgeführt werden. Bei der Berechnung der Körperoberfläche sollen die aktuelle Körpergröße und das Körpergewicht für die Berechnung der Körperoberfläche (KOF) herangezogen werden. Bei übergewichtigen Patienten sollte eine maximale KOF von 2 m² zugrunde gelegt werden. Die Behandlung mit G-CSF (Granocyte ) sollte sekundär-prophylaktisch in einer Dosierung von einer Ampulle G34 / Tag gegeben werden bei: jeder febrilen Neutropenie Neutropenie < 0,5 x 10 9 /l über mehr als 5 Tage Neutropenie < 0,1 x 10 9 /l Intervallverlängerung wegen Leukopenie Tritt eines dieser Kriterien auf, so erfolgt in allen nachfolgenden Zyklen die Gabe von G-CSF. Die sekundär-prophylaktische Gabe von 1 Ampulle G34 / Tag erfolgt von Tag 5 bis Tag 10, oder bis die Leukozytenzahl nach dem Nadir 5.000/µl überschritten hat. Beim Auftreten einer Neutropenie Grad 3/4 kann in beiden Therapiearmen fakultativ eine prophylaktische orale Antibiose (z.b. Ciprofloxacin (Ciprobay ) 500 mg p.o. 2 x/tgl., Levofloxacin (Tavanic ) 500 mg p.o. 1 x/tgl.) gegeben werden. Diese wird jedoch empfohlen, falls die Neutrophilen Granulozyten auf < 0,5 x 10 9 /l abfallen (unabhängig von G-CSF-Gabe). Bei jedem Fieber ist unbedingt eine Abklärung (s.u.) erforderlich. Jede febrile Neutropenie muss stationär mit i.v.-antibiose behandelt werden! Während der Zoledronattherapie bekommen die Patientinnen zusätzlich 500 mg Calcium p.o. q.i.d. und 400 I.E. Vitamin D p.o. q.i.d. verabreicht. Die Serumspiegel von Calcium, Phosphat und Magnesium sollten nach Einleitung der Zoledronattherapie sorgfältig überwacht werden. Komplikationen während der Neutropenie Febrile Neutropenien sollten nach dem NCI-Score beurteilt werden. Die Körpertemperatur sollte möglichst als Körperkerntemperatur bestimmt werden. Kommt es bei einer Patientin zu Fieber (Kerntemperatur > 38.0{SYMBOL 176 \f "Symbol" \s 12}C) im Rahmen einer Neutropenie Grad 3 oder 4, so wird das folgende Vorgehen vorgeschlagen: 1 Stationäre Einweisung ( keine ambulante Antibiotikatherapie! ), ggf. Umkehrisolation. 2 Differential-Blutbildkontrolle, stündl. Temperatur-, Puls- und RR-Kontrolle, ggf. Rö.-Thorax zum Ausschluss einer Pneumonie. Ausführliche körperliche Untersuchung. Mikrobiologische Diagnostik (Blutkulturen, Rachenabstrich, Urin, etc.) 3 Beginn einer empirischen antibiotischen Therapie mit breiter Abdeckung im grampositiven und gramnegativen Bereich, z.b. 3-fach-Antibiose i.v. (Gentamycin 240 mg 1-0-0, Piperacillin 4 g 1-1-1, Combactam 1 g 1-1-1). 4 G-CSF-Applikation (Granocyte ) 1 x täglich Nach einer febrilen Neutropenie, die trotz sekundär-prophylaktischer G-CSF-Gabe aufgetreten ist, muss die Dosis im nächsten Zyklus um einen Dosislevel gesenkt werden. In den weiteren Zyklen sollte dann wieder ein Therapieversuch mit der ursprünglichen Dosis unter sekundärprophylaktischer G-CSF-Gabe vorgenommen werden! 7
8 Intervallverlängerung Der nächste Zyklus kann wegen hämatologischer bzw. nicht-hämatologischer Toxizität um maximal 2 Wochen verschoben werden. Dies gilt auch für Gemzar, (d1 und d8): Wenn Tag 8 um weniger als eine Woche verschoben wurde, soll der nächste Zyklus protokollgemäß gegeben werden. Liegt aber eine Zyklusverschiebung um eine Woche oder mehr vor, so sollte der nächste Zyklus soweit verschoben werden, dass der Abstand zum nächsten Zyklus 14 Tage beträgt. Voraussetzungen für den neuen Zyklus sind: Neutrophile Granulozyten 1.5 x 10 9 /l oder Leukozyten 2.0 x 10 9 /l Thrombozyten 100 x 10 9 /l Bei weiterer Intervallverlängerung muss mit der Studienleitung Rücksprache gehalten werden. Unter Zoledronattherapie sollte das Serum-Kreatinin vor jeder Gabe überwacht werden. Bei Erhöhung des Kreatinins über den Ausgangswert bei Studieneintritt sollte ein Aussetzen aus der Therapie in Erwägung gezogen werden: War der Kreatinin-Grundwert bei < 1,4 mg/dl, verlangt eine Zunahme des Werts von mindestens 0,5 mg/dl ein Aussetzen aus der Therapie. Wenn der Kreatinin-Grundwert bei 1,4 mg/dl lag, wird bei jeglicher Erhöhung des Kreatinins um 1,0 mg/dl oder mehr ein Aufschieben der Therapie erforderlich. Die Therapie kann dann fortgesetzt werden, wenn der Kreatinin-Wert nicht mehr als 10% des Ausgangswertes beträgt. Die Zoledronattherapie sollte dabei mit der gleichen Dosis wie vor der Behandlungsunterbrechung wieder aufgenommen werden. Randomisation A: Empfehlungen zur Dosisreduktion Dosisreduktionsstufen Fluorouracil 500 mg/m² 400 mg/m² 300 mg/m² Epirubicin 100 mg/m² 80 mg/m² 60 mg/m² Cyclophosphamid 500 mg/m² 400 mg/m² 300 mg/m² Docetaxel (Arm AA) 75 mg/m² 60 mg/m² 45 mg/m² Gemcitabin 1000 mg/m² 800 mg/m² 600 mg/m² Docetaxel (Arm AB) 100 mg/m² 80 mg/m² 60 mg/m² Randomisation B: Der Beginn der Zoledronattherapie ist 4 Wochen nach Ende der Chemotherapie vorgesehen. Vor jeder Zoledronattherapie muss die Creatinin-Clearance bestimmt werden. Die Dosis von Zoledronat wird anhand der Creatinin-Clearance reduziert, wenn eine Crea-Clearance < 60 ml/min auftritt (s. Tabelle). Diese Dosierungen sollten dieselbe AUC erreichen, wie bei Patientinnen mit einer Crea-Clearance von 75 ml/min. Die Infusionsdauer sollte dabei nicht unter 15 min liegen. Zur Bestimmung der Crea-Clearance wird folgende Formel verwendet (Cockcroft-Gault-Formel): Alter(Jahre) * Gewicht(kg )* 0,85 CrCl= 72 * Serum - Kreatinin(mg/dl) Creatinin-Clearance (ml/min) Zometa Dosierung* mg mg mg mg 8
9 Hämatologische Toxizität Die Chemotherapiedosis im folgenden Zyklus sollte reduziert werden, falls trotz sekundärprophylaktischer G-CSF-Gabe mindestens eine der folgenden hämatologischen Toxizitäten auftraten: jede febrile Neutropenie (Temperatur > 38.0 C, Neutropenie < 0.5 x 10 9 /l, stationäre Aufnahme und intravenöse Antibiose) Neutropenie < 0,5 x 10 9 /l über mehr als 5 Tage Thrombopenie NCI-Grad 4 (< 25,0 x 10 9 /l) Intervallverlängerung wegen Leukopenie Nicht-hämatologische Toxizität Toxizitäten werden anhand der NCI-Kriterien bewertet. Patientinnen mit einer nichthämatologischen Toxizität Grad 0-2 erhalten die vorgegebene Gesamtdosis. Falls für ein bestimmtes Symptom keine NCI-Graduierung beschrieben ist, sollte die Toxizität in der folgenden Form kategorisiert werden: 1 = schwach, 2 = mäßig, 3 = schwer und 4 = lebensbedrohlich Gastrointestinal Mukositis NCI-Grad 3 Mukositis oder Erbrechen NCI-Grad 4 Hepatisch (unter Therapie mit Docetaxel) Erhöhung der Transaminasen (GOT oder GPT) > 1,5fach oder der alkalischen Phosphatase > 2,5fach der oberen Normalwerte Erhöhung des Serumbilirubins > oberer Normalwert, oder der Transaminasenwerte > 3,5fach oder der alkalischen Phosphatase {SYMBOL 179 \f "Symbol" \s 12} 6fach der oberen Normalwerte Neurologisch NCI-Grad 2 NCI-Grad 3 (intolerable Parästhesien oder schlechter) und NCI-Grad 4 (Paralyse) Pulmonal (v.a. in Hinsicht auf Gemcitabin) Pneumonitis {SYMBOL 179 \f "Symbol" \s 12} Grad 2, verursacht durch Gemcitabin Kardial AV-Block Grad 1, asymptom. Bradykardie, isolierte asymptom. ventrikuläre Extrasystolen Behandlungsbedürftige Arrhythmie, AV-Block > Grad 1, LVEF-Abfall um >20% oder um >10% und LVEF unterhalb des Klinikgrenzwertes Andere gravierende Organtoxizität NCI-Grad {SYMBOL 179 \f "Symbol" \s 12} 3 (außer Alopezie, Übelkeit und Erbrechen) Reduktion der Chemotherapie um 1 Stufe Abbruch der Behandlung Reduktion der Chemotherapie um 1 Stufe Kein Fortführen der Behandlung mit Docetaxel, ggf. Umstellung auf FEC (500/100/500) für die noch ausstehenden Zyklen Reduktion der Chemotherapie um 1 Stufe Abbruch der Behandlung Abbruch der Behandlung, Therapie mit Kortikoiden Weiterbehandlung unter kardialem Monitoring Abbruch der Behandlung Abbruch der Therapie (bzw. Reduktion der Chemotherapie um 1 Stufe nach Ermessen des Prüfarztes) Sollten schwerwiegende Toxizitäten (Grad 3 und 4) auch nach Reduktion der Chemotherapie- Dosierung auftreten, ist zur Absprache des weiteren studientherapeutischen Vorgehens Rücksprache mit der Studienleitung zu nehmen. Weitere Hinweise zur Studientherapie und FAQs unter Weitere Hinweise zur Studientherapie und FAQs unter { HYPERLINK " } 9
10 Begleittherapie Die palliative und supportive Behandlung von mit der Tumorerkrankung zusammenhängenden Symptomen wird allen Patientinnen im Rahmen dieser Studie angeboten. Komplementäre naturheilkundliche Präparate sind erlaubt. Keine anderen antineoplastisch wirksamen Substanzen, welche nicht im Protokoll vorgesehen sind, dürfen während der Verabreichung der Studienmedikamente gegeben werden (Therapie mit Trastuzumab / Herceptin ist, wenn indiziert, erlaubt, siehe Seite 5). Kontrolluntersuchungen Zeitpunkt Vor Beginn Vor jedem 28 Tage nach 6 Wochen nach Follow up Untersuchung Therapie Chemotherapie Strahlentherapie der letzter letzter Zyklus Demographische Daten Ein- und Ausschlusskriterien Einverständniserklärung d. Pat. Registrierung/Randomisation Anamnese Klinische Untersuchung Größe, Gewicht Begleitmedikation Begleiterkrankungen Aktivitätsstatus (ECOG) EORTC QLQ-C30 + BR23 Lebensqualitätsfragebogen vor 4.Zyklus Blutentnahme für MRD- Surveillance Blutbild (Differential-BB erforderlich) Natrium, Kalium Kreatinin Bilirubin, GOT, GPT, Albumin, Eiweiß INR, PTT GT, AP Schwangerschaftstest (prämenop.) 2 und 5 Jahre nach Ende der Chemotherapie 1-2x / b.b. Woche b.b. Zusätzlich vor jeder Zoledronattherapie (s. a. Randomisation B) b.b. b.b. b.b. b.b. Bildgebende Diagnostik (Lebersono, Knochenszinti, b.b. Röntgen-Thorax) bis 5 Wochen vor Randomisation Mammographie/ In den Mamma-Sonographie ipsilateral ersten nach BET 3 Jahren alle 6 Monate, danach alle 12 Monate EKG 6 Monate nach CHT Toxizität (NCI) Überlebens-/Rezidivstatus 10
11 Translationales Forschungsprogramm Minimal Residual Disease im peripheren Blut Zu vier Zeitpunkten im Verlauf der adjuvanten Therapie werden Blutproben zur Bestimmung von Tumormarkern und zirkulierenden Tumorzellen im peripheren Blut untersucht. Es werden 50 ml Blut in den zur Verfügung gestellten Blutröhrchen (1 Kästchen pro Blutentnahme) zu den folgenden Zeitpunkten entnommen: - 1. BE: Vor Beginn der Chemotherapie - 2. BE: Nach Ende der Chemotherapie, jedoch vor Beginn der endokrinen und Bisphosphonattherapie - 3. BE: 2 Jahre nach Abschluss der Chemotherapie - 4. BE: 5 Jahre nach Abschluss der Chemotherapie Die Versendung der Blutproben sollte bei Raumtemperatur möglichst innerhalb von 24 Stunden per Post erfolgen an: I. Frauenklinik, Klinikum Innenstadt Tumorimmunologisches Labor, Zimmer 123 c/o Dr. B. Rack / S. Hofmann Maistr. 11 D München Phone: Fax: Möglichst keine Abnahme und Versendung vor Wochenende und Feiertagen, um eine umgehende Verarbeitung zu gewährleisten. Beim Nachweis von MRD sollte eine erneute Blutentnahme im Abstand von 3 Monaten erfolgen. Beim Nachweis von MRD in 2 aufeinander folgenden Blutproben empfehlen wir eine intensivierte bildgebende Diagnostik alle 3 Monate für die Dauer eines halben Jahres. Diese Diagnostik sollte beinhalten: - eingehende klinische Untersuchung - Röntgenbild der Lunge - Ultraschall der Leber - Knochenszintigramm - Blutentnahme zur MRD-Diagnostik Eine Rezidivtherapie sollte jedoch nur beim Nachweis einer Metastasierung mittels bildgebender Diagnostik eingeleitet werden. Studienmedikation Folgende Medikamente werden kostenfrei zur Verfügung gestellt: Gemcitabin Zoledronat Docetaxel (bei N0-Patientinnen) Die Bestellung erfolgt automatisch bei der Randomisation durch ALCEDIS. Diese Studie wird unterstützt von den Firmen AstraZeneca, Chugai, Lilly, Novartis, Veridex und Sanofi Aventis. 11
12
Zielsetzung der Studie
 SUCCESS-Studie Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC- Doc-Chemotherapie versus FEC-DocG-Chemotherapie, sowie 2 oder 5 Jahre Zoledronattherapie in der adjuvanten
SUCCESS-Studie Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC- Doc-Chemotherapie versus FEC-DocG-Chemotherapie, sowie 2 oder 5 Jahre Zoledronattherapie in der adjuvanten
ADEBAR-Studie. Randomisierte Phase III Studie zum Vergleich von FEC-Chemotherapie
 ADEBAR-Studie Randomisierte Phase III Studie zum Vergleich von FEC-Chemotherapie Studienleitung: versus EC-Doc-Chemotherapie in der adjuvanten Therapie des Mammakarzinoms ( 4 LK) Prof. Dr. H. Sommer Gütesiegel
ADEBAR-Studie Randomisierte Phase III Studie zum Vergleich von FEC-Chemotherapie Studienleitung: versus EC-Doc-Chemotherapie in der adjuvanten Therapie des Mammakarzinoms ( 4 LK) Prof. Dr. H. Sommer Gütesiegel
SUCCESS-B-Studie. Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie
 SUCCESS-B-Studie Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie in Kooperation mit : Kurzprotokoll Studienleitung: Prof. Dr.
SUCCESS-B-Studie Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie in Kooperation mit : Kurzprotokoll Studienleitung: Prof. Dr.
Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie
 SUCCESS-B-Studie Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie in Kooperation mit : Kurzprotokoll Studienleitung: Prof. Dr.
SUCCESS-B-Studie Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie in Kooperation mit : Kurzprotokoll Studienleitung: Prof. Dr.
in Kooperation mit : Hauptzielkriterium:
 Deutsches Kurzprotokoll Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC-Doc-Chemotherapie versus Doc-C-Chemotherapie, sowie dem Einfluss einer Lifestyle Intervention beim
Deutsches Kurzprotokoll Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC-Doc-Chemotherapie versus Doc-C-Chemotherapie, sowie dem Einfluss einer Lifestyle Intervention beim
Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie SUCCESS B-STUDIE
 SUCCESS B-Studie Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie SUCCESS B-STUDIE (Simultaneous Study of Gemcitabine-Docetaxel
SUCCESS B-Studie Vergleichende Untersuchung einer adjuvanten Gemcitabine-Docetaxel Kombinationstherapie sowie einer biologischen Zieltherapie SUCCESS B-STUDIE (Simultaneous Study of Gemcitabine-Docetaxel
Paclitaxel Gemcitabin
 135 16 16.2 Fortgeschrittener Harnblasen tumor Zweitlinientherapie 16.2 Fortgeschrittener Harnblasen tumor Zweitlinientherapie 16.2.1 Paclitaxel Gemcitabin Paclitaxel Gemcitabin Fortgeschrittenes Urothelkarzinom
135 16 16.2 Fortgeschrittener Harnblasen tumor Zweitlinientherapie 16.2 Fortgeschrittener Harnblasen tumor Zweitlinientherapie 16.2.1 Paclitaxel Gemcitabin Paclitaxel Gemcitabin Fortgeschrittenes Urothelkarzinom
Gemcitabin Carboplatin
 155 16 16.4 Fortgeschrittener Harnblasen tumor Niereninsuffizienz 16.4 Fortgeschrittener Harnblasen tumor Niereninsuffizienz 16.4.1 Gemcitabin Carboplatin Gemcitabin Carboplatin Fortgeschrittenes Urothelkarzinom
155 16 16.4 Fortgeschrittener Harnblasen tumor Niereninsuffizienz 16.4 Fortgeschrittener Harnblasen tumor Niereninsuffizienz 16.4.1 Gemcitabin Carboplatin Gemcitabin Carboplatin Fortgeschrittenes Urothelkarzinom
SUCCESS - C - Studie Kurzprotokoll Version 1.3
 SUCCESS - C - Studie Kurzprotokoll Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC- Doc-Chemotherapie versus Doc-C-Chemotherapie, sowie dem Einfluss einer Lebensstil -
SUCCESS - C - Studie Kurzprotokoll Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC- Doc-Chemotherapie versus Doc-C-Chemotherapie, sowie dem Einfluss einer Lebensstil -
Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil
 CLL5-Protokoll der deutschen CLL-Studiengruppe 15 Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil - CLL5-Protokoll der
CLL5-Protokoll der deutschen CLL-Studiengruppe 15 Therapie von Patienten über 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Chlorambucil - CLL5-Protokoll der
Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid
 10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
10 CLL4-Protokoll der deutschen CLL-Studiengruppe Therapie von Patienten bis 65 Jahren mit fortgeschrittener chronischer lymphatischer Leukämie mit Fludarabin versus Fludarabin/Cyclophosphamid - CLL4-Protokoll
Vinflunin (Javlor ) Zyklus: T1 q3w, Tag 22 = Tag 1 = neuer Zyklus. Patientenaufkleber
 143 16 16.2.2 Vinflunin (Javlor ) Vinflunin (Javlor ) Zyklus: T1 q3w, Tag 22 = Tag 1 = neuer Zyklus Patientenaufkleber Kalkulierte Kreatinin-Clearance (GFR) nach Cockcroft und Gault: Mann: (140 Alter)
143 16 16.2.2 Vinflunin (Javlor ) Vinflunin (Javlor ) Zyklus: T1 q3w, Tag 22 = Tag 1 = neuer Zyklus Patientenaufkleber Kalkulierte Kreatinin-Clearance (GFR) nach Cockcroft und Gault: Mann: (140 Alter)
SUCCESS - C - Studie Kurzprotokoll Version 1.4
 SUCCESS - C - Studie Kurzprotokoll Version 1.4 Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC- Doc-Chemotherapie versus Doc-C-Chemotherapie, sowie dem Einfluss einer Lebensstil
SUCCESS - C - Studie Kurzprotokoll Version 1.4 Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC- Doc-Chemotherapie versus Doc-C-Chemotherapie, sowie dem Einfluss einer Lebensstil
Neue Studienkonzepte SUCCESS
 Campus Innenstadt für Frauenheilkunde und Geburtshilfe Neue Studienkonzepte SUCCESS PD Dr. med. Brigitte Rack für Frauenheilkunde und Geburtshilfe Ludwig-Maximilians-Universität München Campus Innenstadt
Campus Innenstadt für Frauenheilkunde und Geburtshilfe Neue Studienkonzepte SUCCESS PD Dr. med. Brigitte Rack für Frauenheilkunde und Geburtshilfe Ludwig-Maximilians-Universität München Campus Innenstadt
Pemetrexed (ALIMTA ) Monotherapie. Drittlinientherapie des fortgeschrittenen/metastasierten Urothelkarzinoms Tag 22 = Tag 1 = neuer Zyklus
 150 Kapitel Harnblasentumor.3 Fortgeschrittener Harnblasen tumor Drittlininentherapie.3.1 Pemetrexed (ALIMTA ) Monotherapie Pemetrexed (ALIMTA ) Monotherapie Drittlinientherapie des fortgeschrittenen/metastasierten
150 Kapitel Harnblasentumor.3 Fortgeschrittener Harnblasen tumor Drittlininentherapie.3.1 Pemetrexed (ALIMTA ) Monotherapie Pemetrexed (ALIMTA ) Monotherapie Drittlinientherapie des fortgeschrittenen/metastasierten
Charitè, Campus Benjamin Franklin Medizinische Klinik III Hämatologie, Onkologie und Transfusionsmedizin Direktor Prof. Dr. E.Thiel Berlin Bonn, 04/05
 VERGLEICHENDE PROSPEKTIVE STUDIE FÜR DIE PRIMÄRE UND SEKUNDÄRE PROPHYLAXE VON MYKOTISCHEN INFEKTIONEN BEI PATIENTEN MIT LANGER NEUTROPENIEDAUER MIT TOPISCHEN ANTIMYKOTIKA IM VERGLEICH MIT SYSTEMISCHER
VERGLEICHENDE PROSPEKTIVE STUDIE FÜR DIE PRIMÄRE UND SEKUNDÄRE PROPHYLAXE VON MYKOTISCHEN INFEKTIONEN BEI PATIENTEN MIT LANGER NEUTROPENIEDAUER MIT TOPISCHEN ANTIMYKOTIKA IM VERGLEICH MIT SYSTEMISCHER
Target-Therapie mit dem mtor-inhibitor Temsirolimus (Torisel )
 212 Kapitel Nierentumor.2 Erstlinientherapie bei Poor-risk-Patienten.2.1 Target-Therapie mit dem mtor-inhibitor Temsirolimus (Torisel ) Target-Therapie mit dem mtor-inhibitor Temsirolimus (Torisel ) Wochenschema
212 Kapitel Nierentumor.2 Erstlinientherapie bei Poor-risk-Patienten.2.1 Target-Therapie mit dem mtor-inhibitor Temsirolimus (Torisel ) Target-Therapie mit dem mtor-inhibitor Temsirolimus (Torisel ) Wochenschema
Universität zu Lübeck Institut für Krebsepidemiologie e.v.
 Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Vorstellung der aktuellen DETECT Studiendesigns. S. Krause Studienkoordinatorin Studienzentrale UFK Ulm
 Vorstellung der aktuellen DETECT Studiendesigns S. Krause Studienkoordinatorin Studienzentrale UFK Ulm Aktuelles Design der DETECT-Studien DETECT III DETECT IV a und b DETECT V Meeting-Mappen: Übersichtsfolien
Vorstellung der aktuellen DETECT Studiendesigns S. Krause Studienkoordinatorin Studienzentrale UFK Ulm Aktuelles Design der DETECT-Studien DETECT III DETECT IV a und b DETECT V Meeting-Mappen: Übersichtsfolien
Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie
 Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Mammakarzinom - Zulassungsstatus von Medikamenten Leitlinie Empfehlungen der Fachgesellschaft zur Diagnostik und Therapie hämatologischer und onkologischer Erkrankungen Herausgeber DGHO Deutsche Gesellschaft
Seite Diskussion
 Seite 99 4 Diskussion In der Behandlung lokal fortgeschrittener oder inflammatorischer Mammakarzinome gilt die neoadjuvante Chemotherapie schon lange als Standard. Dass diese Therapieform in Hinblick auf
Seite 99 4 Diskussion In der Behandlung lokal fortgeschrittener oder inflammatorischer Mammakarzinome gilt die neoadjuvante Chemotherapie schon lange als Standard. Dass diese Therapieform in Hinblick auf
Protokol ID: AGO-OVAR OP.4 (AGO DESKTOP OVAR III)
 EINE RANDOMISIERTE, MULTIZENTRISCHE STUDIE ZUM VERGLEICH DER WIRKSAMKEIT EINER ZUSÄTZLICHEN TUMORDEBULKING-OPERATION GEGEN EINE ALLEINIGE CHEMOTHERAPIE BEI PATIENTINNEN MIT EINEM PLATIN-SENSIBLEN OVARIALKARZINOM-REZIDIV
EINE RANDOMISIERTE, MULTIZENTRISCHE STUDIE ZUM VERGLEICH DER WIRKSAMKEIT EINER ZUSÄTZLICHEN TUMORDEBULKING-OPERATION GEGEN EINE ALLEINIGE CHEMOTHERAPIE BEI PATIENTINNEN MIT EINEM PLATIN-SENSIBLEN OVARIALKARZINOM-REZIDIV
Nebenwirkungen der Therapie
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Nebenwirkungen der Therapie Nebenwirkungen der Therapie Version 2004: Jackisch/Göhring/Souchon Version 2005-2008: Friedrichs / Lisboa
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Nebenwirkungen der Therapie Nebenwirkungen der Therapie Version 2004: Jackisch/Göhring/Souchon Version 2005-2008: Friedrichs / Lisboa
GBG 54 - MALE. Eine prospektive, randomisierte, multizentrische Phase II Studie zur Evaluierung der Östradiolsuppression unter Tamoxifen alleine
 GBG 54 - MALE Eine prospektive, randomisierte, multizentrische Phase II Studie zur Evaluierung der Östradiolsuppression unter Tamoxifen alleine versus Tamoxifen plus GnRH-Analogon versus Aromatase-Inhibitor
GBG 54 - MALE Eine prospektive, randomisierte, multizentrische Phase II Studie zur Evaluierung der Östradiolsuppression unter Tamoxifen alleine versus Tamoxifen plus GnRH-Analogon versus Aromatase-Inhibitor
Endokrine Therapie des Mammakarzinoms. Bernd Hanswille Klinikum Dortmund Frauenklinik
 Endokrine Therapie des Mammakarzinoms Bernd Hanswille Klinikum Dortmund Frauenklinik Grundlagen Stufe-3-Leitlinie Brustkrebs-Früherkennung in Deutschland www.senologie.org\leitlinien.html S2/S3-Leitlinie
Endokrine Therapie des Mammakarzinoms Bernd Hanswille Klinikum Dortmund Frauenklinik Grundlagen Stufe-3-Leitlinie Brustkrebs-Früherkennung in Deutschland www.senologie.org\leitlinien.html S2/S3-Leitlinie
Orale Target-Therapie mit dem Tyrosinkinaseinhibitor Sunitinib (Sutent )
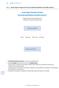 202 Kapitel 18 Nierentumor 18.1.2 Orale Target-Therapie mit dem Tyrosinkinaseinhibitor Sunitinib (Sutent ) Orale Target-Therapie mit dem Tyrosinkinaseinhibitor Sunitinib (Sutent ) Fortgeschrittenes Nierenzellkarzinom
202 Kapitel 18 Nierentumor 18.1.2 Orale Target-Therapie mit dem Tyrosinkinaseinhibitor Sunitinib (Sutent ) Orale Target-Therapie mit dem Tyrosinkinaseinhibitor Sunitinib (Sutent ) Fortgeschrittenes Nierenzellkarzinom
DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen
 DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen Sponsor: Universitätsklinikum Ulm (AöR), Albert-Einstein-Allee 29, 89081
DETECT Studien: Multizentrische Studien bei Patientinnen mit HER2-negativem metastasiertem Brustkrebs und zirkulierenden Tumorzellen Sponsor: Universitätsklinikum Ulm (AöR), Albert-Einstein-Allee 29, 89081
20. Onkologische Konferenz Eisenach. Das Mammakarzinom der älteren und alten Frau
 20. Onkologische Konferenz Eisenach Das Mammakarzinom der älteren und alten Frau Anja Merte Altern ist ein individueller Prozeß, bestimmt durch biologische, soziologische und psychologische Aspekte 3.
20. Onkologische Konferenz Eisenach Das Mammakarzinom der älteren und alten Frau Anja Merte Altern ist ein individueller Prozeß, bestimmt durch biologische, soziologische und psychologische Aspekte 3.
Patienteninformation. zur Teilnahme an
 Prüfstelle: Patienteninformation zur Teilnahme an Randomisierte endokrine Therapieintervention bei postmenopausalen, hormonrezeptorpositiven Patientinnen mit dem Nachweis zirkulierender Tumorzellen im
Prüfstelle: Patienteninformation zur Teilnahme an Randomisierte endokrine Therapieintervention bei postmenopausalen, hormonrezeptorpositiven Patientinnen mit dem Nachweis zirkulierender Tumorzellen im
Adjuvante systemische Therapie des Mammakarzinoms
 Adjuvante systemische Therapie des Mammakarzinoms G. Tschurtschenthaler I. Interne Abteilung Leiter: Univ.Prof.Dr. G. Michlmayr 1 MAMMAKARZINOM Mortalität nach 5 Jahren (%) Tumorgröße (cm) Anzahl der positiven
Adjuvante systemische Therapie des Mammakarzinoms G. Tschurtschenthaler I. Interne Abteilung Leiter: Univ.Prof.Dr. G. Michlmayr 1 MAMMAKARZINOM Mortalität nach 5 Jahren (%) Tumorgröße (cm) Anzahl der positiven
Teil A. 1. Hinweise zur Anwendung von 5-Fluorouracil gemäß Nr. 24
 Stand: 18.04.2007 Beschlüsse zu der Arzneimittel-Richtlinie/ Anlage 9 Off-Label-Use Teil A Folgende Arzneimittel sind unter Beachtung der dazu gegebenen Hinweise in den nachfolgend aufgelisteten nicht
Stand: 18.04.2007 Beschlüsse zu der Arzneimittel-Richtlinie/ Anlage 9 Off-Label-Use Teil A Folgende Arzneimittel sind unter Beachtung der dazu gegebenen Hinweise in den nachfolgend aufgelisteten nicht
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer in der DGGG e.v. sowie Version 2009.1.0 2010.1.0D Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer in der DGGG e.v. sowie Version 2009.1.0 2010.1.0D Neoadjuvante
Projektgruppe Mammakarzinom TZM
 Adjuvante Campus Innenstadt Therapie des Mammakarzinoms & ASCO 2010 Projektgruppe Mammakarzinom TZM 15.7.2010 Brigitte Rack Ludwig-Maximilians-Universität Frauenklinik, Campus Innenstadt Adjuvante Therapie
Adjuvante Campus Innenstadt Therapie des Mammakarzinoms & ASCO 2010 Projektgruppe Mammakarzinom TZM 15.7.2010 Brigitte Rack Ludwig-Maximilians-Universität Frauenklinik, Campus Innenstadt Adjuvante Therapie
APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET
 APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET EUDRACT-NR.: 2010-024238-46 Protokoll-Nr.: D-III Sponsor: Universitätsklinikum Ulm, Albert-Einstein-Allee 29, D-89081 Ulm Wissenschaftliche
APPENDIX I GERMAN PROTOCOL-SYNOPSIS & GERMAN STUDY FLOW SHEET EUDRACT-NR.: 2010-024238-46 Protokoll-Nr.: D-III Sponsor: Universitätsklinikum Ulm, Albert-Einstein-Allee 29, D-89081 Ulm Wissenschaftliche
STUDIENSYNOPSIS. Randomisierte Phase-II-Studie. Art der Studie. Prof. Dr. Volker Heinemann (Leiter der klinischen Prüfung) Studienleitung
 STUDIENSYNOPSIS Randomisierte Studie zur Wirksamkeit von FOLFIRI in Kombination mit Cetuimab vs. Bevacizumab in der Erstlinien-Behandlung des metastasierten kolorektalen Karzinoms mit K- RAS-Wildtyp Art
STUDIENSYNOPSIS Randomisierte Studie zur Wirksamkeit von FOLFIRI in Kombination mit Cetuimab vs. Bevacizumab in der Erstlinien-Behandlung des metastasierten kolorektalen Karzinoms mit K- RAS-Wildtyp Art
1. GELTUNGSBEREICH UND ZWECK:
 COMPREHENSIVE CANCER CENTER VIENNA (Neo)adjuvante systemische Therapie des Mammakarzinoms gültig ab: 21.06.2017 Version: 01 Seite 1 von 6 1. GELTUNGSBEREICH UND ZWECK: AKH MUW Hintergrund: Interdisziplinäre
COMPREHENSIVE CANCER CENTER VIENNA (Neo)adjuvante systemische Therapie des Mammakarzinoms gültig ab: 21.06.2017 Version: 01 Seite 1 von 6 1. GELTUNGSBEREICH UND ZWECK: AKH MUW Hintergrund: Interdisziplinäre
1. Neoadjuvante Therapie. 2. Adjuvante Therapie. 3. Metastasiertes Mamma-Ca. 4. Mamma-Ca. in der Schwangerschaft. 5. Nicht-interventionelle Studien
 1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Adapt-Studie Katherine-Studie TREAT CTC-Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Adapt-Studie Katherine-Studie TREAT CTC-Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
Therapie von Mundhöhlen- und Oropharynx-Karzinomen - Stand der TISOC-1 Studie
 Therapie von Mundhöhlen- und Oropharynx-Karzinomen - Stand der Studie NCT01108042 Studienleiter und Vertreter des Sponsors: Prof. Dr. Orlando Guntinas-Lichius Klinik und Poliklinik für Hals-, Nasen- und
Therapie von Mundhöhlen- und Oropharynx-Karzinomen - Stand der Studie NCT01108042 Studienleiter und Vertreter des Sponsors: Prof. Dr. Orlando Guntinas-Lichius Klinik und Poliklinik für Hals-, Nasen- und
Prüfarztinformation zur Lebensstil-Intervention
 Prüfarztinformation zur Lebensstil-Intervention Studiendesign FLOW-CHART R R LEGENDE Medikamentöse Therapie Chemotherapie Lebensstil-Intervention Interventionsgruppe Telefon basierte Lebensstil-Intervention:
Prüfarztinformation zur Lebensstil-Intervention Studiendesign FLOW-CHART R R LEGENDE Medikamentöse Therapie Chemotherapie Lebensstil-Intervention Interventionsgruppe Telefon basierte Lebensstil-Intervention:
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Versionen 2002 2017: Dall /
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Versionen 2002 2017: Dall /
Dokumentationsbögen für die Lebensqualität
 Dokumentationsbögen für die Lebensqualität Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC-Doc-Chemotherapie versus FED-DocG-Chemotherapie, sowie 2 oder 5 Jahre Zoledronattherapie
Dokumentationsbögen für die Lebensqualität Multizentrische, prospektiv randomisierte Phase III Studie zum Vergleich von FEC-Doc-Chemotherapie versus FED-DocG-Chemotherapie, sowie 2 oder 5 Jahre Zoledronattherapie
Die SUCCESS C Studie. Brigitte Rack. Tumorzentrum München 2. April Frauenklinik Innenstadt Ludwig-Maximilians-Universität München
 Die SUCCESS C Studie Tumorzentrum München 2. April 2009 Brigitte Rack Frauenklinik Innenstadt Ludwig-Maximilians-Universität München SUCCESS-Study Design (Simultaneous Study of Docetaxel-Gemcitabine Combination
Die SUCCESS C Studie Tumorzentrum München 2. April 2009 Brigitte Rack Frauenklinik Innenstadt Ludwig-Maximilians-Universität München SUCCESS-Study Design (Simultaneous Study of Docetaxel-Gemcitabine Combination
Qualitätssicherung am Beispiel Mammakarzinom
 Qualitätssicherung am Beispiel Mammakarzinom Dokumentation der Versorgungsrealität in Onkologischen Praxen in Deutschland Dr. H. W. Tessen, Goslar Sprecher der Projektgruppe Internistische Onkologie Versorgungsforschung
Qualitätssicherung am Beispiel Mammakarzinom Dokumentation der Versorgungsrealität in Onkologischen Praxen in Deutschland Dr. H. W. Tessen, Goslar Sprecher der Projektgruppe Internistische Onkologie Versorgungsforschung
Studiendesign. Gute Gründe für die Teilnahme an den DETECT-Studien
 Studiendesign Gute Gründe für die Teilnahme an den DETECT-Studien NEU: Neue Beurteilung der CTCs in DETECT III (HER2-Positivität von CTCs bei Immunhistochemie 1+, 2+, 3+) NEU: Aufnahme des CDK4/6 Inhibitors
Studiendesign Gute Gründe für die Teilnahme an den DETECT-Studien NEU: Neue Beurteilung der CTCs in DETECT III (HER2-Positivität von CTCs bei Immunhistochemie 1+, 2+, 3+) NEU: Aufnahme des CDK4/6 Inhibitors
PROTOKOLL KURZFASSUNG deutsch
 PROTOKOLL KURZFASSUNG deutsch A multi-national randomized Phase III GCIG Intergroup Study comparing 1 st line chemotherapy with Gemcitabine, Paclitaxel and Carboplatin versus Paclitaxel and Carboplatin
PROTOKOLL KURZFASSUNG deutsch A multi-national randomized Phase III GCIG Intergroup Study comparing 1 st line chemotherapy with Gemcitabine, Paclitaxel and Carboplatin versus Paclitaxel and Carboplatin
Chemotherapie des metastasierten Mammakarzinoms
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie des metastasierten Mammakarzinoms Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie des metastasierten Mammakarzinoms Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Chemotherapie bei metastasiertem Mammakarzinom
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie bei metastasiertem Mammakarzinom Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Chemotherapie bei metastasiertem Mammakarzinom Chemotherapie bei metastasiertem Mammakarzinom Version 2002: von Minckwitz Version 2003
Chronisch myeloproliferative Syndrome - CML-V TIGER
 Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronisch myeloproliferative Syndrome - CML-V TIGER Prüfplancode
Innere Medizin I - Onkologie, Hämatologie, Klinische Infektiologie, Klinische Immunologie, Hämostaseologie, Internistische Intensivmedizin Chronisch myeloproliferative Syndrome - CML-V TIGER Prüfplancode
Metastasiertes kolorektales Karzinom palliative Therapie, 1st-line
 Metastasiertes kolorektales Karzinom palliative Therapie, 1st-line AIO-KRK-0110: Capecitabin plus Bevacizumab versus Capecitabin plus Irinotecan plus Bevacizumab als Erstlinien-Therapie beim metastasierten
Metastasiertes kolorektales Karzinom palliative Therapie, 1st-line AIO-KRK-0110: Capecitabin plus Bevacizumab versus Capecitabin plus Irinotecan plus Bevacizumab als Erstlinien-Therapie beim metastasierten
Anlage 8. Qualitätssicherung. zum Vertrag zur Durchführung des DMP Brustkrebs Berlin
 Anlage 8 Qualitätssicherung zum Vertrag zur Durchführung des DMP Brustkrebs Berlin QS-Ziel QS-Indikator Auslösealgorithmus Angemessener Anteil der Patientinnen Anteil mit brusterhaltender brusterhaltender
Anlage 8 Qualitätssicherung zum Vertrag zur Durchführung des DMP Brustkrebs Berlin QS-Ziel QS-Indikator Auslösealgorithmus Angemessener Anteil der Patientinnen Anteil mit brusterhaltender brusterhaltender
Adjuvante Therapie bei Patienten mit Mammakarzinomen
 Adjuvante Therapie bei Patienten mit Mammakarzinomen Auf der Konsensus-Konferenz in St. Gallen im Februar 2005 wurden die Richtlinien zur adjuvanten Therapie aktualisiert. Es werden wieder drei Gruppen
Adjuvante Therapie bei Patienten mit Mammakarzinomen Auf der Konsensus-Konferenz in St. Gallen im Februar 2005 wurden die Richtlinien zur adjuvanten Therapie aktualisiert. Es werden wieder drei Gruppen
2 Patienten und Methoden
 2 Patienten und Methoden 2.1 Studiendesign Die vorliegende Untersuchung ist eine Therapieoptimierung nach dem Design einer Phase I-Studie der klinischen Arzneimittelprüfung. Es handelt sich um eine therapeutische
2 Patienten und Methoden 2.1 Studiendesign Die vorliegende Untersuchung ist eine Therapieoptimierung nach dem Design einer Phase I-Studie der klinischen Arzneimittelprüfung. Es handelt sich um eine therapeutische
1.4. Protokoll-Synopse
 EudraCT-Nr.: 2005-005473-29 Protokoll Version 2.3 vom 20.12.2006 Seite - 13-1.4. Protokoll-Synopse Protokoll-Nr.: OSHO # 70 (FL-OSHO/GLSG-M3-2005-01) Protokoll-Version und Datum.: 2.3 vom 20.12.2006 Titel
EudraCT-Nr.: 2005-005473-29 Protokoll Version 2.3 vom 20.12.2006 Seite - 13-1.4. Protokoll-Synopse Protokoll-Nr.: OSHO # 70 (FL-OSHO/GLSG-M3-2005-01) Protokoll-Version und Datum.: 2.3 vom 20.12.2006 Titel
Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer AGO e. V. Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer AGO e. V. Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Erste Taxan-basierte Anthrazyklin-freie Chemotherapie
 Erste Taxan-basierte Anthrazyklin-freie Chemotherapie in Kombination mit Herceptin (TCH) für Patientinnen mit HER2-positivem frühem Brustkrebs erhält FDA-Zulassung Edmonton, Kanada (31. Mai 2008, ots/prnewswire)
Erste Taxan-basierte Anthrazyklin-freie Chemotherapie in Kombination mit Herceptin (TCH) für Patientinnen mit HER2-positivem frühem Brustkrebs erhält FDA-Zulassung Edmonton, Kanada (31. Mai 2008, ots/prnewswire)
Anlage 6 zum Vertrag über ein strukturiertes Behandlungsprogramm (DMP) zur Verbesserung der Versorgungssituation von Brustkrebspatientinnen
 Anlage 6 zum Vertrag über ein strukturiertes Behandlungsprogramm (DMP) zur Verbesserung der Versorgungssituation von Brustkrebspatientinnen Die Dokumentation im Rahmen der Strukturierten Behandlungsprogramme
Anlage 6 zum Vertrag über ein strukturiertes Behandlungsprogramm (DMP) zur Verbesserung der Versorgungssituation von Brustkrebspatientinnen Die Dokumentation im Rahmen der Strukturierten Behandlungsprogramme
Primär-systemische Therapie Studien (neo-adjuvante Therapie Studien)
 Übersicht der aktuellen n beim Mamma-Carcinom Stand: Juli 2009 Primär-systemische Therapie n (neo-adjuvante Therapie n) A: Her-2-negativ 4 x EC +/- Bev A1 bei CR/PR 4 x T +/- Bev OP A2 bei NC P weekly
Übersicht der aktuellen n beim Mamma-Carcinom Stand: Juli 2009 Primär-systemische Therapie n (neo-adjuvante Therapie n) A: Her-2-negativ 4 x EC +/- Bev A1 bei CR/PR 4 x T +/- Bev OP A2 bei NC P weekly
Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Operative Therapie des Mammakarzinoms unter onkologischen Aspekten Operative Therapie des Mammakarzinoms unter onkologischen Aspekten
Studienübersicht Brustzentrum Neckar-Donau
 HERA Eine randomisierte, multizentrische Studie zum Vergleich von einem Jahr und 2 Jahren Herceptin gegenüber keinem Herceptin bei Frauen mit Her2- positivem primären Mammakarzinom, die eine adjuvante
HERA Eine randomisierte, multizentrische Studie zum Vergleich von einem Jahr und 2 Jahren Herceptin gegenüber keinem Herceptin bei Frauen mit Her2- positivem primären Mammakarzinom, die eine adjuvante
HECTOR (Hycamtin plus Carboplatin versus Established Regimens for the Treatment of Ovarian Cancer Relapse) EudraCT Number: 2006-004628-34
 Topotecan plus Carboplatin im Vergleich zur Standardtherapie (Paclitaxel plus Carboplatin oder Gemcitabin plus Carboplatin) in der Therapie von Patientinnen mit Platin-sensitivem rezidivierten epithelialen
Topotecan plus Carboplatin im Vergleich zur Standardtherapie (Paclitaxel plus Carboplatin oder Gemcitabin plus Carboplatin) in der Therapie von Patientinnen mit Platin-sensitivem rezidivierten epithelialen
Mammakarzinom. Manual Diagnostik und Therapie. Bearbeitet von Anne Constanze Regierer, Kurt Possinger
 Mammakarzinom Manual Diagnostik und Therapie Bearbeitet von Anne Constanze Regierer, Kurt Possinger 1. Auflage 2005. Taschenbuch. 120 S. Paperback ISBN 978 3 7691 0487 5 Format (B x L): 16,5 x 23,8 cm
Mammakarzinom Manual Diagnostik und Therapie Bearbeitet von Anne Constanze Regierer, Kurt Possinger 1. Auflage 2005. Taschenbuch. 120 S. Paperback ISBN 978 3 7691 0487 5 Format (B x L): 16,5 x 23,8 cm
Brustkrebs Erstdokumentation
 1 DMP-Fallnummer vom Arzt zu vergeben Administrative Daten 2 Krankenkasse bzw. Kostenträger Name der Kasse Name der Kasse 3 Name, Vorname der Versicherten 4 5 6 7 8 9 Geb. am TT.MM.JJ(JJ) TT.MM.JJ(JJ)
1 DMP-Fallnummer vom Arzt zu vergeben Administrative Daten 2 Krankenkasse bzw. Kostenträger Name der Kasse Name der Kasse 3 Name, Vorname der Versicherten 4 5 6 7 8 9 Geb. am TT.MM.JJ(JJ) TT.MM.JJ(JJ)
SABCS 2016 Psychoonkologie und Supportivtherapie
 SABCS 2016 Psychoonkologie und Supportivtherapie Rudolf Weide Praxisklinik für Hämatologie und Onkologie Koblenz Orale Antiemese Randomisierter Vergleich zwischen Granisetron (40ug/kg) an Tag 1 und Palonosetron
SABCS 2016 Psychoonkologie und Supportivtherapie Rudolf Weide Praxisklinik für Hämatologie und Onkologie Koblenz Orale Antiemese Randomisierter Vergleich zwischen Granisetron (40ug/kg) an Tag 1 und Palonosetron
Studienzentrum der Deutschen Gesellschaft für f. SYNCHRONOUS Trial
 Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Studienzentrum der Deutschen Gesellschaft für f Chirurgie SYNCHRONOUS Trial Resection of the primary tumor vs. no resection prior to systemic therapy in patients with colon cancer and synchronous unresectable
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapie Version 2002: Möbus / Nitz Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapie Version 2002: Möbus / Nitz Versionen
Lokal fortgeschrittenes, resektables Adenokarzinom des gastroösophagealen Übergangs oder des Magens
 AIO-STO-0310 Seite 1 of 7 STUDIENSYNOPSE Studientitel Indikation Studientyp Primäres Zielkriterium/Endpunkt Sekundäres Zielkriterium/Endpunkt Multizentrische, explorative Phase II Studie mit perioperativer
AIO-STO-0310 Seite 1 of 7 STUDIENSYNOPSE Studientitel Indikation Studientyp Primäres Zielkriterium/Endpunkt Sekundäres Zielkriterium/Endpunkt Multizentrische, explorative Phase II Studie mit perioperativer
Dokumentation einschließlich der für die Durchführung der Programme erforderlichen personenbezogenen Daten ( 137f Abs. 2 Satz 2 Nr.
 Anlage 7 zum Vertrag ab 01.07.2013 zur Durchführung des strukturierten Behandlungsprogramms nach 137 f SGB V zur Verbesserung der Versorgungssituation von Brustkrebs-Patientinnen - entspricht wörtlich
Anlage 7 zum Vertrag ab 01.07.2013 zur Durchführung des strukturierten Behandlungsprogramms nach 137 f SGB V zur Verbesserung der Versorgungssituation von Brustkrebs-Patientinnen - entspricht wörtlich
ER+, PR+ und Her2/neu-positives Mammakarzinom mit Änderung des Rezeptorstatus
 G. Schaller, München. 03. Juni 2014 ER+, PR+ und Her2/neu-positives Mammakarzinom mit Änderung des Rezeptorstatus Dargestellt wird die Kasuistik einer 57-jährigen Patientin mit einem primär Hormonrezeptorpositiven
G. Schaller, München. 03. Juni 2014 ER+, PR+ und Her2/neu-positives Mammakarzinom mit Änderung des Rezeptorstatus Dargestellt wird die Kasuistik einer 57-jährigen Patientin mit einem primär Hormonrezeptorpositiven
gültig ab: Juli 2008 Version 01 Seite 1 von 9 Hintergrund: Interdisziplinäre Behandlung als Grundlage für Arbeitsabläufe
 VIZEREKTOR FÜR KLINISCHE ANGELEGENHEITEN ÄRZTLICHER DIREKTOR Univ. Prof. Dr. Christoph ZIELINSKI Univ: Prof. Dr. Reinhard KREPLER (Neo)adjuvante systemische Therapie des Mammakarzinom gültig ab: Juli 2008
VIZEREKTOR FÜR KLINISCHE ANGELEGENHEITEN ÄRZTLICHER DIREKTOR Univ. Prof. Dr. Christoph ZIELINSKI Univ: Prof. Dr. Reinhard KREPLER (Neo)adjuvante systemische Therapie des Mammakarzinom gültig ab: Juli 2008
Therapie der älteren Patientin
 Therapie der älteren Patientin P. Wimberger, F. Hilpert Universitätsklinikum Essen Universitätsklinikum Kiel Ovarialkarzinom - State of the Art AGO-Symposium München 20.Juni 2009 Lebenserwartung von Frauen
Therapie der älteren Patientin P. Wimberger, F. Hilpert Universitätsklinikum Essen Universitätsklinikum Kiel Ovarialkarzinom - State of the Art AGO-Symposium München 20.Juni 2009 Lebenserwartung von Frauen
Neoadjuvante (Primäre) systemische Therapie
 Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
Diagnosis Diagnostik and und Treatment Therapie of primärer Patients with und Primary metastasierter and Metastatic Mammakarzinome Breast Cancer Neoadjuvante (Primäre) systemische Therapie Neoadjuvante
1. Neoadjuvante Therapie. 2. Adjuvante Therapie. 3. Metastasiertes Mamma-Ca. 4. Mamma-Ca. in der Schwangerschaft. 5. Nicht-interventionelle Studien
 1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Katherine-Studie TREAT CTC-Studie OLYMPIA Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
1. Neoadjuvante Therapie GeparOcto-Studie Penelope-Studie 2. Adjuvante Therapie GAIN II-Studie Katherine-Studie TREAT CTC-Studie OLYMPIA Studie 3. Metastasiertes Mamma-Ca. First-line Therapie: Ab Second-line
Bisphosphonate und der RANKL-Antikörper Denosumab
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Bisphosphonate und der RANKL-Antikörper Denosumab Bisphosphonate und RANKL-Antikörper Denosumab Versionen bis 2010: Diel / Jackisch /
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Bisphosphonate und der RANKL-Antikörper Denosumab Bisphosphonate und RANKL-Antikörper Denosumab Versionen bis 2010: Diel / Jackisch /
Anlage 7. 2 Kostenträger Name der Krankenkasse. 3 Name des Versicherten Familienname, Vorname
 Anlage 7 zum Vertrag nach 73 a SGB V vom 09.04.2013 zwischen der KVS und den Kassen ( AOK, Knappschaft, IKK, SVLFG und den Ersatzkassen ) im Saarland zur Durchführung des DMP Brustkrebs entspricht wörtlich
Anlage 7 zum Vertrag nach 73 a SGB V vom 09.04.2013 zwischen der KVS und den Kassen ( AOK, Knappschaft, IKK, SVLFG und den Ersatzkassen ) im Saarland zur Durchführung des DMP Brustkrebs entspricht wörtlich
Anlage 9 Qualitätssicherung Stand Version 3.2. Qualitätssicherung Brustkrebs auf Grundlage des Datensatzes gemäß DMP-RL Teil B I Ziffer 5
 Vertrag zum DMP-Brustkrebs vom 30.06.2013 für das Vertragsgebiet Thüringen Seite 1 von 8 Anlage 9 Qualitätssicherung Stand 2012-11-22 Version 3.2 Qualitätssicherung Brustkrebs auf Grundlage des Datensatzes
Vertrag zum DMP-Brustkrebs vom 30.06.2013 für das Vertragsgebiet Thüringen Seite 1 von 8 Anlage 9 Qualitätssicherung Stand 2012-11-22 Version 3.2 Qualitätssicherung Brustkrebs auf Grundlage des Datensatzes
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapie Version 2002: Möbus / Nitz Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapie Version 2002: Möbus / Nitz Versionen
Nebenwirkungen der Therapie
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Nebenwirkungen der Therapie Nebenwirkungen der Therapie Version 2004: Jackisch/Göhring/Souchon Version 2005-2009: Friedrichs / Lisboa
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Nebenwirkungen der Therapie Nebenwirkungen der Therapie Version 2004: Jackisch/Göhring/Souchon Version 2005-2009: Friedrichs / Lisboa
Adjuvante zytostatische und zielgerichtete Therapien
 Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
Diagnostik und Therapie primärer und metastasierter Mammakarzinome Adjuvante zytostatische und zielgerichtete Therapien Adjuvante zytostatische und zielgerichtete Therapien Version 2002: Möbus / Nitz Versionen
1. Vorbemerkung Ziel der vorliegenden Arbeit Das Mammakarzinom Historischer Überblick 2
 INHALTSVERZEICHNIS Seite I. EINLEITUNG 1. Vorbemerkung 1 2. Ziel der vorliegenden Arbeit 1 3. Das Mammakarzinom 2 3.1. Historischer Überblick 2 3.2. Ätiologie 4 3.2.1. Genetische und familiäre Disposition
INHALTSVERZEICHNIS Seite I. EINLEITUNG 1. Vorbemerkung 1 2. Ziel der vorliegenden Arbeit 1 3. Das Mammakarzinom 2 3.1. Historischer Überblick 2 3.2. Ätiologie 4 3.2.1. Genetische und familiäre Disposition
Brustkrebs: Adjuvante Therapie mit Herceptin
 Trastuzumab after adjuvant Chemotherapy in HER2-positive Breast Cancer Piccart-Gebhart et al: New England Journal of Medicine 353 : 1659 72, October 20, 2005. HERA 2-year follow-up of trastuzumab after
Trastuzumab after adjuvant Chemotherapy in HER2-positive Breast Cancer Piccart-Gebhart et al: New England Journal of Medicine 353 : 1659 72, October 20, 2005. HERA 2-year follow-up of trastuzumab after
AGO-OVAR 19 / TRUST. (platinfreies Intervall 6-12 Monate) Intermediär-platinsensibles Rezidiv. Erstdiagnose FIGO IIIB-IV
 Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand juni 2017 Intermediär-platinsensibles Rezidiv (platinfreies
Ovarialkarzinom Aktuelle Studien in der Klinik für Gynäkologie des UKE Kontakt Studiensekretariat: Sylke Krenkel (040/7410-57970, skrenkel@uke.de) Stand juni 2017 Intermediär-platinsensibles Rezidiv (platinfreies
1.4. Protokoll-Synopse
 EudraCT-Nr.: 2005-005473-29 Protokoll Version 2.4 vom 20.7.2009 Seite - 13-1.4. Protokoll-Synopse Protokoll-Nr.: OSHO # 70 (FL-OSHO/GLSG-M3-2005-01) Protokoll-Version und Datum.: 2.4 vom 20.07.2009 Titel
EudraCT-Nr.: 2005-005473-29 Protokoll Version 2.4 vom 20.7.2009 Seite - 13-1.4. Protokoll-Synopse Protokoll-Nr.: OSHO # 70 (FL-OSHO/GLSG-M3-2005-01) Protokoll-Version und Datum.: 2.4 vom 20.07.2009 Titel
Kardio-CT im akuten Koronarsyndrom Gegenwart und Zukun. Hamburg Heart View,
 Kardio-CT im akuten Koronarsyndrom Gegenwart und Zukun. Hamburg Heart View, 05.11.2016 Prof. Dr. Gunnar Lund, Klinik und Poliklinik für diagnostische und interventionelle Radiologie, Universitätskrankenhaus
Kardio-CT im akuten Koronarsyndrom Gegenwart und Zukun. Hamburg Heart View, 05.11.2016 Prof. Dr. Gunnar Lund, Klinik und Poliklinik für diagnostische und interventionelle Radiologie, Universitätskrankenhaus
Studieninitiierungsphase Geplanter Studienstart: 4. Quartal Offene Studien
 Studie Design Rekrutierung Gemeldete Personen BIG 6 13 / D081CC00006 DETECT III A randomised, double blind, parallel group, placebocontrolled multi centre Phase III study to assess the efficacy and safety
Studie Design Rekrutierung Gemeldete Personen BIG 6 13 / D081CC00006 DETECT III A randomised, double blind, parallel group, placebocontrolled multi centre Phase III study to assess the efficacy and safety
GBG Jahrestreffen 2018
 GBG 97- AMICA Antihormonelle Erhaltungstherapie nach First-Line-Chemotherapie mit oder ohne CDK4/6-Inhibitor Ribociclib bei Hormonrezeptorpositivem / HER2 negativem, metastasiertem Brustkrebs: Eine Phase-II-Studie
GBG 97- AMICA Antihormonelle Erhaltungstherapie nach First-Line-Chemotherapie mit oder ohne CDK4/6-Inhibitor Ribociclib bei Hormonrezeptorpositivem / HER2 negativem, metastasiertem Brustkrebs: Eine Phase-II-Studie
Fragebogen Erstvorstellung/Zweitmeinung: Mammakarzinom
 Fragebogen Erstvorstellung/Zweitmeinung: Mammakarzinom Frauenklinik im Nationalen Centrum für Tumorerkrankungen Zertifiziertes Brustzentrum Nachname, Vorname: Geburtsdatum: Letzte Periode: Letzte Krebsvorsorge:
Fragebogen Erstvorstellung/Zweitmeinung: Mammakarzinom Frauenklinik im Nationalen Centrum für Tumorerkrankungen Zertifiziertes Brustzentrum Nachname, Vorname: Geburtsdatum: Letzte Periode: Letzte Krebsvorsorge:
Universität zu Lübeck Institut für Krebsepidemiologie e.v.
 Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Mamma - Karzinom Weniger ist mehr?!
 Gynäkologische Onkologie Mamma - Karzinom Weniger ist mehr?! PD Dr. Brustzentrum Klinik für Gynäkologie und Geburtshilfe Klinikum Frankfurt (Oder) Trend der letzten 40 Jahre Zahl der Brustkrebs- Erkrankungsfälle
Gynäkologische Onkologie Mamma - Karzinom Weniger ist mehr?! PD Dr. Brustzentrum Klinik für Gynäkologie und Geburtshilfe Klinikum Frankfurt (Oder) Trend der letzten 40 Jahre Zahl der Brustkrebs- Erkrankungsfälle
DETECT-STUDIEN: MULTIZENTRISCHE STUDIEN BEI PATIENTINNEN MIT HER2-NEGATIVEM METASTASIERTEM BRUSTKREBS UND ZIRKULIERENDEN TUMORZELLEN (CTCs)
 DEUTSCHES KURZPROTOKOLL DETECT III UND DETECT IV In Kooperation mit Deutsche Gesellschaft für Senologie DETECT-STUDIEN: MULTIZENTRISCHE STUDIEN BEI PATIENTINNEN MIT HER2-NEGATIVEM METASTASIERTEM BRUSTKREBS
DEUTSCHES KURZPROTOKOLL DETECT III UND DETECT IV In Kooperation mit Deutsche Gesellschaft für Senologie DETECT-STUDIEN: MULTIZENTRISCHE STUDIEN BEI PATIENTINNEN MIT HER2-NEGATIVEM METASTASIERTEM BRUSTKREBS
PROTOKOLL SYNOPSE Version 3.1 (Protokollversion 3.1 Amendment 1):
 T-PLL2-Protokoll der Deutschen CLL Studiengruppe (DCLLSG) Phase II Trial of Combined Immunochemotherapy with Fludarabine, Mitoxantrone, Cyclophosphamide and Alemtuzumab (FMC-Alemtuzumab) in Patients with
T-PLL2-Protokoll der Deutschen CLL Studiengruppe (DCLLSG) Phase II Trial of Combined Immunochemotherapy with Fludarabine, Mitoxantrone, Cyclophosphamide and Alemtuzumab (FMC-Alemtuzumab) in Patients with
Palliative Therapie des fortgeschrittenen Mammacarcinoms
 Palliative Therapie des fortgeschrittenen Mammacarcinoms Seminarabend 26.2.2004 E. Rechberger I. Med. Abteilung Prinzipien Mammacarcinom mit Fernmetastasen ist nicht kurativ behandelbar Ziel der Therapie
Palliative Therapie des fortgeschrittenen Mammacarcinoms Seminarabend 26.2.2004 E. Rechberger I. Med. Abteilung Prinzipien Mammacarcinom mit Fernmetastasen ist nicht kurativ behandelbar Ziel der Therapie
Universität zu Lübeck Institut für Krebsepidemiologie e.v.
 Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Universität zu Lübeck Institut für Krebsepidemiologie e.v. Gibt es Unterschiede in der medizinischen Versorgung von Patientinnen und Patienten mit Brustkrebs, Malignem Melanom der Haut oder Prostatakrebs
Antikörpertherapie beim Mammakarzinom
 Antikörpertherapie beim Mammakarzinom (Dr. S. Rückert) Trastuzumab (Herceptin ) ist ein gentechnisch hergestellter Antikörper, welcher gegen das HER2/neu-Protein gerichtet ist. Dieser Wachstumsfaktor kommt
Antikörpertherapie beim Mammakarzinom (Dr. S. Rückert) Trastuzumab (Herceptin ) ist ein gentechnisch hergestellter Antikörper, welcher gegen das HER2/neu-Protein gerichtet ist. Dieser Wachstumsfaktor kommt
Voruntersuchungen. Klinik für Anästhesiologie und Intensivmedizin
 Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Voruntersuchungen ASA Klassifikation Grundlagen für apparative, technische Untersuchungen entscheidende Grundlagen zur Indikation jeder präoperativen technischen Untersuchung: - Erhebung einer sorgfältigen
Die Dokumentation im Rahmen der strukturierten Behandlungsprogramme für Patientinnen mit Brustkrebs erfolgt nach folgenden Vorgaben:
 Brustkrebs - Dokumentation Die Dokumentation im Rahmen der strukturierten Behandlungsprogramme für Patientinnen mit Brustkrebs erfolgt nach folgenden Vorgaben: Brustkrebs Erstdokumentation Lfd. Nr. Dokumentationsparameter
Brustkrebs - Dokumentation Die Dokumentation im Rahmen der strukturierten Behandlungsprogramme für Patientinnen mit Brustkrebs erfolgt nach folgenden Vorgaben: Brustkrebs Erstdokumentation Lfd. Nr. Dokumentationsparameter
Chemotherapie und Antikörpertherapie bei Brustkrebs. Onkologische Gemeinschaftspraxis Siegburg Dr. med. Franz-Josef Heidgen
 Chemotherapie und Antikörpertherapie bei Brustkrebs Onkologische Gemeinschaftspraxis Siegburg Dr. med. Franz-Josef Heidgen Grundlegende Therapieverfahren Operation Chemotherapie und Antikörpertherapie
Chemotherapie und Antikörpertherapie bei Brustkrebs Onkologische Gemeinschaftspraxis Siegburg Dr. med. Franz-Josef Heidgen Grundlegende Therapieverfahren Operation Chemotherapie und Antikörpertherapie
