Materialien für den sprachsensiblen Unterricht Textrekonstruktion: Die Eigenschaften des Wassers
|
|
|
- Linus Gehrig
- vor 7 Jahren
- Abrufe
Transkript
1 Materialien für den sprachsensiblen Unterricht Textrekonstruktion: Die Eigenschaften des Wassers Unterrichtsfach Themenbereich/e Chemie Wasser als ohstoff und Lösungsmittel Schulstufe (Klasse) 8. (4.) Unterrichtseinsatz Sprachliche Kompetenzen Zeitbedarf Material- & Medienbedarf Sozialform/en Methodische Tools Besondere Merkmale und Hinweise zur Durchführung Ersteller/in Erarbeitungsphase oder Wiederholung Erarbeiten von Sachtexten; sprachliche eflexion; Aufbau fachbezogener Sprachkompetenz 1 Unterrichtseinheit Kopierte Arbeitsvorlage; Lehrbuch der Klasse; eventuell Nachschlagswerke und/oder Internetanschluss Schachtel zum Sammeln von Fachbegriffen PartnerInnenarbeit Schnipseltext wird in richtige eiehnfolge gebracht. Langer Liste der Fachbegriffe: Anomalie des Wassers Dipolmoment (polares) Lösungsmittel Oberflächenspannung Schmelzwärme Verdampfungswärme Wärmekapazität Wasserstoffbrücke IFSL-Arbeitsblätter für den sprachsensiblen Unterricht Chemie E. Langer 1/5
2 Arbeitsauftrag Textrekonstruktion: Die Eigenschaften des Wassers Arbeite mit einer Partnerin/einem Partner! Du erhältst einen Text über die besonderen Eigenschaften des Wassers, aber er ist zerschnitten und durcheinander geraten. Bring die Textstreifen in die richtige eihenfolge! Dazu musst du den Text so lesen, dass du auf übereinstimmende Schlüsselworte in verschiedenen Streifen achtest. (Hebe diese Schlüsselworte mit Textmarker hervor). Nummeriere nun die Streifen (mit Bleistift) und lege sie so auf, dass ein zusammenhängender Text entsteht. Klebe den Text dann (nach Überprüfung der eihenfolge durch die Lehrkraft) in dein Heft. Lies ihn dir sorgfältig durch. Ergänze den Text durch Skizzen. Die Textstreifen gehen mitten durch Absätze. Kennzeichne, wo ein neuer Gedankengang beginnt, indem du ein Absatzzeichen ( ) einfügst. Der Text enthält sehr viele (neue) Fachbegriffe. Markiere sie und schreib eine Liste. Kennzeichne jene Begriffe, die deiner Meinung nach im Text ausreichend erklärt sind, mit einem Häkchen. Schreib Begriffe, die du nicht genau verstehst, auf einen Zettel und wirf diesen in die Schachtel auf dem LehrerInnentisch. Zur Klärung aller Begriffe können dann alle SchülerInnen beitragen! (>> Glossar!) Im Folgenden findest du eine eihe von Behauptungen. Vergleiche mit dem Text und markiere die Sätze mit, F oder? richtig; F falsch;? Das geht nicht aus dem Text hervor! Eis hat ein größeres Volumen als flüssiges Wasser. Die Verdampfungswärme von Benzin ist kleiner als die von Wasser. Das Dipolmoment der Wassermoleküle führt zur Bildung von Wasserstoffbrücken. Die Schmelz- und Verdampfungswärme von Wasser sind besonders hoch. Hartes Wasser hat einen hohen Gehalt an Calcium-Salzen. Die Wassermoleküle sind geladen. Für Lösungsmittel gilt: Gegensätze ziehen sich an! Die Schmelz- und die Verdampfungswärme des Wassers beeinflussen das Klima auf der Erde. Der tägliche Wasserverbrauch in Europa beträgt durchschnittlich 150 bis 300 Liter. Die Wärmekapazität ist die Energie, die beim Erwärmen des Wassers abgegeben wird. Die Wassermoleküle sind gewinkelt und haben geladene Enden. IFSL-Arbeitsblätter für den sprachsensiblen Unterricht Chemie E. Langer 2/5
3 Schnipseltext: Die Eigenschaften des Wassers - Anfang Wassermoleküle haben die Formel H 2 O das heißt, sie bestehen aus einem Sauerstoff-Atom (O), das mit 2 Wasserstoff-Atomen (H) verbunden ist. Die Wassermoleküle sind gewinkelt, der von H O H eingeschlossenen Winkel beträgt ca (Zeichne die Strukturformel!) Die Außenelektronen der Atome werden vom O-Atom stärker angezogen als von den H-Atomen. Dadurch hat das Molekül positiv und negativ geladene Enden Das Sauerstoffatom bildet das negative Ende, die Wasserstoff-Atome bilden positive Enden. Die gegensätzlichen Ladungen sind gleich groß, sodass das Molekül insgesamt ungeladen ist. Eine Trennung von positiver und negativer Ladung innerhalb eines Moleküls nennt man ein Dipolmoment Die Wassermoleküle haben also ein Dipolmoment. Man sagt: Wasser ist ein polarer Stoff. Negative Sauerstoff-Enden und positivez Wasserstoff-Enden von benachbarten Molekülen ziehen sich gegenseitig an. So entsteht eine Kraft, die nebeneinander liegende Wasser-Moleküle zusammen hält. Man nennt sie "Wasserstoffbrücke". Die Wasserstoffbrücken halten die Wassermoleküle im festen Aggregatzustand (das heißt im Eis) in einer regelmäßigen Anordnung fest. Dadurch ist der Platzbedarf hoch. (Suche eine entsprechende Abbildung im Lehrbuch oder im Internet!) Zum Schmelzen eines Feststoffes ist immer Energie notwendig, denn die Anziehungskräfte zwischen den Teilchen müssen (zumindest zum Teil) überwunden werden. Diese Energie nennt man die Schmelzwärme. Die Schmelzwärme des Wassers (= Eises) ist besonders hoch, da viele Wasserstoffbrücken aufgebrochen werden müssen. Wenn eine Flüssigkeit verdampft, müssen die noch vorhandenen Anziehungskräfte zwischen den Teilchen gänzlich überwunden werden. Die dafür nötige Energie nennt man die Verdampfungswärme. Auch die Verdampfungswärme des Wassers ist wegen der Wasserstoffbrücken besonders hoch. Wird die Temperatur eines Stoffes erhöht, bewegen sich seine Teilchen schneller. Auch dazu muss man Energie aufwenden. Diese Energie heißt Wärmekapazität. Wasser hat auch eine besonders hohe Wärmekapazität, denn die Wasserstoffbrücken behindern die Bewegung der Moleküle und müssen beim Erwärmen geöffnet werden. An der Wasseroberfläche sind die Dipolkräfte und Wasserstoffbrücken nur nach innen gerichtet. Deshalb hat Wasser eine hohe Oberflächenspannung. (Suche auch dazu eine passende Abbildung!) IFSL-Arbeitsblätter für den sprachsensiblen Unterricht Chemie E. Langer 3/5
4 Die Oberflächenspannung wirkt ähnlich wie eine Haut. Weil die Wasserstoffbrücken im Eis mehr Platz brauchen als im flüssigen Wasser, hat Eis eine geringere Dichte als Wasser. 1 Liter Eis ist also leichter als 1 Liter Wasser bei 4. Das ist sehr ungewöhnlich, denn normaler Weise dehnen sich Stoffe mit steigender Temperatur aus, weil die Wärmebewegung der Teilchen zunimmt. Daher wird der Umstand, dass Eis eine geringere dichte hat als flüssiges Wasser "Anomalie des Wassers" genannt. Eine Flüssigkeit, die imstande ist andere Stoffe aufzulösen, bezeichnet man als Lösungsmittel. Lösungsmittel lösen vor allem solche Stoffe, die einen ähnlichen Aufbau aus Teilchen haben. Wir sagen: "Ähnliches wird von Ähnlichem gelöst". Wasser ist ein polares Lösungsmittel und löst deshalb Stoffe, die ebenfalls polar sind oder aus geladenen Teilchen bestehen. Diese ungewöhnlichen Eigenschaften des Wassers haben viele Folgen für die Natur. Die wichtigsten sind: Die hohe Schmelzwärme des Wassers verhindert, dass der Schnee im Frühjahr so rasch schmilzt, dass es ständig zu Hochwasser und Überschwemmungen kommt. Die hohe Verdampfungswärme und Wärmekapazität des Wassers bewirken, dass es im Frühjahr nicht so schnell heiß wird und im Herbst nicht so rasch abkühlt. Dies gilt besonderes an Gewässern, vor allem am Meer, sodass das Klima dort milder und gleichmäßiger ist. Die hohe Verdampfungswärme bewirkt außerdem, dass unsere Körperoberfläche durch Schwitzen abkühlen kann. Die hohe Oberflächenspannung des Wassers bewirkt, dass Wasser Tropfen bildet und manche Insekten auf der Wasseroberfläche laufen können so z. B. der sogenannte Wasserläufer. Die Anomalie des Wassers bewirkt, dass Eisberge schwimmen und Seen im Winter nicht bis zum Grund zufrieren, sodass die Fische dort überleben können. Wasser ist das wichtigste Lösungs- und Transportmittel im Organismus der meisten Lebewesen, insbesondere im Körper des Menschen. - Ende - IFSL-Arbeitsblätter für den sprachsensiblen Unterricht Chemie E. Langer 4/5
5 Lösungen: Eis hat ein größeres Volumen als flüssiges Wasser. Die Verdampfungswärme von Benzin ist kleiner als die von Wasser.? 1 Das Dipolmoment der Wassermoleküle führt zur Bildung von Wasserstoffbrücken. Die Schmelz- und Verdampfungswärme von Wasser sind besonders hoch. Hartes Wasser hat einen hohen Gehalt an Calcium-Salzen.? Die Wassermoleküle sind geladen. F Für Lösungsmittel gilt: Gegensätze ziehen sich an! F Die Schmelz- und die Verdampfungswärme des Wassers beeinflussen das Klima auf der Erde. Der tägliche Wasserverbrauch in Europa beträgt durchschnittlich 150 bis 300 Liter.? Die Wärmekapazität ist die Energie, die beim Erwärmen des Wassers abgegeben F wird. Die Wassermoleküle sind gewinkelt und haben geladene Enden. 1) Die mit? gekennzeichneten Aussagen sind grundsätzlich richtig. Abbildungen: Watermolecule.svg.png IFSL-Arbeitsblätter für den sprachsensiblen Unterricht Chemie E. Langer 5/5
VORANSICHT I/C. Die Anomalie des Wassers. Der Beitrag im Überblick. 14. Die Anomalie des Wassers 1 von 18. Günther Lohmer, Leverkusen
 14. Die Anomalie des Wassers 1 von 18 Die Anomalie des Wassers Günther Lohmer, Leverkusen Wie können Fische im Winter überleben, obwohl der See zugefroren ist? 1 Warum platzen Wasserflaschen im Gefrierschrank?
14. Die Anomalie des Wassers 1 von 18 Die Anomalie des Wassers Günther Lohmer, Leverkusen Wie können Fische im Winter überleben, obwohl der See zugefroren ist? 1 Warum platzen Wasserflaschen im Gefrierschrank?
Stationenbetrieb DBW. 8. Januar 2011
 Stationenbetrieb DBW 8. Januar 2011 1 Station I AUFGABE. Welche Einheit gehört zu welcher Größe? Schreibe den richtigen Buchstaben hinter jeder Einheit: A B C D E F G H Volumen Länge Zeit Beschleunigung
Stationenbetrieb DBW 8. Januar 2011 1 Station I AUFGABE. Welche Einheit gehört zu welcher Größe? Schreibe den richtigen Buchstaben hinter jeder Einheit: A B C D E F G H Volumen Länge Zeit Beschleunigung
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
Ägypten Das Land am Nil
 Ägypten Das Land am Nil Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Zeitbedarf Material- und Medienbedarf Sozialform/en Methodische
Ägypten Das Land am Nil Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Zeitbedarf Material- und Medienbedarf Sozialform/en Methodische
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Kinetische Energie der Moleküle / Aggregatzustand
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
Das ist ja nicht normal!
 1 Das ist ja nicht normal! Warum bekommen Straßen ständig neue Schlaglöcher? Warum geht eine Wasserflasche kaputt, wenn sie vollgefüllt ins Tiefkühlfach liegt? Warum schwimmt Eis auf Wasser? Und warum
1 Das ist ja nicht normal! Warum bekommen Straßen ständig neue Schlaglöcher? Warum geht eine Wasserflasche kaputt, wenn sie vollgefüllt ins Tiefkühlfach liegt? Warum schwimmt Eis auf Wasser? Und warum
Die 3 Stoffklassen der Elemente
 Die Art der Bindung hängt davon ab, wie stark die Atome ihre Valenzelektronen anziehen. Elektronegativität (Abb. 17, S. 114) Qualitative Angabe, wie stark die Atomrümpfe die Elektronen in der Valenzschale
Die Art der Bindung hängt davon ab, wie stark die Atome ihre Valenzelektronen anziehen. Elektronegativität (Abb. 17, S. 114) Qualitative Angabe, wie stark die Atomrümpfe die Elektronen in der Valenzschale
Posten 1a. Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? Antworten: a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k)
 Posten 1a Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k) d) (=> Posten 13f) Posten 1d Welcher der beiden Stoffe hat den tieferen Siedepunkt?
Posten 1a Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k) d) (=> Posten 13f) Posten 1d Welcher der beiden Stoffe hat den tieferen Siedepunkt?
Zustandsänderungen. Physik
 Zustandsänderungen Aufgabe 1 Du hast schon vielerlei Erfahrungen mit dem lebensnotwendigen Wasser gemacht. In welchen Zustandsformen (Aggregatzuständen) ist dir Wasser bekannt? fest dick schön rot eckig
Zustandsänderungen Aufgabe 1 Du hast schon vielerlei Erfahrungen mit dem lebensnotwendigen Wasser gemacht. In welchen Zustandsformen (Aggregatzuständen) ist dir Wasser bekannt? fest dick schön rot eckig
Gruppenarbeit : Zwischenmolekulare Kräfte
 Expertengruppe A Zwischenmolekulare Kräfte Allgemeines Zwischenmolekulare Kräfte dürfen nicht mit der Kovalenzbindung verwechselt werden. Bei der Kovalenzbindung geht es um Kräfte innerhalb der Moleküle
Expertengruppe A Zwischenmolekulare Kräfte Allgemeines Zwischenmolekulare Kräfte dürfen nicht mit der Kovalenzbindung verwechselt werden. Bei der Kovalenzbindung geht es um Kräfte innerhalb der Moleküle
Titel: Themenkreis Wasser
 Titel: Themenkreis Wasser 1 Kurzbeschreibung: In dieser Unterrichtseinheit werden Möglichkeiten aufgezeigt, chemische und physikalische Eigenschaften des Wassers im naturwissenschaftlichen Unterricht zu
Titel: Themenkreis Wasser 1 Kurzbeschreibung: In dieser Unterrichtseinheit werden Möglichkeiten aufgezeigt, chemische und physikalische Eigenschaften des Wassers im naturwissenschaftlichen Unterricht zu
Aggregatzustände (Niveau 1)
 Aggregatzustände (Niveau 1) 1. Wasser kann verschiedene Zustandsformen haben, die sogenannten Aggregatzustände. Im Frühjahr kannst du die verschiedenen Aggregatzustände beobachten. Ergänze im Text die
Aggregatzustände (Niveau 1) 1. Wasser kann verschiedene Zustandsformen haben, die sogenannten Aggregatzustände. Im Frühjahr kannst du die verschiedenen Aggregatzustände beobachten. Ergänze im Text die
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Die Anomalie des Wassers. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Das komplette Material finden Sie hier: School-Scout.de 14. 1 von 18 Günther Lohmer, Leverkusen Wie können Fische im Winter überleben,
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Das komplette Material finden Sie hier: School-Scout.de 14. 1 von 18 Günther Lohmer, Leverkusen Wie können Fische im Winter überleben,
Die Heizungsanlage eines Hauses wird auf Ölfeuerung umgestellt. Gleichzeitig wird mit dieser Anlage Warmwasser aufbereitet.
 Übungsaufgaben zur Wärmelehre mit Lösungen 1) Die Heizungsanlage eines Hauses wird auf Ölfeuerung umgestellt. Gleichzeitig wird mit dieser Anlage Warmwasser aufbereitet. Berechnen Sie die Wärme, die erforderlich
Übungsaufgaben zur Wärmelehre mit Lösungen 1) Die Heizungsanlage eines Hauses wird auf Ölfeuerung umgestellt. Gleichzeitig wird mit dieser Anlage Warmwasser aufbereitet. Berechnen Sie die Wärme, die erforderlich
Schätzfragen Wasser. Wasser allgemein Trinkwasser Wasserkreislauf - Flüsse Wasser, Tiere, Pflanzen
 Wasser Wasser allgemein Trinkwasser Wasserkreislauf - Flüsse Wasser, Tiere, Pflanzen 1 Wasser allgemein Die Erde heißt blauer Planet weil sie...??? a) bis zur Hälfte mit Wasser bedeckt ist b) zu drei Viertel
Wasser Wasser allgemein Trinkwasser Wasserkreislauf - Flüsse Wasser, Tiere, Pflanzen 1 Wasser allgemein Die Erde heißt blauer Planet weil sie...??? a) bis zur Hälfte mit Wasser bedeckt ist b) zu drei Viertel
Kantonsschule Freudenberg. Chemie. Aufgaben zum Grundlagenfach. Übungen zum Unterricht von A. Bärtsch
 Kantonsschule Freudenberg Chemie Aufgaben zum Grundlagenfach Übungen zum Unterricht von A. Bärtsch Dez. 2013 Inhalt 1. Atombau 2. Radioaktivität 3. Kovalente Bindungen 4. Salze 5. Polarität und zwischenmolekulare
Kantonsschule Freudenberg Chemie Aufgaben zum Grundlagenfach Übungen zum Unterricht von A. Bärtsch Dez. 2013 Inhalt 1. Atombau 2. Radioaktivität 3. Kovalente Bindungen 4. Salze 5. Polarität und zwischenmolekulare
Atome so klein und doch so wichtig
 Atome so klein und doch so wichtig Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Chemie Atombau und Periodensystem 8 (4. Klasse)
Atome so klein und doch so wichtig Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Chemie Atombau und Periodensystem 8 (4. Klasse)
WasserKreuzworträtsel
 Das Element Wasser Das Element Wasser ARBEITSBLATT WasserKreuzworträtsel Teste dein WasserWissen! Um dir etwas zu helfen, haben wir dir ein paar Buchstaben bereits richtig eingesetzt. Tipp: Bei der WasserWerkstatt
Das Element Wasser Das Element Wasser ARBEITSBLATT WasserKreuzworträtsel Teste dein WasserWissen! Um dir etwas zu helfen, haben wir dir ein paar Buchstaben bereits richtig eingesetzt. Tipp: Bei der WasserWerkstatt
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
PHYSIKTEST 3C Dezember 2015 GRUPPE A
 PHYSIKTEST 3C Dezember 2015 GRUPPE A SCHÜLERNAME: PUNKTEANZAHL: /20 NOTE: NOTENSCHLÜSSEL 18-20 Sehr Gut (1) 15-17 Gut (2) 13-14 Befriedigend (3) 10-12 Genügend (4) 0-9 Nicht Genügend (5) Aufgabe 1. (3
PHYSIKTEST 3C Dezember 2015 GRUPPE A SCHÜLERNAME: PUNKTEANZAHL: /20 NOTE: NOTENSCHLÜSSEL 18-20 Sehr Gut (1) 15-17 Gut (2) 13-14 Befriedigend (3) 10-12 Genügend (4) 0-9 Nicht Genügend (5) Aufgabe 1. (3
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium
 Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Sprachliche Kompetenzen Zeitbedarf Material- & Medienbedarf
Reaktionsgleichungen verstehen anhand der Verbrennung von Magnesium Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Sprachliche Kompetenzen Zeitbedarf Material- & Medienbedarf
Wasser löst fast alles
 1 Wasser löst fast alles In manchen Regionen ist das Wasser ganz schön hart. Nicht, dass Steine aus der Dusche fallen, wie in diesem Cartoon; aber durch Verdunsten oder Verdampfen von Wasser können Ablagerungen
1 Wasser löst fast alles In manchen Regionen ist das Wasser ganz schön hart. Nicht, dass Steine aus der Dusche fallen, wie in diesem Cartoon; aber durch Verdunsten oder Verdampfen von Wasser können Ablagerungen
Lineare Gleichungssysteme mit zwei Variablen, lineare Funktionen. Zeit-Weg-Diagramme, Textgleichungen
 MATHEMATIK Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Sprachliche Kompetenzen Zeitbedarf Material- und Medienbedarf Sozialform/en Methodische Tools Hinweise zur Durchführung
MATHEMATIK Unterrichtsfach Themenbereich/e Schulstufe (Klasse) Fachliche Vorkenntnisse Sprachliche Kompetenzen Zeitbedarf Material- und Medienbedarf Sozialform/en Methodische Tools Hinweise zur Durchführung
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
I. Chemische Bindung und Zwischenmolekulare Kräfte
 I. Chemische Bindung und Zwischenmolekulare Kräfte MINT-UNTERRICHTSEINHEIT A. Ausgangslage Die klare Unterscheidung der chemischen Bindung- und der Zwischenmolekularen Kräfte und die korrekte Zuordnung
I. Chemische Bindung und Zwischenmolekulare Kräfte MINT-UNTERRICHTSEINHEIT A. Ausgangslage Die klare Unterscheidung der chemischen Bindung- und der Zwischenmolekularen Kräfte und die korrekte Zuordnung
Unterstreiche in jedem Satz Subjekt, Prädikat und Objekt: Der Froschkönig. In den alten Zeiten lebte ein König. Er hatte mehrere Töchter.
 Unterstreiche in jedem Satz Subjekt, Prädikat und Objekt: Der Froschkönig In den alten Zeiten lebte ein König. Er hatte mehrere Töchter. Aber seine jüngste Tochter war am schönsten. Diese Prinzessin besaß
Unterstreiche in jedem Satz Subjekt, Prädikat und Objekt: Der Froschkönig In den alten Zeiten lebte ein König. Er hatte mehrere Töchter. Aber seine jüngste Tochter war am schönsten. Diese Prinzessin besaß
Flüssigkeitsthermometer Bimetallthermometer Gasthermometer Celsius Fahrenheit
 Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Physik kompetenzorientiert: Wärmelehre 2
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Physik kompetenzorientiert: Wärmelehre 2 Das komplette Material finden Sie hier: Download bei School-Scout.de Ausdehnung von Körpern
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Physik kompetenzorientiert: Wärmelehre 2 Das komplette Material finden Sie hier: Download bei School-Scout.de Ausdehnung von Körpern
Wasser ein besonderer Stoff
 IfU Wasser ein besonderer Stoff Wolfgang Kinzelbach Institut für Umweltingenieurwissenschaft ETH Zürich Email: kinzelbach@ifu.baug.ethz.ch Das Wassermolekül Zusammensetzung H 2 O Molekül insgesamt neutral,
IfU Wasser ein besonderer Stoff Wolfgang Kinzelbach Institut für Umweltingenieurwissenschaft ETH Zürich Email: kinzelbach@ifu.baug.ethz.ch Das Wassermolekül Zusammensetzung H 2 O Molekül insgesamt neutral,
Energie und Energieerhaltung. Mechanische Energieformen. Arbeit. Die goldene Regel der Mechanik. Leistung
 - Formelzeichen: E - Einheit: [ E ] = 1 J (Joule) = 1 Nm = 1 Energie und Energieerhaltung Die verschiedenen Energieformen (mechanische Energie, innere Energie, elektrische Energie und Lichtenergie) lassen
- Formelzeichen: E - Einheit: [ E ] = 1 J (Joule) = 1 Nm = 1 Energie und Energieerhaltung Die verschiedenen Energieformen (mechanische Energie, innere Energie, elektrische Energie und Lichtenergie) lassen
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Temperatur und Wärme - Stationenlernen
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Temperatur und Wärme - Stationenlernen Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Stationenlernen: Temperatur
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Temperatur und Wärme - Stationenlernen Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Stationenlernen: Temperatur
2.2 Spezifische und latente Wärmen
 1 Einleitung Physikalisches Praktikum für Anfänger - Teil 1 Gruppe 2 Wärmelehre 2.2 Spezifische und latente Wärmen Die spezifische Wärme von Wasser gibt an, wieviel Energie man zu 1 kg Wasser zuführen
1 Einleitung Physikalisches Praktikum für Anfänger - Teil 1 Gruppe 2 Wärmelehre 2.2 Spezifische und latente Wärmen Die spezifische Wärme von Wasser gibt an, wieviel Energie man zu 1 kg Wasser zuführen
Wie stelle ich Kärtchen her, auf denen hinten die Lösung aufgedruckt ist?
 Wie stelle ich Kärtchen her, auf denen hinten die Lösung aufgedruckt ist? 1. Fragen- und Lösungsblätter ausdrucken! 3. Von beiden Blättern den Rand abschneiden! 2. Jeweiliges Lösungsblatt zum richtigen
Wie stelle ich Kärtchen her, auf denen hinten die Lösung aufgedruckt ist? 1. Fragen- und Lösungsblätter ausdrucken! 3. Von beiden Blättern den Rand abschneiden! 2. Jeweiliges Lösungsblatt zum richtigen
1 2 Unterrichtseinheiten à 50 Minuten. Plakate, Schnipseltext im Kuvert und Lösung, vorgegebene Begriffe für den Cluster
 Unterrichtsfach/ Lehrplanbezug Physik Schulstufe 7 Thema Fachliche Vorkenntnisse Fachliche Kompetenzen Gewitter und Blitze Kompetenzen mit Verweis zum Kompetenzmodell Naturwissenschaften 8. Schulstufe.
Unterrichtsfach/ Lehrplanbezug Physik Schulstufe 7 Thema Fachliche Vorkenntnisse Fachliche Kompetenzen Gewitter und Blitze Kompetenzen mit Verweis zum Kompetenzmodell Naturwissenschaften 8. Schulstufe.
Mathematik und angewandte Mathematik 1. HAK (1. Jahrgang) 1. AUL (1. Jahrgang) Mathematik und angewandte Mathematik 1. HLW (1.
 Unterrichtsfach Lehrplan HAK: Mathematik und angewandte Mathematik 1. HAK (1. Jahrgang) 1. AUL (1. Jahrgang) Lehrplan HLW: Mathematik und angewandte Mathematik 1. HLW (1. Jahrgang) Lehrplan HTL: Mathematik
Unterrichtsfach Lehrplan HAK: Mathematik und angewandte Mathematik 1. HAK (1. Jahrgang) 1. AUL (1. Jahrgang) Lehrplan HLW: Mathematik und angewandte Mathematik 1. HLW (1. Jahrgang) Lehrplan HTL: Mathematik
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Meine eigene
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Meine eigene
02. Was kann man über die Teilchen eines schmelzenden Stoffes aussagen?
 01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
Auftragskarte für das Lernangebot: Die Zustandsarten des Wassers
 Die Zustandsarten des Wassers - Schere - Kleber - 1 AB Die Zustandsarten des Wassers - 1 AB mit Wörtern zum Ausschneiden Schneide die Wortkärtchen aus Lege sie an die richtige Stelle auf dem Arbeitsblatt
Die Zustandsarten des Wassers - Schere - Kleber - 1 AB Die Zustandsarten des Wassers - 1 AB mit Wörtern zum Ausschneiden Schneide die Wortkärtchen aus Lege sie an die richtige Stelle auf dem Arbeitsblatt
Staunen, was die Natur aus Wasser zaubert : Raureif, Eisblumen, Eiszapfen, Wolken, Nebel, Tau
 Wasser Nicht alle haben alles erlebt! Die Schule hat sich auf den Weg gemacht, aber das Ziel noch lange nicht erreicht. Die Anhänge bieten einen Überblick über die Arbeit einer ganzen Schule während eines
Wasser Nicht alle haben alles erlebt! Die Schule hat sich auf den Weg gemacht, aber das Ziel noch lange nicht erreicht. Die Anhänge bieten einen Überblick über die Arbeit einer ganzen Schule während eines
Element. Verbindung. Reinstoff. Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
John Daltons Atomhypothese. 1. Wie kommt Dalton auf die Atomhypothese? a. Die Eigenschaften des Wassers
 John Daltons Atomhypothese 1. Wie kommt Dalton auf die Atomhypothese? a. Die Eigenschaften des Wassers 2. Welche Aussagen trifft Dalton mit Hilfe des Atommodells? A. Verhalten von Stoffen bei chem. Reaktionen
John Daltons Atomhypothese 1. Wie kommt Dalton auf die Atomhypothese? a. Die Eigenschaften des Wassers 2. Welche Aussagen trifft Dalton mit Hilfe des Atommodells? A. Verhalten von Stoffen bei chem. Reaktionen
Unterrichtskonzept zum Themenbereich Wasser (NT 5.1.2)
 Staatsinstitut für Schulqualität und Bildungsforschung Unterrichtskonzept zum Themenbereich Wasser (NT 5.1.2) Lehrplanbezug Beim Themenbereich Wasser sollen die Schülerinnen und Schüler die drei Aggregatzustände
Staatsinstitut für Schulqualität und Bildungsforschung Unterrichtskonzept zum Themenbereich Wasser (NT 5.1.2) Lehrplanbezug Beim Themenbereich Wasser sollen die Schülerinnen und Schüler die drei Aggregatzustände
Alle Stoffe bestehen aus Teilchen (= Moleküle) Kohäsion (= Zusammenhaltskraft)! gleiche Moleküle. Anziehungskräfte zwischen Teilchen von
 DAS TEILCHENMODELL Zustandsform Adhäsion (= Haftkraft) fest! verschiedene Moleküle flüssig gasförmig Alle Stoffe bestehen aus Teilchen (= Moleküle) Diffusion (= Durchmischung) Kohäsion (= Zusammenhaltskraft)!
DAS TEILCHENMODELL Zustandsform Adhäsion (= Haftkraft) fest! verschiedene Moleküle flüssig gasförmig Alle Stoffe bestehen aus Teilchen (= Moleküle) Diffusion (= Durchmischung) Kohäsion (= Zusammenhaltskraft)!
Arbeitsblatt Wasserkreislauf der Erde
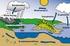 Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Voraussetzungen für das Zustandekommen eines Kaufvertrages
 Unterrichtsfach Betriebswirtschaft (1. Jahrgang HAK); Lehrplan HAK/HAS: Schulstufe 9 Betriebswirtschaft, Wirtschaftliches Rechnen, Rechnungswesen (BWRR) 1. HAS Betriebswirtschaftliche Übungen einschließlich
Unterrichtsfach Betriebswirtschaft (1. Jahrgang HAK); Lehrplan HAK/HAS: Schulstufe 9 Betriebswirtschaft, Wirtschaftliches Rechnen, Rechnungswesen (BWRR) 1. HAS Betriebswirtschaftliche Übungen einschließlich
Eigenschaften von Wasser Oberflächenspannung
 Eigenschaften von Wasser Oberflächenspannung Deine Aufgabe ist es, den Mitschülern deiner Stammgruppe das Phänomen der Oberflächenspannung des Wassers zu erklären. Informiere dich zunächst in deinem Chemiebuch
Eigenschaften von Wasser Oberflächenspannung Deine Aufgabe ist es, den Mitschülern deiner Stammgruppe das Phänomen der Oberflächenspannung des Wassers zu erklären. Informiere dich zunächst in deinem Chemiebuch
oder 10 = 1bar = = 10 Pa Für viele Zwecke wird die Umrechnung 1bar = 10 verwendet.
 R. Brinkmann http://brinkmann-du.de Seite 1 5.11.013 HF14S Arbeitsblatt Wärme als Energieform Die Celsius-Skala ist durch folgende Fixpunkte definiert: 0 0 C: Schmelzpunkt des Eises bei einem Druck von
R. Brinkmann http://brinkmann-du.de Seite 1 5.11.013 HF14S Arbeitsblatt Wärme als Energieform Die Celsius-Skala ist durch folgende Fixpunkte definiert: 0 0 C: Schmelzpunkt des Eises bei einem Druck von
2. Chemische Bindungen 2.1
 2. Chemische Bindungen 2.1 Chemische Bindungen Deutung von Mischungsversuchen Benzin und Wasser mischen sich nicht. Benzin ist somit eine hydrophobe Flüssigkeit. Auch die Siedepunkte der beiden Substanzen
2. Chemische Bindungen 2.1 Chemische Bindungen Deutung von Mischungsversuchen Benzin und Wasser mischen sich nicht. Benzin ist somit eine hydrophobe Flüssigkeit. Auch die Siedepunkte der beiden Substanzen
1.9. Zwischenmolekulare Kräfte
 1.9. Zwischenmolekulare Kräfte 1.9.1. Schmelzen und Verdampfen von Stoffen fester Zustand geordnetes Kristallgitter Teilchen schwingen um Ruhelage flüssiger Zustand Teilchen sind im Tropfen frei beweglich
1.9. Zwischenmolekulare Kräfte 1.9.1. Schmelzen und Verdampfen von Stoffen fester Zustand geordnetes Kristallgitter Teilchen schwingen um Ruhelage flüssiger Zustand Teilchen sind im Tropfen frei beweglich
Wasservorkommen der Erde
 Woher und wofür? Ich weiss, wie das Wasservorkommen auf der Erde verteilt ist Ich weiss, wie das Wasservorkommen in der Schweiz verteilt ist Blauer Planet - und doch Wassermangel? Regen und andere Niederschläge
Woher und wofür? Ich weiss, wie das Wasservorkommen auf der Erde verteilt ist Ich weiss, wie das Wasservorkommen in der Schweiz verteilt ist Blauer Planet - und doch Wassermangel? Regen und andere Niederschläge
Naturwissenschaft Vermutungswissen Alles ist Chemie!!! Analyse Synthese
 SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
Staatsexamen Physikdidaktik Unterrichtsfach (nicht vertieft) Frühjahr 2010, Aufgabe 1: Spezifische Wärmekapazität
 Staatsexamen Physikdidaktik Unterrichtsfach (nicht vertieft) Frühjahr 2010, Aufgabe 1: Spezifische Wärmekapazität 1. Erläutern Sie die Begriffe innere Energie, Wärme, Wärmeleitung und spezifische Wärme
Staatsexamen Physikdidaktik Unterrichtsfach (nicht vertieft) Frühjahr 2010, Aufgabe 1: Spezifische Wärmekapazität 1. Erläutern Sie die Begriffe innere Energie, Wärme, Wärmeleitung und spezifische Wärme
Kernaussagen zum Teilchenmodell
 Kernaussagen zum Teilchenmodell Lernbereich 2: Stoffe und ihre Eigenschaften Von beobachtbaren Stoffeigenschaften zum Teilchenmodell Kompetenzerwartung 8 (NTG) und 9 (SG): Die Schülerinnen und Schüler
Kernaussagen zum Teilchenmodell Lernbereich 2: Stoffe und ihre Eigenschaften Von beobachtbaren Stoffeigenschaften zum Teilchenmodell Kompetenzerwartung 8 (NTG) und 9 (SG): Die Schülerinnen und Schüler
Sicher experimentieren
 Sicher experimentieren A1 Das Experimentieren im Labor kann gefährlich sein. Deswegen muss man sich an Regeln im Labor halten. Lies dir die 6 wichtigsten Regeln im Labor durch. 1. Kein Essen und Trinken
Sicher experimentieren A1 Das Experimentieren im Labor kann gefährlich sein. Deswegen muss man sich an Regeln im Labor halten. Lies dir die 6 wichtigsten Regeln im Labor durch. 1. Kein Essen und Trinken
Lineare Gleichungen in einer Variablen
 Unterrichtsfach Lehrplan HAK: Mathematik und angewandte Mathematik 1. HAK (1. Jahrgang) 1. AUL (1. Jahrgang) Lehrplan HLW: Mathematik und angewandte Mathematik 1. HLW (1. Jahrgang) Lehrplan HTL: Mathematik
Unterrichtsfach Lehrplan HAK: Mathematik und angewandte Mathematik 1. HAK (1. Jahrgang) 1. AUL (1. Jahrgang) Lehrplan HLW: Mathematik und angewandte Mathematik 1. HLW (1. Jahrgang) Lehrplan HTL: Mathematik
Zustandsänderungen. fest dick schön
 Aufgabe 1: Zustandsänderungen Du hast schon vielerlei Erfahrungen mit dem lebensnotwendigen Wasser gemacht. In welchen Zustandsformen (Aggregatzuständen) ist dir Wasser bekannt? Kreuze an! fest dick schön
Aufgabe 1: Zustandsänderungen Du hast schon vielerlei Erfahrungen mit dem lebensnotwendigen Wasser gemacht. In welchen Zustandsformen (Aggregatzuständen) ist dir Wasser bekannt? Kreuze an! fest dick schön
Grundwissen Chemie 8. Klasse NTG
 Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Lösungsbeispiel Oberflächenspannung. Schwimmende Büroklammer
 Lösungsbeispiel Oberflächenspannung Schwimmende Büroklammer Svens Klasse geht einmal im Monat in ein Schülerlabor, um Versuche zu Themen durchzuführen, die im Unterricht theoretisch behandelt wurden. Im
Lösungsbeispiel Oberflächenspannung Schwimmende Büroklammer Svens Klasse geht einmal im Monat in ein Schülerlabor, um Versuche zu Themen durchzuführen, die im Unterricht theoretisch behandelt wurden. Im
Das sind vielleicht Zustände!
 1 Das sind vielleicht Zustände! Wasser ist der einzige Stoff auf unserem Planeten, der in drei verschiedenen Formen, sogenannten Aggregatszuständen, vorkommt: fest, flüssig und gasförmig. Das heißt, Wasser
1 Das sind vielleicht Zustände! Wasser ist der einzige Stoff auf unserem Planeten, der in drei verschiedenen Formen, sogenannten Aggregatszuständen, vorkommt: fest, flüssig und gasförmig. Das heißt, Wasser
Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag
 2.1.1 Aufbau der Materie (Arbeitsaufträge) Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag 1. Beim Bearbeiten
2.1.1 Aufbau der Materie (Arbeitsaufträge) Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag 1. Beim Bearbeiten
NH 3. CCl 4 CO 2. Lösungen zur Lernzielkontrolle Sekunda. Hilfsmittel: PSE, Taschenrechner
 Lösungen zur Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (1) 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) leitfähig,
Lösungen zur Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (1) 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) leitfähig,
Der demografische Übergang und die Bevölkerungspyramide
 Unterrichtsfach/ Lehrplanbezug Schulstufe Thema Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Geographie und Wirtschaftskunde Bevölkerung und Gesellschaft: Die Dynamik der Weltbevölkerung
Unterrichtsfach/ Lehrplanbezug Schulstufe Thema Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Geographie und Wirtschaftskunde Bevölkerung und Gesellschaft: Die Dynamik der Weltbevölkerung
WASSER. Station 1. com. N Arbeitsblatt
 Station 1 Du brauchst einen Kübel gefüllt mit etwas Wasser und die verschiedenen Materialien aus der Liste. Lege die Gegenstände einzeln ins Wasser und überprüfe, do sie auf der Oberfläche schwimmen oder
Station 1 Du brauchst einen Kübel gefüllt mit etwas Wasser und die verschiedenen Materialien aus der Liste. Lege die Gegenstände einzeln ins Wasser und überprüfe, do sie auf der Oberfläche schwimmen oder
Polare Bindungen. Die Elektronen eines bindenden. Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich
 Moleküle Polare Bindungen Die Elektronen eines bindenden (gemeinsamen) Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich zwischen den beiden Atomkernen der Bindungspartner
Moleküle Polare Bindungen Die Elektronen eines bindenden (gemeinsamen) Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich zwischen den beiden Atomkernen der Bindungspartner
Klausur : Allgemeine und Anorganische Chemie. Name...Fachrichtung... Matr.-Nr...
 Klausur : Allgemeine und Anorganische Chemie Mo. 1.03.11 : 13.30 16.30 Uhr 1 Beantworten Sie maximal zehn Fragen. Für jede Frage gibt es maximal 10 Punkte; die Klausur gilt als bestanden, wenn 50 Punkte
Klausur : Allgemeine und Anorganische Chemie Mo. 1.03.11 : 13.30 16.30 Uhr 1 Beantworten Sie maximal zehn Fragen. Für jede Frage gibt es maximal 10 Punkte; die Klausur gilt als bestanden, wenn 50 Punkte
(c) Schulbedarfszentrum
 für die 7. Schulstufe Theoretischer Teil Wärmekapazität Elektrische Ladung Lückentexte Quiz Experimente Wärme und Temperatur Metalle Druck Das Ohm sche Gesetz Wissensüberprüfungen Merktexte Denkaufgaben
für die 7. Schulstufe Theoretischer Teil Wärmekapazität Elektrische Ladung Lückentexte Quiz Experimente Wärme und Temperatur Metalle Druck Das Ohm sche Gesetz Wissensüberprüfungen Merktexte Denkaufgaben
Kompetenzen laut Kompetenzmodell Naturwissenschaften 8. Schulstufe
 Unterrichtsfach/ Lehrplanbezug Physik Schulstufe 6 Thema Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Kompetenzen laut Kompetenzmodell Naturwissenschaften 8. Schulstufe Inhaltsdimension:
Unterrichtsfach/ Lehrplanbezug Physik Schulstufe 6 Thema Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Kompetenzen laut Kompetenzmodell Naturwissenschaften 8. Schulstufe Inhaltsdimension:
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen!
 1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
Die drei Aggregatzustände - Erklärung
 2.1.3 - Die drei Aggregatzustände - Erklärung VERSUCH 1 - DIE WASSERPISTOLE Versuchsdurchführung: Die Wasserpistole (Bild 4) wird zum einerseits mit Wasser und andererseits mit Luft gefüllt. Anschließend
2.1.3 - Die drei Aggregatzustände - Erklärung VERSUCH 1 - DIE WASSERPISTOLE Versuchsdurchführung: Die Wasserpistole (Bild 4) wird zum einerseits mit Wasser und andererseits mit Luft gefüllt. Anschließend
Wasser Stoff und Lebensraum
 NAWI-Forscherheft: Wasser Stoff und Lebensraum Klasse 5 6 Niveau Haupt- und Realschule Fachinhalte erarbeiten Fachsprache üben Katja Hagenmüller Silvija Markic Katja Hagenmüller, Silvija Markic NAWI-Forscherheft:
NAWI-Forscherheft: Wasser Stoff und Lebensraum Klasse 5 6 Niveau Haupt- und Realschule Fachinhalte erarbeiten Fachsprache üben Katja Hagenmüller Silvija Markic Katja Hagenmüller, Silvija Markic NAWI-Forscherheft:
Aufgabe: Erkläre folgende Tatsache mit Hilfe des Teilchenmodells! An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen.
 An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen. Bei einem Flüssigkeitsthermometer kann die Temperatur an der Höhe des Flüssigkeitsstandes im Röhrchen abgelesen werden. 1827
An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen. Bei einem Flüssigkeitsthermometer kann die Temperatur an der Höhe des Flüssigkeitsstandes im Röhrchen abgelesen werden. 1827
FOS: Radioaktivität und Strahlenschutz. Chemische Elemente und ihre kleinsten Teilchen
 R. Brinkmann http://brinkmann-du.de Seite 5..03 Chemische Elemente FOS: Radioaktivität und Strahlenschutz Chemische Elemente und ihre kleinsten Teilchen Der Planet Erde besteht aus 9 natürlich vorkommenden
R. Brinkmann http://brinkmann-du.de Seite 5..03 Chemische Elemente FOS: Radioaktivität und Strahlenschutz Chemische Elemente und ihre kleinsten Teilchen Der Planet Erde besteht aus 9 natürlich vorkommenden
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Experiment Nr. 1: Wasser hat eine Haut. 1. Lege das Seidenpapier vorsichtig auf die Wasseroberfläche.
 Experiment Nr. 1: Wasser hat eine Haut Siehe Pädagogische Unterlagen, Seite 6, 1: Was ist Wasser? Wasser hat eine erhöhte Oberflächenspannung ein Glas, mit Wasser gefüllt Nadel Büroklammer ein kleines
Experiment Nr. 1: Wasser hat eine Haut Siehe Pädagogische Unterlagen, Seite 6, 1: Was ist Wasser? Wasser hat eine erhöhte Oberflächenspannung ein Glas, mit Wasser gefüllt Nadel Büroklammer ein kleines
Diffusion und Osmose. Osmose 1
 Osmose 1 Diffusion und Osmose In flüssigen oder gasförmigen Medien sind die Moleküle in ständiger Bewegung. Sie bewegen sich gradlinig, bis sie auf ein anderes Molekül stossen. Diese Bewegung führt mit
Osmose 1 Diffusion und Osmose In flüssigen oder gasförmigen Medien sind die Moleküle in ständiger Bewegung. Sie bewegen sich gradlinig, bis sie auf ein anderes Molekül stossen. Diese Bewegung führt mit
Bestandteile des Atoms Lehrerinformation
 Lehrerinformation 1/7 Arbeitsauftrag Ziel Material Sozialform Die SuS lesen die Informationstexte. Als Verständnishilfe verwenden sie gleichzeitig das Arbeitsblatt Leitfragen zum Text. Anschliessend zeichnen
Lehrerinformation 1/7 Arbeitsauftrag Ziel Material Sozialform Die SuS lesen die Informationstexte. Als Verständnishilfe verwenden sie gleichzeitig das Arbeitsblatt Leitfragen zum Text. Anschliessend zeichnen
Fachrichtung Klima- und Kälteanlagenbauer
 Fachrichtung Klima- und Kälteanlagenbauer 1-7 Schüler Datum: 1. Titel der L.E. : 2. Fach / Klasse : Fachrechnen, 3. Ausbildungsjahr 3. Themen der Unterrichtsabschnitte : 1. Zustandsänderung 2. Schmelzen
Fachrichtung Klima- und Kälteanlagenbauer 1-7 Schüler Datum: 1. Titel der L.E. : 2. Fach / Klasse : Fachrechnen, 3. Ausbildungsjahr 3. Themen der Unterrichtsabschnitte : 1. Zustandsänderung 2. Schmelzen
Versuch 1. Ist Luft ein Körper?
 LUFT Versuch 1 Ist Luft ein Körper? 1. 2. 3. Nimm zuerst das Wasserglas und fülle es bis zum Rand voll mit Wasser. Lege nun vorsichtig ein Blatt Papier über den Rand. Drehe das Glas über dem Waschbecken
LUFT Versuch 1 Ist Luft ein Körper? 1. 2. 3. Nimm zuerst das Wasserglas und fülle es bis zum Rand voll mit Wasser. Lege nun vorsichtig ein Blatt Papier über den Rand. Drehe das Glas über dem Waschbecken
Grundwissen Physik (8. Klasse)
 Grundwissen Physik (8. Klasse) 1 Energie 1.1 Energieerhaltungssatz 1.2 Goldene egel der Mechanik Energieerhaltungssatz: n einem abgeschlossenen System ist die Gesamtenergie konstant. Goldene egel der Mechanik:
Grundwissen Physik (8. Klasse) 1 Energie 1.1 Energieerhaltungssatz 1.2 Goldene egel der Mechanik Energieerhaltungssatz: n einem abgeschlossenen System ist die Gesamtenergie konstant. Goldene egel der Mechanik:
Bohrsches Atommodell
 Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
Lösungen, Stoffmengen und Konzentrationen
 12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
2. Unterrichtseinheit zum Thema Aggregatzustände: Aggregatzustände und ihre Übergänge Übertragung auf den Wasserkreislauf
 Unterrichtsentwurf 2. Unterrichtseinheit zum Thema Aggregatzustände: Aggregatzustände und ihre Übergänge Übertragung auf den Wasserkreislauf 2. Doppelstunde: Was passiert mit verdunstetem Wasser? Untersuchungen
Unterrichtsentwurf 2. Unterrichtseinheit zum Thema Aggregatzustände: Aggregatzustände und ihre Übergänge Übertragung auf den Wasserkreislauf 2. Doppelstunde: Was passiert mit verdunstetem Wasser? Untersuchungen
Einsatz im Unterricht. Material Arbeitsblatt mit Filmleiste zur Influenz und Arbeitsaufträgen Demonstrationsexperiment zur Influenz
 1 2 3 4 5 6 7 BSP. Filmleiste Erprobung von Josef Leisen EINSATZ Klassenstufe: 9 Schulform: Gymnasium Sozialform: Alle Sozialformen sind möglich und sinnvoll. Unterrichsthema: Elektrizitätslehre der Sekundarstufe
1 2 3 4 5 6 7 BSP. Filmleiste Erprobung von Josef Leisen EINSATZ Klassenstufe: 9 Schulform: Gymnasium Sozialform: Alle Sozialformen sind möglich und sinnvoll. Unterrichsthema: Elektrizitätslehre der Sekundarstufe
AQUA michel.roggo.photographie
 AQUA michel.roggo.photographie - 13.06.2017-26.01.2018 1. Experimente Experiment Nr. 1: Wasser hat eine Haut Anleitung Du brauchst: ein Glas, mit Wasser gefüllt Nadel Büroklammer ein kleines Stück Seidenpapier
AQUA michel.roggo.photographie - 13.06.2017-26.01.2018 1. Experimente Experiment Nr. 1: Wasser hat eine Haut Anleitung Du brauchst: ein Glas, mit Wasser gefüllt Nadel Büroklammer ein kleines Stück Seidenpapier
Passive Transportvorgänge
 Passive Transportvorgänge Diffusion und Osmose sind passive Transportprozesse. Denn die Zelle muss keine Energie aufwenden, um den Transport der Stoffe zu ermöglichen. Diffusion Einzelsubstanzen sind bestrebt,
Passive Transportvorgänge Diffusion und Osmose sind passive Transportprozesse. Denn die Zelle muss keine Energie aufwenden, um den Transport der Stoffe zu ermöglichen. Diffusion Einzelsubstanzen sind bestrebt,
Entwicklung der Weltbevölkerung Arbeiten mit einer Grafik
 Unterrichtsfach Schulstufe Themen Fachliche Vorkenntnisse Sprachliche Kompetenzen Geographie und Wirtschaftskunde 9/10 (1. Klasse AHS, 2. Klasse HAK) Bevölkerung global Entwicklung der Weltbevölkerung
Unterrichtsfach Schulstufe Themen Fachliche Vorkenntnisse Sprachliche Kompetenzen Geographie und Wirtschaftskunde 9/10 (1. Klasse AHS, 2. Klasse HAK) Bevölkerung global Entwicklung der Weltbevölkerung
10. UNTERRICHTSTUNDE: DIE KLIMATA DER USA / DIE MERKMALE DER VERSCHIEDENEN KLIMAZONEN
 10. UNTERRICHTSTUNDE 119 10. UNTERRICHTSTUNDE: DIE KLIMATA DER USA / DIE MERKMALE DER VERSCHIEDENEN KLIMAZONEN Ziele: Die Schüler sollen die verschiedenen Klimazonen in den USA erkennen. Materialien: Fotokopien,
10. UNTERRICHTSTUNDE 119 10. UNTERRICHTSTUNDE: DIE KLIMATA DER USA / DIE MERKMALE DER VERSCHIEDENEN KLIMAZONEN Ziele: Die Schüler sollen die verschiedenen Klimazonen in den USA erkennen. Materialien: Fotokopien,
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid
 Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
8 Teilchenbewegung und Temperatur(movimiento (el) de partículas y
 8 Teilchenbewegung und Temperatur Hofer 1 8 Teilchenbewegung und Temperatur(movimiento (el) de partículas y temperatura, la) 8.1 Molekularkräfte (fuerza (la) intermolecular) A1: Wiederhole, die vier fundamental
8 Teilchenbewegung und Temperatur Hofer 1 8 Teilchenbewegung und Temperatur(movimiento (el) de partículas y temperatura, la) 8.1 Molekularkräfte (fuerza (la) intermolecular) A1: Wiederhole, die vier fundamental
VORANSICHT I/A. Zaubern mit Wasserstoffbrücken oder: Warum sich Wasser so verrückt verhält. Hintergrundinformationen. Ann-Kathrin Wolf, Oldenburg
 18. Warum sich Wasser so verrückt verhält 1 von 22 Zaubern mit Wasserstoffbrücken oder: Warum sich Wasser so verrückt verhält Ann-Kathrin Wolf, Oldenburg Niveau: Sek. I, Klasse 10 Dauer: 4 Unterrichtsstunden
18. Warum sich Wasser so verrückt verhält 1 von 22 Zaubern mit Wasserstoffbrücken oder: Warum sich Wasser so verrückt verhält Ann-Kathrin Wolf, Oldenburg Niveau: Sek. I, Klasse 10 Dauer: 4 Unterrichtsstunden
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Eine Luftsprudelanlage gegen Eis einsetzen
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Eine Luftsprudelanlage gegen Eis einsetzen Das komplette Material finden Sie hier: School-Scout.de 15. Eine Luftsprudelanlage gegen
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Eine Luftsprudelanlage gegen Eis einsetzen Das komplette Material finden Sie hier: School-Scout.de 15. Eine Luftsprudelanlage gegen
Grundwissen Chemie 8I
 1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann und dessen Teilchen(Atome oder Moleküle) aus einer einzigen Atomart (d.h. Teilchen mit gleicher Ordnungszahl) besteht. Verbindung Reinstoff,
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann und dessen Teilchen(Atome oder Moleküle) aus einer einzigen Atomart (d.h. Teilchen mit gleicher Ordnungszahl) besteht. Verbindung Reinstoff,
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate
 Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate Zeitbedarf für die Versuchsdurchführung: ca. 10 Min. Geräte: Magnetrührer mit Magnetrührstäbchen Thermometer (min. 0,5 C Genauigkeit)
Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate Zeitbedarf für die Versuchsdurchführung: ca. 10 Min. Geräte: Magnetrührer mit Magnetrührstäbchen Thermometer (min. 0,5 C Genauigkeit)
