Herstellung von Titan
|
|
|
- Ingeborg Frauke Geier
- vor 7 Jahren
- Abrufe
Transkript
1
2 Inhaltsverzeichnis Vorwort 1 Herstellung von Titantetrachlorid Herstellung von Titanschwamm Umschmelzen 3.1 Verdichten von Titanschwamm Umschmelzen im Vakuumlichtbogenofen...7 Stoffbezeichnungen...9 Verfasser: Andy Reiche
3 Vorwort Titan wurde erstmals 1791 in titanhaltigem Eisensand in oxidischer Form durch den englischen Landgeistlichen William Gregor ( ) in einem Tal des Manaccan in der Grafschaft Cornwall im südwestlichen England gefunden und nach dem Fundort Manaccanit benannt analysierte der Deutsche Martin Heinrich Klapproth ( ) in Berlin ungarische Mineralien und fand eine Titanverbindung in eisenhaltigem Rutil. Diese benannte er nach den Titanen, den Söhnen von Uranus (Gott des Himmels) und Gää (Göttin der Erde) und gab dem Element Titan damit seinen heutigen Namen. In den nächsten Jahren versuchten sich viele Chemiker daran, völlig reines Titan herzustellen. J. J. Berzelius ( ) stellte aus Titandioxid schon 1825 durch Reduktion mit Natrium unreines, metallisches Titan her. Erst 1910 reduzierte der Amerikaner M. A. Hunter Titantetrachlorid mit Hilfe von Natrium zu Titan mit einem Reinheitsgrad von 99,9%. Die industrielle Produktion wurde ab 1938 durch das von W. Kroll entwickelte Verfahren ermöglicht, das aber erst seit 1946 großtechnisch angewendet werden kann. 1
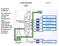
4 1. Herstellung von Titantetrachlorid Zur Herstellung von Titanschwamm wird Titantetrachlorid benötigt. Dieses wird durch Chlorierung und anschließende Destillation von natürlichem und synthetischem Rutil und Titanschlacke hergestellt. Der Vorteil von Chloriden im Vergleich zu Oxiden besteht darin, dass sie früher sieden, und sich somit besser von anderen Substanzen abtrennen. Deswegen chloriert man den TiO 2 Rohstoff und trennt die Destillationskolonnen vom TiCl 4. Bild 1 zeigt Diesen Prozess im Überblick. Titanschlacke natürl. Rutil syntehet. Rutil Bild: 1 Elektrolyse Cl 2 O 2, Luft Chlorierung o C Kohle TiCl 4 Ouensche/Abscheiden/ Kühler CO, CO 2, COS SiO 2, FeCl 3, MgCl 2, CaCl 2 1.Destillation < 136 o C SiCl 4, SnCl 4, CrO 2 Cl 2 H 2 S Cu-Pulver Reaktor/ Abscheider VOCl 2 2.Destillation >136 o C FeCl 3, MnCl 2, AlCl 3, VCl 4 TiCl 4-1 -
5 Die Chlorierung im Wirbelschichtreaktor erfolgt bei Temperaturen zwischen 930 und 980 o C. Da bei steigender Temperatur im zunehmenden Maße Kohlenmonoxid aus Kohlendioxid und Kohlenstoff entsteht, muss zusammen mit Chlor auch Luft oder reiner Sauerstoff eingeblasen werden. So kann die benötigte Reaktionstemperatur erreicht werden. Aus dem Wirbelschichtreaktor tritt das Titantetrachlorid gasförmig aus und wird in einer Gaskühlung, auf etwa 145 o C abgekühlt. Die Gaskühlung erfolgt entweder indirekt über Wärmetauscherflächen oder direkt durch Quenchen mit umlaufendem Roh-TiCl 4. Die Austrittstemperatur aus der Gaskühlung muss so eingestellt werden, dass das zur Kühlung zurückgeführte flüssige TiCl 4 wieder verdampft und gasförmig ausgetragen wird. Im Anschluss folgt der zweite Schritt, die Destillation, welche in zwei Stufen durchgeführt wird. In der ersten Destillationsstufe werden die Verunreinigungen SiCl 4, SnCl 4 und CrO 2 Cl 2 mit einem Siedepunkt unterhalb von 136 o C abgetrennt. Da der Siedepunkt von VOCl 3 nur eine Differenz von 9 o C zum Siedepunkt des TiCl 4 aufweist, ist eine vollständige Abtrennung ohne größere Verluste an TiCl 4 nur durch einen separaten Schritt zu erreichen. Das VOCl 3 wird unter Einsatz von H 2 S und Cu- Pulver als Katalysatoren zu VOCl 3 reduziert und abgeschieden. In der zweiten Destillationsstufe werden die Verunreinigungen FeCl 3, MnCl 2, AlCl 3, und VCl 4 mit einem Siedepunkt von über 136 o C entfernt. Das TiCl 4, das die zweite Destillationsstufe verlässt, hat eine Reinheit von über 99,9%. 2. Herstellung von Titanschwamm Titanschwamm wird aus dem Titantetrachlorid in der industriellen Produktion meist durch das Kroll-Verfahren hergestellt. Titan wird mit Hilfe von Magnesium vom Chlor getrennt. Der gesamte Kroll-Prozess ist in Bild 2 in der Übersicht dargestellt. Die Reduktion des TiCl 4 erfolgt unter Argon als inertem Schutzgas, da das Titan als relativ unedles Metall eine hohe Affinität zu den atmosphärischen Gasen besitzt. Das Verfahren wird in einem aus Stahl oder Chrom-Nickel-Stahl bestehendem Reaktor - 2 -
6 durchgeführt, dessen Innenwände sauber gebürstet sein muss. Je nach Größe des Reaktors werden 1,5 bis 7 t Titanschwamm pro Charge erzeugt. Bild: 2 Zu Beginn des Prozesses wird Magnesium in diesem Reaktor eingeschmolzen. Bei einer Temperatur von 700 o C wird das TiCl 4 dann kontinuierlich über mehrere Tage eingetropft oder gasförmig von oben in den Reaktor zugeführt. Das entstehende Magnesiumchlorid ist flüssig und sinkt aufgrund seiner höheren Dichte gegenüber dem Titan und Magnesium auf den Reaktorboden. Das flüssige MgCl 2 sammelt sich daher unter der Magnesiumschmelze und kann diskontinuierlich abgezogen werden. Der Titanschwamm hingegen schlägt sich am Reaktor nieder und bildet oberhalb der Magnesiumschmelze eine feste Kruste. Das Magnesium steigt auf Grund der Kapillarwirkung durch den porösen Titanschwamm an dessen Oberfläche und reagiert dort weiter mit dem gasförmigen TiCl 4. Ist das zu Beginn in den Reaktor eingefüllte Magnesium verbraucht, wird die TiCl 4 -Zufuhr gestoppt. Anschließend muss der Titanschwamm von Magnesium- und MgCl 2 -Resten gereinigt werden. Dieser Prozess erfolgt heute meistens durch die in Bild 3 dargestellte Vakuumdestillation
7 Bild: 3 Hierbei wird eine Vakuumglocke auf den Reduktionsreaktor aufgesetzt, die über eine Vakuumleitung mit einem zweiten Reaktor in Verbindung steht. Während der Reduktion war die Verbindungsleitung zwischen den beiden Reaktoren getrennt. Es wird sowohl im Reduktions- wie auch im Destillationsreaktor ein Vakuum von etwa 10-3 mbar und eine Temperatur zwischen 900 und 1000 o C erzeugt. Bei diesen Bedingungen gehen die Verunreinigungen ( FeCl 3, vor allem MgCl 2 und TiCl 2 sowie Magnesium) in den gasförmigen Zustand über. Sie werden in den zweiten Destillationsreaktor, der als Kondensator dient, übertragen und kondensieren dort, während der Titanschwamm gereinigt im Reduktionsreaktor zurückbleibt. Kondensiertes Magnesium und MgCl 2 bilden im Kondensator zwei getrennte Phasen, so dass beides getrennt entfern werden kann. Der Schwammkuchen (Bild 4) hat ein Gewicht von 4 t. Er wird mechanisch aus dem Reaktor entfernt und anschließend zerkleinert, wie in Bild 5 gezeigt
8 Bild: 4 Bild: 5 Zunächst werden in der Grobstufe mit Hilfe einer Guillotine grobe Stücke vom Schwammkuchen abgetrennt. Diese groben Bruchstücke werden anschließend in der Feinstufe zwischen rotierenden Walzen zerkleinert. Der in Bild 6 zu sehende Titanschwamm mit einer Dichte von 1,2-3 g/cm 3 dient als Ausgangsbasis für die Herstellung von Halbzeugen auf Titanbasis, aber auch für die Auflegierung von Titanstabilisierten Edelstahlsorten
9 Bild: 6 3 Umschmelzen Da der Schwamm noch Reste von Verunreinigungen aus der Magnesiumreduktion enthält und wegen der Porosität des Schwammes ist ein Umschmelzen notwendig. Dieser Schmelzvorgang beseitigt außerdem die leicht flüchtigen Reduktionsrückstände, wie zum Beispiel Chloride, und ermöglicht die Zugabe von Legierungselementen. 3.1 Verdichten von Titanschwamm Dazu wird der Schwamm zuerst in einer Presse vorverdichtet (Bild 7). Es entstehen so genannte Compacts, aus denen die zur Schmelze vorgesehenen Elektroden zusammengesetzt werden. Diese Compacts können die für Titanlegierungen erforderlichen Legierungselemente oder auch Kleine Schrottstücke Beigemengt werden. Bild: 7-6 -
10 Wegen der hohen Sauerstoffanffinität des Titans werden die Compacts in einer Plasmaschweissanlage unter einer Argon-Schutzgasatmosphäre zur Elektrode zusammengefügt. Dies ist erforderlich, damit sich das beim Schweißen auf über Schmelztemperatur erhitzte Titan nicht mit dem Luftsauerstoff zu TiO 2 verbindet. 3.2 Umschmelzen im Vakuumlichtbogenofen Die verschweißte Elektrode wird in einem Vakuumlichtbogenofen mindestens zwei mal umgeschmolzen. Die Prinzipskizze in Bild 8 zeigt den Aufbau eines solchen Ofens. Bild: 8 Zwischen der Elektrode und dem wassergekühlten Tiegelboden wird ein Lichtbogen gezündet. Durch diesen Lichtbogen schmilzt die Selbstverzehrende Elektrode ab und bildet im Vakuum des Tiegels den gewünschten Block
11 Bild 9 zeigt einen Vakuumlichtbogenofen VAR in Betrieb. Bild10 zeigt die Titan-Blöcke, zweifach im VAR umgeschmolzen. Bild: 9 Bild:
12 Stoffbezeichnungen Auluminiumchlorid = AlCl 3 Calciumchlorid = CaCl 2 Chromylchlorid = CrO 2 Cl 2 Clohr = Cl 2 Eisenchlorid = FeCl 3 Hydrochlorid = HCl Kohlendioxid = CO 2 Kohlenoxid = CO Kupfer = Cu Magnesium = Mg Magnesiumchlorid = MgCl 2 Manganchlorid = MnCl 2 Sauerstoff = O 2 Siliciumdioxid (Quarz, Flint) = SiO 2 Siliciumtetrachlorid = SiCl 4 Titan = Ti Titanchlorid = TiCl 2 Titandioxid = TiO 2 Titantetrachlorid = TiCl 4 Vanadiumtetrachlorid = VCl 4 Vanadiumoxidchlorid = VOCl 3 Wasser = H 2 O Wasserstoffschwefel = H 2 S Zinntetrachlorid = SnCl 4-9 -
Gewinnung und Reinigung der Übergangsmetalle. Von Sebastian Kreft
 Übergangsmetalle Von Sebastian Kreft Übersicht Gewinnung und Raffination von: 1. Scandium 2. Titan 3. Vanadium 4. Chrom 5. Mangan 6. Eisen 7. Cobalt 8. Nickel 9. Kupfer 10. Zink Übergangsmetalle 2 1. Scandium
Übergangsmetalle Von Sebastian Kreft Übersicht Gewinnung und Raffination von: 1. Scandium 2. Titan 3. Vanadium 4. Chrom 5. Mangan 6. Eisen 7. Cobalt 8. Nickel 9. Kupfer 10. Zink Übergangsmetalle 2 1. Scandium
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung
 Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung Chemische Bindungen in Metallen, Elektronengasmodell, elektronische Bänder, Bandstrukturmodell, Metalle, Halbleiter, Isolatoren, Bandlücke,
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung Chemische Bindungen in Metallen, Elektronengasmodell, elektronische Bänder, Bandstrukturmodell, Metalle, Halbleiter, Isolatoren, Bandlücke,
Titandioxid TiO 2. Herstellung und Verwendung. Vortrag von Vera Mans
 Titandioxid TiO 2 Herstellung und Verwendung Inhalt Eigenschaften Vorkommen und Aufbereitung Herstellung Nach dem Chloridverfahren Nach dem Sulfatverfahren Verwendung Quellen Eigenschaften des TiO 2 3
Titandioxid TiO 2 Herstellung und Verwendung Inhalt Eigenschaften Vorkommen und Aufbereitung Herstellung Nach dem Chloridverfahren Nach dem Sulfatverfahren Verwendung Quellen Eigenschaften des TiO 2 3
2 Titan, Rhenium und Ruthenium
 2 Titan, Rhenium und Ruthenium Die Substrate für das Titanoxidwachstum sollten neben den metallischen folgende Eigenschaften aufweisen: geringe Mischbarkeit mit Titan und gute Gitteranpassung für bestimmte
2 Titan, Rhenium und Ruthenium Die Substrate für das Titanoxidwachstum sollten neben den metallischen folgende Eigenschaften aufweisen: geringe Mischbarkeit mit Titan und gute Gitteranpassung für bestimmte
Vom Quarz zum hochreinen Silicium
 Vom Quarz zum hochreinen Silicium Inhalt I. Vorkommen von Silicium II. Industrielle Verwendung III. Isolierung und Reinigung 1. Technische Darstellung 2. Reinstdarstellung 3. Einkristallzucht IV. Zusammenfassung
Vom Quarz zum hochreinen Silicium Inhalt I. Vorkommen von Silicium II. Industrielle Verwendung III. Isolierung und Reinigung 1. Technische Darstellung 2. Reinstdarstellung 3. Einkristallzucht IV. Zusammenfassung
WH-Klausur : Allgemeine und Anorganische Chemie
 WH-Klausur : Allgemeine und Anorganische Chemie Di. 24.03.09 : 13.30-16.30 Uhr 1 1. Isotopensymbole (z.b. 19 9 F) sind wie folgt zu interpretieren: oben links, Massenzahl; unten links, Kernladungszahl.
WH-Klausur : Allgemeine und Anorganische Chemie Di. 24.03.09 : 13.30-16.30 Uhr 1 1. Isotopensymbole (z.b. 19 9 F) sind wie folgt zu interpretieren: oben links, Massenzahl; unten links, Kernladungszahl.
KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor
 1 KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor 2 INHALTSVERZEICHNIS "METALLE" 1. Einleitung...03 2. Reaktionen von Metallen... 05 3. Gewinnung von Metallen... 07 4. Domino: Eigenschaften der
1 KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor 2 INHALTSVERZEICHNIS "METALLE" 1. Einleitung...03 2. Reaktionen von Metallen... 05 3. Gewinnung von Metallen... 07 4. Domino: Eigenschaften der
Die chemische Reaktion
 Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Aus den beiden Ausgangsstoffen (Edukten) entsteht ein neuer Stoff (Produkt) mit eigenen,
Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Aus den beiden Ausgangsstoffen (Edukten) entsteht ein neuer Stoff (Produkt) mit eigenen,
Müller-Rochow-Synthese
 Müller- Folie 1 Einleitung Reaktion Fließbild Produktzusammensetzung Destillation Silicone Zusammenfassung Quellen Folie 2 Müller- = Herstellung von Methylchlorsilanen erstmalig 1940 Dichlordimethylsilan
Müller- Folie 1 Einleitung Reaktion Fließbild Produktzusammensetzung Destillation Silicone Zusammenfassung Quellen Folie 2 Müller- = Herstellung von Methylchlorsilanen erstmalig 1940 Dichlordimethylsilan
Aufgaben zur Elektrolyse
 Aufgaben zur Elektrolyse TechGymJ2 1. Allgemeine Aufgaben (einige davon sind Klausuraufgaben vergangener Jahre) 1.1. Kupfer wird elektrolytisch aus Cu 2+ -Ionen gewonnen. In einer Elektrolysezelle wird
Aufgaben zur Elektrolyse TechGymJ2 1. Allgemeine Aufgaben (einige davon sind Klausuraufgaben vergangener Jahre) 1.1. Kupfer wird elektrolytisch aus Cu 2+ -Ionen gewonnen. In einer Elektrolysezelle wird
Wasserstoff. Helium. Bor. Kohlenstoff. Standort: Name: Ordnungszahl: Standort: Name: Ordnungszahl: 18. Gruppe. Standort: Ordnungszahl: Name:
 H Wasserstoff 1 1. Gruppe 1. Periode He Helium 2 18. Gruppe 1. Periode B Bor 5 13. Gruppe C Kohlenstoff 6 14. Gruppe N Stickstoff 7 15. Gruppe O Sauerstoff 8 16. Gruppe Ne Neon 10 18. Gruppe Na Natrium
H Wasserstoff 1 1. Gruppe 1. Periode He Helium 2 18. Gruppe 1. Periode B Bor 5 13. Gruppe C Kohlenstoff 6 14. Gruppe N Stickstoff 7 15. Gruppe O Sauerstoff 8 16. Gruppe Ne Neon 10 18. Gruppe Na Natrium
Fossile Rohstoffe. Erdöl
 Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Elektroschlackeschmelzen von aluminothermisch hergestellten Titan- Aluminiumlegierungen eine Alternative zum Kroll Prozess?
 Elektroschlackeschmelzen von aluminothermisch hergestellten Titan- Aluminiumlegierungen eine Alternative zum Kroll Prozess? B. Friedrich und J. Hammerschmidt Titanbedarf der Automobilindustrie Chancen
Elektroschlackeschmelzen von aluminothermisch hergestellten Titan- Aluminiumlegierungen eine Alternative zum Kroll Prozess? B. Friedrich und J. Hammerschmidt Titanbedarf der Automobilindustrie Chancen
Holzkohle, Koks, Ruß. Raphael Mehlich
 Holzkohle, Koks, Ruß Raphael Mehlich Inhaltsangabe: Holzkohle: 1. Geschichtliches 2. Herstellung 3. Eigenschaften & Verwendung Koks 1. Geschichtliches 2. Herstellung 3. Nebenprodukte 4. Eigenschaften 5.
Holzkohle, Koks, Ruß Raphael Mehlich Inhaltsangabe: Holzkohle: 1. Geschichtliches 2. Herstellung 3. Eigenschaften & Verwendung Koks 1. Geschichtliches 2. Herstellung 3. Nebenprodukte 4. Eigenschaften 5.
Azeotrope. Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch
 Azeotrope B A Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch zahl- reiche wichtige Systeme weichen davon ab. Ein solches Verhalten kann auftreten, a wenn die Wechselwirkungen
Azeotrope B A Viele binäre flüssige Mischungen zeigen das vorhin diskutierte Siedediagramm, doch zahl- reiche wichtige Systeme weichen davon ab. Ein solches Verhalten kann auftreten, a wenn die Wechselwirkungen
Ammoniaksynthese nach Haber-Bosch
 Sarah Kiefer, Thomas Richter Ammoniaksynthese nach Haber-Bosch 1. Allgemeine Einführung 2. Chemisches Grundprinzip 3. Industrielle Umsetzung 4. Anwendung und Auswirkungen 1. Allgemeine Einführung Steckbrief:
Sarah Kiefer, Thomas Richter Ammoniaksynthese nach Haber-Bosch 1. Allgemeine Einführung 2. Chemisches Grundprinzip 3. Industrielle Umsetzung 4. Anwendung und Auswirkungen 1. Allgemeine Einführung Steckbrief:
Chrom. Vortrag von Kerstin Schaller im Rahmen der "Übungen im Vortragen mit Demonstrationen - Anorganische Chemie", WS 2003/2004.
 Chrom Vortrag von Kerstin Schaller im Rahmen der "Übungen im Vortragen mit Demonstrationen - Anorganische Chemie", WS 2003/2004 Gliederung: 0. Einleitung 1. Allgemeines zum Element Chrom 2. Vorkommen 3.
Chrom Vortrag von Kerstin Schaller im Rahmen der "Übungen im Vortragen mit Demonstrationen - Anorganische Chemie", WS 2003/2004 Gliederung: 0. Einleitung 1. Allgemeines zum Element Chrom 2. Vorkommen 3.
1.11 Welcher Stoff ist es?
 L *** 1.11 Welcher Stoff ist es? Didaktisch-methodische Hinweise Im Arbeitsblatt wird der Versuch des Lösens von vier verschiedenen Salzen in Wasser in einem Labor beschrieben. Aus Zahlenangaben müssen
L *** 1.11 Welcher Stoff ist es? Didaktisch-methodische Hinweise Im Arbeitsblatt wird der Versuch des Lösens von vier verschiedenen Salzen in Wasser in einem Labor beschrieben. Aus Zahlenangaben müssen
C.3.2 Aluminium - Geschichte
 C.3.2 Aluminium - Geschichte Silber aus Lehm: Aluminium wurde zu Beginn des 19. Jahrhunderts entdeckt 1807 Engländer Humphrey Davy: Zerlegung g von Tonerde mit Hilfe des elektrischen Stromes versucht!
C.3.2 Aluminium - Geschichte Silber aus Lehm: Aluminium wurde zu Beginn des 19. Jahrhunderts entdeckt 1807 Engländer Humphrey Davy: Zerlegung g von Tonerde mit Hilfe des elektrischen Stromes versucht!
Antwort 1: Antwort 1:
 Hilfe 1 Hilfe 1 Erklärt euch gegenseitig die Aufgabe noch einmal in euren eigenen Worten. Klärt dabei, wie ihr die Aufgabe verstanden habt und was euch noch unklar ist. Erklärt euch gegenseitig die Aufgabe
Hilfe 1 Hilfe 1 Erklärt euch gegenseitig die Aufgabe noch einmal in euren eigenen Worten. Klärt dabei, wie ihr die Aufgabe verstanden habt und was euch noch unklar ist. Erklärt euch gegenseitig die Aufgabe
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie)
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Anorganische Chemie! der unbelebten Natur keine Kohlenstoffverbindung (Kohlenstoffatome C) Metall Nichtmetallverbindungen Ionenbindung
 3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
GFS: Gewinnung von Aluminium durch Schmelzflusselektrolyse
 Sarah Neuwirth Chemie 4std Klassenstufe 13 / 17.01.2006 GFS: Gewinnung von Aluminium durch Schmelzflusselektrolyse Aufbau: Ausgangsstoff für die Gewinnung: Bauxit Gewinnung von reinem Aluminiumoxid am
Sarah Neuwirth Chemie 4std Klassenstufe 13 / 17.01.2006 GFS: Gewinnung von Aluminium durch Schmelzflusselektrolyse Aufbau: Ausgangsstoff für die Gewinnung: Bauxit Gewinnung von reinem Aluminiumoxid am
CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Einführung Brennendes Magnesiumband reagiert mit Sauerstoff
CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Einführung Brennendes Magnesiumband reagiert mit Sauerstoff
A 2.6 Wie ist die Zusammensetzung der Flüssigkeit und des Dampfes eines Stickstoff-Sauerstoff-Gemischs
 A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
A 2.1 Bei - 10 o C beträgt der Dampfdruck des Kohlendioxids 26,47 bar, die Dichte der Flüssigkeit 980,8 kg/m 3 und die Dichte des Dampfes 70,5 kg/m 3. Bei - 7,5 o C beträgt der Dampfdruck 28,44 bar. Man
Haber Bosch-Verfahren Referat von Tobias Rosendahl und Carsten Müller zum Seminar zum analytischen Grundpraktikum am Donnerstag, dem
 Haber Bosch-Verfahren Referat von Tobias Rosendahl und Carsten Müller zum Seminar zum analytischen Grundpraktikum am Donnerstag, dem 17.12.98 Grundgliederung - allg. Einführung - chemisches Grundprinzip
Haber Bosch-Verfahren Referat von Tobias Rosendahl und Carsten Müller zum Seminar zum analytischen Grundpraktikum am Donnerstag, dem 17.12.98 Grundgliederung - allg. Einführung - chemisches Grundprinzip
Antrieb und Wärmebilanz bei Phasenübergängen. Speyer, März 2007
 Antrieb und Wärmebilanz bei Phasenübergängen Speyer, 19-20. März 2007 Michael Pohlig, WHG-Durmersheim michael@pohlig.de Literatur: Physik in der Oberstufe; Duden-PAETEC Schmelzwärme wird auch als Schmelzenergie
Antrieb und Wärmebilanz bei Phasenübergängen Speyer, 19-20. März 2007 Michael Pohlig, WHG-Durmersheim michael@pohlig.de Literatur: Physik in der Oberstufe; Duden-PAETEC Schmelzwärme wird auch als Schmelzenergie
10TG. Training II2. 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene.
 Training II2 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene. (4X4=1 X4=16P) a. Verbrennung von Kohlenstoff C + O2 CO2 Kohlenstoffdioxid b. Thermolyse
Training II2 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene. (4X4=1 X4=16P) a. Verbrennung von Kohlenstoff C + O2 CO2 Kohlenstoffdioxid b. Thermolyse
Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt.
 1 Definition: Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt. 2 Erscheinungsformen der Materie Homogen oder
1 Definition: Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt. 2 Erscheinungsformen der Materie Homogen oder
Umschmelzen für höchste Ansprüche
 Umschmelzen für höchste Ansprüche Know-How und Verfahrenstechnik: Optimal abgestimmt auf die Bedürfnisse unserer Kunden Unter dem Dach der Düsseldorfer SCHMOLZ+BICKENBACH Gruppe sind die Deutschen Edelstahlwerke
Umschmelzen für höchste Ansprüche Know-How und Verfahrenstechnik: Optimal abgestimmt auf die Bedürfnisse unserer Kunden Unter dem Dach der Düsseldorfer SCHMOLZ+BICKENBACH Gruppe sind die Deutschen Edelstahlwerke
Zustandsbeschreibungen
 Siedediagramme Beispiel: System Stickstoff Sauerstoff - Das Siedeverhalten des Systems Stickstoff Sauerstoff Der Übergang vom flüssigen in den gasförmigen Aggregatzustand. - Stickstoff und Sauerstoff bilden
Siedediagramme Beispiel: System Stickstoff Sauerstoff - Das Siedeverhalten des Systems Stickstoff Sauerstoff Der Übergang vom flüssigen in den gasförmigen Aggregatzustand. - Stickstoff und Sauerstoff bilden
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Fossile Rohstoffe. Kohlenwasserstoffe als Energieträger
 nwasserstoffe als Energieträger Erdöl,, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da sie
nwasserstoffe als Energieträger Erdöl,, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da sie
Luft ist nicht Nichts
 Luft ist nicht Nichts Experiment 1 Luft im Glas: Durchführung: Ein offenes Glas wird verkehrt herum in eine Schale voller Wasser getaucht. Luft im Glas Wasser Beobachtung: Das Glas bleibt auch unter Wasser
Luft ist nicht Nichts Experiment 1 Luft im Glas: Durchführung: Ein offenes Glas wird verkehrt herum in eine Schale voller Wasser getaucht. Luft im Glas Wasser Beobachtung: Das Glas bleibt auch unter Wasser
Kernkraftwerke. Kernkraftwerk mit Siedewasserreaktor
 1 Kernkraftwerke Es werden zur Zeit vier Reaktortypen zur Energiegewinnung verwendet. 54. Siedewasserreaktor 55. Druckwasserreaktor 56. Schneller Brutreaktor 57. Thorium Hochtemperaturreaktor Im Folgenden
1 Kernkraftwerke Es werden zur Zeit vier Reaktortypen zur Energiegewinnung verwendet. 54. Siedewasserreaktor 55. Druckwasserreaktor 56. Schneller Brutreaktor 57. Thorium Hochtemperaturreaktor Im Folgenden
Klausur : Allgemeine und Anorganische Chemie. Name...Fachrichtung... Matr.-Nr...
 Klausur : Allgemeine und Anorganische Chemie Mo. 1.03.11 : 13.30 16.30 Uhr 1 Beantworten Sie maximal zehn Fragen. Für jede Frage gibt es maximal 10 Punkte; die Klausur gilt als bestanden, wenn 50 Punkte
Klausur : Allgemeine und Anorganische Chemie Mo. 1.03.11 : 13.30 16.30 Uhr 1 Beantworten Sie maximal zehn Fragen. Für jede Frage gibt es maximal 10 Punkte; die Klausur gilt als bestanden, wenn 50 Punkte
Wenn es ums Löten geht...
 Wenn es ums Löten geht... Zur Geschichte Löten, ein thermisches Verbindungsverfahren, heute in der Definition nach DIN 8505 unmißverständlich geklärt und von dem verwandten Fügeverfahren Schweißen genau
Wenn es ums Löten geht... Zur Geschichte Löten, ein thermisches Verbindungsverfahren, heute in der Definition nach DIN 8505 unmißverständlich geklärt und von dem verwandten Fügeverfahren Schweißen genau
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
3.4 Änderung des Aggregatzustandes
 34 Änderung des Aggregatzustandes Man unterscheidet 3 Aggregatzustände: Fest Flüssig Gasförmig Temperatur: niedrig mittel hoch Molekülbindung: Gitter lose Bindung keine Bindung schmelzen sieden erstarren
34 Änderung des Aggregatzustandes Man unterscheidet 3 Aggregatzustände: Fest Flüssig Gasförmig Temperatur: niedrig mittel hoch Molekülbindung: Gitter lose Bindung keine Bindung schmelzen sieden erstarren
Labor- und Pilotuntersuchungen für Waschsysteme zur Herstellung von Biomethan"
 Labor- und Pilotuntersuchungen für Waschsysteme zur Herstellung von Biomethan" Lutherstadt Wittenberg, 27.10.2006 Fachtagung INNOGAS: Herstellung von Biomethan aus Biogas Dr. J. Hofmann, U. Freier Zielstellung
Labor- und Pilotuntersuchungen für Waschsysteme zur Herstellung von Biomethan" Lutherstadt Wittenberg, 27.10.2006 Fachtagung INNOGAS: Herstellung von Biomethan aus Biogas Dr. J. Hofmann, U. Freier Zielstellung
Potentiale alternativer Herstellungskonzepte für Titanmetall und Titanlegierungen
 GDMB 44. Metallurgisches Seminar, Hanau, 5.2.2010 Potentiale alternativer Herstellungskonzepte für Titanmetall und Titanlegierungen B. Friedrich, J. Reitz, R. Bolivar, C. Möller IME Metallurgische und
GDMB 44. Metallurgisches Seminar, Hanau, 5.2.2010 Potentiale alternativer Herstellungskonzepte für Titanmetall und Titanlegierungen B. Friedrich, J. Reitz, R. Bolivar, C. Möller IME Metallurgische und
02. Was kann man über die Teilchen eines schmelzenden Stoffes aussagen?
 01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
Titan-Schweisstechnik.
 Sonderdruck Titan-Schweisstechnik. Schweisstechnische Verarbeitung von Titan-Werkstoffen. 02 Sonderdruck Titan-Schweisstechnik Titan-Schweisstechnik. Schweisstechnische Verarbeitung von Titan-Werkstoffen.
Sonderdruck Titan-Schweisstechnik. Schweisstechnische Verarbeitung von Titan-Werkstoffen. 02 Sonderdruck Titan-Schweisstechnik Titan-Schweisstechnik. Schweisstechnische Verarbeitung von Titan-Werkstoffen.
Eisenerz Kokskohle Flüssiges Roheisen C Hochofen
 Stahl Ist Stahl ein junger Werkstoff? Das zur Herstellung von Stahl erforderliche Eisen wird in Europa seit 1.700 vor J.C. hergestellt. Von Anfang an wurden auch kleine Mengen Stahl hergestellt, d.h. mit
Stahl Ist Stahl ein junger Werkstoff? Das zur Herstellung von Stahl erforderliche Eisen wird in Europa seit 1.700 vor J.C. hergestellt. Von Anfang an wurden auch kleine Mengen Stahl hergestellt, d.h. mit
EloPhos. P ho s p hat-red uktion und - Rü c k ge w i n n u n g
 EloPhos P ho s p hat-red uktion und - Rü c k ge w i n n u n g EloPhos IST EIN SYSTEM ZUR RÜCKGEWINNUNG VON PHOSPHAT AUS DEM FAULSCHLAMM VON ABWASSERBEHANDLUNGSANLAGEN MIT BIOLOGISCHER PHOSPHATELIMINATION
EloPhos P ho s p hat-red uktion und - Rü c k ge w i n n u n g EloPhos IST EIN SYSTEM ZUR RÜCKGEWINNUNG VON PHOSPHAT AUS DEM FAULSCHLAMM VON ABWASSERBEHANDLUNGSANLAGEN MIT BIOLOGISCHER PHOSPHATELIMINATION
Potentiale alternativer Herstellungskonzepte für Titanmetall und Titanlegierungen
 Potentiale alternativer Herstellungskonzepte für Titanmetall und Titanlegierungen Potentiale alternativer Herstellungskonzepte für Titanmetall und Titanlegierungen Prof. Dr. Bernd Friedrich, Dipl.-Ing.
Potentiale alternativer Herstellungskonzepte für Titanmetall und Titanlegierungen Potentiale alternativer Herstellungskonzepte für Titanmetall und Titanlegierungen Prof. Dr. Bernd Friedrich, Dipl.-Ing.
V. Vom Experiment zur Reaktionsgleichung. Themen dieses Kapitels:
 Hinweise zum Kapitel V. Vom Experiment zur Reaktionsgleichung Themen dieses Kapitels: - Stoffmengen (Mole), molare Massen und Massen von Stoffportionen und ihre mathematische Bestimmung - Stoffnamen und
Hinweise zum Kapitel V. Vom Experiment zur Reaktionsgleichung Themen dieses Kapitels: - Stoffmengen (Mole), molare Massen und Massen von Stoffportionen und ihre mathematische Bestimmung - Stoffnamen und
Eigenschaften Reinstoffe Elemente Kugelteilchen Elementes Atom
 Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Recycling von gebrauchten Katalysatoren Reaktivierung von Aktivkohle
 Recycling von gebrauchten Katalysatoren Reaktivierung von Aktivkohle Quecksilber Problem oder Herausforderung? Das Recycling gebrauchter Materialien und das möglichst weitgehende Schliessen von Stoffkreisläufen
Recycling von gebrauchten Katalysatoren Reaktivierung von Aktivkohle Quecksilber Problem oder Herausforderung? Das Recycling gebrauchter Materialien und das möglichst weitgehende Schliessen von Stoffkreisläufen
Wiederholungsfragen Metall 9
 Wiederholungsfragen Metall 9 Die richtige Beantwortung der Wiederholungsfragen aus dem Stoff der 9. Jahrgangsstufe ist Voraussetzung für die Vorbereitung auf die Abschlussprüfung. Dazu muss auch das Arbeitsheft
Wiederholungsfragen Metall 9 Die richtige Beantwortung der Wiederholungsfragen aus dem Stoff der 9. Jahrgangsstufe ist Voraussetzung für die Vorbereitung auf die Abschlussprüfung. Dazu muss auch das Arbeitsheft
Erfolgreiche Inbetriebnahme des Greenfield-Hüttenwerks Tata Steel
 Telefon: +49 211 881 4449 Fax: +49 211 881 774449 E-Mail: thilo.sagermann@sms-group.com PRESSEMITTEILUNG Thilo Sagermann Düsseldorf, Juli 06, 2016 Erfolgreiche Inbetriebnahme des Greenfield-Hüttenwerks
Telefon: +49 211 881 4449 Fax: +49 211 881 774449 E-Mail: thilo.sagermann@sms-group.com PRESSEMITTEILUNG Thilo Sagermann Düsseldorf, Juli 06, 2016 Erfolgreiche Inbetriebnahme des Greenfield-Hüttenwerks
GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN
 10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
ELEMENTARSTOFFE, VERBINDUNGEN und chemische Formeln LÖSUNG. Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor.
 Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor. Aufgabe 1: a) Tragen Sie die folgenden chemischen Formeln in die richtige Spalte der Tabelle ein. Beachten Sie, dass mehrere
Hinweis: In den Salzen kommen die Metallatome stets als einatomige Kationen vor. Aufgabe 1: a) Tragen Sie die folgenden chemischen Formeln in die richtige Spalte der Tabelle ein. Beachten Sie, dass mehrere
Semesterarbeit im Wahlpflichtfach Leichtmetalle. Sensor- und Feinwerktechnik. Wintersemester 2000/2001
 Semesterarbeit im Wahlpflichtfach Leichtmetalle Sensor- und Feinwerktechnik Wintersemester 2000/2001-1- Inhalt: Herstellung Vorkommen Eigenschaften Korrosionsbeständigkeit Fazit Normen Quellenverzeichnis
Semesterarbeit im Wahlpflichtfach Leichtmetalle Sensor- und Feinwerktechnik Wintersemester 2000/2001-1- Inhalt: Herstellung Vorkommen Eigenschaften Korrosionsbeständigkeit Fazit Normen Quellenverzeichnis
Verbrennung und Dampferzeugung
 Institut für Energietechnik, Verbrennung und Dampferzeugung - universitäres Fernstudium Wasseraufbereitung, Kühlsysteme, Verschmutzungen im Dampferzeuger - Wasser und Wasseraufbereitung - Folie 2 von 30
Institut für Energietechnik, Verbrennung und Dampferzeugung - universitäres Fernstudium Wasseraufbereitung, Kühlsysteme, Verschmutzungen im Dampferzeuger - Wasser und Wasseraufbereitung - Folie 2 von 30
Institut für Technische Chemie Technische Universität Clausthal. Technisch-chemisches Praktikum TCB. Versuch: Rektifikation
 Institut für Technische Chemie Technische Universität Clausthal Technisch-chemisches Praktikum TCB Versuch: Rektifikation Einleitung In einer Vielzahl von chemischen Produktionsanlagen besteht die Notwendigkeit,
Institut für Technische Chemie Technische Universität Clausthal Technisch-chemisches Praktikum TCB Versuch: Rektifikation Einleitung In einer Vielzahl von chemischen Produktionsanlagen besteht die Notwendigkeit,
6.1 Elektrodenpotenzial und elektromotorische Kraft
 6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
Von Bauxit zum Aluminium
 Von Bauxit zum Aluminium 18.06.2010 1 Themenübersicht Geschichte Vorkommen von Bauxit Allgemeines zum Aluminium Verwendung Herstellungsverfahren Gewinnung des Oxids ( Bayer-Verfahren) Gewinnung des Aluminiums
Von Bauxit zum Aluminium 18.06.2010 1 Themenübersicht Geschichte Vorkommen von Bauxit Allgemeines zum Aluminium Verwendung Herstellungsverfahren Gewinnung des Oxids ( Bayer-Verfahren) Gewinnung des Aluminiums
Wasser à. Nachweis: Wasser ist
 Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Was ist eine Wärmepumpe? Und wie funktioniert die Wärmepumpe?
 Was ist eine Wärmepumpe? Und wie funktioniert die Wärmepumpe? Grundlagen Dies ist zum Beispiel eine Wärmepumpe! Eine Wärmepumpe funktioniert wie ein Kühlschrank Aber was passiert jetzt genau im Kühlschrank,
Was ist eine Wärmepumpe? Und wie funktioniert die Wärmepumpe? Grundlagen Dies ist zum Beispiel eine Wärmepumpe! Eine Wärmepumpe funktioniert wie ein Kühlschrank Aber was passiert jetzt genau im Kühlschrank,
Titan. Materialbeschrieb. Hintergrund. Metall > Nichteisenmetalle > Leichtmetalle. Titan ist ein chemisches Element und gehört zu den Leichtmetallen.
 Materialgruppen: Metall > Nichteisenmetalle > Leichtmetalle Materialbeschrieb Titan ist ein chemisches Element und gehört zu den Leichtmetallen. Heinrich Klaproth entdeckte das Element 1785 und nannte
Materialgruppen: Metall > Nichteisenmetalle > Leichtmetalle Materialbeschrieb Titan ist ein chemisches Element und gehört zu den Leichtmetallen. Heinrich Klaproth entdeckte das Element 1785 und nannte
Was haben wir gelernt?
 Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
Was haben wir gelernt? - Gesetze chemischer Reaktionen - Atommodell von Dalton - Elementsymbole - Die atomare Masseneinheit u - Die Avogadro-Zahl und deren Umkehrung - Von Massenverhältnissen zu Teilchenverhältnissen
Festkörperchemie SYNTHESE. Shake and bake Methode: Sol-Gel-Methode. Am Beispiel :
 Festkörperchemie SYNTHESE Shake and bake Methode: Am Beispiel : Man zerkleinert die Salze mechanisch, damit eine möglichst große Grenzfläche zwischen den beiden Komponenten entsteht und vermischt das ganze.
Festkörperchemie SYNTHESE Shake and bake Methode: Am Beispiel : Man zerkleinert die Salze mechanisch, damit eine möglichst große Grenzfläche zwischen den beiden Komponenten entsteht und vermischt das ganze.
Leistungsnachweis "Metallische Werkstoffe" der Studienrichtung "Metallische Werkstoffe" und "Prozesse" am 21. Oktober 2008 (Nicht-Eisenwerkstoffe)
 RHEINISCH- WESTFÄLISCHE TECHNISCHE HOCHSCHULE AACHEN Institut für Eisenhüttenkunde Leistungsnachweis "Metallische Werkstoffe" der Studienrichtung "Metallische Werkstoffe" und "Prozesse" am 21. Oktober
RHEINISCH- WESTFÄLISCHE TECHNISCHE HOCHSCHULE AACHEN Institut für Eisenhüttenkunde Leistungsnachweis "Metallische Werkstoffe" der Studienrichtung "Metallische Werkstoffe" und "Prozesse" am 21. Oktober
Dienstag den Barleben. Themen: Schweißen von hochlegierten Stählen
 Fachveranstaltung Fachveranstaltung Schweißtechnik Dienstag den 11.11.2003 Barleben Themen: Flammrichten an Stahl und Aluminiumkonstruktionen Schweißen von hochlegierten Stählen MSS Magdeburger Schweißtechnik
Fachveranstaltung Fachveranstaltung Schweißtechnik Dienstag den 11.11.2003 Barleben Themen: Flammrichten an Stahl und Aluminiumkonstruktionen Schweißen von hochlegierten Stählen MSS Magdeburger Schweißtechnik
Redox - Übungsaufgaben:
 Redox - Übungsaufgaben: Schwierigkeitsgrad I: 1.Magnesium reagiert mit Sauerstoff zu Magnesiumoxid. Ox: Mg Mg 2+ + 2e - /*2 Red: O 2 + 4e - 2 O 2- Redox: 2 Mg + O 2 2 MgO 2.Kalium Reagiert mit Schwefel
Redox - Übungsaufgaben: Schwierigkeitsgrad I: 1.Magnesium reagiert mit Sauerstoff zu Magnesiumoxid. Ox: Mg Mg 2+ + 2e - /*2 Red: O 2 + 4e - 2 O 2- Redox: 2 Mg + O 2 2 MgO 2.Kalium Reagiert mit Schwefel
Schweißschutzgase Zusammensetzung Anwendung
 Sauerstoffwerk Steinfurt E. Howe GmbH & Co. KG Sellen 106 48565 Steinfurt Tel.: 0 25 51/ 93 98-0 Fax: 0 25 51/ 93 98-98 Schweißschutzgase Zusammensetzung Anwendung Einstufung der Howe-Schweißschutzgase
Sauerstoffwerk Steinfurt E. Howe GmbH & Co. KG Sellen 106 48565 Steinfurt Tel.: 0 25 51/ 93 98-0 Fax: 0 25 51/ 93 98-98 Schweißschutzgase Zusammensetzung Anwendung Einstufung der Howe-Schweißschutzgase
Organisch-chemisches Praktikum Wintersemester 2005/06. o-chlortoluen. Stephan Steinmann
 rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
rganisch-chemisches Praktikum Wintersemester 005/06 o-chlortoluen 30. 11. 005 Stephan Steinmann 1 1. Methode [1] Mittels einer Sandmeyer-Reaktion wird ortho-toluidin (1) zu ortho-chlortoluen () umgesetzt..
Sauerstoffzuleitung Widerstandsheizung Quarzrohr Wafer in Carrier. Bubblergefäß mit Wasser (~95 C) Abb. 1.1: Darstellung eines Oxidationsofens
 1 Oxidation 1.1 Erzeugung von Oxidschichten 1.1.1 Thermische Oxidation Bei der thermischen Oxidation werden die Siliciumwafer bei ca. 1000 C in einem Oxidationsofen oxidiert. Dieser Ofen besteht im Wesentlichen
1 Oxidation 1.1 Erzeugung von Oxidschichten 1.1.1 Thermische Oxidation Bei der thermischen Oxidation werden die Siliciumwafer bei ca. 1000 C in einem Oxidationsofen oxidiert. Dieser Ofen besteht im Wesentlichen
Struktur und Eigenschaften
 Fachdidaktik Chemie ETH Zwischenmolekulare Kräfte S. 1 Struktur und Eigenschaften 4 Fälle Substanz Siede- und Schmelztemperatur Löslichkeit in Wasser e Leitfähigkeit Fall 1: Moleküle ohne H-Brücken Wasserstoff
Fachdidaktik Chemie ETH Zwischenmolekulare Kräfte S. 1 Struktur und Eigenschaften 4 Fälle Substanz Siede- und Schmelztemperatur Löslichkeit in Wasser e Leitfähigkeit Fall 1: Moleküle ohne H-Brücken Wasserstoff
Kochsalz-Kristalle (Halit) Wichtige Stoffgruppen Atomverband Stoffgruppe Metall Metall: Metallische Stoffe Salzartige Stoffe Metall Nichtmetall:
 Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Steckbrief Bariumcarbonat BaCO 3
 Steckbrief Bariumcarbonat BaCO 3 Bariumcarbonat ist eine thermodynamisch stabile Verbindung, die aus Ba 2+ - Ionen 2- und CO 3 - Ionen besteht. Das farblose Salz gehört zur Stoffklasse der Carbonate und
Steckbrief Bariumcarbonat BaCO 3 Bariumcarbonat ist eine thermodynamisch stabile Verbindung, die aus Ba 2+ - Ionen 2- und CO 3 - Ionen besteht. Das farblose Salz gehört zur Stoffklasse der Carbonate und
Aggregatzustände. Atomradien
 Elementgruppen Aggregatzustände Atomradien Biologische Bedeutung Dichte Elektronegativität Entdeckung der Elemente Ionenradien Ionisierungsenergie Natürliche Isotope Kovalenzradien Metalle und Nichtmetalle
Elementgruppen Aggregatzustände Atomradien Biologische Bedeutung Dichte Elektronegativität Entdeckung der Elemente Ionenradien Ionisierungsenergie Natürliche Isotope Kovalenzradien Metalle und Nichtmetalle
Anorganische Peroxide und Radikale. von Benjamin Scharbert
 Anorganische Peroxide und Radikale von Benjamin Scharbert Inhalt: 1. Anorganische Peroxide: 2. Radikale: 1.1 Grundsätzliches 1.2 Na 2 O 2 1.3 BaO 2 1.4 H 2 O 2 2.1 Grundsätzliches 2.2 Sauerstoff 2.3 Stickstoffmonoxid
Anorganische Peroxide und Radikale von Benjamin Scharbert Inhalt: 1. Anorganische Peroxide: 2. Radikale: 1.1 Grundsätzliches 1.2 Na 2 O 2 1.3 BaO 2 1.4 H 2 O 2 2.1 Grundsätzliches 2.2 Sauerstoff 2.3 Stickstoffmonoxid
Cer und die Verwendung von Ceroxiden. von Christian Kappel
 Cer und die Verwendung von Ceroxiden von Christian Kappel Inhaltsverzeichnis 1. Geschichte des Cer 2. Vorkommen von Cer 3. Spezifische Eigenschaften 4. Chemie des Cers 5. Verwendung von Ceroxiden 1. Beim
Cer und die Verwendung von Ceroxiden von Christian Kappel Inhaltsverzeichnis 1. Geschichte des Cer 2. Vorkommen von Cer 3. Spezifische Eigenschaften 4. Chemie des Cers 5. Verwendung von Ceroxiden 1. Beim
Aufgabenblatt 10 Übungsblatt Stöchiometrie
 Name: Datum: Aufgabenblatt 10 Übungsblatt Stöchiometrie Berechnung von Stoffmengen bei chemischen Reaktionen II _ 20091005 Dr. Hagen Grossholz A1 Zusammenhang zwischen den verschiedenen Größen. Masse m
Name: Datum: Aufgabenblatt 10 Übungsblatt Stöchiometrie Berechnung von Stoffmengen bei chemischen Reaktionen II _ 20091005 Dr. Hagen Grossholz A1 Zusammenhang zwischen den verschiedenen Größen. Masse m
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Praktikumsskript Präparative Anorganische Chemie. Wintersemester 2008/2009
 Skripte zum Praktikum Präparative Anorganische Chemie Wintersemester 2008/2009 FU Berlin/Moritz Kühnel 10/2008 3. Arbeiten unter inerten Bedingungen Viele anorganische Verbindungen sind empfindlich gegenüber
Skripte zum Praktikum Präparative Anorganische Chemie Wintersemester 2008/2009 FU Berlin/Moritz Kühnel 10/2008 3. Arbeiten unter inerten Bedingungen Viele anorganische Verbindungen sind empfindlich gegenüber
Formelsammlung Abfallwirtschaft Seite 1/6 Wärmekapazität Prof. Dr. Werner Bidlingmaier & Dr.-Ing. Christian Springer
 Formelsammlung Abfallwirtschaft Seite 1/6 1 Energiebedarf zur Erwärmung von Stoffen Der Energiebetrag, der benötigt wird, um 1 kg einer bestimmten Substanz um 1 C zu erwärmen, wird als die (auch: Spezifische
Formelsammlung Abfallwirtschaft Seite 1/6 1 Energiebedarf zur Erwärmung von Stoffen Der Energiebetrag, der benötigt wird, um 1 kg einer bestimmten Substanz um 1 C zu erwärmen, wird als die (auch: Spezifische
Klausur : Allgemeine und Anorganische Chemie
 1 Klausur : Allgemeine und Anorganische Chemie Di. 17.2.9 : 15.3-18.3 Uhr 1. Nitrat: entweder (i) Reduktion zu Ammoniak (am Geruch oder mit ph-papier zu erkennen) in alkalischer Lösung mit einem reaktiven
1 Klausur : Allgemeine und Anorganische Chemie Di. 17.2.9 : 15.3-18.3 Uhr 1. Nitrat: entweder (i) Reduktion zu Ammoniak (am Geruch oder mit ph-papier zu erkennen) in alkalischer Lösung mit einem reaktiven
Fachhochschule Wedel. Fertigungstechnik der Elektronik
 Fachhochschule Wedel University of Applied Sciences Klausurrelevante Zusammenfassung erstellt im: Februar 2001 von: Alexander Markowski Basis: Vorlesung im WS 00/01 Inhaltsverzeichnis Abbildungsverzeichnis
Fachhochschule Wedel University of Applied Sciences Klausurrelevante Zusammenfassung erstellt im: Februar 2001 von: Alexander Markowski Basis: Vorlesung im WS 00/01 Inhaltsverzeichnis Abbildungsverzeichnis
Edelstahl. Vortrag von Alexander Kracht
 Edelstahl Vortrag von Alexander Kracht Inhalt I. Historie II. Definition Edelstahl III. Gruppen IV. Die Chemie vom Edelstahl V. Verwendungsbeispiele VI. Quellen Historie 19. Jh. Entdeckung, dass die richtige
Edelstahl Vortrag von Alexander Kracht Inhalt I. Historie II. Definition Edelstahl III. Gruppen IV. Die Chemie vom Edelstahl V. Verwendungsbeispiele VI. Quellen Historie 19. Jh. Entdeckung, dass die richtige
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #12 am 26.01.2007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #12 am 26.01.2007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Urotropin-Ammoniumsulfid-Gruppe
 Urotropin-Ammoniumsulfid-Gruppe Lerninhalte zum Thema Chrom Vorkommen Darstellung (ausführlich) und Aufschluß, Dichromat-Zwischenstufe, kompaktes Chrom - Oxidationsbeständigkeit (aktiver, passiver Zustand)
Urotropin-Ammoniumsulfid-Gruppe Lerninhalte zum Thema Chrom Vorkommen Darstellung (ausführlich) und Aufschluß, Dichromat-Zwischenstufe, kompaktes Chrom - Oxidationsbeständigkeit (aktiver, passiver Zustand)
Die Wirkungsweise einer Brennstoffzelle. Ein Vortrag von Bernard Brickwedde
 Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
Die Wirkungsweise einer Brennstoffzelle Ein Vortrag von Bernard Brickwedde Inhalt Allgemein Definition Geschichte Anwendungsgebiete Aufbau Theoretische Grundlagen Redoxreaktion Wirkungsgrad Elektrochemische
Saurer Regen, was ist das?
 Saurer Regen, was ist das? 1. SO x (x=2,3) => SO 2 und SO 3 SO 2 + H 2 O H 2 SO 3 (schwefelige Säure) SO 3 + H 2 O H 2 SO 4 (Schwefelsäure) 2. NO x (x=1,2) 2 NO + H 2 O + ½O 2 2 H NO 2 (salpetrige Säure)
Saurer Regen, was ist das? 1. SO x (x=2,3) => SO 2 und SO 3 SO 2 + H 2 O H 2 SO 3 (schwefelige Säure) SO 3 + H 2 O H 2 SO 4 (Schwefelsäure) 2. NO x (x=1,2) 2 NO + H 2 O + ½O 2 2 H NO 2 (salpetrige Säure)
Salpetersäure. Herstellung und Bedeutung. von
 Salpetersäure Herstellung und Bedeutung von Patrick Götte Stefan Jovanovic Salpetersäure Herstellung und Bedeutung Salpetersäure und deren Eigenschaften Geschichtliches Herstellung Bedeutung / Verwendung
Salpetersäure Herstellung und Bedeutung von Patrick Götte Stefan Jovanovic Salpetersäure Herstellung und Bedeutung Salpetersäure und deren Eigenschaften Geschichtliches Herstellung Bedeutung / Verwendung
Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht?
 Posten 1a Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht? a) es entsteht Wasserdampf (Wassertropfen kondensieren am Streifen) (=> Posten 5l) b) der Schwefeldampf wird
Posten 1a Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht? a) es entsteht Wasserdampf (Wassertropfen kondensieren am Streifen) (=> Posten 5l) b) der Schwefeldampf wird
3. Stoffgemische und Ihre Zerlegung
 3. Stoffgemische und Ihre Zerlegung Aus Stoffgemischen lassen sich die einzelnen Bestandteile durch physikalische Trennverfahren isolieren. Wenn ein Stoff mittels physikalischen Methoden nicht weiter zerlegen
3. Stoffgemische und Ihre Zerlegung Aus Stoffgemischen lassen sich die einzelnen Bestandteile durch physikalische Trennverfahren isolieren. Wenn ein Stoff mittels physikalischen Methoden nicht weiter zerlegen
KW33/Titan Prof. Dr. Rüdiger Beckhaus
 KW33/Titan Prof. Dr. Rüdiger Beckhaus Name und Eigenschaften Im Jahre 1791 berichtete der Geistliche William Gregor (1761-1817) über das neue Element Titan als Bestandteil im schwarzen Sand von Cornwall
KW33/Titan Prof. Dr. Rüdiger Beckhaus Name und Eigenschaften Im Jahre 1791 berichtete der Geistliche William Gregor (1761-1817) über das neue Element Titan als Bestandteil im schwarzen Sand von Cornwall
+ O. Die Valenzelektronen der Natriumatome werden an das Sauerstoffatom abgegeben.
 A Oxidation und Reduktion UrsprÄngliche Bedeutung der Begriffe UrsprÅnglich wurden Reaktionen, bei denen sich Stoffe mit Sauerstoff verbinden, als Oxidationen bezeichnet. Entsprechend waren Reaktionen,
A Oxidation und Reduktion UrsprÄngliche Bedeutung der Begriffe UrsprÅnglich wurden Reaktionen, bei denen sich Stoffe mit Sauerstoff verbinden, als Oxidationen bezeichnet. Entsprechend waren Reaktionen,
Eder 2AHBTU
 Eigenschaften von Biodiesel: Biodiesel ist ein Kraftstoff, der aus pflanzlichen und tierischen Fetten hergestellt wird. Er hat dunkelbraune bis gelbe Färbung und ist hygroskopisch. Sein Siede- und Flammpunkt
Eigenschaften von Biodiesel: Biodiesel ist ein Kraftstoff, der aus pflanzlichen und tierischen Fetten hergestellt wird. Er hat dunkelbraune bis gelbe Färbung und ist hygroskopisch. Sein Siede- und Flammpunkt
Experiment mit Feinplatin (999,5) und Wasserstoff (H²)
 Experiment mit Feinplatin (999,5) und Wasserstoff (H²) Grundinfo: http://dewikipediaorg/wiki/platin 17062012 ein Auszug daraus: Katalytische Eigenschaften Sowohl Wasserstoff, Sauerstoff als auch andere
Experiment mit Feinplatin (999,5) und Wasserstoff (H²) Grundinfo: http://dewikipediaorg/wiki/platin 17062012 ein Auszug daraus: Katalytische Eigenschaften Sowohl Wasserstoff, Sauerstoff als auch andere
Fragen zum Thema chemische Reaktionen Klasse 4 1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion
 1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion vorliegen? 3. Wie nennt man die Stoffe, die nach der Reaktion vorliegen? 4. Womit wird die Richtung
1. Was gehört zu einer chemische Reaktionsgleichung? 2. Wie nennt man die Stoffe, die vor der Reaktion vorliegen? 3. Wie nennt man die Stoffe, die nach der Reaktion vorliegen? 4. Womit wird die Richtung
Luftzerlegungsanlage Basel. Ihre Quelle für Sauerstoff, Stickstoff und Argon.
 Luftzerlegungsanlage Basel. Ihre Quelle für Sauerstoff, Stickstoff und Argon. Was ist Luft? Die Luft, die wir atmen, ist ein Gasgemisch aus 78 % Stickstoff, 21 % Sauerstoff und 0,9 % Argon. Die restlichen
Luftzerlegungsanlage Basel. Ihre Quelle für Sauerstoff, Stickstoff und Argon. Was ist Luft? Die Luft, die wir atmen, ist ein Gasgemisch aus 78 % Stickstoff, 21 % Sauerstoff und 0,9 % Argon. Die restlichen
Pumpen Fördern Flüssigkeiten
 Anwendungen Bauformen Pumpen Fördern Flüssigkeiten Flüssigkeiten sind inkompressibel Physik der Flüssigkeiten Gewichtsdruck / Höhendruck Stömungspumpen Verdrängerpumpen Energieumwandlung Strömende Flüssigkeiten
Anwendungen Bauformen Pumpen Fördern Flüssigkeiten Flüssigkeiten sind inkompressibel Physik der Flüssigkeiten Gewichtsdruck / Höhendruck Stömungspumpen Verdrängerpumpen Energieumwandlung Strömende Flüssigkeiten
