Produktkatalog 2016/2017. Real-time und Multiplex PCR-Produkte. Informationen aus erster Hand Bakteriologie.
|
|
|
- Lorenz Adler
- vor 7 Jahren
- Abrufe
Transkript
1 Real-time und Multiplex PCR-Produkte Bakteriologie Virologie Gerinnung Multiplex Produktkatalog 2016/2017 Informationen aus erster Hand
2 Inhaltsverzeichnis ISIN/ISEX DNA ISEX RNA Multiplex Vorteile der GeneProof Kits Vorteile der Master Diagnóstica Multiplex PCR Flow Chip Kits Bakteriologie Bordetella pertussis/parapertussis PCR Kit Borrelia burgdorferi PCR Kit Chlamydia pneumoniae PCR Kit Chlamydia trachomatis PCR Kit Presto CT/NG PCR Kit VRE PCR Kit ESBL PCR Kit Legionella pneumophila PCR Kit Mycobacterium tuberculosis PCR Kit Mycoplasma pneumoniae PCR Kit Neisseria gonorrhoeae PCR Kit Virologie Adenovirus PCR Kit BK und JC Virus PCR Kit Cytomegalovirus PCR Kit Epstein-Barr Virus PCR Kit Hepatitis B Virus PCR Kit Hepatitis C Virus PCR Kit Herpes Simplex Virus 1 & 2 PCR Kit Herpes Simplex Virus 1 PCR Kit Herpes Simplex Virus 2 PCR Kit HI Virus Typ 1 PCR Kit JC Virus PCR Kit Varicella-Zoster Virus PCR Kit Multiplex Kits Bacterial CNS Flow Chip Kit Viral CNS Flow Chip Kit HPV Direct Flow Chip Kit Sepsis Flow Chip Kit Tick-borne Bacteria Flow Chip Kit Humangenetik Factor II Prothrombin PCR Kit Factor V Leiden PCR Kit MTHFR C677T PCR Kit MTHFR A1298C PCR Kit PAI-1 Genotypisierung PCR Kit DNA und RNA Isolierung PathogenFree DNA Isolierungs-Kit PathogenFree RNA Isolierungs-Kit Geräte HybriSpot 12 (HS12) DNA-Hybridisierungs-System HybriSpot 24 (HS24) DNA-Hybridisierungs-System Produktliste Kundenservice / Kontakt / Bestellungen
3 TECHNOLOGIE 4
4 Real-time DNA Kits PROBE PROBE Positive Probe enthält Erreger-DNA ( ) Die interne Kontrolle (IS) wird von der Extraktion in die Probe addiert ( ) DNA-ISOLIERUNG DNA-ISOLIERUNG Die extrahierte DNA ist nach der Isolierung in das ready to use Master-Mix addiert und das Vial wird in den Real-time positioniert Nach der Isolierung wird die extrahierte DNA zusammen mit der IS in den ready to use Master-Mix und in den Real-time positioniert PCR-AMPLIFIKATION PCR-AMPLIFIKATION Erreger- und IS-DNA sind amplifiziert Erreger- und IS-DNA sind amplifiziert AUSWERTUNG POSITIVE PROBE - Exponentielles Fluoreszenz-Wachstum im FAM-Kanal QUALITÄTS-KONTROLLE für den diagnostischen Prozess - Exponentielles Wachstum des HEX-Kanals als Beweis für die Amplifikation der internen Kontrolle (IS): 1) Inhibition und Effizienz der PCR-Amplifikation - ISIN Version 2) Qualität der DNA-Extraktion und Effizienz der PCR-Amplifikation - ISEX Version 5
5 Real-time RNA Kits PROBE Positive Probe enthält ) Virus-RNA ( Humane GAPDH mrna ( ) RNA-ISOLIERUNG Die extrahierte RNA ist nach der Isolierung in das ready to use Master-Mix addiert und das Vial wird in den Real-time positioniert rtpcr-amplifikation Während der rtpcr wird die virale RNA von einem PrimerPaar und die humane mrna von einem zweiten Primer-Paar amplifiziert AUSWERTUNG POSITIVE PROBE - Exponentielles Fluoreszenz-Wachstum im FAM-Kanal QUALITÄTS-KONTROLLE für den diagnostischen Prozess - Exponentielles Wachstum des HEX-Kanals als Beweis für die Amplifikation der humanen mrna 6
6 Multiplex PCR Flow Chip Kits PROBE Positive Probe enthält Erreger-DNA ( ) PROBE-VORBEREITUNG Abhängig von der Probenart mit oder ohne DNA-Extraktion Probe + Mastermix REVERSE DOT-BLOTHYBRIDISIERUNG BEFUND 7
7 VORTEILE der GeneProof Kits (siehe Seite u ) Hohe Qualität Alle Kits sind CE IVD zertifiziert. Alle Kits werden regelmäßig bei QCMD und INSTAND e.v. getestet. Universelles PCR-Protokoll Alle DNA-Erreger PCR-Kits laufen unter dem gleichen Temperatur-Protokoll. Sichere Ergebnisse UDG (Uracil-DNA-Glycosylase) verhindert falsch-positive Ergebnisse. Eine interne Kontrolle vermeidet falsch-negative Ergebnisse. Interne Kontrolle Jedes Kit enthält eine interne Kontrolle, entweder im Master Mix (Version ISIN) als PCR Inhibitionskontrolle oder separat (Version ISEX) als PCR-Inhibitionskontrolle und DNA Extraktionskontrolle. Ready to use Master-Mix Das bedeutet: l l l l Leichte und schnelle Handhabung Hohe Stabilität Hohe Sensitivität ( hot start ) Hohe Validiert für gängige Geräte wie z. B. Rotor-Gene 3000/6000/Q (QIAGEN) Light 2.0/480 (ROCHE) Applied Biosystems 7300/70 Real-Time PCR System (Life s) StepOne Real-Time PCR System (Life s) CFX96 Real-Time PCR Detection System (Bio-Rad) Dx Real-Time System (Bio-Rad) Mx3005P QPCR System (Agilent s) qtower 2.0/2.2 (Analytik Jena AG) 8
8 VORTEILE der Master Diagnóstica Multiplex PCR Flow Chip Kits (siehe Seite 36 bis 40) l Breites Multiplex-Panel l Gleichzeitiger Nachweis von mehreren Erregern und/oder Antibiotikaresistenzen l Robuster Assay, zum Teil keine DNA-Extraktion notwendig l UNG basierte PCR für mehr Sicherheit l Geringe Hands-on-Time l Schnelle Durchführung l Flexibel: 1 bis 24 Proben pro Lauf l Automatisierte Hybridisierung und Auswertung l Hohe Sensitivität und l Auswahl von 2 Hybridisierungsgeräten je nach Bedarf l IVD 9
9 BAKTERIOLOGIE 10
10 Bordetella pertussis/parapertussis PCR Kit Das Kit dient zum Nachweis von Bordetella pertussis- und Bordetella parapertussis-dna mittels Realtime PCR. Konservative Region der Insertionssequenz 1 und 2 (IS1 & IS2) Bordetella pertussis (IS1 + IS2) & Bordetella parapertussis (IS1) Sensitivität (LOD) Für B. pertussis 0,02 Genome/µl (Wahrscheinlichkeit 95%) Für B. parapertussis 0,01 Genome/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Bordetella pertussis Cy5: Bordetella parapertussis HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Sputum, Nasalsekret, Nasopharyngialsekret Von -20 C bis -80 C Rotor-Gene 3000/6000*/Q* Light 480 Applied Biosystems 70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System qtower 2.0/2.2 QCMD & INSTAND e.v. (Ergebnisse bei * Die Validierung wurde mit Geräten durchgeführt, die FAM, HEX und Cy5 unterstützen. GeneProof Bordetella pertussis/parapertussis PCR Kit BP/ISIN/0 BP/ISEX/0 BP/ISIN/0 BP/ISEX/0 BP/ISIN/ BP/ISEX/ 11
11 Borrelia burgdorferi PCR Kit Das Kit dient zum Nachweis der Spezies der Borrelia burgdorferi sensu lato Gruppe mittels Real-time PCR. Die Zielsequenz entstammt einem chromosomalen Gen, das die bakterielle 16S RNA kodiert und spezifisch für die B. burgdorferi sensu lato Gruppe ist. Die Methode wurde anhand eines großen Kollektives europäischer Borrelia- und Spirochätenstämme überprüft. Konservative DNA Region des 16S rdna Genes Für B. burgdorferi sensu stricto, B. garinii, B. afzelii, B. andersonii, B. bissettii, B. valaisiana, B. lusitaniae, B. japonica, B. tanukii, B. turdi,b. sinica Sensitivität (LOD) 0,532 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Borrelia burgdorferi HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, Liquor, Urin, Zecke Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei 12 GeneProof Borrelia burgdorferi PCR Kit BB/ISIN/0 BB/ISEX/0 BB/ISIN/0 BB/ISEX/0 BB/ISIN/ BB/ISEX/
12 Chlamydia pneumoniae PCR Kit Das Kit dient zum Nachweis von Chlamydia pneumoniae-dna mittels. Konservative DNA Region des Major Outer Membrane Proteins (MOMP) Chlamydia pneumoniae Sensitivität (LOD) 1,111 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Chlamydia pneumoniae HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Sputum, Bronchiallavage, Nasopharyngial-Abstrich, Nasopharyngial-Aspirat Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System StepOne Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Chlamydia pneumoniae PCR Kit CHP/ISIN/0 CHP/ISEX/0 CHP/ISIN/0 CHP/ISEX/0 CHP/ISIN/ CHP/ISEX/ 13
13 Chlamydia trachomatis PCR Kit Das Kit dient zum Nachweis von Chlamydia trachomatis genomischer und Plasmid-DNA mittels Realtime PCR. Konservative DNA Region des 16S rdna Gens und kryptischen Plasmids Chlamydia trachomatis, inkl. Mutationen und Deletionen auf dem kryptischen Plasmid (inkl. Schwedische Variante) Sensitivität (LOD) 0,984 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Chlamydia trachomatis HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Vaginal-/Rektal-/Pharyngial-Abstrich, Sperma, Urin Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System StepOne Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System qtower 2.0/2.2 QCMD & INSTAND e.v. (Ergebnisse bei 14 GeneProof Chlamydia trachomatis PCR Kit CHT/ISIN/0 CHT/ISEX/0 CHT/ISIN/0 CHT/ISEX/0 CHT/ISIN/ CHT/ISEX/
14 Presto CT & NG PCR Kit Das Kit dient zum Nachweis von Chlamydia trachomatis-(ct) und Neisseria gonorrhoeae-dna (NG) mittels. CT & NG Sensitivität (LOD) 0,1 lfu/test (CT); 2,5 G. Eq./test (NG) Kanäle FAM: CT VIC: NG Cy5: Interne Kontrolle (IS) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle Vaginal-/Zervikal-/Urethral-/Rektal-Abstriche, Urin Von -20 C bis -80 C -Geräte mit FAM, VIC, ROX, Cy5 Fluorophore QCMD Goffin Presto CT/NG RT Duplex PCR Kit GM CG
15 VRE PCR Kit Das Kit dient zum Nachweis von Vancomycinresistenten Enterokokken (VRE), Enterococcus faecalis und Enterococcus faecium mittels. VanA und VanB Gen Enterococcus faecalis und Enterococcus faecium Sensitivität (LOD) VanA: 1,398 Kopien/µl (Wahrscheinlichkeit 95%) VanB: 1,026 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: VanA Cy5: VanB HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Vollblut, Sputum, Stuhl, Urin -85 C bis -10 C CFX96 /Dx Real-Time PCR Detection System Light 480 LineGene 9600 Rotor-Gene 3000/Q SLAN Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei 16 GeneProof VRE PCR Kit VRE/ISIN/0 VRE/ISEX/0 VRE/ISIN/0 VRE/ISEX/0 VRE/ISIN/ VRE/ISEX/
16 ESBL PCR Kit Das Kit dient zum Nachweis von blashv und blactx-m Genen, die den ESBL (Extended-Spectrum BetaLactamases) Genotyp bestimmen mittels. blashv und blactx-m Gene Die SHV-ESBL Polymorphismen in den Positionen 179, 238 und 240; CTX-M-1, CTX-M-2, CTX-M-8, CTX-M-9, CTX-M- Cluster Sensitivität (LOD) für SHV: 0,365 Kopien/μl (Wahrscheinlichkeit 95%) für CTX: 1,281 Kopien/μl (Wahrscheinlichkeit 95%) Kanäle FAM: SHV Mutation 238 und 240 Cy5: SHV Mutation 179 HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Sputum, Nasalsekret, Nasopharyngialsekret Von -10 C bis -85 C Applied Biosystems 70 Real-Time PCR System CFX96TM/Dx Real-Time PCR Detection System LineGene 9600 Rotor-Gene 3000/Q SLAN Real-Time PCR System crobee Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof ESBL PCR Kit ESBL/ISIN/0 ESBL/ISEX/0 ESBL/ISIN/0 ESBL/ISEX/0 ESBL/ISIN/ ESBL/ISEX/ 17
17 Legionella pneumophila PCR Kit Das Kit dient zum Nachweis von Legionella pneumophila-dna mittels. Konservative DNA Region des 16S rdna Gens L. pneumophila (Stamm Corby, Stamm Lens, Stamm Paris, subsp. Pneumophila, subsp. Fraseri, subsp. Pascullei) Sensitivität (LOD) 1,398 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Legionella pneumophila HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Bronchioalveolarlavage, Sputum Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei 18 GeneProof Legionella pneumophila PCR Kit LP/ISIN/0 LP/ISEX/0 LP/ISIN/0 LP/ISEX/0 LP/ISIN/ LP/ISEX/
18 Mycobacterium tuberculosis PCR Kit Das Kit dient zum Nachweis des Mycobacterium tuberculosis-dna-komplexes (MTC) IS6110 mittels. Spezifische multi-copy DNA Insertionssequenz IS6110 Mycobacterium tuberculosis complex (M. tuberculosis, M. bovis, M. africanum, M. microti and vaccine strain BCG) Sensitivität (LOD) 0,06 Genome/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Mycobacterium tuberculosis HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Sputum, Bronchiallavage, Liquor, Biopsien, Knochenmark, Stuhl, Magenspülung Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System StepOne Real-Time PCR System CFX96 Real-Time PCR Detection System DX-Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Mycobacterium tuberculosis PCR Kit MT/ISIN/0 MT/ISEX/0 MT/ISIN/0 MT/ISEX/0 MT/ISIN/ MT/ISEX/ 19
19 Mycoplasma pneumoniae PCR Kit Das Kit dient zum Nachweis von Mycoplasma pneumoniae-dna mittels. Konservative DNA-Region M181 für das CARDS Toxin Mycoplasma pneumoniae Sensitivität (LOD) 1,331 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Mycoplasma pneumoniae HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Sputum, Oropharyngial-/Nasopharyngial-Abstrich Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei 20 GeneProof Mycoplasma pneumoniae PCR Kit MP/ISIN/0 MP/ISEX/0 MP/ISIN/0 MP/ISEX/0 MP/ISIN/ MP/ISEX/
20 Neisseria gonorrhoeae PCR Kit Das Kit dient zum Nachweis von genomischer Neisseria gonorrhoeae-dna mittels. Konservative DNA-Region des single copy pora-pseudo- und 16S rdna Gens Neisseria gonorrhoeae Sensitivität (LOD) 0,219 Genome/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Neisseria gonorrhoeae HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) Urethral-/Zervikal-/Rektal-Abstrich, Sperma, Urin Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System StepOne Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Neisseria gonorrhoeae PCR Kit NG/ISIN/0 NG/ISEX/0 NG/ISIN/0 NG/ISEX/0 NG/ISIN/ NG/ISEX/ 21
21 VIROLOGIE 22
22 Adenovirus (ADV) PCR Kit Das Kit dient zum Nachweis von Adenovirus-DNA mittels. Konservative DNA Region des E2B-Gens Adenovirus Sensitivität (LOD) 2 Kopien/ml Kanäle FAM: Adenovirus (ADV) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, Plasma, Urin, Stuhl, Abstriche (Nasopharynx, Oropharynx) Von -10 C bis -85 C Rotor-Gene 3000/Q Light 2.0/480 CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Adenovirus (ADV) PCR Kit ADV/ISIN/0 ADV/ISEX/0 ADV/ISIN/0 ADV/ISEX/0 ADV/ISIN/ ADV/ISEX/ 23
23 BK/JC-Virus (BKV/JCV) PCR Kit Das Kit dient zum Nachweis von BKV- und JCV-DNA mittels. Konservative DNA Region des single copy Gens zwischen dem VP1 und VP2 Protein BK-Virus (BKV) und JC-Virus (JCV) Sensitivität (LOD) 0,596 Kopien/µl (BKV) (Wahrscheinlichkeit 95%) 0,528 Kopien/µl (JCV) (Wahrscheinlichkeit 95%) Kanäle FAM: BK-Virus (BKV) Cy5: JC-Virus (JCV) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, Liquor, Urin Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei 24 Kat. Nr. GeneProof BK- und JC-Virus (BKV/JCV) PCR Kit BKJC/ISIN/0 BKJC/ISEX/0 BKJC/ISIN/0 BKJC/ISEX/0 BKJC/ISIN/ BKJC/ISEX/
24 Cytomegalovirus (CMV) PCR Kit Das Kit dient zum Nachweis von CMV-DNA mittels. Konservative DNA-Region des single copy Gens für das IE Antigen Exon 4 Cytomegalovirus (CMV) Sensitivität (LOD) 0,907 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Cytomegalovirus (CMV) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, EDTA-Plasma, Liquor, Knochenmark, Stuhl, Urin Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System qtower 2.0/2.2 QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Cytomegalovirus (CMV) PCR Kit CMV/ISIN/0 CMV/ISEX/0 CMV/ISIN/0 CMV/ISEX/0 CMV/ISIN/ CMV/ISEX/
25 Epstein-Barr Virus (EBV) PCR Kit Das Kit dient zum Nachweis von EBV-DNA mittels. Konservative DNA Region des nukleären Antigens 1 (EBNA1) Epstein-Barr Virus Typ 1, Epstein-Barr Virus Typ 2 Sensitivität (LOD) 1,405 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Epstein-Barr Virus (EBV) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, Liquor Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System StepOne Real-Time PCR System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei 26 GeneProof Epstein-Barr Virus (EBV) PCR Kit EBV/ISIN/0 EBV/ISEX/0 EBV/ISIN/0 EBV/ISEX/0 EBV/ISIN/ EBV/ISEX/
26 Hepatitis B Virus (HBV) PCR Kit Das Kit dient zum Nachweis von Hepatitis B Virus-RNA mittels. Konservative DNA Region des single copy Gens für den TranskriptionsTransaktivator (px) HBV Genotyp A - H, HBV pre-core Mutanten (HBeAg negativ) Sensitivität (LOD) 26,124 lu/ml (Wahrscheinlichkeit 95%) Messbereich: von 600 lu/ml lu/ml. 1lU/ml = 4,2 Kopien/ml Kanäle FAM: Hepatitis B Virus (HBV) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Plasma, Serum Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System qtower 2.0/2.2 QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Hepatitis B Virus (HBV) PCR Kit HBV/ISEX/0 HBV/ISEX/0 HBV/ISEX/ 27
27 Hepatitis C Virus (HCV) PCR Kit Das Kit dient zum Nachweis von Hepatitis C Virus-RNA mittels. Konservative Region der 5' UTR Sequenz HCV Genotyp 1-6 Sensitivität (LOD) 18,354 lu/ml (Wahrscheinlichkeit 95%) Messbereich: von lu/ml. Reporting Units: 1lU/ml = 3,2 Kopien/ml Kanäle FAM: Hepatitis C Virus (HCV) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Plasma, Serum Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei 28 GeneProof Hepatitis C Virus (HCV) PCR Kit HCV/ISEX/0 HCV/ISEX/0 HCV/ISEX/
28 Herpes Simplex Virus 1 & 2 (HSV-1/2) PCR Kit Das Kit dient zum Nachweis von HSV-1-DNA und HSV-2-DNA mittels. Konservative DNA Region des single copy Gens für das Glykoprotein B (gb) Herpes simplex Virus Typ 1 (HSV-1) Herpes simplex Virus Typ 2 (HSV-2) Sensitivität (LOD) 0,764 Kopien/µl (Wahrscheinlichkeit 95%) - HSV-1 1,309 Kopien/µl (Wahrscheinlichkeit 95%) - HSV-2 Kanäle FAM: Herpes Simplex Virus 1 (HSV-1) Cy5: Herpes Simplex Virus 2 (HSV-2) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, Plasma, Liquor, Urin, Abstrich Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 480 Applied Biosystems 70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Herpes Simplex Virus 1/2 (HSV-1/2) PCR Kit HSV/ISIN/0 HSV/ISEX/0 HSV/ISIN/0 HSV/ISEX/0 HSV/ISIN/ HSV/ISEX/ 29
29 Herpes Simplex Virus 1 (HSV-1) PCR Kit Das Kit dient zum Nachweis von HSV-1-DNA mittels. Konservative DNA Region des single copy Gens für das Glykoprotein B (gb) Herpes simplex Virus Typ 1 (HSV-1) Sensitivität (LOD) 0,764 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Herpes Simplex Virus 1 (HSV-1) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, Plasma, Liquor, Urin, Abstrich Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System StepOne Real-Time PCR System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei 30 GeneProof Herpes Simplex Virus 1 (HSV-1) PCR Kit HSV1/ISIN/0 HSV1/ISEX/0 HSV1/ISIN/0 HSV1/ISEX/0 HSV1/ISIN/ HSV1/ISEX/
30 Herpes Simplex Virus 2 (HSV-2) PCR Kit Das Kit dient zum Nachweis von HSV-2-DNA mittels. Konservative DNA Region des single copy Gens für das Glykoprotein B (gb) Herpes simplex Virus Typ 2 (HSV-2) Sensitivität (LOD) 1,309 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Herpes Simplex Virus 2 (HSV-2) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, Plasma, Liquor, Urin, Abstrich Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Herpes Simplex Virus 2 (HSV-2) PCR Kit HSV2/ISIN/0 HSV2/ISEX/0 HSV2/ISIN/0 HSV2/ISEX/0 HSV2/ISIN/ HSV2/ISEX/ 31
31 HIV Typ 1 (HIV-1) PCR Kit Das Kit dient zum Nachweis von HIV-1-RNA mittels. Dual target: LTR und GaG Gen Human immunodeficiency virus Typ 1 (HIV-1) Sensitivität (LOD) 20,045 lu/ml (Wahrscheinlichkeit 95%) Messbereich: von 20, lu/ml. Reporting Units: 1lU/ml = 0,52 Kopien/ml. Genauigkeit innerhalb von lu/ml liegt bei 0,5 log. Kanäle FAM: HIV Typ 1 (HIV-1) HEX: Interne Kontrolle (GAPDH) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Plasma Von -10 C bis -85 C Applied Biosystems 7300/70 Real-Time PCR System AriaMx Real-Time PCR System CFX Connect / CFX96 / Dx Real-Time PCR Detection System Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System Rotor-Gene 3000/6000/Q SLAN Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei 32 GeneProof HIV Typ 1 (HIV-1) PCR Kit HIV1/ISEX/0 HIV1/ISEX/0 HIV1/ISEX/
32 JC-Virus (JCV) PCR Kit Das Kit dient zum Nachweis von JCV-DNA mittels. Konservative DNA Region des single copy Gens zwischen dem VP1 und VP2 Protein JC-Virus (JCV) Sensitivität (LOD) 0,528 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: JC-Virus (JCV) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, Liquor, Urin Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof JC-Virus (JCV) PCR Kit JCV/ISIN/0 JCV/ISEX/0 JCV/ISIN/0 JCV/ISEX/0 JCV/ISIN/ JCV/ISEX/ 33
33 Varicella-Zoster Virus (VZV) PCR Kit Das Kit dient zum Nachweis von VZV-DNA mittels. Konservative DNA Region des ORF62 Gens Varicella-Zoster Virus (VZV) Sensitivität (LOD) 0,995 Kopien/µl (Wahrscheinlichkeit 95%) Kanäle FAM: Varicella-Zoster Virus (VZV) HEX: Interne Kontrolle (IS) Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) Extraktions-/ Inhibitionskontrollen PCR Inhibitionskontrolle (ISIN-Version) Extraktions- und PCR Inhibitionskontrolle (ISEX-Version) EDTA-Blut, EDTA-Plasma, Serum, Liquor, Abstrich, Bronchiallavage Von -20 C bis -80 C Rotor-Gene 3000/6000/Q Light 2.0/480 Applied Biosystems 7300/70 Real-Time PCR System CFX96 Real-Time PCR Detection System Dx Real-Time System SLAN Real-Time PCR System Mx3005P QPCR System QCMD & INSTAND e.v. (Ergebnisse bei 34 GeneProof Varicella Zoster Virus (VZV) PCR Kit VZV/ISIN/0 VZV/ISEX/0 VZV/ISIN/0 VZV/ISEX/0 VZV/ISIN/ VZV/ISEX/
34 MULTIPLEX KITS 35
35 Bacterial CNS Flow Chip Multiplex PCR/Hybridisierungs-Kit Das Kit dient zum Nachweis von Bakterien und Pilzen, die für humane Meningitis und Enzephalitis verantwortlich sind. Die Detektion erfolgt mittels PCR und reverser Dot-Blot-Hybridisierung. Das Bacterial CNS Flow chip Kit erlaubt den gleichzeitigen Nachweis von neun Bakterien- (Neisseria meningitidis, Streptococcus pneumoniae, Streptococcus agalactiae, Listeria monocytogenes, Haemophilus influenzae, Mycobacterium tuberculosis complex, Treponema pallidum, Coxiella burnetti, and Borrelia burgdorferi) und einer Pilzspezies (Cryptococcus neoformans). Das Kit dient zur in-vitro Diagnostik und ermöglicht qualitative Ergebnisse. Multiplex PCR mit reverser Dot-Blot-Hybridisierung Neisseria meningitidis Haemophilus influenzae Streptococcus pneumoniae Streptococcus agalactiae Listeria monocytogenes Cryptococcus neoformans Treponema pallidum Mycobacterium tuberculosis complex Coxiella burnetti Borrelia burgdorferi ctra gyrb ply cfb hly 18S PolA IS6110 trans orp Sensitivität Neisseria meningitidis Haemophilus influenzae Streptococcus pneumoniae Streptococcus agalactiae Listeria monocytogenes Cryptococcus neoformans Treponema pallidum Mycobacterium tuberculosis complex Coxiella burnetti Borrelia burgdorferi 10 Kopien 10 Kopien 40 Kopien Kopien 40 Kopien 10 Kopien Kopien 10 Kopien Kopien Kopien Liquor PCR Kit: -20 C, Hybridisierungs-Kit: 4 C Alle Endpoint- 36 Master Diagnóstica Bacterial CNS Flow Chip Kit MAD M-HS MAD M-HS
36 Viral CNS Flow Chip Multiplex PCR/Hybridisierungs-Kit Das Kit dient zum Nachweis von Viren, die für humane Meningitis und Enzephalitis verantwortlich sind. Die Detektion erfolgt mittels PCR und reverser Dot-Blot-Hybridisierung. Das Viral CNS Flow chip Kit erlaubt den gleichzeitigen Nachweis von acht Virusspezies: Herpes Simplex 1 (HSV-1), Herpes Simplex 2 (HSV-2), Cytomegalovirus (CMV), Epstein-Barr Virus (EBV), Varicella-Zoster (VZV), Toscana (TOSV), Enterovirus (EV) und Parechovirus (HPeV). Das Kit dient zur in-vitro Diagnostik und ermöglicht qualitative Ergebnisse. Multiplex PCR mit reverser Dot-Blot-Hybridisierung / Herpes Simplex 1 Herpes Simplex 2 Cytomegalovirus Epstein-Barr Varicella-Zoster Toscana Virus Enterovirus * Parechovirus Gen-Region L1 US5, envlope Glykoprotein J. UL48, transactivating Tegument Protein VP16 HCMVUL111A, ORF in transforming Region BALF5, DNA Polymerase ORF31 core Gen Nukleoprotein Gen 5'UTR Polyprotein Sensitivität Herpes Simplex 1 Herpes Simplex 2 Cytomegalovirus Epstein-Barr Varicella-Zoster Toscana Virus Enterovirus * Parechovirus 10 Kopien 10 Kopien 40 Kopien 10 Kopien 40 Kopien 10 Kopien 40 Kopien 40 Kopien Liquor PCR Kit: -20 C, Hybridisierungs-Kit: 4 C Alle Endpoint- * Coxsackievirus A: A2, A3, A4, A5, A6, A7, A8, A9, A10, A11, A12, A13, A14, A15, A16, A17, A18, A19, A20, A21, A22, A24. Coxsackievirus B: B1, B2, B3, B4, B5, B6. Poliovirus: 1, 2, 3 Echovirus: E1, E2, E3, E4, E5, E6, E7, E9, E11, E12, E13, E14, E15, E16, E17, E18, E19, E20, E21, E24, E, E26, E27, E29, E30, E31, E32, E33, E68, E70, E71. Master Diagnóstica Viral CNS Flow Chip Kit MAD M-HS MAD M-HS
37 HPV Direct Flow Chip Multiplex PCR/Hybridisierungs-Kit Das Kit dient zur Genotypisierung von HPV mittels PCR und reverser Dot-Blot-Hybridisierung. Nachgewiesen werden 16 Low-Risk und 16 High-Risk HPV-Genotypen: High-Risk: 16, 18, 26, 31, 33, 35, 39, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82. Low-Risk: 6, 11, 40, 42, 43, 44, 54, 55, 61, 62, 67, 69, 70, 71, 72, 81, 84, 89 (= CP6108) Zum Nachweis ist keine vorherige DNA-Extraktion notwendig. Lediglich bei in Formalin fixierten, Paraffin eingebetteten Proben wird ein Reinigungskit zur Entfernung des Paraffins benötigt. Das Kit dient zur in-vitro Diagnostik und ermöglicht qualitative Ergebnisse. PCR mit reverser Dot-Blot-Hybridisierung Gen-Region L1 HPV Direct Flow Chip: 18 HPV High-Risk und 18 HPV Low-Risk Sensitivität (LOD) 1-10 virale Genomäquivalente/Reaktion Abstriche, Dünnschichtzytologien, Paraffinschnitte PCR-Reagenzien: -20 C; Hybridisierungsreagenzien: 2-8 C Alle Endpoint- Master Diagnóstica HPV Direct Flow Chip MAD MUT-HS MAD MUT-HS MAD MUT-HS MAD MUT-HS MAD M 30 Master Diagnóstica Paraffin Tissue Processing Kit 38
38 Sepsis Flow Chip Multiplex PCR/Hybridisierungs-Kit Das Sepsis Flow Chip Kit erlaubt den gleichzeitigen Nachweis von mehreren Sepsis-Pathogenen inkl. Gram+Kokken, Gram-Bazillen, Pilzen und Antibiotika-resistenten Formen, MRSA, meca, vana, ESBL und Carbapenemasen. Das Kit dient zur in-vitro Diagnostik und ermöglicht qualitative Ergebnisse. Multiplex PCR mit reverser Dot-Blot-Hybridisierung / Koagulase-Negative Staphylokokken Staphylococcus aureus Streptococcus spp. Streptococcus pneumoniae Streptococcus agalactiae Listeria monocytogenes Enterococcus spp. Pseudomonas aeruginosa Acinetobacter baumannii Neisseria meningitidis Stenotrophomonas maltophilia Escherichia coli Klebsiella pneumoniae Serratia marcescens Enterobacteriaceae Proteus spp. Candida spp. Candida albicans 16S rdna nuc 16S rdna cpsa 16S rdna 16S rdna 16S rdna ecfx 16S rdna 16S rdna 16S rdna 16S rdna khe 16S rdna 16S rdna 16S rdna 18S-5.8S ITS rdna 18S-5.8S ITS rdna Sensitivität Zwischen 10 und Genomäquivalenten Blutkultur, rektale Abstriche PCR Kit: -20 C, Hybridisierungs-Kit: 4 C Alle Endpoint- Master Diagnóstica Sepsis Flow Chip Kit MAD M-HS MAD M-HS MAD M-HS MAD M-HS
39 Tick-borne Bacteria Flow Chip Multiplex PCR/Hybridisierungs-Kit Das Kit dient zum Nachweis Zecken-übertragbarer Erreger mittels Multiplex-PCR und reverser DotBlot-Hybridisierung. Der Nachweis erfolgt nach vorheriger DNA-Extraktion. Multiplex-PCR mit reverser Dot-Blot-Hybridisierung Anaplasma spp. rrna AN A. phagocytophilum MSP2 AN Ehrlichia chaffeensis, E. ewingii und Candidatus Neoehrlichia mikurensis 16S rrna EH Bartonella spp. 16S BAR Bartonella spp. glta BAR-2 Borrelia spp. 16S rrna BOR Coxiella burnetii Transposase Is1111 COX Francisella spp. kda TUL4FR Rickettsia spp. 23A-5S GR Rickettsia typhus group 23S-5S TG Rickettsia spotted fever group 23S-5S SFG Borrelia spp., Bartonella spp., Anaplasma spp. (inkl. Candidatus Neoehrlichia mikurensis), Coxiella, Ehrlichia, Francisella spp., Rickettsia Sensitivität (LOD) 10 Kopien/µl EDTA-Blut, Gewebeproben, Zecke PCR-Reagenzien: -20 C; Hybridisierungsreagenzien: 2-8 C Alle Endpoint- 40 Master Diagnóstica Tick-borne Bacteria Flow Chip MAD M-HS MAD M-HS
40 HUMANGENETIK 41
41 Factor II Prothrombin PCR Kit Das Kit dient zum Nachweis der G20210A Mutation im Prothrombin Gen (Faktor II) mittels Real-time PCR. Das DNA-Fragment, auf dem die G20210A Mutation beherbergt sein kann, wird durch PCRAmplifikation in Anwesenheit von allelspezifischen, fluoreszenzmarkierten Hybridisierungssonden nachgewiesen. Mit dem Assay kann eine Alleldiskriminierung der Genotypen homozygot, heterozygot und Wildtyp mit %iger Präzision vorgenommen werden. DNA-Sequenz von Prothrombin-Gen für plasmatisches Glykoprotein (human factor II) G20210A single-nukleotid Mutation in der non-encoding Region des Gens Qualitative Detektion Mutation vorhanden/nicht vorhanden Evaluierung G/G-Standard Homozygote (Wild-Typ) A/A-Mutante Homozygote A/G-Heterozygote EDTA-Blut Von -85 C bis -10 C Applied Biosystems 7300/70 Real-Time PCR System CFX Connect / CFX96 / Dx Real-Time PCR Detection System Light 480 LineGene 9600 Rotor-Gene 3000/6000 SLAN Real-Time PCR System StepOne TM Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei 42 GeneProof Factor II Prothrombin PCR Kit FII/0 FII/
42 Factor V Leiden PCR Kit Das Kit dient zum Nachweis der G1691A Mutation im Faktor V Gen (Leiden Mutation) mittels Real-time PCR. Das DNA-Fragment, auf dem die G1691A Mutation beherbergt sein kann, wird durch PCRAmplifikation in Anwesenheit von allelspezifischen, fluoreszenzmarkierten Hybridisierungssonden nachgewiesen. Mit dem Assay kann eine Alleldiskriminierung der Genotypen homozygot, heterozygot und Wildtyp mit %iger Präzision vorgenommen werden. DNA-Sequenz des Hämokoagulation factor V Gens (Leiden mutation) G1691A single-nukleotid Mutation in Exon 10 (Arg 6 Gln) Qualitative Detektion Mutation vorhanden/nicht vorhanden Evaluierung G/G-Standard Homozygote (Wild-Typ) A/A-Mutante Homozygote A/G-Heterozygote EDTA-Blut Von -85 C bis -10 C Applied Biosystems 7300/70 Real-Time PCR System CFX Connect / CFX96 / Dx Real-Time PCR Detection System Light 2480 LineGene 9600 Rotor-Gene 3000/6000 SLAN Real-Time PCR System StepOne TM Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof Factor V Leiden PCR Kit FV/0 FV/ 43
43 MTHFR C677T PCR Kit Das Kit dient zum Nachweis der C677T Mutation auf dem 5,10-Methylentetrahydrofolatreduktase-Gen (MTHFR) mittels. Das DNA-Fragment, auf dem die C667T Mutation beherbergt sein kann, wird durch PCR-Amplifikation in Anwesenheit von allelspezifischen, fluoreszenzmarkierten Hybridisierungssonden nachgewiesen. Mit dem Assay kann eine Alleldiskriminierung der Genotypen homozygot, heterozygot und Wildtyp mit %iger Präzision vorgenommen werden. DNA-Sequenz eines Methylentetrahydropholat-Reduktase-Gens (MTHFR) C677T single-nukleotid Mutation (Ala 222 Val) Qualitative Detektion Mutation vorhanden/nicht vorhanden Evaluierung C/C-Standard Homozygote (Wild-Typ) T/T-Mutante Homozygote C/T-Heterozygote EDTA-Blut Von -85 C bis -10 C Applied Biosystems 7300/70 Real-Time PCR System CFX Connect / CFX96 / Dx Real-Time PCR Detection System Light 2.0/480 LineGene 9600 Rotor-Gene 3000/6000 SLAN Real-Time PCR System StepOne TM Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei 44 GeneProof MTHFR C677T PCR Kit M677/0 M677/
44 MTHFR A1298C PCR Kit Das Kit dient zum Nachweis der A1298C Mutation auf dem 5,10-MethylentetrahydrofolatreduktaseGen (MTHFR) mittels. Das DNA-Fragment, auf dem die A1298C Mutation beherbergt sein kann, wird durch PCR-Amplifikation in Anwesenheit von allelspezifischen, fluoreszenzmarkierten Hybridisierungssonden nachgewiesen. Mit dem Assay kann eine Alleldiskriminierung der Genotypen homozygot, heterozygot und Wildtyp mit %iger Präzision vorgenommen werden. DNA-Sequenz eines Methylentetrahydropholat-Reduktase-Gens (MTHFR) A1298C single-nucleotide Mutation (Glu 429 Ala) Qualitative Detektion Mutation vorhanden/nicht vorhanden Evaluierung A/A-Standard Homozygote (Wild-Typ) C/C-Mutante Homozygote A/C-Heterozygote EDTA-Blut Von -85 C bis -10 C Applied Biosystems 7300/70 Real-Time PCR System CFX Connect / CFX96 / Dx Real-Time PCR Detection System Light 2.0/480 LineGene 9600 Rotor-Gene 3000/6000 SLAN Real-Time PCR System StepOne TM Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei GeneProof MTHFR A1298C PCR Kit M1298/0 M1298/ 45
45 PAI-1 Genotypisierung PCR Kit Dieses -Kit dient zum Nachweis von Polymorphismus in der Promotorregion des PAI-1 Gens. Das Verfahren basiert auf der Amplifikation und dem Nachweis der Targetsequenz mittels allelspezifischen, fluorophormarkierten Sonden. Zielsequenz ist der Insertions- bzw. DeletionsPolymorphismus 4G/5G. Die Präsenz der Wildtyp Allele (5G/5G) wird vom FAM-Fluorophor und Vorhandensein der mutanten Allele (4G/4G) vom HEX-Fluorophor angezeigt. Ein heterozygoter Genotyp (4G/5G) wird auf beiden Kanälen ausgewiesen. Das Nachweis-Kit enthält einen gebrauchsfertigen Master Mix und beruht auf der sogenannten Hot-Start-PCR, die nicht-spezifische minimiert und maximale Sensitivität bietet. Dieses Kit ist zur In-vitro-Diagnostik bestimmt. DNA-Sequenz der Promotorregion des PAI-Gens, Typ 1 (Serpin 1) Einzel-Nukleotid Insertion/Deletion von Guanosin in der Position 675 Qualitative Detektion Mutation vorhanden/nicht vorhanden Evaluierung 5G/5G-Standard Homozygote 4G/4G-Mutante Homozygote 4G/5G-Heterozygote Kontaminationsschutz Uracil-DNA-Glycosylase (UDG) EDTA-Blut Von -10 C bis -85 C Applied Biosystems 7300/70 Real-Time PCR System CFX Connect / CFX96 / Dx Real-Time PCR Detection System Light 480 LineGene 9600 Rotor-Gene 3000/6000/Q SLAN Real-Time PCR System QCMD & INSTAND e.v. (Ergebnisse bei 46 GeneProof PAI-1 Genotypisierung PCR Kit PAI/0 PAI/
46 DNA & RNA ISOLIERUNG 47
47 PathogenFree DNA Isolierungs-Kit Das Kit dient zur Isolierung von DNA aus Blut, EDTA-Blut, Zellkultur, Serum, Plasma, Körperflüssigkeiten und anderen klinischen Proben. Kat. Nr. GeneProof PathogenFree DNA Isolation kit IDNA0 IDNA2 2 PathogenFree RNA Isolierungs-Kit Das Kit dient zur Isolierung von RNA aus biologischen Proben, Serum und Plasma. Es ist nicht für Vollblut geeignet. 48 GeneProof PathogenFree RNA Isolation kit IRNA0 IRNA2 2
48 GERÄTE 49
49 HybriSpot 12 (HS12) DNA-Hybridisierungs-System Das HybriSpot-12-System ist eine Plattform zur reversen Dot-Blot-Hybridisierung nach PCRAmplifikation: siehe Seiten Die Plattform bietet die Möglichkeit 1-12 Proben (Amplifikate) pro Lauf zu bearbeiten. Nach manueller Aufnahme der Chips mit einer CCD-Kamera erfolgt die Auswertung des Arrays/Chips automatisch. Das Gerät wird mit Computer und Software geliefert. HybriSpot 24 (HS24) DNA-Hybridisierungs-System Das HybriSpot-24-System ist eine automatisierte Plattform zur reversen Dot-Blot-Hybridisierung nach PCR-Amplifikation: siehe Seiten Das System kann 1-24 Proben (Amplifikate) pro Lauf bearbeiten. Die Proben werden auf zwei Module à 12 Positionen verteilt. Diese zwei Module können individuell mit angesteuert werden. Dies ermöglicht auch die gleichzeitige Bearbeitung von zwei unterschiedlichen Testkits. Die Auswertung des Arrays/Chips sowie die Erstellung eines Ergebnisreports erfolgt automatisch. Das Gerät wird mit Computer und Software geliefert. Technische Spezifikationen hybrispot12 (HS12) hybrispot24 (HS24) Manuelles Hybridisierungssystem Automatisiertes Hybridisierungssystem Probenkapazität 1-12 pro Lauf 1-24 pro Lauf UV/DNA Dekontamination NEIN JA Betriebstemperatur 15 C bis 32 C 15 C bis 32 C Abmessungen* 3 x 230 x 200 mm 690 x 605 x 840 mm Gewicht 4 kg 55 kg Manuelle Arbeitszeit (max.) 90 min 45 min VIT-HS12 VIT-HS24 * zzgl. cm Breite für den PC
50 PRODUKTLISTE 51
51 BAKTERIOLOGIE Beschreibung Kontrolle intern Kontrolle separat Best. GeneProof Bordetella pertussis/parapertussis PCR Kit Nachweis von Bordetella pertussis/parapertussis-dna Zielsequenz: IS 1 und IS 2 BP/ISIN/0 BP/ISIN/0 BP/ISIN/ BP/ISEX/0 BP/ISEX/0 BP/ISEX/ GeneProof Borrelia burgdorferi PCR Kit Nachweis von Borrelia burgdorferi sensu lato Zielsequenz: 16S RNA BB/ISIN/0 BB/ISIN/0 BB/ISIN/ BB/ISEX/0 BB/ISEX/0 BB/ISEX/ GeneProof Chlamydia pneumoniae PCR Kit Nachweis von Chlamydia pneumoniae-dna Zielsequenz: ompa CHP/ISIN/0 CHP/ISIN/0 CHP/ISIN/ CHP/ISEX/0 CHP/ISEX/0 CHP/ISEX/ GeneProof Chlamydia trachomatis PCR Kit Nachweis von Chlamydia trachomatis-dna Zielsequenz: 16S RNA und Sequenz auf kryptischem Plasmid CHT/ISIN/0 CHT/ISIN/0 CHT/ISIN/ CHT/ISEX/0 CHT/ISEX/0 CHT/ISEX/ Presto CT/NG PCR Kit Nachweis von Chlamydia trachomatis- und Neisseria gonorrhoeae-dna; Zielsequenz: kryptisches Plasmid (CT) und opa (NG) GM CG 1600 GeneProof VRE PCR Kit Nachweis von vancomycinresistenten Enterokokken Zielsequenz: VanA und VanB VRE/ISIN/0 VRE/ISIN/0 VRE/ISIN/ VRE/ISEX/0 VRE/ISEX/0 VRE/ISEX/ GeneProof ESBL PCR Kit Nachweis des Extended-Spectrum Beta-Laktamase Genotyps (ESBL). Zielsequenz: blashv & blactx-m ESBL/ISIN/0 ESBL/ISIN/0 ESBL/ISIN/ ESBL/ISEX/0 ESBL/ISEX/0 ESBL/ISEX/ GeneProof Legionella pneumophila PCR Kit Nachweis von Legionella pneumophila-dna Zielsequenz: 16S RNA LP/ISIN/0 LP/ISIN/0 LP/ISIN/ LP/ISEX/0 LP/ISEX/0 LP/ISEX/ GeneProof Mycobacterium tuberculosis PCR Kit Nachweis des Mycobacterium tuberculosis Komplexes Zielsequenz: IS6110 MT/ISIN/0 MT/ISIN/0 MT/ISIN/ MT/ISEX/0 MT/ISEX/0 MT/ISEX/ GeneProof Mycoplasma pneumoniae PCR Kit Nachweis von Mycoplasma pneumoniae-dna Zielsequenz: CARDS Toxin MP/ISIN/0 MP/ISIN/0 MP/ISIN/ MP/ISEX/0 MP/ISEX/0 MP/ISEX/ GeneProof Neisseria gonorrhoeae PCR Kit Nachweis von Neisseria gonorrhoeae-dna Zielsequenz: pora Pseudogen NG/ISIN/0 NG/ISIN/0 NG/ISIN/ NG/ISEX/0 NG/ISEX/0 NG/ISEX/ Multiplex PCR Beschreibung Master Diagnóstica Tick-borne Bacteria Flow Chip Kit Nachweis von Zoonosen (Borrelia, Coxiella, Ehrlichia, Anaplasma, Bartonella, Francisella, Rickettsia) mit reverser Dot-Blot-Hybridisierung MAD M-HS12-24 MAD M-HS Master Diagnóstica Bacterial CNS Flow Chip Kit Nachweis von bakteriellen MeningitisErregern mit reverser Dot-Blot-Hybridisierung MAD M-HS12-24 MAD M-HS Master Diagnóstica Viral CNS Flow Chip Kit Nachweis von viralen Meningitis-Erregern mit reverser Dot-Blot-Hybridisierung MAD M-HS12-24 MAD M-HS Master Diagnóstica HPV Direct Flow Chip Kit HPV-Genotypisierung mit reverser Dot-BlotHybridisierung (18 low-risk & 18 high-risk Genotypen) MAD MUT-HS12-24/-48 MAD MUT-HS24-24/-48 24/48 24/48 Master Diagnóstica Sepsis Flow Chip Kit Nachweis von Sepsiserregern und Antibiotika-Resistenzen mit reverser Dot-Blot-Hybridisierung MAD M-HS12-24/-48 MAD M-HS24-24/-48 24/48 24/48 Master Diagnóstica Paraffin tissue processing Kit Geeignet zur Isolierung von Zellen aus in Formalinfixierten, Paraffineingebetteten Proben MAD M MULTIPLEX 52 Best. 30
52 VIROLOGIE Beschreibung Kat. Nr. Kontrolle intern Kontrolle separat Best. GeneProof Adenovirus (ADV) PCR Kit Quantitativer Nachweis von ADV-DNA. Zielsequenz: E2B Gen ADV/ISIN/0 ADV/ISIN/0 ADV/ISIN/ ADV/ISEX/0 ADV/ISEX/0 ADV/ISEX/ GeneProof Cytomegalovirus (CMV) PCR Kit Quantitativer Nachweis von CMV-DNA. Zielsequenz: Exon4IE Antigen CMV/ISIN/0 CMV/ISIN/0 CMV/ISIN/ CMV/ISEX/0 CMV/ISEX/0 CMV/ISEX/ GeneProof Epstein-Barr Virus (EBV) PCR Kit Quantitativer Nachweis von EBV-DNA. Zielsequenz: EBNA1 Antigen EBV/ISIN/0 EBV/ISIN/0 EBV/ISIN/ EBV/ISEX/0 EBV/ISEX/0 EBV/ISEX/ GeneProof Hepatitis B Virus (HBV) PCR Kit Quantitativer Nachweis von HBV-DNA. Zielsequenz: gorfx HBV/ISEX/0 HBV/ISEX/0 HBV/ISEX/ GeneProof Hepatitis C Virus (HCV) PCR Kit Quantitativer Nachweis von HCV-RNA. Zielsequenz: 5'UTR HCV/ISEX/0 HCV/ISEX/0 HCV/ISEX/ GeneProof Herpes Simplex Virus (HSV-1/2) PCR Kit Quantitativer Nachweis von HSV-1- und HSV-2-DNA. Zielsequenz: gb (Glycoprotein B) HSV/ISIN/0 HSV/ISIN/0 HSV/ISIN/ HSV/ISEX/0 HSV/ISEX/0 HSV/ISEX/ GeneProof Herpes Simplex Virus 1 (HSV-1) PCR Kit Quantitativer Nachweis von HSV-1-DNA. Zielsequenz: gb (Glycoprotein B) HSV1/ISIN/0 HSV1/ISIN/0 HSV1/ISIN/ HSV1/ISEX/0 HSV1/ISEX/0 HSV1/ISEX/ GeneProof Herpes Simplex Virus 2 (HSV-2) PCR Kit Quantitativer Nachweis von HSV-2-DNA. Zielsequenz: gb (Glycoprotein B) HSV2/ISIN/0 HSV2/ISIN/0 HSV2/ISIN/ HSV2/ISEX/0 HSV2/ISEX/0 HSV2/ISEX/ GeneProof Humanes Immundefizienz-Virus-1 (HIV-1) PCR Kit Quantitativer Nachweis von HIV-1-RNA. Zielsequenz: LTR & GaG-Gen HIV1/ISEX/0 HIV1/ISEX/0 HIV1/ISEX/ GeneProof Varicella Zoster Virus (VZV) PCR Kit Quantitativer Nachweis von VZV-DNA. Zielsequenz: orf62 VZV/ISIN/0 VZV/ISIN/0 VZV/ISIN/ VZV/ISEX/0 VZV/ISEX/0 VZV/ISEX/ GeneProof BK und JC Virus (BKV/JCV) PCR Kit Quantitativer Nachweis von BKV- und JCV-DNA. Zielsequenz: Gen für VP1-VP2 Proteine BKJC/ISIN/0 BKJC/ISIN/0 BKJC/ISIN/ BKJC/ISEX/0 BKJC/ISEX/0 BKJC/ISEX/ GeneProof JC Virus (JCV) PCR Kit Quantitativer Nachweis von JCV-DNA. Zielsequenz: Gen für VP1-VP2 Proteine JCV/ISIN/0 JCV/ISIN/0 JCV/ISIN/ JCV/ISEX/0 JCV/ISEX/0 JCV/ISEX/ HUMANGENETIK Beschreibung Best. GeneProof Factor II Prothrombin PCR Kit Nachweis der Mutation G20210A im Prothrombingen FII/0 FII/ GeneProof Factor V Leiden PCR Kit Nachweis der Mutation G1691A (Leiden Mutation) FV/0 FV/ GeneProof MTHFR A1298C PCR Kit Nachweis der Mutation A1298C der Methylentetrahydrofolat Reduktase M1298/0 M1298/ GeneProof MTHFR C677T PCR Kit Nachweis der Mutation C677T der Methylentetrahydrofolat Reduktase M677/0 M677/ GenProof PAI-1 Genotyping PCR Kit Nachweis der Insertion/Deletion von Guanosin in der Position 675 des PAI-1 Gens PAI/0 PAI/ 53
53 DNA und RNA ISOLIERUNG Nukleinsäureextraktion Beschreibung GeneProof PathogenFree DNA isolation Kit Zur DNA-Isolierung aus Vollblut, Zellkultur, Serum, Plasma und anderen Körperflüssigkeiten IDNA0 IDNA2 2 GeneProof PathogenFree RNA isolation Kit Zur Isolierung von viraler RNA aus biologischen Proben wie Plasma, Serum und Urin, nicht für Vollblut geeignet IRNA0 IRNA2 2 Best. GERÄTE Geräte Beschreibung Unit hybrispot 12 (HS12) Manuelles System zur reversen Dot-Blot-Hybridisierung 1-12 VIT-HS12 1 hybrispot 24 (HS24) Automatisches System zur reversen Dot-Blot-Hybridisierung 1-24 VIT-HS24 1 Ihre Notizen 54
54 Kundenservice Kontakt / Bestellungen medac Gesellschaft für klinische Spezialpräparate mbh Theaterstraße Wedel Tel.: +49 (0) Fax: +49 (0) diagnostika@medac.de Für eine schnellere Abwicklung Ihrer Anfragen und/oder Ihrer Aufträge bitten wir Sie um folgende Angaben: Ÿ Kit-Name Ÿ Katalog-Nummer Ÿ Eventuell Chargen-Nummer Ÿ PCR-file 55
Produktkatalog 2014/2015
 Real-time und Multiplex PCR-Produkte Gerinnung Virologie Bakteriologie Produktkatalog 2014/2015 Informationen aus erster Hand www.medac-diagnostika.de Inhaltsverzeichnis Vorteile der GeneProof PCRs...
Real-time und Multiplex PCR-Produkte Gerinnung Virologie Bakteriologie Produktkatalog 2014/2015 Informationen aus erster Hand www.medac-diagnostika.de Inhaltsverzeichnis Vorteile der GeneProof PCRs...
Neuigkeiten bei CMV / Herpes Panel, Enterovirus 68 Ausbruch in Nordamerika
 Neuigkeiten bei CMV / Herpes Panel, Influenza / respiratorische Viren, sowie Enterovirus 68 Ausbruch in Nordamerika Dr. Johannes Kehle Seminar Molekulare Diagnostik 2014 Hotel Fleming s Wien-Westbahnhof
Neuigkeiten bei CMV / Herpes Panel, Influenza / respiratorische Viren, sowie Enterovirus 68 Ausbruch in Nordamerika Dr. Johannes Kehle Seminar Molekulare Diagnostik 2014 Hotel Fleming s Wien-Westbahnhof
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13168-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 01.09.2017 bis 23.07.2018 Ausstellungsdatum: 01.09.2017 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13168-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 01.09.2017 bis 23.07.2018 Ausstellungsdatum: 01.09.2017 Urkundeninhaber:
Rheinische Friedrich-Wilhelms-Universität Institut für Medizinische Mikrobiologie Immunologie und Parasitologie
 Inhaltsverzeichnis Rheinische Friedrich-Wilhelms-Universität Institut für Medizinische Mikrobiologie Immunologie und Parasitologie Direktor: Prof. Dr. A. HÖRAUF 1 Direkte Erregernachweise 1 1.1 Mikroskopie..............
Inhaltsverzeichnis Rheinische Friedrich-Wilhelms-Universität Institut für Medizinische Mikrobiologie Immunologie und Parasitologie Direktor: Prof. Dr. A. HÖRAUF 1 Direkte Erregernachweise 1 1.1 Mikroskopie..............
Leistungsverzeichnis des Labordiagnostischen Zentrums / Uniklinik Aachen (LDZ)
 Adenovirus Antigen Stuhl FIA 0,5 3-5x wo Adenovirus DNA EDTA, Abstrich Kopien/ml PCR 0,5 2x wo Adenovirus IgA Serum VE ELISA 0,5 2x wo Adenovirus IgG Serum VE ELISA 0,5 2x wo Adenovirus IgM Serum VE ELISA
Adenovirus Antigen Stuhl FIA 0,5 3-5x wo Adenovirus DNA EDTA, Abstrich Kopien/ml PCR 0,5 2x wo Adenovirus IgA Serum VE ELISA 0,5 2x wo Adenovirus IgG Serum VE ELISA 0,5 2x wo Adenovirus IgM Serum VE ELISA
Unsere Testparameter für Ihr PCR-Labor
 Unsere Testparameter für Ihr PCR-Labor Tests für die in-vitro-diagnostik CE-IVD validierte Analyse von der Probenaufarbeitung bis zur Ergebnisausgabe Parameter Testtypus Analysesystem Probenmaterial Testspezifikationen
Unsere Testparameter für Ihr PCR-Labor Tests für die in-vitro-diagnostik CE-IVD validierte Analyse von der Probenaufarbeitung bis zur Ergebnisausgabe Parameter Testtypus Analysesystem Probenmaterial Testspezifikationen
Zentrum für Diagnostik Institut für Med. Mikrobiologie, Virologie und Hygiene
 Zentrum für Diagnostik Institut für Med. Mikrobiologie, Virologie und Hygiene Analyse/ Analyt Methode(n) Material Dauer Hintergrundinformation/ Interpretation Serologie/PCR 16S RNA-Gen (Bakterien) Liquor
Zentrum für Diagnostik Institut für Med. Mikrobiologie, Virologie und Hygiene Analyse/ Analyt Methode(n) Material Dauer Hintergrundinformation/ Interpretation Serologie/PCR 16S RNA-Gen (Bakterien) Liquor
Analyse/ Analyt Methode(n) Material Dauer Hintergrundinformation/ Interpretation Serologie/PCR
 16S RNA Gen (Bakterien) Liquor (1ml), EDTA Blut (5ml), Punktat, Gewebe 18S RNA Gen (Pilze) Liquor (1ml), EDTA Blut (5ml), Punktat, Gewebe Adenoviren AK (IgG, IgM) EIA 5 10 ml Serum (Serummonovette) 1 3d
16S RNA Gen (Bakterien) Liquor (1ml), EDTA Blut (5ml), Punktat, Gewebe 18S RNA Gen (Pilze) Liquor (1ml), EDTA Blut (5ml), Punktat, Gewebe Adenoviren AK (IgG, IgM) EIA 5 10 ml Serum (Serummonovette) 1 3d
Liste der gültigen Prüfverfahren für den akkreditierten Bereich "Abteilung Infektionsdiagnostik", Basel
 Sämtliche n können täglich durchgeführt werden. nliste des EDI) 1 Adenovirus EDTA-Blut, Urin,, Konjuktivalabstrich, Liquor (Kit) PCR Genom qn E 195 2 Adenovirus Ig Serum KBR qn M 28 3 Adeno- und Rotavirus,
Sämtliche n können täglich durchgeführt werden. nliste des EDI) 1 Adenovirus EDTA-Blut, Urin,, Konjuktivalabstrich, Liquor (Kit) PCR Genom qn E 195 2 Adenovirus Ig Serum KBR qn M 28 3 Adeno- und Rotavirus,
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13264-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 18.07.2016 bis 30.11.2019 Ausstellungsdatum: 18.07.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13264-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 18.07.2016 bis 30.11.2019 Ausstellungsdatum: 18.07.2016 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13297-04-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 11.06.2015 bis 24.07.2017 Ausstellungsdatum: 11.06.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13297-04-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 11.06.2015 bis 24.07.2017 Ausstellungsdatum: 11.06.2015 Urkundeninhaber:
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13297-04-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 18.05.2017 bis 29.03.2022 Ausstellungsdatum: 18.05.2017 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13297-04-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 18.05.2017 bis 29.03.2022 Ausstellungsdatum: 18.05.2017 Urkundeninhaber:
Pro Multiplex PCR bei Sepsis
 Pro Multiplex PCR bei Sepsis Klinik für Interdisziplinäre Intensivmedizin und Intermediate Care PD Dr. med. habil. T. Bingold HELIOS Dr. Horst Schmidt Kliniken GmbH Blutkultur, der Goldstandard Prepepsin
Pro Multiplex PCR bei Sepsis Klinik für Interdisziplinäre Intensivmedizin und Intermediate Care PD Dr. med. habil. T. Bingold HELIOS Dr. Horst Schmidt Kliniken GmbH Blutkultur, der Goldstandard Prepepsin
Anlage zur Akkreditierungsurkunde D ML 19288 01 00
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D ML 19288 01 00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 11.12.2014 bis 10.12.2019 Ausstellungsdatum: 11.12.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D ML 19288 01 00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 11.12.2014 bis 10.12.2019 Ausstellungsdatum: 11.12.2014 Urkundeninhaber:
Bericht MQ Mikrobiologie: Molekulare Diagnostik
 Bericht MQ 2017 2 Unser aktuelles Ringversuchsangebot ist optimiert für die Geräte GeneXpert, Alere i, Liat und Biofire. Die Proben können aber auch mit anderen Systemen analysiert werden. B11 Chlamydia
Bericht MQ 2017 2 Unser aktuelles Ringversuchsangebot ist optimiert für die Geräte GeneXpert, Alere i, Liat und Biofire. Die Proben können aber auch mit anderen Systemen analysiert werden. B11 Chlamydia
evademecum Analysenverzeichnis
 evademecum Analysenverzeichnis Analysen, Tarife, Durchführung Erreger: Analyse: AL-Pos.: TP: Durchführung: Kultur allg. für breites en, und/oder 3000.00 74 Virusspektrum Virus-Isolierung mittels Kurzkultur
evademecum Analysenverzeichnis Analysen, Tarife, Durchführung Erreger: Analyse: AL-Pos.: TP: Durchführung: Kultur allg. für breites en, und/oder 3000.00 74 Virusspektrum Virus-Isolierung mittels Kurzkultur
MIKROBIOLOGIE. 1) Strep A und Urine Slide. 2) Gramfärbung 3) Virologie (HCV, HBV, HIV) SPTS 0004
 MIKROBIOLOGIE 1. Strep A und Urine Slide 2. Gramfärbung 3. Virologie (HCV, HBV, HIV) 4. UKNEQAS Microbiology 5. QCMD Programme 1, 2 und 3 werden direkt durch das in Zusammenarbeit mit Experten organisiert.
MIKROBIOLOGIE 1. Strep A und Urine Slide 2. Gramfärbung 3. Virologie (HCV, HBV, HIV) 4. UKNEQAS Microbiology 5. QCMD Programme 1, 2 und 3 werden direkt durch das in Zusammenarbeit mit Experten organisiert.
Tabelle 1: Probenzusammensetzung und erwartetes Ergebnis.
 PD Dr. Udo Reischl PCR-/NAT C. trachomatis & GO (RV 530) April 2011 1115301 / 64 Neisseria meningitidis 1115302 / + 63 Neisseria gonorrhoeae (~ 1x10 4 CFU/mL) 1115303 + / 61 Chlamydia trachomatis (~ 1x10
PD Dr. Udo Reischl PCR-/NAT C. trachomatis & GO (RV 530) April 2011 1115301 / 64 Neisseria meningitidis 1115302 / + 63 Neisseria gonorrhoeae (~ 1x10 4 CFU/mL) 1115303 + / 61 Chlamydia trachomatis (~ 1x10
Anlage zur Akkreditierungsurkunde D-ML-13069-09-00 nach DIN EN ISO 15189:2007
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13069-09-00 nach DIN EN ISO 15189:2007 Gültigkeitsdauer: 03.09.2012 bis 02.09.2017 Urkundeninhaber: Institut für Medizinische
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13069-09-00 nach DIN EN ISO 15189:2007 Gültigkeitsdauer: 03.09.2012 bis 02.09.2017 Urkundeninhaber: Institut für Medizinische
High End Innovation in Molecular Diagnostics
 High End Innovation in Molecular Diagnostics Charakteristika Single und Multiplex real-time Kits Geeignet für viele gängige -Geräte Mit diversen Extraktionsprotokollen kompatibel Interne Extraktionkontrolle
High End Innovation in Molecular Diagnostics Charakteristika Single und Multiplex real-time Kits Geeignet für viele gängige -Geräte Mit diversen Extraktionsprotokollen kompatibel Interne Extraktionkontrolle
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13199-06-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 07.09.2017 bis 06.09.2022 Ausstellungsdatum: 07.09.2017 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13199-06-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 07.09.2017 bis 06.09.2022 Ausstellungsdatum: 07.09.2017 Urkundeninhaber:
Inhalt. Teil I (Heft 35a) V o rw o rt Einleitung... 3
 Inhalt Teil I (Heft 35a) V o rw o rt... 1 1 Einleitung... 3 2 Definition serologischer G rundbegriffe... 6 2.1 Antikörper und Antigene... 6 2.1.1 A ntigene... 7 2.1.2 Antikörper... 8 2.1.3 Verlauf der
Inhalt Teil I (Heft 35a) V o rw o rt... 1 1 Einleitung... 3 2 Definition serologischer G rundbegriffe... 6 2.1 Antikörper und Antigene... 6 2.1.1 A ntigene... 7 2.1.2 Antikörper... 8 2.1.3 Verlauf der
Anlage zur Akkreditierungsurkunde D ML 14095 01 00
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D ML 14095 01 00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 12.06.2015 bis 10.12.2018 Ausstellungsdatum: 12.06.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D ML 14095 01 00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 12.06.2015 bis 10.12.2018 Ausstellungsdatum: 12.06.2015 Urkundeninhaber:
FluoroCycler : Die smarte Offensive. Seminar Molekulare Diagnostik 27. November 2013, Wien, David Hain, Hain Lifescience GmbH, Nehren
 FluoroCycler : Die smarte Offensive Seminar Molekulare Diagnostik 27. November 2013, Wien, David Hain, Hain Lifescience GmbH, Nehren Wer wir sind Hain Lifescience ist ein Unternehmen mit über 25-jähriger
FluoroCycler : Die smarte Offensive Seminar Molekulare Diagnostik 27. November 2013, Wien, David Hain, Hain Lifescience GmbH, Nehren Wer wir sind Hain Lifescience ist ein Unternehmen mit über 25-jähriger
SERION ELISA classic/antigen
 Institut Virion\Serion GmbH Friedrich-Bergius-Ring 19 D-97076 Würzburg, Germany Phone +49 931 3045 0 Fax +49 931 3045 100 E-Mail: order@virion-serion.de Internet: www.virion-serion.de Kundendaten/Client
Institut Virion\Serion GmbH Friedrich-Bergius-Ring 19 D-97076 Würzburg, Germany Phone +49 931 3045 0 Fax +49 931 3045 100 E-Mail: order@virion-serion.de Internet: www.virion-serion.de Kundendaten/Client
Universitätsklinikum Jena Zentrum für Gesundheits- und Sicherheitsmanagement
 (Bakterien, Viren, Pilze, Protozoen u. a) Seite 1 von 6 1. Bakterien Arbeitsstoff Bakterien Bacillus antracis 3 Milzbrand Borrelia burgdorferi 2 Lyme-Borreliose Bordetella pertussis 2 Keuchhusten Brucella
(Bakterien, Viren, Pilze, Protozoen u. a) Seite 1 von 6 1. Bakterien Arbeitsstoff Bakterien Bacillus antracis 3 Milzbrand Borrelia burgdorferi 2 Lyme-Borreliose Bordetella pertussis 2 Keuchhusten Brucella
Anlage zur Akkreditierungsurkunde D-ML-13314-02-00 nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13314-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 21.07.2015 bis 09.12.2017 Ausstellungsdatum: 21.07.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13314-02-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 21.07.2015 bis 09.12.2017 Ausstellungsdatum: 21.07.2015 Urkundeninhaber:
BakNAT1 1/ BakNAT1 2/
 BakNAT1 - Genom Nachweise BakNAT1 1/15 23.03.15 06.05.15 11.05.15 23.05.15 12.05.15 BakNAT1 2/15 24.08.15 28.10.15 02.11.15 14.11.15 03.11.15 Preise je inklusive Probenmaterial und, zzgl. MwSt. Material
BakNAT1 - Genom Nachweise BakNAT1 1/15 23.03.15 06.05.15 11.05.15 23.05.15 12.05.15 BakNAT1 2/15 24.08.15 28.10.15 02.11.15 14.11.15 03.11.15 Preise je inklusive Probenmaterial und, zzgl. MwSt. Material
Product Catalogue PCR Test for Detection of Infectious Diseases
 Product Catalogue 2011-2012 PCR Test for Detection of Infectious Diseases geneon.net A good decision... GeneON GmbH Hubertusstraße 20 D-67065 Ludwigshafen PCR Test for Detection of Infectious Diseases
Product Catalogue 2011-2012 PCR Test for Detection of Infectious Diseases geneon.net A good decision... GeneON GmbH Hubertusstraße 20 D-67065 Ludwigshafen PCR Test for Detection of Infectious Diseases
PRDbak. Bios GmbH Labordiagnostik, München Biosite Fon/Fax /40
 B i o s P r o d u k t l i s t e PRDbak 2 0 1 6 B a k t e r i e n Bios Produktliste 2 0 1 6 B a k t e r i e n Best. Nr. PRDbak Inhaltsverzeichnis Bakterien Antikörper und Antigen Nachweise Parameter/Methode
B i o s P r o d u k t l i s t e PRDbak 2 0 1 6 B a k t e r i e n Bios Produktliste 2 0 1 6 B a k t e r i e n Best. Nr. PRDbak Inhaltsverzeichnis Bakterien Antikörper und Antigen Nachweise Parameter/Methode
medizinisches Laboratorium
 medizinisches Laboratorium Rechtsperson Herrenstraße 12, 4010 Linz Internet www.bhs.at/ried Ident 0298 Standort Institut für klinische Pathologie, Mikrobiologie und molekulare Diagnostik Schlossberg 1,
medizinisches Laboratorium Rechtsperson Herrenstraße 12, 4010 Linz Internet www.bhs.at/ried Ident 0298 Standort Institut für klinische Pathologie, Mikrobiologie und molekulare Diagnostik Schlossberg 1,
gültig ab: Dokumentnummer der Norm bzw. SOP CLSI M100
 Akkreditierungsumfang des medizinischen Laboratoriums (EN ISO 15189:201 1 2 3 4 5 CLSI M100 DIN 58967-30 EUCAST-Clinical Breakpoint Tables Histologie SOP001 Histologie SOP002 2014-01 Clinical Laboratory
Akkreditierungsumfang des medizinischen Laboratoriums (EN ISO 15189:201 1 2 3 4 5 CLSI M100 DIN 58967-30 EUCAST-Clinical Breakpoint Tables Histologie SOP001 Histologie SOP002 2014-01 Clinical Laboratory
QIAsymphony DSP Virus/Pathogen Kit
 QIAsymphony DSP Virus/Pathogen Kit Die QIAsymphony DSP Virus/Pathogen Kits sind nur für den Gebrauch mit dem QIAsymphony SP vorgesehen. Die QIAsymphony DSP Virus/Pathogen Kits enthalten die Reagenzien
QIAsymphony DSP Virus/Pathogen Kit Die QIAsymphony DSP Virus/Pathogen Kits sind nur für den Gebrauch mit dem QIAsymphony SP vorgesehen. Die QIAsymphony DSP Virus/Pathogen Kits enthalten die Reagenzien
MIKROBIOLOGIE. 1) Strep A und Urine Slide. 2) Gramfärbung 3) Virologie (HCV, HBV, HIV) SPTS 0004
 MIKROBIOLOGIE 1. Strep A und Urine Slide ( 1) 2. Gramfärbung ( 1) 3. Virologie (HCV, HBV, HIV) ( 1) 4. UKNEQAS Microbiology ( 2) 5. QCMD ( 4) Programme 1, 2 und 3 werden direkt durch das in Zusammenarbeit
MIKROBIOLOGIE 1. Strep A und Urine Slide ( 1) 2. Gramfärbung ( 1) 3. Virologie (HCV, HBV, HIV) ( 1) 4. UKNEQAS Microbiology ( 2) 5. QCMD ( 4) Programme 1, 2 und 3 werden direkt durch das in Zusammenarbeit
VZV EBV. AdV CMV HHV7 HHV8. BK virus HSV1 HSV2. R-gene Real-Time PCR Kits HHV6
 VIRUSINFEKTIONEN BEI IMMUNSUPPRIMIERTEN PATIENTEN HSV1 EBV CMV HHV7 HHV8 VZV HSV2 HHV6 BK virus AdV R-gene Real-Time PCR Kits Nachweis und quantitative Bestimmung aller relevanten Viren zur Überwachung
VIRUSINFEKTIONEN BEI IMMUNSUPPRIMIERTEN PATIENTEN HSV1 EBV CMV HHV7 HHV8 VZV HSV2 HHV6 BK virus AdV R-gene Real-Time PCR Kits Nachweis und quantitative Bestimmung aller relevanten Viren zur Überwachung
Entwicklung und Validierung von multiplex real-time RT-PCR assays in der Virusdiagnostik
 Entwicklung und Validierung von multiplex real-time RT-PCR assays in der Virusdiagnostik Bernd Hoffmann, Klaus R. Depner, Horst Schirrmeier & Martin Beer Friedrich-Loeffler-Institut Greifswald-Insel Riems
Entwicklung und Validierung von multiplex real-time RT-PCR assays in der Virusdiagnostik Bernd Hoffmann, Klaus R. Depner, Horst Schirrmeier & Martin Beer Friedrich-Loeffler-Institut Greifswald-Insel Riems
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-19082-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 04.06.2014 bis 03.06.2019 Ausstellungsdatum: 04.06.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-19082-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 04.06.2014 bis 03.06.2019 Ausstellungsdatum: 04.06.2014 Urkundeninhaber:
KBR-REAGENZIEN CFT-REAGENTS
 KBR-REAGENZIEN CFT-REAGENTS Institut Virion\Serion GmbH Friedrich-Bergius-Ring 19 D-97076 Würzburg, Germany Phone +49 931 3045 0 Fax +49 931 3045 100 E-Mail: order@virion-serion.de Internet: www.virion-serion.de
KBR-REAGENZIEN CFT-REAGENTS Institut Virion\Serion GmbH Friedrich-Bergius-Ring 19 D-97076 Würzburg, Germany Phone +49 931 3045 0 Fax +49 931 3045 100 E-Mail: order@virion-serion.de Internet: www.virion-serion.de
VIROTYPE PRRSV Gebrauchsinformation
 V1_2012-04-16 VIROTYPE PRRSV Gebrauchsinformation Real-time Multiplex RT-PCR Testkit zum Nachweis von EU-, NA- und HP-PRRS-Viren in vitro-diagnostikum für Schweine Die deutsche Gebrauchsinformation ist
V1_2012-04-16 VIROTYPE PRRSV Gebrauchsinformation Real-time Multiplex RT-PCR Testkit zum Nachweis von EU-, NA- und HP-PRRS-Viren in vitro-diagnostikum für Schweine Die deutsche Gebrauchsinformation ist
Soforttests, Serologie, Immunologische Tests Kapitel 5
 Soforttests, Serologie, Immunologische Tests Kapitel 5 5 Bakteriologie... 2 Virologie... 5 Antigene... 6 Antiseren... 9 Direkte Fluoreszenzantikörpertechnik... 19 Diverse immunologische Tests... 20 Bakteriologie
Soforttests, Serologie, Immunologische Tests Kapitel 5 5 Bakteriologie... 2 Virologie... 5 Antigene... 6 Antiseren... 9 Direkte Fluoreszenzantikörpertechnik... 19 Diverse immunologische Tests... 20 Bakteriologie
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle
 Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: April 2013 (redaktionelle Änderung November 2014) Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: April 2013 (redaktionelle Änderung November 2014) Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich
cobas T HSV 1/2 Test Erweiterung Ihres STI Menüs mit Dual-Target Detektion für zuverlässige Befunde
 cobas T HSV 1/2 Test Erweiterung Ihres STI Menüs mit Dual-Target Detektion für zuverlässige Befunde Zuverlässige HSV 1/2 Ergebnisse, zukunftssicher Herpes simplex Viren zählen zu den am häufigsten sexuell
cobas T HSV 1/2 Test Erweiterung Ihres STI Menüs mit Dual-Target Detektion für zuverlässige Befunde Zuverlässige HSV 1/2 Ergebnisse, zukunftssicher Herpes simplex Viren zählen zu den am häufigsten sexuell
Verzeichnis biologischer Arbeitsstoffe Bakterien (Stand 01/08)
 Bakterien (Stand 01/08) Arbeitsstoff Bakterien Bacillus antracis 3 Milzbrand Borrelia burgdorferi 2 Lyme-Borreliose Bordetella pertussis 2 Keuchhusten Brucella 3 Brucellose Campylobacter jejuni, coli 2
Bakterien (Stand 01/08) Arbeitsstoff Bakterien Bacillus antracis 3 Milzbrand Borrelia burgdorferi 2 Lyme-Borreliose Bordetella pertussis 2 Keuchhusten Brucella 3 Brucellose Campylobacter jejuni, coli 2
58. Jahrestagung der deutschen STD-Gesellschaft
 58. Jahrestagung der deutschen STD-Gesellschaft 17.-19. September 2009 Bochum Neues zur Chlamydien Diagnostik T. Meyer Institut für Medizinische Mikrobiologie, Virologie und Hygiene Universitätsklinikum
58. Jahrestagung der deutschen STD-Gesellschaft 17.-19. September 2009 Bochum Neues zur Chlamydien Diagnostik T. Meyer Institut für Medizinische Mikrobiologie, Virologie und Hygiene Universitätsklinikum
IVD Komplettlösungen für MRSA und TB
 IVD Komplettlösungen für MRSA und TB Seminar Molekulare Diagnostik Wien 26. November 2014 Ulrich Eigner Labor Limbach, Heidelberg Labor Limbach Heidelberg 1979 gegründet g (Dr. Limbach) Gesamtpersonal:
IVD Komplettlösungen für MRSA und TB Seminar Molekulare Diagnostik Wien 26. November 2014 Ulrich Eigner Labor Limbach, Heidelberg Labor Limbach Heidelberg 1979 gegründet g (Dr. Limbach) Gesamtpersonal:
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle
 Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: Mai 2010 Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich an das Gesundheitsamt nicht namentlich an
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: Mai 2010 Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich an das Gesundheitsamt nicht namentlich an
Sensitiver Bakteriennachweis - Neue Sepsisdiagnostik im
 Sensitiver Bakteriennachweis - Neue Sepsisdiagnostik im GenoType-Format Michael Weizenegger Laboratory Limbach, Heidelberg Wien, 28. November 2012 Sepsis HIV/Aids HIV/Aids 1.800.000 Tuberkulose Tuberkulose
Sensitiver Bakteriennachweis - Neue Sepsisdiagnostik im GenoType-Format Michael Weizenegger Laboratory Limbach, Heidelberg Wien, 28. November 2012 Sepsis HIV/Aids HIV/Aids 1.800.000 Tuberkulose Tuberkulose
VOLLAUTOMATISCHES MULTI-PARAMETER SYSTEM ZUR EINZELTEST-ANALYSE
 INNOVATIVES IMMUNOASSAY SYSTEM VOLLAUTOMATISCHES MULTI-PARAMETER SYSTEM ZUR EINZELTEST-ANALYSE Analyse von Infektions- und Autoimmunkrankheiten in einem System Vielseitig 1-30 Testeinheiten pro Lauf Bis
INNOVATIVES IMMUNOASSAY SYSTEM VOLLAUTOMATISCHES MULTI-PARAMETER SYSTEM ZUR EINZELTEST-ANALYSE Analyse von Infektions- und Autoimmunkrankheiten in einem System Vielseitig 1-30 Testeinheiten pro Lauf Bis
Juni Ringversuche geschlossen. Information zu Probeneigenschaften. Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel
 Juni 2017 e geschlossen Information zu Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel Herausgegeben von: INSTAND Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Düsseldorf/Berlin,
Juni 2017 e geschlossen Information zu Prof. Dr. Heinz Zeichhardt Dr. Martin Kammel Herausgegeben von: INSTAND Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e.v. Düsseldorf/Berlin,
Amplifikation von EGFR beim Lungen- (Adenokarzinom) oder Magenkarzinom
 Leistungsspektrum Alle Untersuchungen können grundsätzlich an formalinfixierten paraffineingebetteten Gewebeproben, Schnittpräparaten oder EDTA-Blut durchgeführt werden. Auflistung nach Untersuchungen
Leistungsspektrum Alle Untersuchungen können grundsätzlich an formalinfixierten paraffineingebetteten Gewebeproben, Schnittpräparaten oder EDTA-Blut durchgeführt werden. Auflistung nach Untersuchungen
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle
 Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: September 2017 Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich an das Gesundheitsamt nicht namentlich
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: September 2017 Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich an das Gesundheitsamt nicht namentlich
Diagnostik-Info Meldepflicht nach dem Infektionsschutzgesetzt (IfSG)
 Diagnostik-Info Meldepflicht nach dem Infektionsschutzgesetzt (IfSG) Allgemeines: Die Meldepflicht ist ein Instrument zur Überwachung (Surveillance) von Infektionskrankheiten. Allgemeiner Zweck des Gesetzes
Diagnostik-Info Meldepflicht nach dem Infektionsschutzgesetzt (IfSG) Allgemeines: Die Meldepflicht ist ein Instrument zur Überwachung (Surveillance) von Infektionskrankheiten. Allgemeiner Zweck des Gesetzes
artus HCV QS-RGQ Kit Leistungsmerkmale Januar 2014 Sample & Assay Technologies Nachweisgrenze (LOD) Angaben zur Version
 artus HCV QS-RGQ Kit Leistungsmerkmale artus HCV QS-RGQ Kit, Version 1, 4518363, 4518366 Angaben zur Version Dieses Dokument sind die artus HCV QS-RGQ Kit Leistungsmerkmale, Version 1, R3. Prüfen Sie vor
artus HCV QS-RGQ Kit Leistungsmerkmale artus HCV QS-RGQ Kit, Version 1, 4518363, 4518366 Angaben zur Version Dieses Dokument sind die artus HCV QS-RGQ Kit Leistungsmerkmale, Version 1, R3. Prüfen Sie vor
MPP Multiplex 2x PCR-Mastermix
 Datenblatt Artikel-Nr. BS91.522.0250 250 Reaktionen in 20µl Artikel-Nr. BS91.522.1250 1250 Reaktionen a 20µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Datenblatt Artikel-Nr. BS91.522.0250 250 Reaktionen in 20µl Artikel-Nr. BS91.522.1250 1250 Reaktionen a 20µl (Nur für Forschung und in vitro-anwendungen) Chargen-Nr.: Mindestens haltbar bis: Aussehen:
Analysenangebot. IMS-ID:2503 Version 5 1 / 15
 Hornhautabradat, Hornhautbiopsie, Kontaktlinse, Kontaktlinsen- Bei Bedarf, jedoch mindestens 1 mal pro Acanthamoeba spp. Nukleinsäureamplifikation PCR Aufbewahrungslösung Externe Analyse Woche Nein U6
Hornhautabradat, Hornhautbiopsie, Kontaktlinse, Kontaktlinsen- Bei Bedarf, jedoch mindestens 1 mal pro Acanthamoeba spp. Nukleinsäureamplifikation PCR Aufbewahrungslösung Externe Analyse Woche Nein U6
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13102-03-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 09.12.2013 bis 08.12.2018 Ausstellungsdatum: 09.12.2013 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13102-03-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 09.12.2013 bis 08.12.2018 Ausstellungsdatum: 09.12.2013 Urkundeninhaber:
Erregerhäufigkeit bei akuter bakterieller Meningitis
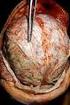 Erregerhäufigkeit bei akuter bakterieller Meningitis 70 60 % 50 40 30 20 10 Listeria B-Streptok. N. meningitidis S. pneumoniae H. influenzae 0 60 J. Schuchat et al
Erregerhäufigkeit bei akuter bakterieller Meningitis 70 60 % 50 40 30 20 10 Listeria B-Streptok. N. meningitidis S. pneumoniae H. influenzae 0 60 J. Schuchat et al
Infektionen des Zentralnervensystems: Klinik
 : Klinik Leitsymptome Meningitis Enzephalitis Abszess Meningismus Kopfschmerzen Fieber Veränderungen der Bewusstseinslage Reizsymptome (Epilepsie) Fokus, periphere neurologische Defizite Hirnlokales Psychosyndrom
: Klinik Leitsymptome Meningitis Enzephalitis Abszess Meningismus Kopfschmerzen Fieber Veränderungen der Bewusstseinslage Reizsymptome (Epilepsie) Fokus, periphere neurologische Defizite Hirnlokales Psychosyndrom
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13294-07-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 25.07.2014 bis 27.02.2018 Ausstellungsdatum: 25.07.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13294-07-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 25.07.2014 bis 27.02.2018 Ausstellungsdatum: 25.07.2014 Urkundeninhaber:
Etablierung, Validierung und praktische Anwendung einer multiplex real-time RT-PCR zum Nachweis des Rabbit Haemorrhagic Disease Virus
 Aus dem Institut für Virologie der Tierärztlichen Hochschule Hannover und dem Institut für Virusdiagnostik des Friedrich-Loeffler-Instituts, Insel Riems Etablierung, Validierung und praktische Anwendung
Aus dem Institut für Virologie der Tierärztlichen Hochschule Hannover und dem Institut für Virusdiagnostik des Friedrich-Loeffler-Instituts, Insel Riems Etablierung, Validierung und praktische Anwendung
STS-Verzeichnis Akkreditierungsnummer: STS 0266
 Internationale Norm: ISO/IEC 17025:2005 Schweizer Norm: SN EN ISO/IEC 17025:2005 Institut für Medizinische Mikrobiologie der Universität Zürich Gloriastr. 30/32 8006 Zürich Leiter: Prof. Dr. Erik C. Böttger
Internationale Norm: ISO/IEC 17025:2005 Schweizer Norm: SN EN ISO/IEC 17025:2005 Institut für Medizinische Mikrobiologie der Universität Zürich Gloriastr. 30/32 8006 Zürich Leiter: Prof. Dr. Erik C. Böttger
IMMUVIEW URIN-ANTIGEN-TEST ZUM NACHWEIS VON S. PNEUMONIAE UND L. PNEUMOPHILA
 IMMUVIEW URIN-ANTIGEN-TEST ZUM NACHWEIS VON S. PNEUMONIAE UND L. PNEUMOPHILA DEutsch Para otras lenguas Para outros lenguas Für andere Sprachen Pour d autres langues Per le altre lingue For andre språk
IMMUVIEW URIN-ANTIGEN-TEST ZUM NACHWEIS VON S. PNEUMONIAE UND L. PNEUMOPHILA DEutsch Para otras lenguas Para outros lenguas Für andere Sprachen Pour d autres langues Per le altre lingue For andre språk
Bessere Diagnostik von Lungeninfekten durch Multiplex-PCR?
 Bessere Diagnostik von Lungeninfekten durch Multiplex-PCR? Dr. med. Reno Frei Klinische Mikrobiologie Universitätsspital Basel CH-4031 Basel reno.frei@usb.ch Pneumonie Ambulant erworbene P. (CAP): 3-8/1000
Bessere Diagnostik von Lungeninfekten durch Multiplex-PCR? Dr. med. Reno Frei Klinische Mikrobiologie Universitätsspital Basel CH-4031 Basel reno.frei@usb.ch Pneumonie Ambulant erworbene P. (CAP): 3-8/1000
Auswertung PCR. Übersicht Nachweise mittels PCR. 1. Beta-Globin
 Übersicht Nachweise mittels PCR Lfd.-Nr. Nachweis von: Elektrophorese/Photometrie/ Luminometrie/ Fragmentanalyse/Sequenzierung/ Restriktionsanalyse 1. Beta-Globin 267 bp (zum Nachweis der DNA- Qualität)
Übersicht Nachweise mittels PCR Lfd.-Nr. Nachweis von: Elektrophorese/Photometrie/ Luminometrie/ Fragmentanalyse/Sequenzierung/ Restriktionsanalyse 1. Beta-Globin 267 bp (zum Nachweis der DNA- Qualität)
Analysenübersicht. Analysen, Tarife, Durchführung. 1. Routineuntersuchungen 1.1 Viren
 Analysenübersicht Analysen, Tarife, Durchführung 1. Routineuntersuchungen 1.1 Viren 1.2 Toxoplasma gondii 2. Spitalhygienische Untersuchungen Noroviren 3. Notfalluntersuchungen für das USZ Durchgeführt
Analysenübersicht Analysen, Tarife, Durchführung 1. Routineuntersuchungen 1.1 Viren 1.2 Toxoplasma gondii 2. Spitalhygienische Untersuchungen Noroviren 3. Notfalluntersuchungen für das USZ Durchgeführt
Während der Synthese synthetisiert die Polymerase den neuen Strang in 5 3 Richtung und bewegt sich in 3 5 -Richtung am Matrizenstrang entlang:
 4.4 Replikation und PCR Ablauf der Replikation in vivo: Die Replikation wird von einer DNA-abhängigen DNA- Polymerase katalysiert. Jede DNA-Polymerase synthetisiert den neuen Strang in 5 3 Richtung, hierzu
4.4 Replikation und PCR Ablauf der Replikation in vivo: Die Replikation wird von einer DNA-abhängigen DNA- Polymerase katalysiert. Jede DNA-Polymerase synthetisiert den neuen Strang in 5 3 Richtung, hierzu
Aktuelle Änderungen im Infektionsschutzgesetz 11. NRW-Dialog Infektionsschutz, in Dortmund
 Aktuelle Änderungen im Infektionsschutzgesetz 11. NRW-Dialog Infektionsschutz, 10.04.2013 in Dortmund Landeszentrum Gesundheit Nordrhein-Westfalen Fachgruppe Infektiologie und Hygiene Gesetz zur Durchführung
Aktuelle Änderungen im Infektionsschutzgesetz 11. NRW-Dialog Infektionsschutz, 10.04.2013 in Dortmund Landeszentrum Gesundheit Nordrhein-Westfalen Fachgruppe Infektiologie und Hygiene Gesetz zur Durchführung
Stand: 20.05.2015. Leistungsverzeichnis Infektions-Serologie
 Stand: 20.05.2015 Leistungsverzeichnis Infektions-Serologie Allgemeine Hinweise Dieses Leistungsverzeichnis enthält alle vom Klinisch-immunologischen Labor angebotenen Untersuchungen mit Angaben über die
Stand: 20.05.2015 Leistungsverzeichnis Infektions-Serologie Allgemeine Hinweise Dieses Leistungsverzeichnis enthält alle vom Klinisch-immunologischen Labor angebotenen Untersuchungen mit Angaben über die
INSTAND e.v. in Zusammenarbeit mit:
 Vorauswertung zu den virologischen en Juni 2015 Korrigierte Version: 10. August 2015 (Siehe Tabelle 3; Programm 346) INSTAND e.v. in Zusammenarbeit mit: Deutsche Vereinigung zur Bekämpfung der krankheiten
Vorauswertung zu den virologischen en Juni 2015 Korrigierte Version: 10. August 2015 (Siehe Tabelle 3; Programm 346) INSTAND e.v. in Zusammenarbeit mit: Deutsche Vereinigung zur Bekämpfung der krankheiten
Meldepflichtige Krankheiten und Krankheitserreger
 Meldepflichtige Krankheiten und Krankheitserreger namentlich an das Gesundheitsamt nicht namentlich an das Gesundheitsamt namentlich an das Gesundheitsamt nicht namentlich an das Gesundheitsamt nicht namentlich
Meldepflichtige Krankheiten und Krankheitserreger namentlich an das Gesundheitsamt nicht namentlich an das Gesundheitsamt namentlich an das Gesundheitsamt nicht namentlich an das Gesundheitsamt nicht namentlich
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle
 Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: April 2013 Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich an das Gesundheitsamt nicht namentlich
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: April 2013 Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich an das Gesundheitsamt nicht namentlich
artus HI Virus-1 QS-RGQ Kit
 artus HI Virus-1 QS-RGQ Kit Leistungsmerkmale artus HI Virus-1 QS-RGQ Kit, Version 1, 4513363, 4513366 Prüfen Sie vor einer Testausführung die Verfügbarkeit neuer elektronischer Etikettierungsrevisionen
artus HI Virus-1 QS-RGQ Kit Leistungsmerkmale artus HI Virus-1 QS-RGQ Kit, Version 1, 4513363, 4513366 Prüfen Sie vor einer Testausführung die Verfügbarkeit neuer elektronischer Etikettierungsrevisionen
Anlage zur Akkreditierungsurkunde D-ML-13238-01-00 nach DIN EN ISO 15189:2007
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13238-01-00 nach DIN EN ISO 15189:2007 Gültigkeitsdauer: 24.03.2014 bis 03.03.2016 Ausstellungsdatum: 24.03.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13238-01-00 nach DIN EN ISO 15189:2007 Gültigkeitsdauer: 24.03.2014 bis 03.03.2016 Ausstellungsdatum: 24.03.2014 Urkundeninhaber:
Leiter: MS-Verantwortlicher: Telefon: Telefax: Internet: Erstakkreditierung: Letzte Akkreditierung: Aktuellste Version:
 Seite 1 von 5 Prüfstelle für molekularbiologische und mikrobiologische Prüfverfahren im Lebensmittel-, Genussmittel-, Futtermittel-, Kosmetik-, Umwelt-, Pharma-, Humandiagnostik- und Veterinärdiagnostikbereich
Seite 1 von 5 Prüfstelle für molekularbiologische und mikrobiologische Prüfverfahren im Lebensmittel-, Genussmittel-, Futtermittel-, Kosmetik-, Umwelt-, Pharma-, Humandiagnostik- und Veterinärdiagnostikbereich
Vermehrung oder Eliminierung antibiotikaresistenter Bakterien in Biogasanlagen?
 Vermehrung oder Eliminierung antibiotikaresistenter Bakterien in Biogasanlagen? Prof. Dr. Dr.-Ing. Peter Kämpfer Dr. rer. nat. Stefanie P. Glaeser Msc. Thorsten Schauss Institut für Angewandte Mikrobiologie
Vermehrung oder Eliminierung antibiotikaresistenter Bakterien in Biogasanlagen? Prof. Dr. Dr.-Ing. Peter Kämpfer Dr. rer. nat. Stefanie P. Glaeser Msc. Thorsten Schauss Institut für Angewandte Mikrobiologie
Real-time PCR Tests zum Nachweis von Pilzinfektionen
 Real-time PCR Tests zum Nachweis von Pilzinfektionen Claudia Schabereiter-Gurtner Ingenetix real-time PCR Tests für Viren Ingenetix real-time PCR Tests für Bakterien und Pilze Pilzinfektionen (Mykosen)
Real-time PCR Tests zum Nachweis von Pilzinfektionen Claudia Schabereiter-Gurtner Ingenetix real-time PCR Tests für Viren Ingenetix real-time PCR Tests für Bakterien und Pilze Pilzinfektionen (Mykosen)
Klassifizierung multiresistenter Keime. Dr. Ingrid Heller Sektion für Hygiene und Medizinische Mikrobiologie Hygieneteam LKI
 Klassifizierung multiresistenter Keime Dr. Ingrid Heller Sektion für Hygiene und Medizinische Mikrobiologie Hygieneteam LKI Definition Multiresistenz Mycobacteriumtuberculosis: MDR: Resistenz gegen INH
Klassifizierung multiresistenter Keime Dr. Ingrid Heller Sektion für Hygiene und Medizinische Mikrobiologie Hygieneteam LKI Definition Multiresistenz Mycobacteriumtuberculosis: MDR: Resistenz gegen INH
Anlage zur Akkreditierungsurkunde D-ML nach DIN EN ISO 15189:2014
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13374-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 16.11.2015 bis 15.11.2020 Ausstellungsdatum: 16.11.2015 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13374-01-00 nach DIN EN ISO 15189:2014 Gültigkeitsdauer: 16.11.2015 bis 15.11.2020 Ausstellungsdatum: 16.11.2015 Urkundeninhaber:
Leistungsspektrum. Auflistung nach Untersuchungen. Pathologie
 Pathologie Leistungsspektrum Alle Untersuchungen können grundsätzlich an formalinfixierten paraffineingebetteten Gewebeproben, Schnittpräparaten oder EDTA-Blut durchgeführt werden. Auflistung nach Untersuchungen
Pathologie Leistungsspektrum Alle Untersuchungen können grundsätzlich an formalinfixierten paraffineingebetteten Gewebeproben, Schnittpräparaten oder EDTA-Blut durchgeführt werden. Auflistung nach Untersuchungen
Labor:Medizin Krefeld MVZ GmbH Lutherplatz 40 D Krefeld
 Abstrich E-Swab TM 480CE Rosa Deckel Direktnachweis von Bakterien, Pilze und Viren Standard Abstrichtupfer z.b. für Wunde, Haut, Screening SAP: 30078256; Art.: 80490CEA (Copan) Abstrich E-Swab TM 481CE
Abstrich E-Swab TM 480CE Rosa Deckel Direktnachweis von Bakterien, Pilze und Viren Standard Abstrichtupfer z.b. für Wunde, Haut, Screening SAP: 30078256; Art.: 80490CEA (Copan) Abstrich E-Swab TM 481CE
Klausur Mikrobiologie, Hygiene und Virologie SS (Humanmedizin, Universität zu Köln) Gedächtnisprotokoll Revision: v1.0 /
 Klausur Mikrobiologie, Hygiene und Virologie SS 2007 (Humanmedizin, Universität zu Köln) Gedächtnisprotokoll Revision: v1.0 / 13.07.2007 IK Studiengang: Anzahl: Format: Zeit: RSG und MSG 54 short-answer-
Klausur Mikrobiologie, Hygiene und Virologie SS 2007 (Humanmedizin, Universität zu Köln) Gedächtnisprotokoll Revision: v1.0 / 13.07.2007 IK Studiengang: Anzahl: Format: Zeit: RSG und MSG 54 short-answer-
Ringversuche geschlossen. Information zu Probeneigenschaften. INSTAND e.v. in Zusammenarbeit mit:
 Virologische e November/Dezember 2015 e geschlossen Information zu INSTAND e.v. in Zusammenarbeit mit: Deutsche Vereinigung zur Bekämpfung der krankheiten (DVV) Gesellschaft für Virologie (GfV) Deutsche
Virologische e November/Dezember 2015 e geschlossen Information zu INSTAND e.v. in Zusammenarbeit mit: Deutsche Vereinigung zur Bekämpfung der krankheiten (DVV) Gesellschaft für Virologie (GfV) Deutsche
Anlage zur Akkreditierungsurkunde D-EP für die relevanten Abschnitte der DIN EN ISO/IEC 17043:2010
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-EP-15027-02-00 für die relevanten Abschnitte der DIN EN ISO/IEC 17043:2010 Gültigkeitsdauer: 30.11.2015 bis 07.04.2019 Ausstellungsdatum:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-EP-15027-02-00 für die relevanten Abschnitte der DIN EN ISO/IEC 17043:2010 Gültigkeitsdauer: 30.11.2015 bis 07.04.2019 Ausstellungsdatum:
Stand der molekularen Resistenzbestimmung - sind die Methoden schon routinetauglich?
 Stand der molekularen Resistenzbestimmung - sind die Methoden schon routinetauglich? Peter Heisig Pharmazeutische Biologie und Mikrobiologie Universität Hamburg PH2008, UniHH 1 Vor- und Nachteile genetischer
Stand der molekularen Resistenzbestimmung - sind die Methoden schon routinetauglich? Peter Heisig Pharmazeutische Biologie und Mikrobiologie Universität Hamburg PH2008, UniHH 1 Vor- und Nachteile genetischer
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle
 Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: März 2013 Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich an das Gesundheitsamt nicht namentlich an
Meldepflichtige Krankheiten und Krankheitserreger Übersichtstabelle Stand: März 2013 Krankheit; Krankheitserreger: Arztmeldepflicht Labormeldepflicht namentlich an das Gesundheitsamt nicht namentlich an
Bei dem vorliegenden Dokument handelt es sich um die Leistungsmerkmale des QIAamp DSP DNA FFPE Tissue Kits, Version 1, R3.
 Leistungsmerkmale QIAamp DSP DNA FFPE Tissue Kit, Version 1 60404 Versionsmanagement Bei dem vorliegenden Dokument handelt es sich um die Leistungsmerkmale des QIAamp DSP DNA FFPE Tissue Kits, Version
Leistungsmerkmale QIAamp DSP DNA FFPE Tissue Kit, Version 1 60404 Versionsmanagement Bei dem vorliegenden Dokument handelt es sich um die Leistungsmerkmale des QIAamp DSP DNA FFPE Tissue Kits, Version
NEWSLETTER. Inhalt. Multiresistente Erreger und deren Nachweis 10/2010
 NEWSLETTER 10/2010 Inhalt CHROMagar TM MRSA CHROMagar TM ESBL CHROMagar TM CTX-M CHROMagar TM KPC CHROMagar TM VRE CHROMagar TM Acinetobacter Multiresistente Erreger und deren Nachweis Vor wenigen Tagen
NEWSLETTER 10/2010 Inhalt CHROMagar TM MRSA CHROMagar TM ESBL CHROMagar TM CTX-M CHROMagar TM KPC CHROMagar TM VRE CHROMagar TM Acinetobacter Multiresistente Erreger und deren Nachweis Vor wenigen Tagen
Molekularbiologische Laboruntersuchungen. Labormedizinvorlesung Krisztina Káldi
 Molekularbiologische Laboruntersuchungen Labormedizinvorlesung 03.04.2017 Krisztina Káldi Ziel der molekularbiologischen Laboruntersuchungen Untersuchungen der DNA-Struktur und der Expression von RNA 3,2
Molekularbiologische Laboruntersuchungen Labormedizinvorlesung 03.04.2017 Krisztina Káldi Ziel der molekularbiologischen Laboruntersuchungen Untersuchungen der DNA-Struktur und der Expression von RNA 3,2
Aseptische Meningitis. Eosinophile Meningitis/ Meningoenzephalitis
 Viren / Adenovirus 2, 3 NI a, 4 ; ST, TH: V, E, T d Enteroviren (z. B. Coxsackie-Viren, ECHO-Viren) Stuhl, Virusisolierung Stuhl (> 0 %) 5 (< 0 %) (< 0 %) SN: NI d SN,ST,TH: ET d Epstein-Barr-Virus 6 3
Viren / Adenovirus 2, 3 NI a, 4 ; ST, TH: V, E, T d Enteroviren (z. B. Coxsackie-Viren, ECHO-Viren) Stuhl, Virusisolierung Stuhl (> 0 %) 5 (< 0 %) (< 0 %) SN: NI d SN,ST,TH: ET d Epstein-Barr-Virus 6 3
Entwicklung und Validierung der VIROTYPE BVDV real-time RT-PCR
 Entwicklung und Validierung der real-time RT-PCR Gaunitz C, Engemann C, Labitzke M, Schroeder C, Kühn TE, Gabert, J Labor Diagnostik GmbH Leipzig Gliederung Testprinzip Testprotokoll Testcharakteristik
Entwicklung und Validierung der real-time RT-PCR Gaunitz C, Engemann C, Labitzke M, Schroeder C, Kühn TE, Gabert, J Labor Diagnostik GmbH Leipzig Gliederung Testprinzip Testprotokoll Testcharakteristik
Surveillance, Ausbruchsanalyse und Prävention von Infektionen mit Antibiotika-resistenten Bakterien. Osamah Hamouda Abteilung Infektionsepidemiologie
 Surveillance, Ausbruchsanalyse und Prävention von Infektionen mit Antibiotika-resistenten Bakterien Osamah Hamouda Abteilung Infektionsepidemiologie 16. September 2015 Inhalt Einleitung Surveillance Ausbruchsuntersuchungen
Surveillance, Ausbruchsanalyse und Prävention von Infektionen mit Antibiotika-resistenten Bakterien Osamah Hamouda Abteilung Infektionsepidemiologie 16. September 2015 Inhalt Einleitung Surveillance Ausbruchsuntersuchungen
Multiplex-Teste in der Virologie neue Antworten, aber auch neue Fragen
 18.08.2011 Multiplex-Teste in der Virologie neue Antworten, aber auch neue Fragen Jürgen Rissland Institut für Virologie/Staatliche Medizinaluntersuchungsstelle Struktur Multiplex-Verfahren: Technik und
18.08.2011 Multiplex-Teste in der Virologie neue Antworten, aber auch neue Fragen Jürgen Rissland Institut für Virologie/Staatliche Medizinaluntersuchungsstelle Struktur Multiplex-Verfahren: Technik und
Anlage zur Akkreditierungsurkunde D-ML-13193-01-00 nach DIN EN ISO 15189:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13193-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 20.08.2014 bis 04.03.2017 Ausstellungsdatum: 20.08.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ML-13193-01-00 nach DIN EN ISO 15189:2013 Gültigkeitsdauer: 20.08.2014 bis 04.03.2017 Ausstellungsdatum: 20.08.2014 Urkundeninhaber:
Resistenzen bei gram-positiven Bakterien gegen Linezolid, Tigecyclin und Daptomycin
 Resistenzen bei gram-positiven Bakterien gegen Linezolid, Tigecyclin und Daptomycin G. Werner, F. Layer, B. Strommenger, C. Cuny, S. Fiedler, J. Bender, I. Klare Nationales Referenzzentrum für Staphylokokken
Resistenzen bei gram-positiven Bakterien gegen Linezolid, Tigecyclin und Daptomycin G. Werner, F. Layer, B. Strommenger, C. Cuny, S. Fiedler, J. Bender, I. Klare Nationales Referenzzentrum für Staphylokokken
IfSGMeldeVO. Verordnung
 Verordnung des Sächsischen Staatsministeriums für Soziales und Verbraucherschutz über die Erweiterung der Meldepflicht für übertragbare Krankheiten und Krankheitserreger nach dem Infektionsschutzgesetz
Verordnung des Sächsischen Staatsministeriums für Soziales und Verbraucherschutz über die Erweiterung der Meldepflicht für übertragbare Krankheiten und Krankheitserreger nach dem Infektionsschutzgesetz
Epidemiologische Information für den Monat Juni 2015
 Landesuntersuchungsanstalt für das Gesundheits- und Veterinärwesen (LUA) Sachsen 01099 Dresden, Jägerstraße 8/10 - Tel. (0351) 8144-0 - Fax (0351) 8144-1020 - Web: www.lua.sachsen.de Epidemiologische Information
Landesuntersuchungsanstalt für das Gesundheits- und Veterinärwesen (LUA) Sachsen 01099 Dresden, Jägerstraße 8/10 - Tel. (0351) 8144-0 - Fax (0351) 8144-1020 - Web: www.lua.sachsen.de Epidemiologische Information
Ergebnisse der 4 MRGN-PCR
 Ergebnisse der 4 MRGN-PCR CarbaR PCR und kulturelles MRGN Screening am Klinikum Darmstadt (2015 / 2016) MRE-Netzwerk Südhessen 12. Dezember 2016 Dr. J. LUGAUER Zentrum für Labormedizin Klinikum Darmstadt
Ergebnisse der 4 MRGN-PCR CarbaR PCR und kulturelles MRGN Screening am Klinikum Darmstadt (2015 / 2016) MRE-Netzwerk Südhessen 12. Dezember 2016 Dr. J. LUGAUER Zentrum für Labormedizin Klinikum Darmstadt
Enterovirus/Parechovirus Infektionen. Daniela Huzly Institut für Virologie Freiburg
 Enterovirus/Parechovirus Infektionen Daniela Huzly Institut für Virologie Freiburg Virologie Beide gehören zur Familie der PICORNAVIRIDAE Enteroviren werden traditionell unterteilt in: Poliovirus 1 3 Echoviren
Enterovirus/Parechovirus Infektionen Daniela Huzly Institut für Virologie Freiburg Virologie Beide gehören zur Familie der PICORNAVIRIDAE Enteroviren werden traditionell unterteilt in: Poliovirus 1 3 Echoviren
LANDESUNTERSUCHUNGS- ANSTALT FÜR DAS GESUNDHEITS- UND VETERINÄRWESEN
 LANDESUNTERSUCHUNGS- ANSTALT FÜR DAS GESUNDHEITS- UND VETERINÄRWESEN Handbuch für die Probenahme von humanmedizinischen mikrobiologischen Untersuchungsmaterialien Abteilung Medizinische Mikrobiologie und
LANDESUNTERSUCHUNGS- ANSTALT FÜR DAS GESUNDHEITS- UND VETERINÄRWESEN Handbuch für die Probenahme von humanmedizinischen mikrobiologischen Untersuchungsmaterialien Abteilung Medizinische Mikrobiologie und
