Einfluss der Implantatanzahl im zahnlosen Unterkiefer auf die Kaueffektivität eine klinische intra-individuelle Studie
|
|
|
- Karoline Fürst
- vor 6 Jahren
- Abrufe
Transkript
1 zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Studienteilnehmern 1 Prüfstelle: Klinik für Zahnärztliche Prothetik, Propädeutik und Werkstoffkunde Universitätsklinikum Kiel, Arnold-Heller-Str.16, Kiel, Tel: / 402 Prüfarzt: Dr. Sad Chaar, Arnold-Heller-Str.16, Kiel, Tel: Studientitel: Einfluss der Implantatanzahl im zahnlosen Unterkiefer auf die Kaueffektivität eine klinische intra-individuelle Studie Sehr geehrte Dame, sehr geehrter Herr, wir möchten Sie fragen, ob Sie bereit sind, an der von uns vorgesehenen klinischen Studie teilzunehmen. Klinische Studien sind notwendig, um Erkenntnisse über die Sicherheit, Eignung und Leistungsfähigkeit von neuen Verfahren zu gewinnen oder zu erweitern. Die klinische Studie, die wir Ihnen hier vorstellen, wurde wie es die Berufsordnung verlangt von der zuständigen Ethikkommission zustimmend bewertet. Ihre Teilnahme an dieser klinischen Studie ist freiwillig. Sie werden in diese Studie also nur dann einbezogen, wenn Sie dazu schriftlich Ihre Einwilligung erklären. Sofern Sie nicht an der klinischen Studie teilnehmen oder später aus ihr ausscheiden möchten, entstehen Ihnen daraus keine Nachteile. Der Prüfarzt/ die Prüfärztin hat Ihnen bereits einige Informationen zu der geplanten Studie gegeben. Der nachfolgende Text soll Ihnen die Ziele und den Ablauf der Studie erläutern. Anschließend wird der Prüfarzt/ die Prüfärztin das Aufklärungsgespräch mit Ihnen führen. Bitte zögern Sie nicht, alle Punkte anzusprechen, die Ihnen unklar sind. Sie werden danach ausreichend Bedenkzeit erhalten, um über Ihre Teilnahme zu entscheiden. 1 Im Rahmen dieses Textes schließt die männliche Bezeichnung stets die weibliche Bezeichnung mit ein. Seite 1 von 13
2 1. Warum wird diese Studie durchgeführt? Die Verankerung unterer Totalprothesen über Implantate ist ein etabliertes Verfahren, wenn zahnlose Patienten mit ihren unteren Totalprothesen nicht zurechtkommen. Die verwendeten Implantate besitzen für die Behandlung ein gültiges CE-Kennzeichen. In der geplanten klinischen Studie soll der Einfluss einer unterschiedlichen Anzahl an Implantaten im Unterkiefer auf die Kaueffektivität untersucht werden. Die Studie wird folgendermaßen durchgeführt: Zahnlose Patienten, die mit ihrer oberen Totalprothese gut, aber mit ihrer unteren Totalprothese schlecht zurecht kommen, und in die Studie aufgenommen werden wollen, um dort drei Implantate im Unterkiefer zur Verankerung ihrer unteren Prothese zu erhalten, werden klinisch untersucht und gebeten zwei Fragebögen auszufüllen. Ein Fragebogen dient dazu, die Zufriedenheit/Unzufriedenheit mit beiden Prothesen näher zu erfassen, und ein zweiter Fragebogen dient dazu die aktuelle mundgesundheitsbezogene Lebensqualität zu ermitteln. Im Anschluss wird dann eine Röntgenaufnahme der Kiefer mit Messkugeln angefertigt um das Knochenangebot im Unterkiefer bestimmen zu können. Sollte ein Knochenaufbau im Unterkiefer erforderlich sein ist eine Teilnahme an der Studie leider nicht möglich. Eine Versorgung mit Implantaten kann dann außerhalb der Studie erfolgen. Ist eine Implantation innerhalb der Studie ohne aufbauende Verfahren möglich, wird eine Untersuchung zur Kaufähigkeit durch Kauen von Testnahrung durchgeführt. Danach erfolgt das Einsetzen dreier Implantate im Unterkiefer in einer Operation welche unter der Schleimhaut einheilen. Die vorhandene Unterkieferprothese wird mit einem Metallgerüst verstärkt. 2 Monate später wird in einem zweiten Eingriff das mittlere Implantat freigelegt und über einen Druckknopf mit der Prothese verbunden. Drei Monate später erfolgt eine Nachuntersuchung mit einem Kautest und der Wiederholung der Befragungen. In dieser Sitzung erfolgt die Freilegung der anderen zwei Implantate, die ebenfalls über einen Druckknopf mit der Prothese verbunden werden. Das mittlere Implantat wird für die nächsten drei Monate mit einer Kappe versorgt, so dass das Implantat nicht unmittelbar mit der Prothese verbunden ist. Weitere drei Monate später erfolgt eine Nachuntersuchung mit einem Kautest und der Wiederholung der Befragungen in dieser Sitzung wird ein Röntgenbild zur Kontrolle angefertigt. Dieses Röntgenintervall entspricht dem Standardvorgehen zur röntgenologischen Kontrolle im Rahmen einer zahnärztlichen Implantattherapie. Seite 2 von 13
3 2. Wie ist der Ablauf der Studie und was muss ich bei Teilnahme beachten? Vor Aufnahme in diese klinische Studie werden Sie zu Ihren Vorerkrankungen und Ihrem aktuellen Gesundheitsstatus befragt, und Sie werden einer umfassenden zahnärztlichen Untersuchung unterzogen. Dazu gehören insbesondere die klinische Inspektion Ihrer Mundhöhle und der Prothesen, das Ausfüllen von Fragebögen zur Zufriedenheit/Unzufriedenheit mit den Prothesen Die Möglichkeit Ihrer weiteren Teilnahme an dieser klinischen Studie wird von den Ergebnissen dieser Voruntersuchung abhängen. Bei Teilnahme an der Studie werden Sie bei den Nachuntersuchungsterminen jeweils klinisch untersucht und gebeten, eine Testnahrung zur Ermittlung Ihrer Kaueffektivität zu kauen. Zusätzlich werden Sie Fragebögen zur mundgesundheitsbezogenen Lebensqualität und Ihrer Prothesenzufriedenheit ausfüllen. Röntgenuntersuchungen werden zur Implantatplanung, zur Kontrolle der eingesetzten Implantate und zur Verlaufskontrolle am Ende der Studie angefertigt. Wenn Sie von anderen Zahnärzten/Ärzten behandelt werden, müssen Sie diese über Ihre Teilnahme an der klinischen Studie informieren. Auch Ihr Prüfarzt muss über jede zahnmedizinische Behandlung, die Sie durch einen anderen Zahnarzt während der klinischen Studie erhalten, informiert werden. 4. Welchen persönlichen Nutzen habe ich von der Teilnahme an der Studie? Sie erhalten im Rahmen dieser Studie drei Implantate zur Verankerung Ihrer unteren Prothese. Hierdurch wird sich in der Regel der Prothesenhalt und dadurch Ihr Kauvermögen deutlich verbessern. 5. Welche Risiken sind mit der Teilnahme an der Studie verbunden? Die Anwendung von zahnärztlichen Implantaten beinhaltet intraoperative und postoperative Komplikationen. Zu den intraoperative Komplikationen Seite 3 von 13
4 gehören: Blutungen, Weichteil- und Nervverletzungen. Zu den postoperativen Komplikationen gehören die üblichen Risiken eines jeden chirurgischen Eingriffs wie z.b. mögliche Wundheilungsstörung, Wundinfektion, Schwellungen und postoperative Blutungen und Blutergussbildungen. Die Infektion kann den Implantatverlust zur Folge haben. Dieses Risiko liegt im zahnlosen Unterkiefer bei üblicher Einheilung unter 3%. Muss das Implantat wegen fehlender Einheilung entfernt werden, heilt der Knochen in der Regel wie nach einer Zahnextraktion komplikationslos ab. Darüber hinaus können die im Rahmen dieser klinischen Studie durchgeführten Maßnahmen mit Risiken behaftet sein oder zu Beschwerden führen. Im Einzelnen handelt es sich um Komplikationen mit Lokalanästhetika: Schmerzen, Schwellung, Bluterguss, Nervschädigung, Entzündung, körperliche Beschwerden wie Schwindel oder allergische Reaktionen. Sowie Gefahren durch ionisierende Strahlung (Röntgen) die potentiell Keimschädigend ist und eine Schädigung des Erbmaterials verursachen kann. Bitte teilen Sie den Mitarbeitern der Prüfstelle alle Beschwerden, Erkrankungen oder Verletzungen mit, die im Verlauf der klinischen Studie auftreten. Falls diese schwerwiegend sind, teilen Sie den Mitarbeitern der Prüfstelle diese bitte umgehend mit, ggf. telefonisch. Unmittelbar nach lokaler Anästhesie dürfen Sie für 3-4 Std. nicht aktiv am Straßenverkehr teilnehmen oder Maschinen führen. Ferner sollten Sie für den Zeitraum der Betäubung keine Speisen zu sich nehmen, um eine Verletzung der Mundhöhle durch die Zähne zu vermeiden. Seite 4 von 13
5 6. Wer darf an dieser klinischen Studie nicht teilnehmen? Sie können an dieser klinischen Studie nur teilnehmen, wenn Sie gesund sind und sich nicht gleichzeitig für andere klinische Studien oder andere klinische Forschungsprojekte zur Verfügung stellen. 7. Entstehen für mich Kosten durch die Teilnahme an der klinischen Studie? Erhalte ich eine Aufwandsentschädigung? Die Materialkosten der Implantate und der prothetischen Verbindungselemente, die Sie im Rahmen der Studie erhalten, werden Ihnen nicht in Rechnung gestellt. Sie erhalten keine Aufwandsentschädigung für Fahrtkosten etc. Als Folge der Einbringung des Verbindungselementes kann es durch die Materialschwächung im Bereich der Unterkieferprothese zu einem Bruch der Prothese kommen. Daher erfolgt zur Verstärkung das Einarbeiten eines nicht sichtbaren Metallgerüstes in Ihre Unterkiefertotalprothese. Durch das Einarbeitung und die Herstellung des Gerüstes werden Ihnen Mehrkosten i. H. v. ca. 250 entstehen. Die genaue Höhe der Kosten ist unterschiedlich, ebenso die Übernahme durch die Krankenkassen. Wir bitten Sie daher die Kosten mit Ihrer Krankenkasse zu besprechen, gerne erstellen wir Ihnen hierzu einen Heil- und Kostenplan. 8. Werden mir neue Erkenntnisse während der klinischen Studie mitgeteilt? Sie werden über neue Erkenntnisse, die in Bezug auf diese klinische Studie bekannt werden und die für Ihre Bereitschaft zur weiteren Teilnahme wesentlich sein können, informiert. Dies soll Sie darin unterstützen Ihre Entscheidung zur weiteren Teilnahme an dieser klinischen Studie überdenken. Seite 5 von 13
6 9. Wer entscheidet, ob ich aus der klinischen Studie ausscheide? Sie können jederzeit, auch ohne Angabe von Gründen, Ihre Teilnahme beenden, ohne dass Ihnen dadurch irgendwelche Nachteile entstehen. Unter gewissen Umständen ist es aber auch möglich, dass der Prüfarzt/die Prüfärztin entscheidet, Ihre Teilnahme an der klinischen Studie vorzeitig zu beenden, ohne dass Sie auf die Entscheidung Einfluss haben. Die Gründe hierfür können z. B. sein: Ihre weitere Teilnahme an der klinischen Studie ist ärztlich nicht mehr vertretbar. es wird die gesamte klinische Studie abgebrochen. Sie nehmen die geforderten Termine nicht wahr, so dass Ihre Daten nicht zu verwenden sind. Sofern Sie sich dazu entschließen, vorzeitig aus der klinischen Studie auszuscheiden, oder Ihre Teilnahme aus einem anderen der genannten Gründe vorzeitig beendet wird, ist es für Ihre eigene Sicherheit wichtig, dass Sie sich einer empfohlenen abschließenden Kontrolluntersuchung unterziehen. Der Prüfarzt wird mit Ihnen besprechen, ob und wann weitere Kontrolluntersuchungen notwendig sind. 11. Was geschieht mit meinen Daten? Während der klinischen Studie werden medizinische Befunde und persönliche Informationen von Ihnen erhoben und in der Prüfstelle in Ihrer persönlichen Akte niedergeschrieben oder elektronisch gespeichert. Die für die klinische Studie wichtigen Daten werden zusätzlich in pseudonymisierter Form gespeichert, ausgewertet und gegebenenfalls weitergegeben. Pseudonymisiert bedeutet, dass keine Initialen verwendet werden, sondern nur ein Nummern- und/oder Buchstabencode, evtl. mit Angabe des Geburtsjahres. Die Daten sind gegen unbefugten Zugriff gesichert. Eine Entschlüsselung erfolgt nur unter den vom Gesetz vorgeschriebenen Voraussetzungen. Seite 6 von 13
7 Die gesetzlichen Bestimmungen enthalten nähere Vorgaben für den erforderlichen Umfang der Einwilligung in die Datenerhebung und - verwendung. Einzelheiten, insbesondere zur Möglichkeit eines Widerrufs, entnehmen Sie bitte der Einwilligungserklärung, die im Anschluss an diese Studienteilnehmerinformation abgedruckt ist. 12. Was geschieht mit meinen Röntgenaufnahmen und Modellen Die Röntgenaufnahmen werden entsprechend den Vorgaben der gültigen Röntgenverordnung aufbewahrt. Die zahntechnischen Gipsmodelle werden am Prüfzentrum auf unbestimmte Zeit gelagert und werden zu späteren Zeitpunkten ggf. zur Auswertung herangezogen. 13. An wen wende ich mich bei weiteren Fragen? Beratungsgespräche an der Prüfstelle Sie haben stets die Gelegenheit zu weiteren Beratungsgesprächen mit dem auf Seite 1 genannten oder einem anderen Prüfarzt /einer anderen Prüfärztin, um weitere Fragen im Zusammenhang mit der klinischen Studie zu klären. Auch Fragen, die Ihre Rechte und Pflichten als Teilnehmer an der klinischen Studie betreffen, werden gerne beantwortet. Prüfstelle: Klinik für Zahnärztliche Prothetik, Propädeutik und Werkstoffkunde Universitätsklinikum Kiel, Arnold-Heller-Str.16, Kiel, Tel: / 402 Prüfarzt: Dr. Sad Chaar, Arnold-Heller-Str.16, Kiel, Tel: Seite 7 von 13
8 Einfluss der Implantatanzahl im zahnlosen Unterkiefer auf die Kaueffektivität eine klinische intra-individuelle Studie Einwilligungserklärung... Name des Studienteilnehmers in Druckbuchstaben geb. am... Teilnehmer-Nr.... Ich bin in einem persönlichen Gespräch durch den Prüfarzt/ die Prüfärztin... Name der Ärztin/des Arztes ausführlich und verständlich über das Verfahren sowie über Wesen, Bedeutung, Risiken und Tragweite der klinischen Studie aufgeklärt worden. Ich habe darüber hinaus den Text der Studienteilnehmerinformation sowie die hier nachfolgend abgedruckte Datenschutzerklärung gelesen und verstanden. Ich hatte die Gelegenheit, mit dem Prüfarzt/ der Prüfärztin über die Durchführung der klinischen Studie zu sprechen. Alle meine Fragen wurden zufrieden stellend beantwortet. Möglichkeit zur Dokumentation zusätzlicher Fragen seitens des Studienteilnehmers oder sonstiger Aspekte des Aufklärungsgesprächs: Ich hatte ausreichend Zeit, mich zu entscheiden. Mir ist bekannt, dass ich jederzeit und ohne Angabe von Gründen meine Einwilligung zur Teilnahme an der Studie zurückziehen kann (mündlich oder schriftlich), ohne dass mir daraus Nachteile entstehen. Seite 8 von 13
9 Datenschutz: Mir ist bekannt, dass bei dieser klinischen Studie personenbezogene Daten, insbesondere medizinische Befunde über mich erhoben, gespeichert und ausgewertet werden sollen. Die Verwendung der Angaben über meine Gesundheit erfolgt nach gesetzlichen Bestimmungen (u.a. Bundesdatenschutzgesetzt 4) und setzt vor der Teilnahme an der klinischen Studie folgende freiwillig abgegebene Einwilligungserklärung voraus, das heißt ohne die nachfolgende Einwilligung kann ich nicht an der klinischen Studie teilnehmen. 1. Ich erkläre mich damit einverstanden, dass im Rahmen dieser klinischen Studie personenbezogene Daten, insbesondere Angaben über meine Gesundheit, über mich erhoben und in Papierform sowie auf elektronischen Datenträgern in der Klinik für Zahnärztliche Prothetik, Propädeutik und Werkstoffkunde, Universitätsklinikum Kiel, Arnold-Heller Str. 16, Kiel aufgezeichnet werden. Soweit erforderlich, dürfen die erhobenen Daten pseudonymisiert (verschlüsselt) weitergegeben werden: a) eine von der Klinik für Zahnärztliche Prothetik, Propädeutik und Werkstoffkunde, Universitätsklinikum Kiel, Arnold-Heller Str. 16, Kiel, beauftragte Stelle zum Zwecke der wissenschaftlichen Auswertung, b) im Falle unerwünschter Ereignisse: an die zuständige Ethikkommission. 2. Außerdem erkläre ich mich damit einverstanden, dass autorisierte und zur Verschwiegenheit verpflichtete Beauftragte des Auftraggebers in meine beim Prüfarzt/bei der Prüfärztin vorhandenen personenbezogenen Daten, insbesondere meine Gesundheitsdaten, Einsicht nehmen, soweit dies für die Überprüfung der ordnungsgemäßen Durchführung der Studie notwendig ist. Für diese Maßnahme entbinde ich den Prüfarzt/ die Prüfärztin von der ärztlichen Schweigepflicht. 3. Ich bin darüber aufgeklärt worden, dass ich jederzeit die Teilnahme an der klinischen Studie beenden kann. Beim Widerruf meiner Einwilligung, an der Studie teilzunehmen, habe ich das Recht, die Löschung aller meiner bis dahin gespeicherten personenbezogenen Daten zu verlangen. Seite 9 von 13
10 4. Ich erkläre mich damit einverstanden, dass meine Daten nach Beendigung oder Abbruch der Studie mindestens zehn Jahre aufbewahrt werden. Danach werden meine personenbezogenen Daten gelöscht, soweit nicht gesetzliche, satzungsmäßige oder vertragliche Aufbewahrungsfristen entgegenstehen. 5. Ich bin damit einverstanden, dass mein Hausarzt/Zahnarzt Name über meine Teilnahme an der klinischen Studie informiert wird (falls nicht gewünscht, bitte streichen). Seite 10 von 13
11 Ich erkläre mich bereit, an der oben genannten klinischen Studie freiwillig teilzunehmen. Ein Exemplar der habe ich erhalten. Ein Exemplar verbleibt im Prüfzentrum.... Name des Studienteilnehmers in Druckbuchstaben Datum Unterschrift des Studienteilnehmers Ich habe das Aufklärungsgespräch geführt und die Einwilligung des Studienteilnehmers eingeholt.... Name des Prüfarztes/der Prüfärztin in Druckbuchstaben Datum Unterschrift des aufklärenden Prüfarztes/der Prüfärztin Seite 11 von 13
für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten
 PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
Strategische Mini-Dental-Implantate (MDI) zur Stabilisierung von herausnehmbaren Teilprothesen.
 Prüfeinrichtung: Prüfstelle: Studienleiter: Koordinator Studien: Prüfarzt: Universitätsmedizin Greifswald Poliklinik für Zahnärztliche Prothetik, Alterszahnmedizin und medizinische Werkstoffkunde Rorgerberstr.
Prüfeinrichtung: Prüfstelle: Studienleiter: Koordinator Studien: Prüfarzt: Universitätsmedizin Greifswald Poliklinik für Zahnärztliche Prothetik, Alterszahnmedizin und medizinische Werkstoffkunde Rorgerberstr.
wir möchten Sie fragen, ob Sie bereit sind, an der von uns vorgesehenen klinischen Studie teilzunehmen.
 Universitätsklinikum Essen. Neurologische Klinik und Poliklinik. Hufelandstr. 55. 45122 Essen Sehr geehrte Dame, sehr geehrter Herr, wir möchten Sie fragen, ob Sie bereit sind, an der von uns vorgesehenen
Universitätsklinikum Essen. Neurologische Klinik und Poliklinik. Hufelandstr. 55. 45122 Essen Sehr geehrte Dame, sehr geehrter Herr, wir möchten Sie fragen, ob Sie bereit sind, an der von uns vorgesehenen
Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen
 Prüfstelle: Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen Simultaneous Study of Docetaxel Based Anthracycline Free Adjuvant Treatment Evaluation,
Prüfstelle: Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen Simultaneous Study of Docetaxel Based Anthracycline Free Adjuvant Treatment Evaluation,
Klinik für Herz-, Kinderherz- und Gefäßchirurgie Prof. Dr. med. A. Böning
 Klinik für Herz-, Kinderherz- und Gefäßchirurgie Prof. Dr. med. A. Böning Prüfarzte: Klinik für Herz-, Kinderherz- und Gefäßchirurgie Prof. Dr. Andreas Böning Dr. Peter Roth Dr. Coskun Orhan Prof. Dr.
Klinik für Herz-, Kinderherz- und Gefäßchirurgie Prof. Dr. med. A. Böning Prüfarzte: Klinik für Herz-, Kinderherz- und Gefäßchirurgie Prof. Dr. Andreas Böning Dr. Peter Roth Dr. Coskun Orhan Prof. Dr.
Probandeninformation für Patienten mit Bluthochdruck
 Medizinischen Klinik und Poliklinik III Direktor: Prof. Dr. med. Stefan Bornstein Probandeninformation für Patienten mit Bluthochdruck Studie über Monoamine-produzierende Tumore The PMT-study: Prospective
Medizinischen Klinik und Poliklinik III Direktor: Prof. Dr. med. Stefan Bornstein Probandeninformation für Patienten mit Bluthochdruck Studie über Monoamine-produzierende Tumore The PMT-study: Prospective
MUSTERTEXT. empfohlen vom Arbeitskreis Medizinischer Ethik-Kommissionen gemäß Beschluss vom
 MUSTERTEXT für die Probanden-Information und -Einwilligung zur Durchführung einer klinischen Prüfung eines Medizinprodukts mit volljährigen einwilligungsfähigen Probanden 1 empfohlen vom Arbeitskreis Medizinischer
MUSTERTEXT für die Probanden-Information und -Einwilligung zur Durchführung einer klinischen Prüfung eines Medizinprodukts mit volljährigen einwilligungsfähigen Probanden 1 empfohlen vom Arbeitskreis Medizinischer
MUSTERTEXT. Alle kursiv gedruckten Textstellen enthalten Hinweise zum Erstellen der Patienten-Information und -Einwilligung
 MUSTERTEXT für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Prüfung eines Medizinprodukts mit volljährigen einwilligungsfähigen Patienten 1 Hinweis Dieser Mustertext basiert
MUSTERTEXT für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Prüfung eines Medizinprodukts mit volljährigen einwilligungsfähigen Patienten 1 Hinweis Dieser Mustertext basiert
MUSTERTEXT. empfohlen vom Arbeitskreis Medizinischer Ethik-Kommissionen gemäß Beschluss vom
 MUSTERTEXT für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Prüfung eines Medizinprodukts mit volljährigen einwilligungsfähigen Patienten 1 empfohlen vom Arbeitskreis Medizinischer
MUSTERTEXT für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Prüfung eines Medizinprodukts mit volljährigen einwilligungsfähigen Patienten 1 empfohlen vom Arbeitskreis Medizinischer
Patienteninformation zur klinischen Studie:
 UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
97080 Würzburg Tel.:
 97080 Würzburg Tel.: 0931 201 47307 Email: peter.heuschmann@uni-wuerzburg.de Anhang 2 Muster der Patienteninformation / Teilnehmerinformation Berlin, den 04.01.2012 Patienteninformation / Teilnehmerinformation
97080 Würzburg Tel.: 0931 201 47307 Email: peter.heuschmann@uni-wuerzburg.de Anhang 2 Muster der Patienteninformation / Teilnehmerinformation Berlin, den 04.01.2012 Patienteninformation / Teilnehmerinformation
Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie
 Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie APRES: Angemessenheit der Antibiotika -Verschreibungen in der hausärztlichen Praxis in Europa im Hinblick
Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie APRES: Angemessenheit der Antibiotika -Verschreibungen in der hausärztlichen Praxis in Europa im Hinblick
MUSTERTEXT. Alle kursiv gedruckten Textstellen enthalten Hinweise zum Erstellen der Probanden-Information und -Einwilligung
 MUSTERTEXT für die Probanden-Information und -Einwilligung zur Durchführung einer klinischen Prüfung eines Arzneimittels mit volljährigen einwilligungsfähigen Probanden 1 Hinweis Dieser Mustertext basiert
MUSTERTEXT für die Probanden-Information und -Einwilligung zur Durchführung einer klinischen Prüfung eines Arzneimittels mit volljährigen einwilligungsfähigen Probanden 1 Hinweis Dieser Mustertext basiert
Titel der Studie Genetik des chronischen idiopathischen Stotterns
 Studienstelle: Klinik für Klinische Neurophysiologie, Medizinische Fakultät, Universität Göttingen, Robert-Koch-Str. 40, 37075 Göttingen, Tel.: 0551/3966650, Telefax: 0551/398126 Studienarzt: Prof. Dr.
Studienstelle: Klinik für Klinische Neurophysiologie, Medizinische Fakultät, Universität Göttingen, Robert-Koch-Str. 40, 37075 Göttingen, Tel.: 0551/3966650, Telefax: 0551/398126 Studienarzt: Prof. Dr.
Patienteninformation:
 Patienteninformation: Synthetisches Netz versus kein Netz bei Nabelbrüchen: eine prospektive, doppelblinde, randomisierte, kontrollierte Studie Synthetic mesh versus no mesh for umbilical hernias: a prospective
Patienteninformation: Synthetisches Netz versus kein Netz bei Nabelbrüchen: eine prospektive, doppelblinde, randomisierte, kontrollierte Studie Synthetic mesh versus no mesh for umbilical hernias: a prospective
PATIENTEN INFORMATION. Deutsches Klinisches Register. Therapie und medizinische Versorgung von Patienten mit moderater bis schwerer Neurodermitis
 PATIENTEN INFORMATION Deutsches Klinisches Register Therapie und medizinische Versorgung von Patienten mit moderater bis schwerer Neurodermitis Sehr geehrte Patientin, Sehr geehrter Patient, wir möchten
PATIENTEN INFORMATION Deutsches Klinisches Register Therapie und medizinische Versorgung von Patienten mit moderater bis schwerer Neurodermitis Sehr geehrte Patientin, Sehr geehrter Patient, wir möchten
Informationsschrift. Momentum Projekt Heidelberg Aktiver Umgang mit einer Krebserkrankung
 Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Informationsschrift. Momentum Projekt Heidelberg Aktiver Umgang mit einer Krebserkrankung
 Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
UniversitätsKlinikum Heidelberg
 Chirurgische Universitätsklinik Im Neuenheimer Feld 110 D-69120 Heidelberg Studienleitung Prof. Dr.med. Jürgen Weitz, Leiter der Sektion Chirurgische Onkologie der Chirurgischen Universitätsklinik Studienkoordination
Chirurgische Universitätsklinik Im Neuenheimer Feld 110 D-69120 Heidelberg Studienleitung Prof. Dr.med. Jürgen Weitz, Leiter der Sektion Chirurgische Onkologie der Chirurgischen Universitätsklinik Studienkoordination
Patienteninformation
 Patienteninformation zum MS-Register der DMSG, Bundesverband e.v. Sehr geehrte Patientin, sehr geehrter Patient, wir möchten Sie um Ihre Einwilligung zur Teilnahme an dem MS-Register der DMSG, Bundesverband
Patienteninformation zum MS-Register der DMSG, Bundesverband e.v. Sehr geehrte Patientin, sehr geehrter Patient, wir möchten Sie um Ihre Einwilligung zur Teilnahme an dem MS-Register der DMSG, Bundesverband
Patienteninformation und Einwilligungserklärung zur Teilnahme an der klinischen Prüfung
 Patienteninformation und Einwilligungserklärung zur Teilnahme an der klinischen Prüfung EINE RANDOMISIERTE, MULTIZENTRISCHE, PROSPEKTIVE, BEOBACHTER UND PATIENTEN VERBLINDETE STUDIE ZUR BEURTEILUNG VON
Patienteninformation und Einwilligungserklärung zur Teilnahme an der klinischen Prüfung EINE RANDOMISIERTE, MULTIZENTRISCHE, PROSPEKTIVE, BEOBACHTER UND PATIENTEN VERBLINDETE STUDIE ZUR BEURTEILUNG VON
2. Um welche Art von Biomaterialien und Daten handelt es sich?
 150701 Biobank Augenklinik Version 1_modek.docx Klinik für Augenheilkunde Universitätsklinikum Freiburg Killianstraße 5 D-79106 Freiburg Spende, Einlagerung und Nutzung von Biomaterialien sowie Erhebung,
150701 Biobank Augenklinik Version 1_modek.docx Klinik für Augenheilkunde Universitätsklinikum Freiburg Killianstraße 5 D-79106 Freiburg Spende, Einlagerung und Nutzung von Biomaterialien sowie Erhebung,
Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen
 Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen Sehr geehrte Patientin, sehr geehrter Patient Wir laden Sie ein, an der
Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen Sehr geehrte Patientin, sehr geehrter Patient Wir laden Sie ein, an der
Information Dimensionen der Bedeutsamkeit / Spiritualität bei Menschen mit Down-Syndrom
 ( Die folgenden 3 Seiten bitte entweder per Post oder per Email zusenden!) Sehr geehrte Damen und Herren, im Rahmen eines Promotionsvorhabens an der Universität Witten/Herdecke möchten wir Menschen mit
( Die folgenden 3 Seiten bitte entweder per Post oder per Email zusenden!) Sehr geehrte Damen und Herren, im Rahmen eines Promotionsvorhabens an der Universität Witten/Herdecke möchten wir Menschen mit
Wie ist der Ablauf der Studie, welche Daten werden erhoben und was muss ich bei der Teilnahme
 Information und Einverständniserklärung über die Teilnahme an der Studie zur Verbesserung der Ergebnisqualität beim lokal begrenzten Prostatakarzinom ( Prostate Cancer Outcomes Study ) Sehr geehrter Patient,
Information und Einverständniserklärung über die Teilnahme an der Studie zur Verbesserung der Ergebnisqualität beim lokal begrenzten Prostatakarzinom ( Prostate Cancer Outcomes Study ) Sehr geehrter Patient,
PatientInneninformation und Einwilligungserklärung zur Teilnahme an der Pilotstudie
 PatientInneninformation und Einwilligungserklärung zur Teilnahme an der Pilotstudie Effekt einer Reduktion von tierischem Eiweiß auf den Verlauf einer bestehenden Krebserkrankung Sehr geehrte Teilnehmerin,
PatientInneninformation und Einwilligungserklärung zur Teilnahme an der Pilotstudie Effekt einer Reduktion von tierischem Eiweiß auf den Verlauf einer bestehenden Krebserkrankung Sehr geehrte Teilnehmerin,
Versicherteninformation. Versicherteninformation. Besondere Versorgung (DAK-Spezialisten-Netzwerk) BC72IV028 / DA003
 Besondere Versorgung (DAK-Spezialisten-Netzwerk) Anlage 8 zum Diabetes-Vertrag mit der Kassenärztlichen Vereinigung Berlin Vertrags-Nr.: BC72IV028 / 171722DA003 Versicherteninformation Versicherteninformation
Besondere Versorgung (DAK-Spezialisten-Netzwerk) Anlage 8 zum Diabetes-Vertrag mit der Kassenärztlichen Vereinigung Berlin Vertrags-Nr.: BC72IV028 / 171722DA003 Versicherteninformation Versicherteninformation
PATIENTENINFORMATION. Caregiver Burden bei betreuenden Angehörigen schwer betroffener Parkinsonpatienten
 Version 1.2 Neurologische Klinik mit Klinischer Neurophysiologie Kommissarischer Direktor: Prof. Dr. med. M. Stangel PD Dr. med. F. Wegner Telefon: (0511) 532-3110 Fax: (0511) 532-3115 Carl-Neuberg-Straße
Version 1.2 Neurologische Klinik mit Klinischer Neurophysiologie Kommissarischer Direktor: Prof. Dr. med. M. Stangel PD Dr. med. F. Wegner Telefon: (0511) 532-3110 Fax: (0511) 532-3115 Carl-Neuberg-Straße
Antrag zur Durchführung einer epidemiologischen Studie
 Absender/ Begleitschreiben: Antrag zur Durchführung einer epidemiologischen Studie 1. Bezeichnung der Studie 2. Ziel der Studie Fragestellung (einschl. Formulierung der Forschungshypothese) Relevanz für
Absender/ Begleitschreiben: Antrag zur Durchführung einer epidemiologischen Studie 1. Bezeichnung der Studie 2. Ziel der Studie Fragestellung (einschl. Formulierung der Forschungshypothese) Relevanz für
Patientenaufklärungs- und Informationshinweise
 Patientenaufklärungs- und Informationshinweise ZIELSETZUNG DER STUDIE Ihnen wird hiermit die Teilnahme an einer klinischen Studie angeboten. Ziel dieser Studie ist der klinische Ausgang und der Wirksamkeitsnachweis
Patientenaufklärungs- und Informationshinweise ZIELSETZUNG DER STUDIE Ihnen wird hiermit die Teilnahme an einer klinischen Studie angeboten. Ziel dieser Studie ist der klinische Ausgang und der Wirksamkeitsnachweis
Register zur Epidemiologie, Diagnostik und Therapie der C3 Glomerulopathie und der Immunkomplex vermittelten MPGN
 Patienteninformation und Einwilligungserklärung inkl. Datenschutzerklärung Register zur Epidemiologie, Diagnostik und Therapie der C3 Glomerulopathie und der Immunkomplex-vermittelten MPGN Kurzbezeichnung:
Patienteninformation und Einwilligungserklärung inkl. Datenschutzerklärung Register zur Epidemiologie, Diagnostik und Therapie der C3 Glomerulopathie und der Immunkomplex-vermittelten MPGN Kurzbezeichnung:
PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG
 PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG Nicht-interventionelle Studie zu Edoxaban für die Behandlung des nicht-valvulären Vorhofflimmerns in der klinischen Routine (ETNA-AF-Europe) Nummer der klinischen
PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG Nicht-interventionelle Studie zu Edoxaban für die Behandlung des nicht-valvulären Vorhofflimmerns in der klinischen Routine (ETNA-AF-Europe) Nummer der klinischen
Sehr geehrte Damen und Herren,
 1 UKSH, Campus Lübeck, Ratzeburger Allee 160, CBBM, 23538 Lübeck CBBM (Center for Brain, Behavior and Metabolism) Institut für Neurogenetik Direktorin: Prof. Dr. med. Christine Klein Bewegungsstörungen
1 UKSH, Campus Lübeck, Ratzeburger Allee 160, CBBM, 23538 Lübeck CBBM (Center for Brain, Behavior and Metabolism) Institut für Neurogenetik Direktorin: Prof. Dr. med. Christine Klein Bewegungsstörungen
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Information für die Betreuerin / den Betreuer zur Aufklärung zur Studie:
 Information für die Betreuerin / den Betreuer zur Aufklärung zur Studie: Neurochirurgische Klinik und Poliklinik Frühe lumbale Drainage nach aneurysmatischer Subarachnoidalblutung: eine randomisierte,
Information für die Betreuerin / den Betreuer zur Aufklärung zur Studie: Neurochirurgische Klinik und Poliklinik Frühe lumbale Drainage nach aneurysmatischer Subarachnoidalblutung: eine randomisierte,
Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms)
 Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms) Die Anwendung kurz andauernder magnetischer Reize über dem intakten Schädeldach bewirkt auf der Grundlage der elektromagnetischen
Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms) Die Anwendung kurz andauernder magnetischer Reize über dem intakten Schädeldach bewirkt auf der Grundlage der elektromagnetischen
WAS WIRD IN DER STUDIE GEMACHT?
 Probandeninformation Online-Befragung Betreuungspersonen Klinik für Kinder- und Jugendpsychiatrie/ Psychotherapie Ärztlicher Direktor: Prof. Dr. med. Jörg M. Fegert Steinhövelstr. 5 Titel der Studie: Ich
Probandeninformation Online-Befragung Betreuungspersonen Klinik für Kinder- und Jugendpsychiatrie/ Psychotherapie Ärztlicher Direktor: Prof. Dr. med. Jörg M. Fegert Steinhövelstr. 5 Titel der Studie: Ich
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Patienteninformation. Sehr geehrte Patientin, sehr geehrter Patient,
 und Biomaterialbank Biomaterialsammlung und prospektive Datenerfassung zu Diagnostik, Behandlung und Krankheitsverlauf der ALL des Erwachsenen Patienteninformation Sehr geehrte Patientin, sehr geehrter
und Biomaterialbank Biomaterialsammlung und prospektive Datenerfassung zu Diagnostik, Behandlung und Krankheitsverlauf der ALL des Erwachsenen Patienteninformation Sehr geehrte Patientin, sehr geehrter
Aufklärungs- und Einwilligungsbogen für eine Zahnextraktion
 Name: Vorname: Geburtsdatum: Aufklärungs- und Einwilligungsbogen für eine Zahnextraktion Liebe Patientin, lieber Patient, liebe Eltern, ein oder mehrere Zähne müssen gezogen werden. Vor der Zahnextraktion
Name: Vorname: Geburtsdatum: Aufklärungs- und Einwilligungsbogen für eine Zahnextraktion Liebe Patientin, lieber Patient, liebe Eltern, ein oder mehrere Zähne müssen gezogen werden. Vor der Zahnextraktion
Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle,
 Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle, prospektive Kohortenstudie Protokoll: Initiator: EuroTARGET: Europäisches Forschungsprojekt
Patienteninformation und Einverständniserklärung zur Durchführung genetischer Analysen im Zuge einer nichtinterventionelle, prospektive Kohortenstudie Protokoll: Initiator: EuroTARGET: Europäisches Forschungsprojekt
Fachbereich Humanmedizin / Klinikum der Johann Wolfgang Goethe-Universität Frankfurt am Main
 PATIENTENINFORMATIONSBLATT: Patientenaufklärung zur Teilnahme an einer wissenschaftlichen Studie Pilot-Studie: Anwendungsbeobachtung zur Evaluierung der therapeutischen Wirksamkeit und Sicherheit bei Durchführung
PATIENTENINFORMATIONSBLATT: Patientenaufklärung zur Teilnahme an einer wissenschaftlichen Studie Pilot-Studie: Anwendungsbeobachtung zur Evaluierung der therapeutischen Wirksamkeit und Sicherheit bei Durchführung
PATIENTENAUFKLÄRUNG ZWECK DER ZUSATZUNTERSUCHUNG
 Immunologische und molekularbiologische Untersuchungen im Blut und im Gewebe zur Verbesserung der Diagnostik als PATIENTENAUFKLÄRUNG Sie werden gebeten, an einer Zusatzuntersuchung zur Bestimmung Ihres
Immunologische und molekularbiologische Untersuchungen im Blut und im Gewebe zur Verbesserung der Diagnostik als PATIENTENAUFKLÄRUNG Sie werden gebeten, an einer Zusatzuntersuchung zur Bestimmung Ihres
Zahnimplantate. Der sichere Weg zu mehr Lebensqualität. Dr. Eric Liermann Zahnarzt und Implantologe, Köln
 Zahnimplantate Der sichere Weg zu mehr Lebensqualität Dr. Eric Liermann Zahnarzt und Implantologe, Köln Zahnmedizinische Qualifikation Dr. Eric Liermann 1981 1987 Studium der Zahnmedizin 1987 Promotion
Zahnimplantate Der sichere Weg zu mehr Lebensqualität Dr. Eric Liermann Zahnarzt und Implantologe, Köln Zahnmedizinische Qualifikation Dr. Eric Liermann 1981 1987 Studium der Zahnmedizin 1987 Promotion
Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme)......
 Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme) Name und Anschrift der Einrichtung, in der die klinische Prüfung durchgeführt wird (Prüfzentrum) Name und Telefon-Nummer des/r
Einwilligungserklärung zur klinischen Prüfung: Teil 2 (vor Studienaufnahme) Name und Anschrift der Einrichtung, in der die klinische Prüfung durchgeführt wird (Prüfzentrum) Name und Telefon-Nummer des/r
PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG ZUR LAGERUNG VON BLUTPROBEN
 PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG ZUR LAGERUNG VON BLUTPROBEN Eine placebo-kontrollierte, doppelblinde, randomisierte multizentrische dreiarmige Phase III Studie zu Effektivität und Sicherheit
PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG ZUR LAGERUNG VON BLUTPROBEN Eine placebo-kontrollierte, doppelblinde, randomisierte multizentrische dreiarmige Phase III Studie zu Effektivität und Sicherheit
Patienteninformation Teil 2 Untersuchung der Erbsubstanz (genetische und epigenetische Untersuchung) der Blutproben für das
 Technische Universität München Leiter des Forschungsvorhaben Univ.-Prof. Dr. Wolfgang Dott Direktor des Instituts für Hygiene und Umweltmedizin Pauwelsstr. 30 D 52074 Aachen Telefon (+49) 0241 80 88 385
Technische Universität München Leiter des Forschungsvorhaben Univ.-Prof. Dr. Wolfgang Dott Direktor des Instituts für Hygiene und Umweltmedizin Pauwelsstr. 30 D 52074 Aachen Telefon (+49) 0241 80 88 385
1. Nachtrag zum Vertrag nach 73 c SGB V über die Durchführung eines ergänzenden Hautkrebsvorsorge-Verfahrens
 TK-Vertragsnummer: 500015 1. Nachtrag zum Vertrag nach 73 c SGB V über die Durchführung eines ergänzenden Hautkrebsvorsorge-Verfahrens zwischen der Kassenärztlichen Vereinigung Hamburg Humboldtstr. 56
TK-Vertragsnummer: 500015 1. Nachtrag zum Vertrag nach 73 c SGB V über die Durchführung eines ergänzenden Hautkrebsvorsorge-Verfahrens zwischen der Kassenärztlichen Vereinigung Hamburg Humboldtstr. 56
Patientenaufklärung. Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:...
 Patientenaufklärung Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Art der Erkrankung, Ziel der Chemotherapie und Zweck der Studie Sehr geehrte
Patientenaufklärung Patientenname:... Vorname:... Geburtsdatum:... Diagnose:... Das Aufklärungsgespräch erfolgte am:... durch:... Art der Erkrankung, Ziel der Chemotherapie und Zweck der Studie Sehr geehrte
Information für die Betreuerin / den Betreuer zur Aufklärung zur Studie:
 Information für die Betreuerin / den Betreuer zur Aufklärung zur Studie: Frühe lumbale Drainage nach aneurysmatischer Subarachnoidalblutung: eine randomisierte, kontrollierte Studie (EARLYDRAIN) Prüfstelle:
Information für die Betreuerin / den Betreuer zur Aufklärung zur Studie: Frühe lumbale Drainage nach aneurysmatischer Subarachnoidalblutung: eine randomisierte, kontrollierte Studie (EARLYDRAIN) Prüfstelle:
1. Aushändigen der Informationsschrift an die Patientin Q
 1 universitäts Prof. Dr. med. Annegret Geipel Leitung Pränatale Medizin DEGUM Stufe III Spezielle Geburtshilfe und Perinatalmedizin Studienzentrale PraenaTest Frau Claudia Büthke Fon:+49 (0) 228-287 14728
1 universitäts Prof. Dr. med. Annegret Geipel Leitung Pränatale Medizin DEGUM Stufe III Spezielle Geburtshilfe und Perinatalmedizin Studienzentrale PraenaTest Frau Claudia Büthke Fon:+49 (0) 228-287 14728
EUREKA-Register des Europäischen Leukämienetzes (ELN) Patienteninformation
 Universitätsklinikum Jena Prof. Dr. Andreas Hochhaus Klinik für Innere Medizin II Tel. 03641 932 4201 Abteilung Hämatologie/Onkologie Fax 03641 932 4202 Erlanger Allee 101 cml@med.uni-jena.de 07740 Jena
Universitätsklinikum Jena Prof. Dr. Andreas Hochhaus Klinik für Innere Medizin II Tel. 03641 932 4201 Abteilung Hämatologie/Onkologie Fax 03641 932 4202 Erlanger Allee 101 cml@med.uni-jena.de 07740 Jena
Zahnimplantate. für ein sicheres Lächeln. Fester Biss dank sicherer Verbindung mit Implantaten
 Zahnimplantate für ein sicheres Lächeln Fester Biss dank sicherer Verbindung mit Implantaten Fragen Sie uns, wir beraten Sie gern! Herzlich Willkommen in unserer Zahnarztpraxis! Der Aufenthalt bei uns
Zahnimplantate für ein sicheres Lächeln Fester Biss dank sicherer Verbindung mit Implantaten Fragen Sie uns, wir beraten Sie gern! Herzlich Willkommen in unserer Zahnarztpraxis! Der Aufenthalt bei uns
Probanden-Information für Forschungsvorhaben mit fmrt-untersuchungen
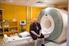 Klinik für Psychiatrie und Psychotherapie Philipps-Universität Marburg Probanden-Information für Forschungsvorhaben mit fmrt-untersuchungen zur Vorbereitung der mündlichen Aufklärung durch den Untersucher
Klinik für Psychiatrie und Psychotherapie Philipps-Universität Marburg Probanden-Information für Forschungsvorhaben mit fmrt-untersuchungen zur Vorbereitung der mündlichen Aufklärung durch den Untersucher
Sehr geehrte/r Interessent/in an der Studie zu den Hirnveränderungen von Meditation,
 vs. 2.0, 06.12.15 Sehr geehrte/r Interessent/in an der Studie zu den Hirnveränderungen von Meditation, Es ist bereits bekannt, dass jede dauerhafte Beschäftigung mit geistiger Anregung (z.b. Klavierspielen)
vs. 2.0, 06.12.15 Sehr geehrte/r Interessent/in an der Studie zu den Hirnveränderungen von Meditation, Es ist bereits bekannt, dass jede dauerhafte Beschäftigung mit geistiger Anregung (z.b. Klavierspielen)
Patienteninformation und Einwilligungserklärung. zur Teilnahme am Nephronophthise-Register
 Patienteninformation und Einwilligungserklärung zur Teilnahme am Nephronophthise-Register Auftraggeber der Studie: Prof. Dr. med. Heymut Omran Direktor der Klinik und Poliklinik für Kinder- und Jugendmedizin
Patienteninformation und Einwilligungserklärung zur Teilnahme am Nephronophthise-Register Auftraggeber der Studie: Prof. Dr. med. Heymut Omran Direktor der Klinik und Poliklinik für Kinder- und Jugendmedizin
Implantate fürs Leben. Feste Zähne am Tag der Implantation
 Implantate fürs Leben Feste Zähne am Tag der Implantation Feste Zähne am Tag der Implantation Leiden Sie darunter, dass Sie Ihre Zähne verloren haben? Haben Sie genug von locker sitzenden dritten Zähnen,
Implantate fürs Leben Feste Zähne am Tag der Implantation Feste Zähne am Tag der Implantation Leiden Sie darunter, dass Sie Ihre Zähne verloren haben? Haben Sie genug von locker sitzenden dritten Zähnen,
Chirurgische Klinik PD Dr. Daniel Weber Leitender Arzt Leiter Handchirurgie
 Chirurgische Klinik PD Dr. Daniel Weber Leitender Arzt Leiter Handchirurgie Kinderspital Zürich - Eleonorenstiftung Steinwiesstrasse 75 CH-8032 Zürich www.kispi.uzh.ch Kontakt Dr. phil. Norma Ruppen-Greeff
Chirurgische Klinik PD Dr. Daniel Weber Leitender Arzt Leiter Handchirurgie Kinderspital Zürich - Eleonorenstiftung Steinwiesstrasse 75 CH-8032 Zürich www.kispi.uzh.ch Kontakt Dr. phil. Norma Ruppen-Greeff
Bundesversicherungsanstalt für Angestellte
 Anregung zur Gestaltung von Patienteninformationen über Forschungsvorhaben in Form von Textbausteinen: 1. Erkennbarkeit der anwerbenden Stelle und ein Hinweis auf die Verantwortlichkeit für das Forschungsvorhaben
Anregung zur Gestaltung von Patienteninformationen über Forschungsvorhaben in Form von Textbausteinen: 1. Erkennbarkeit der anwerbenden Stelle und ein Hinweis auf die Verantwortlichkeit für das Forschungsvorhaben
Weiterverwendung von Patientendaten
 FORSCHUNGSKOMMISSION KSW KANTONSSPITAL WINTERTHUR Brauerstrasse 15 Postfach 834 8401 Winterthur Tel. 052 266 21 21 info@ksw.ch www.ksw.ch Weiterverwendung von Patientendaten Kontakt Zentrale Studienkoordination
FORSCHUNGSKOMMISSION KSW KANTONSSPITAL WINTERTHUR Brauerstrasse 15 Postfach 834 8401 Winterthur Tel. 052 266 21 21 info@ksw.ch www.ksw.ch Weiterverwendung von Patientendaten Kontakt Zentrale Studienkoordination
PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG
 Studiennummer: - PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG Registerstudie zur Proktokolektomie bei Colitis ulcerosa (ReProCu-Studie) Dokumentation zur Erforschung der Colitis ulcerosa für die verbesserte
Studiennummer: - PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG Registerstudie zur Proktokolektomie bei Colitis ulcerosa (ReProCu-Studie) Dokumentation zur Erforschung der Colitis ulcerosa für die verbesserte
empfohlen vom Arbeitskreis Medizinischer Ethik-Kommissionen gemäß Beschluss vom *
 Mustertext für die Information und Einwilligung von Heranwachsenden im Alter von etwa 12 16 Jahren, die an einer klinischen Prüfung eines Arzneimittels teilnehmen empfohlen vom Arbeitskreis Medizinischer
Mustertext für die Information und Einwilligung von Heranwachsenden im Alter von etwa 12 16 Jahren, die an einer klinischen Prüfung eines Arzneimittels teilnehmen empfohlen vom Arbeitskreis Medizinischer
Allgemeiner Anamnesebogen
 Allgemeiner Anamnesebogen Sehr geehrte Patientin, sehr geehrter Patient, Krankheiten aller Art können Auswirkungen auf Ihre Behandlung haben. Bitte füllen Sie deshalb diesen Fragebogen sorgfältig aus.
Allgemeiner Anamnesebogen Sehr geehrte Patientin, sehr geehrter Patient, Krankheiten aller Art können Auswirkungen auf Ihre Behandlung haben. Bitte füllen Sie deshalb diesen Fragebogen sorgfältig aus.
Patienteninformation
 Patienteninformation Erfassung der Komplikationsrate bei rheumaorthopädischen Eingriffen in Abhängigkeit von der eingenommenen Basistherapie. Rheumatische Erkrankungen werden medikamentös mittels sogenannter
Patienteninformation Erfassung der Komplikationsrate bei rheumaorthopädischen Eingriffen in Abhängigkeit von der eingenommenen Basistherapie. Rheumatische Erkrankungen werden medikamentös mittels sogenannter
MUSTER BEM-EINLADUNG
 MUSTER BEM-EINLADUNG Sehr geehrte(r) Frau/Herr, seit dem sind Sie arbeitsunfähig erkrankt. Alternativ: Innerhalb der letzten 12 Monate sind Sie insgesamt länger als 6 Wochen arbeitsunfähig erkrankt. Aufgrund
MUSTER BEM-EINLADUNG Sehr geehrte(r) Frau/Herr, seit dem sind Sie arbeitsunfähig erkrankt. Alternativ: Innerhalb der letzten 12 Monate sind Sie insgesamt länger als 6 Wochen arbeitsunfähig erkrankt. Aufgrund
Schlichtungsantrag. Vollmacht (Bei Vertretung ausfüllen)
 Absender (nur angeben, wenn abweichend von Patientendaten) Telefon An die Schlichtungsstelle für Arzthaftpflichtfragen der norddeutschen Ärztekammern Hans-Böckler-Allee 3 D-30173 Hannover Schlichtungsantrag
Absender (nur angeben, wenn abweichend von Patientendaten) Telefon An die Schlichtungsstelle für Arzthaftpflichtfragen der norddeutschen Ärztekammern Hans-Böckler-Allee 3 D-30173 Hannover Schlichtungsantrag
Einverständnisserklärung
 Einverständnisserklärung Name: Vorname: Geb.:Datum: Wohnort: Strasse: Tel: Handynummer: Email: Hausarzt: Adresse: Krankenkasse: Größe Gewicht: Mein Termin ist am: Sind Sie von der Rezeptgebühr befrei?
Einverständnisserklärung Name: Vorname: Geb.:Datum: Wohnort: Strasse: Tel: Handynummer: Email: Hausarzt: Adresse: Krankenkasse: Größe Gewicht: Mein Termin ist am: Sind Sie von der Rezeptgebühr befrei?
Sehr geehrte Patientin! Sehr geehrter Patient!
 Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
Univ. Klinik f. Innere Medizin LKH Graz Klinische Abteilung für Rheumatologie und Immunologie Univ. Prof. Dr. W. Graninger Auenbruggerplatz 15, A-8036 Graz Tel 0 316-385-12645 PATIENTENAUFKLÄRUNG ZUR THERAPIE
WIR MACHEN S MÖGLICH!
 Mehr Lebensfreude Schluss mit Zahnlosigkeit und Prothesen! FESTSITZENDER ZAHNERSATZ BEI KOMPLETTVERLUST DER EIGENEN ZÄHNE Zahn-Implantate auch für Angsthasen durch neue Behandlungsmethoden! WIR MACHEN
Mehr Lebensfreude Schluss mit Zahnlosigkeit und Prothesen! FESTSITZENDER ZAHNERSATZ BEI KOMPLETTVERLUST DER EIGENEN ZÄHNE Zahn-Implantate auch für Angsthasen durch neue Behandlungsmethoden! WIR MACHEN
Praxis für ganzheitliche Schmerztherapie im Franziskus-Carré. Terminabsprache / Terminabsage
 Praxis für ganzheitliche Schmerztherapie im Franziskus-Carré Dr. Barbara Wilm und Ralf Heidlindemann Hohenzollernring 70 48145 Münster Telefon: 0251/9352460 Fax: 0251/9352469 E-Mail: info@schmerztherapie-carre.de
Praxis für ganzheitliche Schmerztherapie im Franziskus-Carré Dr. Barbara Wilm und Ralf Heidlindemann Hohenzollernring 70 48145 Münster Telefon: 0251/9352460 Fax: 0251/9352469 E-Mail: info@schmerztherapie-carre.de
Implantation eines ICD- oder CRT-Systems
 Implantation eines ICD- oder CRT-Systems Patient: Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist die Implantation eines ICD- (implantierbarer Kadioverter- Defibrillator) oder CRT-(cardiale
Implantation eines ICD- oder CRT-Systems Patient: Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist die Implantation eines ICD- (implantierbarer Kadioverter- Defibrillator) oder CRT-(cardiale
Einverständniserklärung zur Protex Spacer Gel Studie
 Universitätsklinikum Heidelberg Universitätsklinikum Heidelberg INF 400 I 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Einverständniserklärung zur
Universitätsklinikum Heidelberg Universitätsklinikum Heidelberg INF 400 I 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Einverständniserklärung zur
Mit Ihnen einen Schritt weiter in der Forschung
 Mit Ihnen einen Schritt weiter in der Forschung Informationen zur Verwendung von Patientendaten und -proben Sehr geehrte Patientin, sehr geehrter Patient Die Erkennung und Behandlung von Krankheiten hat
Mit Ihnen einen Schritt weiter in der Forschung Informationen zur Verwendung von Patientendaten und -proben Sehr geehrte Patientin, sehr geehrter Patient Die Erkennung und Behandlung von Krankheiten hat
Ein Haus für alle Kinder
 Interne Veröffentlichungen Die internen Veröffentlichungen mit Fotos Ihrer Kinder, die während der Betreuungszeit in der Kindertageseinrichtung von den Fachkräften erstellt werden, ermöglichen Ihnen und
Interne Veröffentlichungen Die internen Veröffentlichungen mit Fotos Ihrer Kinder, die während der Betreuungszeit in der Kindertageseinrichtung von den Fachkräften erstellt werden, ermöglichen Ihnen und
Patienteninformation
 Ionentherapie bei nicht-kleinzelligen Pancoast-Tumoren im trimodalen Behandlungskonzept: Die INKA-Studie Patienteninformation Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist eine bösartige
Ionentherapie bei nicht-kleinzelligen Pancoast-Tumoren im trimodalen Behandlungskonzept: Die INKA-Studie Patienteninformation Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist eine bösartige
Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1
 Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1 Das Programm für Ihre Gesundheit 2 AOK-Curaplan Diabetes mellitus Typ 1 Was AOK-Curaplan ist An den strukturierten Behandlungsprogrammen für chronisch
Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1 Das Programm für Ihre Gesundheit 2 AOK-Curaplan Diabetes mellitus Typ 1 Was AOK-Curaplan ist An den strukturierten Behandlungsprogrammen für chronisch
Patienteninformation zur. MDS-Biobank des Universitätsklinikums Düsseldorf
 Patienteninformation zur MDS-Biobank des Universitätsklinikums Düsseldorf Sehr geehrte Patientin, sehr geehrter Patient, Sie werden gegenwärtig als Patient an der Klinik für Hämatologie, Onkologie und
Patienteninformation zur MDS-Biobank des Universitätsklinikums Düsseldorf Sehr geehrte Patientin, sehr geehrter Patient, Sie werden gegenwärtig als Patient an der Klinik für Hämatologie, Onkologie und
MUSTERTEXT. empfohlen vom Arbeitskreis Medizinischer Ethik-Kommissionen gemäß Beschluss vom *
 MUSTERTEXT für die Information und Einwilligung von Kindern im Alter von etwa 7-11 Jahren, die an einer klinischen Prüfung eines Arzneimittels teilnehmen empfohlen vom Arbeitskreis Medizinischer Ethik-Kommissionen
MUSTERTEXT für die Information und Einwilligung von Kindern im Alter von etwa 7-11 Jahren, die an einer klinischen Prüfung eines Arzneimittels teilnehmen empfohlen vom Arbeitskreis Medizinischer Ethik-Kommissionen
Patienteninformation und Einverständniserklärung zur Teilnahme an der klinischen Prüfung
 Patienteninformation und Einverständniserklärung zur Teilnahme an der klinischen Prüfung Effekte von Nifedipin auf die Eisenhomeostase bei Patienten mit Hämochromatose (ENIO) Sehr geehrter Patient! Wir
Patienteninformation und Einverständniserklärung zur Teilnahme an der klinischen Prüfung Effekte von Nifedipin auf die Eisenhomeostase bei Patienten mit Hämochromatose (ENIO) Sehr geehrter Patient! Wir
Entfernung von Weisheitszähnen
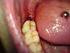 Liebe Patientin, lieber Patient, liebe Eltern, wir raten Ihnen zur operativen Entfernung des verlagerten Weisheitszahnes OK 18 rechts 28 links UK 48 rechts 38 links Befund- und Darstellungsschema Begründung
Liebe Patientin, lieber Patient, liebe Eltern, wir raten Ihnen zur operativen Entfernung des verlagerten Weisheitszahnes OK 18 rechts 28 links UK 48 rechts 38 links Befund- und Darstellungsschema Begründung
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept
 PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden an einer chronischen Polyarthritis (Rheumatoiden Arthritis). Ihr
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden an einer chronischen Polyarthritis (Rheumatoiden Arthritis). Ihr
Hinweise für den Hospizdienst zur Einhaltung der datenschutzrechtlichen Bestimmungen Überarbeitung April 2011
 ServicePoints Hospiz in Baden-Württemberg Arbeitsgruppe Ambulante Hospizdienste im Ministerium für Arbeit und Sozialordnung, Familien und Senioren Baden-Württemberg Hinweise für den Hospizdienst zur Einhaltung
ServicePoints Hospiz in Baden-Württemberg Arbeitsgruppe Ambulante Hospizdienste im Ministerium für Arbeit und Sozialordnung, Familien und Senioren Baden-Württemberg Hinweise für den Hospizdienst zur Einhaltung
Aufklärungs- und Einwilligungsbogen für die Operation einer Kieferzyste
 Name: Vorname: Geburtsdatum: Aufklärungs- und Einwilligungsbogen für die Operation einer Kieferzyste Liebe Patientin, lieber Patient, eine Kieferzyste ist ein Hohlraum im Kieferknochen, der mit Flüssigkeit
Name: Vorname: Geburtsdatum: Aufklärungs- und Einwilligungsbogen für die Operation einer Kieferzyste Liebe Patientin, lieber Patient, eine Kieferzyste ist ein Hohlraum im Kieferknochen, der mit Flüssigkeit
Selbstverständlich haben Sie das Recht auf Zugang zu Ihren Daten bzw. die Korrektur nicht korrekter Daten.
 Informationsblatt zur Datenverarbeitung mit der DaLiD (Datenbank für Leistungssport) für Kaderathleten/-innen und talentierte Nachwuchssportler/-innen (Hinweis: Im weiteren Verlauf wird zur verbesserten
Informationsblatt zur Datenverarbeitung mit der DaLiD (Datenbank für Leistungssport) für Kaderathleten/-innen und talentierte Nachwuchssportler/-innen (Hinweis: Im weiteren Verlauf wird zur verbesserten
Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1
 Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1 Das Programm für Ihre Gesundheit 2 AOK-Curaplan Diabetes mellitus Typ 1 Was ist AOK-Curaplan? An den strukturierten Behandlungsprogrammen für chronisch
Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1 Das Programm für Ihre Gesundheit 2 AOK-Curaplan Diabetes mellitus Typ 1 Was ist AOK-Curaplan? An den strukturierten Behandlungsprogrammen für chronisch
Molekulare Neuropathologie 2.0. zur Erhöhung der diagnostischen Genauigkeit bei Hirntumoren im Kindesalter
 Molekulare Neuropathologie 2.0 zur Erhöhung der diagnostischen Genauigkeit bei Hirntumoren im Kindesalter EINWILLIGUNGSERKLÄRUNG FÜR ERZIEHUNGSBERECHTIGTE Studienleiter: Prof. Dr. Stefan Pfister Deutsches
Molekulare Neuropathologie 2.0 zur Erhöhung der diagnostischen Genauigkeit bei Hirntumoren im Kindesalter EINWILLIGUNGSERKLÄRUNG FÜR ERZIEHUNGSBERECHTIGTE Studienleiter: Prof. Dr. Stefan Pfister Deutsches
Tragende Gründe zum Beschluss. des Gemeinsamen Bundesausschusses. über eine Änderung der. Richtlinie zur Bestimmung der Befunde
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Richtlinie zur Bestimmung der Befunde und der Regelversorgungsleistungen für die Festzuschüsse nach 55, 56 SGB V zu
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Richtlinie zur Bestimmung der Befunde und der Regelversorgungsleistungen für die Festzuschüsse nach 55, 56 SGB V zu
Haben Sie Fragen oder gibt es Unklarheiten beim Ausfüllen der Daten, dann helfen wir Ihnen sehr gerne weiter.
 Herzlich willkommen in unserer Praxis, bevor wir uns in Ruhe über die kieferorthopädischen Wünsche oder Sorgen von Ihrem Kind oder von Ihnen unterhalten, benötigen wir noch einige Auskünfte über den allgemeinen
Herzlich willkommen in unserer Praxis, bevor wir uns in Ruhe über die kieferorthopädischen Wünsche oder Sorgen von Ihrem Kind oder von Ihnen unterhalten, benötigen wir noch einige Auskünfte über den allgemeinen
Additive Aufbaumethoden
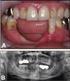 Name, Vorname Liebe Patientin, lieber Patient, in Ihrem individuellen Fall hat sich durch Resorption oder Atrophie die Knochensubstanz von Teilen des Kiefers oder des ganzen Kieferkammes abgebaut. Um dennoch
Name, Vorname Liebe Patientin, lieber Patient, in Ihrem individuellen Fall hat sich durch Resorption oder Atrophie die Knochensubstanz von Teilen des Kiefers oder des ganzen Kieferkammes abgebaut. Um dennoch
Leitfaden Triple-Therapie
 Leitfaden Triple-Therapie 2 Inhaltsverzeichnis Einführung... 4 1. Teilnehmerkreis Ärzte... 4 2. Teilnehmerkreis Patienten... 4 3. Einschreibung... 5 4. Arztwechsel... 6 5. Dokumentationsbogen... 6 Dokumentationsbogen
Leitfaden Triple-Therapie 2 Inhaltsverzeichnis Einführung... 4 1. Teilnehmerkreis Ärzte... 4 2. Teilnehmerkreis Patienten... 4 3. Einschreibung... 5 4. Arztwechsel... 6 5. Dokumentationsbogen... 6 Dokumentationsbogen
FRAGEBOGEN ZUM GESUNDHEITSZUSTAND
 17 FRAGEBOGEN ZUM GESUNDHEITSZUSTAND (Seite 1) Name: Geburtsdatum: Größe (cm): Gewicht (kg): Beruf: Familienstand: Wurden Sie in letzter Zeit ärztlich behandelt, O nein O ja wenn ja weswegen? Leiden Sie
17 FRAGEBOGEN ZUM GESUNDHEITSZUSTAND (Seite 1) Name: Geburtsdatum: Größe (cm): Gewicht (kg): Beruf: Familienstand: Wurden Sie in letzter Zeit ärztlich behandelt, O nein O ja wenn ja weswegen? Leiden Sie
Entscheidungen vor dem Hintergrund des Patientenrechtegesetzes
 Entscheidungen vor dem Hintergrund des Patientenrechtegesetzes Juristische Aspekte Johannes Schopohl 9. Landespsychotherapeutentag Berlin Berlin, 9. März 2013 Überblick 1. Juristischer Hintergrund von
Entscheidungen vor dem Hintergrund des Patientenrechtegesetzes Juristische Aspekte Johannes Schopohl 9. Landespsychotherapeutentag Berlin Berlin, 9. März 2013 Überblick 1. Juristischer Hintergrund von
Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf
 Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf Sehr geehrte Patientin, sehr geehrter Patient, im Folgenden möchten wir Sie um Ihr Einverständnis bitten,
Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf Sehr geehrte Patientin, sehr geehrter Patient, im Folgenden möchten wir Sie um Ihr Einverständnis bitten,
BerlindaVA.de mit dem Hauptstadtbonus
 Einwilligungserklärung zur Speicherung arzneimittelbezogener Daten für die Teilnahme am Versandhandel mit Arzneimitteln 1 Ich bin darüber informiert worden, dass die unten genannte Apotheke Leistungen
Einwilligungserklärung zur Speicherung arzneimittelbezogener Daten für die Teilnahme am Versandhandel mit Arzneimitteln 1 Ich bin darüber informiert worden, dass die unten genannte Apotheke Leistungen
Liebe Patientin, lieber Patient,
 Liebe Patientin, lieber Patient, vielen Dank, dass Sie zur Behandlung in unsere Praxis kommen. Diese wird nach einem Bestellsystem geführt. Das bedeutet für Sie in der Regel nur geringe Wartezeiten. Medizinisch
Liebe Patientin, lieber Patient, vielen Dank, dass Sie zur Behandlung in unsere Praxis kommen. Diese wird nach einem Bestellsystem geführt. Das bedeutet für Sie in der Regel nur geringe Wartezeiten. Medizinisch
Patienteninformation zur klinischen Studie: Protonentherapie der Prostataloge PROLOG-Studie
 UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
 Klinikeinrichtung FRIEDRICH -ALEXANDER UNIVERSITÄT ERLANGEN -NÜRNBERG PHILOSOPHISCHE FAKULTÄT UND FACHBEREICH THEOLOGIE Institut für Sportwissenschaft und Sport, AB Bewegung und Gesundheit Prof. Dr. phil.
Klinikeinrichtung FRIEDRICH -ALEXANDER UNIVERSITÄT ERLANGEN -NÜRNBERG PHILOSOPHISCHE FAKULTÄT UND FACHBEREICH THEOLOGIE Institut für Sportwissenschaft und Sport, AB Bewegung und Gesundheit Prof. Dr. phil.
