Chemie aquatischer Systeme. Herbstsemester 2013
|
|
|
- Ingelore Linden
- vor 6 Jahren
- Abrufe
Transkript
1 Chemie aquatischer Systeme Herbstsemester 2013
2 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen und physikalischen Prozessen Anwendung der chemischen Gleichgewichte
3 Ziele (2) Einsicht in Beeinträchtigung aquatischer Oekosysteme durch anthropogene Einflüsse Interpretation chemischer Daten
4 Chemie aquatischer Systeme Aquatische Chemie Chemie der gelösten und suspendierten Stoffe in aquatischen Systemen: - natürliche Systeme (See, Fluss, Grundwasser) - technische Systeme (Kläranlagen, Trinkwasser). Reaktionen und Phasenübergänge der gelösten Stoffe.
5 Einige aktuelle Probleme Globaler CO 2 -Kreislauf, CO 2 in Ozeanen Arsen im Trinkwasser (Bangladesh, Vietnam) Diffuse Einträge von Nährstoffen in Seen (z. B. Landwirtschaft) Verhalten von Nanopartikeln in aquatischer Umwelt
6 CO 2 -Kreislauf CO 2 -Gleichgewichte im Wasser Gas-Wasser-Austausch Biologische und chemische Kreisläufe
7 Ocean acidification
8 Arsen im Trinkwasser: Bangladesh Auch andere Regionen in Asien
9 Grundlagen für Beurteilung und Wasseraufbereitung Redoxprozesse As; Löslichkeit, Bindung an festen Phasen; Reaktionen von As an Oberflächen
10 Blaualgen verunreinigen den Greifensee Blaualgen sorgen dafür, dass sich der Greifensee verfärbt und ausladend schäumt. (August 2011) Bild Kantonales Labor Zürich
11 Nährstoffe in Seen N-, P-Einträge in Seen Redoxprozesse Stöchiometrie der Nährstoffaufnahme
12 Nanopartikel in Konsumprodukten
13 Nanopartikel in aquatischer Umwelt Löslichkeit der Partikel Oberflächenreaktionen Koagulation, Flockung
14 Problematische anorganische Stoffe in Gewässern Nährstoffe (P, N, C) Starke Säuren Schwermetalle (Cd, Hg, Cu usw.)
15 Globale Wasserprobleme Thematic Scope 2012 Water and Food security Cooperation towards Quality Standards for Aquatic Ecosystems
16 Globaler Wasserverbrauch
17 Aquatische Systeme Seen Fliessgewässer
18 Grundwasser Aquatische Systeme
19 Regenwasser Aquatische Systeme
20 Chemische Prozesse Von molekularen Prozessen zu Systemverhalten...
21 Wassermolekül
22 Wasser: Wasserstoffbrücken
23 Wasser : H3O+
24 Auflösung von NaCl
25 Aquoionen Ionen umgeben von Wassermolekülen, 6 oder 4
26 Anion im Wasser: F-
27 Chemische Reaktionen in aquatischen Systemen Säure-Base-Reaktionen HCO H + H 2 CO 3 Fällungs- / Auflösungsreaktionen CaCO 3(s) + H 2 CO 3 Ca HCO 3 - Austausch Gas-Wasser CO 2(g) CO 2(aq) HCO H +
28 Chemische Reaktionen in aquatischen Systemen Komplexbildung von Metallionen mit Liganden Zn 2+ + EDTA 4- ZnEDTA 2- Redoxprozesse SO e- + 9H + HS H 2 O Wechselwirkungen an Grenzflächen FeOH + Pb 2+ FeOPb + + H +
29 Spezierung in Lösung Redoxzustand, ionische Form : Ca 2+ (aq) H 2 PO 4 - Säure-Base : H 2 PO 4- /HPO 4 2- Komplexbildung
30 Wechselwirkungen der Gewässer mit Atmosphäre, Gesteinen, Biota, Anthroposphäre
31 Typische Konzentrationen in See oder Fluss
32 Wasser feste Phasen Gas Gas gelöst gelöst Organismen N, P gelöst feste Phase
33 Verwitterungsreaktionen Mineral + H 2 O +H 2 CO 3 Kationen + Anionen CaCO 3 (s) + H 2 CO 3 Ca HCO 3 - CaSO 4 (s) + H 2 O Ca 2+ + SO 4 2- Mineral + H 2 O +H 2 CO 3 Kationen + Anionen + Kieselsäure+ Tonmineral NaAlSi 3 O 8 (s) H 2 O + H 2 CO 3 Na + + HCO H 4 SiO Al 2 Si 2 O 5 (OH) 4 (s)
34 Hauptkationen in Gewässern Kationen Regen H + + NH ph "Mittlerer" Fluss Na + K + ph ZH-See Ca 2+ Mg 2+ ph mäq/l
35 Ionenbilanzen Kationen = Anionen Äquivalente / Liter entspricht Mole Ladungen / Liter
36 Hauptanionen in Gewässern Anionen Regen Fluss Cl - ZH-See HCO 3 - SO 4 2- NO mäq/l
37 Zusammensetzung Meerwasser Ca 2+ Kationen Meer Mg 2+ Na + K + ph äq/l HCO 3 - Anionen Meer SO 4 2- Cl äq/l
38 Photosynthese und Respiration
39 Stöchiometrische Verhältnisse der Nährstoffe CO NO HP O 4 + (x H 4 S i O 4 ) H 2 O + 18 H + (+ 16 NH + 4 ) P R {C 106 H 263 O 110 N 16 P 1 ( S i x ) } O 2 (+14 H + )
40 Genfersee, August 0 O2 µmol/l, Px
41 Genfersee: P vs. O2
42 Löslichkeit von Gasen O 2 (g) Luft O 2 (aq) Wasser Gleichgewicht : Henry-Konstante K H = [ O2 ( aq)] p O 2 Charakteristisch für jedes Gas, temperaturabhängig
43 Löslichkeit von Gasen Beispiel Atmosphäre, 25 C: [O 2 ] = K H p O2 = 2.62 x 10-4 mol/l [N 2 ] = K H p N2 = 4.91 x 10-4 mol/l
1.3 Chemische Reaktionen des Wassers - Bildung von Säuren und Basen
 1.3 Chemische Reaktionen des Wassers Bildung von Säuren und Basen Säure und Basebegriff nach Arrhenius (1887) Wasser reagiert mit Nichtmetalloxiden (Säureanhydriden) zu Säuren. Die gebildete Säure löst
1.3 Chemische Reaktionen des Wassers Bildung von Säuren und Basen Säure und Basebegriff nach Arrhenius (1887) Wasser reagiert mit Nichtmetalloxiden (Säureanhydriden) zu Säuren. Die gebildete Säure löst
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Das Chemische Gleichgewicht
 II. Gleichgewichte von Säuren S und Basen 13 Puffer-Lösungen Definition: Lösungen, die einen definierten ph-wert haben, der konstant bleibt, auch wenn Säuren S oder Basen in begrenzten Mengen zugesetzt
II. Gleichgewichte von Säuren S und Basen 13 Puffer-Lösungen Definition: Lösungen, die einen definierten ph-wert haben, der konstant bleibt, auch wenn Säuren S oder Basen in begrenzten Mengen zugesetzt
7. Woche. Gesamtanalyse (Vollanalyse) einfacher Salze. Qualitative Analyse anorganischer Verbindungen
 7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
Grundwasser: chemische Vorgänge bei der Infiltration. Redoxprozesse im Grundwasser Transport reaktiver Spezies
 Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Das chemische Gleichgewicht
 1 Grundlagen Viele Substanzen sind in Wasser praktisch nicht löslich, l d.h. sie sind nur sehr geringfügig gig löslich. (Tatsächlich nicht lösliche Stoffe gibt es nicht! Schwerlösliche Verbindungen In
1 Grundlagen Viele Substanzen sind in Wasser praktisch nicht löslich, l d.h. sie sind nur sehr geringfügig gig löslich. (Tatsächlich nicht lösliche Stoffe gibt es nicht! Schwerlösliche Verbindungen In
Allgemeine Grundlagen 2
 Allgemeine Grundlagen 2 1 Reaktionen und Bindung 1) Redox - Reaktionen 1. Semester 2) Säure - Base - Reaktionen 1. Semester 3) Komplexreaktionen (eigentlich kein neuer Reaktionstyp, sondern eine Säure
Allgemeine Grundlagen 2 1 Reaktionen und Bindung 1) Redox - Reaktionen 1. Semester 2) Säure - Base - Reaktionen 1. Semester 3) Komplexreaktionen (eigentlich kein neuer Reaktionstyp, sondern eine Säure
Themen heute: Säuren und Basen, Redoxreaktionen
 Wiederholung der letzten Vorlesungsstunde: Massenwirkungsgesetz, Prinzip des kleinsten Zwangs, Löslichkeitsprodukt, Themen heute: Säuren und Basen, Redoxreaktionen Vorlesung Allgemeine Chemie, Prof. Dr.
Wiederholung der letzten Vorlesungsstunde: Massenwirkungsgesetz, Prinzip des kleinsten Zwangs, Löslichkeitsprodukt, Themen heute: Säuren und Basen, Redoxreaktionen Vorlesung Allgemeine Chemie, Prof. Dr.
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7
 AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
3.2. Aufgaben zu Säure-Base-Gleichgewichten
 .. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
.. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
Kapiteltest 1.1. Kapiteltest 1.2
 Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Kapiteltest 1.1 a) Perchlorsäure hat die Formel HClO 4. Was geschieht bei der Reaktion von Perchlorsäure mit Wasser? Geben Sie zuerst die Antwort in einem Satz. Dann notieren Sie die Reaktionsgleichung.
Praktikumsprotokoll. Grundlagen der Chemie Teil II SS Praktikum vom
 Grundlagen der Chemie Teil II SS 2002 Praktikumsprotokoll Praktikum vom 02.05.2002 Versuch 11: Herstellung einer Pufferlösung von definiertem ph Versuch 12: Sauer und alkalisch reagierende Salzlösungen
Grundlagen der Chemie Teil II SS 2002 Praktikumsprotokoll Praktikum vom 02.05.2002 Versuch 11: Herstellung einer Pufferlösung von definiertem ph Versuch 12: Sauer und alkalisch reagierende Salzlösungen
Letzte Woche. Auswirkung chemischer Bestandteile der Atmosphäre auf das Klima Energiehaushalt Treibhausgase Das atmosphärische IR-Fenster GWPs
 Letzte Woche. Auswirkung chemischer Bestandteile der Atmosphäre auf das Klima Energiehaushalt Treibhausgase Das atmosphärische IR-Fenster GWPs Der anthropogene Treibhauseffekt Feedbacks 0 Fließender Übergang
Letzte Woche. Auswirkung chemischer Bestandteile der Atmosphäre auf das Klima Energiehaushalt Treibhausgase Das atmosphärische IR-Fenster GWPs Der anthropogene Treibhauseffekt Feedbacks 0 Fließender Übergang
Wiederholungen. Puffergleichung (Henderson-Hasselbalch) Ionenprodukt des Wassers. ph-wert-berechnungen. Titrationskurvenberechnung
 Vorlesung 22: Wiederholungen Puffergleichung (Henderson-Hasselbalch) Ionenprodukt des Wassers ph-wert-berechnungen Titrationskurvenberechnung Säuren und Basen Hydroxonium + Chlorid Ammonium + Hydroxid
Vorlesung 22: Wiederholungen Puffergleichung (Henderson-Hasselbalch) Ionenprodukt des Wassers ph-wert-berechnungen Titrationskurvenberechnung Säuren und Basen Hydroxonium + Chlorid Ammonium + Hydroxid
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie
 Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Analytische Chemie. B. Sc. Chemieingenieurwesen. 02. Februar Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 02. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 02. Februar 2011 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Boden Versauerung Dynamik-Gefährdung
 Rochuspark I Erdbergstraße 10/33 I 1020 Wien T (+43 1) 236 10 30 33 I M (+43 0) 676 364 10 30 E office@bodenoekologie.com I www.bodenoekologie.com Boden Versauerung Dynamik-Gefährdung Univ. Lek. DI Hans
Rochuspark I Erdbergstraße 10/33 I 1020 Wien T (+43 1) 236 10 30 33 I M (+43 0) 676 364 10 30 E office@bodenoekologie.com I www.bodenoekologie.com Boden Versauerung Dynamik-Gefährdung Univ. Lek. DI Hans
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Teilnahmebescheinigungen Mail an christoph.woelper@uni-due.de
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Teilnahmebescheinigungen Mail an christoph.woelper@uni-due.de
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kinetik Reaktionsgeschwindigkeit Konzentrationsabhängigkeit
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kinetik Reaktionsgeschwindigkeit Konzentrationsabhängigkeit
Crashkurs Säure-Base
 Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Dissoziation, ph-wert und Puffer
 Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Analytische Chemie. B. Sc. Chemieingenieurwesen. 14. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
0.3 Formeln, Gleichungen, Reaktionen
 0.3 Formeln, Gleichungen, Reaktionen Aussage von chemischen Formeln Formeln von ionischen Verbindungen - Metallkation, ein- oder mehratomiges Anion - Formel entsteht durch Ausgleich der Ladungen - Bildung
0.3 Formeln, Gleichungen, Reaktionen Aussage von chemischen Formeln Formeln von ionischen Verbindungen - Metallkation, ein- oder mehratomiges Anion - Formel entsteht durch Ausgleich der Ladungen - Bildung
Lösung Sauerstoff: 1s 2 2s 2 2p 4, Bor: 1s 2 2s 2 2p 1, Chlor: 1s 2 2s 2 2p 6 3s 2 3p 5 Neon: 1s 2 2s 2 2p 6
 1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
2. Woche. Anorganische Analysenmethodik
 2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
Praktische Bedeutung der Ca/Mg-Bestimmung: Wasserhärte wird erzeugt durch den Gehalt an Ca- und Mg-Hydrogencarbonat und -Sulfat im Grundwasser;
 Praktische Bedeutung der Ca/Mg-Bestimmung: Wasserhärte wird erzeugt durch den Gehalt an Ca- und Mg-Hydrogencarbonat und -Sulfat im Grundwasser; (Wasserhärte) Herkunft: Sulfate durch Auflösen entsprechender
Praktische Bedeutung der Ca/Mg-Bestimmung: Wasserhärte wird erzeugt durch den Gehalt an Ca- und Mg-Hydrogencarbonat und -Sulfat im Grundwasser; (Wasserhärte) Herkunft: Sulfate durch Auflösen entsprechender
Bauchemische Grundlagen Reaktionen Säure Base
 Bauchemische Grundlagen Reaktionen Säure Base Thomas A. BIER Institut für Keramik, Glas- und Baustofftechnik, Leipziger Straße 28, 09596 Freiberg, Bauchemische Grundlagen WS 2011/12 Allgemeine Grundlagen
Bauchemische Grundlagen Reaktionen Säure Base Thomas A. BIER Institut für Keramik, Glas- und Baustofftechnik, Leipziger Straße 28, 09596 Freiberg, Bauchemische Grundlagen WS 2011/12 Allgemeine Grundlagen
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2016 Organisation Informationen: www.wuttkegroup.de
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2016 Organisation Informationen: www.wuttkegroup.de
Laborbericht. Wasserhärte Leitfähigkeit. Anna Senn Bianca Theus
 Laborbericht Wasserhärte Leitfähigkeit Anna Senn Bianca Theus 14.09. 2004 03.11. 2004 Inhaltsverzeichnis 1. Ziel... 1 2. Theorie... 1 2.1 Leitfähigkeit... 1 2.2 Wasserhärte... 2 2.3 Entstehung von Wasserhärte...
Laborbericht Wasserhärte Leitfähigkeit Anna Senn Bianca Theus 14.09. 2004 03.11. 2004 Inhaltsverzeichnis 1. Ziel... 1 2. Theorie... 1 2.1 Leitfähigkeit... 1 2.2 Wasserhärte... 2 2.3 Entstehung von Wasserhärte...
bestimmte mehratomige Anionen mit Sauerstoff werden mit dem lateinischen Namen benannt und enden auf at.
 DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Chemische Gleichgewichte, Säuren und
 Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
Wiederholung der letzten Vorlesungsstunde: Das chemische Gleichgewicht, Massenwirkungsgesetz, Löslichkeit von Salzen in Flüssigkeiten, Löslichkeitsprodukt, Thema heute: Chemische Gleichgewichte, Säuren
ELEKTROCHEMIE. Elektrischer Strom: Fluß von elektrischer Ladung. elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie.
 ELEKTROCHEMIE Elektrischer Strom: Fluß von elektrischer Ladung Elektrische Leitung: metallische (Elektronen) elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie Galvanische Zellen Elektrolyse Die
ELEKTROCHEMIE Elektrischer Strom: Fluß von elektrischer Ladung Elektrische Leitung: metallische (Elektronen) elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie Galvanische Zellen Elektrolyse Die
Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I
 Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Analytische Chemie. B. Sc. Chemieingenieurwesen. 03. Februar 2010. Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 03. Februar 2010 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 03. Februar 2010 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Universität des Saarlandes - Fachrichtung Anorganische Chemie C h e m i s c h e s E i n f ü h r u n g s p r a k t i k u m.
 Universität des Saarlandes - Fachrichtung Anorganische Chemie C h e m i s c h e s E i n f ü h r u n g s p r a k t i k u m Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb
Universität des Saarlandes - Fachrichtung Anorganische Chemie C h e m i s c h e s E i n f ü h r u n g s p r a k t i k u m Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb
Aufgabe 1: Geben Sie die korrespondierenden Basen zu folgenden Verbindungen an: a) H 3 PO 4 b) H 2 PO 4
 Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Übungsaufgaben zum Thema Säuren, Basen und Puffer Säure/Base Definition nach Brǿnsted: Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren). Basen sind Stoffe, die Protonen aufnehmen können
Säure/Base - Reaktionen. 6) Titration starker und schwacher Säuren/Basen
 Säure/Base - Reaktionen 1) Elektrolytische Dissoziation 2) Definitionen Säuren Basen 3) Autoprotolyse 4) ph- und poh-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Säure/Base - Reaktionen 1) Elektrolytische Dissoziation 2) Definitionen Säuren Basen 3) Autoprotolyse 4) ph- und poh-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Wasserchemie Modul 4
 Wasserchemie Modul 4 Ionenchromatographie / HPLC Plausibilitätstests tstests Ionensensitive Elektroden Chromatographie Trennung von Stoffgemischen Zwei nicht mischbare Phasen - stationäre Phase (Ionentauscher)
Wasserchemie Modul 4 Ionenchromatographie / HPLC Plausibilitätstests tstests Ionensensitive Elektroden Chromatographie Trennung von Stoffgemischen Zwei nicht mischbare Phasen - stationäre Phase (Ionentauscher)
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte)
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte) Lösungen, Konzentration Viele chemische Reaktionen werden
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte) Lösungen, Konzentration Viele chemische Reaktionen werden
CHEMIE KAPITEL 4 SÄURE- BASE. Timm Wilke. Georg- August- Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE- BASE Timm Wilke Georg- August- Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Historisches Im 17. Jahrhundert wurden von Robert Boyle Gemeinsamkeiten verschiedener Verbindungen
CHEMIE KAPITEL 4 SÄURE- BASE Timm Wilke Georg- August- Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Historisches Im 17. Jahrhundert wurden von Robert Boyle Gemeinsamkeiten verschiedener Verbindungen
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 6 Entropie und Gibbs Enthalpie Gibbs-elmholtz-Gleichung Absolute Entropien Gibbs Standardbildungsenthalpien Kinetik
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 6 Entropie und Gibbs Enthalpie Gibbs-elmholtz-Gleichung Absolute Entropien Gibbs Standardbildungsenthalpien Kinetik
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
7. Tag: Säuren und Basen
 7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
Lösung 7. Allgemeine Chemie I Herbstsemester Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf.
 Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Grundwissenkarten Hans-Carossa-Gymnasium. 9. Klasse. Chemie SG
 Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundlagen Chemie. Dipl.-Lab. Chem. Stephan Klotz. Freiwill ige Feuerwehr Rosenheim
 Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Wasserchemie und Wasseranalytik SS 2015
 Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Analytische Chemie. B. Sc. Chemieingenieurwesen. 9. September 2015, Uhr. Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 9. September 2015, 13.30 16.30 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Analytische Chemie B. Sc. Chemieingenieurwesen 9. September 2015, 13.30 16.30 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Säuren, Basen, Salze
 Säuren, Basen, Salze Namensgebung (=Nomenklatur) Es gibt für chemische Verbindungen grundsätzlich zwei Arten von Namen: Trivialname der alltäglich bzw. umgangssprachlich benutzte Name z. B.: Wasser, Salzsäure,
Säuren, Basen, Salze Namensgebung (=Nomenklatur) Es gibt für chemische Verbindungen grundsätzlich zwei Arten von Namen: Trivialname der alltäglich bzw. umgangssprachlich benutzte Name z. B.: Wasser, Salzsäure,
Eine Arbeitsgemeinschaft der Verlage
 UTB 8463 Eine Arbeitsgemeinschaft der Verlage Böhlau Verlag Wien Köln Weimar Verlag Barbara Budrich Opladen Farmington Hills facultas.wuv Wien Wilhelm Fink München A. Francke Verlag Tübingen und Basel
UTB 8463 Eine Arbeitsgemeinschaft der Verlage Böhlau Verlag Wien Köln Weimar Verlag Barbara Budrich Opladen Farmington Hills facultas.wuv Wien Wilhelm Fink München A. Francke Verlag Tübingen und Basel
Säuren und Basen. Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O H 3 O + + OH -
 Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O + (aq)-ionen anzugeben. Aus der Gleichung: H 2 O + H 2 O H 3 O + + OH - c(h 3 O + ) c(oh - ) K
Der ph-wert Zur Feststellung, ob eine Lösung sauer oder basisch ist genügt es, die Konzentration der H 3 O + (aq)-ionen anzugeben. Aus der Gleichung: H 2 O + H 2 O H 3 O + + OH - c(h 3 O + ) c(oh - ) K
Elemente des Periodensystems. Natürliche Häufigkeit der Elemente
 Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel und auf
Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel und auf
2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom 02.02.2011 A1 A2 A3 F1 F2 R1 R2 E1 Σ Note 8 7 10 4 5 3 6 7 NAME/VORNAME:... LÖSUNGEN Matrikelnummer:... Schreiben Sie bitte gut leserlich:
2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom 02.02.2011 A1 A2 A3 F1 F2 R1 R2 E1 Σ Note 8 7 10 4 5 3 6 7 NAME/VORNAME:... LÖSUNGEN Matrikelnummer:... Schreiben Sie bitte gut leserlich:
SS 2010. Thomas Schrader. der Universität Duisburg-Essen. (Teil 7: Säuren und Basen, Elektrolyte)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 7: Säuren und Basen, Elektrolyte) Definition Säure/Base Konjugierte Säure/Base-Paare Konjugierte
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 7: Säuren und Basen, Elektrolyte) Definition Säure/Base Konjugierte Säure/Base-Paare Konjugierte
Komplexometrie. = Elektronenpaar- Akzeptor = Elektronenpaar- Donator. Koordinationsverbindung. stöchiometrischer Komplex. praktisch undissoziiert
 Komplexometrie mehrwertige Kationen organ. Chelatbildner = Zentralion + = mehrzähniger Ligand = Elektronenpaar- Akzeptor = Elektronenpaar- Donator z.b.: Ca, Mg, Fe 3+, Zn, Hg, Bi, Cd... z.b.: EDTA Nitrilotriessigsäure
Komplexometrie mehrwertige Kationen organ. Chelatbildner = Zentralion + = mehrzähniger Ligand = Elektronenpaar- Akzeptor = Elektronenpaar- Donator z.b.: Ca, Mg, Fe 3+, Zn, Hg, Bi, Cd... z.b.: EDTA Nitrilotriessigsäure
ABFALLWIRTSCHAFT UND ABFALLENTSORGUNG
 ABFALLWIRTSCHAFT UND ABFALLENTSORGUNG Peter Lechner & Marion Huber-Humer MVA-Schlacke LVA-Nr. 813.100 & 101 Studienjahr 2011/2012 Studienjahr 2011/12 LVA 813.100 & 101 2 Stoffströme einer MVA Restabfall
ABFALLWIRTSCHAFT UND ABFALLENTSORGUNG Peter Lechner & Marion Huber-Humer MVA-Schlacke LVA-Nr. 813.100 & 101 Studienjahr 2011/2012 Studienjahr 2011/12 LVA 813.100 & 101 2 Stoffströme einer MVA Restabfall
(Atommassen: Ca = 40, O = 16, H = 1;
 1.) Welche Molarität hat eine 14,8%ige Ca(OH) 2 - Lösung? (Atommassen: Ca = 40, O = 16, H = 1; M: mol/l)! 1! 2! 2,5! 3! 4 M 2.) Wieviel (Gewichts)%ig ist eine 2-molare Salpetersäure der Dichte 1,100 g/cm
1.) Welche Molarität hat eine 14,8%ige Ca(OH) 2 - Lösung? (Atommassen: Ca = 40, O = 16, H = 1; M: mol/l)! 1! 2! 2,5! 3! 4 M 2.) Wieviel (Gewichts)%ig ist eine 2-molare Salpetersäure der Dichte 1,100 g/cm
Einführung. Galvanische Zelle. Korrosion + - Univ.-Prof. Dr. Max J. Setzer Vorlesung - Korrosion Seite 1
 Univ.-Prof. Dr. Max J. Setzer Vorlesung - Korrosion Seite 1 Einführung MWG 8 / Die Korrosion ist ein Redox-Prozess Bei der Änderung der Oxidationsstufe entstehen Ionen geladene Teilchen. Der Oxidationsprozess
Univ.-Prof. Dr. Max J. Setzer Vorlesung - Korrosion Seite 1 Einführung MWG 8 / Die Korrosion ist ein Redox-Prozess Bei der Änderung der Oxidationsstufe entstehen Ionen geladene Teilchen. Der Oxidationsprozess
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Grundwissen Chemie Mittelstufe (9 MNG)
 Grundwissen Chemie Mittelstufe (9 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Grundwissen Chemie Mittelstufe (9 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1
![ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1](/thumbs/33/16365353.jpg) ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
+ O. Die Valenzelektronen der Natriumatome werden an das Sauerstoffatom abgegeben.
 A Oxidation und Reduktion UrsprÄngliche Bedeutung der Begriffe UrsprÅnglich wurden Reaktionen, bei denen sich Stoffe mit Sauerstoff verbinden, als Oxidationen bezeichnet. Entsprechend waren Reaktionen,
A Oxidation und Reduktion UrsprÄngliche Bedeutung der Begriffe UrsprÅnglich wurden Reaktionen, bei denen sich Stoffe mit Sauerstoff verbinden, als Oxidationen bezeichnet. Entsprechend waren Reaktionen,
1. Der Lösungsvorgang
 9. Löslichkeitsprodukt 9.1 1. Der Lösungsvorgang Bei Lösungen handelt es sich um homogene Systeme, sie bestehen aus einer Phase. Damit sich ein Stoff löst, muss Arbeit gegen die Gitterkräfte des Salzes
9. Löslichkeitsprodukt 9.1 1. Der Lösungsvorgang Bei Lösungen handelt es sich um homogene Systeme, sie bestehen aus einer Phase. Damit sich ein Stoff löst, muss Arbeit gegen die Gitterkräfte des Salzes
Kleine Formelsammlung Chemie
 Karl Schwister Kleine Forelsalung Cheie ISBN-1: 3-446-41545-9 ISBN-13: 978-3-446-41545-4 Leseprobe Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-41545-4 sowie i Buchhandel.
Karl Schwister Kleine Forelsalung Cheie ISBN-1: 3-446-41545-9 ISBN-13: 978-3-446-41545-4 Leseprobe Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-41545-4 sowie i Buchhandel.
PRÜFBERICHT 925043-675912
 Tel.: +49 (843) 79, Fax: +49 (843) 724 [@ANALYNR_START=67592] [@BARCODE= R] Dr.Blasy-Dr.Busse Moosstr. 6A, 82279 Eching ZV ZUR WASSERVERSORGUNG ACHENGRUPPE Herr Jürs RATHAUSPLATZ 8 8347 KIRCHANSCHÖRING
Tel.: +49 (843) 79, Fax: +49 (843) 724 [@ANALYNR_START=67592] [@BARCODE= R] Dr.Blasy-Dr.Busse Moosstr. 6A, 82279 Eching ZV ZUR WASSERVERSORGUNG ACHENGRUPPE Herr Jürs RATHAUSPLATZ 8 8347 KIRCHANSCHÖRING
Professur Radiochemie Sommersemester 2009
 Professur Radiochemie Sommersemester 2009 Vorlesung: Umweltchemie Gliederung: 0 Einleitung 0.1 Vorbemerkungen 0.2 Definition Umweltchemie 1 Entstehung der Umwelt 1.1 Bildung der Elemente 1.2 Aufbau der
Professur Radiochemie Sommersemester 2009 Vorlesung: Umweltchemie Gliederung: 0 Einleitung 0.1 Vorbemerkungen 0.2 Definition Umweltchemie 1 Entstehung der Umwelt 1.1 Bildung der Elemente 1.2 Aufbau der
Biologische und chemische Vorgänge in stehenden Gewässern. Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer
 Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer Der ph-wert Das Karbonathärte-Puffersystem Algen verstehen und bekämpfen Phosphatfrachten Der Teich Symbiose aller Lebewesen In einem
Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer Der ph-wert Das Karbonathärte-Puffersystem Algen verstehen und bekämpfen Phosphatfrachten Der Teich Symbiose aller Lebewesen In einem
Natürliche ökologische Energie- und Stoffkreisläufe
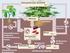 Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Chemische Bindung. Wie halten Atome zusammen? Welche Atome können sich verbinden? Febr 02
 Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Chemie für Studierende der Biologie I
 SäureBaseGleichgewichte Es gibt verschiedene Definitionen für SäureBaseReaktionen, an dieser Stelle ist die Definition nach BrønstedLowry, die Übertragung eines H + Ions ( Proton ), gemeint. Nach BrønstedLowry
SäureBaseGleichgewichte Es gibt verschiedene Definitionen für SäureBaseReaktionen, an dieser Stelle ist die Definition nach BrønstedLowry, die Übertragung eines H + Ions ( Proton ), gemeint. Nach BrønstedLowry
a.) Wie groß ist die Reaktionsenthalpie für die Diamantbildung aus Graphit? b.) Welche Kohlenstoffform ist unter Standardbedingungen die stabilere?
 Chemie Prüfungsvorbereitung 1. Aufgabe Folgende Reaktionen sind mit ihrer Enthalpie vorgegeben C (Graphit) + O 2 CO 2 R = 393,43 KJ C (Diamant) + O 2 CO 2 R = 395,33 KJ CO 2 O 2 + C (Diamant) R = +395,33
Chemie Prüfungsvorbereitung 1. Aufgabe Folgende Reaktionen sind mit ihrer Enthalpie vorgegeben C (Graphit) + O 2 CO 2 R = 393,43 KJ C (Diamant) + O 2 CO 2 R = 395,33 KJ CO 2 O 2 + C (Diamant) R = +395,33
Hinweise für den Schüler. Von den 2 Prüfungsblöcken A und B ist einer auszuwählen.
 Abitur 2001 Chemie Gk Seite 1 Hinweise für den Schüler Aufgabenauswahl: Von den 2 Prüfungsblöcken A und B ist einer auszuwählen. Bearbeitungszeit: Die Arbeitszeit beträgt 210 Minuten, zusätzlich stehen
Abitur 2001 Chemie Gk Seite 1 Hinweise für den Schüler Aufgabenauswahl: Von den 2 Prüfungsblöcken A und B ist einer auszuwählen. Bearbeitungszeit: Die Arbeitszeit beträgt 210 Minuten, zusätzlich stehen
B Chemisch Wissenwertes. Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden.
 -I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
-I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
Chemikalien: Salzsäure (Schwefelsäure) Magnesiumspäne, Eisen-, Zink-, Kupfer-Späne, Silberstreifen
 I) Verhalten von Säuren gegenüber Metallen II) Der Saure Regen in Modellversuchen III) Neutralisation a) Neutralisation ( Salzsäure mit Natronlauge) b) Eindampfen der Salzlösung c) Elektrische Leitfähigkeitsmessung
I) Verhalten von Säuren gegenüber Metallen II) Der Saure Regen in Modellversuchen III) Neutralisation a) Neutralisation ( Salzsäure mit Natronlauge) b) Eindampfen der Salzlösung c) Elektrische Leitfähigkeitsmessung
Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser
 REPORT Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser DI Otmar Plank Verteiler: 1-3 Fa. YVE & BIO GmbH, Bremen 4 Otmar Plank 5 HET August 2014
REPORT Chemische und Mikrobiologische Untersuchung von mittels YVE-310-Filterkanne aufbereitetem Leitungswasser DI Otmar Plank Verteiler: 1-3 Fa. YVE & BIO GmbH, Bremen 4 Otmar Plank 5 HET August 2014
Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Hydrate
 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH Al(OH) 3 Al(OH) 3 + OH - [Al(OH) 4 ] - Hydrate Amphoteres Verhalten von Hydroxiden (z.b. Al 3+, Sn 2+, Pb 2+, Zn 2+ ): löslich
Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH Al(OH) 3 Al(OH) 3 + OH - [Al(OH) 4 ] - Hydrate Amphoteres Verhalten von Hydroxiden (z.b. Al 3+, Sn 2+, Pb 2+, Zn 2+ ): löslich
Benennen Sie folgende Salze: 1. Li[AlCl 2 Br 2 ] 2. [Co(NH 3 ) 2 (H 2 O) 2 ][FeCl 6 ] 3. Na 2 S 2 O 4
![Benennen Sie folgende Salze: 1. Li[AlCl 2 Br 2 ] 2. [Co(NH 3 ) 2 (H 2 O) 2 ][FeCl 6 ] 3. Na 2 S 2 O 4 Benennen Sie folgende Salze: 1. Li[AlCl 2 Br 2 ] 2. [Co(NH 3 ) 2 (H 2 O) 2 ][FeCl 6 ] 3. Na 2 S 2 O 4](/thumbs/39/18756663.jpg) ... Nomenklatur Frage 41... Nomenklatur Antwort 41 Benennen Sie folgende Salze: 1. Li[AlCl 2 Br 2 ] 2. [Co(NH 3 ) 2 (H 2 O) 2 ][FeCl 6 ] 3. Na 2 S 2 O 4 Kap. 4.9 Chalkogene Frage 42 Kap. 4.9 Chalkogene
... Nomenklatur Frage 41... Nomenklatur Antwort 41 Benennen Sie folgende Salze: 1. Li[AlCl 2 Br 2 ] 2. [Co(NH 3 ) 2 (H 2 O) 2 ][FeCl 6 ] 3. Na 2 S 2 O 4 Kap. 4.9 Chalkogene Frage 42 Kap. 4.9 Chalkogene
Fällungsreaktion. Flammenfärbung. Fällungsreaktion:
 2 Fällungsreaktion: 2 Fällungsreaktion Entsteht beim Zusammengießen zweier Salzlösungen ein Niederschlag eines schwer löslichen Salzes, so spricht man von einer Fällungsreaktion. Bsp: Na + (aq) + Cl -
2 Fällungsreaktion: 2 Fällungsreaktion Entsteht beim Zusammengießen zweier Salzlösungen ein Niederschlag eines schwer löslichen Salzes, so spricht man von einer Fällungsreaktion. Bsp: Na + (aq) + Cl -
ETW Aufbaukurs Chemie Vorlesung 1: Einführung. Jörg Petrasch
 ETW Aufbaukurs Chemie Vorlesung 1: Einführung Jörg Petrasch joerg.petrasch@fhv.at http://www.fhv.at/forschung/energie Literatur C.E. Mortimer, U. Müller, Chemie - Das Basiswissen der Chemie, 8. Auflage,
ETW Aufbaukurs Chemie Vorlesung 1: Einführung Jörg Petrasch joerg.petrasch@fhv.at http://www.fhv.at/forschung/energie Literatur C.E. Mortimer, U. Müller, Chemie - Das Basiswissen der Chemie, 8. Auflage,
Chemie. Schwerpunktfach. Bitte lesen Sie die folgenden Hinweise sorgfältig durch bevor Sie mit dem Lösen der Aufgaben beginnen.
 Maturitätsprüfung 2006 Klasse 4B + 4AB Gymnasium Muttenz Chemie Schwerpunktfach Name: Vorname: Klasse: Bitte lesen Sie die folgenden Hinweise sorgfältig durch bevor Sie mit dem Lösen der Aufgaben beginnen.
Maturitätsprüfung 2006 Klasse 4B + 4AB Gymnasium Muttenz Chemie Schwerpunktfach Name: Vorname: Klasse: Bitte lesen Sie die folgenden Hinweise sorgfältig durch bevor Sie mit dem Lösen der Aufgaben beginnen.
 www.zaubervorlesung.de Institut für Anorganische Chemie Institut für Anorganische Chemie Universität Erlangen-Nürnberg Donnerstag 19. Okt. 2006 Einlass: 18:00 Uhr Beginn: 20:00 Uhr Getränke dürfen nur
www.zaubervorlesung.de Institut für Anorganische Chemie Institut für Anorganische Chemie Universität Erlangen-Nürnberg Donnerstag 19. Okt. 2006 Einlass: 18:00 Uhr Beginn: 20:00 Uhr Getränke dürfen nur
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1 Stoffe und ihre Eigenschaften Stoffe: Gegenstände bzw. Körper bestehen aus Stoffen. Eine Stoffportion hat ein bestimmtes Volumen und eine bestimmte Masse. Fest, flüssig
Grundwissen Chemie 9. Jahrgangsstufe 1 Stoffe und ihre Eigenschaften Stoffe: Gegenstände bzw. Körper bestehen aus Stoffen. Eine Stoffportion hat ein bestimmtes Volumen und eine bestimmte Masse. Fest, flüssig
Stoffeigenschaften und Teilchenmodell
 Stoffeigenschaften und Teilchenmodell Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser
Stoffeigenschaften und Teilchenmodell Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Änderungen für nächste Woche Vorlesung
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Änderungen für nächste Woche Vorlesung
7. Chemische Reaktionen
 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte 7.3 Redox - Reaktionen
7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte 7. Chemische Reaktionen 7.1 Thermodynamik chemischer Reaktionen 7.2 Säure Base Gleichgewichte 7.3 Redox - Reaktionen
Vorlesung Wasserinhaltsstoffe. Dr. Thomas Dittmar. Gase
 Vorlesung Wasserinhaltsstoffe Dr. Thomas Dittmar Gase 07/011 Gelöste Gase in der Hydrosphäre O, CO, H S, CH 4, N. Vorkommen, Quellen (natürlich, anthropogen), Wirkung (Humangesundheit, Ökologie), Entfernung
Vorlesung Wasserinhaltsstoffe Dr. Thomas Dittmar Gase 07/011 Gelöste Gase in der Hydrosphäre O, CO, H S, CH 4, N. Vorkommen, Quellen (natürlich, anthropogen), Wirkung (Humangesundheit, Ökologie), Entfernung
allgemeine Aussagen zum Wasser Aufgaben des Wassers Aggregatzustände Aufbau des Wassermoleküls
 Gliederung allgemeine Aussagen zum Wasser Aufgaben des Wassers Aggregatzustände Aufbau des Wassermoleküls physikalische Eigenschaften Lichtdurchlässigkeit Wassertemperatur, Wärmespeichervermögen Dichte,
Gliederung allgemeine Aussagen zum Wasser Aufgaben des Wassers Aggregatzustände Aufbau des Wassermoleküls physikalische Eigenschaften Lichtdurchlässigkeit Wassertemperatur, Wärmespeichervermögen Dichte,
Gegeben sind die folgenden Werte kovalenter Bindungsenthalpien:
 Literatur: Housecroft Chemistry, Kap. 22.1011 1. Vervollständigen Sie folgende, stöchiometrisch nicht ausgeglichene Reaktions gleichungen von Sauerstoffverbindungen. Die korrekten stöchiometrischen Faktoren
Literatur: Housecroft Chemistry, Kap. 22.1011 1. Vervollständigen Sie folgende, stöchiometrisch nicht ausgeglichene Reaktions gleichungen von Sauerstoffverbindungen. Die korrekten stöchiometrischen Faktoren
Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m(h) = 1 u
 Analytische Chemie Stöchiometrie Absolute Atommasse Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m() = 1 u Stoffmenge n Die Stoffmenge
Analytische Chemie Stöchiometrie Absolute Atommasse Die Einheit der Atommasse m ist u. Das ist der 12. Teil der Masse eines Kohlenstoffatoms. 1 u = 1,6608 * 10-27 kg m() = 1 u Stoffmenge n Die Stoffmenge
Elektrodenpotenziale im Gleichgewicht
 Elektrodenpotenziale im Gleichgewicht Zn e - e - e - Cu e - e - Zn 2+ e - Zn 2+ e - Cu 2+ Zn 2+ Zn 2+ Cu 2+ Wenn ein Metallstab in die Lösung seiner Ionen taucht, stellt sich definiertes Gleichgewichtspotential
Elektrodenpotenziale im Gleichgewicht Zn e - e - e - Cu e - e - Zn 2+ e - Zn 2+ e - Cu 2+ Zn 2+ Zn 2+ Cu 2+ Wenn ein Metallstab in die Lösung seiner Ionen taucht, stellt sich definiertes Gleichgewichtspotential
d Chemical Vapor Deposition (CVD)
 d Chemical Vapor Deposition (CVD) Verfahrensprinzip chemical vapor deposition : Abscheidung aus der Gasphase Verwandte Verfahren d Chemical Vapor Deposition (CVD) Prozessablauf CVD: Bildung eines Kupfer-Nanofilms
d Chemical Vapor Deposition (CVD) Verfahrensprinzip chemical vapor deposition : Abscheidung aus der Gasphase Verwandte Verfahren d Chemical Vapor Deposition (CVD) Prozessablauf CVD: Bildung eines Kupfer-Nanofilms
3.4 Schadwirkungen. Toxizität
 3.4 Schadwirkungen Toxizität Toxische Wirkungen bereits in geringen Konzentrationen durch - Schwermetalle und Arsen - Cyanide - aromatische Kohlenwasserstoffe - PAK - Phenole - Halogenkohlenwasserstoffe
3.4 Schadwirkungen Toxizität Toxische Wirkungen bereits in geringen Konzentrationen durch - Schwermetalle und Arsen - Cyanide - aromatische Kohlenwasserstoffe - PAK - Phenole - Halogenkohlenwasserstoffe
Chemische Bindung. Chemische Bindung
 Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
