Erdölraffination & Energieträgergewinnung
|
|
|
- Bärbel Maria Schmitt
- vor 6 Jahren
- Abrufe
Transkript
1 Schulversuchspraktikum Maximilian Wolf Sommersemester 2015 Klassenstufen 9 & 10 Erdölraffination & Energieträgergewinnung
2 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die Aufbereitung von Erdöl, Erdölraffination genannt, umfasst eine Vielzahl von großtechnischen Prozessen, die es ermöglichen die 500 im Erdöl gemischten Stoffe voneinander zu trennen und umzuwandeln. Versuch 1 widmet sich dem auch in der Industrie eingesetztem Prozess des Crackens von langkettigen Alkanen in Paraffinöl. Ein zweiter Versuch weißt mit einer einfachen Nachweisreaktion Alkohol bzw. ( Bio -)Ethanol in Ottokraftstoff nach, der als E10 zum Betrieb von Autos an jeder Tankstelle getankt werden kann. Inhalt 1 Beschreibung des Themas und zugehörige Lernziele Relevanz des Themas für SuS der 9. und 10. Jahrgangsstufe und didaktische Reduktion Lehrerversuch V1 Cracken von Paraffinöl Schülerversuch V2 Nachweis von Ethanol Didaktischer Kommentar zum Schülerarbeitsblatt Erwartungshorizont (Kerncurriculum) Erwartungshorizont (Inhaltlich)... 7
3 1 Beschreibung des Themas und zugehörige Lernziele 1 Beschreibung des Themas und zugehörige Lernziele In einer Erdölraffinerie wird Erdöl, ein Stoffgemisch aus über 500 verschiedenen Stoffen, durch fraktionierte Destillation, bzw. im großtechnischen Prozess Rektifikation genannt, voneinander getrennt. Dazu werden Gruppen aus verschiedenen Stoffen entsprechend ihrer Siedetemperatur aufgetrennt und in ihren Fraktionen gesammelt. Es werden Gase (Siedetemperatur ca. 35 C), Benzinfraktion/Naphta ( C), Mitteldestillat ( C) und Rückstände aus Bitumen/Wachsen (> 350 C) unterschieden. Die Benzinfraktion umfasst ca. 20 % der Masse des Erdöls. Um die Ausbeute dieser Fraktion zu vergrößern, wird das Verfahren des Crackings angewendet. Hier werden langkettige, schwersiedende Stoffe thermisch oder katalytisch in kürzere gecrackt, d.h. gebrochen. Durch homolytische Spaltung werden die Ketten gebrochen es entstehen Alkan-Radikale. Diese Rekombinieren zu neuen Alkanen unterschiedlicher Länge. Da die Rekombination zufällig ist, entstehen längerkettige, gleichlange oder eben kürzerkettige Alkane [1]. Als Nebenprodukte entstehen auch Alkene und cyclische Kohlenwasserstoffe. Die beim Cracking entstandenen Produkte werden erneut der Rektifikation zugeführt, um die Ausbeute der Benzinfraktion zu erhöhen. Dieser Prozess wird ständig wiederholt. Im nachfolgenden Versuchsaufbau wird zähflüssiges Paraffinöl, das aus Alkanen einer Kettenlänge von ca. 15 C-Atomen besteht, an Perlkatalysator aus Aliminium- und Siliciumoxid umgesetzt. Die entstandene Gasphase wird kondensiert und in einer Kühlfalle aufgefangen. Um die Umsetzung zu überprüfen, wird die Brennbarkeit der entstandenen Produkte mit der des Paraffinöls verglichen. Nach neuen EU-Richtlinien wird Benzin Ethanol zugesetzt. Hierbei wird zwischen Super-E5 mit bis zu 5 Vol.-% Ethanol und Super-E10 mit bis zu 10 Vol.-% Bioethanol unterschieden. Bioethanol wird durch alkoholische Gärung von Zucker bzw. Stärke oder Cellulose und anschließender Destillation gewonnen. Zucker, Stärke und Cellulose werden aus Pflanzen, wie z.b. der Zuckerrübe, gewonnen. Im Schülerversuch wird Ethanol mit salpetersaurer, gelb-orangener Cer(IV)- ammoniumnitrat-lösung als roter Cer(IV)-ethanolat-Komplex nachgewiesen. Die Schülerinnen und Schüler (SuS) beschreiben Energieträger wie Erdölprodukte und Bioethanol und wichtige Rohstoffe wie Rohöl und Pflanzen für die chemische Industrie. (FW, Struktur-Eigenschaft) führen Nachweisreaktionen auf das Vorhandensein von bestimmten Teilchen (Alkanolen) zurück. (FW, Stoff-Teilchen) führen qualitative Nachweisreaktionen von Alkanolen durch. (EG, Stoff-Teilchen)
4 2 Relevanz des Themas für SuS der 9. und 10. Jahrgangsstufe und didaktische Reduktion erklären Eigenschaften (wie Siedetemperatur, Viskosität) von anorganischen und organischen Stoffen anhand zwischenmolekularer Wechselwirkungen (Van der Waals- Wechselwirkungen). (FW, Struktur-Eigenschaft) diskutieren und bewerten gesellschaftsrelevante chemische Reaktionen (z. B. großtechnische Prozesse) aus unterschiedlichen Perspektiven. (BW, Chemische Reaktion) stellen Bezüge zu anderen Fächern wie Erdkunde, Politik-Wirtschaft (z. B. Erdöl) her. (BW, Chemische Reaktion) erkennen die Bedeutung von Energieübertragungen in ihrer Umwelt (z. B. Treibstoffe). (BW, Energie) klassifizieren Stoffe wie Heptan, Benzin, Ethanol und Stoffklassen wie Alkane, Aromaten, Alkanole als Energieträger. (FW, Energie) Quelle: [1] Herges, R. (unbekanntes Jahr). Cracking: Mechanismus. /vsc/de/ch/2/oc/stoffklassen/systematik_struktur/acyclische_verbindungen/gesaettigte_k ohlenwasserstoffe/cracking/mechanismus.vscml.html [abgerufen am ] 2 Relevanz des Themas für SuS der 9. und 10. Jahrgangsstufe und didaktische Reduktion Die Gewinnung und Verarbeitung von Erdöl stellen großtechnische Prozesse dar, ohne die die heutige Welt nicht vorzustellen wäre. In diesen Prozessen werden Erdölprodukte gewonnen, die Grundlage für Kunststoffe und Kraftstoffe sind, die uns überall im Alltag begegnen. Sowohl die Handyhülle als auch das Benzin im Tank eines Kraftfahrzeuges entstammen ursprünglich der Gewinnung von Erdöl oder Erdgas. Zu sehen, welcher aufwendige großtechnische Prozess dahintersteht und auch zu sehen, welcher Energiebedarf in der Aufbereitung steckt, ist für SuS interessant, da ein hoher Bezug zur Lebenswelt beinhaltet ist. Der Unterricht zum Thema der Erdölraffination kann als Einstieg in die organische Chemie dienen. Als Vorwissen sollten die Eigenschaft und Nomenklatur der Alkane und Alkanole vorhanden sein. Anhand des Crackens und der Beobachtung der Viskosität und Brennbarkeit können theoretisches Wissen mit praktischer Erfahrung verknüpft werden. Die didaktische Reduktion wird vorgenommen, indem die Reaktionen ohne Übergänge als Radikale behandelt werden. Auch wird die Bildung von Alkenen und zyklischen Kohlenwasserstoffen als Nebenprodukte nicht zwingend behandelt. Beim Nachweis von Ethanol wird nicht von einer koordinativen Bin-
5 3 Lehrerversuch V1 Cracken von Paraffinöl dung ausgegangen, sondern die Reaktion als Bildung eines gelösten, roten Alkoholatsalzes beschrieben. Paraffinöl enthält Alkane mit Kohlenstoffkettenlängen von ca. 15 C-Atomen. Bei der Erdölraffination entspräche dies dem Mitteldestillat. Dieses wird zu kürzerkettigen Alkanen gecrackt, die sich in den Stoffeigenschaften der Viskosität und Brennbarkeit deutlich vom Ausgangsstoff unterscheiden. Als Vorwissen werden typische Eigenschaften (Viskosität, Brennbarkeit, Siedetemperatur) und Nomenklatur der Alkane vorausgesetzt. Der Versuch muss im Abzug durchgeführt werden, da die entstehenden Reaktionsprodukte stark riechen und nicht eingeatmet werden sollen. 3 Lehrerversuch V1 Cracken von Paraffinöl Gefahrenstoffe Benzin H: 225, 315, 304, 336, 411 Heptan H: 225, 304, 315, 336, 410 Cyclohexan H: 225, 304, 315, 336, 410 P: 210, 273, , 331, P: 210, 273, , 331, , P: 210, 240, 273, , 331, Es können noch weitere Stoffe entstehen, für die ähnliche Gefahrenhinweise gelten. Zur Vermeidung von Gefahren ist stets unter dem Abzug zu arbeiten. Beim Abbau und der Reinigung der Apparatur Handschuhe tragen. Materialien: 2 Stative, Stativklemmen, gebogenes Glasrohr, hitzefestes Reagenzglas, Reagenzglas, durchbohrter Stopfen, Glasschale, Spatel, Gasbrenner, Pinzette, Holzstab Chemikalien: Durchführung: Perlkatalysator, Paraffinöl, Eis-Wasser-Gemisch, Glaswolle In das Reagenzglas werden 2 3 ml Paraffinöl und zwei Spatellöffel Perlkatalysator gegeben. Darüber wird etwas Glaswolle in das Reagenzglas geschoben, damit das Paraffinöl beim Sieden nicht direkt in die Destillierbrücke übergehen kann. Das Reagenzglas wird mit einem durchbohrten Gum-
6 3 Lehrerversuch V1 Cracken von Paraffinöl mistopfen verschlossen durch den das Glasrohr gesteckt wurde. Das Glasrohr führt in ein Reagenzglas, das in einem Eis-Wasser-Gemisch gekühlt wird. Das Paraffinöl mit dem Perlkatalysator wird mit dem Gasbrenner erhitzt. Das aufgefangene Kondensat wird mit Paraffinöl verglichen. In einer Porzellanschale wird sich beiden Stoffen mit der brennenden Holzstabspitze genähert. Abb. 1: Versuchsaufbau: Paraffinöl wird mit Perlkatalysator über der Brennerflamme umgesetzt. Im Glasrohr werden Dämpfe kondensiert und in der Kühlfalle aus einem Reagenzglas im Eis-Wasser-Gemisch aufgefangen. Beobachtung: Das Paraffinöl siedet nach kurzer Zeit unter Aufschäumen. Entstandenes weißes Gas kondensiert im Glasrohr und sammelt sich als Flüssigkeit im Reagenzglas im Eis-Wasser-Gemisch. Der Perlkatalysator verfärbt sich zunächst braun und wird im Verlauf schwarz. Das entstandene Produkt riecht benzinartig. Während sich Paraffinöl nicht entzünden lässt und sehr zähflüssig ist, ist das Reaktionsprodukt dünnflüssig und entzündet sich sehr schnell. Die Flamme leuchtet gelb und es kommt zu einer starken Rußbildung.
7 3 Lehrerversuch V1 Cracken von Paraffinöl Abb. 2: Links: Rückstände im Reagenzglas weisen eine Verfärbung auf und der Perlkatalysator hat sich schwarz verfärbt. Rechts: Das aufgefangene Destillat. Deutung: Paraffinöl wurde durch starkes Erhitzen gecrackt: Aus den langkettigen Alkanen (15 C-Atome) sind verschiedene kürzerkettige Alkane entstanden. Diese sind verdampft und nicht kondensiert (1-4 C-Atome) oder als Kondensat, d.h. als Flüssigkeit im Reagenzglas aufgefangen worden (5-10 C- Atome). Die entstandenen Produkte sieden sehr leicht und sind gut brennbar. Entsorgung: Paraffinöl und Destillat werden im Abfallbehälter für organische Lösungsmittel entsorgt. Perlkatalysator und Glaswolle werden gewaschen im Feststoffabfall entsorgt. Literatur: Henkel, S. (2008). Versuch: Thermisches Cracken von Paraffinöl. araffinoel.pdf [abgerufen am ] Schuchlenz, C. (2003). Cracken von Paraffinöl [abgerufen am ]
8 4 Schülerversuch V2 Nachweis von Ethanol Unterrichtsanschlüsse Erdöl und Erdölraffination kann als Einstieg in die Grundlagen der organischen Chemie behandelt werden. Auch anhand des Crackens können gesättigte und ungesättigte Kohlenwasserstoffe in ihren wesentlichen Eigenschaften betrachtet werden. In Klassen mit guter Experimentierkompetenz kann der Versuch auch als (Gruppen- )SchülerInnenexperiment durchgeführt werden, wenn genügend Abzüge vorhanden sind. 4 Schülerversuch V2 Nachweis von Ethanol Alkohol in Form von Ethanol ist den meisten aus alkoholischen Getränken bekannt. Doch Ethanol wird auch als Treibstoff bzw. Treibstoffzusatz verwendet, um den Bedarf an nicht erneuerbaren Energieträgern zu mindern. In diesem Versuch wird in n-heptan gelöstes Ethanol (stellvertretend für Benzin) mit Cer(IV)-ammoniumnitrat nachgewiesen. Die Ausgangslösungen können aus Gründen der Zeitersparnis vorbereitet oder von den SuS selbst hergestellt werden. Gefahrenstoffe Ethanol H: 225 P: 210 Heptan H225, 304, 315, 336, 410 P: 210, 273, , 331, , Salpetersäure H: 314, 290 P: 260, 280, , Cer(IV)-ammoniumnitrat H: 272, 302, 318 P: 219, 280, Materialien: Chemikalien: Durchführung: 3 Reagenzgläser, Pasteurpipetten Ethanol, Heptan, Salpetersäure (30 %), Cer(IV)-ammoniumnitrat, 1 g Cer(IV)-ammoniumnitrat wird in 2,5 ml halbkonzentrierter Salpetersäure gelöst und ggf. leicht erwärmt.
9 4 Schülerversuch V2 Nachweis von Ethanol Zu einer 5%igen sowie einer 10%igen Lösung von Ethanol in Heptan, sowie einer Blindprobe aus reinem Heptan werden einige Tropfen der Cer(IV)- ammoniumnitrat-lösung hinzugegeben. Abb. 3: Salpetersaure Cer(IV)-ammoniumnitrat-Lösung weist je nach Verdünnungsgrad eine gelblich-orangene Färbung auf. Beobachtung: Es bildet sich eine Phasengrenze aus organischer Heptan-Ethanol-Phase oben und wässriger Phase aus Nachweisreagenz unten. An der Phasengrenze verfärbt sich die wässrige, gelb-orangene Cer(IV)-ammoniumnitrat- Lösung braunrot. Die Blindprobe weist keine Farbveränderung auf, die Lösung bleibt orange. Abb. 4: Die farblosen Lösungen mit v.l.n.r. 5, 10 und 0 Vol.-% Ethanol weisen nach Cer(IV)-ammoniumnitrat-Lösung einen Farbveränderung von gelb nach rot auf. Die Vergleichslösung rechts weist nur die gelbliche Färbung des Nachweisreagenz auf. Deutung: Ethanol kann in die wässrige Phase diffundieren. Gelb-orangene Cer(IV)- ammoniumnitrat reagiert mit Ethanol zu rotem Cer(IV)-ethanolat. Dieser Nachweis ist spezifisch für Alkanole, also auch andere Alkanole als Ethanol. RG: [Ce(NO 3) 6] 2- + CH 3CH 2OH + H 2O [Ce(NO 3) 5(CH 3CH 2O)] 2- + NO H 3O +
10 4 Schülerversuch V2 Nachweis von Ethanol Entsorgung: Cer(IV)-ammoniumnitrat-Lösung wird im Abfallbehälter für Schwermetalle entsorgt. Heptan-Ethanol-Lösung bzw. Heptan oder Ethanol werden im Behälter für organische Lösungsmittel entsorgt. Salpetersäure wird im Behälter für Säure-Base-Abfälle entsorgt. Literatur: Heger, K. (2006). Zucker. [abgerufen am ] Illumnia-Chemie.de (2009). Nachweis von Alkoholen. (abgerufen am ) Unterrichtsanschlüsse Der Nachweis von Alkanolen kann als Einstieg in die Unterrichtseinheit über die Stoffklasse der Alkanole erfolgen. Anschließend können weitere Eigenschaften und die Verwendung von Alkanolen besprochen werden.
11 Arbeitsblatt Erdöl und seine Verwendung Aufgabe 1) Benenne durch Ankreuzen die Gegenstände, die aus Erdölprodukten bestehen. Recherchiere dazu in Quellen deiner Wahl. Nylon-Strumpf Nagel Dübel Kerze Kosmetik Lego-Steine Spiegel Tesafilm Medikament Druckerpapier Aufgabe 2) Ermittle die Summenformel für folgende Stoffe. Ethan Hexan Nonan Butan-2-ol Butan-1-ol Propan Aufgabe 3) Erkläre, warum es wichtig ist den Erdölverbrauch zu senken. Nenne Beispiele, wie dies im Alltag umgesetzt werden kann.
12 5 Didaktischer Kommentar zum Schülerarbeitsblatt 5 Didaktischer Kommentar zum Schülerarbeitsblatt Erdöl und Erdölprodukte finden sich im Alltag überall wieder. Dabei ist es oft nicht direkt ersichtlich, dass Erdöl verwendet wurde die Erdölprodukte sind versteckt. Das Arbeitsblatt kann zum Ende der Unterrichtseinheit zu Erdöl und der Einführung in Themenbereiche der organischen Chemie verwendet werden. Es stellt einen Zusammenhang zwischen der Verwendung von Erdölprodukten und der gesellschaftlichen Bedeutung, sowie der Bedeutung für die Umwelt her. Übergeordnet sind die folgenden prozessbezogenen Lernziele: Die SuS diskutieren und bewerten die gesellschaftsrelevante Herstellung von Erdöl und Erdölprodukten aus unterschiedlichen Perspektiven (BW, Chemische Reaktion). stellen Bezüge zu anderen Fächern wie Erdkunde, Politik-Wirtschaft durch das Thema Erdöl her (BW, Chemische Reaktion). 5.1 Erwartungshorizont (Kerncurriculum) Aufgabe 1) Die SuS beschreiben Energieträger wie Erdölprodukte und Bioethanol und wichtige Rohstoffe wie Rohöl für die chemische Industrie (FW, Struktur-Eigenschaft). Die SuS erkennen in den genannten Alltagsgegenständen die Verwendung von Produkten der chemischen Industrie wieder, die sich den Stoffen bedient, die in Erdöl vorkommen. Dabei gibt es auch überraschende Entdeckungen, da Erdölprodukte auch in Alltagsgegenständen verwendet wird, in denen es auf den ersten Blick nicht der Fall zu sein scheint. Da Gegenstände benannt werden, die schon mit Erdölprodukten in Verbindung gebracht wurden, aber welche, die unbekannt sind, deckt diese Aufgabe Anforderungsbereich I und III ab. Die Liste kann beliebig erweitert werden und die Gegenstände können als zum Anfassen ausgelegt werden, was das identifizieren als Erdölprodukt erleichtern kann. Dass z.b. in Papier Erdölprodukte als Füllstoffe oder leicht überschaubar als Druckfarbe verwendet wird, soll überraschen. Aufgabe 2) Die Schülerinnen und Schüler nennen die Summenformeln einfacher Alkane und Alkanole. Die Nomenklatur von Alkanen und Alkanolen ist nicht direkt im Kerncurriculum Niedersachsen als Kompetenz aufgeführt. Jedoch beziehen sich die ergänzenden Differenzierungen der in dem Kompetenzbereich Fachwissen genannten Inhalte und Begriffe auf ebendiese Stoffgruppen der Alkane und Alkanole. Die Nomenklatur von unverzweigten Alkanen und Alkanolen mit ihrer funktionellen Hydroxy-Gruppe sollte zuvor im Unterricht behandelt werden. Eine Liste der Al-
13 5 Didaktischer Kommentar zum Schülerarbeitsblatt kanvorsilben, die zulässt auf die Anzahl der C-Atome zu schließen sollte verfügbar gemacht werden. Wenn die Nomenklatur zuvor im Unterricht besprochen wurde deckt diese Aufgabe den Anforderungsbereich II ab, indem die SuS ihr Wissen anwenden und Stoffnamen Summenformeln zuordnen. Aufgabe 3) Die SuS diskutieren und bewerten gesellschaftsrelevante chemische Reaktionen (z. B. großtechnische Prozesse) aus unterschiedlichen Perspektiven (BW, Chemische Reaktion). Die SuS sollen bei dieser Aufgabe die gesellschaftliche Bedeutung der Verwendung von fossilen Brennstoffen diskutieren und die Bedeutung für die Umwelt erkennen. Hierzu können Artikel aus Zeitungen oder dem Internet bereitgelegt werden, die bei der Darstellung des Themas helfen. Die SuS betrachten die gesamtgesellschaftliche Bedeutung und stellen ihr Wissen in einen größeren Zusammenhang. Es werden Bezüge zum Kohlenstoff-Stoffkreislauf gezogen. Diese Aufgabe entspricht dem Anforderungsniveau III. 5.2 Erwartungshorizont (Inhaltlich) Aufgabe 1) Erdölprodukte sind Nylon-Strümpfe, Dübel, Kerzen, Kosmetik, Legosteine, Tesafilm, Medikamente und auch Druckerpapier kann Erdölprodukte enthalten. Die Strümpfe, Dübel, Lego-Steine und Tesafilm bestehen aus verschiedenen Kunststoffen, die dem Erdöl abgewonnen werden können. Das Paraffin, welches als Kerzenwachs verwendet wird ist in vielen Kerzen ebenfalls ein Erdölprodukt. Überraschenderweise ist auch in vielen Papiersorten Bindemittel enthalten, die Erdölprodukte sind. Hierbei handelt es sich um Polymere auf Basis von Acrylaten oder Polyurethanen. In Medikamenten dienen die organischen Erdölprodukte oft als Edukte zur Synthese von Wirkstoffen. Außerdem dient Paraffin aus Erdöl als Grundstoff zur Herstellung von Vaseline, die die Wirkstoffe in Salben aufnimmt. Aufgabe 2) Ethan C 2H 6 Hexan C 6H 14 Nonan C 9H 20 Butan-2-ol C 4H 10O bzw. C 4H 9OH Butan-1-ol C 4H 10O bzw. C 4H 9OH Propan: C 3H 8 Aufgabe 3)
14 5 Didaktischer Kommentar zum Schülerarbeitsblatt Erdöl wird meist als Treibstoff verwendet, zu Kunststoffen weiterverarbeitet oder dient als Grundlage für viele andere Stoffe, die täglich verbraucht werden. Die meisten Stoffe werden verbrannt. Ob direkt als Kraftstoff, in Müllverbrennungsanlagen oder Kerzenwachs. Dabei wurde das Erdöl aus der Erde gefördert und als fossiler Energieträger in den Kohlenstoffkreislauf der Erde eingebracht. Es entsteht schon bei der Aufarbeitung viel Kohlenstoffdioxid, da hierzu viel Energie benötigt wird. Werden die Rohstoffe letztendlich verbrannt befindet sich in der Atmosphäre mehr Kohlenstoffdioxid, das ein Treibhausgas ist. Treibhausgase sind dafür verantwortlich, dass sich die Atmosphäre langsam erwärmt, was weitreichende Folgen hat. Senkt man den persönlichen Erdölverbrauch hilft man die Umwelt zu schützen und daraus entstehende gesellschaftliche Probleme zu vermeiden. Im Alltag können vermehrt auf pflanzliche Produkte (pflanzliches Kerzenwachs, Biokunststoffe) umsteigen und kurze Strecken mit dem Fahrrad gefahren werden. Pflanzliche Energieträger wurden von den Pflanzen dem Kohlenstoffkreislauf entnommen und beim Verbrauch wieder zugeführt. Dem Kohlenstoffkreislauf entzogenes und wieder zugeführtes Kohlenstoffdioxid halten sich die Waage.
Versuch: Thermisches Cracken von Paraffinöl
 Philipps-Universität Marburg 21.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2, Alkane Versuch: Thermisches Cracken von Paraffinöl
Philipps-Universität Marburg 21.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2, Alkane Versuch: Thermisches Cracken von Paraffinöl
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 25.11.2008 Zeitbedarf Vorbereitung: 5 Minuten Durchführung:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 25.11.2008 Zeitbedarf Vorbereitung: 5 Minuten Durchführung:
Schulversuchspraktikum. Name Thomas Polle. Sommersemester Klassenstufen 5 & 6. Feuer und Kerzen
 Schulversuchspraktikum Name Thomas Polle Sommersemester 2015 Klassenstufen 5 & 6 Feuer und Kerzen 2 Auf einen Blick: Es werden je ein Schüler- und Lehrerversuch zum Thema Kerzen und Feuer für den 5. und
Schulversuchspraktikum Name Thomas Polle Sommersemester 2015 Klassenstufen 5 & 6 Feuer und Kerzen 2 Auf einen Blick: Es werden je ein Schüler- und Lehrerversuch zum Thema Kerzen und Feuer für den 5. und
Thema: Sauerstoff Klasse 7 / 8. Schulversuchspraktikum. Bastian Hollemann. Sommersemester Klassenstufen 7 & 8. Sauerstoff
 Thema: Sauerstoff Klasse 7 / 8 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 7 & 8 Sauerstoff Thema: Sauerstoff Klasse 7 / 8 Auf einen Blick: Diese Unterrichtseinheit für die
Thema: Sauerstoff Klasse 7 / 8 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 7 & 8 Sauerstoff Thema: Sauerstoff Klasse 7 / 8 Auf einen Blick: Diese Unterrichtseinheit für die
Schulversuchspraktikum. Friederike Kellner. Sommersemester Klassenstufen 11 & 12. Alkanone
 Schulversuchspraktikum Friederike Kellner Sommersemester 2014 Klassenstufen 11 & 12 Alkanone 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Die im Folgenden vorgestellte Unterrichtseinheit
Schulversuchspraktikum Friederike Kellner Sommersemester 2014 Klassenstufen 11 & 12 Alkanone 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Die im Folgenden vorgestellte Unterrichtseinheit
Vom Alkohol zum Alken
 1 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufe 9 & 10 Vom Alkohol zum Alken 2 Auf einem Blick: Diese Unterrichtseinheit für die Klasse 9 & 10 enthält Lehrerversuche und 1 Schülerversuch
1 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufe 9 & 10 Vom Alkohol zum Alken 2 Auf einem Blick: Diese Unterrichtseinheit für die Klasse 9 & 10 enthält Lehrerversuche und 1 Schülerversuch
Dichte und Nachweis von Kohlenstoffdioxid
 Schulversuchspraktikum Name: Lydia Reinhardt Semester: Sommersemester 2014 Klassenstufen 7 & 8 Dichte und Nachweis von Kohlenstoffdioxid 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Name: Lydia Reinhardt Semester: Sommersemester 2014 Klassenstufen 7 & 8 Dichte und Nachweis von Kohlenstoffdioxid 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
V 1 Herstellung von Natriumchlorid
 1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
Schulversuchspraktikum. Isabelle Faltiska. Sommersemester Klassenstufen 11 & 12. Quantitative Analyse von. Kohlenwasserstoffen
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 11 & 12 Quantitative Analyse von Kohlenwasserstoffen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Im Folgenden
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 11 & 12 Quantitative Analyse von Kohlenwasserstoffen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Im Folgenden
Energie und Energieumwandlung
 Schulversuchspraktikum Maximilian Wolf Sommersemester Klassenstufen 7 & 8 Energie und Energieumwandlung Kurzprotokoll Auf einen Blick: In Versuch 1 werden Lycopodium-Sporen (Bärlapp) in der Gasbrennerflamme
Schulversuchspraktikum Maximilian Wolf Sommersemester Klassenstufen 7 & 8 Energie und Energieumwandlung Kurzprotokoll Auf einen Blick: In Versuch 1 werden Lycopodium-Sporen (Bärlapp) in der Gasbrennerflamme
Schulversuchspraktikum. Isabel Böselt. Sommersemester Klassenstufen 5 & 6. Aggregatzustände. und deren Temperaturabhängigkeit
 Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden einfache
Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden einfache
Fluoreszierende Verbindungen
 Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Merkmale einer chemischen Reaktion
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale einer chemischen Reaktion 1 Auf Beschreibung einen Blick: des Themas und zugehörige Lernziele Im Folgenden werden
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale einer chemischen Reaktion 1 Auf Beschreibung einen Blick: des Themas und zugehörige Lernziele Im Folgenden werden
Endotherm und Exotherm
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen
Versuch: Qualitativer Nachweis von Kohlenstoff und Wasserstoff
 Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Warum korrodiert Eisen?
 Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser?
 http://www.kostenloseausmalbilder.de/media/.gallery/main606.jpg (02.08.2015) Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser? Pip, die kleine Maus, benötigt zum Atmen Luft, vor allem den Sauerstoff,
http://www.kostenloseausmalbilder.de/media/.gallery/main606.jpg (02.08.2015) Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser? Pip, die kleine Maus, benötigt zum Atmen Luft, vor allem den Sauerstoff,
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Alkane - eine vielseitige Stoffgruppe. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Alkane - eine vielseitige Stoffgruppe Das komplette Material finden Sie hier: School-Scout.de RAAbits Hauptschule 7 9 Naturwissenschaften
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Alkane - eine vielseitige Stoffgruppe Das komplette Material finden Sie hier: School-Scout.de RAAbits Hauptschule 7 9 Naturwissenschaften
1 Lehrerversuch Alkalimetalle in Wasser
 1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
Schulversuchspraktikum. Julia Müller. Eigenschaften gesättigter Kohlenwasserstoffe
 Schulversuchspraktikum Name: Julia Müller Semester: SoSe 2012 Klassenstufen: 9 und 10 Eigenschaften gesättigter Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Name: Julia Müller Semester: SoSe 2012 Klassenstufen: 9 und 10 Eigenschaften gesättigter Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Arbeitsblatt Ist groß besser als klein?
 Arbeitsblatt Ist groß besser als klein? Aufgabe 1: Führe folgendes Experiment durch und notiere deine Beobachtungen. Materialien: 4 Reagenzgläser, Reagenzglasständer, Spatel Chemikalien: Gefahrenstoffe
Arbeitsblatt Ist groß besser als klein? Aufgabe 1: Führe folgendes Experiment durch und notiere deine Beobachtungen. Materialien: 4 Reagenzgläser, Reagenzglasständer, Spatel Chemikalien: Gefahrenstoffe
Aggregatzustände und deren Temperaturabhängigkeit
 Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Merkmale chemischer Reaktionen
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale chemischer Reaktionen Kurzprotokoll Auf einen Blick: Im Folgenden werden weitere Versuche zum Thema Merkmale einer
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale chemischer Reaktionen Kurzprotokoll Auf einen Blick: Im Folgenden werden weitere Versuche zum Thema Merkmale einer
Arbeitsblatt Wasserkreislauf der Erde
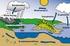 Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Wasser als Lösungsmittel
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die Versuche zum Thema Wasser
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die Versuche zum Thema Wasser
Ungesättigte Kohlenwasserstoffe
 Schulversuchspraktikum Name: Stefan Krüger Semester: SoSe 2014 Klassenstufen: 11/12 Ungesättigte Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum Name: Stefan Krüger Semester: SoSe 2014 Klassenstufen: 11/12 Ungesättigte Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll
Eine Reaktion mit Kupfer und Schwefel
 Eine Reaktion mit Kupfer und Schwefel Materialien: Chemikalien: Duranglas, Stativstange mit Stativklemme, Gasbrenner Schwefelpulver, Kupferblech Durchführung: Fülle vorsichtig ca. 1cm breit Schwefelpulver
Eine Reaktion mit Kupfer und Schwefel Materialien: Chemikalien: Duranglas, Stativstange mit Stativklemme, Gasbrenner Schwefelpulver, Kupferblech Durchführung: Fülle vorsichtig ca. 1cm breit Schwefelpulver
Endotherm und Exotherm
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen Schülerversuch
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen Schülerversuch
Vom Alkohol zum Alken
 Schulversuchspraktikum Sabine Wolff SoSe 2013 Klassenstufen 9 & 10 Vom Alkohol zum Alken 2 Auf einen Blick: Im Folgenden werden zwei Lehrerversuche vorgestellt, die die Darstellung von gasförmigen Alkenen
Schulversuchspraktikum Sabine Wolff SoSe 2013 Klassenstufen 9 & 10 Vom Alkohol zum Alken 2 Auf einen Blick: Im Folgenden werden zwei Lehrerversuche vorgestellt, die die Darstellung von gasförmigen Alkenen
Schulversuchspraktikum. Constanze Koch. Sommersemester Klassenstufen 5 & 6. Wasser als Lösungsmittel. Kurzprotokoll
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum. Dennis Roggenkämper. Sommersemester Klassenstufen 5 & 6. Brandbekämpfung
 Schulversuchspraktikum Dennis Roggenkämper Sommersemester 2015 Klassenstufen 5 & 6 Brandbekämpfung 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Das Protokoll umfasst ein Lehrer-
Schulversuchspraktikum Dennis Roggenkämper Sommersemester 2015 Klassenstufen 5 & 6 Brandbekämpfung 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Das Protokoll umfasst ein Lehrer-
Von Arrhenius zu Brönsted
 Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
Schulversuchspraktikum Name Annika Münch Sommersemester 2015 Klassenstufen 9/10 Von Arrhenius zu Brönsted Kurzprotokoll Auf einen Blick: Für die Unterrichtseinheit zum Themas Säure-Base-Konzepte und im
4. Reaktionsgeschwindigkeit und chemisches Gleichgewicht
 Chemie RG mit DG, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit DG, 5-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemie RG mit DG, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit DG, 5-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch
Eigenschaften gesättigter Kohlenwasserstoffe
 Schulversuchspraktikum Anne Steinkuhle Sommersemester 2013 Klassenstufen 9 & 10 Eigenschaften gesättigter Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In dem
Schulversuchspraktikum Anne Steinkuhle Sommersemester 2013 Klassenstufen 9 & 10 Eigenschaften gesättigter Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In dem
Reaktionen von Metallen mit Sauerstoff und mit Luft
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Fossile Rohstoffe. Erdöl
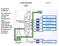 Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Fraktionierte Destillation Die stufenweise Abtrennung einzelner Komponenten eines Stoffgemisches aufgrund der unterschiedlichen Siedepunkte wird als fraktionierte Destillation bezeichnet. 1 Fraktionierte
Reinstoffe und Stoffgemische, Verfahren zur Stofftrennung
 Schulversuchspraktikum Name: Jana Pfefferle Semester: SoSe 2014 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische, Verfahren zur Stofftrennung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen
Schulversuchspraktikum Name: Jana Pfefferle Semester: SoSe 2014 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische, Verfahren zur Stofftrennung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen
Konsequenzen der Ozeanversauerung
 Thema: Stoffkreisläufe Jahrgang 9 & 10 Konsequenzen der Ozeanversauerung Lies den Ausschnitt aus dem nachfolgenden Zeitungsartikel eines Wissenschaftsmagazins aufmerksam durch und betrachte im Diagramm
Thema: Stoffkreisläufe Jahrgang 9 & 10 Konsequenzen der Ozeanversauerung Lies den Ausschnitt aus dem nachfolgenden Zeitungsartikel eines Wissenschaftsmagazins aufmerksam durch und betrachte im Diagramm
4. Chemische Reaktionen und Energieumsatz, Thermochemie
 Chemie RG mit LS, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemie RG mit LS, Themenbereiche, Seite 1 von 4 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
chulportfolio 3. Schulkonzept 3.7 Kern- und Schulcurricula G9 (Klasse 5 11) Chemie Chemie Klasse 11
 Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Stoffverteilungsplan Lehrplan für den Erwerb des Hauptschul- und des Realschulabschlusses (Regelschule) in Thüringen 2012 PRISMA Chemie Thüringen
 Stoffverteilungsplan Lehrplan für den Erwerb des Hauptschul- und des Realschulabschlusses (Regelschule) in Thüringen 2012 PRISMA Chemie Thüringen Band 9/10 Schule: Klett 978-3-12-068567-8 Lehrer/Lehrerin:
Stoffverteilungsplan Lehrplan für den Erwerb des Hauptschul- und des Realschulabschlusses (Regelschule) in Thüringen 2012 PRISMA Chemie Thüringen Band 9/10 Schule: Klett 978-3-12-068567-8 Lehrer/Lehrerin:
Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung
 Chemie RG mit LS, Themenbereiche, Seite 1 von 5 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Chemie RG mit LS, Themenbereiche, Seite 1 von 5 Chemie im Realgymnasium mit LS, 6-stündig Themenbereiche für die Reifeprüfung 1. Atombau und Periodensystem Die geschichtliche Entwicklung der Atommodelle
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll
Vom Alkan zum Alkohol
 Schulversuchspraktikum Sommersemester 2016 Klassenstufen 9 & 10 Vom Alkan zum Alkohol Auf einen Blick: Das Protokoll Vom Alkan zum Alkohol enthält zwei Lehrerversuche und zwei Schülerversuche. Die Lehrerversuche
Schulversuchspraktikum Sommersemester 2016 Klassenstufen 9 & 10 Vom Alkan zum Alkohol Auf einen Blick: Das Protokoll Vom Alkan zum Alkohol enthält zwei Lehrerversuche und zwei Schülerversuche. Die Lehrerversuche
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10. Die Brennstoffzelle
 Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10 Die Brennstoffzelle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10 Die Brennstoffzelle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Schulversuchspraktikum. Marc Ehlers. Sommersemester Klassenstufen 7 & 8. Sauerstoff. Kurzprotokoll
 Schulversuchspraktikum Marc Ehlers Sommersemester 2016 Klassenstufen 7 & 8 Sauerstoff Kurzprotokoll Auf einen Blick: In diesem Protokoll werden weitere Versuche zum Thema Sauerstoff als Bestandteil der
Schulversuchspraktikum Marc Ehlers Sommersemester 2016 Klassenstufen 7 & 8 Sauerstoff Kurzprotokoll Auf einen Blick: In diesem Protokoll werden weitere Versuche zum Thema Sauerstoff als Bestandteil der
Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer
 Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer chemischen Reaktion? In der letzten Chemiestunde hast du eine Hypothese zu der Frage formuliert: Verändert sich die Masse von
Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer chemischen Reaktion? In der letzten Chemiestunde hast du eine Hypothese zu der Frage formuliert: Verändert sich die Masse von
Schulversuchspraktikum. Alexander König. Sommersemester Klassenstufen 11 & 12. Katalysatoren
 Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 11 & 12 Katalysatoren Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält einen Schülerversuch und einen
Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 11 & 12 Katalysatoren Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält einen Schülerversuch und einen
Korrosion und Korrosionsschutz
 Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 7 & 8 Korrosion und Korrosionsschutz Auf einen Blick: Diese Unterrichtseinheit für die Klassen 7 & 8 enthält 1 Schülerversuch und
Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 7 & 8 Korrosion und Korrosionsschutz Auf einen Blick: Diese Unterrichtseinheit für die Klassen 7 & 8 enthält 1 Schülerversuch und
Umwelt und Recycling
 Schulversuchspraktikum Anonym_16 Sommersemester 2016 Klassenstufen 5 & 6 Umwelt und Recycling Kurzprotokoll Auf einen Blick: Versuch 1 und 2 behandeln die Problematik der Meeresverschmutzung mit Ölen.
Schulversuchspraktikum Anonym_16 Sommersemester 2016 Klassenstufen 5 & 6 Umwelt und Recycling Kurzprotokoll Auf einen Blick: Versuch 1 und 2 behandeln die Problematik der Meeresverschmutzung mit Ölen.
Schulversuchspraktikum. Sommersemester Klassenstufen 7 & 8. Vom Erz zum Metall. (oxidische und sulfidische Erze)
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Vom Erz zum Metall (oxidische und sulfidische Erze) Auf einen Blick: In der 7./8. Klasse wird noch statt von Redoxreaktionen von Sauerstoffübertragungsreaktionen
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Vom Erz zum Metall (oxidische und sulfidische Erze) Auf einen Blick: In der 7./8. Klasse wird noch statt von Redoxreaktionen von Sauerstoffübertragungsreaktionen
Schulversuchspraktikum. Michaela Micke. Sommersemester Klassenstufen 9 & 10. Chemie der Kohlenwasserstoffe. Methan & Erdgas
 Schulversuchspraktikum Michaela Micke Sommersemester 2012 Klassenstufen 9 & 10 Chemie der Kohlenwasserstoffe Methan & Erdgas 1 Konzept und Ziele 1 Auf einen Blick: Die vorliegende Unterrichtseinheit für
Schulversuchspraktikum Michaela Micke Sommersemester 2012 Klassenstufen 9 & 10 Chemie der Kohlenwasserstoffe Methan & Erdgas 1 Konzept und Ziele 1 Auf einen Blick: Die vorliegende Unterrichtseinheit für
Wie verändern sich die Eigenschaften der Alkohole bei Zunahme der Kohlenstoffzahl?
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Fette, Öle und Tenside
 Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside Kurzprotokoll Inhalt Inhaltsverzeichnis 1Weitere Lehrerversuche... 3 V1 Verseifungszahl... 3 2Weitere
Eigenschaften, Vorkommen und Anwendungen einiger C 5 -C 10 -Alkane
 Eigenschaften, Vorkommen und Anwendungen einiger C 5 -C 10 -Alkane C 5 H 12 : Pentane (3 Konstitutions-Isomere) n-pentan: SdT 36 C SmT - 130 C Dichte 0,63g/cm 3 (20 C) F +, X n, N R 12-65-66-51/53 S (2)-9-16-29-33-61-62
Eigenschaften, Vorkommen und Anwendungen einiger C 5 -C 10 -Alkane C 5 H 12 : Pentane (3 Konstitutions-Isomere) n-pentan: SdT 36 C SmT - 130 C Dichte 0,63g/cm 3 (20 C) F +, X n, N R 12-65-66-51/53 S (2)-9-16-29-33-61-62
Schulversuchspraktikum. Jans Manjali. Sommersemester. Klassenstufen 11 & 12. Löslichkeitsprodukt
 Schulversuchspraktikum Jans Manjali Sommersemester Klassenstufen 11 & 12 Löslichkeitsprodukt 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll wird das Thema Löslichkeit
Schulversuchspraktikum Jans Manjali Sommersemester Klassenstufen 11 & 12 Löslichkeitsprodukt 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll wird das Thema Löslichkeit
Synthese, Analyse, Umsetzung
 Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 7&8 Synthese, Analyse, Umsetzung Auf einen Blick Die Thematik Synthese, Analyse und Umsetzung umfasst die Grundtypen chemischer Reaktionen.
Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 7&8 Synthese, Analyse, Umsetzung Auf einen Blick Die Thematik Synthese, Analyse und Umsetzung umfasst die Grundtypen chemischer Reaktionen.
Reaktion von Nichtmetallen mit Sauerstoff und mit Luft
 Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 7 & 8 Reaktion von Nichtmetallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 7 & 8 Reaktion von Nichtmetallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Carbonsäuren, Ester und Ether
 Schulversuchspraktikum Jannik Nöhles Sommersemester 2016 Klassenstufen 11,12 & 13 Carbonsäuren, Ester und Ether 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Dieses Protokoll beinhaltet
Schulversuchspraktikum Jannik Nöhles Sommersemester 2016 Klassenstufen 11,12 & 13 Carbonsäuren, Ester und Ether 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Dieses Protokoll beinhaltet
Schulversuchspraktikum. Name: Jennifer Ahrens. Semester: Sommersemester Klassenstufen 9 & 10. Alkalimetalle
 Schulversuchspraktikum Name: Jennifer Ahrens Semester: Sommersemester 2012 Klassenstufen 9 & 10 Alkalimetalle Auf einen Blick: In dieser Unterrichtseinheit werden Versuche zu den Alkalimetallen der ersten
Schulversuchspraktikum Name: Jennifer Ahrens Semester: Sommersemester 2012 Klassenstufen 9 & 10 Alkalimetalle Auf einen Blick: In dieser Unterrichtseinheit werden Versuche zu den Alkalimetallen der ersten
Korrosion und Korrosionsschutz
 Schulversuchspraktikum Christian Köhler Sommersemester 2016 Klassenstufen 7&8 Korrosion und Korrosionsschutz Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll beinhaltet drei weitere Schülerversuche
Schulversuchspraktikum Christian Köhler Sommersemester 2016 Klassenstufen 7&8 Korrosion und Korrosionsschutz Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll beinhaltet drei weitere Schülerversuche
Wir untersuchen Mineralwasser
 Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Metalle und Nichtmetalle
 Schulversuchspraktium Bastian Hollemann Sommersemester 2015 Klassenstufen 9 & 10 Metalle und Nichtmetalle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Diese Unterrichtseinheit für
Schulversuchspraktium Bastian Hollemann Sommersemester 2015 Klassenstufen 9 & 10 Metalle und Nichtmetalle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Diese Unterrichtseinheit für
Nährstoffe und Nahrungsmittel
 1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
Fachschaft Chemie. Schuleigenes Curriculum für die Klassen 10
 Fachschaft Schuleigenes Curriculum für die Klassen 10 04.05.2009 Didaktische Prinzipen Kurzformulierte Pflichtinhalte Geforderte Kompetenz Hinweise/Methodik Std. organische Kohlenstoffverbindungen funktionelle
Fachschaft Schuleigenes Curriculum für die Klassen 10 04.05.2009 Didaktische Prinzipen Kurzformulierte Pflichtinhalte Geforderte Kompetenz Hinweise/Methodik Std. organische Kohlenstoffverbindungen funktionelle
Erscheinungsformen und Eigenschaften des Wassers
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 5 & 6 Erscheinungsformen und Eigenschaften des Wassers 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 5 & 6 Erscheinungsformen und Eigenschaften des Wassers 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 7 & 8. Dichte und Nachweis von CO2
 Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 7 & 8 Dichte und Nachweis von CO2 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 7 & 8 Dichte und Nachweis von CO2 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind
Schulversuchspraktikum. Dennis Roggenkämper. Sommersemester Klassenstufen 11 & 12. Kohlenhydrate
 Schulversuchspraktikum Dennis Roggenkämper Sommersemester 2015 Klassenstufen 11 & 12 Kohlenhydrate 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Das Protokoll umfasst ein Lehrer-
Schulversuchspraktikum Dennis Roggenkämper Sommersemester 2015 Klassenstufen 11 & 12 Kohlenhydrate 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Das Protokoll umfasst ein Lehrer-
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Destillation von Rohöl. + Rohbenzine + Petroleum
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 28.09.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Destillation von Rohöl Gruppe
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 28.09.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Destillation von Rohöl Gruppe
Verfahren zur Stofftrennung
 Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Verfahren zur Stofftrennung Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll enthält
Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Verfahren zur Stofftrennung Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll enthält
Unterrichtsvorhaben II Vom Alkohol zum Aromastoff
 Unterrichtsvorhaben II Vom Alkohol zum Aromastoff Umfang: Jgst.: 38 EF Schwerpunkte / Inhalt Konkrete Kompetenzerwartungen Vgl. Kapitel im Schulbuch Anmerkungen Rund um das Parfum: Aromastoffe (Vorkommen,
Unterrichtsvorhaben II Vom Alkohol zum Aromastoff Umfang: Jgst.: 38 EF Schwerpunkte / Inhalt Konkrete Kompetenzerwartungen Vgl. Kapitel im Schulbuch Anmerkungen Rund um das Parfum: Aromastoffe (Vorkommen,
Schulversuchspraktikum. Johanna Osterloh. Sommersemester Klassenstufen 9 & 10. Stoffkreisläufe. Kurzprotokoll
 Schulversuchspraktikum Johanna Osterloh Sommersemester 2015 Klassenstufen 9 & 10 Stoffkreisläufe Kurzprotokoll Auf einen Blick: Dieses Protokoll enthält vier Schülerversuche, die zum Thema Kohlenstoffdioxidkreislauf
Schulversuchspraktikum Johanna Osterloh Sommersemester 2015 Klassenstufen 9 & 10 Stoffkreisläufe Kurzprotokoll Auf einen Blick: Dieses Protokoll enthält vier Schülerversuche, die zum Thema Kohlenstoffdioxidkreislauf
Decan Homologe Reihe der Alkane, unterschiedlich lange C-Ketten mit C- C (sp 3 /sp 3 ) und C-H (sp 3 /s)-bindungen (σ-bindungen) Beispiele: Butan
 1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
Versuch: Destillation von Rohöl
 Philipps-Universität Marburg 26.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Destillation von Rohöl
Philipps-Universität Marburg 26.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Destillation von Rohöl
Schulversuchspraktikum. Ansgar Misch. Sommersemester Klassenstufen 7 & 8. Stickstoff. Kurzprotokoll
 Schulversuchspraktikum Ansgar Misch Sommersemester 2016 Klassenstufen 7 & 8 Stickstoff Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll zum Thema Stickstoff enthält weitere Versuche, die die Eigenschaften
Schulversuchspraktikum Ansgar Misch Sommersemester 2016 Klassenstufen 7 & 8 Stickstoff Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll zum Thema Stickstoff enthält weitere Versuche, die die Eigenschaften
STOFFE U N D STOFFTRENNUNG
 Inhalt WAS IST CHEMIE? 10 STOFFE U N D STOFFTRENNUNG 22 Chemie erlebt Chem ie-chancen und Gefahren...12 Umgang mit Chemikalien... 14 Chemie erlebt Chemie is t... 16 Methode Regeln beim Experimentieren...17
Inhalt WAS IST CHEMIE? 10 STOFFE U N D STOFFTRENNUNG 22 Chemie erlebt Chem ie-chancen und Gefahren...12 Umgang mit Chemikalien... 14 Chemie erlebt Chemie is t... 16 Methode Regeln beim Experimentieren...17
1 Arbeitsblatt. 1.1 Erwartungshorizont
 1 Arbeitsblatt Das Arbeitsblatt dient der Protokollierung und der Auswertung des Lehrerversuches V1. Während die Versuchsdurchführung und Versuchbeobachtung wenig strukturiert ist, ist die Deutung des
1 Arbeitsblatt Das Arbeitsblatt dient der Protokollierung und der Auswertung des Lehrerversuches V1. Während die Versuchsdurchführung und Versuchbeobachtung wenig strukturiert ist, ist die Deutung des
Alkohole und deren Eigenschaften
 Schulversuchspraktikum Dirk Schlemme Sommersemester 2012 Klassenstufen 9 & 10 Alkohole und deren Eigenschaften 1 Konzept und Ziele 1 Auf einen Blick: Die homologe Reihe der Alkohole grenzt sich durch einige
Schulversuchspraktikum Dirk Schlemme Sommersemester 2012 Klassenstufen 9 & 10 Alkohole und deren Eigenschaften 1 Konzept und Ziele 1 Auf einen Blick: Die homologe Reihe der Alkohole grenzt sich durch einige
Schulversuchspraktikum. Moritz Pemberneck. Sommersemester Klassenstufen 7 & 8. Fällungsreaktionen. Kurzprotokoll
 Schulversuchspraktikum Moritz Pemberneck Sommersemester 2016 Klassenstufen 7 & 8 Fällungsreaktionen Kurzprotokoll Auf einen Blick: In diesem Protokoll werden weitere Schülerversuche zum Thema Fällungsreaktionen
Schulversuchspraktikum Moritz Pemberneck Sommersemester 2016 Klassenstufen 7 & 8 Fällungsreaktionen Kurzprotokoll Auf einen Blick: In diesem Protokoll werden weitere Schülerversuche zum Thema Fällungsreaktionen
Schulversuchspraktikum. Sommersemester 2014 Klassenstufen 7 & 8. Reaktionen von Metallen mit Sauerstoff und mit Luft.
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum. Olga Streck. Sommersemester Klassenstufen 5 & 6. Papier
 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 5 & 6 Papier 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 enthält 2 Lehrerversuche und 2 Schülerversuche zum Thema
Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 5 & 6 Papier 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 enthält 2 Lehrerversuche und 2 Schülerversuche zum Thema
Erdöl. "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in. keiner Weise verwendet werden kann.
 Erdöl "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in keiner Weise verwendet werden kann." ('Akademie der Wissenschaften' in St. Petersburg 1806) Erdöl, schwarzes
Erdöl "... ist eine nutzlose Absonderung der Erde eine klebrige Flüssigkeit, die stinkt und in keiner Weise verwendet werden kann." ('Akademie der Wissenschaften' in St. Petersburg 1806) Erdöl, schwarzes
Thema: Die Luftbatterie
 Klasse: 9/10 Name: Datum: Thema: Die Luftbatterie Gefahrenstoffe Natriumchlorid - - Materialien: Graphit-Elektrode, Aluminium-Folie, Küchenpapier oder Handpapier, Pipette Chemikalien: Durchführung: Natriumchlorid-Lösung
Klasse: 9/10 Name: Datum: Thema: Die Luftbatterie Gefahrenstoffe Natriumchlorid - - Materialien: Graphit-Elektrode, Aluminium-Folie, Küchenpapier oder Handpapier, Pipette Chemikalien: Durchführung: Natriumchlorid-Lösung
Schulversuchspraktikum. Sommersemester Klassenstufen 5 & 6. Feuer und Kerzen
 Schulversuchspraktikum Sommersemester 2013 Klassenstufen 5 & 6 Feuer und Kerzen Text zuzuweisen, der hier Fehler! Verwenden Sie 2 Auf einen Blick: In diesem Protokoll werden sechs Versuche dargestellt,
Schulversuchspraktikum Sommersemester 2013 Klassenstufen 5 & 6 Feuer und Kerzen Text zuzuweisen, der hier Fehler! Verwenden Sie 2 Auf einen Blick: In diesem Protokoll werden sechs Versuche dargestellt,
Die SuS erklären die Entstehung saurer Lösungen mit dem Konzept von Arrhenius als Dissoziation von Chlorwasserstoff zu Hydoniumionen und
 1 Arbeitsblatt Das Arbeitsblatt dient der Protokollierung und der Auswertung des Lehrerversuches V1. Während die Versuchsdurchführung und Versuchbeobachtung wenig strukturiert sind, da die SuS über diese
1 Arbeitsblatt Das Arbeitsblatt dient der Protokollierung und der Auswertung des Lehrerversuches V1. Während die Versuchsdurchführung und Versuchbeobachtung wenig strukturiert sind, da die SuS über diese
Schuleigener Lehrplan Chemie (Grundlage: KLP 2008) Klasse 9. Schuleigener Lehrplan. Chemie - Klasse 9 -
 Schuleigener Lehrplan Chemie - Klasse 9 - 9 Saure und alkalische Lösungen Ionen in sauren und alkalischen Lösungen Neutralisation Protonenaufnahme und Abgabe an einfachen Beispielen Stöchiometrische Berechnungen
Schuleigener Lehrplan Chemie - Klasse 9 - 9 Saure und alkalische Lösungen Ionen in sauren und alkalischen Lösungen Neutralisation Protonenaufnahme und Abgabe an einfachen Beispielen Stöchiometrische Berechnungen
Heinrich-Böll-Gesamtschule SILP Chemie Jahrgang 10
 Inhaltsfeld: Säuren und Basen Inhaltliche Schwerpunkte Mögliche Kontexte Basiskonzepte Eigenschaften saurer und alkalischer Lösungen Neutralisation Eigenschaften von Salzen Kompetenzen Fachwissen Erkenntnisgewinnung
Inhaltsfeld: Säuren und Basen Inhaltliche Schwerpunkte Mögliche Kontexte Basiskonzepte Eigenschaften saurer und alkalischer Lösungen Neutralisation Eigenschaften von Salzen Kompetenzen Fachwissen Erkenntnisgewinnung
Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad
 Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele
Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele
Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden?
 Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden? Beschrifte die Kästchen mit je einem Aggregatzustand. Benenne die Nummern, es handelt sich dabei um Fachbegriffe für die Übergänge
Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden? Beschrifte die Kästchen mit je einem Aggregatzustand. Benenne die Nummern, es handelt sich dabei um Fachbegriffe für die Übergänge
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 11 & 12. Katalyse
 Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 11 & 12 Katalyse 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 11 & 12 Katalyse 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Anhand welcher Eigenschaften lässt sich Sauerstoff identifizieren?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75400) 5. Nachweis von Sauerstoff Experiment von: Phywe Gedruckt:.0.203 3:00:4 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Allgemeine Chemie - 5 Nachweisreaktionen (P75400) 5. Nachweis von Sauerstoff Experiment von: Phywe Gedruckt:.0.203 3:00:4 intertess (Version 3.06 B200, Export 2000) Aufgabe
Siede- und Schmelztemperatur
 Schulversuchspraktikum Name: Anna Elisabeth Gulyas Semester: Sommersemester 2013 Klassenstufen 5 & 6 Siede- und Schmelztemperatur Auf einen Blick: In dieser Unterrichtseinheit lernen die SuS Siede- und
Schulversuchspraktikum Name: Anna Elisabeth Gulyas Semester: Sommersemester 2013 Klassenstufen 5 & 6 Siede- und Schmelztemperatur Auf einen Blick: In dieser Unterrichtseinheit lernen die SuS Siede- und
Schulversuchspraktikum. Johanna Schakowske Sommersemester 2013 Klassenstufen 7 & 8. Aktivierungsenergie
 Schulversuchspraktikum Johanna Schakowske Sommersemester 2013 Klassenstufen 7 & 8 Aktivierungsenergie 1 Konzept und Ziele 1 Auf einen Blick: In diesem Protokoll sind SuS- uns LuL-Versuche aufgeführt, die
Schulversuchspraktikum Johanna Schakowske Sommersemester 2013 Klassenstufen 7 & 8 Aktivierungsenergie 1 Konzept und Ziele 1 Auf einen Blick: In diesem Protokoll sind SuS- uns LuL-Versuche aufgeführt, die
Schulversuchspraktikum. Denise Heckmann. Sommersemester Klassenstufen 7&8. Stickstoff
 Schulversuchspraktikum Denise Heckmann Sommersemester 2013 Klassenstufen 7&8 Stickstoff 1 Auf einen Blick: In diesem Protokoll wird das Element Stickstoff als Hauptbestandteil der Luft eingeführt. Hierzu
Schulversuchspraktikum Denise Heckmann Sommersemester 2013 Klassenstufen 7&8 Stickstoff 1 Auf einen Blick: In diesem Protokoll wird das Element Stickstoff als Hauptbestandteil der Luft eingeführt. Hierzu
,Prinzip: Versuchsaufbau - Variante I: Materialliste:
 Computer im Chemieunterricht Gaschromatographische Identifizierung Chromatogr.,Prinzip: Einige Kohlenwasserstoffe werden aus Carbiden im Minigasentwickler hergestellt. Weitere Kohlenwasserstoffe lassen
Computer im Chemieunterricht Gaschromatographische Identifizierung Chromatogr.,Prinzip: Einige Kohlenwasserstoffe werden aus Carbiden im Minigasentwickler hergestellt. Weitere Kohlenwasserstoffe lassen
4.1 Vergleich von physikalischem Vorgang und chemischer Reaktion. Aufgabe. Woran lassen sich chemische Reaktionen erkennen? (1)
 Naturwissenschaften - Chemie - Allgemeine Chemie - 4 Chemische Reaktionen (P75200) 4. Vergleich von physikalischem Vorgang und chemischer Reaktion Experiment von: Phywe Gedruckt:.0.203 2:58:37 intertess
Naturwissenschaften - Chemie - Allgemeine Chemie - 4 Chemische Reaktionen (P75200) 4. Vergleich von physikalischem Vorgang und chemischer Reaktion Experiment von: Phywe Gedruckt:.0.203 2:58:37 intertess
