20. Sofortkühlkompressen eine Verknüpfung von Löseprozess und Energetik. Sofortkühlkompressen eine Verknüpfung von Löseprozess und Energetik
|
|
|
- Anton Knopp
- vor 6 Jahren
- Abrufe
Transkript
1 1 von 22 Sofortkühlkompressen eine Verknüpfung von Löseprozess und Energetik Dr. Marc Stuckey, Wilhelmshaven Niveau: Sek. I/II Klassenstufe 9, 10 und 11 Dauer: 4 Unterrichtsstunden Kompetenzen: Die Schülerinnen und Schüler können anhand des Kontextes Sofortkühlkompressen den Löseprozess von Salz in Wasser auf Teilchenebene erklären und den energetischen Verlauf beschreiben einen modellhaften Ablauf des Lösevorgangs von Salz in Wasser entwickeln die Funktionalität eines einfachen Anschauungsmodells erkennen in Teamarbeit eigenständig Experimente planen, durchführen und auswerten Experimente und ihre Erkenntnisse in angemessener Fachsprache präsentieren Der Beitrag enthält Materialien für: Offene Unterrichtsformen Gruppenarbeit Schülerversuche Differenzierungsmöglichkeiten Hintergrundinformationen Bei Verstauchungen oder Prellungen bietet es sich an, die verletzte Stelle zu kühlen, damit sich die Blutgefäße zusammenziehen und mögliche Schwellungen sowie Entzündungsreaktionen gehemmt werden. Hierfür bieten sich Sofortkühlkompressen an, in denen i. d. R. ein Salz (z. B. Ammoniumchlorid) oder Harnstoff und Wasser räumlich getrennt vorliegen. Durch kräftiges Schütteln und Drücken wird die Trennwand aufgebrochen, wodurch sich das Salz im Wasser löst und die Kühlung erfolgt. Vorteilhaft an den Kompressen ist der mobile Einsatz, da das Kühlen durch den Löseprozess hervorgerufen wird. Nachteilig ist, dass die Sofortkühlkompressen nur einmalig einsetzbar sind. Hinweise zur Didaktik und Methodik Generell ist den Schülern der Löseprozess von Salzen und anderen Stoffen wie Zucker in Wasser aus dem Alltag bekannt jedoch oft nur auf Stoff- und nicht auf Teilchenebene. Im vorliegenden Beitrag ist das Hauptaugenmerk darauf gelegt, dass die Schüler den Löseprozess auf Teilchenebene verstehen, um anschließend energetische Aspekte besser nachvollziehen zu können. Hierbei werden Kenntnisse über Wasser und Salze auf einen aus dem Alltag entnommenen Kontext übertragen und angewendet. In der neuen Fassung des Niedersächsischen Kerncurriculums für das Gymnasium für die naturwissenschaftlichen Fächer heißt es im Basiskonzept Struktur-Eigenschaft, dass die Schüler die Löslichkeit von Salzen erklären und aus energetischer Sicht mithilfe der Gitter- und Hydratationsenergie beschreiben können (Niedersächsisches Kerncurriculum, 2015). Stoffeigenschaften, wie z. B. Löslichkeit, sollen anhand des Bindungstyps bzw. der zwischenmolekularen Wechselwirkungen mit den passenden Modellen unter Anwendung der Fachsprache erklärt werden (KMK, 2005; z. B. Niedersächsisches Kerncurriculum, 2012). * Im weiteren Verlauf wird aus Gründen der einfacheren Lesbarkeit nur Schüler verwendet. Schülerinnen sind genauso gemeint.
2 2 von Sofortkühlkompressen eine Verknüpfung von Löseprozess und Energetik Auch in den Abiturprüfungen im Fach Chemie wurde das Thema Sofortkühlkompressen bereits vorgeschlagen. Um die Funktionsweise einer Sofortkühlkompresse beschreiben zu können, müssen die Schüler auf Stoff-Teilchen-Ebene zwischen Ionen, Dipolmolekülen und unpolaren Molekülen unterscheiden können. Der vorliegende Beitrag zum Thema Sofortkühlkompressen greift sowohl den Löseprozess als auch die Energetik auf. Um die Schüler der Mittelstufe inhaltlich nicht zu überfrachten, wurde der Themenbereich der Energetik bewusst vereinfacht. Durchführung Der Stundeneinstieg erfolgt im Plenum: Als erster Impuls wird den Schülern eine Originalsofortkühlpackung oder Folie M 1 gezeigt. Dieser Impuls soll die Schüler aktivieren, ihre Kenntnisse zu Sofortkühlkompressen im Unterrichtsgespräch zu formulieren. Einige Schüler kennen die Kompressen bereits aus dem Sportbereich oder dem Vereinssport. Anschließend werden Sofortkühlkompressen innerhalb der Tischreihen ausgeteilt und die Schüler untersuchen die Verpackungshinweise nach Inhaltsstoffen. Auf den Verpackungen ist jedoch nicht etikettiert, welche Stoffe enthalten sind. In der Erarbeitungsphase teilen sich die Schüler in 8 Gruppen zu jeweils 4 Schülern auf. Jeweils 2 Gruppen bearbeiten die gleiche Station. Für jede Station stehen zwei Materialkästen zur Verfügung. Um die Funktionsweise der Sofortkühlkompressen klären zu können, werden folgende Fragen (M 2 M 5) untersucht: Gruppe A/B: Station 1 (M 2): Welche Stoffe sind in den Sofortkühlkompressen enthalten? Wie lässt sich nachweisen, dass es sich um Wasser und Salz handelt? Gruppe C/D: Station 2 (M 3): Welche Vorgänge spielen sich auf Teilchenebene ab, wenn sich ein Salz in Wasser löst? Gruppe E/F: Station 3 (M 4): Wird die Lösung immer kalt, wenn sich ein Salz in Wasser löst? Gruppe G/H: Station 4 (M 5): Lösen sich Salze auch in anderen Flüssigkeiten? Für die Präsentationsphase wählen die Schüler ein Präsentationsmedium (Active board, Dokumentenkamera, Plakate etc.). Die Sicherung erfolgt über kurze Schülervorträge. Aus Zeitgründen bietet es sich an, immer nur eine Tischgruppe vorstellen zu lassen, während die andere Gruppe mit dem gleichen Versuch anschließend Ergänzungen vornehmen kann. Zur Sicherung der erarbeiteten Ergebnisse bekommen alle Schüler das Arbeitsblatt (M 6) ausgehändigt. Steht mehr Zeit zur Verfügung, wäre auch die Methodik des Gruppenpuzzles als Sicherungsmethode einsetzbar. Differenzierung Es kann folgendermaßen differenziert werden: M 2 eignet sich besonders für Schüler, die im Fach Chemie große Unsicherheiten haben. Für die Bestätigungsexperimente des Wasser- und Salznachweises können diese Schüler zum Teil auf Erkenntnisse und Versuche zurückgreifen, die bereits im Rahmen der Einheiten Wasser und Salze durchgeführt wurden. Auch die Versuche in M 5 können Schüler mit Lernschwierigkeiten bearbeiten. Leistungsstärkere Schüler sollten hingegen die Modellvorlagen M 3b nutzen und das Anwenden der Fachsprache weiter einüben. Auch bietet es sich an, die Präsentation am Computer erfolgen zu lassen, wo die Teilchen verschoben werden können (z. B. mit ActivInspire). Auch M 4 und M 4a eignen sich für Schüler, die im Fach Chemie großes Interesse und viele Vorkenntnisse zeigen. Je nach Lerngruppe können die Durchführungen stets mit angegeben werden. Bei den einfacheren Versuchen, wie in M 2a, wurden diese bewusst weggelassen, um die Schülerinnen und Schüler ausprobieren zu lassen.
3 5 von 22 Materialübersicht für die jeweiligen Gruppen V = Vorbereitungszeit SV = Schülerversuch AB = Arbeitsblatt/Informationsblatt D = Durchführungszeit LV = Lehrerversuch Fo = Folie M 1 Fo Sofortkühlkompressen was ist drin? M 2a SV (Station 1) M 2b Ab M 2c SV V: 5 min D: 25 min V: 5 min D: 25 min Nachweis von Salz und Wasser Inhalt der aufgeschnittenen Kühlkompresse der Firma Frosti Fix wasserfreies Kupfersulfat Universalindikator dest. Wasser Hilfekarten Nachweis von Harnstoff Inhalt der aufgeschnittenen Kühlkompresse 10%ige Kupfer(II)-sulfatpentahydrat-Lösung Schere Einweghandschuhe Leitfähigkeitsprüfer Stromquelle 1 Becherglas (25 ml) Spatel Gasbrenner Reagenzglasklammer Reagenzglas (Duran) M 3a Ab (Station 2) M 3b Ab M 3c Ab M 4a SV (Station 3) M 4b Ab V: 5 min D: 25 min 10%ige Natronlauge dest. Wasser Der Lösevorgang Modellvorlagen Hilfekarten Der Kühlungseffekt Calciumchlorid Ammoniumchlorid Kochsalz (Natriumchlorid) dest. Wasser Hilfekarten Schere Einweghandschuhe 1 Becherglas (25 ml) 1 Löffel 1 Glasstab 1 Gasbrenner 1 Reagenzglasklammer 1 Reagenzglas (Duran) Pipette Molekülpappstücke Waage Uhrglas 3 Bechergläser (50 ml) Glasstab Thermometer
4 6 von Sofortkühlkompressen eine Verknüpfung von Löseprozess und Energetik M 5 SV (Station 4) Alternative Lösemittel V: 5 min D: 25 min Salz aus der Kühlkompresse Wasser Sonnenblumenöl Tafelessig oder verdünnte Essigsäure verdünnte Natronlauge Waage Uhrglas Spatel 4 Bechergläser (50 ml) Glasstab Thermometer M 6 Ab Gesamtauswertung zu den Untersuchungen Minimalplan Ihnen steht nur wenig Zeit zur Verfügung? Dann lässt sich die Unterrichtseinheit auf zwei Stunden kürzen. Die Planung sieht dann wie folgt aus: 1./2. Stunde (M 1 M 6) Die Lehrperson zeigt Sofortkühlkompresse, um Vorkenntnisse der Schüler zu aktivieren. Sollten die Schüler die Inhaltsstoffe der Sofortkühlkompresse nicht kennen, dann schneiden sie die Verpackung auf. Die Schüler teilen sich auf 4 Stationen auf (siehe M 2 M 5) und erarbeiten sich mithilfe von vorbereiteten Materialkästen die Fragestellungen. Es stehen außerdem Hilfekarten und Vertiefungsmaterialien zur Verfügung. Die Schüler bereiten ihre Präsentation vor und sprechen sich ab, wer vorstellen wird, und stellen ihre Ergebnisse vor. Als Stundenzusammenfassung dient M 6. Die Erläuterungen und Lösungen zu den Materialien inden Sie ab Seite 18.
5 9 von 22 M 2b Hilfekarten Hilfekarte 1: Nachweis von Wasser Um Wasser nachzuweisen, gibt man entweder wasserfreies Kupfersulfat oder Universalindikator zu der zu untersuchenden Flüssigkeit. Das wasserfreie Kupfersulfat färbt sich mit Wasser tiefblau. Der Universalindikator zeigt in Wasser eine gelb/ grüne Färbung (neutrale Lösung) an. Hilfekarte 2: Nachweis von Ionenverbindungen (Salzen) Um Ionen in Salzen nachzuweisen, untersucht man entweder eine wässrige Lösung des Salzes oder aber eine Salzschmelze auf ihre elektrische Leitfähigkeit. Hilfekarte 2a: Nachweis von Ionenverbindungen in einer Salzlösung Hilfekarte 2b: Nachweis von Ionenverbindungen in einer Salzschmelze Um Ionen in Salzen nachzuweisen, erhitzt man das Salz so lange, bis das Salz schmilzt, und prüft die Schmelze mithilfe des Leitfähigkeitsprüfers auf elektrische Leitfähigkeit.
6 11 von 22 M 3a Der Lösevorgang Welche Vorgänge spielen sich auf Teilchenebene ab, wenn sich ein Salz in Wasser löst? Aufgaben 1. Skizziert in die Filmleiste den Lösevorgang von Kochsalz (Natriumchlorid) in Wasser. Geht dabei auf die Anordnung der Ionen und Wassermoleküle ein. Um die Vorgänge darzustellen, können euch die Modellvorlagen (M 3b) helfen. Erklärung zu Bild 1: Erklärung zu Bild 2: Erklärung zu Bild 3: 2. Beschreibt in eurem Heft unter Verwendung der Fachsprache den Lösevorgang von Kochsalz in Wasser. Verwendet folgende Begriffe: Ionengitter, Wassermoleküle, Anionen, Kationen, Ionenbindung, positive/negative Teilladung. Die Hilfekarten (M 3c) können euch Tipps geben.
7 12 von Sofortkühlkompressen eine Verknüpfung von Löseprozess und Energetik M 3b Modellvorlagen Wassermolekül Wassermolekül Wassermolekül Natrium-Ion Natrium-Ion Natrium-Ion Natrium-Ion Natrium-Ion Chlorid-Ion Chlorid-Ion Chlorid-Ion
8 13 von 22 M 3c Hilfekarten Hilfekarte 1 Zeichnet einen kleinen Ausschnitt des Ionengitters von Kochsalz. Zeichnet anschließend einige Wasserdipolmoleküle. Hilfekarte 2 Markiert auf dieser Vorlage die Anionen, Kationen und Wasserdipole. Hilfekarte 3 Beantwortet folgende Fragen mithilfe von Hilfekarte 2: a) Welche Vorgänge spielen sich ab, wenn sich die Wasserdipole an das Ionengitter anlagern? b) An welchen Stellen finden diese Vorgänge bevorzugt statt? Hilfekarte 4 Zeichnet ein Kation und ein Anion mit Hydrathülle. Achtet dabei auf die Orientierung der Wasserdipole.
9 14 von Sofortkühlkompressen eine Verknüpfung von Löseprozess und Energetik M 4a Der Kühlungseffekt Kommt es zu Prellungen oder Gelenkschmerzen bei einem Sportunfall, so sollte man die verletzte Stelle möglichst sofort mit Eis oder einer Kühlkompresse kühlen. Bei welchen Ionenverbindungen tritt ein Kühlungseffekt ein, bei welchen nicht? Schülerversuch: Verschiedene Salze (Ionenverbindungen) in Wasser lösen Vorbereitung: 5 min Durchführung: 25 min Chemikalien / Gefahrenhinweise Geräte Calciumchlorid Waage Ammoniumchlorid Uhrglas Kochsalz (Natriumchlorid) 3 Bechergläser (50 ml) dest. Wasser Glasstab Thermometer Entsorgung: Die Lösungen können in den Ausguss gegeben werden. Versuchsdurchführung Wiegt 4 g Calciumchlorid auf einem Filterpapier ab. Füllt in ein Becherglas 25 ml destilliertes Wasser und gebt das Calciumchlorid hinzu. Misst die Temperatur zwei bis vier Minuten lang alle 30 Sekunden. Dabei mit dem Glasstab rühren. Notiert die Werte in eurem Protokoll. Wiederholt den Versuch einmal mit 4 g Natriumchlorid, das zweite Mal mit 4 g Ammoniumchlorid. Aufgaben 1. Protokolliert eure Versuchsbeobachtungen. 2. Erklärt den Kühlungseffekt beim Lösen des Kristallgitters und der Hydratation mithilfe der energetischen Vorgänge. Die unten stehende Abbildung und die Hilfekarten M 4b können euch Tipps geben. 3. Zusatzfrage: Nehmt das Periodensystem zu Hilfe und überlegt, von welchen Faktoren die Stärke der Hydratation abhängen könnte.
VORANSICHT. Zaubern mit Wasserstoffbrücken oder: Warum sich Wasser so verrückt verhält. Hintergrundinformationen. Ann-Kathrin Wolf, Oldenburg
 Zaubern mit stoffbrücken oder: Warum sich so verrückt verhält Ann-Kathrin Wolf, Oldenburg Niveau: Sek. I, Klasse 10 Dauer: 4 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards Fachwissen: Die Schülerinnen
Zaubern mit stoffbrücken oder: Warum sich so verrückt verhält Ann-Kathrin Wolf, Oldenburg Niveau: Sek. I, Klasse 10 Dauer: 4 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards Fachwissen: Die Schülerinnen
Salze genauer betrachtet die Ionenbindung
 1 von 26 Salze genauer betrachtet die Ionenbindung Sandra Kaut, Hamburg Salze gehören zu unserem Alltag. So begegnet uns Kochsalz jeden Tag in unserem Essen manchmal sichtbar, wie auf Brezeln, meistens
1 von 26 Salze genauer betrachtet die Ionenbindung Sandra Kaut, Hamburg Salze gehören zu unserem Alltag. So begegnet uns Kochsalz jeden Tag in unserem Essen manchmal sichtbar, wie auf Brezeln, meistens
Fachcurriculum Chemie Jahrgang 10 ab 2017/18 (ASG-Zugang 15/16)
 Fachcurriculum Chemie Jahrgang 10 ab 2017/18 (ASG-Zugang 15/16) Ganzjähriger Unterricht 2-stündig Unterthemen Inhaltsbezogene Kompetenzen (FW) Prozessbezogene Kompetenzen (EG, KK, BW) Bemerkungen Salze,
Fachcurriculum Chemie Jahrgang 10 ab 2017/18 (ASG-Zugang 15/16) Ganzjähriger Unterricht 2-stündig Unterthemen Inhaltsbezogene Kompetenzen (FW) Prozessbezogene Kompetenzen (EG, KK, BW) Bemerkungen Salze,
Schulversuchspraktikum. Isabel Böselt. Sommersemester Klassenstufen 5 & 6. Aggregatzustände. und deren Temperaturabhängigkeit
 Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden einfache
Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden einfache
Schulversuchspraktikum. Constanze Koch. Sommersemester Klassenstufen 5 & 6. Wasser als Lösungsmittel. Kurzprotokoll
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Schuleigener Arbeitsplan für das Fach Chemie (vorläufige Fassung, gültig ab Schuljahr 2008/09)
 Laurentius-Siemer-Gymnasium Saterland Schuleigener Arbeitsplan für das Fach Chemie (vorläufige Fassung, gültig ab Schuljahr 2008/09) Jahrgangsstufe: 9 Lehrwerke / Hilfsmittel: Elemente Chemie 1, Klett
Laurentius-Siemer-Gymnasium Saterland Schuleigener Arbeitsplan für das Fach Chemie (vorläufige Fassung, gültig ab Schuljahr 2008/09) Jahrgangsstufe: 9 Lehrwerke / Hilfsmittel: Elemente Chemie 1, Klett
Schulversuchspraktikum. Name: Jennifer Kölling. Sommersemester: Klassenstufen: 9/10. Salze
 Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 9/10 Salze 1 Schulversuchspraktikum 1 Auf einen Blick:. Die Thematik der Salze ist sehr umfangreich. Die hier dargestellten
Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 9/10 Salze 1 Schulversuchspraktikum 1 Auf einen Blick:. Die Thematik der Salze ist sehr umfangreich. Die hier dargestellten
Gruppenarbeit physikalische und chemische Eigenschaften von Alkansäuren
 Gruppenarbeit Gruppe 1: Siedetemperaturen von Alkansäuren Löst die gestellten Aufgaben in eurer Gruppe. Ihr habt dafür 20 Minuten Zeit. Tragt die Ergebnisse in die Folie ein. Wählt eine Gruppensprecherin
Gruppenarbeit Gruppe 1: Siedetemperaturen von Alkansäuren Löst die gestellten Aufgaben in eurer Gruppe. Ihr habt dafür 20 Minuten Zeit. Tragt die Ergebnisse in die Folie ein. Wählt eine Gruppensprecherin
Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser?
 http://www.kostenloseausmalbilder.de/media/.gallery/main606.jpg (02.08.2015) Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser? Pip, die kleine Maus, benötigt zum Atmen Luft, vor allem den Sauerstoff,
http://www.kostenloseausmalbilder.de/media/.gallery/main606.jpg (02.08.2015) Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser? Pip, die kleine Maus, benötigt zum Atmen Luft, vor allem den Sauerstoff,
PÄDAGOGISCHES LANDESINSTITUT VIER VERSUCHE FÜR DEN CHEMIEUNTERRICHT AB SEKUNDARSTUFE I
 PÄDAGOGISCHES LANDESINSTITUT VIER VERSUCHE FÜR DEN CHEMIEUNTERRICHT AB SEKUNDARSTUFE I Passend zu den Versuchsanleitungen sind Videoaufnahmen im Rahmen eines Weiterbildungslehrgangs des Pädagogischen Landesinstituts
PÄDAGOGISCHES LANDESINSTITUT VIER VERSUCHE FÜR DEN CHEMIEUNTERRICHT AB SEKUNDARSTUFE I Passend zu den Versuchsanleitungen sind Videoaufnahmen im Rahmen eines Weiterbildungslehrgangs des Pädagogischen Landesinstituts
9. Schwefelsäure und ihre Salze (Kl. 9/10) Ein saurer Alleskönner Eigenschaften und Verwendung von Schwefelsäure und ihren Salzen
 1 von 28 Ein saurer Alleskönner Eigenschaften und Verwendung von und ihren Salzen Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Wolfgang Zettlmeier, Barbing Mit einer Jahresproduktion
1 von 28 Ein saurer Alleskönner Eigenschaften und Verwendung von und ihren Salzen Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Wolfgang Zettlmeier, Barbing Mit einer Jahresproduktion
Kernaussagen zum Teilchenmodell
 Kernaussagen zum Teilchenmodell Lernbereich 2: Stoffe und ihre Eigenschaften Von beobachtbaren Stoffeigenschaften zum Teilchenmodell Kompetenzerwartung 8 (NTG) und 9 (SG): Die Schülerinnen und Schüler
Kernaussagen zum Teilchenmodell Lernbereich 2: Stoffe und ihre Eigenschaften Von beobachtbaren Stoffeigenschaften zum Teilchenmodell Kompetenzerwartung 8 (NTG) und 9 (SG): Die Schülerinnen und Schüler
Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer
 Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer chemischen Reaktion? In der letzten Chemiestunde hast du eine Hypothese zu der Frage formuliert: Verändert sich die Masse von
Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer chemischen Reaktion? In der letzten Chemiestunde hast du eine Hypothese zu der Frage formuliert: Verändert sich die Masse von
VORANSICHT I/B. Der Hebel ein fundamentales Werkzeug. Ohne Hebel läuft im Alltag nichts! Der Beitrag im Überblick
 28. Der Hebel ein fundamentales Werkzeug 1 von 16 Der Hebel ein fundamentales Werkzeug Jost Baum, Wuppertal Haben Sie sich schon einmal Gedanken darüber gemacht, wie oft am Tag Sie einen Hebel benutzen?
28. Der Hebel ein fundamentales Werkzeug 1 von 16 Der Hebel ein fundamentales Werkzeug Jost Baum, Wuppertal Haben Sie sich schon einmal Gedanken darüber gemacht, wie oft am Tag Sie einen Hebel benutzen?
Vitamine unter der chemischen Lupe Die Löslichkeitseigenschaft von Vitaminen im kompetenzorientierten Unterricht
 21. Vitamine unter der chemischen Lupe 1 von 14 Vitamine unter der chemischen Lupe Die Löslichkeitseigenschaft von Vitaminen im kompetenzorientierten Unterricht Sylvia Pross, Marburg Niveau: Sek. II Dauer:
21. Vitamine unter der chemischen Lupe 1 von 14 Vitamine unter der chemischen Lupe Die Löslichkeitseigenschaft von Vitaminen im kompetenzorientierten Unterricht Sylvia Pross, Marburg Niveau: Sek. II Dauer:
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.de 2 von 18 6. Wir bauen eine Zitronenbatterie (Kl. 9/10) Chemische
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Strom aus Obst? Das komplette Material finden Sie hier: School-Scout.de 2 von 18 6. Wir bauen eine Zitronenbatterie (Kl. 9/10) Chemische
VORANSICHT. Offene Unterrichtsformen (2-4-Alle-Methode) Schülerarbeitsblätter Lernerfolgskontrolle
 Der Louche-Effekt zum Struktur-Eigenschafts-Konzept mit der 2-4-Alle-Methode Torsten Witteck, Bielefeld Niveau: Dauer: Sek. II 2 3 Stunden Bezug zu den KMK-Bildungsstandards Heinz Wambach, Köln Fachwissen:
Der Louche-Effekt zum Struktur-Eigenschafts-Konzept mit der 2-4-Alle-Methode Torsten Witteck, Bielefeld Niveau: Dauer: Sek. II 2 3 Stunden Bezug zu den KMK-Bildungsstandards Heinz Wambach, Köln Fachwissen:
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Was blubbert da im Wasserglas? (als veränderbare PDF- Datei)
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Was blubbert da im Wasserglas? (als veränderbare PDF- Datei) Das komplette Material finden Sie hier: School-Scout.de 11. Was blubbert
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Was blubbert da im Wasserglas? (als veränderbare PDF- Datei) Das komplette Material finden Sie hier: School-Scout.de 11. Was blubbert
Wie wirkt sich die Zugabe von Salz auf den Schmelz- und Siedepunkt von Wasser aus?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Mische einige Stoffe mit Wasser und untersuche die entstandenen Gemischarten.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Fluoreszierende Verbindungen
 Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Projekt- Nachweisreaktionen. Dieses Skript gehört: NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz
 Projekt- Nachweisreaktionen NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz Dieses Skript gehört: 1 Nachweise von Anionen 1. Nachweis von Sulfat 3 Reagenzgläser im Reagenzglasständer
Projekt- Nachweisreaktionen NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz Dieses Skript gehört: 1 Nachweise von Anionen 1. Nachweis von Sulfat 3 Reagenzgläser im Reagenzglasständer
Glucose: Von den Stoffeigenschaften zur chemischen Formel
 Glucose: Von den Stoffeigenschaften zur chemischen Formel Dr. Hans-Peter Haseloff Niveau: Sek. II Dauer: 2 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards Fachwissen: Durch einfache Versuche werden
Glucose: Von den Stoffeigenschaften zur chemischen Formel Dr. Hans-Peter Haseloff Niveau: Sek. II Dauer: 2 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards Fachwissen: Durch einfache Versuche werden
Was haben Säuren und Laugen mit Körperpflege zu tun? Ein Lernzirkel
 Stoffe im Alltag Beitrag 10 Säuren und Laugen (Klassen 7/8) 1 von 30 Was haben Säuren und Laugen mit Körperpflege zu tun? Ein Lernzirkel Ein Beitrag von Nicola Patricia Budau, LIS Bremen und Silvija Markic,
Stoffe im Alltag Beitrag 10 Säuren und Laugen (Klassen 7/8) 1 von 30 Was haben Säuren und Laugen mit Körperpflege zu tun? Ein Lernzirkel Ein Beitrag von Nicola Patricia Budau, LIS Bremen und Silvija Markic,
Wir untersuchen Mineralwasser
 Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll
Glucose: Von den Stoffeigenschaften zur chemischen Formel
 24. Glucose: Von den Stoffeigenschaften zur chemischen Formel 1 von 14 Glucose: Von den Stoffeigenschaften zur chemischen Formel Dr. Hans-Peter Haseloff Niveau: Sek. II Dauer: 2 Unterrichtsstunden Bezug
24. Glucose: Von den Stoffeigenschaften zur chemischen Formel 1 von 14 Glucose: Von den Stoffeigenschaften zur chemischen Formel Dr. Hans-Peter Haseloff Niveau: Sek. II Dauer: 2 Unterrichtsstunden Bezug
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Aggregatzustände und deren Temperaturabhängigkeit
 Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Versuchsprotokoll: Ampel-Bottle - Experiment
 Versuchsprotokoll: Ampel-Bottle - Experiment Zeitaufwand: Aufbau: 5 Minuten Durchführung: 1 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Versuchsprotokoll: Ampel-Bottle - Experiment Zeitaufwand: Aufbau: 5 Minuten Durchführung: 1 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Elektrochemie einfach verständlich (PDF-Datei)
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Elektrochemie einfach verständlich (PDF-Datei) Das komplette Material finden Sie hier: School-Scout.de 2 von 28 16. Grundlagen und
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Elektrochemie einfach verständlich (PDF-Datei) Das komplette Material finden Sie hier: School-Scout.de 2 von 28 16. Grundlagen und
Säuren und Basen 8. Titration (Kl. 9/10) Tropfen für Tropfen mit Titration die Konzentration einer Base bestimmen
 1 von 20 Tropfen für Tropfen mit Titration die Konzentration einer Base bestimmen Ein Beitrag von Sandra Kaut, Hamburg Mit Illustrationen von Julia Lenzmann, Stuttgart Oje, der arme Maler-Azubi Tom Er
1 von 20 Tropfen für Tropfen mit Titration die Konzentration einer Base bestimmen Ein Beitrag von Sandra Kaut, Hamburg Mit Illustrationen von Julia Lenzmann, Stuttgart Oje, der arme Maler-Azubi Tom Er
Warum korrodiert Eisen?
 Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Säure-Base-Reaktionen
 Säure-Base-Reaktionen Versuch 1: Wir schmecken Lebensmittel! Material: Kleine Trinkbecher Getränkeproben Füllt von jeder bereitstehenden Probe zunächst etwas in einen Trinkbecher und probiert einen kleinen
Säure-Base-Reaktionen Versuch 1: Wir schmecken Lebensmittel! Material: Kleine Trinkbecher Getränkeproben Füllt von jeder bereitstehenden Probe zunächst etwas in einen Trinkbecher und probiert einen kleinen
Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz
 Name: Datum: Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz Material: Kochsalz (NaCl), Leitungswasser, Mineralwasser, Becherglas, Spatel, destilliertes Wasser, Alu-Teelichtschalen,
Name: Datum: Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz Material: Kochsalz (NaCl), Leitungswasser, Mineralwasser, Becherglas, Spatel, destilliertes Wasser, Alu-Teelichtschalen,
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Was ist was? Identifizierung von Säuren und Basen mit gestuften Hilfen
 1 von 22 Was ist was? Identifizierung von mit gestuften Hilfen Ein Beitrag von Karin Schmidt, Netphen Mit Illustrationen von Julia Lenzmann, Stuttgart Was ist was? In unbeschrifteten Bechergläsern befinden
1 von 22 Was ist was? Identifizierung von mit gestuften Hilfen Ein Beitrag von Karin Schmidt, Netphen Mit Illustrationen von Julia Lenzmann, Stuttgart Was ist was? In unbeschrifteten Bechergläsern befinden
HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser
 HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser DIE ZERDRÜCKTE ALUDOSE LEERE Alu-Getränkedose (1/2 Liter!) Tiegelzange Schüssel mit kaltem Wasser 1. Fülle die leere Getränkedose mit wenig Wasser 2. Stelle die
HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser DIE ZERDRÜCKTE ALUDOSE LEERE Alu-Getränkedose (1/2 Liter!) Tiegelzange Schüssel mit kaltem Wasser 1. Fülle die leere Getränkedose mit wenig Wasser 2. Stelle die
Brenner Streichhölzer Eis
 Versuch 1: Wir erhitzen Eis! Reagenzglas Reagenzglasklammer Reagenzglasständer Brenner Streichhölzer Eis Fülle soviel Eis in das Reagenzglas, dass es zu einem Drittel gefüllt ist. Damit Du Dir beim Erhitzen
Versuch 1: Wir erhitzen Eis! Reagenzglas Reagenzglasklammer Reagenzglasständer Brenner Streichhölzer Eis Fülle soviel Eis in das Reagenzglas, dass es zu einem Drittel gefüllt ist. Damit Du Dir beim Erhitzen
Kontext. Doch wie sieht Salzwasser eigentlich auf der Teilchenebene aus?
 Kontext Wenn ihr schon einmal Urlaub am Meer gemacht habt und im Meer schwimmen gegangen seid, dann kennt ihr es sicherlich: Kaum verschluckt man ein wenig Wasser, schon hat man einen unangenehmen Geschmack
Kontext Wenn ihr schon einmal Urlaub am Meer gemacht habt und im Meer schwimmen gegangen seid, dann kennt ihr es sicherlich: Kaum verschluckt man ein wenig Wasser, schon hat man einen unangenehmen Geschmack
VORANSICHT. Elektrochemie einfach verständlich Teil II: Galvanische Zellen. Hinweise zur Didaktik und Methodik. Kerstin Langer, Kiel
 Elektrochemie einfach verständlich Teil II: Galvanische Zellen Kerstin Langer, Kiel Niveau: Dauer: Sek. II 9 Unterrichtsstunden (Minimalplan: 6 Unterrichtsstunden) Kompetenzen: Die Schüler* nutzen ein
Elektrochemie einfach verständlich Teil II: Galvanische Zellen Kerstin Langer, Kiel Niveau: Dauer: Sek. II 9 Unterrichtsstunden (Minimalplan: 6 Unterrichtsstunden) Kompetenzen: Die Schüler* nutzen ein
Gruppe I : Darstellung und Nachweis von Säuren
 Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Titel: Alltagsstoffe mischen und trennen
 1 Titel: Alltagsstoffe mischen und trennen Kurzbeschreibung: Anhand von Alltagsstoffen aus der Küche können Kinder einfache Erfahrungen zur Stoffeigenschaft, Löslichkeit von Stoffen und Trennverfahren
1 Titel: Alltagsstoffe mischen und trennen Kurzbeschreibung: Anhand von Alltagsstoffen aus der Küche können Kinder einfache Erfahrungen zur Stoffeigenschaft, Löslichkeit von Stoffen und Trennverfahren
Mikrokosmos Vorstellungen von der Welt des Kleinen
 II Stoffe im Alltag Beitrag 2 Mikrokosmos (Klassen 5 7) 1 von 32 Mikrokosmos Vorstellungen von der Welt des Kleinen Ariane Pieta, Leonberg Unterschiedliche Alltagsphänomene können durch einfache Experimente
II Stoffe im Alltag Beitrag 2 Mikrokosmos (Klassen 5 7) 1 von 32 Mikrokosmos Vorstellungen von der Welt des Kleinen Ariane Pieta, Leonberg Unterschiedliche Alltagsphänomene können durch einfache Experimente
VORANSICHT. Erlebnis Natur Böden und Tiere im Ökosystem Wald. Mit Programmvorschlägen. für eine Waldexkursion. Das Wichtigste auf einen Blick
 VIII Ökologie Beitrag 2 Böden und Tiere im Ökosystem Wald (Klasse 7/8) 1 von 26 Erlebnis Natur Böden und Tiere im Ökosystem Wald Christoph Randler, Schriesheim, und Eberhard Hummel, Korntal Der Wald gehört
VIII Ökologie Beitrag 2 Böden und Tiere im Ökosystem Wald (Klasse 7/8) 1 von 26 Erlebnis Natur Böden und Tiere im Ökosystem Wald Christoph Randler, Schriesheim, und Eberhard Hummel, Korntal Der Wald gehört
Robinson braucht Hilfe Stoffeigenschaften experimentell erkunden
 1 von 30 Robinson braucht Hilfe Stoffeigenschaften experimentell erkunden Ira Caspari und Sebastian Reusch, Höhr-Grenzhausen Der schiffbrüchige Robinson indet Vorratssäcke, die gleich aussehende Stoffe
1 von 30 Robinson braucht Hilfe Stoffeigenschaften experimentell erkunden Ira Caspari und Sebastian Reusch, Höhr-Grenzhausen Der schiffbrüchige Robinson indet Vorratssäcke, die gleich aussehende Stoffe
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
1 Feuer 24. Zum Aufwärmen 12 INHALT. Versuche und Material 18 Erarbeitung 20. Startklar? 26. Versuche und Material 28 Erarbeitung 30
 INHALT Zum Aufwärmen 12 FACHMETHODE: Sicher experimentieren im Chemieunterricht 14 FACHMETHODE: Erhitzen mit dem Brenner 16 Stoffe und Stoffeigenschaften Versuche und Material 18 Erarbeitung 20 FACHMETHODE:
INHALT Zum Aufwärmen 12 FACHMETHODE: Sicher experimentieren im Chemieunterricht 14 FACHMETHODE: Erhitzen mit dem Brenner 16 Stoffe und Stoffeigenschaften Versuche und Material 18 Erarbeitung 20 FACHMETHODE:
Schulversuchspraktikum. Name Thomas Polle. Sommersemester Klassenstufen 5 & 6. Feuer und Kerzen
 Schulversuchspraktikum Name Thomas Polle Sommersemester 2015 Klassenstufen 5 & 6 Feuer und Kerzen 2 Auf einen Blick: Es werden je ein Schüler- und Lehrerversuch zum Thema Kerzen und Feuer für den 5. und
Schulversuchspraktikum Name Thomas Polle Sommersemester 2015 Klassenstufen 5 & 6 Feuer und Kerzen 2 Auf einen Blick: Es werden je ein Schüler- und Lehrerversuch zum Thema Kerzen und Feuer für den 5. und
Nach uns die Sintflut?
 Nach uns die Sintflut? Interdisziplinäre Untersuchungen zum Thema Wasser Modul: Analytik Jahrgangsstufe 9 Autor: SEITE 1 Abstract Das experimentelle Arbeiten in den Vordergrund stellen. Mit einem Portfolio
Nach uns die Sintflut? Interdisziplinäre Untersuchungen zum Thema Wasser Modul: Analytik Jahrgangsstufe 9 Autor: SEITE 1 Abstract Das experimentelle Arbeiten in den Vordergrund stellen. Mit einem Portfolio
Harnstoffspaltung durch Urease
 Martin Raiber Chemie Protokoll Nr.5 Harnstoffspaltung durch Urease Versuch 1: Materialien: Reagenzglasgestell, Reagenzgläser, Saugpipetten, 100 ml-becherglas mit Eiswasser, 100 ml-becherglas mit Wasser
Martin Raiber Chemie Protokoll Nr.5 Harnstoffspaltung durch Urease Versuch 1: Materialien: Reagenzglasgestell, Reagenzgläser, Saugpipetten, 100 ml-becherglas mit Eiswasser, 100 ml-becherglas mit Wasser
Ampelabfrage: Unterrichtseinstieg oder -abschluss in der Sek. I
 1 von 20 Ampelabfrage: Unterrichtseinstieg oder -abschluss in der Sek. I Sandra Kaut, Hamburg Niveau: Dauer: Sek. I 1 Unterrichtsstunde pro Thema Bezug zu den KMK-Bildungsstandards Fachwissen: Säure-Base/Ionenbindung
1 von 20 Ampelabfrage: Unterrichtseinstieg oder -abschluss in der Sek. I Sandra Kaut, Hamburg Niveau: Dauer: Sek. I 1 Unterrichtsstunde pro Thema Bezug zu den KMK-Bildungsstandards Fachwissen: Säure-Base/Ionenbindung
9.2 Augensummen beim Würfeln mit zwei Würfeln
 9.2 Augensummen beim Würfeln mit zwei Würfeln Thema der Unterrichtsstunde Augensummen beim Würfeln Beschreibung der Lerngruppe Die Klasse 6 setzt sich aus 9 Schülerinnen und 2 Schülern (im Folgenden kurz
9.2 Augensummen beim Würfeln mit zwei Würfeln Thema der Unterrichtsstunde Augensummen beim Würfeln Beschreibung der Lerngruppe Die Klasse 6 setzt sich aus 9 Schülerinnen und 2 Schülern (im Folgenden kurz
Schulversuchspraktikum. Anna Hille. Sommersemester 2013. Klassenstufen 9 & 10. Salz und Salzbildung
 Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 9 & 10 Salz und Salzbildung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll enthält verschiedene
Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 9 & 10 Salz und Salzbildung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll enthält verschiedene
VORANSICHT II/E. Elektrochemie einfach verständlich. Teil II: Galvanische Zellen. Hinweise zur Didaktik und Methodik. Kerstin Langer, Kiel
 1 von 22 Elektrochemie einfach verständlich Teil II: Galvanische Zellen Kerstin Langer, Kiel Niveau: Dauer: Sek. II 9 Unterrichtsstunden (Minimalplan: 6 Unterrichtsstunden) Kompetenzen: Die Schüler* nutzen
1 von 22 Elektrochemie einfach verständlich Teil II: Galvanische Zellen Kerstin Langer, Kiel Niveau: Dauer: Sek. II 9 Unterrichtsstunden (Minimalplan: 6 Unterrichtsstunden) Kompetenzen: Die Schüler* nutzen
1. Bezeichnung des Materials Lernen an Stationen zum Thema: Eigenschaften von NaCl 2. Autor(en) Dr. Krey, Olaf, Dr. Siehr, Ilona
 1. Bezeichnung des Materials Lernen an Stationen zum Thema: 2. Autor(en) Dr. Krey, Olaf, Dr. Siehr, Ilona 3. Doppeljahrgangsstufe / Fach 7/8 Chemie 4. Rahmlehrplanbezug P4 Schätze der Erde (Brandenburg)
1. Bezeichnung des Materials Lernen an Stationen zum Thema: 2. Autor(en) Dr. Krey, Olaf, Dr. Siehr, Ilona 3. Doppeljahrgangsstufe / Fach 7/8 Chemie 4. Rahmlehrplanbezug P4 Schätze der Erde (Brandenburg)
und folgenden Unterricht Kooperation Vorunterrichtliche Erfahrungen,
 Schulinterner Lehrplan für das Fach Chemie in der Jahrgangsstufe 6 (Klassenunterricht) Holzkamp-Gesamtschule, Witten (aktualisiert 2/2013) Unterrichtseinheit / Thema: Stoffe im Alltag, Stoffe können gefährlich
Schulinterner Lehrplan für das Fach Chemie in der Jahrgangsstufe 6 (Klassenunterricht) Holzkamp-Gesamtschule, Witten (aktualisiert 2/2013) Unterrichtseinheit / Thema: Stoffe im Alltag, Stoffe können gefährlich
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Elektrizität und Magnetismus - einfache Experimente
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Elektrizität und Magnetismus - einfache Experimente Das komplette Material finden Sie hier: Download bei School-Scout.de 19. Elektrizität
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Elektrizität und Magnetismus - einfache Experimente Das komplette Material finden Sie hier: Download bei School-Scout.de 19. Elektrizität
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Fit beim Aufstellen von Reaktionsgleichungen eine Trainingseinheit. Karin Keller, Bad Salzulen VORSCHAU VORANSICHT
 1 von 22 Fit beim Aufstellen von Reaktionsgleichungen eine Trainingseinheit Karin Keller, Bad Salzulen Reaktionsgleichungen sind ein für die Lehrkraft oft frustrierendes Thema. Häuig steigen die Lernenden
1 von 22 Fit beim Aufstellen von Reaktionsgleichungen eine Trainingseinheit Karin Keller, Bad Salzulen Reaktionsgleichungen sind ein für die Lehrkraft oft frustrierendes Thema. Häuig steigen die Lernenden
Säuren und Basen kommen in vielen
 1 von 32 Von der Cola zum Kakao der ph-wert von Lösungen Dr. Meike Reinhold, Duisburg Säuren und Basen kommen in vielen Lebensmitteln vor. Jugendliche sind oft überrascht, dass Sprudel oder Cola saure
1 von 32 Von der Cola zum Kakao der ph-wert von Lösungen Dr. Meike Reinhold, Duisburg Säuren und Basen kommen in vielen Lebensmitteln vor. Jugendliche sind oft überrascht, dass Sprudel oder Cola saure
Unterrichtsentwurf Physik
 Universität Duisburg-Essen Fachbereich DaZ/DaF Seminar: Sprachförderung im Physikunterricht Unterrichtsentwurf Physik Christopher Skubeckas Atakan Suözer Burcu Özbek Nadine Gritzan Fach: Physik Thema der
Universität Duisburg-Essen Fachbereich DaZ/DaF Seminar: Sprachförderung im Physikunterricht Unterrichtsentwurf Physik Christopher Skubeckas Atakan Suözer Burcu Özbek Nadine Gritzan Fach: Physik Thema der
Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt VORANSICHT
 V Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) 1 von 30 Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt Tobias Dunst, Kißlegg Welche Verbindung besteht zwischen dem mysteriösen
V Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) 1 von 30 Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt Tobias Dunst, Kißlegg Welche Verbindung besteht zwischen dem mysteriösen
Ganz schön ätzend! Eigenschaften, Herstellung und Verwendung von Säuren
 1 von 30 Ganz schön ätzend! Eigenschaften, Herstellung und Verwendung von Säuren Karin Schmidt, Netphen Hört man das Wort Säure, denkt man gleich an Verätzungen und den sauren Geschmack von Zitronen. Aber
1 von 30 Ganz schön ätzend! Eigenschaften, Herstellung und Verwendung von Säuren Karin Schmidt, Netphen Hört man das Wort Säure, denkt man gleich an Verätzungen und den sauren Geschmack von Zitronen. Aber
Licht und Farben. Kurzprotokoll
 Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
1 Stoffe in Alltag und Technik
 Schülerband Blickpunkt Chemie 1 Niedersachsen (978-3-507-77292-2) Basiskonzept inhaltsbezogene Kompetenzen: Fachwissen prozessbezogene Kompetenzen: Erkenntnisgewinnung, Kommunikation, Bewertung Die Schülerinnen
Schülerband Blickpunkt Chemie 1 Niedersachsen (978-3-507-77292-2) Basiskonzept inhaltsbezogene Kompetenzen: Fachwissen prozessbezogene Kompetenzen: Erkenntnisgewinnung, Kommunikation, Bewertung Die Schülerinnen
Kompetenzen und Aufgabenbeispiele Natur und Technik
 Institut für Bildungsevaluation Assoziiertes Institut der Universität Zürich Kompetenzen und Aufgabenbeispiele Natur und Technik Informationen für Lehrpersonen und Eltern 1. Wie sind die Ergebnisse dargestellt?
Institut für Bildungsevaluation Assoziiertes Institut der Universität Zürich Kompetenzen und Aufgabenbeispiele Natur und Technik Informationen für Lehrpersonen und Eltern 1. Wie sind die Ergebnisse dargestellt?
Rein oder nicht rein?
 Station 1: Rein oder nicht rein? Versuche: 1 Bestimmen Sie experimentell die Löslichkeit von Kochsalz. [Hinweis: Unter der Löslichkeit versteht man die Masse eines Stoffes in Gramm, die sich gerade noch
Station 1: Rein oder nicht rein? Versuche: 1 Bestimmen Sie experimentell die Löslichkeit von Kochsalz. [Hinweis: Unter der Löslichkeit versteht man die Masse eines Stoffes in Gramm, die sich gerade noch
Schulversuchspraktikum. Olga Streck. Sommersemester Klassenstufen 5 & 6. Papier
 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 5 & 6 Papier 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 enthält 2 Lehrerversuche und 2 Schülerversuche zum Thema
Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 5 & 6 Papier 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 enthält 2 Lehrerversuche und 2 Schülerversuche zum Thema
3.3.1 Basiskonzept: Stoff-Teilchen
 1 3.3.1 Basiskonzept: Stoff-Teilchen Fachwissen Erkenntnisgewinnung Kommunikation Bewertung Atome und Atomverbände werden zu Stoffmengen zusammengefasst unterscheiden zwischen Stoffportion und Stoffmenge.
1 3.3.1 Basiskonzept: Stoff-Teilchen Fachwissen Erkenntnisgewinnung Kommunikation Bewertung Atome und Atomverbände werden zu Stoffmengen zusammengefasst unterscheiden zwischen Stoffportion und Stoffmenge.
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Checkliste. Stoffe nennen, die der Mensch aus der Natur nutzt und sie anhand von Kriterien ordnen.
 Checkliste Beantworte alle Fragen ehrlich. Mit Hilfe deiner eigenen Einschätzung kannst du anschließend aus Materialien zum Üben und Wiederholen auswählen, wenn du bei einigen Nummern Nein oder Unsicher
Checkliste Beantworte alle Fragen ehrlich. Mit Hilfe deiner eigenen Einschätzung kannst du anschließend aus Materialien zum Üben und Wiederholen auswählen, wenn du bei einigen Nummern Nein oder Unsicher
Schulcurriculum Gymnasium Korntal-Münchingen
 Klasse: 8 Seite 1 Minimalanforderungskatalog; Themen des Schuljahres gegliedert nach Arbeitsbereichen m Schulcurriculum Themen, die dem Motto der jeweiligen Klassenstufe entsprechen und den Stoff des s
Klasse: 8 Seite 1 Minimalanforderungskatalog; Themen des Schuljahres gegliedert nach Arbeitsbereichen m Schulcurriculum Themen, die dem Motto der jeweiligen Klassenstufe entsprechen und den Stoff des s
Tätowierungen: Chemie, die unter die Haut geht
 Tätowierungen: Chemie, die unter die Haut geht Marc Stuckey, Ingo Eilks, Bremen Niveau: Dauer: Sek. I 4 6 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards Fachwissen: Die Schülerinnen und Schüler
Tätowierungen: Chemie, die unter die Haut geht Marc Stuckey, Ingo Eilks, Bremen Niveau: Dauer: Sek. I 4 6 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards Fachwissen: Die Schülerinnen und Schüler
Analytische Chemie. B. Sc. Chemieingenieurwesen. 14. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Geräte und Maschinen im Alltag
 und Maschinen im Alltag Dieses Skript gehört: und Maschinen im Alltag Seite 2 Versuch 1: Fotos ohne Fotoapparat In dem folgenden Versuch wollen wir uns ein altes fotografisches Verfahren genauer anschauen
und Maschinen im Alltag Dieses Skript gehört: und Maschinen im Alltag Seite 2 Versuch 1: Fotos ohne Fotoapparat In dem folgenden Versuch wollen wir uns ein altes fotografisches Verfahren genauer anschauen
3.5 Hydrolyse von Salzen. Aufgabe. Reagieren wässrige Salzlösungen neutral? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Veranstaltung 5: Chemie macht hungrig!
 Veranstaltung 5: Chemie macht hungrig! Station 1: Kohlenhydrate E1 Gummibärchen gehen baden! E2 Ist Zucker gleich Zucker? E3 Was macht eine Kartoffel stark? Station 2: Fette E4 Können Fette verschwinden?
Veranstaltung 5: Chemie macht hungrig! Station 1: Kohlenhydrate E1 Gummibärchen gehen baden! E2 Ist Zucker gleich Zucker? E3 Was macht eine Kartoffel stark? Station 2: Fette E4 Können Fette verschwinden?
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Arbeitsblatt Wasserkreislauf der Erde
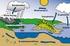 Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Lernzirkel WAS Station 1 Herstellung von Seife aus Kokosfett
 Station 1 Herstellung von Seife aus Kokosfett Zeitbedarf: 35 min. Durchführung 10 g Kokosfett und 5 ml destilliertes Wasser werden langsam in einem Becherglas erhitzt. Unter Rühren werden 10 ml Natronlauge
Station 1 Herstellung von Seife aus Kokosfett Zeitbedarf: 35 min. Durchführung 10 g Kokosfett und 5 ml destilliertes Wasser werden langsam in einem Becherglas erhitzt. Unter Rühren werden 10 ml Natronlauge
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid
 Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Schulversuchspraktikum. Name: Jennifer Ahrens. Semester: Sommersemester Klassenstufen 9 & 10. Alkalimetalle
 Schulversuchspraktikum Name: Jennifer Ahrens Semester: Sommersemester 2012 Klassenstufen 9 & 10 Alkalimetalle Auf einen Blick: In dieser Unterrichtseinheit werden Versuche zu den Alkalimetallen der ersten
Schulversuchspraktikum Name: Jennifer Ahrens Semester: Sommersemester 2012 Klassenstufen 9 & 10 Alkalimetalle Auf einen Blick: In dieser Unterrichtseinheit werden Versuche zu den Alkalimetallen der ersten
Schulversuchspraktikum. Isabel Böselt. Sommersemester Klassenstufen 9 & 10. Alkalimetalle
 Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 9 & 10 Alkalimetalle 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sollen Versuche zum
Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 9 & 10 Alkalimetalle 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sollen Versuche zum
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Vom Sinn der Arbeit - literarische Texte verstehen und in Strukturskizzen reflektieren Das komplette Material finden Sie hier: School-Scout.de
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Vom Sinn der Arbeit - literarische Texte verstehen und in Strukturskizzen reflektieren Das komplette Material finden Sie hier: School-Scout.de
Struktur-Eigenschafts-Beziehungen von unverzweigten Alkanen
 1 von 16 Struktur-Eigenschafts-Beziehungen von unverzweigten Alkanen Martin Trockel, Dorsten; Petra Wlotzka, Dortmund Niveau: Dauer: Sek. I/II 3 Unterrichtsstunden Kompetenzen: Die Schülerinnen und Schüler*
1 von 16 Struktur-Eigenschafts-Beziehungen von unverzweigten Alkanen Martin Trockel, Dorsten; Petra Wlotzka, Dortmund Niveau: Dauer: Sek. I/II 3 Unterrichtsstunden Kompetenzen: Die Schülerinnen und Schüler*
Schulversuchspraktikum. Alexander König. Sommersemester Klassenstufen 11 & 12. Katalysatoren
 Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 11 & 12 Katalysatoren Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält einen Schülerversuch und einen
Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 11 & 12 Katalysatoren Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält einen Schülerversuch und einen
Schwimmen, Schweben, Sinken
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 5 & 6 Schwimmen, Schweben, Sinken Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 beinhaltet einen Lehrer- und vier Schülerversuche.
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 5 & 6 Schwimmen, Schweben, Sinken Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 beinhaltet einen Lehrer- und vier Schülerversuche.
Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm Klasse 9 Themen Das Kern-Hülle-Modell Modell des Atomkerns Die Atomhülle im Energiestufenmodell Elektrische Ladung im Atom Das Kern-Hülle-Modell
Curriculum Chemie Klasse 9 Albert-Einstein-Gymnasium Ulm Klasse 9 Themen Das Kern-Hülle-Modell Modell des Atomkerns Die Atomhülle im Energiestufenmodell Elektrische Ladung im Atom Das Kern-Hülle-Modell
Die Spalte Zeitbedarf gibt die ungefähre Schulstundenanzahl der Sequenz (Spalte zwei) eines Kontextes an.
 Vorwort zur exemplarischen Reihenplanung (Grobplanung) Die Reihenplanung ist nach der folgenden Struktur aufgebaut: Die zwei Kopfzeilen nennen den Titel des Inhaltsfeldes, den zugehörigen Fachlichen Kontext
Vorwort zur exemplarischen Reihenplanung (Grobplanung) Die Reihenplanung ist nach der folgenden Struktur aufgebaut: Die zwei Kopfzeilen nennen den Titel des Inhaltsfeldes, den zugehörigen Fachlichen Kontext
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Geschichten aus veränderter Perspektive schreiben - Aufsatztraining leicht gemacht Das komplette Material finden Sie hier: School-Scout.de
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Geschichten aus veränderter Perspektive schreiben - Aufsatztraining leicht gemacht Das komplette Material finden Sie hier: School-Scout.de
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Der Dieb im Elektroladen. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Der Dieb im Elektroladen Das komplette Material finden Sie hier: School-Scout.de 29. Ein Comic zur E-Lehre 1 von 34 Der Dieb im Elektroladen
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Der Dieb im Elektroladen Das komplette Material finden Sie hier: School-Scout.de 29. Ein Comic zur E-Lehre 1 von 34 Der Dieb im Elektroladen
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Sina Bachsmann Sommersemester 2014 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Im Folgenden
Schulversuchspraktikum Sina Bachsmann Sommersemester 2014 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Im Folgenden
SÄUR E. BASE oder LAU GE SAUE R BASI SCH
 SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Eine Einführung in die Lehre von den Schwingungen und Wellen
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Eine Einführung in die Lehre von den Schwingungen und Wellen Das komplette Material finden Sie hier: School-Scout.de 25. Eine Einführung
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Eine Einführung in die Lehre von den Schwingungen und Wellen Das komplette Material finden Sie hier: School-Scout.de 25. Eine Einführung
Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker
 Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Lerne Nachweismöglichkeiten für Eiweiße kennen und untersuche verschiedene Lebensmittel auf Eiweiße.
 Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802600) 4.5 Eiweißhaltige Nahrungsmittel Experiment von: Phywe Gedruckt: 07.0.203 5:40:59 intertess (Version
Naturwissenschaften - Biologie - Allgemeine Biologie - 4 Unsere Nahrungsmittel und ihre Verdauung (P802600) 4.5 Eiweißhaltige Nahrungsmittel Experiment von: Phywe Gedruckt: 07.0.203 5:40:59 intertess (Version
