Das Gewebegesetz in der Überwachungspraxis
|
|
|
- Charlotte Bauer
- vor 6 Jahren
- Abrufe
Transkript
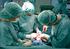
1 Das Gewebegesetz in der Überwachungspraxis Anforderungen an Entnahmeeinrichtungen und Gewebespenderlabore Dr. Dr. Gabriele Wanninger, Regierung von von Oberbayern
2 Gewebe und Zellen Gewebe und Zellen EG-Richtlinien Spende, Beschaffung, Testung, Verarbeitung, Konservierung, Lagerung, Verteilung von menschlichen Geweben und Zellen Technische Vorschriften für die Spende, Beschaffung und Testung Rückverfolgbarkeit, Meldung schwerwiegender Zwischenfälle/unerwünschte Reaktionen; techn. Anforderungen an die Kodierung, Verarbeitung, Konservierung, Lagerung, Verteilung Richtlinie 2004/23/EG Richtlinie 2006/17/EG Richtlinie 2006/86/EG 2
3 Umsetzung in deutsches Recht Umsetzung in deutsches Recht Gewebegesetz - Artikelgesetz zur Änderung des Transplantationsgesetzes (TPG) Arzneimittelgesetzes (AMG) Transfusionsgesetzes (TFG) Änderung der Apothekenbetriebsordnung (ApBetrO) Änderung der BetriebsV für Arzneimittelgroßhandelsbetriebe Änderung anderer Rechtsvorschriften (Infektionsschutzgesetz) TPG-Gewebeverordnung (TPG-GewV) vom enthält Anforderungen an die Qualität und Sicherheit von Geweben und deren Übertragung nach dem TPG Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) vom enthält Regelungen für Gewebe- und Entnahmeeinrichtungen sowie Gewebespenderlabore 3
4 Begriffsbestimmungen Gewebe sind alle aus Zellen bestehenden Bestandteile des menschlichen Körpers, die keine Organe sind, einschließlich einzelner menschlicher Zellen ( 1a Nr. 4 TPG) Gewebezubereitungen sind Arzneimittel, die Gewebe i. S. von 1a Nr. 4 TPG sind oder aus solchen Geweben hergestellt worden sind. Menschliche Samen- und Eizellen einschließlich imprägnierter Eizellen (Keimzellen), und Embryonen sind weder Arzneimittel noch Gewebezubereitungen ( 4 Abs. 30 AMG) 4
5 Begriffsbestimmungen Gewebeeinrichtung gemäß 2 Nr. 10 AMWHV: Einrichtung, die Gewebe entnimmt, untersucht, aufbereitet, be- oder verarbeitet, konserviert, kennzeichnet, verpackt, freigibt, aufbewahrt, in den Verkehr bringt, einführt, ausführt oder in oder aus dem Geltungsbereich des AMG verbringt Entnahmeeinrichtung gemäß 2 Nr. 11 AMWHV: Einrichtung, die ausschließlich Gewebe gewinnt einschließlich aller Maßnahmen, die dazu bestimmt sind, das Gewebe in einem be- oder verarbeitungsfähigen Zustand zu erhalten, eindeutig zu identifizieren und zu transportieren 5
6 Begriffsbestimmungen Gewebespenderlabor gemäß 2 Nr. 13 AMWHV: Labor, das die für die Gewebegewinnung erforderlichen Laboruntersuchungen durchführt Gewinnung im Sinne des 20b Abs. 1 AMG: die direkte oder extrakorporale Entnahme von Gewebe einschließlich aller Maßnahmen, die dazu bestimmt sind, das Gewebe in einem be- oder verarbeitungsfähigen Zustand zu erhalten, eindeutig zu identifizieren und zu transportieren 6
7 Ausnahmen vom Transplantationsgesetz Ausnahmen vom Transplantationsgesetz 1 TPG Das Transplantationsgesetz findet keine Anwendung auf Gewebe, die innerhalb ein und desselben chirurgischen Eingriffs einer Person entnommen werden, um auf diese rückübertragen zu werden 7
8 Ausnahmen vom Arzneimittelgesetz Ausnahmen vom Arzneimittelgesetz Arzneimittel sind nicht Organe im Sinne des 1 Nr.1 TPG, wenn sie zur Übertragung auf menschliche Empfänger bestimmt sind ( 3 Abs. 2 Nr. 8 AMG) die Gewinnung und das Inverkehrbringen von Keimzellen zur künstlichen Befruchtung bei Tieren ( 4a Nr. 2 AMG) Arzneimittel, die ein Arzt unter seiner unmittelbaren fachlichen Verantwortung herstellt und anwendet ( 4a Nr. 3 AMG) Gewebe, die innerhalb eines Behandlungsvorgangs einer Person entnommen werden, um auf diese rückübertragen zu werden ( 4a Nr. 4 AMG) 8
9 Organe-Gewebe-Blutzubereitungen Organe Vermittlungspflichtig: Herz, Lunge, Leber, Niere, Bauchspeicheldrüse, Darm Geregelt im TPG Gewebe Beispiele: Knochenmark Knochen, Knorpel Sehnen, Bänder Herzklappen Augenhornhäute Keimzellen Fötales Gewebe Geregelt im TPG und AMG Blutzubereitungen Beispiele: Periphere Blutstammzellzubereitungen Stammzellen aus Nabelschnurblut Geregelt im TFG und AMG 9
10 Herstellungserlaubnis 13 Abs. 1 AMG: Erfordernis einer Herstellungserlaubnis für die Be- oder Verarbeitung von Geweben und Gewebezubereitungen mit industriellen Verfahren oder für Be- und Verarbeitungsverfahren, die in der EU nicht hinreichend bekannt sind für die Gewinnung von Blutstammzellen und die Herstellung von Blutstammzellzubereitungen Keine Herstellungserlaubnis gemäß 13 Abs. 1 AMG erforderlich für Gewebe im Sinne von 1a Nr. 4 TPG (Gewinnung und Untersuchung) Gewebezubereitungen, für die eine Erlaubnis nach 20 c AMG erteilt wird 10
11 Gewinnung von Geweben Gewinnung von Geweben 20b Abs. 1 AMG: Erlaubnis für die Gewinnung von Geweben und Laboruntersuchungen Erlaubnispflicht für Einrichtungen, die Gewebe gewinnen (Entnahmeeinrichtungen) oder die für die Gewinnung erforderlichen Laboruntersuchungen durchführen (Gewebespenderlabore) Antragstellung bei der zuständigen Landesbehörde Ausländische Antragsteller: Nutzungsabgrenzungsvertrag mit den Kliniken erforderlich (sog. Detmolder Modell) 11
12 Gewinnung von Geweben Gewinnung von Geweben 20b Abs. 1 AMG: Erlaubnis für die Gewinnung von Geweben und die Laboruntersuchungen Anforderungen: Angemessen ausgebildete Person mit der erforderlichen Berufserfahrung; kann zugleich die ärztliche Person im Sinne von 8d Abs. 1 Satz 1 TPG sein Weiter mitwirkendes Personal mit der erforderlichen Qualifikation Angemessene Räume und Einrichtungen für die Gewinnung und Laboruntersuchung Gewinnung und Prüfung nach dem Stand von Wissenschaft und Technik 12
13 Gewinnung von Geweben Gewinnung von Geweben 20b Abs. 1 AMG: Erlaubnis für die Gewinnung von Geweben und Laboruntersuchungen Inspektion und Erteilung der Erlaubnis: Von einer Besichtigung gemäß 64 Abs. 3 Satz 2 AMG kann die zuständige Behörde absehen Die Erlaubnis wird der Entnahmeeinrichtung für eine bestimmte Betriebsstätte und für bestimmtes Gewebe und dem Labor für eine bestimmte Betriebsstätte und für bestimmte Tätigkeiten erteilt Die zuständige Behörde kann die zuständige Bundesoberbehörde beteiligen 13
14 Gewinnung von Geweben Gewinnung von Geweben 20b Abs. 2 AMG: Entnahme oder Prüfung unter vertraglicher Bindung mit einem Hersteller, der eine Erlaubnis nach 13 oder 20 c AMG besitzt keine eigene Erlaubnis für die Entnahmeeinrichtung oder das Labor erforderlich Eine Beauftragung durch Firmen in anderen EU-Mitgliedstaaten ist nur möglich, wenn sie in Deutschland eine Erlaubnis nach 13 oder 20 c AMG besitzen Verfahrensablauf: Inhaber der Erlaubnis zeigt Entnahmeeinrichtung oder Labor der für diese jeweils zuständigen Behörde an und fügt Unterlagen über Personal, Räume und die Einhaltung der Guten fachlichen Praxis bei 14
15 Gewinnung von Geweben Gewinnung von Geweben 20b Abs. 2 AMG: Entnahme oder Prüfung unter vertraglicher Bindung. Inhaber der Erlaubnis zeigt einen Monat nach der o. g. Anzeige die Einrichtung/ das Labor seiner zuständigen Behörde an, es sei denn, dass die für die Entnahmeeinrichtung/das Labor zuständige Behörde widersprochen hat. In Ausnahmefällen verlängert sich die Frist um weitere 2 Monate. Der Hersteller/Be-/ Verarbeiter ist hiervon vor Fristablauf unter Mitteilung der Gründe in Kenntnis zu setzen. Hat die zuständige Behörde widersprochen, sind die Fristen gehemmt, bis der Grund für den Widerspruch behoben ist. 15
16 Gewinnung von Geweben Gewinnung von Geweben 20b Abs. 2 AMG: Entnahme oder Prüfung unter vertraglicher Bindung. Anforderungen an Entnahmeeinrichtung oder Labor: Siehe 20b Abs. 1 AMG Erteilung der Erlaubnis: Die Erlaubnis für die Entnahmeeinrichtung oder das Gewebespenderlabor wird dem Hersteller, Be- oder Verarbeiter erteilt. 16
17 Antragsunterlagen (1) Antragsunterlagen (1) Erlaubnisantrag für Gewebeeinrichtung oder Entnahmeeinrichtung Formlose Anzeige mit Darstellung der beabsichtigten Tätigkeiten Angemessen ausgebildete Person gem. 20b AMG Benennung und Nachweis der Ausbildung und Berufserfahrung Weiter mitwirkendes Personal Berufsausbildung und -erfahrung des beteiligten Personals Bestellter Arzt gem. 8d Abs. 1 TPG Benennung und Nachweis der Sachkunde 17
18 Antragsunterlagen (2) Antragsunterlagen (2) Fortsetzung Genaue Angabe der Gewebe Benennung der Räumlichkeiten/Ausrüstung Ggf. Vertrag mit Gewebeeinrichtung Kurze Darstellung des QM-/QS-Systems Wesentliche Verfahrensbeschreibungen Ggf. Angabe der beauftragten Transportunternehmen Vertrag 18
19 Überwachung 64 AMG Abs. 1 AMG Überwachung durch zuständige Landesbehörden Im Falle des 20b Abs. 2 AMG unterliegen die Entnahmeeinrichtungen und Labore der Überwachung durch die für sie örtlich zuständigen Behörde 64 Abs. 2 AMG Hinzuziehen von Sachverständigen der Bundesoberbehörde (für Gewebe und Gewebezubereitungen: Paul-Ehrlich-Institut) 64 Abs. 3 AMG Abnahmebesichtigung vor Erteilung einer Herstellungs- oder Einfuhrerlaubnis gem. 13, 72 AMG; nicht zwingend vor der Erlaubniserteilung gem. 20b AMG Regelinspektionen alle 2 Jahre 19
20 TPG-Gewebeverordnung TPG-Gewebeverordnung regelt folgende Bereiche: Festlegung von Anforderungen für Gewebeeinrichtung zur Gewinnung von Geweben ( Entnahmeeinrichtungen ) an die Entnahme von Gewebe an die ärztliche Beurteilung der medizinischen Eignung des Spenders an die Laboruntersuchungen und Untersuchungsverfahren an die Spenderakte und den Entnahmebericht 20
21 TPG-Gewebeverordnung Die TPG-Gewebeverordnung regelt ferner die Verpflichtungen von Einrichtung der medizinischen Versorgung zur Dokumentation von übertragenen Geweben und zu Meldungen schwerwiegender Zwischenfälle sowie schwerwiegender unerwünschter Reaktionen festlegen. die Voraussetzungen für die Verwendung von Keimzellen im Rahmen von medizinisch unterstützten Fertilisationsverfahren. 21
22 AMWHV Auf Gewebe und Gewebezubereitungen ist die Verordnung über die Anwendung der Guten Herstellungspraxis bei der Herstellung von Arzneimitteln und Wirkstoffen und über die Anwendung der Guten fachlichen Praxis bei der Herstellung von Produkten menschlicher Herkunft = Arzneimittel- und Wirkstoffhersteller-Verordnung (AMWHV) anwendbar Anwendung der Guten fachlichen Praxis GMP nicht anwendbar auf Gewebe- und Entnahmeeinrichtungen ( 3 Abs. 1 AMWHV) 22
23 AMWHV Die AMWHV regelt für Gewebe und Gewebezubereitungen Allgemeine Anforderungen (Abschnitt 2: QM-System, Personal, Betriebsräume und Ausrüstungen, Hygienemaßnahmen, Lagerung und Transport, Tätigkeiten im Auftrag, Allgemeine Dokumentation, Selbstinspektion und Lieferantenqualifizierung) Sondervorschriften für Entnahme- und Gewebeeinrichtungen sowie für Gewebespenderlabore Ergänzende allgemeine Anforderungen, Spendereignung, Laboruntersuchungen, Gewinnung von Gewebe, Transport zur Be- oder Verarbeitung, Be- oder Verarbeitung und Lagerung, Prüfung und Freigabe, Inverkehrbringen, Einfuhr, Meldung schwerwiegender unerwünschter Reaktionen und schwerwiegender Zwischenfälle und Rückruf 23
24 Gute fachliche Praxis Gute fachliche Praxis 3 Abs. 3 AMWHV Standards der Guten fachlichen Praxis: Was ist das? Richtlinie 2006/17/EG Standards für die Spende, Beschaffung und Testung von menschlichen Geweben und Zellen Richtlinie 2006/86/EG Standards für die Kodierung, Verarbeitung, Konservierung, Lagerung und Verteilung von menschlichen Geweben und Zellen Richtlinien der Bundesärztekammer Leitlinien von Fachgesellschaften und Behörden Anderes wissenschaftliches Erkenntnismaterial 24
25 QM-/QS-System QM-System ist ein System, das. die Gute fachliche Praxis beinhaltet ( 2 Nr. 4 AMWHV) Anforderungen an das QM-System ( 32 AMWHV) QM-System erforderlich für: Gewebeeinrichtung Entnahmeeinrichtung Das QM-System ist vollständig zu dokumentieren. 25
26 Personal 20b Abs. 1 AMG; 8d TPG; 34 Abs. 1 AMWHV Personalschulung und Personalhygiene Ausbildung und praktische Erfahrung des Personals Aufgabenbeschreibungen Schulungsprogramme und Überprüfung des Schulungserfolgs Personalhygiene Gesundheits- und Sicherheitsvorschriften 26
27 Räume und Einrichtungen Räume und Einrichtungen 20b Abs. 1 AMG; 34 Abs. 2 AMWHV Eignung der Räume und Ausrüstung Behandlungs- und OP-Räume, die für vergleichbare Eingriffe an Menschen genutzt werden, gelten als geeignet Hygieneplan lokaler steriler Bereich für postmortale Spende Verwendung steriler Medizinprodukte Gewebeentnahme durch mobile Teams Geeignete Räume und Ausrüstung im Gewebespenderlabor 27
28 Spendereignung 3, 6 TPG-GewV, 33, 34 Abs. 5 AMWHV Tote Spender: Siehe Anlage 1 TPG-GewV Lebende Spender: Siehe Anlage 2 TPG-GewV Spenderevaluierung durch einen Arzt nach SOP Befragung des Patienten ggf. anhand eines Fragebogens Auswahl- und Ausschlussgründe Vermeidung von Kreuzkontamination und Verwechslung von Geweben von Spendern mit positiven Befunden 28
29 Laboruntersuchungen 4 und Anlage 3, 4, 6 der TPG-GewV, 33 AMWHV Spenderauswahl und Untersuchungen nach schriftlichen Anweisungen Anweisungen müssen den Genehmigungsunterlagen gem. 21a AMG entsprechen (falls zutreffend) Validierung kritischer Prüfverfahren Durchführung und Protokollierung der Prüfungen Dokumentation und Bewertung von Abweichungen Eignung und Prüfung von Materialien und Reagenzien Teilnahme an Ringversuchen 29
30 Entnahme von Geweben Entnahme von Geweben 3, 4, 4a, TPG, 5 TPG-GewV, 34 AMWHV Spenderakte: Identität, Eignung, Einwilligung, Anamnese, Laboruntersuchungen, Code, Unterschrift des Arztes Entnahmeanweisung: Überprüfung der Spenderakte, Entnahme des Gewebes und der Proben für die Laboruntersuchungen, Instrumente, Vermeidung von Kontaminationen, Ort und Zeit der Entnahme, Transportbehältnisse Entnahmebericht: Identität, Gewebe, Personal, Ort und Zeitpunkt der Entnahme, Freigabe zur Weiterverarbeitung, Reagenzien und Transportlösungen Untersuchung von Zwischenfällen: Ermittlung der Ursachen Archivierung 30
31 Transport 35 AMWHV Eignung der Behältnisse Vermeidung von Kontaminationen Kennzeichnung des Primärpackmittels Kennzeichnung des Transportbehälters Kennzeichnung der Gewebe- und Blutproben Kontrolle und Validierung der Transportbedingungen Vermeidung von Zugriffen Unbefugter Vertragliche Vereinbarung mit Kurieren, Transportunternehmen etc.; Qualifizierung des Auftragnehmers 31
32 Einfuhr Einfuhrerlaubnisse Einfuhrerlaubnis für industriell hergestellte oder nicht hinreichend bekannte Gewebezubereitungen ( 72 Abs. 1 AMG) Zertifikate ( 72a AMG) Einfuhrerlaubnis für Arzneimittel menschlicher Herkunft zur unmittelbaren Anwendung ( 72 Abs. 2 AMG) Einfuhrerlaubnis und Zertifikat für Gewebe i. S. v. 1a Nr. 4 TPG und Gewebezubereitungen i. S. v. 20c AMG ( 72b AMG) 32
33 Einfuhrerlaubnis 72 Abs. 1 AMG Einfuhrerlaubnis 72 Abs. 1 AMG Gemäß 72 Abs. 1 AMG für industriell hergestellte oder nicht hinreichend bekannte Gewebezubereitungen Import von Gewebezubereitungen aus Drittländern zur Abgabe an andere oder zur Weiterverarbeitung Voraussetzungen entsprechend Herstellungserlaubnis 72 Abs. 1 AMG findet keine Anwendung auf Gewebe im Sinne von 1a Nr. 4 TPG und auf Gewebezubereitungen im Sinne von 20c AMG ( 72 Abs. 3 AMG) 33
34 Zertifikate 72a Abs. 1 AMG Zertifikate 72a Abs. 1 AMG Zertifikate gemäß 72a Abs. 1 AMG sind zusätzlich zur Einfuhrerlaubnis gemäß 72 Abs. 1 AMG erforderlich 72a Abs. 1 AMG findet keine Anwendung auf Gewebe im Sinne von 1a Nr. 4 TPG und auf Gewebezubereitungen im Sinne von 20c AMG ( 72a Abs. 3 AMG) 34
35 Einfuhrerlaubnis 72b AMG Einfuhrerlaubnis 72b AMG 72b AMG Einfuhrerlaubnis für Gewebe i. S. v. 1a Nr. 4 TPG und Gewebezubereitungen i. S. v. 20c AMG Gilt für den Import von Gewebe im Sinne von 1a Nr. 4 TPG oder Gewebezubereitungen im Sinne von 20c AMG aus Drittländern, gewerbs- oder berufsmäßig zum Zwecke der Abgabe an andere oder zur Be- oder Verarbeitung Anforderungen: Siehe Erlaubnis nach 20c AMG 35
36 Zertifikate nach 72b AMG Zertifikate nach 72b AMG 72b AMG Zertifikate für Gewebe i. S. v. 1a Nr. 4 TPG und Gewebezubereitungen i. S. v. 20c AMG Gegenseitig anerkannte Zertifikate, die bestätigen, dass die Gewinnung oder Be- oder Verarbeitung und die Laboruntersuchungen nach den Standards der Guten Fachlichen Praxis durchgeführt werden Bestätigung der Einhaltung der Guten Fachlichen Praxis durch die zuständige deutsche Behörde (Drittlandinspektion). Von einer Besichtigung kann unter bestimmten Bedingungen abgesehen werden. Bescheinigung des öffentlichen Interesses 36
37 Übergangsvorschriften 142 AMG Übergangsvorschriften Wer für Gewebe oder Gewebezubereitungen bis zum eine Erlaubnis nach 20b Abs. 1 oder Abs. 2 oder 20c Abs. 1 oder eine Herstellungserlaubnis nach 13 Abs. 1 oder bis zum eine Genehmigung nach 21a Abs. 1 oder bis zum eine Zulassung nach 21 Abs. 1 beantragt hat, darf diese Gewebe oder Gewebezubereitungen weiter gewinnen, im Labor untersuchen, be- oder verarbeiten, konservieren, lagern oder in den Verkehr bringen, bis über den Antrag entschieden worden ist. 37
38 Häufig gestellte Fragen Regulatorische und fachliche Anforderungen an die Gewinnung, Be- und Verarbeitung, Konservierung, Lagerung, das Inverkehrbringen und den Import von Geweben und Gewebezubereitungen
39 Fragen Was versteht man unter einem Behandlungsvorgang im Sinne von 4a Nr. 4 AMG (Ausnahme vom Anwendungsbereich des AMG)? Voraussetzung für die Inanspruchnahme dieser Ausnahmemöglichkeit vom Anwendungsbereich des AMG ist, dass Entnahme und Rückübertragung im Rahmen eines Behandlungsvorgangs und damit in engem fachlichen Zusammenhang stehen. Erfasst werden auch solche Behandlungsvorgänge, die länger andauern oder sogar unterbrochen werden und an denen mehrere Ärzte beteiligt sein können. 39
40 Fragen Welche räumlichen Anforderungen bestehen an Entnahmeeinrichtungen? Operations- und Behandlungsräume Eignung für vergleichbare medizinische Eingriffe Dokumentierte Hygienemaßnahmen Grundlagen: Anforderungen der Hygiene bei Operationen und anderen invasiven Eingriffen (Ziffer C 5.3 der Richtlinie für Krankenhaushygiene und Infektionsprävention des Robert-Koch-Instituts, erstveröffentlicht im Bundesgesundheitsblatt 2000; 43: DIN , Raumlufttechnik - Teil 4: Raumlufttechnische Anlagen in Krankenhäusern, April 2005 (Entwurf); -> Abschnitte 6 und 7 40
41 Fragen Wie ist die Erlaubniserteilung bei der Biopsatentnahme bei gleichzeitiger Entnahme von autologem Blut geregelt? Erforderlich ist eine Erlaubnis nach 20b (1) AMG für die Biopsatentnahme und eine zweite Erlaubnis nach 13 (1) AMG für die Eigenblutentnahme. Gewinnung der Gewebe unter vertraglicher Bindung an den Erlaubnisinhaber gemäß AMG 20b (2) AMG möglich Entnahme des Eigenbluts unter vertraglicher Bindung an den Erlaubnisinhaber als beauftragter Betrieb aufgrund der Regelung nach 14 (4) Nr. 4 AMG. 41
42 Fragen Wer stellt den Antrag auf Erlaubnis nach 20b AMG? Antragstellung durch Entnahmemeinrichtung oder Gewebespenderlabor ( 20b Abs. 1 AMG) oder Verarbeiter mit Erlaubnis nach 13 AMG oder 20c AMG ( 20b Abs. 2 AMG), wenn die Tätigkeit (s. o.) unter vertraglicher Bindung mit einem Hersteller ( 13 AMG) oder einem Be- oder Verarbeiter ( 20c AMG) erfolgt ausländischen Hersteller nach dem sog. Detmolder Modell (Verfügungsgewalt über Räume und Einrichtungen sowie Personal in der Entnahmeeinrichtung für die Zeiten der Gewebeentnahme) 42
43 Fragen Sind für die Herstellung von peripheren Blutstammzellzubereitungen und Stammzellzubereitungen aus Knochenmark unterschiedliche Erlaubnisse notwendig? Für die Gewinnung von peripheren Blutstammzellen und die Herstellung von peripheren Blutstammzellzubereitungen ist eine Erlaubnis gem. 13 Abs. 1 AMG erforderlich. Für die Gewinnung und Verarbeitung von Knochenmark ist eine Erlaubnis gem. 20b und 20c AMG erforderlich. Einrichtungen, die o. g. Tätigkeiten durchführen, benötigen zwei Erlaubnisse. 43
44 Fragen Wann werden Inspektionen in Einrichtungen nach 20b AMG durchgeführt? Die Durchführung einer Inspektion für die Erteilung einer Erlaubnis nach 20b AMG liegt im Ermessen der zuständigen Behörde. Die meisten Behörden führen stichpunktartige Inspektionen durch. 44
45 Vielen Dank für Ihre Aufmerksamkeit 45
Be- und Verarbeitung von. Anforderungen an Reinräume. Dr. Dr. Jürgen Mählitz, Regierung von von Oberbayern juergen.maehlitz@reg-ob.bayern.
 Be- und Verarbeitung von Gewebe und Gewebezubereitungen gem. 20c AMG; Anforderungen an Reinräume Dr., Regierung von von Oberbayern juergen.maehlitz@reg-ob.bayern.de Rechtliche Rahmenbedingungen (1) Rechtliche
Be- und Verarbeitung von Gewebe und Gewebezubereitungen gem. 20c AMG; Anforderungen an Reinräume Dr., Regierung von von Oberbayern juergen.maehlitz@reg-ob.bayern.de Rechtliche Rahmenbedingungen (1) Rechtliche
Workshop on the EU Clinical Trials Directive. GMP für Prüfpräparate und die Rolle der sachkundigen Person
 Workshop on the EU Clinical Trials Directive GMP für Prüfpräparate und die Rolle der sachkundigen Person Dr. Gabriele Wanninger Bayer. Landesamt für Klinische Prüfung von Arzneimitteln Ethikkommission
Workshop on the EU Clinical Trials Directive GMP für Prüfpräparate und die Rolle der sachkundigen Person Dr. Gabriele Wanninger Bayer. Landesamt für Klinische Prüfung von Arzneimitteln Ethikkommission
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II 2. November 2011 in Mainz
 WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II in Mainz Folie 1 2 Begriffsbestimmungen 3. ist der EG-GMP Leitfaden (BAnz. S. 6887)
WS 2011 / 2012 Spezielles Arzneimittelrecht Industrielle Arzneimittelherstellung versus Individualherstellung Teil II in Mainz Folie 1 2 Begriffsbestimmungen 3. ist der EG-GMP Leitfaden (BAnz. S. 6887)
Verordnung über das Register der Gewebeeinrichtungen nach dem Transplantationsgesetz (TPG-Gewebeeinrichtungen- Registerverordnung - TPG-GewRegV)
 Bundesrat Drucksache 743/08 16.10.08 Verordnung des Bundesministeriums für Gesundheit G - In Verordnung über das Register der Gewebeeinrichtungen nach dem Transplantationsgesetz (TPG-Gewebeeinrichtungen-
Bundesrat Drucksache 743/08 16.10.08 Verordnung des Bundesministeriums für Gesundheit G - In Verordnung über das Register der Gewebeeinrichtungen nach dem Transplantationsgesetz (TPG-Gewebeeinrichtungen-
Münsterische Beiträge zur Rechtswissenschaft Neue Folge 18
 Münsterische Beiträge zur Rechtswissenschaft Neue Folge 18 Kerstin Wolfgard Bock Der Rechtsrahmen für Arzneimittel für neuartige Therapien auf unionaler und nationaler Ebene mit Fokus auf Therapien mit
Münsterische Beiträge zur Rechtswissenschaft Neue Folge 18 Kerstin Wolfgard Bock Der Rechtsrahmen für Arzneimittel für neuartige Therapien auf unionaler und nationaler Ebene mit Fokus auf Therapien mit
Antrag auf Erteilung einer Erlaubnis zum Versand apothekenpflichtiger Arzneimittel nach 11a Apothekengesetz (ApoG)
 Antrag auf Erteilung einer Erlaubnis zum Versand apothekenpflichtiger Arzneimittel nach 11a Apothekengesetz (ApoG) Antragsteller (Inhaber der Betriebserlaubnis): Name Vorname. Name und Anschrift der Versandapotheke:
Antrag auf Erteilung einer Erlaubnis zum Versand apothekenpflichtiger Arzneimittel nach 11a Apothekengesetz (ApoG) Antragsteller (Inhaber der Betriebserlaubnis): Name Vorname. Name und Anschrift der Versandapotheke:
Wirkstoffüberwachung
 Wirkstoffüberwachung Zuständigkeiten bei der Überwachung der GMP-Compliance von Wirkstoffherstellern (Behörde MAH) Auftragsaudits bei Wirkstoffherstellern Einsichtnahme in Auditberichte durch die Behörde
Wirkstoffüberwachung Zuständigkeiten bei der Überwachung der GMP-Compliance von Wirkstoffherstellern (Behörde MAH) Auftragsaudits bei Wirkstoffherstellern Einsichtnahme in Auditberichte durch die Behörde
Gesetz über die Qualität und Sicherheit von menschlichen Geweben (Gewebegesetz) Wesentliche Vorschriften und ihre Bedeutung für die Praxis
 Institut für Klinische Transfusionsmedizin und Hämotherapie Direktor: Prof. Dr. M. Böck Institut für klinische Transfusionsmedizin und Hämotherapie Universitätsklinikum Würzburg Josef-Schneider-Str. 2
Institut für Klinische Transfusionsmedizin und Hämotherapie Direktor: Prof. Dr. M. Böck Institut für klinische Transfusionsmedizin und Hämotherapie Universitätsklinikum Würzburg Josef-Schneider-Str. 2
Jahrestagung der AGRR 2011 Aktuelle Problemstellungen bei der Herstellung von Radiopharmaka
 Jahrestagung der AGRR 2011 Aktuelle Problemstellungen bei der Herstellung von Radiopharmaka Themen Regulatorische Grundlagen und das Gesetz vom 17. Juli 2009 in der Praxis: 13 Abs. 2b AMG Zulassungspflicht;
Jahrestagung der AGRR 2011 Aktuelle Problemstellungen bei der Herstellung von Radiopharmaka Themen Regulatorische Grundlagen und das Gesetz vom 17. Juli 2009 in der Praxis: 13 Abs. 2b AMG Zulassungspflicht;
Bewertungsstandards für Auditsituationen
 www.pcs-gmp.com Bewertungsstandards für Auditsituationen Standards for Auditors: Welche GMP-Standards und QS-Normen sind bei welchen Audits anwendbar? 11. und 12. Februar 2015 Mannheim Kurzprofil Bedeutsamkeit
www.pcs-gmp.com Bewertungsstandards für Auditsituationen Standards for Auditors: Welche GMP-Standards und QS-Normen sind bei welchen Audits anwendbar? 11. und 12. Februar 2015 Mannheim Kurzprofil Bedeutsamkeit
Abschnitt 1 Anwendungsbereich und Allgemeine Anforderungen an die Konformitätsbewertung 1 Anwendungsbereich
 13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
Vom 24. Februar 2010 (BGBl. I S. 140) letzte eingearbeitete Änderung: Artikel 54 der Verordnung vom 31. August 2015 (BGBl. I S.
 Nur die Originaltexte sind rechtsverbindlich! E 1.2.15 Verordnung über das datenbankgestützte Informationssystem über Arzneimittel des Deutschen Instituts für Medizinische Dokumentation und Information
Nur die Originaltexte sind rechtsverbindlich! E 1.2.15 Verordnung über das datenbankgestützte Informationssystem über Arzneimittel des Deutschen Instituts für Medizinische Dokumentation und Information
Inhaltsverzeichnis Seite
 Leitfaden der Deutschen Gesellschaft für Chirurgie zur Guten Fachlichen Praxis (GFP) für die Entnahme von menschlichen Geweben und Zellen zur Herstellung eines Arzneimittels Deutsche Gesellschaft für Chirurgie
Leitfaden der Deutschen Gesellschaft für Chirurgie zur Guten Fachlichen Praxis (GFP) für die Entnahme von menschlichen Geweben und Zellen zur Herstellung eines Arzneimittels Deutsche Gesellschaft für Chirurgie
Wie werde ich Versandapotheker?
 Wie werde ich Versandapotheker? Zunächst einmal muss ein Versandapotheker überhaupt approbierter Apotheker sein: Das vom Europäischen Gerichtshof für zulässig gehaltene deutsche Fremdbesitzverbot gilt
Wie werde ich Versandapotheker? Zunächst einmal muss ein Versandapotheker überhaupt approbierter Apotheker sein: Das vom Europäischen Gerichtshof für zulässig gehaltene deutsche Fremdbesitzverbot gilt
zu Punkt... der 856. Sitzung des Bundesrates am 6. März 2009
 Bundesrat Drucksache 22/1/09 23.02.09 Empfehlungen der Ausschüsse EU - G - Wi zu Punkt.. der 856. Sitzung des Bundesrates am 6. März 2009 Vorschlag für eine Richtlinie des Europäischen Parlaments und des
Bundesrat Drucksache 22/1/09 23.02.09 Empfehlungen der Ausschüsse EU - G - Wi zu Punkt.. der 856. Sitzung des Bundesrates am 6. März 2009 Vorschlag für eine Richtlinie des Europäischen Parlaments und des
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV)
 Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) MPV Ausfertigungsdatum: 20.12.2001 Vollzitat: "Medizinprodukte-Verordnung vom 20. Dezember 2001 (BGBl. I S. 3854), die zuletzt durch Artikel
Verordnung über Medizinprodukte (Medizinprodukte-Verordnung - MPV) MPV Ausfertigungsdatum: 20.12.2001 Vollzitat: "Medizinprodukte-Verordnung vom 20. Dezember 2001 (BGBl. I S. 3854), die zuletzt durch Artikel
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Arzneimittelüberwachung in Deutschland. Jahresbericht der Länder
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Arzneimittelüberwachung in Deutschland Jahresbericht der Länder 2010 Inhaltsverzeichnis 1 Deskriptiver Teil... 3 1.1
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Arzneimittelüberwachung in Deutschland Jahresbericht der Länder 2010 Inhaltsverzeichnis 1 Deskriptiver Teil... 3 1.1
Entwurf eines Zweiten Gesetzes zur Änderung arzneimittelrechtlicher und anderer Vorschriften Ihr Az.: 112-40000-04/001
 Prof. Dr. med. Gerhard Ehninger Geschäftsführender Vorsitzender Hauptstadtbüro der DGHO Alexanderplatz 1 10178 Berlin Hauptstadtbüro der DGHO Alexanderplatz 1 10178 Berlin Tel. 030.27 87 60 89-0 Fax: 030.27
Prof. Dr. med. Gerhard Ehninger Geschäftsführender Vorsitzender Hauptstadtbüro der DGHO Alexanderplatz 1 10178 Berlin Hauptstadtbüro der DGHO Alexanderplatz 1 10178 Berlin Tel. 030.27 87 60 89-0 Fax: 030.27
Gesetz über die Spende, Entnahme und Übertragung von Organen und Geweben (Transplantationsgesetz - TPG)
 Gesetz über die Spende, Entnahme und Übertragung von Organen und Geweben (Transplantationsgesetz - TPG) TPG Ausfertigungsdatum: 05.11.1997 Vollzitat: "Transplantationsgesetz in der Fassung der Bekanntmachung
Gesetz über die Spende, Entnahme und Übertragung von Organen und Geweben (Transplantationsgesetz - TPG) TPG Ausfertigungsdatum: 05.11.1997 Vollzitat: "Transplantationsgesetz in der Fassung der Bekanntmachung
Bundeszentrale für gesundheitliche Aufklärung (BZgA), Köln 2014
 Bundeszentrale für gesundheitliche Aufklärung (BZgA), Köln 2014 Nur wer informiert ist, kann eine stabile Entscheidung zur Organ- und Gewebespende treffen Viele Menschen haben für sich noch keine Entscheidung
Bundeszentrale für gesundheitliche Aufklärung (BZgA), Köln 2014 Nur wer informiert ist, kann eine stabile Entscheidung zur Organ- und Gewebespende treffen Viele Menschen haben für sich noch keine Entscheidung
EG-Leitfaden der Guten Herstellungspraxis
 pharmind serie dokumentation EG-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe / mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) von Gert Auterhoff Neuausgabe EG-Leitfaden
pharmind serie dokumentation EG-Leitfaden der Guten Herstellungspraxis für Arzneimittel und Wirkstoffe / mit Arzneimittel- und Wirkstoffherstellungsverordnung (AMWHV) von Gert Auterhoff Neuausgabe EG-Leitfaden
Ausgewählte Aspekte des Transfusionsgesetzes
 Ausgewählte Aspekte des Transfusionsgesetzes Grundlagen und Änderungen World Health Organisation (WHO) - Motto - The overall goal of the National Regulatory Authorities is to ensure that only blood products
Ausgewählte Aspekte des Transfusionsgesetzes Grundlagen und Änderungen World Health Organisation (WHO) - Motto - The overall goal of the National Regulatory Authorities is to ensure that only blood products
Vorblatt. A. Problem und Ziel
 Vorblatt A. Problem und Ziel Mit dem Verordnungsentwurf werden die Anforderungen an Qualität und Sicherheit der Entnahme von Geweben und deren Übertragung zur Abwehr von Gefahren für die menschliche Gesundheit
Vorblatt A. Problem und Ziel Mit dem Verordnungsentwurf werden die Anforderungen an Qualität und Sicherheit der Entnahme von Geweben und deren Übertragung zur Abwehr von Gefahren für die menschliche Gesundheit
Grundlagen für die Ausübung des ärztlichen Berufs durch Ärztinnen und Ärzte mit Ausbildungsnachweisen aus dem Ausland
 Grundlagen für die Ausübung des ärztlichen Berufs durch Ärztinnen und Ärzte mit Ausbildungsnachweisen aus dem Ausland - 1 - Grundlagen für die Ausübung des ärztlichen Berufs durch Ärztinnen und Ärzte mit
Grundlagen für die Ausübung des ärztlichen Berufs durch Ärztinnen und Ärzte mit Ausbildungsnachweisen aus dem Ausland - 1 - Grundlagen für die Ausübung des ärztlichen Berufs durch Ärztinnen und Ärzte mit
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement. Stand der Revision: 13.11.
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 13.11.2013 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 13.11.2013 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Versandhandel mit Arzneimitteln
 Versandhandel mit Arzneimitteln Mit der sogenannten Fälschungsrichtlinie (RL 2011/62/EU) wurde ein neuer Artikel 85c in die Richtlinie 2001/83/EWG eingefügt. Er betrifft den Versandhandel mit Arzneimitteln
Versandhandel mit Arzneimitteln Mit der sogenannten Fälschungsrichtlinie (RL 2011/62/EU) wurde ein neuer Artikel 85c in die Richtlinie 2001/83/EWG eingefügt. Er betrifft den Versandhandel mit Arzneimitteln
Rechtliche Rahmenbedingungen für die Herstellung. sowie das Inverkehrbringen von hämatopoetischen
 Rechtliche Rahmenbedingungen für die Herstellung und das Inverkehrbringen von hämatopoetischen Stammzellpräparaten Dr. med. Markus Wiesneth 1 Dr. jur. Arnd Pannenbecker 2 1 Institut für Klinische Transfusionsmedizin
Rechtliche Rahmenbedingungen für die Herstellung und das Inverkehrbringen von hämatopoetischen Stammzellpräparaten Dr. med. Markus Wiesneth 1 Dr. jur. Arnd Pannenbecker 2 1 Institut für Klinische Transfusionsmedizin
Durch das Arzneimittelgesetz wird
 Neufassung des Gesetzes über den Verkehr mit Arzneimitteln (Arzneimittelgesetz AMG) Der Deutsche Bundestag hat mit Zustimmung des Bundesrates das Arzneimittelgesetz mit Beschluss vom 19.10.2012 geändert.
Neufassung des Gesetzes über den Verkehr mit Arzneimitteln (Arzneimittelgesetz AMG) Der Deutsche Bundestag hat mit Zustimmung des Bundesrates das Arzneimittelgesetz mit Beschluss vom 19.10.2012 geändert.
Regulative Aspekte der Aufbereitung chirurgischer Implantate
 Regulative Aspekte der Aufbereitung chirurgischer Implantate 35.Veranstaltung des Arbeitskreis Infektionsprophylaxe 16. Oktober 2012 in Potsdam 17.Oktober 2012 in Leipzig 1 Person Anja Fechner Dipl.-Ing.
Regulative Aspekte der Aufbereitung chirurgischer Implantate 35.Veranstaltung des Arbeitskreis Infektionsprophylaxe 16. Oktober 2012 in Potsdam 17.Oktober 2012 in Leipzig 1 Person Anja Fechner Dipl.-Ing.
AMWHV. Ausfertigungsdatum: 03.11.2006. Vollzitat:
 Verordnung über die Anwendung der Guten Herstellungspraxis bei der Herstellung von Arzneimitteln und Wirkstoffen und über die Anwendung der Guten fachlichen Praxis bei der Herstellung von Produkten menschlicher
Verordnung über die Anwendung der Guten Herstellungspraxis bei der Herstellung von Arzneimitteln und Wirkstoffen und über die Anwendung der Guten fachlichen Praxis bei der Herstellung von Produkten menschlicher
BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH. Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II
 1 von 5 BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II 57. Verordnung: Konformitätsbewertung von Medizinprodukten [CELEX-Nr.: 32000L0070, 32001L0104,
1 von 5 BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH Jahrgang 2004 Ausgegeben am 28. Jänner 2004 Teil II 57. Verordnung: Konformitätsbewertung von Medizinprodukten [CELEX-Nr.: 32000L0070, 32001L0104,
Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen
 Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen Dr. med. univ. Sebastian Werner 1,2 1 HygCen Austria GmbH, Bischofshofen 2 Abteilung für Hygiene, Sozial und Umweltmedizin, Ruhruniversität
Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen Dr. med. univ. Sebastian Werner 1,2 1 HygCen Austria GmbH, Bischofshofen 2 Abteilung für Hygiene, Sozial und Umweltmedizin, Ruhruniversität
Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B Stand
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne CMR-Eigenschaften der Kategorie 1A oder 1B Stand
GMP Wirkstoffe und Rezepetursubstanzen Probleme und Lösungsansätze. Dr. Mona Tawab Zentrallaboratorium Deutscher Apotheker
 GMP Wirkstoffe und Rezepetursubstanzen Probleme und Lösungsansätze Dr. Mona Tawab Zentrallaboratorium Deutscher Apotheker Die Pharma-Industrie in den Schlagzeilen Die Pharma-Industrie in den Schlagzeilen
GMP Wirkstoffe und Rezepetursubstanzen Probleme und Lösungsansätze Dr. Mona Tawab Zentrallaboratorium Deutscher Apotheker Die Pharma-Industrie in den Schlagzeilen Die Pharma-Industrie in den Schlagzeilen
Kapitel 1 Qualitätsmanagement 1 QUALITÄTSSICHERUNGSSYSTEM. Grundsätze
 Anlage 2 zur Bekanntmachung des Bundesministeriums für Gesundheit zu 2 Nr. 3 der Arzneimittel- und Wirkstoffherstellungsverordnung AMWHV vom 18. Juli 2008 (BAnz. S. 2798) Kapitel 1 des Teils 1 EG-GMP Leitfaden,
Anlage 2 zur Bekanntmachung des Bundesministeriums für Gesundheit zu 2 Nr. 3 der Arzneimittel- und Wirkstoffherstellungsverordnung AMWHV vom 18. Juli 2008 (BAnz. S. 2798) Kapitel 1 des Teils 1 EG-GMP Leitfaden,
Stammzellenforschung Karina Köppl LK Biologie
 Stammzellenforschung Karina Köppl LK Biologie 1.Was sind Stammzellen? Reparaturreserve des Körpers undifferenzierte Zellen von Menschen und Tieren Stammzellen sind in der Lage, sich zu teilen und neue
Stammzellenforschung Karina Köppl LK Biologie 1.Was sind Stammzellen? Reparaturreserve des Körpers undifferenzierte Zellen von Menschen und Tieren Stammzellen sind in der Lage, sich zu teilen und neue
Qualitätsbeauftragte für Hämotherapie Diskussionsbeitrag aus Erlangen
 Qualitätsbeauftragte für Hämotherapie Diskussionsbeitrag aus Erlangen PD Dr. R. Zimmermann Transfusionsmedizinische und Hämostaseologische Abteilung, Universitätsklinikum Erlangen Transfusionsmedizinische
Qualitätsbeauftragte für Hämotherapie Diskussionsbeitrag aus Erlangen PD Dr. R. Zimmermann Transfusionsmedizinische und Hämostaseologische Abteilung, Universitätsklinikum Erlangen Transfusionsmedizinische
Anhang 16 zum EG-Leitfaden für die Gute Herstellungspraxis (GMP) Zertifizierung durch eine sachkundige Person und Chargenfreigabe
 Anhang 16 zum EG-Leitfaden für die Gute Herstellungspraxis (GMP) Zertifizierung durch eine sachkundige Person und Chargenfreigabe 1. Anwendungsbereich 1.1 Dieser Anhang zum Leitfaden für die Gute Herstellungspraxis
Anhang 16 zum EG-Leitfaden für die Gute Herstellungspraxis (GMP) Zertifizierung durch eine sachkundige Person und Chargenfreigabe 1. Anwendungsbereich 1.1 Dieser Anhang zum Leitfaden für die Gute Herstellungspraxis
Ausfüllanleitung. Antrag auf Förderung der Aus- und Weiterbildung
 Förderprogramm A/W Förderperiode 2010 Ausfüllanleitung zum Antrag auf Förderung der Aus- und Weiterbildung nach der Richtlinie des Bundesministeriums für Verkehr, Bau und Stadtentwicklung über die Förderung
Förderprogramm A/W Förderperiode 2010 Ausfüllanleitung zum Antrag auf Förderung der Aus- und Weiterbildung nach der Richtlinie des Bundesministeriums für Verkehr, Bau und Stadtentwicklung über die Förderung
Aufbewahrungsfristen für ärztliche Unterlagen
 Aufbewahrungsfristen für ärztliche Unterlagen Nahezu alle ärztlichen Dokumente sind aufzubewahren - gemäß 10 (Dokumentationspflicht) Absatz 3 der Berufsordnung für Ärztinnen und Ärzte in Hessen Länger
Aufbewahrungsfristen für ärztliche Unterlagen Nahezu alle ärztlichen Dokumente sind aufzubewahren - gemäß 10 (Dokumentationspflicht) Absatz 3 der Berufsordnung für Ärztinnen und Ärzte in Hessen Länger
Genehmigung von autologen und gerichteten allogenen Stammzellzubereitungen aus Knochenmark, peripherem Blut bzw. Nabelschnurblut nach 21a AMG
 Genehmigung von autologen und gerichteten allogenen Stammzellzubereitungen aus Knochenmark, peripherem Blut bzw. Nabelschnurblut nach 21a AMG Margarethe Heiden Helga Marie Huber Paul-Ehrlich-Institut Paul-Ehrlich-Straße
Genehmigung von autologen und gerichteten allogenen Stammzellzubereitungen aus Knochenmark, peripherem Blut bzw. Nabelschnurblut nach 21a AMG Margarethe Heiden Helga Marie Huber Paul-Ehrlich-Institut Paul-Ehrlich-Straße
Immunologische Leistungen im Rahmen der Organtransplantation
 1 von 5 AWMF online Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften Standards der Deutschen Gesellschaft für Immungenetik (DGI) Immunologische Leistungen im Rahmen der Organtransplantation
1 von 5 AWMF online Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften Standards der Deutschen Gesellschaft für Immungenetik (DGI) Immunologische Leistungen im Rahmen der Organtransplantation
!"#$%&'()*& +,-&',.-)/,.012-34151"/46!1
 !"#$%&'()*& +,-&',.-)/,.012-34151"/46!1 111111111111111111111111111111111111117/8'1#9.:&1+$+;1"0),)*.01
!"#$%&'()*& +,-&',.-)/,.012-34151"/46!1 111111111111111111111111111111111111117/8'1#9.:&1+$+;1"0),)*.01
80% aller Teilnehmer werden von Behörden mindestens 1x pro Jahr inspiziert, wobei fast jeder vierte mindestens monatlich inspiziert wird.
 Audits 74 Firmen haben an unserer monatlichen Umfrage, dieses Mal zum Thema Audits, teilgenommen. Das große Interesse zeigt, dass dieses Thema immer noch ein Dauerbrenner ist. Hier finden Sie eine Kurzfassung
Audits 74 Firmen haben an unserer monatlichen Umfrage, dieses Mal zum Thema Audits, teilgenommen. Das große Interesse zeigt, dass dieses Thema immer noch ein Dauerbrenner ist. Hier finden Sie eine Kurzfassung
Nicht kommerzielle Studien mit Arzneimitteln. Arzneimittelforschung an Hochschulen hat für alle Beteiligten einen hohen Stellenwert.
 1 Nicht kommerzielle Studien mit Arzneimitteln Hans-Peter Hofmann, BMGS, Berlin Arzneimittelforschung an Hochschulen hat für alle Beteiligten einen hohen Stellenwert. Im politischen Raum belegen dies nicht
1 Nicht kommerzielle Studien mit Arzneimitteln Hans-Peter Hofmann, BMGS, Berlin Arzneimittelforschung an Hochschulen hat für alle Beteiligten einen hohen Stellenwert. Im politischen Raum belegen dies nicht
Deutsche Akkreditierungsstelle GmbH
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14103-01-02 nach DIN EN ISO/IEC 17025:2005 1 und den Richtlinien 90/385/EWG 2 und 93/42/EWG 3 als Prüflaboratorium Gültigkeitsdauer:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14103-01-02 nach DIN EN ISO/IEC 17025:2005 1 und den Richtlinien 90/385/EWG 2 und 93/42/EWG 3 als Prüflaboratorium Gültigkeitsdauer:
Aufbewahrungsfristen amtlicher Unterlagen in Apotheken (Stand 06/2012)
 Aufbewahrungsfristen amtlicher Unterlagen in Apotheken (Stand 06/2012) Dokumentation Erläuterung Aufbewahrungsfrist Anzeige der Nutzung von Standardzulassungen beim BfArM seit 1. Januar 2010, einmalig
Aufbewahrungsfristen amtlicher Unterlagen in Apotheken (Stand 06/2012) Dokumentation Erläuterung Aufbewahrungsfrist Anzeige der Nutzung von Standardzulassungen beim BfArM seit 1. Januar 2010, einmalig
Nicht-kommerzielle klinische Prüfungen
 Bekanntmachung des Bundesinstituts für Arzneimittel und Medizinprodukte, des Paul-Ehrlich Instituts und des Bundesministeriums für Gesundheit Vom 21. Oktober 2009 Nicht-kommerzielle klinische Prüfungen
Bekanntmachung des Bundesinstituts für Arzneimittel und Medizinprodukte, des Paul-Ehrlich Instituts und des Bundesministeriums für Gesundheit Vom 21. Oktober 2009 Nicht-kommerzielle klinische Prüfungen
Informationsblatt Widerspruch gegenüber einer Organ- und/oder Gewebe- und/oder Zellenentnahme
 Informationsblatt Widerspruch gegenüber einer Organ- und/oder Gewebe- und/oder Zellenentnahme Stand: Oktober 2014 Erläuterungen In Österreich sind Transplantation und Organspende im Organtransplantationsgesetz
Informationsblatt Widerspruch gegenüber einer Organ- und/oder Gewebe- und/oder Zellenentnahme Stand: Oktober 2014 Erläuterungen In Österreich sind Transplantation und Organspende im Organtransplantationsgesetz
(Langfassung) I. Vorbemerkungen
 Erläuterungen zum Antrag auf Ausstellung einer IHK-Fachkundebescheinigung nach dem Muster des Anhangs III zu Art. 8 Abs. 3 der Berufszugangs -Verordnung (EG) Nr. 1071/2011 (Langfassung) I. Vorbemerkungen
Erläuterungen zum Antrag auf Ausstellung einer IHK-Fachkundebescheinigung nach dem Muster des Anhangs III zu Art. 8 Abs. 3 der Berufszugangs -Verordnung (EG) Nr. 1071/2011 (Langfassung) I. Vorbemerkungen
Anwendungsbereiche von Rechtsvorschriften
 Kapitel 26.11.2007 10:04 Uhr Seite 1 /1 Übersicht Wenn Rechtsvorschriften Regelungen für Medizinprodukte enthalten, so bedeutet dies noch nichts für ihre Verbindlichkeit. Maßgeblich ist, von welcher Personengruppe
Kapitel 26.11.2007 10:04 Uhr Seite 1 /1 Übersicht Wenn Rechtsvorschriften Regelungen für Medizinprodukte enthalten, so bedeutet dies noch nichts für ihre Verbindlichkeit. Maßgeblich ist, von welcher Personengruppe
Nicht-kommerzielle klinische Prüfungen
 Bekanntmachung des Bundesinstituts für Arzneimittel und Medizinprodukte, des Paul-Ehrlich Instituts und des Bundesministeriums für Gesundheit Vom 21. Oktober 2009 Nicht-kommerzielle klinische Prüfungen
Bekanntmachung des Bundesinstituts für Arzneimittel und Medizinprodukte, des Paul-Ehrlich Instituts und des Bundesministeriums für Gesundheit Vom 21. Oktober 2009 Nicht-kommerzielle klinische Prüfungen
Espoir PV: Häufig gestellte Fragen. corlife ohg Feodor-Lynen-Str. 23 D-30625 Hannover. Phone: +49 (0)511 563 539 40 Telefax: +49 (0)511 563 539 55
 Espoir PV: Häufig gestellte Fragen corlife ohg Feodor-Lynen-Str. 23 D-30625 Hannover Phone: +49 (0)511 563 539 40 Telefax: +49 (0)511 563 539 55 info@colife.eu www.corlife.eu Technische Fragen Was ist
Espoir PV: Häufig gestellte Fragen corlife ohg Feodor-Lynen-Str. 23 D-30625 Hannover Phone: +49 (0)511 563 539 40 Telefax: +49 (0)511 563 539 55 info@colife.eu www.corlife.eu Technische Fragen Was ist
Vorsitzender Dr. med. Friedrich Overkamp
 Hauptstadtbüro der DGHO Alexanderplatz 1 10178 Berlin Per E-Mail Hauptstadtbüro der DGHO Alexanderplatz 1 10178 Berlin Tel. 030.27 87 60 89-0 Fax: 030.27 87 60 89-18 info@dgho.de Ausschuss für Gesundheit
Hauptstadtbüro der DGHO Alexanderplatz 1 10178 Berlin Per E-Mail Hauptstadtbüro der DGHO Alexanderplatz 1 10178 Berlin Tel. 030.27 87 60 89-0 Fax: 030.27 87 60 89-18 info@dgho.de Ausschuss für Gesundheit
Einfrieren von Nabelschnurblut. oder überflüssig?
 Einfrieren von Nabelschnurblut notwendig oder überflüssig? Einfrieren von Nabelschnurblut notwendig oder überflüssig? Impressum: Einfrieren von Nabelschnurblut notwendig oder überflüssig? Herausgeber,
Einfrieren von Nabelschnurblut notwendig oder überflüssig? Einfrieren von Nabelschnurblut notwendig oder überflüssig? Impressum: Einfrieren von Nabelschnurblut notwendig oder überflüssig? Herausgeber,
Hintergrundinformation
 Hintergrundinformation Häufige Fragen zur Organspende Wird meine Entscheidung zur Organspende registriert? Die Bereitschaft zur Organspende wird in Deutschland nicht registriert. Deshalb ist es wichtig,
Hintergrundinformation Häufige Fragen zur Organspende Wird meine Entscheidung zur Organspende registriert? Die Bereitschaft zur Organspende wird in Deutschland nicht registriert. Deshalb ist es wichtig,
Eltern-Broschüre. Hinweise zum Umgang mit Nabelschnurrestblut in katholischen Krankenhäusern. caritas
 Eltern-Broschüre Hinweise zum Umgang mit Nabelschnurrestblut in katholischen Krankenhäusern Katholischer Krankenhausverband der Diözese Osnabrück e.v. für die Diözese Osnabrück e.v. für die Diözese Münster
Eltern-Broschüre Hinweise zum Umgang mit Nabelschnurrestblut in katholischen Krankenhäusern Katholischer Krankenhausverband der Diözese Osnabrück e.v. für die Diözese Osnabrück e.v. für die Diözese Münster
EU-Zulassung für Großküchen
 DE EV 9999999 EG EU-Zulassung für Großküchen Strengere Auflagen für das Hygienemanagement Jetzt Klarheit über Zulassungspflicht verschaffen! Rechtliche Grundlagen der EU-Zulassung Welche Betriebe benötigen
DE EV 9999999 EG EU-Zulassung für Großküchen Strengere Auflagen für das Hygienemanagement Jetzt Klarheit über Zulassungspflicht verschaffen! Rechtliche Grundlagen der EU-Zulassung Welche Betriebe benötigen
MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT. Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung
 KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung DGSV Kongress 2010 Fulda 08.10.2010 Inhalt Compliance
KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung DGSV Kongress 2010 Fulda 08.10.2010 Inhalt Compliance
Merkblatt. für die Beantragung einer Versandhandelserlaubnis nach 11a ApoG
 Ennepe-Ruhr-Kreis Der Landrat 58452 Witten Merkblatt für die Beantragung einer Versandhandelserlaubnis nach 11a ApoG Die Erlaubnis zum Versand von Arzneimitteln richtet sich nach 11a Apothekengesetz. Demnach
Ennepe-Ruhr-Kreis Der Landrat 58452 Witten Merkblatt für die Beantragung einer Versandhandelserlaubnis nach 11a ApoG Die Erlaubnis zum Versand von Arzneimitteln richtet sich nach 11a Apothekengesetz. Demnach
Fragen & Antworten-Papier Pflichten und behördliche Überwachung von pharmazeutischen Unternehmern
 Fragen & Antworten-Papier Pflichten und behördliche Überwachung von pharmazeutischen Unternehmern Inhaltsverzeichnis: Einleitung: Was ist der Zweck des Fragen & Antworten Dokumentes?... 2 Frage 1: Wer
Fragen & Antworten-Papier Pflichten und behördliche Überwachung von pharmazeutischen Unternehmern Inhaltsverzeichnis: Einleitung: Was ist der Zweck des Fragen & Antworten Dokumentes?... 2 Frage 1: Wer
EUROPÄISCHES PARLAMENT
 EUROPÄISCHES PARLAMENT 1999 2004 Ausschuss für Umweltfragen, Volksgesundheit und Verbraucherpolitik 5. März 2003 PE 319.423/32-159 ÄNRUNGSANTRÄGE 32-159 Entwurf eines Berichts (PE 319.423) Peter Liese
EUROPÄISCHES PARLAMENT 1999 2004 Ausschuss für Umweltfragen, Volksgesundheit und Verbraucherpolitik 5. März 2003 PE 319.423/32-159 ÄNRUNGSANTRÄGE 32-159 Entwurf eines Berichts (PE 319.423) Peter Liese
AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6
 AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6 Information der Arzneimittelkommission der deutschen Heilpraktiker bezüglich der arzneimittelrechtlichen Änderungen zur Anzeigepflicht der Herstellung von
AMK-AMG-Herstell-Anz-2010-01-25 Seite 1 von 6 Information der Arzneimittelkommission der deutschen Heilpraktiker bezüglich der arzneimittelrechtlichen Änderungen zur Anzeigepflicht der Herstellung von
Inhaltsverzeichnis VII
 Inhaltsverzeichnis A. Einleitung... 1 I. Die Bedeutung der Transplantationsmedizin... 1 II. Schnittstellen Organe und Gewebe... 3 III. Gegenstand und Gang der Untersuchung... 4 B. Medizinische Grundlagen
Inhaltsverzeichnis A. Einleitung... 1 I. Die Bedeutung der Transplantationsmedizin... 1 II. Schnittstellen Organe und Gewebe... 3 III. Gegenstand und Gang der Untersuchung... 4 B. Medizinische Grundlagen
Änderungen der MPBetreibV 2014
 Änderungen der MPBetreibV 2014 3 Instandhaltung von Medizinprodukten (1) Die Instandhaltung von Medizinprodukten umfasst insbesondere Instandhaltungsmaßnahmen und die Instandsetzung. Instandhaltungsmaßnahmen
Änderungen der MPBetreibV 2014 3 Instandhaltung von Medizinprodukten (1) Die Instandhaltung von Medizinprodukten umfasst insbesondere Instandhaltungsmaßnahmen und die Instandsetzung. Instandhaltungsmaßnahmen
1 Aufgaben des Bundesamtes für Verbraucherschutz und Lebensmittelsicherheit. EGGenTDurchfG. Ausfertigungsdatum: 22.06.2004.
 Gesetz zur Durchführung der Verordnungen der Europäischen Gemeinschaft oder der Europäischen Union auf dem Gebiet der Gentechnik und über die Kennzeichnung ohne Anwendung gentechnischer Verfahren hergestellter
Gesetz zur Durchführung der Verordnungen der Europäischen Gemeinschaft oder der Europäischen Union auf dem Gebiet der Gentechnik und über die Kennzeichnung ohne Anwendung gentechnischer Verfahren hergestellter
Warum? Orthopäden; 5336. Dermatologen; 3342. Urologen; 2674. Chirurgen; 3976. Neurochirurgen; 491. Gynäkologen; 9875
 Können Medizinprodukte ohne CE-Kennzeichnung betrieben werden? Warum? Urologen; 2674 Neurochirurgen; 491 MKG; 1027 Allgemeinärzte/ praktische Ärzte; 40.246 Orthopäden; 5336 Chirurgen; 3976 Anästhesisten;
Können Medizinprodukte ohne CE-Kennzeichnung betrieben werden? Warum? Urologen; 2674 Neurochirurgen; 491 MKG; 1027 Allgemeinärzte/ praktische Ärzte; 40.246 Orthopäden; 5336 Chirurgen; 3976 Anästhesisten;
RICHTLINIE 2003/94/EG DER KOMMISSION
 L 262/22 RICHTLINIE 2003/94/EG R KOMMISSION vom 8. Oktober 2003 zur Festlegung der Grundsätze und Leitlinien der Guten Herstellungspraxis für Humanarzneimittel und für zur Anwendung beim Menschen bestimmte
L 262/22 RICHTLINIE 2003/94/EG R KOMMISSION vom 8. Oktober 2003 zur Festlegung der Grundsätze und Leitlinien der Guten Herstellungspraxis für Humanarzneimittel und für zur Anwendung beim Menschen bestimmte
Freier Mitarbeitervertrag für einen Qualitätsbeauftragten für die Überwachung des QM-Systems der Anwendung von Blutprodukten.
 Freier Mitarbeitervertrag für einen Qualitätsbeauftragten für die Überwachung des QM-Systems der Anwendung von Blutprodukten zwischen dem Krankenhaus/der Klinik (genaue Adresse) - nachfolgend Krankenhaus
Freier Mitarbeitervertrag für einen Qualitätsbeauftragten für die Überwachung des QM-Systems der Anwendung von Blutprodukten zwischen dem Krankenhaus/der Klinik (genaue Adresse) - nachfolgend Krankenhaus
Aktuelles aus dem Medizinprodukterecht
 KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT IN KOOPERATION MIT BERLIN DÜSSELDORF Aktuelles aus dem Medizinprodukterecht DGSV-Kongress 2014 Fulda 09.10.2014 Inhalt 1. AUSBLICK
KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT IN KOOPERATION MIT BERLIN DÜSSELDORF Aktuelles aus dem Medizinprodukterecht DGSV-Kongress 2014 Fulda 09.10.2014 Inhalt 1. AUSBLICK
Prof. Dr. Werner Fresenius / Vorsitzender AG AAMP. Tierarzneimittelbereich: Dr. Heinrich Bottermann / Vorsitzender AG AfAM. <Oberste Landesbehörde>
 Dokumenten-Nr.: 07110702 Verfahrensanweisung Gültig ab: Zentralstelle der Länder für Gesundheitsschutz bei Arzneimiteln und Medizinprodukten 1/5 Titel: Site Master File (SMF) Geltungsbereich: Inspektorat
Dokumenten-Nr.: 07110702 Verfahrensanweisung Gültig ab: Zentralstelle der Länder für Gesundheitsschutz bei Arzneimiteln und Medizinprodukten 1/5 Titel: Site Master File (SMF) Geltungsbereich: Inspektorat
Beschluss des Gemeinsamen Bundesausschusses gemäß 2. Kapitel 14 Absatz 4 Spiegelstrich 2 der Verfahrensordnung des Gemeinsamen Bundesausschusses
 Beschluss des Gemeinsamen Bundesausschusses gemäß 2. Kapitel 14 Absatz 4 Spiegelstrich 2 der Verfahrensordnung des Gemeinsamen Bundesausschusses Der Gemeinsame Bundesausschuss hat im Rahmen der Bewertung
Beschluss des Gemeinsamen Bundesausschusses gemäß 2. Kapitel 14 Absatz 4 Spiegelstrich 2 der Verfahrensordnung des Gemeinsamen Bundesausschusses Der Gemeinsame Bundesausschuss hat im Rahmen der Bewertung
GMP-Vereinbarung betreffend XXXX
 Dokumenten-Nr.: EVxxxx-Vyy Gültig ab: Autorisierte Kopie Nr.: hier z.b. Herstellung und Produkt eintragen Zwischen hier Name des AUFTRAGGEBERS eintragen im folgenden AUFTRAGGEBER (AG) genannt und hier
Dokumenten-Nr.: EVxxxx-Vyy Gültig ab: Autorisierte Kopie Nr.: hier z.b. Herstellung und Produkt eintragen Zwischen hier Name des AUFTRAGGEBERS eintragen im folgenden AUFTRAGGEBER (AG) genannt und hier
Übersicht über die Neuregelung der Verbraucherrechte zum 13. Juni 2014
 Übersicht über die Neuregelung der Verbraucherrechte zum 13. Juni 2014 Geschäftsbereich Recht Deutsches Apothekerhaus Jägerstraße 49/50 10117 Berlin Telefon: 030 / 400 04-0 Telefax: 030 / 400 04-598 E-Mail:
Übersicht über die Neuregelung der Verbraucherrechte zum 13. Juni 2014 Geschäftsbereich Recht Deutsches Apothekerhaus Jägerstraße 49/50 10117 Berlin Telefon: 030 / 400 04-0 Telefax: 030 / 400 04-598 E-Mail:
Stammzellen. Therapie der Zukunft?
 Stammzellen Therapie der Zukunft? Was sind Stammzellen? Embryo, aus embryonalen Stammzellen bestehend Stammzellen sind Ausgangszellen für die Bildung aller Gewebe und Organe, aus denen ein Lebewesen besteht
Stammzellen Therapie der Zukunft? Was sind Stammzellen? Embryo, aus embryonalen Stammzellen bestehend Stammzellen sind Ausgangszellen für die Bildung aller Gewebe und Organe, aus denen ein Lebewesen besteht
Allgemeine Regelungen
 Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie), aufgestellt gemäß 12a u. 18 Transfusionsgesetz von der Bundesärztekammer im Einvernehmen mit
Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie), aufgestellt gemäß 12a u. 18 Transfusionsgesetz von der Bundesärztekammer im Einvernehmen mit
KÖRPERSCHAFT DES ÖFFENTLICHEN RECHTS. Satzung. für ein Qualitätsmanagement in tierärztlichen Praxen, Kliniken und anderen tierärztlichen Einrichtungen
 LANDESTIERÄRZTEKAMMER HESSEN KÖRPERSCHAFT DES ÖFFENTLICHEN RECHTS Satzung für ein Qualitätsmanagement in tierärztlichen Praxen, Kliniken und anderen tierärztlichen Einrichtungen gemäß 6 Abs. 4 der Berufsor
LANDESTIERÄRZTEKAMMER HESSEN KÖRPERSCHAFT DES ÖFFENTLICHEN RECHTS Satzung für ein Qualitätsmanagement in tierärztlichen Praxen, Kliniken und anderen tierärztlichen Einrichtungen gemäß 6 Abs. 4 der Berufsor
Prüfpräparate was ist zu beachten? Hämatologie im Wandel Studienupdate und GCP-Training
 Prüfpräparate was ist zu beachten? Hämatologie im Wandel Studienupdate und GCP-Training Nadja Panzilius, Klinik-Apotheke Universitätsklinikum (AöR) der TU Dresden Frankfurt/ Main, 28.02.2015 Organigramm
Prüfpräparate was ist zu beachten? Hämatologie im Wandel Studienupdate und GCP-Training Nadja Panzilius, Klinik-Apotheke Universitätsklinikum (AöR) der TU Dresden Frankfurt/ Main, 28.02.2015 Organigramm
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ)
 Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Gesetz zum Schutze der Berufsbezeichnung Ingenieur und Ingenieurin (Ingenieurgesetz - IngG)
 Gesetz zum Schutze der Berufsbezeichnung Ingenieur und Ingenieurin (Ingenieurgesetz - IngG) Art. 1 (1) Die Berufsbezeichnung "Ingenieur und Ingenieurin" allein oder in einer Wortverbindung darf führen,
Gesetz zum Schutze der Berufsbezeichnung Ingenieur und Ingenieurin (Ingenieurgesetz - IngG) Art. 1 (1) Die Berufsbezeichnung "Ingenieur und Ingenieurin" allein oder in einer Wortverbindung darf führen,
- 2 - - 3 - B. Lösung Erlass der Rechtsverordnung. C. Alternativen Keine. D. Haushaltsausgaben ohne Vollzugsaufwand Keine.
 Vorblatt Verordnung zur Umsetzung der Regelungen der Europäischen Union über die Anerkennung von in anderen Mitgliedstaaten ausgestellten ärztlichen oder zahnärztlichen Verschreibungen von Arzneimitteln
Vorblatt Verordnung zur Umsetzung der Regelungen der Europäischen Union über die Anerkennung von in anderen Mitgliedstaaten ausgestellten ärztlichen oder zahnärztlichen Verschreibungen von Arzneimitteln
ENTWURF EINES BERICHTS
 EUROPÄISCHES PARLAMENT 2009 2014 Ausschuss für Umweltfragen, öffentliche Gesundheit und Lebensmittelsicherheit 9.3.2012 2011/2307(INI) ENTWURF EINES BERICHTS über freiwillige und unbezahlte Spenden von
EUROPÄISCHES PARLAMENT 2009 2014 Ausschuss für Umweltfragen, öffentliche Gesundheit und Lebensmittelsicherheit 9.3.2012 2011/2307(INI) ENTWURF EINES BERICHTS über freiwillige und unbezahlte Spenden von
Generative medizinische Versorgung
 Gesetzentwurf zur regenerativen medizinischen Versorgung Ausgerichtet auf die regenerative Medizin und Zelltherapie. regenerative Medizin bedeutet, krankes Gewebe bei einem Patienten zu ersetzen oder zu
Gesetzentwurf zur regenerativen medizinischen Versorgung Ausgerichtet auf die regenerative Medizin und Zelltherapie. regenerative Medizin bedeutet, krankes Gewebe bei einem Patienten zu ersetzen oder zu
Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen
 Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen Bibliografische Information der Deutschen Bibliothek Die Deutsche Bibliothek verzeichnet diese
Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen Bibliografische Information der Deutschen Bibliothek Die Deutsche Bibliothek verzeichnet diese
BMWi Berlin, 9. Juli 2009 IV A 3 32 71 00 / 11 Hausruf: 73 16
 BMWi Berlin, 9. Juli 2009 IV A 3 32 71 00 / 11 Hausruf: 73 16 V E R M E R K Betr.: Interpretation des Begriffs Inverkehrbringen im Sinne der Ökodesign-Richtlinie Hinweis: Die nachfolgende Darstellung beinhaltet
BMWi Berlin, 9. Juli 2009 IV A 3 32 71 00 / 11 Hausruf: 73 16 V E R M E R K Betr.: Interpretation des Begriffs Inverkehrbringen im Sinne der Ökodesign-Richtlinie Hinweis: Die nachfolgende Darstellung beinhaltet
Gesetz über das Fahrlehrerwesen (Fahrlehrergesetz - FahrlG)
 Gesetz über das Fahrlehrerwesen (Fahrlehrergesetz - FahrlG) FahrlG Ausfertigungsdatum: 25.08.1969 Vollzitat: "Fahrlehrergesetz vom 25. August 1969 (BGBl. I S. 1336), das durch Artikel 2 des Gesetzes vom
Gesetz über das Fahrlehrerwesen (Fahrlehrergesetz - FahrlG) FahrlG Ausfertigungsdatum: 25.08.1969 Vollzitat: "Fahrlehrergesetz vom 25. August 1969 (BGBl. I S. 1336), das durch Artikel 2 des Gesetzes vom
9.5 Medizinprodukte-Betreiberverordnung - MPBetreibV
 9.5 -Betreiberverordnung - MPBetreibV Die -Betreiberverordnung (MPBetreibV) regelt das Errichten, Betreiben und Anwenden von n und von Zubehör für. Zubehör sind Gegenstände, Stoffe, Zubereitungen aus Stoffen
9.5 -Betreiberverordnung - MPBetreibV Die -Betreiberverordnung (MPBetreibV) regelt das Errichten, Betreiben und Anwenden von n und von Zubehör für. Zubehör sind Gegenstände, Stoffe, Zubereitungen aus Stoffen
Umsetzung der Hygienerichtlinien
 Umsetzung der Hygienerichtlinien Andrea Percht, MBA Hygienefachkraft allgemein beeidete und gerichtlich zertifizierte Sachverständige für f r Hygiene Richtlinien Diese Leitlinie wurde auf Basis des Medizinproduktegesetzes
Umsetzung der Hygienerichtlinien Andrea Percht, MBA Hygienefachkraft allgemein beeidete und gerichtlich zertifizierte Sachverständige für f r Hygiene Richtlinien Diese Leitlinie wurde auf Basis des Medizinproduktegesetzes
Verordnung, mit der die Gewebeentnahmeeinrichtungsverordnung geändert wird. Vorblatt. Ziele. Inhalt
 1 von 5 Verordnung, mit der die Gewebeentnahmeeinrichtungsverordnung geändert wird Einbringende Stelle: BMG Laufendes Finanzjahr: 2014 Inkrafttreten/ Wirksamwerden: 2014 Vorblatt Ziele - Erhöhung der Sicherheit
1 von 5 Verordnung, mit der die Gewebeentnahmeeinrichtungsverordnung geändert wird Einbringende Stelle: BMG Laufendes Finanzjahr: 2014 Inkrafttreten/ Wirksamwerden: 2014 Vorblatt Ziele - Erhöhung der Sicherheit
Gesetz über explosionsgefährliche Stoffe. Begründet von. ehemals Ministerialdirigent im Bundesministerium für Arbeit und Sozialordnung
 Sprengstoffgesetz Gesetz über explosionsgefährliche Stoffe Ergänzbare Textsammlung und Kommentar Begründet von Dr. Hans Schmatz ehemals Ministerialdirektor im Bayerischen Staatsministerium für Arbeit und
Sprengstoffgesetz Gesetz über explosionsgefährliche Stoffe Ergänzbare Textsammlung und Kommentar Begründet von Dr. Hans Schmatz ehemals Ministerialdirektor im Bayerischen Staatsministerium für Arbeit und
Die Medikamentenproduktion und -logistik und ihre Planung. Dr. Gesine Bejeuhr
 Die Medikamentenproduktion und -logistik und ihre Planung Dr. Gesine Bejeuhr Chemische Wirkstoffproduktion sollte so aussehen Sanofi Seite 2 und darf nicht so aussehen Keine Option, um kurzfristig Ersatz
Die Medikamentenproduktion und -logistik und ihre Planung Dr. Gesine Bejeuhr Chemische Wirkstoffproduktion sollte so aussehen Sanofi Seite 2 und darf nicht so aussehen Keine Option, um kurzfristig Ersatz
AWMF Tagung am 26./27.04.2013 in Würzburg
 AWMF Tagung am 26./27.04.2013 in Würzburg Fall: Haftung eines Pathologen bei Verwechslung einer Gewebeprobe mit der Konsequenz zweier unnötiger operativer Eingriffe im Hinblick auf ein unterstelltes Mamarkarzinom
AWMF Tagung am 26./27.04.2013 in Würzburg Fall: Haftung eines Pathologen bei Verwechslung einer Gewebeprobe mit der Konsequenz zweier unnötiger operativer Eingriffe im Hinblick auf ein unterstelltes Mamarkarzinom
Klinische Prüfungen von Arzneimitteln aktuelle Anforderungen
 Klinische Prüfungen von Arzneimitteln aktuelle Anforderungen Aus der Sicht der Überwachungsbehörde Sabine Hofsäss (Regierungspräsidium Karlsruhe) Gemeinsame Ziele: Sicherheit, Rechte und Wohl der Patienten
Klinische Prüfungen von Arzneimitteln aktuelle Anforderungen Aus der Sicht der Überwachungsbehörde Sabine Hofsäss (Regierungspräsidium Karlsruhe) Gemeinsame Ziele: Sicherheit, Rechte und Wohl der Patienten
Aufbewahrung von Waffen
 Aufbewahrung von Waffen Der tragische Amoklauf von Winnenden gibt dem Deutschen Schützenbund e.v. erneut Veranlassung, unsere Sportschützinnen und Sportschützen nachdrücklich darauf hinzuweisen, dass eine
Aufbewahrung von Waffen Der tragische Amoklauf von Winnenden gibt dem Deutschen Schützenbund e.v. erneut Veranlassung, unsere Sportschützinnen und Sportschützen nachdrücklich darauf hinzuweisen, dass eine
Inhaltsverzeichnis I Allgemeine Bestimmungen
 Inhaltsverzeichnis I Allgemeine Bestimmungen 1 Basis-VO (EG) Nr. 178/2002, SARAH STÜRENBURG 1.1 Art. 1 Ziel und Anwendungsbereich 1.2 Art. 2 Definition von Lebensmittel 1.3 Artikel 3 Sonstige Definitionen
Inhaltsverzeichnis I Allgemeine Bestimmungen 1 Basis-VO (EG) Nr. 178/2002, SARAH STÜRENBURG 1.1 Art. 1 Ziel und Anwendungsbereich 1.2 Art. 2 Definition von Lebensmittel 1.3 Artikel 3 Sonstige Definitionen
Muster-Weiterbildungsordnung der Bundeszahnärztekammer Zahnarzt für öffentliches Gesundheitswesen
 Muster-Weiterbildungsordnung der Bundeszahnärztekammer Zahnarzt für öffentliches Gesundheitswesen Beschluss des Vorstandes vom 30.05.1996 geändert mit Beschluss vom 27.03.1998 und 23.05.03 l. Abschnitt
Muster-Weiterbildungsordnung der Bundeszahnärztekammer Zahnarzt für öffentliches Gesundheitswesen Beschluss des Vorstandes vom 30.05.1996 geändert mit Beschluss vom 27.03.1998 und 23.05.03 l. Abschnitt
Liechtensteinisches Landesgesetzblatt Jahrgang 2015 Nr... ausgegeben am... 2015
 Referendumsvorlage 232.11 Liechtensteinisches Landesgesetzblatt Jahrgang 2015 Nr.... ausgegeben am... 2015 Gesetz vom 3. September 2015 über die Abänderung des Markenschutzgesetzes Dem nachstehenden vom
Referendumsvorlage 232.11 Liechtensteinisches Landesgesetzblatt Jahrgang 2015 Nr.... ausgegeben am... 2015 Gesetz vom 3. September 2015 über die Abänderung des Markenschutzgesetzes Dem nachstehenden vom
Antrag auf Erteilung einer
 Antrag auf Erteilung einer Kreis Euskirchen Erlaubnis für den gewerblichen Güterkraftverkehr Der Landrat Abt. 36 Straßenverkehr Gemeinschaftslizenz (Art. 4 VO (EG) 1072 / 2009) Jülicher Ring 32 53879 Euskirchen
Antrag auf Erteilung einer Kreis Euskirchen Erlaubnis für den gewerblichen Güterkraftverkehr Der Landrat Abt. 36 Straßenverkehr Gemeinschaftslizenz (Art. 4 VO (EG) 1072 / 2009) Jülicher Ring 32 53879 Euskirchen
