(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
|
|
|
- Pia Grosser
- vor 6 Jahren
- Abrufe
Transkript
1 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem mit 4n2 Elektronen (n = 1 nach ückel). Es ist also aromatisch und daher besonders stabil. d) Anmerkung: Keinen Einfluss hat z.. die Zahl der Atome in der Verbindung oder die Ladung der am System beteiligten Atome. Cyclopentadienyl-Kation (Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.) Das Kation ist instabiler als das entsprechende negativ geladene Anion; daher ist es sehr reaktiv. Grund: vier π-elektronen, antiaromatisch (nicht aromatisch kann auch als richtig anerkannt werden) e) Die substituierte Dicyanoverbindung des 1,3-Cyclopentadiens ist saurer als die unsubstituierte Verbindung. Grund: Substituenten entziehen dem Ring Elektronen (-I-Effekt bzw. M-Effekt); C--indung wird geschwächt bzw. entstehendes Anion wird stabilisiert. f) FeX 2 2 ac 5 5 (C 5 5 ) 2 Fe 2 ax (X = alogen) g) Ferrocen (analog zu enzol (enzen)) Doppelkegel-Struktur oder Sandwich-Struktur 1
2 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen h) (1) (2) Anmerkung: Die Substitution wäre auch an beiden Cp - Ringen möglich. i) Reaktionstyp beider Umsetzungen: Elektrophile Substitution am Aromaten (1) hier: entsprechend einer Friedel-Crafts-Alkylierung am enzol (R = C 3 ) Erster Schritt : Aktivierung des Kohlenstoff-Atoms im alogenalkan: RC 2 Cl AlCl 3 RC 2 ClAlCl 3 Zweiter Schritt : (2) hier: entsprechend einer Sulfonierung am enzol: SO 3 aus der konzentrierten Schwefelsäure ist der elektrophile Partner. Durch die große elektronenanziehende Wirkung der drei Sauerstoffatome ist das Schwefel-Atom stark elektrophil. Es greift den elektronenreichen Cp-Ring direkt an. Danach entsteht durch Transfer des Protons das Sulfonsäurederivat. 2
3 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen eispiel 2: a) Die Verbindung muss: 1. zyklisch sein, 2. planar sein, 3. vollständig konjugiert sein, 4. die ückel-regel erfüllen, d.h. 4n 2 π-elektronen besitzen (n = 0, 1, 2,...) b) Es erfüllen alle Regeln und sind aromatisch: (ii) Azulen (10 π-elektronen), (iv) das Pyridinium-Kation (6 π-elektronen), (v) Koffein (10 π- Elektronen bzw. 6 π-elektronen im Fünfring-Untersystem) icht aromatisch oder antiaromatisch sind: das (i) Allyl-Anion (4 π-elektronen; verletzt Regel 4 und Regel 1), (iii) 1-Pyrrolium-Kation (protoniertes Pyrrol) (verletzt Regel 3) eispiel 3: a) Alkene: Elektrophile Addition (z.. r 2 ), aber kaum Substitution. Aromaten: Kaum elektrophile Addition, da dann der aromatische Ring zerstört werden würden, hier daher elektrophile Substitution; insgesamt trägere Reaktionen. b) Aromaten erfüllen die ückel-regel: Sind im Ring eines Systems (4n2) π-elektronen enthalten, so ist das System besonders stabil und damit aromatisch. c) Es ensteht Cyclopentadienyl-atrium, das 6 π-elektronen (je ein Elektron von jedem Kohlenstoff-Atom und ein zusätzliches Elektron wegen der negativen Ladung) enthält und somit aromatisch ist. Das Anion ist planar, damit die p-orbitale gut miteinander überlappen können. d) eim Cyclobutadien werden nur vier Elektronen von den Kohlenstoff-Atomen geliefert; es fehlen also zwei Elektronen (zwei negative Ladungen) zur Erfüllung der ückel-regel: Ein Cyclobutadien-Dianion sollte daher aromatisch sein. Das gleiche gilt für ein Cyclobutadien- Dikation mit zwei π-elektronen. e) Auch in diesem planaren Ringsystem sind konjugierte und delokalisierte 4 n 2 = 6 π-elektronen enthalten. Die Analogie zeigt sich jedoch nur in den physikalischen Eigenschaften. Chemisch ist orazin wesentlich reaktionsfähiger und addiert beispielsweise Cl: Cl Cl 3 3
4 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen eispiel 4: Cl Cl 2 3 Cl Arin Als Zwischenprodukt entsteht ein sehr reaktives Arin, das sofort weiterreagiert: Anmerkung: Ohne 14 -C-Dotierung sind die beiden Produkte identisch. Cl 3 C C 3 2 ( 3 ) keine Arinbildung möglich, keine Reaktion eispiel 5: a) C 3 C 3 C 3 C 3 C2C3 C 2 C 3 3 C C 3 C 2 C 3 o-ethyltoluol m-ethyltoluol p-ethyltoluol 1,3,5-Trimethylbenzol 1,2-Ethylmethylbenzol 1,3-Ethylmethylbenzol 1,4-Ethylmethylbenzol Mesitylen C 3 C3 C 3 C3 C 2 C 2 C 3 3 C C 3 C C 3 C 3 1,2,3- Trimethylbenzol 2,4-Dimethyltoluol 1,2,4-Trimethylbenzol n-propylbenzol 1-Phenylpropan Cumol Isopropylbenzol 2-Phenylpropan 4
5 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen b) Gesuchtes Isomer A: C 3 C 2 C 3 romderivate: C 3 C 2 r C 3 r 2, h ν C 2 C 3 C 2 C 3 1/2 CrC 3 1/2 C 3 C 3 r 2 (Fe) r C 3 C 2 C 3 C 2 C 3 r C1/C2 C 2 C 3 r 2 (Fe) r C 3 r C 3 C 3 r r C 3 r r r r C 2 C 3 C 2 C 3 C 2 C 3 C 2 C 3 D1/D2/D3/D4 5
6 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen eispiel 6: a) schwach sauer:, stark sauer (hier ist die (C 3 ) 2 -Gruppe protoniert): C 3 C C 3 C C3 3 C 3 C 3 C 3 C 3 O 2 ortho- Angriff C 3 C 3 O 2 C 3 C C 3 C C 3 3 C C 3 C O 2 O 2 C 3 C 3 C 3 O 2 C 3 C 3 C 3 C 3 C 3 C 3 C meta- Angriff C 3 C O 2 C 3 O 2 O C 2 C 3 eim ortho-angriff (bzgl. der Dimethylammoniumgruppe) tritt eine äußerst ungünstige Resonanzstruktur auf, bei der das Kohlenstoff-Atom neben dem ohnehin schon positiv geladenen Stickstoff-Atom zusätzlich noch eine positive Formalladung trägt. Diese Resonanzstruktur ist so ungünstig, dass in stark saurer Lösung ausschließlich das meta-produkt entsteht, bei dessen ildung eine solche Resonanzstruktur nicht auftritt. b), c) (C 3 ) 2 (C 3 ) 2 O 2 3 Zn, 6 Cl 2-3 ZnCl 2, O C 3 C 3 D 6
7 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen (C 3 ) 2 C 3 E eispiel 7: a) ach Lewis (1923) sind Säuren Elektronenpaar-Akzeptoren, z.. ein Molekül oder Ion mit unvollständiger Edelgaskonfiguration ( Elektronenmangelverbindungen, Elektronenlücke ). Lewis-Säuren nehmen ein von einer Lewis-ase (Elektronenpaar-Donatoren) zur Verfügung gestelltes Elektronenpaar auf. eispiel (Typ MeX 3 ): F 3, AlCl 3, FeCl 3, etc. b) Reaktionsmechanismus: Elektrophile Alkylierung (Friedel-Crafts-Reaktion) 1. Schritt: Das aktive Reagenz entsteht RCl AlCl 3 R AlCl 4 (R = C 3 (C 2 ) 2 C 2 ; Lewis-Säure: z.. AlCl 3 ) 2. Schritt: Zwischenprodukt (elektrophiler Angriff) δ δ R ClAlCl 3 R AlCl 4 3. Schritt: ildung des Endprodukts (Protonenabgabe und Aromat-ildung) R R c) Die ildung der enzolalkylverbindung aktiviert den Ring (I-Effekt) zur ildung polysubstituierter Alkylverbindungen. Das heißt, die Monoalkylbenzolverbindung ist reaktiver als das enzol selbst. Ein großer Überschuss von enzol schränkt die ildung von polysubstituierten Verbindungen ein. d) Das elektrophile Reagenz der Alkylierung ist ein komplex gebundenes Carbokation (Carbeniumion). Die Stabilität der Carbokationen ist bei sek. bzw. tert. Alkylrest gegenüber der gestreckten Kette erhöht. Durch Umlagerungen bildet sich aus dem primären Alkylrest der stabilere tert.-utylrest aus: C 3 3 C C C 3 stabileres Carbokation 7
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Aromatische Kohlenwasserstoffe
 Benzol: 6 6 (Faraday 1825) Aromatische Kohlenwasserstoffe OI_folie201 Vorgeschlagene Konstitutionen von Benzol 1,3,5-yclohexatrien-Struktur 1858 Kekulé Erklärt nicht, warum es nur drei regioisomere disubstituierte
Benzol: 6 6 (Faraday 1825) Aromatische Kohlenwasserstoffe OI_folie201 Vorgeschlagene Konstitutionen von Benzol 1,3,5-yclohexatrien-Struktur 1858 Kekulé Erklärt nicht, warum es nur drei regioisomere disubstituierte
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Lösungen 3. Übungsblatt SS 2002
 Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Name, Vorname: Matrikelnummer: Studienrichtung: Fragen auf den folgenden Seiten: Musterlösung zur Klausur zur Experimentalvorlesung Organische Chemie
 rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
rganisch-chemisches nstitut Fakultät für Chemie und Geowissenschaften Universität eidelberg 23. Juni 2015 Musterlösung zur Klausur zur Experimentalvorlesung rganische Chemie von Prof. Stephen ashmi Name,
2. Elektroneneffekte in den organischen Molekülen
 2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
2. Elektroneneffekte in den organischen Molekülen Induktive und mesomere Effekte Die Ladungsverteilung in einer Kohlenwasserstoffkette wird durch Substituenten (Halogen, OH, NH 2 usw.) beeinflusst. Man
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Bundesrealgymnasium Imst. Chemie Klasse 8. Aromaten und deren Reaktionen
 Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 und deren Reaktionen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2016
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
3. Aromatische Verbindungen Benzol(en)
 3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
3. Aromatische Verbindungen Benzol(en) Benzol erweist sich merkwürdigerweise als ungewöhnlich stabil gegen viele angreifende Reagenzien. So finden die typischen Additionen an die Doppelbindungen nicht
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
1 Lösung 5 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Falls Sie Fragen zur Vorlesung/Übung/generellen Konzepten haben schreiben
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Br 1. Auch bei der folgenden Kombination, sind die Strukturen nicht identisch, sie lassen sich durch Drehung nicht ineinander überführen.
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Organische Chemie I Molekül der Woche - Azulen
 I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
I Molekül der Woche - Azulen 1 I Alkine C n H 2n-2 Bindungslängen Der C-H-Abstand verringert sich in dem Maße, wie der s-anteil an der Hybridisierung des C-Atoms wächst Schwermetallacetylide Ag 2 C 2 und
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Lösung 3 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Zum Nachlesen/Vertiefen des Vorlesungsstoffs von heute siehe Maitland
1 Lösung 3 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Zum Nachlesen/Vertiefen des Vorlesungsstoffs von heute siehe Maitland
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
Organische Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de Arene Arene sind cyclisch konjugierte
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
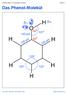 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag)
 Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
Pharmazeutische Chemie Seite 1 Die Bearbeitung erfolgt mit Textausschnitten des Buches Chemie Teil 2 (Diesterweg Verlag) Fragen zu der sp³ Hybridisierung (S. 124-128): 1.) Notieren Sie die Elektronenverteilung
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
H δ+ H H H H. Addition von HBr an Ethen. Zufällig kommt ein HBr-Molekül in die Nähe der elektronenreichen Doppelbindung. Schritt 1
 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 1/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen δ- δ+ Ulrich elmich 2015
hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 1/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen δ- δ+ Ulrich elmich 2015
Arene (Benzolderivate)
 Arene (Benzolderivate) Im Verlauf der Vorlesung haben wir bereits einige kennengelernt: DDT, DIXI, Cumol... hier nun weitere wichtige Vertreter: Acetylsalicylsäure (Aspirin) Synthese über die Kolbe-Schmitt-Synthese
Arene (Benzolderivate) Im Verlauf der Vorlesung haben wir bereits einige kennengelernt: DDT, DIXI, Cumol... hier nun weitere wichtige Vertreter: Acetylsalicylsäure (Aspirin) Synthese über die Kolbe-Schmitt-Synthese
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Aromatische Substitution. Dr. Florian Achrainer AK Zipse
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Energie. 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital
 sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
sp 2 -ybridisierung sp 2 -ybridisierung sp 2 -ybridisierung 1 x 2p Orbital Energie 3 x sp Orbitale 3 x sp-orbital 1 x 2p-Orbital z y x planare Anordnung in sp 2 -hybridisierten -Atomen: Alle 4 (3 s- und
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 5: )
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Organische Chemie I. OC I Lehramt F. H. Schacher 1
 Organische Chemie I OC I Lehramt F. H. Schacher 1 Organisatorisches Kontakt: Felix H. Schacher IOMC, Lessingstr. 8, Raum 122 Email: felix.schacher@uni jena.de Termine: Vorlesung: Freitag 12 14 Uhr Hörsaal,
Organische Chemie I OC I Lehramt F. H. Schacher 1 Organisatorisches Kontakt: Felix H. Schacher IOMC, Lessingstr. 8, Raum 122 Email: felix.schacher@uni jena.de Termine: Vorlesung: Freitag 12 14 Uhr Hörsaal,
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2017 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Inhaltsverzeichnis. Teil I Volle Kraft voraus: Die Chemie des Kohlenstoffs 23. Einführung 17. Kapitel 1 Die wundervolle Welt der organischen Chemie 25
 Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Aromaten H H H C C C C C C C C H C H. Naphthalin: C 10 H 8. Benzol: C 6 H 6. Anthracen: C 14 H 10. Phenanthren: C 14 H 10.
 Aromaten Folie30 C C C C C C Benzol: C 6 6 C C C C C C C C C C aphthalin: C 10 8 7 6 8 8a 5 4a 1 4 3 7 6 8 8a 9 9a 5 10a 10 4a 1 4 3 Anthracen: C 14 10 1 10 9 3 8 4 5 7 6 Phenanthren: C 14 10 Benzpyren:
Aromaten Folie30 C C C C C C Benzol: C 6 6 C C C C C C C C C C aphthalin: C 10 8 7 6 8 8a 5 4a 1 4 3 7 6 8 8a 9 9a 5 10a 10 4a 1 4 3 Anthracen: C 14 10 1 10 9 3 8 4 5 7 6 Phenanthren: C 14 10 Benzpyren:
Organische Chemie I SS 2018
 Organische Chemie I SS 2018 Organische Chemie I LA / J. C. Brendel 1 Organisatorisches Kontakt: Johannes C. Brendel ZAF, Philosophenweg 7, Raum 103 Email: johannes.brendel@uni-jena.de Felix H. Schacher,
Organische Chemie I SS 2018 Organische Chemie I LA / J. C. Brendel 1 Organisatorisches Kontakt: Johannes C. Brendel ZAF, Philosophenweg 7, Raum 103 Email: johannes.brendel@uni-jena.de Felix H. Schacher,
Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen.
 1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
1 Übung 13 AC/OC I, HS 2017 Name Assistent/in Verwenden Sie keinen Bleistift für die Abgabe und heften Sie einzelne Blätter zusammen. Ms: Mesyl-Gruppe (CH 3 SO 3 -), Tf: Triflyl-Gruppe (CF 3 SO 3 -), Ts:
N N. Chinolin. Pyridin. Imidazol
 6. eterocyclische Verbindungen 51 Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen aufgebaut sind. In den sogenannten eterocyclen ist mindestens ein Kohlenstoff des ings
6. eterocyclische Verbindungen 51 Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen aufgebaut sind. In den sogenannten eterocyclen ist mindestens ein Kohlenstoff des ings
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 6. eterocyclische Verbindungen Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen
CE 102.1: Grundlagen der Chemie - rganische Chemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 6. eterocyclische Verbindungen Als carbocyclisch bezeichnet man ingmoleküle, deren inge nur aus Kohlenstoffatomen
Basisprüfung Allgemeine Chemie (Teil OC) Montag, 3. September 2007
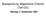 Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Basisprüfung Allgemeine Chemie (Teil C) Montag, 3. September 2007 1. omenklatur (20 Pt) 1.1 (10Pt) Benennen Sie die Verbindungen A - D nach IUPAC inkl. stereochemischer Deskriptoren. A B (2E,5E)4-Prop-1-inylhepta-2,5-dien
Radikalische Substitution von Alkanen
 adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
Herstellung und Oxidation von 2,4,6-Tri-tert-butylphenol
 2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
Beispiele. Polysubstituierte Benzole. Chapter 16. Organic Chemistry. Reaktionen of Substituierter Benzole. Bezeichnung durch Numerierung oder Präfix
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Beispiele Chapter 16 Reaktionen of Substituierter Benzole Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Bezeichnung durch
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Beispiele Chapter 16 Reaktionen of Substituierter Benzole Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Bezeichnung durch
1. a) Geben sie den Reaktionsmechanismus für die Nitrierung und die Sulfonierung von Benzol an. Beginnen sie mit der Erzeugung des Elektrophils.
 Übungsblatt 05 - C I - SoSe 2014 (Prof. Bunz) 1. a) Geben sie den Reaktionsmechanismus für die itrierung und die Sulfonierung von Benzol an. Beginnen sie mit der rzeugung des lektrophils. I) rzeugung lektrophil:
Übungsblatt 05 - C I - SoSe 2014 (Prof. Bunz) 1. a) Geben sie den Reaktionsmechanismus für die itrierung und die Sulfonierung von Benzol an. Beginnen sie mit der rzeugung des lektrophils. I) rzeugung lektrophil:
Übergangsmetall-π-Komplexe
 Übergangsmetall-π-Komplexe ausschließlich π-wechselwirkungen von Liganden- mit etallorbitalen Alken od. Olefin Diolefin Alkenkomplexe Alkin od. Acetylen Allyl yclopentadienyl sehr häufig, Beispiele mit
Übergangsmetall-π-Komplexe ausschließlich π-wechselwirkungen von Liganden- mit etallorbitalen Alken od. Olefin Diolefin Alkenkomplexe Alkin od. Acetylen Allyl yclopentadienyl sehr häufig, Beispiele mit
13. Amine und ihre Derivate
 Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhalt Index 13. Amine und ihre Derivate Amine sind Derivate des Ammoniaks, bei dem ein bis drei Wasserstoffatome durch Alkyloder Arylgruppen ersetzt wurden. Entsprechend gibt es primäre Amine, sekundäre
Inhaltsverzeichnis zu Kapitel 6. Aromaten
 Inhaltsverzeichnis zu Kapitel 6. Aromaten 6. Aromaten 6.1 Aromatizität 73 6.2 omenklatur 75 6.3 Darstellung 76 6.4 lektrophile Substitution am Aromaten 76 6.5 Beispiele für S -Reaktionen (was ist?) 77
Inhaltsverzeichnis zu Kapitel 6. Aromaten 6. Aromaten 6.1 Aromatizität 73 6.2 omenklatur 75 6.3 Darstellung 76 6.4 lektrophile Substitution am Aromaten 76 6.5 Beispiele für S -Reaktionen (was ist?) 77
3. Klausur zum Praktikum Organische Chemie I für Studierende der Chemie und der Biochemie im SS 2000
 Prof. Dr. B. König Prof. Dr. Th. Troll 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Donnerstag, dem 27. Juli 2000 ame: Mustermann...Vorname: Max...
Prof. Dr. B. König Prof. Dr. Th. Troll 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Donnerstag, dem 27. Juli 2000 ame: Mustermann...Vorname: Max...
Bromierung von Cycloalkenen
 hemie Q1 / 4. Reaktionswege der organischen hemie / 4.2 Alkene und elektrophile Addition 1/ omierung von ycloalkenen Zufällig kommt ein 2-Molekül in die Nähe der elektronenreichen Doppelbindung. Ulrich
hemie Q1 / 4. Reaktionswege der organischen hemie / 4.2 Alkene und elektrophile Addition 1/ omierung von ycloalkenen Zufällig kommt ein 2-Molekül in die Nähe der elektronenreichen Doppelbindung. Ulrich
3. Gruppe: Aromatische Substitution
 1 1) Zum chanismus der elektrophilen aromatischen Substitution Aromatischer Charakter Antiaromatischer Charakter (4 n 2)π-lektronen 4 nπ e 3 C C 3 2 C C 2 1.48Å 1.54Å 1.34Å 1.39Å ingstrom-ffekte δ = 5
1 1) Zum chanismus der elektrophilen aromatischen Substitution Aromatischer Charakter Antiaromatischer Charakter (4 n 2)π-lektronen 4 nπ e 3 C C 3 2 C C 2 1.48Å 1.54Å 1.34Å 1.39Å ingstrom-ffekte δ = 5
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen.
 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 CE 102.1: Grundlagen der Chemie - Organische Chemie Prof Dr. E. Landau und Prof. Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1
CE 102.1: Grundlagen der Chemie - Organische Chemie Prof Dr. E. Landau und Prof. Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Chemisches Praktikum für Studierende der umanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 2. Klausur zum 2. Praktikumsteil (C) vom 25.07.17 NAME;
Arzneistoff der Woche. Alkohole. Eliminierungen. Organische Chemie Agenda. Johann Wolfgang Goethe -Universität Frankfurt am Main
 Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Agenda Arzneistoff der Woche Alkohole Eliminierungen 1 Prof. Dr. Manfred Schubert-Zsilavecz Dabigatran - Struktur 2 Prof. Dr. Manfred Schubert-Zsilavecz Lucas-Test 3 Prof. Dr. Manfred Schubert-Zsilavecz
Reaktionsmechanismen der Organischen Chemie
 Peter Sykes Reaktionsmechanismen der Organischen Chemie Eine Einführung Mit einem Geleitwort von Lord A. R. Todd Übersetzt von Hans F. Ebel und Henning Hopf 9., überarbeitete Auflage Inhalt 1 Struktur,
Peter Sykes Reaktionsmechanismen der Organischen Chemie Eine Einführung Mit einem Geleitwort von Lord A. R. Todd Übersetzt von Hans F. Ebel und Henning Hopf 9., überarbeitete Auflage Inhalt 1 Struktur,
Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 Carbonylgruppen und eine C=C Doppelbindung.
 rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
Organische Chemie für MST 5. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
4. Alkene und Alkine : Reaktionen und Darstellung
 Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
Inhalt Index 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann sich unter Bildung eines Carbeniumions an eine
SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE
 SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE Wikipedia: Die organische Chemie (kurz: OC), häufig auch kurz Organik, ist ein Teilgebiet der
SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE Wikipedia: Die organische Chemie (kurz: OC), häufig auch kurz Organik, ist ein Teilgebiet der
Alkene / Additions-, Eliminierungsreaktionen
 2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
2.2.2. Alkene / Additions-, Eliminierungsreaktionen 64 65 Struktur und Bindung in Ethen Ethen ist planar 2 trigonale C-Atome Bindungswinkel annähernd 120 o C ist sp2-hybridisiert Einfachbindung durch Überlapp
Welche Arten von Formeln stehen dem Chemiker zur Verfügung?
 Welche Arten von Formeln stehen dem Chemiker zur Verfügung? 1. Summenformeln 2. Valenzstrichformeln (Lewis-Strichformeln) 3. Strukturformeln Summenformel: Die Summenformel dient dazu Art und Anzahl der
Welche Arten von Formeln stehen dem Chemiker zur Verfügung? 1. Summenformeln 2. Valenzstrichformeln (Lewis-Strichformeln) 3. Strukturformeln Summenformel: Die Summenformel dient dazu Art und Anzahl der
Zusammenfassung 101 L 2 H 3
 Zusammenfassung 101 6. Zusammenfassung In dieser Arbeit gelang zum ersten Mal die Synthese und Charakterisierung von Übergangsmetall koordinierten Anilinoradikalen. Die Eigenschaften der koordinierten
Zusammenfassung 101 6. Zusammenfassung In dieser Arbeit gelang zum ersten Mal die Synthese und Charakterisierung von Übergangsmetall koordinierten Anilinoradikalen. Die Eigenschaften der koordinierten
Organische Chemie I Chemie am 16.11.2012. Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2
 Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
CHE 172.1: Organische Chemie für die Life Sciences
 1 CE 172.1: Organische Chemie für die Life Sciences Prof Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der lkene
1 CE 172.1: Organische Chemie für die Life Sciences Prof Dr. J.. Robinson 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der lkene
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2017 Die Klausur besteht aus 10 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
Chemisches Praktikum für Biologen Klausur am 13.02.2017 Die Klausur besteht aus 10 Seiten. Bitte zu den folgenden Aufgaben die jeweils richtige Antwort (A, B, C, D) bzw. den berechneten Wert (ohne Maßeinheit)
Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-OC-II Prof. R. Peters
 Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-C- Prof. R. Peters 1. Ergänzen Sie das folgende Schema durch Angabe der fehlenden Produkte oder Reagenzien! Bitte achten Sie auf die korrekte Darstellung
Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-C- Prof. R. Peters 1. Ergänzen Sie das folgende Schema durch Angabe der fehlenden Produkte oder Reagenzien! Bitte achten Sie auf die korrekte Darstellung
Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2
![Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2](/thumbs/95/126253543.jpg) Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
OC 4 Aromaten / Heterocyclen. Aromatizität 1
 OC 4 Aromaten / Heterocyclen Aromatizität 1 Benzol Der Modellaromatt Historische Entwicklung 1825 1833 Entdeckung durch Michael Faraday (Pyrolyse) Mitscherlich: Erste Benzolsynthese Entdeckung der Summenformel
OC 4 Aromaten / Heterocyclen Aromatizität 1 Benzol Der Modellaromatt Historische Entwicklung 1825 1833 Entdeckung durch Michael Faraday (Pyrolyse) Mitscherlich: Erste Benzolsynthese Entdeckung der Summenformel
4. Alkene und Alkine : Reaktionen und Darstellung
 Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Dienstag, 22. Oktober 2002 Allgemeine Chemie B II Page: 1 4. Alkene und Alkine : Reaktionen und Darstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken Säure kann
Auf der rechten Seite sind Beispiele für kovalente Bindungen.
 Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Aromaten, Fette und Tenside Seminar zu chem2010 Stephan Bernt
 , Fette und Tenside 12.05.2010 Seminar zu chem2010 Stephan Bernt Kriterien für Aromatizität: cyclisch planar vollständig konjugiertes π-elektronensystem Hückel-Regel: 4n+2 π-elektronen Prototyp des Aromaten:
, Fette und Tenside 12.05.2010 Seminar zu chem2010 Stephan Bernt Kriterien für Aromatizität: cyclisch planar vollständig konjugiertes π-elektronensystem Hückel-Regel: 4n+2 π-elektronen Prototyp des Aromaten:
Die Übungsfragen sind online Besprechung: Mittwoch, 28. September 2016
 Die Übungsfragen sind online http://www.cup.lmu.de/oc/linser/oc-for-biologists/ esprechung: Mittwoch, 28. eptember 2016 Link zur Klausuranmeldung: http://www.cup.lmu.de/anmeld/ocbioklausur/ Wiederholungsklausur:
Die Übungsfragen sind online http://www.cup.lmu.de/oc/linser/oc-for-biologists/ esprechung: Mittwoch, 28. eptember 2016 Link zur Klausuranmeldung: http://www.cup.lmu.de/anmeld/ocbioklausur/ Wiederholungsklausur:
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Elektrophile Additionen von HX an die CC-Doppelbindung (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart, S ; Buddrus, S.
 Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
5. Aromatische Kohlenwasserstoffe
 Inhalt Index 5. Aromatische Kohlenwasserstoffe Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten.
Inhalt Index 5. Aromatische Kohlenwasserstoffe Aufgrund der starken Aromas, das viele Benzolderivate ausströmen, nennt man sie aromatische Verbindungen. Deshalb gilt Benzol als Stammverbindung der Aromaten.
2 Nucleophile Substitutionen am gesättigten Kohlenstoff
 2 ucleophile Substitutionen am gesättigten Kohlenstoff 21 Allgemeiner eaktionsablauf X Y: Y X: allgemeiner: Substrat ucleophil Produkt ucleofug Elektrophil ucleophil Elektrophil ucleophil ucleophile: Anionen
2 ucleophile Substitutionen am gesättigten Kohlenstoff 21 Allgemeiner eaktionsablauf X Y: Y X: allgemeiner: Substrat ucleophil Produkt ucleofug Elektrophil ucleophil Elektrophil ucleophil ucleophile: Anionen
Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol
 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Dietikon, 3. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Dietikon, 3. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Die Substituenten und ihre Positionen werden dem Namen des Alkens als Präfixe vorgestellt:
 23 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der lkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die für die lkene
23 3. Organische Reaktionen - Einordung nach chanismen. lkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der lkene Eine C=C Doppelbindung ist die funktionelle Gruppe, die für die lkene
4.2 Kovalente Bindung. Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916)
 4.2 Kovalente Bindung Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916) Treten Atome von Nichtmetallen miteinander in Wechselwirkung, kommt es nicht zu einer Übertragung von Elektronen. Nichtmetallatome
4.2 Kovalente Bindung Theorie der kovalenten Bindung, Gilbert Newton Lewis (1916) Treten Atome von Nichtmetallen miteinander in Wechselwirkung, kommt es nicht zu einer Übertragung von Elektronen. Nichtmetallatome
Übergangsmetall-π-Komplexe
 Übergangsmetall-π-Komplexe ausschließlich π-wechselwirkungen von Liganden- mit etallorbitalen Alken od. Olefin Diolefin Alkenkomplexe Alkin od. Acetylen Allyl yclopentadienyl sehr häufig, Beispiele mit
Übergangsmetall-π-Komplexe ausschließlich π-wechselwirkungen von Liganden- mit etallorbitalen Alken od. Olefin Diolefin Alkenkomplexe Alkin od. Acetylen Allyl yclopentadienyl sehr häufig, Beispiele mit
Vorlesung OC-V. Carbeniumionen
 Carbeniumionen Woher kennen wir bereits Carbeniumionen? 1. Triphenylmethanfarbstoffe Adolf von Bayer erzeugte 1902 die ersten stabilen intensiv farbigen Triarylmethylkationen Lebensdauer in Wasser > 1h
Carbeniumionen Woher kennen wir bereits Carbeniumionen? 1. Triphenylmethanfarbstoffe Adolf von Bayer erzeugte 1902 die ersten stabilen intensiv farbigen Triarylmethylkationen Lebensdauer in Wasser > 1h
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Zeichnen von Valenzstrichformeln
 Zeichnen von Valenzstrichformeln ür anorganische Salze werden keine Valenzstrichformeln gezeichnet, da hier eine ionische Bindung vorliegt. Die Elektronen werden vollständig übertragen und die Ionen bilden
Zeichnen von Valenzstrichformeln ür anorganische Salze werden keine Valenzstrichformeln gezeichnet, da hier eine ionische Bindung vorliegt. Die Elektronen werden vollständig übertragen und die Ionen bilden
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
