Gruppenpräparat: Versuch Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon
|
|
|
- Karl Kaiser
- vor 6 Jahren
- Abrufe
Transkript
1 P II Praktikum im WS 2008/2009 Gruppenpräparat: Versuch Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon 1.Gruppe: Christoph Mann Marco Schott 2.Gruppe: Tim Walter Holger Hartleb Stefan Maisch
2 1 Aufgabenstellung Der Versuch , die Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)-ethanon, soll erfolgreich durchgeführt, und die Ausbeute optimiert werden. Dies gilt ins besondere für den otoversuch in der 2. Stufe, welcher wiederholt zu keiner Ausbeute führte. 2 Reaktionsgleichungen 1. Stufe Cl AlCl 3 Toluol, T 43 % C 7 H 5 Cl C 7 H 8 AlCl 3 C 14 H 12 ( g/mol) (92.14 g/mol) ( g/mol) ( g/mol) 2. Stufe 2 hv, HAc (kat.) 275 W Tageslichtlampe i-prh, RT, 3d 60 % H 3 C H H C 14 H 12 C 28 H 26 2 ( g/mol) ( g/mol)
3 3. Stufe H I 2, HAc, reflux H 3 C H C 28 H g/mol H 3 C H 3 C + 90:10 H 3 C C 28 H 24 C 28 H g/mol g/mol 3 Gefahrenpotential Aluminiumtrichlorid: R 34 S 7/ Toluol: R / S 36/ Benzoylchlorid: R 34 S Methlybenzophenon: S 24/25
4 iso-propanol: R S /25-26 Essigsäure (konz.): R S ,2-Diphenyl-2,2-(4-methylphenyl)-ethanon: R45 (Stoff mit unbekannten Eig.) Iod: R20/21-50 S Entsorgung Aluminiumtrichlorid: Vorsichtig in Eiswasser eintragen. Mit Natronlauge neutralisieren und zu den wässrigen, basischen Lösungsmittelabfällen geben. Toluol, iso-propanol: Als halogenfreie, organische Lösungsmittel. Benzoylchlorid: In Überschuss Methanol tropfen, mit NaH neutralisieren und als halogenhaltige, organische Lösungsmittel entsorgen. 4-Methlybenzophenon, 4,4 -Dimethylpenzopinakol: Gelöst als halogenfreie, organische Lösungsmittel. konz. Essigsäure: Vorsichtig mit Natriumhydrogencarbonat oder NaH neutralisieren und mit viel Wasser ins Abwasser geben.
5 1,2-Diphenyl-2,2-(4-methylphenyl)-ethanon: Gelöst in organische, halogenfreie Lösungsmittelabfälle Iod: Gelöst in organische, halogenhaltige Lösungsmittelabfälle 5 Mechanismus 1. Stufe: Friedel-Crafts-Acylierung: Im ersten Schritt entsteht durch Angriff von AlCl 3 (Lewis-Säure) das Acyl-Kation. Dieses wird nun in para-position zur Methylgruppe vom elektronenreichen Aromaten angegriffen. Der para-angriff ist dem ortho-angriff auf Grund der Sterik bevorzugt. Hierbei wird HCl frei. AlCl 3 AlCl 4 Cl -HCl H AlCl 4
6 2. Stufe: otoreduktion: hv, HAc (kat.) H H i-prh H H H H 2 H 3 C H 3. Stufe: Die Essigsäure protoniert eine der Alkohol-Gruppen des 4,4 -Dimethylbenzopinakols. Diese wird als Wasser abgespalten und es kommt zu einer Pinakol-Umlagerung. Hierbei kann entweder der enyl- oder der Toluol-Rest wandern. Da Toluol positive Ladungen besser stabilisieren kann als Benzol, entstehen die beiden Produkte in einem Verhältnis von 9:1.
7 H I 2, HAc, reflux -H 2 0 H 3 C H H + H 3 C + H 3 C 90:10 H 3 C 6 Durchführung Das Gruppenpräparat wurde von zwei Gruppen gleichzeitig bearbeitet. Da es nur eine begrenzte Anzahl von otoapparaturen und Lampen gab, wurden die einzelnen Ansätze so abgesprochen, dass sie aufeinander aufbauen. Die Durchführung der Versuche orientierte sich an der Anleitung aus Literaturquelle (1). 1. Stufe: 4-Methylbenzophenon Ansatz 1: Ansatzgröße: 35.0 g (262 mmol) Aluminiumtrichlorid 150 ml (1.41 mol) Toluol 36.6 g (260 mmol, 30 ml) Benzoylchlorid
8 Durchführung: In einem 500 ml Dreihalskolben mit Tropftrichter, Rückflusskühler und Magnetrührer wurden 35.0 g (262 mmol) trockenes Aluminiumtrichlorid und 150 ml (1.41 mol) Toluol vorgelegt. Dazu wurden langsam unter Rühren 36.6 g (260 mmol, 30 ml) Benzoylchlorid getropft. Das entstehende Gas wurde über zwei Waschflaschen, von denen die zweite mit NaH-Lösung gefüllt war, in den Abzug geleitet. Es wurde solange refluxiert, bis kein Gas mehr entstand. Nach beendeter Reaktion wurde die warme Reaktionsmischung auf 250 g Eis und 110 ml konz. HCl geschüttet. Es wurde gerührt bis die Toluolphase eine gelb-grünliche Farbe annahm. Die Toluolphase wurde mit 100 ml 5%iger NaH-Lösung und 100 ml dest. Wasser gewaschen. Danach wurde zuerst das Lösungsmittel abrotiert und anschließend unter Einsatz eines Heizpilzes das Produkt destilliert (Heizpilz, Sdp.: C / 300 mbar Membranpumpenvakuum). Nach Auskristallisation wurde über einen Büchnertrichter abfiltriert und der Rückstand mit Filterpapier gepresst, um Reste des Öls zu entfernen. Das Filtrat wurde nochmals über einen Büchnertrichter abfiltriert, um weiteres Produkt zu erhalten. Der Rückstand wurde in 80%igem Ethanol umkristallisiert. Ausbeute: 27.1 g (138 mmol, 53%) eines weißen, kristallinen Feststoffes (Lit.: 43%) DC Kontrolle: Laufmittel: Petrolether : Essigsäureethylester = 6 : 1 E: Benzoylchlorid P: Reaktionsmischung
9 Charakterisierung: Schmelzpunkt: 57 C (Lit.: C) IR-Spektrum: 3055 cm -1 : =C-H-Valenzschwingung von Aromaten 1655 cm -1 : -C=-Valenzschwingung 1600 cm -1, 1590 cm -1 : Ringschwingung von Aromaten
10 Vergleichsspektrum: Die erhaltenen Daten weisen daraufhin, dass das gewünschte Produkt 4-Methlybenzophenon synthetisiert wurde. Fehlerdiskussion: Der Versuch hat gut funktioniert, Ausbeute und Reinheit des Produktes waren sehr gut. Auch bei der Durchführung gab es keine größeren Probleme.
11 Ansatz 2: Ansatzgröße: 48.5g (0.36 mol) Aluminiumtrichlorid 210 ml (1.97 mol) Toluol 50.6g (0.36 mol, 30 ml) Benzoylchlorid Durchführung: In einem 500 ml Dreihalskolben mit Tropftrichter, Rückflusskühler und Magnetrührer wurden 48.5 g (360 mmol) trockenes Aluminiumtrichlorid und 210 ml (1.97 mol) Toluol vorgelegt. Dazu wurden langsam unter Rühren 50.6 g (360 mmol, 42 ml) destilliertes Benzoylchlorid getropft. Das entstehende Gas wurde über zwei Waschflaschen, von denen die zweite mit NaH-Lösung gefüllt war, in den Abzug geleitet. Es wurde solange refluxiert, bis kein Gas mehr entstand. Nach beendeter Reaktion wurde die warme Reaktionsmischung auf 250 g Eis und 110 ml konz. HCl geschüttet. Es wurde gerührt bis die Toluolphase eine gelb-grünliche Farbe annahm. Die Toluolphase wurde mit 100 ml 5%iger NaH-Lösung und 100 ml dest. Wasser gewaschen. Danach wurde zuerst das Lösungsmittel abrotiert und anschließend unter Einsatz eines Heizpilzes das Produkt destilliert (Heizpilz, Sdp.: C / 300 mbar Membranpumpenvakuum). Nach Auskristallisation wurde über einen Büchnertrichter abfiltriert und der Rückstand mit Filterpapier gepresst, um Reste des Öls zu entfernen. Das Filtrat wurde nochmals über einen Büchnertrichter abfiltriert, um weiteres Produkt zu erhalten. Der Rückstand wurde in 80%igem Ethanol umkristallisiert. Ausbeute: 40.0 g (0.20 mmol, 55%) eines weißen, kristallinen Feststoffes (Lit.: 43%) DC Kontrolle: Laufmittel: Toluol E = Benzoylchlorid R = Reaktionsmischung
12 Charakterisierung: Schmelzpunkt: 58 C (Lit.: C) IR-Spektrum: Identisch zu dem von Ansatz Stufe: 4,4 -Dimethylpenzopinakol Ansatz 1: Zuerst wurde ein UV-Vis Spektrum des Eduktes aufgenommen. Nach Absprache mit dem betreuenden Assistenten wurde für den ersten Ansatz eine Fotoapparatur aus Duranglas verwendet.
13 Ansatzgröße: 4.00 g (20.0 mmol) 4-Methlybenzophenon 25 ml iso-propanol 2 Tropfen konz. Essigsäure Durchführung: 4.00 g (20.0 mmol) 4-Dimetzhylbenzophenon, 25 ml iso-propanol und 2 Tropfen konz. Essigsäure wurden in dem Reaktionsgefäß einer Fotoapparatur (Duranglas) vorgelegt. Nun wurde kurz erhitzt, um das 4-Dimethylbenzophenon zu lösen. Die Reaktionslösung wurde dann für 5 Tage mit einer Quecksilberhochdrucklampe (455 W Hanovia, Maximum bei 366 nm) bestrahlt. Es fand kein Reaktionsumsatz statt. DC Kontrolle: Laufmittel: Petrolether : Essigsäureethylester = 5 : 1,5 E = 4-Dimetzhylbenzophenon P = Reaktionsmischung Fehlerbetrachtung Der erste Ansatz wurde mit den in der Literatur angegeben Mengen gekocht. Bei der verwendeten Fotoapparatur ging aber ein Großteil der Strahlung der Lampe verloren, da die Lampe fast gar nicht von der Reaktionslösung umflossen war. Im zweiten Ansatz wurden daher die Ansatzgrößen erhöht. Außerdem wurde im ersten Ansatz das Lösungsmittel nicht entgast.
14 Ansatz 2: Ansatzgröße: 8.00 g (40.0 mmol) 4-Methlybenzophenon 100 ml iso-propanol 5 Tropfen konz. Essigsäure Durchführung: 8.00 g (40.0 mmol) 4-Methylbenzophenon, 100 ml entgastes iso-propanol und 5 Tropfen konz. Essigsäure wurden in einer Fotoapparatur aus Duranglas vorgelegt. Um das 4- Methylbenzophenon zu lösen, wurde die Lösung kurz erhitzt. Die Reaktionslösung wurde dann für 5 Tage unter Schutzgas mit einer Quecksilberhochdrucklampe (455 W Hanovia, Maximum bei 366 nm) bestrahlt. Es fiel ein weiß-gelblicher Niederschlag aus. Die Reaktionsmischung wurde im Eisbad gekühlt und über einen Büchnertrichter abgesaugt. Der Rückstand wurde in n-propanol umkristallisiert. Es kristallisierte ein weißer Feststoff aus. Ausbeute: 1.61 g (4.08 mmol, 20%) eines weißen Feststoffes (Lit.: 60%) DC-Kontrolle: Laufmittel: Petrolether : Essigsäureethylester = 10 : 1 E = 4-Dimetzhylbenzophenon P1 = Produkt weiß P2 = Produkt gelblich P1 und P2 sind nach Umkristallisation identisch.
15 Charakterisierung: Schmelzpunkt: 164 C (Lit.: C) IR-Spektrum: 3550 cm -1 : --H-Valenzschwingung 3010 cm -1 : =C-H-Valenzschwingung von Aromaten 2960 cm -1 : - -Valenzschwingung 1610 cm -1, 1590 cm -1, 1510 cm -1, 1490 cm -1 : Ringschwingung von Aromaten
16 Vergleichsspektrum: Fehlerbetrachtung: Es konnte eine Umsetzung beobachtet werden, allerdings war die Ausbeute nicht besonders hoch. Da die Bestrahlungszeit bereits länger war als in der riginalliteratur angegeben (3 Tage), könnte das verwendete Duranglas möglicherweise zu Intensitätsverlusten geführt haben. Aus diesem Grund wurde beim nächsten Ansatz eine otoapparatur aus Quarzglas verwendet.
17 Ansatz 3: Ansatzgröße: 12.0 g (60.0 mmol) 4-Methylbenzophenon 100 ml iso-propanol 5 Tropfen konz. Essigsäure Durchführung: 12.0 g (60.0 mmol) 4-Methylbenzophenon wurden in 100 ml iso-propanol unter kurzem Erhitzen gelöst. Es wurden 5 Tropfen konz. Essigsäure hinzugegeben und die Lösung mit Hilfe von Stickstoff entgast. Die Lösung wurde in eine Fotoapparatur (Quarzglas) gegeben und 5 Tage unter Schutzgas (Luftballon) mit einer Quecksilberhochdrucklampe (455 W Hanovia, Maximum 366 nm) bestrahlt. Es fiel ein weiß-gelblicher Niederschlag aus. Die Reaktionsmischung wurde im Eisbad gekühlt und über einem Büchnertrichter abgesaugt. Das Rohprodukt (6.80 g) wurde in ca. 75 ml n-propanol umkristallisiert. Ausbeute: 4.66 g (11.8 mmol, 39%) eines weißen Feststoffes (Lit.: 60%) DC Kontrolle: Laufmittel: Toluol E = 4-Methylbenzophenon P = Produkt F = Filtrat
18 Charakterisierung: Schmelzpunkt: C (Lit.: C) IR-Spektrum: Stimmt mit dem von Ansatz 2 überein. Fehlerbetrachtung: Die Ausbeute war besser als bei den vorherigen Versuchen, aber noch immer nicht befriedigend. Zudem war die Einwaagemenge des Eduktes sehr hoch. Um Edukt zu sparen, wurden im nächsten Ansatz nur 4.00 g (20.0 mmol) 4-Methylbenzopheneon eingesetzt. Die Lösungsmittelmenge wurde beibehalten, um zu gewährleisten, dass die gesamte Reaktionslösung von der Lampe bestrahlt wurde. Die Lösung wurde dadurch im Vergleich zu den vorherigen Ansätzen stark verdünnt. Ansatz 4: Ansatzgröße: 4.00 g (20 mmol) 4-Methlybenzophenon 100 ml iso-propanol 5 Tropfen konz. Essigsäure Durchführung: 4.00 g (20.0 mmol) 4-Methylbenzophenon, 100 ml entgastem iso-propanol und 5 Tropfen konz. Essigsäure wurden in dem Reaktionsgefäß einer Fotoapparatur aus Quarzglas vorgelegt. Nun wurde kurz erhitzt, um das 4-Methylbenzophenon zu lösen. Die Reaktionslösung wurde dann für 5 Tage unter Schutzgas mit einer Quecksilberhochdrucklampe (455 W Hanovia, Maximum bei 366 nm) bestrahlt. Es fand keine Reaktion statt.
19 DC-Kontrolle: Laufmittel: Petrolether : Essigsäureethylester = 10 : 1 Fehlerbetrachtung: Es konnte keine Umsetzung beobachtet werden. Da eine Quarzapparatur verwenden wurde, welche im vorherigen Versuch zu einer akzeptablen Ausbeute führte, hat die Reaktion vermutlich wegen der zu geringen Konzentration nicht stattgefunden. Ansatz 5: Da die Quecksilberhochdrucklampen sehr häufig für Versuche benötigt werden, sollte im nächsten Versuch eine 500 W Tageslichtlampe getestet werden. Ansatzgröße: 4.00 g (20 mmol) 4-Methylbenzophenon 25.0 ml iso-propanol 2 Tropfen konz. Essigsäure Durchführung: 4.00 g (20.0 mmol) 4-Methylbenzophenon wurden in einem 100 ml Schlenkkolben in 25.0 ml iso-propanol gelöst. Die Lösung wurde entgast, 2 Tropfen konz. Essigsäure hinzugegeben und anschließend unter Stickstoff (Luftballon) 7 Tage mit einer 500 W Tageslichtlampe (sram) bestrahlt. Es fand keine Reaktion statt.
20 DC Kontrolle: Laufmittel: Toluol E = 4-Methylbenzophenon R = Reaktionsmischung Fehlerbetrachtung: Ein möglicher Grund für die Nichtumsetzung könnte die zu geringe Intensität der sram Tageslichtlampe in dem für die Reaktion benötigten Wellenlängenbereich sein. Nach Internet Recherche wurde herausgefunden, dass es sich bei der in der riginalliteratur verwendeten Lampe um eine General Electrics 275 W Bräunungslampe handelte. Diese strahlt vor allem im UV-Bereich. Wahrscheinlich ist sie deshalb nicht mit einer normalen Tageslichtlampe gleichzusetzen. Da keine technischen Informationen zur sram Lampe verfügbar waren, kann dies nicht genau geklärt werden. Ansatz 6: Im letzten Ansatz sollte noch einmal die Reaktion in einer Duranglas Apparatur getestet werden, da diese in größerer Stückzahl verfügbar ist als die aus Quarzglas. Ansatzgröße: 20.0 g (0.10 mol) 4-Methylbenzophenon 140 ml iso-propanol 10 Tropfen konz. Essigsäure
21 Durchführung: 20.0 g (100 mmol) 4-Methylbenzophenon wurden in 140 ml iso-propanol unter kurzem Erhitzen gelöst. Es wurden 10 Tropfen konz. Essigsäure hinzugegeben und die Lösung im Ultraschallbad entgast. Die Lösung wurde in eine Fotoapparatur aus Duranglas gegeben und 7 Tage unter Schutzgas (Luftballon) mit einer Quecksilberhochdrucklampe (455 W Hanovia, Maximum 366 nm) bestrahlt. Es fiel ein weiß-gelblicher Niederschlag aus. Die Reaktionsmischung wurde im Eisbad gekühlt und über einem Büchnertrichter abgesaugt. Das Rohprodukt (13.0 g) wurde in ca. 125 ml n-propanol umkristallisiert. Ausbeute: 10.1 g (25.7 mmol, 51%) eines weißen Feststoffes (Lit.: 60 %) DC Kontrolle: Laufmittel: Toluol E = 4-Methylbenzophenon P = Produkt F = Filtrat Charakterisierung: Schmelzpunkt: C (Lit.: C) IR-Spektrum: Stimmt mit dem von Ansatz 2 überein. Fehlerbetrachtung: Die Ausbeute dieses Ansatzes war die bisher beste, vermutlich weil die größte Konzentration verwendet wurde. Außerdem wurde eine andere Fotoapparatur verwendet, die eine bessere Durchmischung ermöglichte, und die Belichtungszeit um 2 Tage erhöht.
22 3. Stufe (V ): 1,2-Diphenyl-2,2-(4-methylphenyl)-ethanon und 2,2-Diphenyl-1,2-(4-methylphenyl)-ethanon Ansatzgrößen: 1.60 g (4.06 mmol) 4,4`-Dimethylbenzopinakol 25 ml Eisessig 5 Tropfen 2%iger Jod-Eisessiglösung Durchführung: In einem 100 ml Rundkolben wurden 1.60 g (4.06 mmol) 4,4 -Dimethylbenzopinakol in 15 ml Eisessig gelöst und 5 Tropfen einer 2%igen Jod-Eisessiglösung hinzugegeben, bis die Reaktionslösung leicht gelblich wurde. Die Lösung wurde anschließend 10 min unter Rückfluss erhitzt, das Lösemittel am Rotationsverdampfer abgezogen und 15 ml Eisessig zugetropft. Anschließend wurde dieser erneut unter reduziertem Druck entfernt. Ausbeute: nicht bestimmbar, da keine Aufarbeitung DC Kontrolle: Laufmittel: Petrolether / Essigsäureethylester = 5 / 1 E = 4,4 -Dimethylbenzopinakol P = Reaktionsmischung
23 Charakterisierung: 1 H-NMR: (300 MHz, CDCl 3 ) Hauptprodukt: δ = 2.29 (6H, s, 2x ), (4H, m, AA, 2x2 -CH arom.), (4H, m, BB, 2x2 -CH arom.), (2H, m, 2x -CH arom.), (5H, m, -CH arom.), (1H, m, -C-H arom.), (2H, m, -C-H arom.) ppm. Nebenprodukt: δ = 2.26 (3H, s, - ), 2.45 (3H, s, - ), (4H, -CH arom.), (2H, -CH arom.), (4H, -CH arom.), (2H, -CH arom.), (2H, -CH arom.) Die fehlenden Protonen befinden sich im aromatischen Bereich und sind von den Protonen des Hauptproduktes überlagert. Man kann Haupt- und Nebenprodukt sehr schön anhand der Signale für die Methylgruppen unterscheiden. Zudem erkennt man auch deutlich das Verhältnis von 9:1 in der Signalintensität.
24 Fehlerbetrachtung: Wie die NMR-Auswertung zeigt, hat dieser Teil des Versuches gut funktioniert, die Produkte liegen im angegebenen Verhältnis zueinander vor. Da ansonsten keine Signale im NMR zu finden sind, kann von einer fast vollständigen Umsetzung ausgegangen werden. 7 Gesamtdiskussion Alle Stufen des Versuches konnten erfolgreich durchgeführt werden. Beim otoversuch zeigte sich, dass wahrscheinlich die Konzentration des Eduktes und die Wahl der Lampe eine große Rolle spielen. Zwischen Duran- und Quarzglas scheint es hingegen nur geringe Unterschiede zu geben, so hatte sogar die letzte Umsetzung mit Duranglas die beste Ausbeute. Allerdings sind Ansatz 3 (39% Ausbeute, Quarzglas) und Ansatz 6 (50% Ausbeute, Duranglas) nur bedingt miteinander vergleichbar, da Ansatz 6 eine höhere Konzentration und bessere Durchmischung, sowie eine längere Laufzeit aufwies. 8 Literatur (1) N.M. Zaczek, J.C. Ruff, A.H. Jackewitz, D.F. Roswell, J. Chem. Educ. 1971, 48, (2) C.J. Collins, Quart. Rev. 1960, 14, 357 (3) W.E. Bachmann, F.H. Moser, J. Am. Chem. Soc., 1932, 54 (3),
Protokoll zum Gruppenpra parat
 Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
3002 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure
 32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
NO 2 Rühren mit Magnetrührer, Extrahieren, Ausschütteln, Abrotieren, Umkristallisieren, Abfiltrieren,
 1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
3021 Oxidation von Anthracen zu Anthrachinon
 xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
Betreuer: Tobias Olbrich Literatur: Nach Organic Syntheses Coll. Vol. 10 (2004), 96.
 rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid
 1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95.1) (63.0) (98.1) C 5 H 4 N 2 O 3 (140.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95.1) (63.0) (98.1) C 5 H 4 N 2 O 3 (140.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
Organisch chemisches Praktikum II
 18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
1005 Bromierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol
 1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
2017 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid
 217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid
 1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
5007 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin
 57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4009 Synthese von Adipinsäure aus Cyclohexen
 4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on)
 6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on) H 2 + KH H 2 /EtH/THF C 7 H 6 C 3 H 6 KH (56.1) C 17 H 14 (106.1) (58.1) (234.3) Klassifizierung Reaktionstypen
6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on) H 2 + KH H 2 /EtH/THF C 7 H 6 C 3 H 6 KH (56.1) C 17 H 14 (106.1) (58.1) (234.3) Klassifizierung Reaktionstypen
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
6011 Hippursäure aus Glycin und Benzoylchlorid
 P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus
 NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester
 NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf Inhaltsverzeichnis 1. Aufgabenstellung.
2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid
 2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid H + SCl 2 Cl + HCl + S 2 C 9 H 8 2 (148.2) (119.0) C 9 H 7 Cl (166.6) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid H + SCl 2 Cl + HCl + S 2 C 9 H 8 2 (148.2) (119.0) C 9 H 7 Cl (166.6) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
3012 Synthese von Adamantylidenadamantan aus Adamantanon
 Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol
 4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b
 3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
4010 Synthese von p-methoxyacetophenon aus Anisol
 4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
4002 Synthese von Benzil aus Benzoin
 4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
3011 Synthese von erythro-9,10-dihydroxystearinsäure aus Ölsäure
 311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b).
 2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid
 NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
8.1 Durchführung gemäß Gruppenpräparat WS 2008/2009
 Inhalt: 1. Mustervorschrift aus dem WS2008/2009 2. Problemstellung 3. Literaturrecherche 4. Reaktionsgleichung 5. Gefahrenpotenzial 6. Entsorgung 7. Mechanismus 8. Durchgeführte Experimente 8.1 Durchführung
Inhalt: 1. Mustervorschrift aus dem WS2008/2009 2. Problemstellung 3. Literaturrecherche 4. Reaktionsgleichung 5. Gefahrenpotenzial 6. Entsorgung 7. Mechanismus 8. Durchgeführte Experimente 8.1 Durchführung
Gruppenpräparat 8.5. Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain
 Gruppenpräparat 8.5 Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain NaN 2,5nHCl H N Zn/HCl Cl NH 3 t-bu t-bu H C 14 H 22 206.33
Gruppenpräparat 8.5 Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain NaN 2,5nHCl H N Zn/HCl Cl NH 3 t-bu t-bu H C 14 H 22 206.33
170 C C 2 H C C 11 H 10 (174.2) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid
 4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen
 3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
Darstellung von Malachitgrün Präparat 5
 Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol
 1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
5001 Nitrierung von Phenol zu 2-Nitrophenol und 4-Nitrophenol
 00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion)
 4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
1035 Synthese von p-methoxyacetophenon aus Anisol
 NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
5009 Synthese von Kupferphthalocyanin
 P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
4006 Synthese von 2-(3-Oxobutyl)cyclopentanon-2- carbonsäureethylester
 4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2
![Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2](/thumbs/95/126253543.jpg) Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Herstellung und Oxidation von 2,4,6-Tri-tert-butylphenol
 2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
2.9B erstellung und xidation von 2,4,6-Tri-tert-butylphenol Chemikalien 4,7 g (50 mmol) Phenol R: 24, 25, 45 S: 28.2, 45 17,6 g (200 mmol) tertylmethylether R: 11, 36, 37, 38 Kp = 55 C S: 9, 16, 26, 29,
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien
 3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid
 NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Mustervorschrift 2.3.1
 Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Indan-1,3-dion. Reaktionsgleichung. H- und P-Sätze. Für alle Reagenzien und Produkte. Ausformulierte H- und P-Sätze. Vor(Abschluss)protokoll
 Indan-1,3-dion Reaktionsgleichung H- und P-Sätze Substanz Gefahrensymbol Smp. ( C) Sdp. ( C) Phtalsäurediethylester Essigsäureethylester Flammpkt. ( C) H-Sätze P-Sätze - -40 302 150 - - Gefahr -83 77-4
Indan-1,3-dion Reaktionsgleichung H- und P-Sätze Substanz Gefahrensymbol Smp. ( C) Sdp. ( C) Phtalsäurediethylester Essigsäureethylester Flammpkt. ( C) H-Sätze P-Sätze - -40 302 150 - - Gefahr -83 77-4
Organisch-chemisches Praktikum Wintersemester 2005/06. 1-Phenyl-propan-1-ol. Stephan Steinmann
 Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13
 Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
2. Herstellung der α,β-ungesättigten Kupplungskomponenten C H 3 H 33. Br 22 25
 2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
6016 Oxidation von 2,2-Dimethyl-1,3-propandiol zu 2,2- Dimethylmalonsäure
 6016 Oxidation von 2,2-Dimethyl-1,3-propandiol zu 2,2- Dimethylmalonsäure HNO 3 O O C 5 H 12 O 2 HNO 3 C 5 H 8 O 4 (104.2) (63.0) (132.1) Klassifizierung Reaktionstypen und Stoffklassen Oxidation Alkohol,
6016 Oxidation von 2,2-Dimethyl-1,3-propandiol zu 2,2- Dimethylmalonsäure HNO 3 O O C 5 H 12 O 2 HNO 3 C 5 H 8 O 4 (104.2) (63.0) (132.1) Klassifizierung Reaktionstypen und Stoffklassen Oxidation Alkohol,
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol
 3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Oxidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) CO 2
 6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
Für das Praktikum muss ein Laborjournal (Kladde) geführt werden, und zwar handschriftlich. Kladde bitte mit Namen beschriften.
 Für das Praktikum muss ein Laborjournal (Kladde) geführt werden, und zwar handschriftlich. Kladde bitte mit Namen beschriften. Bitte über jeden Versuch dann ein Datum schreiben. Das zu führende Laborjournal
Für das Praktikum muss ein Laborjournal (Kladde) geführt werden, und zwar handschriftlich. Kladde bitte mit Namen beschriften. Bitte über jeden Versuch dann ein Datum schreiben. Das zu führende Laborjournal
Synthese von 3-Aminophthalsäurehydrazid
 Illumina-Chemie.de - Artikel Synthesen Synthese von 3-Aminophthalsäurehydrazid Hier wird eine zweistufige Synthese von Luminol beschrieben. Luminol findet insbesondere für Chemilumineszenz Verwendung,
Illumina-Chemie.de - Artikel Synthesen Synthese von 3-Aminophthalsäurehydrazid Hier wird eine zweistufige Synthese von Luminol beschrieben. Luminol findet insbesondere für Chemilumineszenz Verwendung,
Protokoll zum Gruppenpräparat Versuch / 8.5
 Protokoll zum Gruppenpräparat Versuch 3.3.2.2 / 8.5 Organisch-chemisches Praktikum 2 Julius-Maximilians-Universität Würzburg Fakultät für Chemie und Pharmazie Vorgelegt von: Julian Koeller, Carl Schiller,
Protokoll zum Gruppenpräparat Versuch 3.3.2.2 / 8.5 Organisch-chemisches Praktikum 2 Julius-Maximilians-Universität Würzburg Fakultät für Chemie und Pharmazie Vorgelegt von: Julian Koeller, Carl Schiller,
Gruppenpräparat im Rahmen des OPII-Praktikums an der Universität Würzburg
 Gruppenpräparat im Rahmen des OPII-Praktikums an der Universität Würzburg Versuch 4.3.3 Darstellung von cis-2,3,5-triphenylisoxazolidin Praktikanten Baus, Johannes Dück, Klaus Schilling, Daniel Assistenten
Gruppenpräparat im Rahmen des OPII-Praktikums an der Universität Würzburg Versuch 4.3.3 Darstellung von cis-2,3,5-triphenylisoxazolidin Praktikanten Baus, Johannes Dück, Klaus Schilling, Daniel Assistenten
2023 Reduktion von D-(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b).
 23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
Organisch Chemisches Praktikum II. Gruppenpräparat: Darstellung von Z Crotonsäure
 Organisch Chemisches Praktikum II Gruppenpräparat: 5.3.1.1 Darstellung von Z Crotonsäure Gruppe 5: Andreas Kraft Thomas Kramer Johannes Landmann Datum: 3.10.2009 Aufgabenstellung: Die Aufgabe bestand darin,
Organisch Chemisches Praktikum II Gruppenpräparat: 5.3.1.1 Darstellung von Z Crotonsäure Gruppe 5: Andreas Kraft Thomas Kramer Johannes Landmann Datum: 3.10.2009 Aufgabenstellung: Die Aufgabe bestand darin,
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon)
 1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
1024 Eliminierung von Wasser aus 4-Hydroxy-4-methyl-2- pentanon
 0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
Benzol-d. Illumina-Chemie.de - Artikel
 Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
1. Darstellung von 2-Chlor-2-methylpropan Trivialname: tert. Butylchlorid
 1. Darstellung von 2-Chlor-2-methylpropan Trivialname: tert. Butylchlorid Theorie Nucleophile Substitution 1. Ordnung am gesättigten Kohlenstoffatom. Darstellung tertiärer Alkylhalogenide durch Umsetzung
1. Darstellung von 2-Chlor-2-methylpropan Trivialname: tert. Butylchlorid Theorie Nucleophile Substitution 1. Ordnung am gesättigten Kohlenstoffatom. Darstellung tertiärer Alkylhalogenide durch Umsetzung
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)-
 Christina Sauermann 1 Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)- C + Et 2 C H C 13 H 10 (M=182,22 g/mol) C 6 H 5
Christina Sauermann 1 Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)- C + Et 2 C H C 13 H 10 (M=182,22 g/mol) C 6 H 5
Gruppenpräparat. im Rahmen des OPII Praktikums. Darstellung von Triphenylethen V Darstellung von 9 Phenylphenanthren
 26.1.2009 Julius Maximilians Universität Würzburg Gruppenpräparat im Rahmen des OPII Praktikums V 6.2.4 Darstellung von Triphenylethen V 7.3.2.2 Darstellung von 9 Phenylphenanthren Gruppe 1: Gruppe 2:
26.1.2009 Julius Maximilians Universität Würzburg Gruppenpräparat im Rahmen des OPII Praktikums V 6.2.4 Darstellung von Triphenylethen V 7.3.2.2 Darstellung von 9 Phenylphenanthren Gruppe 1: Gruppe 2:
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
Synthese von Dibenzalaceton (DBA) (1,5-Bisphenylpenta-1E,4E-dien-3-on)
 Praktikum rganische Chemie I Zürich, 08.01.2006 529-0229-00L (für Biol./arm.Wiss) Wintersemester 05/06 Sylke öhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von Dibenzalaceton (DBA)
Praktikum rganische Chemie I Zürich, 08.01.2006 529-0229-00L (für Biol./arm.Wiss) Wintersemester 05/06 Sylke öhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von Dibenzalaceton (DBA)
(±)-4-Methyl-3- heptanon
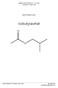
 Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
Darstellung von Chelidamsäure (gekürzte Version)
 CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol
 Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Grundpraktikum. Organische Chemie. Präparat x von 10. Präparatname nach IUPAC. Strukturformel des Produktes. Max Mustermann
 Grundpraktikum Organische Chemie Präparat x von 10 Präparatname nach IUPAC Strukturformel des Produktes Kommentar [AM1]: Laufende Nr. des Präparates. Kommentar [AM2]: Der Name ist der Literatur zu entnehmen.
Grundpraktikum Organische Chemie Präparat x von 10 Präparatname nach IUPAC Strukturformel des Produktes Kommentar [AM1]: Laufende Nr. des Präparates. Kommentar [AM2]: Der Name ist der Literatur zu entnehmen.
V 1 Herstellung von Natriumchlorid
 1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
2003 Säurekatalysierte Acetalisierung von 3-Nitrobenzaldehyd mit Ethandiol zum entsprechenden 1,3-Dioxolan
 2003 Säurekatalysierte Acetalisierung von 3-Nitrobenzaldehyd mit Ethandiol zum entsprechenden 1,3-Dioxolan H O NO 2 O O + HO 4-Toluolsulfonsäure Cyclohexan + HO H 2 O NO 2 C 7 H 5 NO 3 C 2 H 6 O 2 C 7
2003 Säurekatalysierte Acetalisierung von 3-Nitrobenzaldehyd mit Ethandiol zum entsprechenden 1,3-Dioxolan H O NO 2 O O + HO 4-Toluolsulfonsäure Cyclohexan + HO H 2 O NO 2 C 7 H 5 NO 3 C 2 H 6 O 2 C 7
Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan
 Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Endersch, Jonas 16.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.6/1: Benutzung des Wasserabscheiders zur Synthese von 2 (m Nitrophenyl) 1,3 dioxalan Reaktionsgleichung:
Organisches Praktikum I - SS 2006 Assistentin: Gabi Marti. Synthese von. Isobutylacetat. Zürich, Balzers & Eschen, Mai 2005
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
Synthese von 4-tert-Butyl-o-Xylol (4-tert-Butyl-1,2-Dimethylbenzol)
 Praktikum Organische Chemie I Chemnitz, 07.01.2006 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von 4-tert-Butyl-o-Xylol
Praktikum Organische Chemie I Chemnitz, 07.01.2006 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von 4-tert-Butyl-o-Xylol
5004 Säurekatalysierte Acetalisierung von 3-Nitrobenzaldehyd mit Ethandiol zum entsprechenden 1,3-Dioxolan
 5004 Säurekatalysierte Acetalisierung von 3-Nitrobenzaldehyd mit Ethandiol zum entsprechenden 1,3-Dioxolan H O O O NO 2 + HO HO 4-Toluolsulfonsäure + NO 2 O H 2 C 7 H 5 NO 3 C 2 H 6 O 2 C 7 H 8 O 3 S.
5004 Säurekatalysierte Acetalisierung von 3-Nitrobenzaldehyd mit Ethandiol zum entsprechenden 1,3-Dioxolan H O O O NO 2 + HO HO 4-Toluolsulfonsäure + NO 2 O H 2 C 7 H 5 NO 3 C 2 H 6 O 2 C 7 H 8 O 3 S.
Synthese von Acetessigsäureethylester
 Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Praktikumsprotokoll OP II Gruppenpräparat. Synthese von 2S 3S Epoxygeraniol
 Praktikumsprotokoll P II 10.4.4.1 Gruppenpräparat Synthese von 2S 3S Epoxygeraniol Praktikanten: Christian Possiel und Kai Stephan Feichtner Bachelor Datum: 14.4.2010 Verwendete Literatur 1) L. M. Bradley,
Praktikumsprotokoll P II 10.4.4.1 Gruppenpräparat Synthese von 2S 3S Epoxygeraniol Praktikanten: Christian Possiel und Kai Stephan Feichtner Bachelor Datum: 14.4.2010 Verwendete Literatur 1) L. M. Bradley,
Dibenzoylmethan
 9.1.2. Dibenzoylmethan Dibenzoylmethan ist eine Stufe eines Zweistufenprärates: Benzoylchlorid (8.1.11) Benzoesäureethylester (8.1.3) Dibenzoylmethan Reaktion: Ansatz: 1,75 g Natrium, 16,0 g Acetophenon,
9.1.2. Dibenzoylmethan Dibenzoylmethan ist eine Stufe eines Zweistufenprärates: Benzoylchlorid (8.1.11) Benzoesäureethylester (8.1.3) Dibenzoylmethan Reaktion: Ansatz: 1,75 g Natrium, 16,0 g Acetophenon,
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Gruppenpräparat im Rahmen des organisch-chemischen Praktikums II im Wintersemester 2006/2007 an der Universität Würzburg
 Gruppenpräparat im Rahmen des organisch-chemischen raktikums II im Wintersemester 2006/2007 an der Universität Würzburg Versuch 10.1.1: Trennung eines racemischen Gemisches aus (M)- und ()-2,2 -Dihydroxy-1,1
Gruppenpräparat im Rahmen des organisch-chemischen raktikums II im Wintersemester 2006/2007 an der Universität Würzburg Versuch 10.1.1: Trennung eines racemischen Gemisches aus (M)- und ()-2,2 -Dihydroxy-1,1
2002 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan
 22 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan 2 H 5 + H H Montmorillonit K 1 yclohexan 2 H 5 + H 2 6 H 1 3 (13.1) 2 H 6 2 (62.1) 8 H 14 4 (174.2)
22 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan 2 H 5 + H H Montmorillonit K 1 yclohexan 2 H 5 + H 2 6 H 1 3 (13.1) 2 H 6 2 (62.1) 8 H 14 4 (174.2)
6015 Bromaddition an Styrol zu 1,2-Dibrom-1-phenylethan
 6015 omaddition an Styrol zu 1,2-Dibrom-1-phenylethan 2 Dichlormethan C 8 H 8 2 (159.8) C 8 H 8 2 (104.2) (264.0) Klassifizierung Reaktionstypen und Stoffklassen Addition an Alkene, Stereoselektive Addition,
6015 omaddition an Styrol zu 1,2-Dibrom-1-phenylethan 2 Dichlormethan C 8 H 8 2 (159.8) C 8 H 8 2 (104.2) (264.0) Klassifizierung Reaktionstypen und Stoffklassen Addition an Alkene, Stereoselektive Addition,
Grundpraktikum Organische Chemie
 Grundpraktikum Organische Chemie Präparat X von 10 Präparatname nach IUPAC Name des Praktikanten Abgabedatum Unterschrift des Assistenten 1. Datum der Abgabe 2. 3. 1. Reaktionstyp: 1. Diazotierung 2. Sandmeyer-Reaktion
Grundpraktikum Organische Chemie Präparat X von 10 Präparatname nach IUPAC Name des Praktikanten Abgabedatum Unterschrift des Assistenten 1. Datum der Abgabe 2. 3. 1. Reaktionstyp: 1. Diazotierung 2. Sandmeyer-Reaktion
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
5 Chemisch-experimenteller Teil
 5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
Praktikum Advanced Inorganic Chemistry. Praktikumsanleitung Version 10/2012. Graetzel Zelle
 Praktikum Advanced Inorganic Chemistry Praktikumsanleitung Version 10/2012 Graetzel Zelle Synthese von cis-ru II (dcbpy) 2 (CS) 2 Chemikalien: RuCl 3 x H 2 5,5 -Dicarboxyl-2,2`-bipyridin (Herstellung s.
Praktikum Advanced Inorganic Chemistry Praktikumsanleitung Version 10/2012 Graetzel Zelle Synthese von cis-ru II (dcbpy) 2 (CS) 2 Chemikalien: RuCl 3 x H 2 5,5 -Dicarboxyl-2,2`-bipyridin (Herstellung s.
