III. Cycloalkane (Stereochemie II)
|
|
|
- David Björn Hofer
- vor 6 Jahren
- Abrufe
Transkript
1 49 III. Cycloalkane (Stereochemie II) (C 2 ) n-2 2 C C 2 (C 2 ) n-2 2 C C 2 C n 2n+2 Cn 2n Nomenklatur: Alkan Cycloalkan für n = 5 n-pentan Cyclopentan Bruttoformel allgemein C n 2n oder (C 2 ) n Cycloalkane verhalten sich in vieler insicht gleich wie acyclische Alkane, aber die geometrische Besonderheit der ingstruktur führt zu einigen Besonderheiten, die hier aufgrund ihrer Bedeutung genauer diskutiert werden müssen. Spannungsenergie C-C-spaltende eaktionen besitzen, verglichen mit acyclischen Verbindungen, bei Cyclen oft anormal hohe eaktivität Beispiel Verbrennung: C n 2n +.5 O 2 n CO 2 + n 2 O Δ n Die Verbrennungsenthalpie pro C 2 -Gruppe hängt stark von von n, also der inggröße, ab.
2 50 Verbrennungsenthalpien pro C 2 -Gruppe, Spannungsenergien und Bindungswinkeldeformation in Cycloalkanen (KJ/mol) Verbrennungsenthalpie Δ pro C n-alkan Cycloalkan inggröße Spannungsenergie im Molekül Bindungswinkeldeformation = = = = 0 Enthalp.cw2 Spannungsenergie (SE) = Δ n - n. (Δ 6 /6)
3 5 SE/n kleine nor male mi ttler e große inge (2) ingspannung: Typen, Ursache, Konsequenzen Drei Grundtypen von Spannung: - Winkeldeformation Baeyer-Spannung - Konformative Spannung Pitzer-Spannung - Transannulare WW Prelog-Spannung Der relative Anteil dieser Spannungen zur gesamten SE eines Moleküls ist von der inggröße abhängig Kleine inge (,4) Δα = C all-ekliptisch Baeyer-Spannung 78 kj/mol Pitzer-Spannung 8 kj/mol 6 KJ/mol
4 52 90 Δα = Δα = 2.5 Baeyer-Spannung 7 kj/mol Pitzer-Spannung 8 kj/mol 09 kj/mol - und 4-ing: Gesamtspannungsenergie fast gleich, aber SE/C 2 für 4-ing kleiner (Normierung) Allgemein: Abknicken des ings aus der planaren Struktur => Verkleinerung des Bindungswinkels => Verringerung der Baeyer-Spannung Wegen hoher ingspannung mögliche eaktionen: 2 /Pt 2 /Pt C C C C Br 2 Br 2 Br Br Normale inge (5,6,7) 08 planar 06 Baeyer-Spannung 0 kj/mol Pitzer-Spannung 27 kj/mol 27 KJ/mol
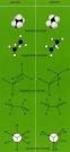
5 5 20 Sachse 906 Mohr 926 äquatorial axial ungünstig: Δα =49.5 all-ekliptisch 09.5 all-gestaffelt Mittlere inge (8-2/) Keine Bayer- und Pitzer-Spannung, dafür neu transannulare Spannung (Prelog-Spannung) Große inge (> ) Weitgehend spannungsfrei Konstruktion als Ausschnitt des Diamantgitters 4 Konformationen des Cyclohexans und seiner Monosubstitutionsprodukte Cyclohexanring bei weitem der wichtigste ing, da in zahlreichen Naturstoffen vorhanden Allgemein zwei Konformere:
6 54 Wanne/Boot Sessel eq Sessel ax Umklappen der Sessel-Form über die Boot-Form: Boot ungünstig aufgrund - der ekliptischen - Bug/eck-Interaktion Sessel: eq (C ) um ca. 7 kj/mol günstiger als ax Grund: 2 x anti versus 2 x gauche Methylcyclohexan: Ursache für die Bevorzugung des äquatorialen Isomers (vgl. Butan) C C C C axiales C gauche-n-butan C C C C äquatoriales C anti-n-butan
7 55 Substituenteneinfluß auf die Lage des Konformeren-Gleichgewichts von monosubstituierten Cyclohexanen K axial äquatorial K = [äquatorial] / [axial] ΔG = - T ln K für = C (-7. kj/mol) = - ( kj/mol) (298 K) ln K K=7.6 Gruppe G 0 [kjmol ] (axial äquatorial) F.05 Cl 2. Br 2. I.88 O 4.2 OC 2.0 OCOC 2.97 C 7. C 2 C 7.5 C C.72 C(C ) C(C ) C COO 5.4 COO 5.9 CN 0.8 OSO 2 C 6 4 C 2.8 Achtung: Anomerer Effekt! Bei Acetalen (Zucker) ist ein axialer Substituent bevorzugt: O O O O axial äquatorial Grund: C O C O hat andere Vorzugkonformation als C C C C (Butan-Typ)
8 56 Allgemeine konformationelle Situation von Cyclohexan: E pot [kj mol - ] Briefumschlag (Envelope) 40 2 Adamantan Wanne 6 2 Norbornan 2 Twist 27 0 eatkionskoordinate Twistan Abhängigkeit der Energie von der Konformation des Cyclohexans Disubstituierte Cyclohexane, Konfigurationsisomere Konstitution,2,,4 Konfiguration C C C C C trans cis C C C Diastereomere Umwandlung: Bindungsbruch Konfigurationsisomere C C
9 57 Konformation: Substituenten Sessel mit möglichst vielen equatorialen trans cis Chiralität Spiegel C C C C SE achiral Dia C C EN Enantiomere chiral Dia
10 58 Chiralität und verwandte Begriffe Chiralität ändigkeit (chiral) (händig) Nicht-Deckbarkeit von Bild und Spiegelbild Chirale Objekte: and Schuh Schnecke Schraube Aminosäure-Molekül (z.b. Alanin) Propeller Bedingung für Chiralität Objekt darf keine Spiegelebene Symmetriezentrum S 4 -Achse besitzen Achtung: Objekt darf Drehachsen besitzen (Propeller sind Chiral) asymetrisch chiral! Objekt ist asymetrisch, wenn kein Symmetrieelement vorhanden ist. achiral = nicht chiral achirale Objekte: Würfel (ohne Augen!) Methan-Molekül Mensch idealisiert Chiralitätszentrum tetraedrisches Atom mit 4 materiell oder geometrisch verschiedenen Liganden C C Cl COO
11 59 Dekalin, Steroide Decalin Konfiguration achiral! cis trans Konformation cis trans spannungsfrei Steroide
12 60 C C O C C O Cholesterol besser: C C O Wannen-artig
13 6 Systematische Bezeichnung von Bi-, Tri-, und Tetra-cycloalkanen. Man überführt das eventuell dreidimensionale Formelbild in eine geignete planare Darstellung. 2. Man legt denjenigen ing als auptring fest, der die meisten C-Atome enthält.. Man legt die auptbrücke so fest, daß der auptring möglichst symmetrisch geteilt wird, und daß die auptbrücke möglichst groß wird. 4. Die Bezifferung beginnt an einem Brückenkopf und läuft auf dem längsten Weg (auptring) dahin zurück. Dann folgen die auptbrücke und die Sekundärbrücken. Die Brückenköpfe der Sekundärbrücken werden durch Superscripte angegeben.
14 Norbornan Bicyclo[2.2.]heptan cis-dekalin cis-bicyclo[4.4.0]decan 2 4 Tetrahedran Tricyclo[ ,4 ]butan 6 2 Prisman 5 4 Tetracyclo[ ,6.0,5 ]- hexan Adamantan Tricyclo[...,7 ]decan Twistan Tricyclo[ ,8 ]decan 8
Stereochemie organischer Verbindungen
 Stereochemie organischer Verbindungen Stereochemische Prinzipien 1.1 Symmetrie, Symmetrieoperationen, Punktgruppen Der Begriff Stereochemie (griech: stereos = Feststoff) bezieht sich auf die Betrachtung
Stereochemie organischer Verbindungen Stereochemische Prinzipien 1.1 Symmetrie, Symmetrieoperationen, Punktgruppen Der Begriff Stereochemie (griech: stereos = Feststoff) bezieht sich auf die Betrachtung
2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen
 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle Gruppen Es gibt
Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle Gruppen Es gibt
2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen
 Inhalt Index 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle Gruppen Es gibt heute ungefähr neun Millionen bekannter organischer
Inhalt Index 2. Organische Verbindungen - Einordnung nach funktionellen Gruppen. Alkane : Moleküle ohne funktionelle Gruppen 2.1 Funktionelle Gruppen Es gibt heute ungefähr neun Millionen bekannter organischer
Organische Chemie für MST 6. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
Organische Chemie für MST 6 Lienkamp/ Prucker/ Rühe Valenzisomere Inhalt 6 Isomerie Konstitutionsisomere Tautomere/ Protonenisomere (= Strukturisomere) Skelett-Isomere Isomerie Isomere = Substanzen mit
Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig
 26 sisomerie (Stereoisomerie I) Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig Isomerie II: sisomere: sisomere (bzw. Konformere) sind Isomere, die sich durch
26 sisomerie (Stereoisomerie I) Konstitutionsisomerie nicht einzige Art der Isomerie, daneben sind auch Stereoisomerie wichtig Isomerie II: sisomere: sisomere (bzw. Konformere) sind Isomere, die sich durch
Moleküle mit mehr als einem Chiralitätselement
 Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Moleküle mit mehr als einem hiralitätselement Natürlich kommt es häufig vor, dass Moleküle mehr als ein hiralitätselement enthalten. ierbei ist eine neue Art der Isomerie zu finden. Im Folgenden sind zunächst
Organisch-Chemisches Institut Fakultät für Chemie und Geowissenschaften Universität Heidelberg 4. September 2015
 Organisch-Chemisches Institut Fakultät für Chemie und Geowissenschaften Universität Heidelberg 4. September 2015 Musterlösung Zwischennachklausur II zur Experimentalvorlesung Organische Chemie von Prof.
Organisch-Chemisches Institut Fakultät für Chemie und Geowissenschaften Universität Heidelberg 4. September 2015 Musterlösung Zwischennachklausur II zur Experimentalvorlesung Organische Chemie von Prof.
Prof. Dr. Stephen Hashmi, Sommersemester Organische Chemie für Technische Biologen, Organische Chemie für Lehramtskandidaten, Teil 2.
 Prof. Dr. ashmi, Sommersemester 2005 13 IV. Alkane Methan -C 2 - Ethan -C 2 -C 2 - Propan -C 2 -C 2 -C 2 - Butan -C 2 -C 2 -C 2 -C 2 - Pentan -C 2 -C 2 -C 2 -C 2 -C 2 - exan -C 2 -C 2 -C 2 -C 2 -C 2 -C
Prof. Dr. ashmi, Sommersemester 2005 13 IV. Alkane Methan -C 2 - Ethan -C 2 -C 2 - Propan -C 2 -C 2 -C 2 - Butan -C 2 -C 2 -C 2 -C 2 - Pentan -C 2 -C 2 -C 2 -C 2 -C 2 - exan -C 2 -C 2 -C 2 -C 2 -C 2 -C
Grundlagen zum Verständnis chemischer Reaktionen = Handwerkszeug
 Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Grundlagen zum Verständnis chemischer Reaktionen = andwerkszeug chemische Bindung: ionische, kovalente, Dipolmomente, Bindungsstärke, Atom- und Molekülorbitale, ybridisierung Substanzklassen, funktionelle
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
Beuth Hochschule für Technik Berlin, Studiengang Pharma- und Chemietechnik Tutorium Organische Chemie 1 (SS 2011), Tutor: Sascha Behne
 IUPAC-Nomenklatur 1.) Zeichnen Sie die Struktur von: a) 4-(1-Methylethyl)heptan b) 2,3,4,4-Tetramethylhexan c) cis-1,2-dimethylcyclohexan d) 6-Brom-7-(chlormethyl)nonan-2,3-diol e) Isopren f) trans-1,2-diethylcyclopropan
IUPAC-Nomenklatur 1.) Zeichnen Sie die Struktur von: a) 4-(1-Methylethyl)heptan b) 2,3,4,4-Tetramethylhexan c) cis-1,2-dimethylcyclohexan d) 6-Brom-7-(chlormethyl)nonan-2,3-diol e) Isopren f) trans-1,2-diethylcyclopropan
Chiralität in der Natur und synthetisch
 Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
Chiralität in der Natur und synthetisch Universität Ulm Demonstrationskurs 09/10 Christine Ohmayer Folie 1 Beispiel Carvon Summenformel von Carvon : C 12 H 10 O Eigenschaften: farblose Flüssigkeit Geruch:
OC 3 - Stereochemie. Allgemeine Hintergründe
 OC 3 - Stereochemie Allgemeine Hintergründe Einführung Folie Nr. 2 3-dimensionale Anordnung (relativ/absolut) in der realen Welt sind extrem wichtig Bild rechts: http://de.wikipedia.org/wiki/pfefferminz,
OC 3 - Stereochemie Allgemeine Hintergründe Einführung Folie Nr. 2 3-dimensionale Anordnung (relativ/absolut) in der realen Welt sind extrem wichtig Bild rechts: http://de.wikipedia.org/wiki/pfefferminz,
Stoffklassen in der Organischen Chemie. Nomenklaturfragen. Isomerie und sterischer Bau
 Stoffklassen in der Organischen Chemie Nomenklaturfragen Isomerie und sterischer Bau 1 Stoffklassen in der organischen Chemie Kohlenwasserstoffe Kohlenwasserstoffe mit Substituenten Y (eteroatom oder funktionelle
Stoffklassen in der Organischen Chemie Nomenklaturfragen Isomerie und sterischer Bau 1 Stoffklassen in der organischen Chemie Kohlenwasserstoffe Kohlenwasserstoffe mit Substituenten Y (eteroatom oder funktionelle
Isomerie organischer Verbindungen
 15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
15 Isomerie organischer Verbindungen Organische Verbindungen können, bei gleicher Summenformel, sehr unterschiedliche Strukturen besitzen. Moleküle mit gleicher Summenformel aber unterschiedlicher Struktur
Vokabular zur Stereochemie
 Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Vokabular zur tereochemie Zwei Moleküle mit gleicher ummenformel sind: deckungsgleich = identisch Isomere Konstitutionsisomere tereoisomere Enantiomere Diastereomere Konstitutionsisomere: Moleküle mit
Seminar zum Praktikum Anorganische Chemie III III
 Seminar zum Praktikum Anorganische Chemie III III Metallorganische Chemie Dr. J. Wachter IR-Teil3 www.chemie.uni-regensburg.de/anorganische_chemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_chemie/wachter/lehre.html
Seminar zum Praktikum Anorganische Chemie III III Metallorganische Chemie Dr. J. Wachter IR-Teil3 www.chemie.uni-regensburg.de/anorganische_chemie/scheer/lehre.html www.chemie.uniregensburg.de/anorganische_chemie/wachter/lehre.html
Spezielle Methoden der pharmazeutischen Chemie 2
 Spezielle thoden der pharmazeutischen Chemie 2 Asymmetrische Synthese (für Diplomanden und Dissertanten im Fach Pharmazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Symmetrie, Asymmetrie, Chiralität
Spezielle thoden der pharmazeutischen Chemie 2 Asymmetrische Synthese (für Diplomanden und Dissertanten im Fach Pharmazeutischen Chemie/Synthese) Kapiteleinteilung: 1. Symmetrie, Asymmetrie, Chiralität
10. MODELLE VON MOLEKÜLEN
 73 10. MODELLE VON MOLEKÜLEN Durch die Kenntnis der dreidimensionalen Gestalt der Moleküle lassen sich ihre biologischen Funktionen und der oft überraschend große Einfluss kleiner Veränderungen der Struktur
73 10. MODELLE VON MOLEKÜLEN Durch die Kenntnis der dreidimensionalen Gestalt der Moleküle lassen sich ihre biologischen Funktionen und der oft überraschend große Einfluss kleiner Veränderungen der Struktur
H 3 C. alphabetische Reihenfolge! kleinerer Ring wird zum Rest
 ycloalkane Kohlenwasserstoffe, die einfach geundene -Atome in ringförmiger Anordnung enthalten, werden als ycloalkane, cyclische Alkane oder arocyclen ezeichnet. Die Mehrzahl aller organischer Verindungen
ycloalkane Kohlenwasserstoffe, die einfach geundene -Atome in ringförmiger Anordnung enthalten, werden als ycloalkane, cyclische Alkane oder arocyclen ezeichnet. Die Mehrzahl aller organischer Verindungen
Stereochemie. mit Vitamin C. Süßstoff Aspartam (QWKlOWÃHLQHÃ3KHQ\ODODQLQTXHOOH. L(+)-Milchsäure. Zuckeraustauschstoff Sorbit
 Stereochemie mit Vitamin Süßstoff Aspartam (QWKlWÃLQÃ3KQ\DDQLQTX L(+)-Milchsäure Zuckeraustauschstoff Sorbit hemie für Mediziner Isomerie organischer Verbindungen Isomere Konstitutionsisomere Stereoisomere
Stereochemie mit Vitamin Süßstoff Aspartam (QWKlWÃLQÃ3KQ\DDQLQTX L(+)-Milchsäure Zuckeraustauschstoff Sorbit hemie für Mediziner Isomerie organischer Verbindungen Isomere Konstitutionsisomere Stereoisomere
Decan Homologe Reihe der Alkane, unterschiedlich lange C-Ketten mit C- C (sp 3 /sp 3 ) und C-H (sp 3 /s)-bindungen (σ-bindungen) Beispiele: Butan
 1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
1 30.09.005 0.1 Alkane Eine einfache Stoffgruppe der organischen Chemie sind die Alkane. Dabei handelt es sich um eine spezielle Gruppe der Kohlenwasserstoffe (KW). Alle Alkane gehorchen folgendem Prinzip:
Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe
 1 Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe Warm Up 1) Erweitern Sie die Ihnen bekannten Regeln der Nomenklatur für Alkene und benennen danach folgende Verbindungen. Die Regel zur
1 Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe Warm Up 1) Erweitern Sie die Ihnen bekannten Regeln der Nomenklatur für Alkene und benennen danach folgende Verbindungen. Die Regel zur
Stereochemie. Allgemeines. Einteilung. Darstellung. Analytik. Was ist Chiralität Welche Relevanz hat sie
 Stereochemie Allgemeines Was ist Chiralität Welche elevanz hat sie Einteilung Zentrale Chiralität Axiale Chiralität elicale Chiralität Darstellung Fischer-Projektion CIP-Konvention Analytik Instrumentelle
Stereochemie Allgemeines Was ist Chiralität Welche elevanz hat sie Einteilung Zentrale Chiralität Axiale Chiralität elicale Chiralität Darstellung Fischer-Projektion CIP-Konvention Analytik Instrumentelle
8. Stereochemie organischer Moleküle 8.1
 8. Stereochemie organischer Moleküle 8.1 Stereochemie organischer Moleküle Zur Darstellung der Struktur organischer Moleküle werden oft Formeln verwendet, welche den räumlichen Bau nicht zum Ausdruck bringen.
8. Stereochemie organischer Moleküle 8.1 Stereochemie organischer Moleküle Zur Darstellung der Struktur organischer Moleküle werden oft Formeln verwendet, welche den räumlichen Bau nicht zum Ausdruck bringen.
Organische Chemie. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie Name: Fachprüfung Vorname: 11. März 2002, 8 00-10 00 h Matr.-Nr.: Raum 204 + 206 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10 Punkten
Organische Chemie Name: Fachprüfung Vorname: 11. März 2002, 8 00-10 00 h Matr.-Nr.: Raum 204 + 206 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10 Punkten
Chiralitätszentrum X X
 hiralitätszentrum Die weitaus meisten chiralen Verbindungen ist deswegen chiral, weil sie sog. asymmetrische Kohlenstoffatome enthalten. Dies sind tetraedrisch konfigurierte -Atome mit vier verschiedenen
hiralitätszentrum Die weitaus meisten chiralen Verbindungen ist deswegen chiral, weil sie sog. asymmetrische Kohlenstoffatome enthalten. Dies sind tetraedrisch konfigurierte -Atome mit vier verschiedenen
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
L.9 Organische Chemie I
 L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
Stereochemie. Grundbegriffe. Bearbeitet von K.-H Hellwich
 Stereochemie Grundbegriffe Bearbeitet von K.-H Hellwich Neuausgabe 2007. Taschenbuch. xii, 120 S. Paperback ISBN 978 3 540 71707 2 Format (B x L): 14 x 21,6 cm Gewicht: 181 g Weitere Fachgebiete > Chemie,
Stereochemie Grundbegriffe Bearbeitet von K.-H Hellwich Neuausgabe 2007. Taschenbuch. xii, 120 S. Paperback ISBN 978 3 540 71707 2 Format (B x L): 14 x 21,6 cm Gewicht: 181 g Weitere Fachgebiete > Chemie,
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester am
 Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester 2014 am 18.06.2014 Name: Matrikelnummer: Studiengang: Unterschrift: Aufgabe 1 2 3 4 5 6 7 8 9 10 Gesamt max. Punktzahl 10 10
Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester 2014 am 18.06.2014 Name: Matrikelnummer: Studiengang: Unterschrift: Aufgabe 1 2 3 4 5 6 7 8 9 10 Gesamt max. Punktzahl 10 10
13.12.2014. Chemie für Mediziner. Kapitel 9: Aufbau und Struktur organischer Verbindungen. Kapitel 9: Aufbau und Struktur organischer Verbindungen
 . 13.12.2014 Chemie für Mediziner Jun.-Prof. Dr. Michael Giese Raum S07 S04 C25 michael.giese@uni-due.de 9.1 Was ist Organische Chemie? 9.2 Das besondere am Kohlenstoff 9.3 Bindungsverhältnisse in organischen
. 13.12.2014 Chemie für Mediziner Jun.-Prof. Dr. Michael Giese Raum S07 S04 C25 michael.giese@uni-due.de 9.1 Was ist Organische Chemie? 9.2 Das besondere am Kohlenstoff 9.3 Bindungsverhältnisse in organischen
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 0-2, S04 T0 A02 Paul Rademacher Institut für rganische hemie der Universität Duisburg-Essen (Teil 2: 2.0.2005) MILESS: hemie für Biologen 28 Konstitutionsisomere:
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 0-2, S04 T0 A02 Paul Rademacher Institut für rganische hemie der Universität Duisburg-Essen (Teil 2: 2.0.2005) MILESS: hemie für Biologen 28 Konstitutionsisomere:
ORGANISCHE CHEMIE. Prof. Dipl.-Ing. Manfred SUSSITZ. Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt
 ORGANISCHE CHEMIE Prof. Dipl.-Ing. Manfred SUSSITZ Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt 1. Kohlenwasserstoffe KW Kohlenstoff "Kohlenstoff ist in organischen Verbindungen
ORGANISCHE CHEMIE Prof. Dipl.-Ing. Manfred SUSSITZ Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt 1. Kohlenwasserstoffe KW Kohlenstoff "Kohlenstoff ist in organischen Verbindungen
Schriftliche Sessionsprüfung Organische Chemie. Teilprüfung OC I F. Diederich, C. Schaack. Herbstsemester 2015
 Schriftliche Sessionsprüfung rganische Chemie Teilprüfung C I F. Diederich, C. Schaack erbstsemester 2015 Bitte überprüfen Sie: der Prüfungsbogen beinhaltet 5 Aufgaben auf 8 Seiten. Bitte beachten Sie:
Schriftliche Sessionsprüfung rganische Chemie Teilprüfung C I F. Diederich, C. Schaack erbstsemester 2015 Bitte überprüfen Sie: der Prüfungsbogen beinhaltet 5 Aufgaben auf 8 Seiten. Bitte beachten Sie:
I. Alkane Homologe Reihe, Nomenklatur
 Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
CCl 3. 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan
 V. alogenalkane 2 l 2, l 3, l 4 : wichtige Lösungsmittel l l 1,2-Dichlorethan Insektizid DDT l l 2 1 l 3 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan - Insektizid (P. Müller,
V. alogenalkane 2 l 2, l 3, l 4 : wichtige Lösungsmittel l l 1,2-Dichlorethan Insektizid DDT l l 2 1 l 3 1,1,1-Trichlor-2,2-di(4-chlorphenyl)ethan Dichlordiphenyltrichlorethan - Insektizid (P. Müller,
STEREOCHEMIE. Eine kurze Einführung für die AHS (Unterricht, WPG, Olympiade)
 STERECEMIE Eine kurze Einführung für die AS (Unterricht, WPG, lympiade) Manfred Kerschbaumer, 2006 Inhaltsverzeichnis A. Einleitung B. Die Struktur von Teilchen 1. Arten von Teilchen 2. Konstitution -
STERECEMIE Eine kurze Einführung für die AS (Unterricht, WPG, lympiade) Manfred Kerschbaumer, 2006 Inhaltsverzeichnis A. Einleitung B. Die Struktur von Teilchen 1. Arten von Teilchen 2. Konstitution -
Skript für die. Experimentalvorlesung Organische Chemie I (OCI) Sommersemester 2003. Paul Rademacher
 Experimentalvorlesung rganische Chemie I, SS 2003 Skript für die Experimentalvorlesung rganische Chemie I (CI) im Sommersemester 2003 Paul ademacher (Stand 23.02.2005) 2 Experimentalvorlesung rganische
Experimentalvorlesung rganische Chemie I, SS 2003 Skript für die Experimentalvorlesung rganische Chemie I (CI) im Sommersemester 2003 Paul ademacher (Stand 23.02.2005) 2 Experimentalvorlesung rganische
3. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
 3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
Molekülsymmetrie und Kristallographie. Chiralität
 hiralität Die hiralität ist eines der wichtigsten Grundprinzipien der Natur überhaupt. Sie bezeichnet die Tatsache, dass es Gegenstände gibt, die sich zueinander wie Bild und Spiegelbild verhalten, sich
hiralität Die hiralität ist eines der wichtigsten Grundprinzipien der Natur überhaupt. Sie bezeichnet die Tatsache, dass es Gegenstände gibt, die sich zueinander wie Bild und Spiegelbild verhalten, sich
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Organische Chemie. Einstieg. Chemie-Formeldarstellungen. Formeldarstellungen der Chemie: Bei Ionenverbindungen: Verhältnisformeln. , AlF 3. etc.
 Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Chemische Thermodynamik ENTROPIE LÖSUNGEN
 L-Üb29: Die Standardentropie der Edelgase steigt in regelmässiger Weise mit der molaren Masse. Diese schöne Regelmässigkeit kommt daher, dass die Edelgase nur Translationsenergie besitzen und keine Schwingungsenergie
L-Üb29: Die Standardentropie der Edelgase steigt in regelmässiger Weise mit der molaren Masse. Diese schöne Regelmässigkeit kommt daher, dass die Edelgase nur Translationsenergie besitzen und keine Schwingungsenergie
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Konfigurationsisomerie (Stereoisomerie)
 Konfigurationsisomerie (Stereoisomerie) Komplexe, die dieselbe chemische Zusammensetzung (gleiche Summenformel) und Ladung, aber einen verschiedenen räumliche Anordnung (Konfiguration) der Atome haben,
Konfigurationsisomerie (Stereoisomerie) Komplexe, die dieselbe chemische Zusammensetzung (gleiche Summenformel) und Ladung, aber einen verschiedenen räumliche Anordnung (Konfiguration) der Atome haben,
2.1 Homologe Reihe, Nomenklatur, Konstitution, Konformation CH 2
 Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler. Alkane.1 omologe Reihe, Nomenklatur, Konstitution, Konformation.1.1 omologe Reihe
Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler. Alkane.1 omologe Reihe, Nomenklatur, Konstitution, Konformation.1.1 omologe Reihe
Einführung in die Organische Chemie. Benjamin Grimm
 Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen
 Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Vorlesung Anorganische Chemie II im SS 2007 (Teil 2) Hans-Jörg Deiseroth Anorganische Chemie Fb 8 Universität Siegen (unter Verwendung von Folien des Buches Allgemeine und Anorganische Chemie, Binnewies
Organische Chemie I/II. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1
 Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1 Brownsche Bewegung Beobachte die Bewegung von Rauchteilchen unter dem Miskroskop. Wie kann man die vom schottischen Botaniker
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Blatt 1 Brownsche Bewegung Beobachte die Bewegung von Rauchteilchen unter dem Miskroskop. Wie kann man die vom schottischen Botaniker
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1
 Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Organische Chemie 1 SS2011 Tutorium Übungsblatt 12 Seite 1 1) Ordnen Sie die folgenden aromatischen Verbindungen nach steigender Reaktivität in der elektrophilen aromatischen Substitution. Chlorbenzol,
Chemie der Kohlenhydrate
 Chemie der Kohlenhydrate Grundlegendes Der Begriff Kohlenhydrate: Wurde ursprünglich aus der Formel für Glukose abgeleitet. C 6 H 12 O 6 = C 6 (H 2 O) 6 Bzw. allgemein: C n (H 2 O) m Diese missleitende
Chemie der Kohlenhydrate Grundlegendes Der Begriff Kohlenhydrate: Wurde ursprünglich aus der Formel für Glukose abgeleitet. C 6 H 12 O 6 = C 6 (H 2 O) 6 Bzw. allgemein: C n (H 2 O) m Diese missleitende
Hellwich Stereochemie Grundbegriffe
 Hellwich Stereochemie Grundbegriffe K.-H. Hellwich Stereochemie Grundbegriffe 2., erweiterte Auflage 123 Dr. Karl-Heinz Hellwich Postfach 10 07 31 63007 Offenbach E-Post: khellwich@web.de Bibliografische
Hellwich Stereochemie Grundbegriffe K.-H. Hellwich Stereochemie Grundbegriffe 2., erweiterte Auflage 123 Dr. Karl-Heinz Hellwich Postfach 10 07 31 63007 Offenbach E-Post: khellwich@web.de Bibliografische
ein Zweig der chemischen Wissenschaft, der sich mit der dreidimensionalen Struktur der Moleküle beschäftigt
 Stereochemie Stereochemie: ein Zweig der chemischen Wissenschaft, der sich mit der dreidimensionalen Struktur der Moleküle beschäftigt Stereoisomerie: unterschiedliche räumliche Anordnungen der Atome oder
Stereochemie Stereochemie: ein Zweig der chemischen Wissenschaft, der sich mit der dreidimensionalen Struktur der Moleküle beschäftigt Stereoisomerie: unterschiedliche räumliche Anordnungen der Atome oder
ChO/OCI/ /A. Griesbeck. Chiralität optische Aktivität Stereoisomerie Enantiomere & Diastereomere Symmetrie Symmetrieelemente
 Ch/CI/25.5.07/A. Griesbeck Chiralität optische Aktivität Stereoisomerie Enantiomere & Diastereomere Symmetrie Symmetrieelemente Chiralität ptische Aktivität 3- und 2-dimensionale Chiralität echte Hand
Ch/CI/25.5.07/A. Griesbeck Chiralität optische Aktivität Stereoisomerie Enantiomere & Diastereomere Symmetrie Symmetrieelemente Chiralität ptische Aktivität 3- und 2-dimensionale Chiralität echte Hand
M U S T E R L Ö S U N G
 Universität egensburg Institut für rganische Chemie Prof. Dr.. eiser 3. Klausur zum rganisch-chemischen Praktikum I für Studierende der Chemie und der Biochemie im SS 999 am Freitag, dem 3. Juli 999 M
Universität egensburg Institut für rganische Chemie Prof. Dr.. eiser 3. Klausur zum rganisch-chemischen Praktikum I für Studierende der Chemie und der Biochemie im SS 999 am Freitag, dem 3. Juli 999 M
Ein Alkan, dem ein H-Atom fehlt, wird Alkyl-Rest genannt. Der Name ergibt sich aus dem Alkan, jedoch mit der Endung yl:
 Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Organische Chemie. 11. Juli 2002, h Matr.-Nr.: Raum 183. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie Name: Fachprüfung Vorname: 11. Juli 2002, 8 00-10 00 h Matr.-Nr.: Raum 183 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10 Punkten
Organische Chemie Name: Fachprüfung Vorname: 11. Juli 2002, 8 00-10 00 h Matr.-Nr.: Raum 183 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10 Punkten
7. Zucker - Kohlenhydrate
 7. Zucker - Kohlenhydrate 7.1 Die Namen und Strukturen der Kohlenhydrate Die einfachsten Kohlenhydrate sind Monosaccharide, z.b. Glucose und Fructose. Sie enthalten eine Aldehyd- oder Keton-Gruppe mit
7. Zucker - Kohlenhydrate 7.1 Die Namen und Strukturen der Kohlenhydrate Die einfachsten Kohlenhydrate sind Monosaccharide, z.b. Glucose und Fructose. Sie enthalten eine Aldehyd- oder Keton-Gruppe mit
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 06.07.2013 NAME;
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 06.07.2013 NAME;
Chemistry - accept the challenge
 Chemistry - accept the challenge Vorlesung Grundlagen der rganischen Chemie Prof. Dr. Thomas Lindel, www.oc.tu-bs.de/lindel TU Braunschweig Literatur: K. P. C. Vollhardt, N. E. Schore, "rganische Chemie",
Chemistry - accept the challenge Vorlesung Grundlagen der rganischen Chemie Prof. Dr. Thomas Lindel, www.oc.tu-bs.de/lindel TU Braunschweig Literatur: K. P. C. Vollhardt, N. E. Schore, "rganische Chemie",
Vorlesung. Einführung in die Chemie Teil B: Organische Chemie WS 2004 / Thomas Ziegler
 Vorlesung Einführung in die Chemie Teil B: Organische Chemie WS 2004 / 2005 Thomas Ziegler INHALT Allgemeines (Literatur) 1. Chemische Bindung in der Organischen Chemie 1.1. Orbitale am Kohlenstoff 1.2.
Vorlesung Einführung in die Chemie Teil B: Organische Chemie WS 2004 / 2005 Thomas Ziegler INHALT Allgemeines (Literatur) 1. Chemische Bindung in der Organischen Chemie 1.1. Orbitale am Kohlenstoff 1.2.
Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen
 2. Alkane Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen 2.1 unverzweigte Alkane Formel: C n 2n+2 = -(C 2 ) n - homologe Reihe n Name Formel Schmp.
2. Alkane Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen 2.1 unverzweigte Alkane Formel: C n 2n+2 = -(C 2 ) n - homologe Reihe n Name Formel Schmp.
Organische Stofflehre
 Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Organische Chemie. Kohlenwasserstoffe. Alkane. Alkane
 1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
3.1 Chemische Bindung (siehe auch Ehlers, Chemie I, Kap. 1.4)
 3 3.1 Chemische Bindung (siehe auch Ehlers, Chemie I, Kap. 1.4) 3.1.1 Orbitale, deren Hybridisierung und Überlappung 3.1.1.1 Atomorbitale Als Folge der Heisenbergschen Unschärferelation lassen sich Ort
3 3.1 Chemische Bindung (siehe auch Ehlers, Chemie I, Kap. 1.4) 3.1.1 Orbitale, deren Hybridisierung und Überlappung 3.1.1.1 Atomorbitale Als Folge der Heisenbergschen Unschärferelation lassen sich Ort
C. Röhr, Phosphor, WS 09/10. Phosphor Phosphane Phosphide -
 Phosphor Phosphane Phosphide - Inhalt Einleitung Elementmodifikationen Phosphane/Phosphide mit PH/P : P > 1 (Kettenstücke) Phosphane/Phosphide mit PH/P : P = 1 (Ketten und Ringe) Phosphane/Phosphide mit
Phosphor Phosphane Phosphide - Inhalt Einleitung Elementmodifikationen Phosphane/Phosphide mit PH/P : P > 1 (Kettenstücke) Phosphane/Phosphide mit PH/P : P = 1 (Ketten und Ringe) Phosphane/Phosphide mit
Stereochemie. Vorlesung SS 2003 FU-Berlin Professor M. Kalesse
 Stereochemie Vorlesung SS 2003 FU-Berlin Professor M. Kalesse Einführung in die Stereochemie 1) Molekulare Konnektivität beschreibt, in welcher Reihenfolge die Atome einer Substanz miteinander verbunden
Stereochemie Vorlesung SS 2003 FU-Berlin Professor M. Kalesse Einführung in die Stereochemie 1) Molekulare Konnektivität beschreibt, in welcher Reihenfolge die Atome einer Substanz miteinander verbunden
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen II
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen II Elektronenpaarbindung, Elektronegativität, polare Atombindung, Dipolmoment, Hybridisierung von Atomorbitalen, sp 3 -, sp 2 -, sp-hybridorbitale,
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische Bindungen II Elektronenpaarbindung, Elektronegativität, polare Atombindung, Dipolmoment, Hybridisierung von Atomorbitalen, sp 3 -, sp 2 -, sp-hybridorbitale,
Kohlenstoffverbindungen
 Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Zucker und Polysaccharide (Voet Kapitel 10)
 Zucker und Polysaccharide (Voet Kapitel 10) 1. Monosaccharide 2. Polysaccharide 3. Glycoproteine Kohlenhydrate oder Saccharide = essentielle Bestandteile der Organismen = Hydrate des Kohlenstoffs Grundbaustein
Zucker und Polysaccharide (Voet Kapitel 10) 1. Monosaccharide 2. Polysaccharide 3. Glycoproteine Kohlenhydrate oder Saccharide = essentielle Bestandteile der Organismen = Hydrate des Kohlenstoffs Grundbaustein
Fachbereich Chemie Philipps-Universität Marburg. Stereochemie
 Fachbereich Chemie Philipps-Universität Marburg Stereochemie Dies ist kein vollständiges Skript. ier finden Sie vorlesungsbegleitende Unterlagen (Definitionen, Abbildungen, Literatur), die kein Ersatz
Fachbereich Chemie Philipps-Universität Marburg Stereochemie Dies ist kein vollständiges Skript. ier finden Sie vorlesungsbegleitende Unterlagen (Definitionen, Abbildungen, Literatur), die kein Ersatz
Inhaltsverzeichnis zu Kapitel 2. Alkane
 Inhaltsverzeichnis zu Kapitel 2. Alkane 2. Alkane 2.1. Valenzstrichformel, omologe Reihe, Nomenklatur, Konstitution, 22 Konformation 2.1.1. Valenzstrichformel 22 2.1.2. omologe Reihe 23 2.1.3. Konstitutionsisomere
Inhaltsverzeichnis zu Kapitel 2. Alkane 2. Alkane 2.1. Valenzstrichformel, omologe Reihe, Nomenklatur, Konstitution, 22 Konformation 2.1.1. Valenzstrichformel 22 2.1.2. omologe Reihe 23 2.1.3. Konstitutionsisomere
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
z y n ; C n n-m Cn = E
 9. Molekülsymmetrie (Punktgruppen) 9. Symmetrieelemente und -operationen (SE und SO) Koordinatenzuweisung erfolgt nach der Finger-Regel der rechten Hand: y z D Zf Mf z y = z y Identität E = C Drehung um
9. Molekülsymmetrie (Punktgruppen) 9. Symmetrieelemente und -operationen (SE und SO) Koordinatenzuweisung erfolgt nach der Finger-Regel der rechten Hand: y z D Zf Mf z y = z y Identität E = C Drehung um
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Grundlagen der organischen Chemie: Gesättigte Kohlenwasserstoffe
 Grundlagen der organischen Chemie: Gesättigte Kohlenwasserstoffe Patrick Bucher 13. August 2011 Inhaltsverzeichnis 1 Einführung in die organische Chemie 1 1.1 Die Einteilung der organischen Verbindungen..................
Grundlagen der organischen Chemie: Gesättigte Kohlenwasserstoffe Patrick Bucher 13. August 2011 Inhaltsverzeichnis 1 Einführung in die organische Chemie 1 1.1 Die Einteilung der organischen Verbindungen..................
Eliminierungsreaktionen: E1- und E2- Mechanismen; Olefine
 Eliminierungsreaktionen: E1 und E2 chanismen; lefine Allgemeine Gleichung der Eliminierung: Base X X Die Bindung wird am Atom gebrochen. Für die Qualität der Abgangsgruppe X gelten die selben egeln wie
Eliminierungsreaktionen: E1 und E2 chanismen; lefine Allgemeine Gleichung der Eliminierung: Base X X Die Bindung wird am Atom gebrochen. Für die Qualität der Abgangsgruppe X gelten die selben egeln wie
Std. Stoffklassen Konzepte & Methoden Reaktionen 2 Struktur und Bindung 2 Alkane Radikale Radikal-Reaktionen 2 Cycloalkane Konfiguration &
 Materialien (Version: 26.06.2001) Diese Materialien dienen zur Überprüfung des Wissens und sind keine detailierten Lernunterlagen. Vorschlag: fragen Sie sich gegenseitig entsprechend dieser Listen ab.
Materialien (Version: 26.06.2001) Diese Materialien dienen zur Überprüfung des Wissens und sind keine detailierten Lernunterlagen. Vorschlag: fragen Sie sich gegenseitig entsprechend dieser Listen ab.
Inhaltsverzeichnis. Teil I Volle Kraft voraus: Die Chemie des Kohlenstoffs 23. Einführung 17. Kapitel 1 Die wundervolle Welt der organischen Chemie 25
 Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Diene: C n H 2n-2 : 2 Doppelbindungen
 Diene: n 2n-2 : 2 Doppelbindungen I_folie63 ) Isolierte Diene: Die beiden Doppelbindungen sind durch ein oder mehrere sp 3 -hybridisierte - Atome getrennt. 2 2 3 2 4 5 2,4-Pentadien sp 3 2) Kumulierte
Diene: n 2n-2 : 2 Doppelbindungen I_folie63 ) Isolierte Diene: Die beiden Doppelbindungen sind durch ein oder mehrere sp 3 -hybridisierte - Atome getrennt. 2 2 3 2 4 5 2,4-Pentadien sp 3 2) Kumulierte
Auswahlverfahren Medizin Prüfungsgebiet Chemie. 6.Termin Organische Chemie Naturstoffe
 Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Studiengang Bsc Biowissenschaften. Modul-begleitende Prüfung. Organische Chemie
 Studiengang Bsc Biowissenschaften Modul-begleitende Prüfung Organische Chemie 26.07.2016 Name: Vorname: Matrikelnummer: Geboren am: in: Wiederholer/in dieser Klausur: Ja Nein Dauer der Klausur: 90 Minuten
Studiengang Bsc Biowissenschaften Modul-begleitende Prüfung Organische Chemie 26.07.2016 Name: Vorname: Matrikelnummer: Geboren am: in: Wiederholer/in dieser Klausur: Ja Nein Dauer der Klausur: 90 Minuten
1. Klausur zur Vorlesung. Einführung in die organische Chemie WS 03/04 11.12.2003
 1. Klausur zur Vorlesung Einführung in die organische Chemie WS 03/04 11.12.2003 Vorname (bitte deutlich schreiben): Nachname (bitte deutlich schreiben): Matrikelnummer: Studiengang: o Chemie (Diplom)
1. Klausur zur Vorlesung Einführung in die organische Chemie WS 03/04 11.12.2003 Vorname (bitte deutlich schreiben): Nachname (bitte deutlich schreiben): Matrikelnummer: Studiengang: o Chemie (Diplom)
Übungsbeispiele Kapitel Organische Verbindungen
 Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
1. Vorlesungsblock: Die chemische Struktur Organischer Verbindungen
 1. Vorlesungsblock: Die chemische Struktur Organischer Verbindungen Lernziele Am Ende des 1. Vorlesungsblocks sollten Sie: definieren können, was Organische Chemie ist, Ihre Kenntnisse vom Aufbau der Atome
1. Vorlesungsblock: Die chemische Struktur Organischer Verbindungen Lernziele Am Ende des 1. Vorlesungsblocks sollten Sie: definieren können, was Organische Chemie ist, Ihre Kenntnisse vom Aufbau der Atome
Lösungen zu Übung 22
 rganische hemie I Lösungen zu Übung 22 1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan
rganische hemie I Lösungen zu Übung 22 1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan
Landeshauptstadt Hannover
 Landeshauptstadt Hannover Schulbiologiezentrum 19.81 Stöchiometrie zum Anfassen Reaktionsgleichungen und Energiebilanzen mit Molekülmodellen begreifbar machen November 2015 Herausgeber: Landeshauptstadt
Landeshauptstadt Hannover Schulbiologiezentrum 19.81 Stöchiometrie zum Anfassen Reaktionsgleichungen und Energiebilanzen mit Molekülmodellen begreifbar machen November 2015 Herausgeber: Landeshauptstadt
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 07.07.09
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Nachschreibklausur zum 2. Praktikumsteil (OC) vom 07.07.09
Charakterisierung chiraler Moleküle
 Teil 6 Charakterisierung chiraler Moleküle Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Chiralität ein kurzer Reminder Cahn-Ingold-Prelog-Regeln (CIP) Zuordnung
Teil 6 Charakterisierung chiraler Moleküle Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Chiralität ein kurzer Reminder Cahn-Ingold-Prelog-Regeln (CIP) Zuordnung
3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen.
 Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene
Tuesday, January 30, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 3. Organische Reaktionen - Einordung nach Mechanismen. Alkene : Kohlenwasserstoffe mit Doppelbindungen. 3.1 Die Nomenklatur der Alkene
Harold Hart. Organische Chemie. Ein kurzes Lehrbuch. übersetzt und ergänzt von Jochen Lehmann
 Harold Hart Organische Chemie Ein kurzes Lehrbuch übersetzt und ergänzt von Jochen Lehmann Inhalt Einführung 1 1 Chemische Bindung und Isomerie 5 1.1 Wie Elektronen in Atomen angeordnet sind 5 1.2 Ionische
Harold Hart Organische Chemie Ein kurzes Lehrbuch übersetzt und ergänzt von Jochen Lehmann Inhalt Einführung 1 1 Chemische Bindung und Isomerie 5 1.1 Wie Elektronen in Atomen angeordnet sind 5 1.2 Ionische
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel )
 EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
EXKURS: Ligandenfeld-Theorie (bitte lesen: Riedel 5.4.6.1-3) 1 1. Definition eines Komplexes (A. Werner ca. 1900): Ein Komplex ist eine Koordinationsverbindung, in der das Zentralatom (eine Lewis-Säure)
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Säuren und Basen Säure-Base-Konzepte Säure-Base-Gleichgewichte Säurestärke, Basenstärke ph-, poh-, pk-werte Pufferlösungen Titrationen 1 Säure-Base-Definition nach ARRHENIUS
Praktikumsrelevante Themen Säuren und Basen Säure-Base-Konzepte Säure-Base-Gleichgewichte Säurestärke, Basenstärke ph-, poh-, pk-werte Pufferlösungen Titrationen 1 Säure-Base-Definition nach ARRHENIUS
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
