Schulversuchspraktikum. Friederike Kellner. Sommersemester Klassenstufen 11 & 12. Alkanone
|
|
|
- Sylvia Becke
- vor 6 Jahren
- Abrufe
Transkript
1 Schulversuchspraktikum Friederike Kellner Sommersemester 2014 Klassenstufen 11 & 12 Alkanone
2 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Die im Folgenden vorgestellte Unterrichtseinheit zum Thema Alkanone enthält zwei Lehrer- und drei Schülerversuche. Alle Versuche werden mit Aceton, dem bekanntesten Vertreter der Alkanone durchgeführt. In V1 und V5 wird Aceton synthetisiert, bei V1 aus Isopropanol, bei V5 aus Calciumacetat. In V2 wird ein Nachweis für Ketone vorgestellt und V3 und V4 befassen sich mit Eigenschaften von Aceton als Lösungsmittel. Inhalt 1 Beschreibung des Themas und zugehörige Lernziele Lehrerversuche V 1 Darstellung von Aceton aus Propan-2-ol V 2 Nachweis von Ketonen Schülerversuche V 3 Ein hungriges Lösungsmittel V 4 Der Aussalzeffekt V 5 Darstellung von Aceton aus Calciumacetat Didaktischer Kommentar des Arbeitsblattes Erwartungshorizont (Kerncurriculum) Erwartungshorizont (Inhaltlich)... 12
3 1 Beschreibung des Themas und zugehörige Lernziele 2 1 Beschreibung des Themas und zugehörige Lernziele Die Stoffklasse der Alkanone, auch Ketone genannt, ist den Schülerinnen und Schülern (im Folgenden als SuS bezeichnet) wahrscheinlich durch den am meisten verwendeten Vertreter dieser Gruppe, das Aceton, bereits aus dem Alltag bekannt. Im Kernkurriculum für die Oberstufe werden die Alkanone innerhalb des Basiskonzepts Stoff- Teilchen gefordert. Die SuS sollen die Molekülstruktur und die funktionellen Gruppen von verschiedenen Stoffklassen, darunter die Alkanone beschreiben (Fachwissen) und die IUPAC- Nomenklatur zur Benennung organischer Verbindungen anwenden (Erkenntnisgewinnung). Die Unterrichtseinheit zu den Alkanonen kann mit einer Einheit zu den Alkanalen (Aldehyden) verbunden werden, da diese auch im Kernkuriculum gefordert werden und aufgrund einer bestehenden Verwandtschaft. Alkanone entstehen aus der Oxidation sekundärer Alkohole, Alkanale aus der Oxidation primärer Alkohole. Dementsprechend enthalten beide Stoffklassen eine Carbonylgruppe, wobei diese bei den Alkanalen endständig ist, bei den Alkanonen jedoch nicht. In dieser Unterrichtseinheit zu den Alkanonen finden sich fünf Versuche, darunter zwei Lehrerund drei Schülerversuche. Im ersten Lehrerversuch V1 Darstellung von Aceton aus Isopropanol geht es um die Synthese von Aceton aus Isopropanol. In V2 Nachweis von Ketonen geht es um eine Möglichkeit Ketone einfach im Reagenzglas durch das Ausfallen eines Niederschlags nachzuweisen. In V3 Ein hungriges Lösungsmittel wird Polystyrol in Aceton gelöst und in V4 Der Aussalzeffekt wird Aceton aus einer Aceton-Wasser-Lösung durch Zugabe von Salz abgetrennt. In V5 Darstellung von Aceton aus Calciumacetat wird eine Alternative zu V1 für die Herstellung von Aceton vorgestellt. 2 Lehrerversuche 2.1 V 1 Darstellung von Aceton aus Propan-2-ol In diesem Versuch soll Aceton aus Propan-2-ol (Isopropanol) synthetisiert werden. Die SuS sollten mit den Molekülstrukturen von sekundären Alkoholen und Ketonen vertraut sein. Gefahrenstoffe Propan-2-ol H: P:
4 2 Lehrerversuche 3 Materialien: ml Bechergläser, schwer schmelzbares Glasrohr, Liebigkühler, 2 Reagenzgläser mit seitlichem Ansatz, gewinkeltes Glasrohr, kurze gebogene Glasrohre, durchbohrte Stopfen, Schlauchverbindungen, Bunsenbrenner, Wasserstrahlpumpe Chemikalien: Durchführung: Propan-2-ol, Kupfernetz Der Versuch wird wie in Abbildung 1 gezeigt aufgebaut. In das linke Reagenzglas werden 20 ml Propan-2-ol gegeben, dabei muss darauf geachtet werden, dass das rechtwinklige Rohr zum Belüften in die Flüssigkeit eintaucht. Das Reagenzglas wird in ein Becherglas mit warmem Wasser gestellt. Von dem Reagenzglas führt ein Schlauch zu der Glasröhre mit dem Kupfernetz. Von dieser geht wiederum ein Schlauch zum Liebigkühler und dieser endet am zweiten Reagenzglas, welches in einem Becherglas mit kaltem Wasser und Eis steht. Das zweite Reagenzglas ist an die Wasserstrahlpumpe angeschlossen. Nun wird der Wasserhahn der Wasserstrahlpumpe aufgedreht und das Kupfernetz wird stark erhitzt, bis es rot glüht. Durch das Ansaugen der Wasserstrahlpumpe wird das Propan-2-ol im ersten Reagenzglas mit Luft durchströmt. Dies wird durch die Blasen im ersten Reagenzglas sichtbar. Sollten diese nicht vorhanden sein, muss die Wasserstrahlpumpe stärker aufgedreht werden. Ein weiteres Reagenzglas wird mit etwa der gleichen Menge an Aceton gefüllt wie das Reagenzglas mit dem Reaktionsprodukt. Beobachtung: Im zweiten Reagenzglas sammelt sich eine klare Flüssigkeit an. Der Geruch des Reaktionsprodukts wird mit der Referenzprobe verglichen. Abb. 1-2 links Versuchsaufbau, rechts Reaktionsprodukt.
5 2 Lehrerversuche 4 Deutung: Bei der klaren Flüssigkeit handelt es sich um Aceton, welches gemäß folgender Reaktionsgleichung synthetisiert worden ist: Entsorgung: Literatur: Produkte und Edukte werden im Behälter für organische Lösungsmittel entsorgt. [1] W. Glöckner, W. Jansen, Handbuch der experimentellen Chemie Sekundarbereich II Band 10, Aulis, 2008, S. 120 ff. Der Versuch kann auch von SuS durchgeführt werden, ist im Aufbau allerdings sehr aufwendig. Das Reaktionsprodukt kann im folgenden Versuch V2 verwendet werden und es kann so überprüft werden, ob wirklich Aceton synthetisiert wurde. 2.2 V 2 Nachweis von Ketonen Dieser Versuch eignet sich, um Ketone nachzuweisen. Mit diesem Versuch kann das Reaktionsprodukt aus V1 getestet werden. Die Schüler benötigen kein spezielles Vorwissen. Gefahrenstoffe 2,4-Dinitrophenylhydrazin H: P: Konz. Salzsäure H: P: Materialien: Chemikalien: Durchführung: Erlenmeyerkolben 150 ml, Stopfen, Reagenzglas 2,4-Dinitrophenylhydrazin, konzentrierte Salzsäure, Wasser, Keton Zu 0,2 g des 2,4-Dinitrophenylhydrazins werden 5 ml konzentrierte Salzsäure und 100 ml Wasser dazugegeben. Der Erlenmeyerkolben wird kräftig geschüttelt. Dann wird ein Reagenzglas ungefähr zu einem Drittel mit der Lösung gefüllt und die auf Ketone zu untersuchende Probe (1-2 ml) dazugegeben.
6 2 Lehrerversuche 5 Beobachtung: Die Lösung verfärbt sich zu einem satten Gelb und es fällt ein gelber Niederschlag aus. Abb. 3 links Nachweisreagenz, rechts positiver Nachweis. Deutung: Unter sauren Bedingungen fällt 2,4-Dinitrophenylhydrazon aus. Der Nachweis ist positiv, die untersuchte Probe enthält Ketone. Entsorgung: Literatur: 2,4-Dinitrophenylhydrazin am besten gesondert im dafür vorgesehenen Behälter entsorgen, alternativ im Behälter für organische Feststoffe bzw. organische Lösungsmittel. [2] H. Keune, M. Just, Chemische Schulexperimente Band 2 Organische Chemie, Cornelsen Volk und Wissen, 2009, S Dieser Versuch darf nicht von den SuS durchgeführt werden, da diese nicht mit 2,4- Dinitrophenylhydrazin arbeiten dürfen. 2,4-Dinitrophenylhydrazin ist explosiv!
7 3 Schülerversuche 6 3 Schülerversuche 3.1 V 3 Ein hungriges Lösungsmittel Dieser Versuch eignet sich wegen seiner hohen Effektstärke gut als Showversuch, kann an dieser Stelle aber auch zur Thematisierung der Eigenschaften von Alkanonen als Lösungsmittel genutzt werden. Spezielles Vorwissen wird nicht benötigt. Gefahrenstoffe Aceton H: P: Materialien: Chemikalien: Durchführung: Beobachtung: Becherglas 250 ml, Tiegelzange, Polystyrol (Styropor) Aceton 10 ml Aceton werden in das Becherglas gegeben, dann wird darin das Styropor gelöst. Es können mehrere große Stücke Styropor gelöst werden, ungefähr 10 g. Das Styropor löst sich unter leichtem Zischen schnell in Aceton. Abb. 4 Auflösen von Styropor in Aceton. Deutung: Entsorgung: Polystyrol hat eine sehr geringe Dichte, weshalb sich große Mengen in Aceton lösen lassen. Es handelt sich bei Polystyrol um einen Duroplasten. Die flüssige Phase in den Sammelbehälter für organische Lösungsmittel geben, die feste Phase in den organischen Feststoffbehälter.
8 3 Schülerversuche 7 Literatur: [3] H. Schmidkunz, Chemische Freihandversuche Band 2, Aulis, 2011, S Alternativ kann ein Stück Styropor auch mit Aceton beträufelt werden. Hierbei frisst sich das Aceton von oben durch das Styropor. Abb. 5 Beträufeln von Styropor mit Aceton 3.2 V 4 Der Aussalzeffekt Dieser Versuch befasst sich mit der Polarität von Aceton. Die SuS sollten wissen, dass Wasser ein polares Lösungsmittel ist. Gefahrenstoffe Aceton H: P: Materialien: Chemikalien: Durchführung: Standzylinder (50 ml) oder Reagenzglas, Löffel, Glasstab Aceton, Natriumchlorid In den Standzylinder werden 10 ml Wasser gegeben (bzw. 4 cm hoch in das Reagenzglas) und die gleiche Menge an Aceton. Nun wird umgerührt bis nur noch eine Phase vorliegt. Anschließend wird ein Löffel voll (ca. 2-3 g) Natriumchlorid dazugegeben und erneut umgerührt.
9 3 Schülerversuche 8 Beobachtung: Wasser und Aceton lösen sich ineinander, es entsteht eine klare Lösung. Beim Zugeben des Salzes kommt es zu einer Entmischung und es bilden sich zwei Phasen. Abb. 6 - Aceton-Wasser nach der Zugabe von Salz (das Wasser wurde mit Tinte eingefärbt). Deutung: Entsorgung: Die wässrige Phase ist die untere und die obere ist das Aceton. Das Aussalzen einer organischen Substanz aus einer wässrigen Lösung beruht auf der Zunahme der Polarität des Systems. Aceton und Wasser haben eine ähnliche Polarität, durch die Zugabe von Salz, welches sich in Wasser löst, in Aceton aber nicht, erhöht sich die Polarität des Wassers und die des Acetons bleibt gleich. Dadurch kommt es zu einer Entmischung der Phasen. Das Aceton wird abgetrennt und im Behälter für organische Lösungsmittel entsorgt, das Wasser kann in das Abwasser gegeben werden. Literatur: [4] H. Schmidkunz, Chemische Freihandversuche Band 2, Aulis, 2011, S Es können noch weitere Versuche zur Löslichkeit von Aceton in verschiedenen Lösungsmitteln durchgeführt werden um den unpolaren Charakter des Acetons hervorzuheben. 3.3 V 5 Darstellung von Aceton aus Calciumacetat Dieser Versuch stellt eine Alternative zu V1 dar. Die SuS sollten mit dem klassischen Reaktionsweg für die Herstellung von Aceton aus einem sekundären Alkohol vertraut sein.
10 3 Schülerversuche 9 Gefahrenstoffe Aceton H: P: Materialien: Chemikalien: Durchführung: Beobachtung: 400 ml Becherglas, schwer schmelzbares Reagenzglas, Reagenzglas, durchbohrter Stopfen, rechtwinklig gebogenes Glasrohr, Bunsenbrenner Calciumacetat Mono-Hydrat 1 g Calciumacetat Mono-Hydrat wird in das schwer schmelzbare Reagenzglas gegeben und mit dem durchbohrten Stopfen verschlossen. Das rechtwinklige Glasrohr wird auf der einen Seite durch den Stopfen gesteckt und auf der anderen in das zweite Reagenzglas. Dieses Reagenzglas steht in dem mit Wasser und Eis befüllten Becherglas. Das Calciumacetat Mono- Hydrat wird mit dem Bunsenbrenner stark erhitzt. Im Verlauf der Reaktion beginnt das Calciumacetat Mono-Hydrat zu glühen und verfärbt sich schwarz-grau. Ein Gas entsteht und kondensiert im zweiten Reagenzglas zu einer leicht gelben Flüssigkeit. Abb. 7-8 links: Versuchsaufbau, rechts: Reaktionsprodukt. Deutung: Bei der entstandenen Flüssigkeit handelt es sich um Aceton. Das Aceton wurde gemäß folgender Reaktionsgleichung synthetisiert: Entsorgung: Edukt- und Produktreste werden in den Behälter für organische Lösungsmittel gegeben.
11 3 Schülerversuche 10 Literatur: [5] W. Glöckner, W. Jansen, Handbuch der experimentellen Chemie Sekundarbereich II Band 10, Aulis, 2008, S. 119f. Das Reagenzglas mit dem Calciumacetat lässt sich durch das entstandene Calciumcarbonat nach der Reaktion nicht mehr vollständig reinigen. Dieser Versuch stellt eine Alternative zu V1 dar und zeigt einen alternativen Syntheseweg für die Herstellung von Aceton auf. Auch ist dieser Versuch im Vergleich zu V1 deutlich schneller durchführbar.
12 Arbeitsblatt Lösungsverhalten von Aceton 1. Geben Sie die Strukturformel von Aceton an und kennzeichnen Sie die funktionelle Gruppe und benennen Sie diese. 2. Überprüfen Sie das Lösungsverhalten von Aceton in verschiedenen Lösungsmitteln: nehmen Sie dafür 3 Reagenzgläser und füllen Sie alle mit 2 ml Aceton. Geben Sie nun 2 ml Wasser in das erste Reagenzglas, 2 ml Ethanol in das zweite Reagenzglas und 2 ml Heptan in das dritte Reagenzglas. Befüllen Sie ein viertes Reagenzglas mit je 2 ml Wasser und Ethanol. Deuten Sie ihre Beobachtungen. 3. Lesen Sie sich nun die Versuchsbeschreibung zu V4 Der Aussalzeffekt durch. a) Stellen Sie Hypothesen auf, was geschehen wird. b) Führen Sie den Versuch durch und überprüfen Sie Ihre Hypothesen. c) Sie können den Versuch auch mit den Lösungen aus Aufgabe 1 ausprobieren. Was stellen Sie hierbei fest? Was für eine Erklärung gibt es hierfür? d) Ziehen Sie Rückschlüsse auf das Löseverhalten von Aceton.
13 4 Didaktischer Kommentar des Arbeitsblattes 12 4 Didaktischer Kommentar des Arbeitsblattes Das Arbeitsblatt befasst sich mit dem Lösungsverhalten von Aceton. Es kann in Zusammenhang mit Versuch V4 Der Aussalzeffekt im Unterricht eingesetzt werden. Die SuS sollen ein Verständnis dafür erlangen, warum Aceton ein wichtiges Lösungsmittel ist und welche Eigenschaften es hat. Auch sollen sie Rückschlüsse auf andere organische Lösungsmittel ziehen. 4.1 Erwartungshorizont (Kerncurriculum) Im Kernkurriculum für die Oberstufe werden die Alkanone innerhalb des Basiskonzepts Stoff- Teilchen gefordert. Die SuS sollen die Molekülstruktur und die funktionellen Gruppen von verschiedenen Stoffklassen, darunter die Alkanone beschreiben (Fachwissen). Außerdem sollen die SuS geeignete Anschauungsmodelle zur Visualisierung der Struktur von Verbindungen nutzen (Erkenntnisgewinnung) und die Fach- und Alltagssprache voneinander abgrenzen (Kommunikation). Das Arbeitsblatt deckt die drei im Kernkurriculum geforderten Anforderungsbereiche (Faktenwissen, Anwendung und Transfer) ab. In Aufgabe 1 wird Faktenwissen gefordert, in Aufgabe 2 steht die Anwendung im Vordergrund und in Aufgabe 3 geht es um die Anwendung von Wissen und um den Transfer von Konzepten. 4.2 Erwartungshorizont (Inhaltlich) 1. Die funktionelle Gruppe ist eingekreist. Es handelt sich um eine Carbonyl-Gruppe. 2. Aceton löst sich komplett in allen drei Lösungsmitteln. Ethanol löst sich auch in Wasser. Lösungsmittel mit ähnlicher Polarität lösen sich ineinander. 3.a) An dieser Stelle gibt es keine richtigen oder falschen Antworten. Mögliche Schülerantworten könnten sein: I) Bei dem Aceton-Wasser-Gemisch verändert sich durch die Zugabe von Salz nichts. II) Durch die Zugabe von Salz trennt sich das Gemisch in Aceton und Wasser, das Salz ist in beiden Phasen gelöst. III) Es kommt zu einer Trennung, das Salz ist nur in der wässrigen Phase gelöst.
14 4 Didaktischer Kommentar des Arbeitsblattes 12 b) Die Hypothesen werden bestätigt oder falsifiziert. Hypothese III) bestätigt sich, dass das Salz nur in der wässrigen Phase gelöst ist. c) Bei den Lösungen ohne Wasser kommt es zu keiner Entmischung der Phasen. Die Ethanol- Wasser-Lösung verhält sich analog zur Aceton-Wasser-Lösung. d) Aceton ist sowohl in wässrigen als auch in organischen Lösungsmitteln lösbar. Wenn die Polarität der wässrigen Phase allerdings steigt, wie dies durch die Zugabe von Salzen geschieht, kommt es zu einer Trennung des Gemisches und es bilden sich zwei Phasen.
Dichte und Nachweis von Kohlenstoffdioxid
 Schulversuchspraktikum Name: Lydia Reinhardt Semester: Sommersemester 2014 Klassenstufen 7 & 8 Dichte und Nachweis von Kohlenstoffdioxid 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Name: Lydia Reinhardt Semester: Sommersemester 2014 Klassenstufen 7 & 8 Dichte und Nachweis von Kohlenstoffdioxid 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum. Name Thomas Polle. Sommersemester Klassenstufen 5 & 6. Feuer und Kerzen
 Schulversuchspraktikum Name Thomas Polle Sommersemester 2015 Klassenstufen 5 & 6 Feuer und Kerzen 2 Auf einen Blick: Es werden je ein Schüler- und Lehrerversuch zum Thema Kerzen und Feuer für den 5. und
Schulversuchspraktikum Name Thomas Polle Sommersemester 2015 Klassenstufen 5 & 6 Feuer und Kerzen 2 Auf einen Blick: Es werden je ein Schüler- und Lehrerversuch zum Thema Kerzen und Feuer für den 5. und
Schulversuchspraktikum. Constanze Koch. Sommersemester Klassenstufen 5 & 6. Wasser als Lösungsmittel. Kurzprotokoll
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Fluoreszierende Verbindungen
 Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Thema: Fluoreszierende Verbindungen Klasse 11 / 12 Schulversuchspraktikum Bastian Hollemann Sommersemester 2015 Klassenstufen 11 & 12 Fluoreszierende Verbindungen Thema: Fluoreszierende Verbindungen Klasse
Merkmale einer chemischen Reaktion
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale einer chemischen Reaktion 1 Auf Beschreibung einen Blick: des Themas und zugehörige Lernziele Im Folgenden werden
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale einer chemischen Reaktion 1 Auf Beschreibung einen Blick: des Themas und zugehörige Lernziele Im Folgenden werden
Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser?
 http://www.kostenloseausmalbilder.de/media/.gallery/main606.jpg (02.08.2015) Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser? Pip, die kleine Maus, benötigt zum Atmen Luft, vor allem den Sauerstoff,
http://www.kostenloseausmalbilder.de/media/.gallery/main606.jpg (02.08.2015) Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser? Pip, die kleine Maus, benötigt zum Atmen Luft, vor allem den Sauerstoff,
Schulversuchspraktikum. Isabel Böselt. Sommersemester Klassenstufen 5 & 6. Aggregatzustände. und deren Temperaturabhängigkeit
 Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden einfache
Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden einfache
Vom Alkohol zum Alken
 1 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufe 9 & 10 Vom Alkohol zum Alken 2 Auf einem Blick: Diese Unterrichtseinheit für die Klasse 9 & 10 enthält Lehrerversuche und 1 Schülerversuch
1 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufe 9 & 10 Vom Alkohol zum Alken 2 Auf einem Blick: Diese Unterrichtseinheit für die Klasse 9 & 10 enthält Lehrerversuche und 1 Schülerversuch
Warum korrodiert Eisen?
 Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Schulversuchspraktikum. Dirk Schlemme. Sommersemester Klassenstufen 11 & 12. Alkanone
 Schulversuchspraktikum Dirk Schlemme Sommersemester 2012 Klassenstufen 11 & 12 Alkanone 1 Konzept und Ziele 1 Auf einen Blick: Die Alkanone spielen im alltäglichen Leben nur noch eine untergeordnete Rolle.
Schulversuchspraktikum Dirk Schlemme Sommersemester 2012 Klassenstufen 11 & 12 Alkanone 1 Konzept und Ziele 1 Auf einen Blick: Die Alkanone spielen im alltäglichen Leben nur noch eine untergeordnete Rolle.
Schulversuchspraktikum. Name: Jennifer Kölling. Sommersemester: Klassenstufen: 9/10. Salze
 Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 9/10 Salze 1 Schulversuchspraktikum 1 Auf einen Blick:. Die Thematik der Salze ist sehr umfangreich. Die hier dargestellten
Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 9/10 Salze 1 Schulversuchspraktikum 1 Auf einen Blick:. Die Thematik der Salze ist sehr umfangreich. Die hier dargestellten
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer
 Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer chemischen Reaktion? In der letzten Chemiestunde hast du eine Hypothese zu der Frage formuliert: Verändert sich die Masse von
Arbeitsblatt Verändert sich die Masse von Edukten und Produkten während einer chemischen Reaktion? In der letzten Chemiestunde hast du eine Hypothese zu der Frage formuliert: Verändert sich die Masse von
Schulversuchspraktikum. Name: Jennifer Ahrens. Semester: Sommersemester Klassenstufen 9 & 10. Alkalimetalle
 Schulversuchspraktikum Name: Jennifer Ahrens Semester: Sommersemester 2012 Klassenstufen 9 & 10 Alkalimetalle Auf einen Blick: In dieser Unterrichtseinheit werden Versuche zu den Alkalimetallen der ersten
Schulversuchspraktikum Name: Jennifer Ahrens Semester: Sommersemester 2012 Klassenstufen 9 & 10 Alkalimetalle Auf einen Blick: In dieser Unterrichtseinheit werden Versuche zu den Alkalimetallen der ersten
Licht und Farben. Kurzprotokoll
 Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Schulversuchspraktikum. Sommersemester 2014 Klassenstufen 7 & 8. Reaktionen von Metallen mit Sauerstoff und mit Luft.
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Aggregatzustände und deren Temperaturabhängigkeit
 Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Erweiterter Redoxbegriff
 Schulversuchspraktikum Friederike Kellner Sommersemester 2014 Klassenstufen 7 & 8 Erweiterter Redoxbegriff 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Die im Folgenden vorgestellte
Schulversuchspraktikum Friederike Kellner Sommersemester 2014 Klassenstufen 7 & 8 Erweiterter Redoxbegriff 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Die im Folgenden vorgestellte
Reaktionen von Metallen mit Sauerstoff und mit Luft
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10. Die Brennstoffzelle
 Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10 Die Brennstoffzelle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 9 & 10 Die Brennstoffzelle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum. Alexander König. Sommersemester Klassenstufen 11 & 12. Katalysatoren
 Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 11 & 12 Katalysatoren Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält einen Schülerversuch und einen
Schulversuchspraktikum Alexander König Sommersemester 2015 Klassenstufen 11 & 12 Katalysatoren Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält einen Schülerversuch und einen
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll
Wir untersuchen Mineralwasser
 Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad
 Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele
Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele
Schulversuchspraktikum. Johanna Osterloh. Sommersemester Klassenstufen 9 & 10. Stoffkreisläufe. Kurzprotokoll
 Schulversuchspraktikum Johanna Osterloh Sommersemester 2015 Klassenstufen 9 & 10 Stoffkreisläufe Kurzprotokoll Auf einen Blick: Dieses Protokoll enthält vier Schülerversuche, die zum Thema Kohlenstoffdioxidkreislauf
Schulversuchspraktikum Johanna Osterloh Sommersemester 2015 Klassenstufen 9 & 10 Stoffkreisläufe Kurzprotokoll Auf einen Blick: Dieses Protokoll enthält vier Schülerversuche, die zum Thema Kohlenstoffdioxidkreislauf
Haushaltsreiniger und Waschmittel
 Schulversuchspraktikum Name: Tobias Piotrowski Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Haushaltsreiniger und Waschmittel 3 Schülerversuche 2 Auf einen Blick: Dieses Protokoll befasst sich mit
Schulversuchspraktikum Name: Tobias Piotrowski Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Haushaltsreiniger und Waschmittel 3 Schülerversuche 2 Auf einen Blick: Dieses Protokoll befasst sich mit
1 Lehrerversuch Alkalimetalle in Wasser
 1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
Homogene und Heterogene Gemische
 Schulversuchspraktikum Name Nicolai ter Horst Semester SS 2013 Klassenstufen 7 & 8 Homogene und Heterogene Gemische 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum Name Nicolai ter Horst Semester SS 2013 Klassenstufen 7 & 8 Homogene und Heterogene Gemische 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll
Vom Alkohol zum Alken
 Schulversuchspraktikum Sabine Wolff SoSe 2013 Klassenstufen 9 & 10 Vom Alkohol zum Alken 2 Auf einen Blick: Im Folgenden werden zwei Lehrerversuche vorgestellt, die die Darstellung von gasförmigen Alkenen
Schulversuchspraktikum Sabine Wolff SoSe 2013 Klassenstufen 9 & 10 Vom Alkohol zum Alken 2 Auf einen Blick: Im Folgenden werden zwei Lehrerversuche vorgestellt, die die Darstellung von gasförmigen Alkenen
Schulversuchspraktikum. Sommersemester Klassenstufen 5 & 6. Feuer und Kerzen
 Schulversuchspraktikum Sommersemester 2013 Klassenstufen 5 & 6 Feuer und Kerzen Text zuzuweisen, der hier Fehler! Verwenden Sie 2 Auf einen Blick: In diesem Protokoll werden sechs Versuche dargestellt,
Schulversuchspraktikum Sommersemester 2013 Klassenstufen 5 & 6 Feuer und Kerzen Text zuzuweisen, der hier Fehler! Verwenden Sie 2 Auf einen Blick: In diesem Protokoll werden sechs Versuche dargestellt,
Schulversuchspraktikum. Name: Jennifer Kölling. Sommersemester: 2012. Klassenstufen: 11/12. Tenside
 Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 11/12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. Die Themeneinheit der Tenside in der
Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 11/12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. Die Themeneinheit der Tenside in der
Schulversuchspraktikum. Name: Jennifer Kölling. Sommersemester: Klassenstufen: 7/8. Sauerstoff. Das Gas des Lebens
 Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 7/8 Sauerstoff Das Gas des Lebens 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. Die Themeneinheit
Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 7/8 Sauerstoff Das Gas des Lebens 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. Die Themeneinheit
Reinstoffe und Stoffgemische
 Schulversuchspraktikum Dörte Hartje Sommersemester 2013 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Auf einen Blick: Dieses Versuchsprotokoll enthält zwei Lehrer- und vier SchülerInnenexperimente
Schulversuchspraktikum Dörte Hartje Sommersemester 2013 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Auf einen Blick: Dieses Versuchsprotokoll enthält zwei Lehrer- und vier SchülerInnenexperimente
Synthese, Analyse, Umsetzung
 Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 7&8 Synthese, Analyse, Umsetzung Auf einen Blick Die Thematik Synthese, Analyse und Umsetzung umfasst die Grundtypen chemischer Reaktionen.
Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 7&8 Synthese, Analyse, Umsetzung Auf einen Blick Die Thematik Synthese, Analyse und Umsetzung umfasst die Grundtypen chemischer Reaktionen.
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Sina Bachsmann Sommersemester 2014 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Im Folgenden
Schulversuchspraktikum Sina Bachsmann Sommersemester 2014 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Im Folgenden
Energie und Energieumwandlung
 Schulversuchspraktikum Maximilian Wolf Sommersemester Klassenstufen 7 & 8 Energie und Energieumwandlung Kurzprotokoll Auf einen Blick: In Versuch 1 werden Lycopodium-Sporen (Bärlapp) in der Gasbrennerflamme
Schulversuchspraktikum Maximilian Wolf Sommersemester Klassenstufen 7 & 8 Energie und Energieumwandlung Kurzprotokoll Auf einen Blick: In Versuch 1 werden Lycopodium-Sporen (Bärlapp) in der Gasbrennerflamme
Endotherm und Exotherm
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen Schülerversuch
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen Schülerversuch
Reinstoffe und Stoffgemische, Verfahren zur Stofftrennung
 Schulversuchspraktikum Name: Jana Pfefferle Semester: SoSe 2014 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische, Verfahren zur Stofftrennung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen
Schulversuchspraktikum Name: Jana Pfefferle Semester: SoSe 2014 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische, Verfahren zur Stofftrennung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen
Schulversuchspraktikum. Name: Jennifer Kölling. Sommersemester: Klassenstufen: 5/6. Die Luft. Das unsichtbare Gasgemisch
 Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 5/6 Die Luft Das unsichtbare Gasgemisch 1Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. In dieser
Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 5/6 Die Luft Das unsichtbare Gasgemisch 1Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. In dieser
Schulversuchspraktikum. Julia Müller. Eigenschaften gesättigter Kohlenwasserstoffe
 Schulversuchspraktikum Name: Julia Müller Semester: SoSe 2012 Klassenstufen: 9 und 10 Eigenschaften gesättigter Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Name: Julia Müller Semester: SoSe 2012 Klassenstufen: 9 und 10 Eigenschaften gesättigter Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum. Olga Streck. Sommersemester Klassenstufen 5 & 6. Papier
 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 5 & 6 Papier 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 enthält 2 Lehrerversuche und 2 Schülerversuche zum Thema
Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 5 & 6 Papier 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 enthält 2 Lehrerversuche und 2 Schülerversuche zum Thema
Metalle und Nichtmetalle
 Schulversuchspraktium Bastian Hollemann Sommersemester 2015 Klassenstufen 9 & 10 Metalle und Nichtmetalle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Diese Unterrichtseinheit für
Schulversuchspraktium Bastian Hollemann Sommersemester 2015 Klassenstufen 9 & 10 Metalle und Nichtmetalle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Diese Unterrichtseinheit für
Verbrennung von Eisenwolle und Holz
 Name: Datum: Versuch: Verbrennung von Eisenwolle und Holz Geräte: 1 Stativ 2 Muffen 2 Klemmen 1 Laborboy (hier Holzklotz) 1 Porzellanschale 1 Analysetrichter 1 Gaswaschflasche 1 Wasserstrahlpumpe 1 Gummischlauch
Name: Datum: Versuch: Verbrennung von Eisenwolle und Holz Geräte: 1 Stativ 2 Muffen 2 Klemmen 1 Laborboy (hier Holzklotz) 1 Porzellanschale 1 Analysetrichter 1 Gaswaschflasche 1 Wasserstrahlpumpe 1 Gummischlauch
Reaktion von Nichtmetallen mit Sauerstoff und mit Luft
 Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 7 & 8 Reaktion von Nichtmetallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 7 & 8 Reaktion von Nichtmetallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Temperaturabhängigkeit, Schmelz- und Siedetemperatur
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit, Schmelz- und Siedetemperatur Auf einen 1 Beschreibung Blick: des Themas
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit, Schmelz- und Siedetemperatur Auf einen 1 Beschreibung Blick: des Themas
Schulversuchspraktikum. Name: Tobias Piotrowski. Semester: Sommersemester 2013. Klassenstufen 9 & 10. ph-wert
 Schulversuchspraktikum Name: Tobias Piotrowski Semester: Sommersemester 2013 Klassenstufen 9 & 10 ph-wert 1 Beschreibung des Themas und zugehörige Lernziele (Max. 1 Seite) 2 Auf einen Blick: Dieses Protokoll
Schulversuchspraktikum Name: Tobias Piotrowski Semester: Sommersemester 2013 Klassenstufen 9 & 10 ph-wert 1 Beschreibung des Themas und zugehörige Lernziele (Max. 1 Seite) 2 Auf einen Blick: Dieses Protokoll
Säuren und Laugen im Haushalt
 Schulversuchspraktikum Maximilian Konrad Sommersemester 2012 Klassenstufen 9 & 10 Säuren und Laugen im Haushalt Auf einen Blick: Diese Unterrichtseinheit für die Klassen 9 und 10 enthält 2 Lehrerversuche,
Schulversuchspraktikum Maximilian Konrad Sommersemester 2012 Klassenstufen 9 & 10 Säuren und Laugen im Haushalt Auf einen Blick: Diese Unterrichtseinheit für die Klassen 9 und 10 enthält 2 Lehrerversuche,
Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Schwimmen, Schweben, Sinken
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 5 & 6 Schwimmen, Schweben, Sinken Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 beinhaltet einen Lehrer- und vier Schülerversuche.
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 5 & 6 Schwimmen, Schweben, Sinken Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 beinhaltet einen Lehrer- und vier Schülerversuche.
Erscheinungsformen und Eigenschaften des Wassers
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 5 & 6 Erscheinungsformen und Eigenschaften des Wassers Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 5 & 6 Erscheinungsformen und Eigenschaften des Wassers Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen
Schulversuchspraktikum. Sommersemester Klassenstufen 11 & 12. Chromatografie
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 11 & 12 Chromatografie Auf einen Blick: Das Protokoll beschäftigt sich mit dem Thema Chromatografie und insbesondere dem Auftrennen von Blattfarbstoffen.
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 11 & 12 Chromatografie Auf einen Blick: Das Protokoll beschäftigt sich mit dem Thema Chromatografie und insbesondere dem Auftrennen von Blattfarbstoffen.
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch und
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch und
Energie und Energiequellen
 Schulversuchspraktikum Friederike Kellner Sommersemester 2014 Klassenstufen 5 & 6 Energie und Energiequellen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Die im Folgenden vorgestellte
Schulversuchspraktikum Friederike Kellner Sommersemester 2014 Klassenstufen 5 & 6 Energie und Energiequellen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Die im Folgenden vorgestellte
Vom Alkohol zum Oxidationsprodukte der Alkohole
 Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Gruppe I : Darstellung und Nachweis von Säuren
 Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Schulversuchspraktikum. Name Lydia Reinhardt. Semester Sommersemester Klassenstufen 11 & 12. Tenside
 Schulversuchspraktikum Name Lydia Reinhardt Semester Sommersemester 2014 Klassenstufen 11 & 12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Diese Unterrichtseinheit zum
Schulversuchspraktikum Name Lydia Reinhardt Semester Sommersemester 2014 Klassenstufen 11 & 12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Diese Unterrichtseinheit zum
Vom Schwefel zur Schwefelsäure
 Schulversuchspraktikum Patricia Hiller Sommersemester 2015 Klassenstufen 9 & 10 Vom Schwefel zur Schwefelsäure 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll wird
Schulversuchspraktikum Patricia Hiller Sommersemester 2015 Klassenstufen 9 & 10 Vom Schwefel zur Schwefelsäure 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll wird
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Schulversuchspraktikum. Michaela Micke. Sommersemester Klassenstufen 9 & 10. Chemie der Kohlenwasserstoffe. Methan & Erdgas
 Schulversuchspraktikum Michaela Micke Sommersemester 2012 Klassenstufen 9 & 10 Chemie der Kohlenwasserstoffe Methan & Erdgas 1 Konzept und Ziele 1 Auf einen Blick: Die vorliegende Unterrichtseinheit für
Schulversuchspraktikum Michaela Micke Sommersemester 2012 Klassenstufen 9 & 10 Chemie der Kohlenwasserstoffe Methan & Erdgas 1 Konzept und Ziele 1 Auf einen Blick: Die vorliegende Unterrichtseinheit für
Schulversuchspraktikum. Denise Heckmann. Sommersemester Klassenstufen 7&8. Stickstoff
 Schulversuchspraktikum Denise Heckmann Sommersemester 2013 Klassenstufen 7&8 Stickstoff 1 Auf einen Blick: In diesem Protokoll wird das Element Stickstoff als Hauptbestandteil der Luft eingeführt. Hierzu
Schulversuchspraktikum Denise Heckmann Sommersemester 2013 Klassenstufen 7&8 Stickstoff 1 Auf einen Blick: In diesem Protokoll wird das Element Stickstoff als Hauptbestandteil der Luft eingeführt. Hierzu
Verfahren zur Stofftrennung
 Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Verfahren zur Stofftrennung Auf einen Blick: Dieses Protokoll enthält 3 Schülerversuche
Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Verfahren zur Stofftrennung Auf einen Blick: Dieses Protokoll enthält 3 Schülerversuche
Schulversuchspraktikum. Johanna Schakowske Sommersemester 2013 Klassenstufen 7 & 8. Aktivierungsenergie
 Schulversuchspraktikum Johanna Schakowske Sommersemester 2013 Klassenstufen 7 & 8 Aktivierungsenergie 1 Konzept und Ziele 1 Auf einen Blick: In diesem Protokoll sind SuS- uns LuL-Versuche aufgeführt, die
Schulversuchspraktikum Johanna Schakowske Sommersemester 2013 Klassenstufen 7 & 8 Aktivierungsenergie 1 Konzept und Ziele 1 Auf einen Blick: In diesem Protokoll sind SuS- uns LuL-Versuche aufgeführt, die
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
7. Studieneinheit. Siebte Studieneinheit
 86 Siebte Studieneinheit 7. Studieneinheit Lernziele Löslichkeit organisch-chemischer Substanzen unter verschiedenen Bedingungen Charakteristische Reaktionen ausgewählter organisch-chemischer Stoffklassen
86 Siebte Studieneinheit 7. Studieneinheit Lernziele Löslichkeit organisch-chemischer Substanzen unter verschiedenen Bedingungen Charakteristische Reaktionen ausgewählter organisch-chemischer Stoffklassen
Schulversuchspraktikum. Carl Föst. Sommersemester Klassenstufen 5 & 6. Einfache Messgeräte
 Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 5 & 6 Einfache Messgeräte 1 1 Auf einen Blick: In dieser Versuchsreihe geht es um den Bau von Messinstrumenten für Temperatur, Luftfeuchtigkeit
Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 5 & 6 Einfache Messgeräte 1 1 Auf einen Blick: In dieser Versuchsreihe geht es um den Bau von Messinstrumenten für Temperatur, Luftfeuchtigkeit
Schulversuchspraktikum. Maximilian Konrad. Sommersemester Klassenstufen 11 & 12. Kunststoffe
 Schulversuchspraktikum Maximilian Konrad Sommersemester 2012 Klassenstufen 11 & 12 Kunststoffe 1 Konzept und Ziele 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält 2 Lehrerversuche
Schulversuchspraktikum Maximilian Konrad Sommersemester 2012 Klassenstufen 11 & 12 Kunststoffe 1 Konzept und Ziele 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält 2 Lehrerversuche
Fluoreszierende organische Verbindungen
 Schulversuchspraktikum Moritz Pemberneck Sommersemester 2016 Klassenstufen 11, 12 und 13 Fluoreszierende organische Verbindungen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem
Schulversuchspraktikum Moritz Pemberneck Sommersemester 2016 Klassenstufen 11, 12 und 13 Fluoreszierende organische Verbindungen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem
Ungesättigte Kohlenwasserstoffe
 Schulversuchspraktikum Name: Stefan Krüger Semester: SoSe 2014 Klassenstufen: 11/12 Ungesättigte Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum Name: Stefan Krüger Semester: SoSe 2014 Klassenstufen: 11/12 Ungesättigte Kohlenwasserstoffe 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll
Arbeitsblatt Wasserkreislauf der Erde
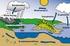 Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Teilchenmodell, Brown sche Molekularbewegung
 Schulversuchspraktikum Stefan Krüger SoSe 2014 Klassenstufen 7/8 Teilchenmodell, Brown sche Molekularbewegung und Diffusion 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses
Schulversuchspraktikum Stefan Krüger SoSe 2014 Klassenstufen 7/8 Teilchenmodell, Brown sche Molekularbewegung und Diffusion 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses
Mische einige Stoffe mit Wasser und untersuche die entstandenen Gemischarten.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
Schulversuchspraktikum. Isabel Böselt. Sommersemester Klassenstufen 9 & 10. Alkalimetalle
 Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 9 & 10 Alkalimetalle 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sollen Versuche zum
Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 9 & 10 Alkalimetalle 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sollen Versuche zum
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 5 & 6. Verfahren zur Stofftrennung
 Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 5 & 6 Verfahren zur Stofftrennung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 5 & 6 Verfahren zur Stofftrennung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind
Becherglas mit Wasser, 4 Reagenzgläser, Thermometer, Brenner. Proben von Schweineschmalz, Butter, Kokosfett, Sonnenblumenöl
 Station 1: Schmelztemperatur der Fette Becherglas mit Wasser, 4 Reagenzgläser, Thermometer, Brenner Proben von Schweineschmalz, Butter, Kokosfett, Sonnenblumenöl Geben Sie Proben verschiedener Fette in
Station 1: Schmelztemperatur der Fette Becherglas mit Wasser, 4 Reagenzgläser, Thermometer, Brenner Proben von Schweineschmalz, Butter, Kokosfett, Sonnenblumenöl Geben Sie Proben verschiedener Fette in
Reinstoffe und Stoffgemische
 Schulversuchspraktikum Name: Birte Zieske Sommersemester 2012 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische 4 Schülerversuche 7 Auf einen Blick: Das Protokoll umfasst 2 Lehrerversuche und 3 Schülerversuche,
Schulversuchspraktikum Name: Birte Zieske Sommersemester 2012 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische 4 Schülerversuche 7 Auf einen Blick: Das Protokoll umfasst 2 Lehrerversuche und 3 Schülerversuche,
Vitamine unter der chemischen Lupe Die Löslichkeitseigenschaft von Vitaminen im kompetenzorientierten Unterricht
 21. Vitamine unter der chemischen Lupe 1 von 14 Vitamine unter der chemischen Lupe Die Löslichkeitseigenschaft von Vitaminen im kompetenzorientierten Unterricht Sylvia Pross, Marburg Niveau: Sek. II Dauer:
21. Vitamine unter der chemischen Lupe 1 von 14 Vitamine unter der chemischen Lupe Die Löslichkeitseigenschaft von Vitaminen im kompetenzorientierten Unterricht Sylvia Pross, Marburg Niveau: Sek. II Dauer:
Schulversuchspraktikum. Michaela Micke. Sommersemester Klassenstufen 11 & 12. Chemie der Kohlenwasserstoffe. Ether & Ester
 Schulversuchspraktikum Michaela Micke Sommersemester 2012 Klassenstufen 11 & 12 Chemie der Kohlenwasserstoffe Ether & Ester Auf einen Blick: Die vorliegende Unterrichtseinheit für die Klassen 11 & 12 enthält
Schulversuchspraktikum Michaela Micke Sommersemester 2012 Klassenstufen 11 & 12 Chemie der Kohlenwasserstoffe Ether & Ester Auf einen Blick: Die vorliegende Unterrichtseinheit für die Klassen 11 & 12 enthält
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 11 & 12. Katalyse
 Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 11 & 12 Katalyse 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 11 & 12 Katalyse 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind drei Lehrerversuche
Schulversuchspraktikum. Anna Hille. Sommersemester Klassenstufen 7 & 8. Korrosion
 Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 7 & 8 Korrosion 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet Versuche zum Thema
Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 7 & 8 Korrosion 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll beinhaltet Versuche zum Thema
Versuche zum Thema Aminosäuren
 Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Versuche zum Thema Aminosäuren und Proteine 1/5 Versuche zum Thema Aminosäuren ❶ ph-abhängigkeit der Löslichkeit von Tyrosin 1) In zwei Reagenzgläser gibt man je eine Spatelspitze Tyrosin und etwa 2 cm
Qualitative Nachweise von Säuren und Basen
 Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 9 & 10 Qualitative Nachweise von Säuren und Basen Auf einen Blick: Dieses Protokoll beinhaltet 3 Lehrerversuche und 2 Schülerversuche
Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 9 & 10 Qualitative Nachweise von Säuren und Basen Auf einen Blick: Dieses Protokoll beinhaltet 3 Lehrerversuche und 2 Schülerversuche
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure
 Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Reaktion von Nichtmetallen mit Sauerstoff
 Schulversuchspraktikum Name: Benjamin Heuer Semester: SS2013 Klassenstufen 7&8 Reaktion von Nichtmetallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Name: Benjamin Heuer Semester: SS2013 Klassenstufen 7&8 Reaktion von Nichtmetallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum. SoSe 2013. Klassenstufen 7 & 8. Dichte
 Schulversuchspraktikum SoSe 2013 Klassenstufen 7 & 8 Dichte 2 Auf einen Blick: Im Folgenden werden zwei Lehrerversuche und vier Schülerversuche vorgestellt, die sich mit der Dichte von Gasen und Flüssigkeiten,
Schulversuchspraktikum SoSe 2013 Klassenstufen 7 & 8 Dichte 2 Auf einen Blick: Im Folgenden werden zwei Lehrerversuche und vier Schülerversuche vorgestellt, die sich mit der Dichte von Gasen und Flüssigkeiten,
Nährstoffe und Nahrungsmittel
 Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel 1 Lernziele 1 Auf einen Blick: Ein Lehrerversuch und fünf Schülerversuche vermitteln SuS
Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel 1 Lernziele 1 Auf einen Blick: Ein Lehrerversuch und fünf Schülerversuche vermitteln SuS
Säuren und Basen im Haushalt
 Schulversuchspraktikum Lars Lichtenberg Sommersemester 2015 Klassenstufen 9 & 10 Säuren und Basen im Haushalt 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die Unterrichtseinheit,,Säuren
Schulversuchspraktikum Lars Lichtenberg Sommersemester 2015 Klassenstufen 9 & 10 Säuren und Basen im Haushalt 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die Unterrichtseinheit,,Säuren
2.1 Eigenschaften von Stoffgemischen. Aufgabe. Welche Eigenschaften haben Stoffgemische?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750600) 2. Eigenschaften von Stoffgemischen Experiment von: Phywe Gedruckt:.0.203 2:49:48 intertess (Version 3.06 B200, Export 2000)
Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750600) 2. Eigenschaften von Stoffgemischen Experiment von: Phywe Gedruckt:.0.203 2:49:48 intertess (Version 3.06 B200, Export 2000)
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Schulversuchspraktikum. Sina Bachsmann. Sommersemester. Klassenstufen 11 &12. Kosmetikartikel
 Schulversuchspraktikum Sina Bachsmann Sommersemester Klassenstufen 11 &12 Kosmetikartikel 1 Lehrerversuche 1 Auf einen Blick: Dieses Protokoll enthält einen Lehrerversuch und vier Schülerversuche zum Thema
Schulversuchspraktikum Sina Bachsmann Sommersemester Klassenstufen 11 &12 Kosmetikartikel 1 Lehrerversuche 1 Auf einen Blick: Dieses Protokoll enthält einen Lehrerversuch und vier Schülerversuche zum Thema
Fette, Öle und Tenside
 Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside 2 Auf einen Blick: Es werden zwei Versuche zum Thema Fette vorgestellt, welche aufeinander aufgebaut
Schulversuchspraktikum Thomas Polle Sommersemester 2015 Klassenstufen 11 & 12 Fette, Öle und Tenside 2 Auf einen Blick: Es werden zwei Versuche zum Thema Fette vorgestellt, welche aufeinander aufgebaut
Versuchsprotokoll: Fehling- Spaltung von Saccharose
 Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Schulversuchspraktikum. Sommersemester 2014 Klassenstufen 9 & 10. Reaktionen von Metallen und Metallverbindungen sowie von Nichtmetallen (Ammoniak)
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 9 & 10 Reaktionen von Metallen und Metallverbindungen sowie von Nichtmetallen (Ammoniak) 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 9 & 10 Reaktionen von Metallen und Metallverbindungen sowie von Nichtmetallen (Ammoniak) 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf
Quantitative Analyse von Kohlenwasserstoffen
 Schulversuchspraktikum SoSe 2013 Klassenstufen 11 & 12 Quantitative Analyse von Kohlenwasserstoffen 2 Auf einen Blick: Im Folgenden werden zunächst drei Versuche vorgestellt, welche die benötigten Teilschritte
Schulversuchspraktikum SoSe 2013 Klassenstufen 11 & 12 Quantitative Analyse von Kohlenwasserstoffen 2 Auf einen Blick: Im Folgenden werden zunächst drei Versuche vorgestellt, welche die benötigten Teilschritte
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Aktivierungsenergie und Katalyse
 1 Beschreibung des Themas und zugehörige Lernziele Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 7 & 8 Aktivierungsenergie und Katalyse 1 Beschreibung des Themas und zugehörige
1 Beschreibung des Themas und zugehörige Lernziele Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 7 & 8 Aktivierungsenergie und Katalyse 1 Beschreibung des Themas und zugehörige
Trennverfahren auf Basis der Dichte
 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 7 & 8 Dichte und dessen Abhängigkeit von der Temperatur; Trennverfahren auf Basis der Dichte 2 Auf einen Blick: Diese Unterrichtseinheit
Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 7 & 8 Dichte und dessen Abhängigkeit von der Temperatur; Trennverfahren auf Basis der Dichte 2 Auf einen Blick: Diese Unterrichtseinheit
1 V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure
 V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure 1 1 V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure Der Satz von Hess besagt, dass die Wärmemenge
V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure 1 1 V 3 Versuch zum Wärmesatz von Hess bei der Reaktion von Calcium mit Salzsäure Der Satz von Hess besagt, dass die Wärmemenge
Korrosion und Korrosionsschutz
 Schulversuchspraktikum Sommersemester 2013 Klassenstufen 11 & 12 Korrosion und Korrosionsschutz 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch
Schulversuchspraktikum Sommersemester 2013 Klassenstufen 11 & 12 Korrosion und Korrosionsschutz 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch
Bist Du nicht "FIT", dann musst Du nacharbeiten.
 Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
Überlege zunächst, ob Du die gestellte Frage beantworten kannst und kreuze in der Tabelle entsprechend an. Überprüfe Deine Angabe an Hand der entsprechenden Aufgabe. (Die Nummerierung der Frage und der
