Umsetzung der neuen KRINKO(RKI)-BfArM-Empfehlung
|
|
|
- Louisa Hummel
- vor 6 Jahren
- Abrufe
Transkript
1 MEDICA TECH FORUM Umsetzung der neuen KRINKO(RKI)-BfArM-Empfehlung Marc Thanheiser Fachgebiet Angewandte Infektions- und Krankenhaushygiene, Robert Koch-Institut
2 Marc Thanheiser Leiter der AG des RKI: Physikalische Verfahren zur Inaktivierung von Erregern und Raumdesinfektionsverfahren DIN-Ausschüsse Dampfsterilisation, Indikatoren, NTF- Sterilisation, RDG und Sterilgutversorgung des Normenausschuss Medizin. Länderarbeitskreis "Offene Fragen der Aufbereitung" Arbeitskomitee HAK-RDS der ZLG Fachausschuss Prüfwesen der ÖGSV Expertenkreis Labortechnik des ABAS VDI-Fachbeirat Biotechnologie Leiter der KRINKO / BfArM-AG Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten
3 Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten Aktualisierte Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) beim Robert Koch-Institut (RKI) und des Bundesinstitutes für Arzneimittel und Medizinprodukte (BfArM) zu den "Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten ist seit wenigen Wochen auf den Internetseiten des RKI und im Bundesgesundheitsblatt (Bundesgesundheitsbl : ) veröffentlicht. Zur Unterstützung der Einführung der aktualisierten Empfehlung haben wir eine frei verfügbare Musterpräsentation erstellt:
4 Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten 2012 Aktualisierte Empfehlung der KRINKO und des BfArM Eine Musterpräsentation des Robert Koch-Institutes Erstellt von: Marc Thanheiser
5 Gliederung Zweck und Umfang der Präsentation, Zielgruppe Anlass und Rechtsgrundlagen Ablauf der Aktualisierung Neuer Aufbau der Empfehlung und Anlagen Beispiele für Änderungen/Präzisierungen Weitere Informationsquellen 5 von 35
6 Rechtlicher Hinweis zur Verwendung der Präsentation Diese Präsentation wurde vom RKI FG 14 erstellt. Sie darf frei vervielfältigt und verwendet werden, vorausgesetzt, es werden keine Änderungen vorgenommen und es wird auf die Urheber verwiesen. Eine kommerzielle Verwendung (Verkauf, Verwendung in bezahlten Vorträgen) ist ausgeschlossen. Keine Entbindung von der Sorgfaltspflicht! Kontakt bei Fragen: 6 von 35
7 Zweck und Umfang, Zielgruppe Diese Präsentation beschäftigt sich mit der aktualisierten Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) beim Robert Koch-Institut (RKI) und des Bundesinstitutes für Arzneimittel und Medizinprodukte (BfArM) zu den "Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten". Sie soll die für die Aufbereitung Verantwortlichen (Betreiber), das Hygienepersonal und die Hygienekommissionen in Ihrer Arbeit unterstützen und richtet sich primär an alle Einrichtungen des Gesundheitswesens im ambulanten und stationären Sektor die Medizinprodukte aufbereiten. 7 von 35
8 Anlass und Rechtsgrundlagen Eine ordnungsgemäße Aufbereitung von Medizinprodukten wird vom Gesetzgeber vermutet, wenn die KRINKO-BfArM-Empfehlung beachtet wird ( 4 Absatz 2 MPBetreibV). Die bisherige KRINKO-BfArM-Empfehlung zu den Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten stammte aus dem Jahre 2001 und bedurfte einer Aktualisierung. Weitere Empfehlungen und Kommentare zu speziellen Bereichen der Aufbereitung wurden zwischenzeitlich von der KRINKO und dem BfArM veröffentlicht. 8 von 35
9 Ablauf der Aktualisierung Grundlage: Erfahrungsbericht zur Aufbereitung von Medizinprodukten in Deutschland (BMG, 2008) Vorbereitung eines Entwurfes in der Arbeitsgruppe Diskussion des Entwurfes in der KRINKO mit Beteiligung des BfArM Vorlage des Entwurfs zur Anhörung bei Ländern und Verbänden (u.a. AWMF, BÄK, BZÄK, DGKH, DGSV, DIN, DKG, DPR, KBV, PKV, VDI, VHD, ZLG) Beratung der eingegangenen Kommentare in der Kommission mit Vertretern des BfArM und des BMG Verabschiedung des Textes in der Kommission mit Vertretern des BfArM und des BMG Veröffentlichung im Bundesgesundheitsblatt und auf den Internetseiten des RKI 9 von 35
10 Aufbau der Empfehlung und Anlagen Die Empfehlung Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten ist wie bisher gegliedert in: 1. Grundsätzliches (Verantwortung, Voraussetzungen für die Aufbereitung, Risikobewertung und Einstufung von Medizinprodukten vor der Aufbereitung, Angaben des Herstellers, Validierung der Aufbereitungsverfahren/- prozesse, Sicherung der Qualität der zur Anwendung kommenden Aufbereitungsprozesse) 2. Durchführung der Aufbereitung (Vorbereitung der Aufbereitung (Vorbehandlung, Sammlung, Vorreinigung, ggf. Zerlegen, Zwischenlagerung und Transport), Reinigung, Desinfektion, Spülung und Trocknung, Prüfung der technischfunktionellen Sicherheit, Verpackung, Sterilisation, Kennzeichnung, Freigabe zur Anwendung, Chargendokumentation) 3. Transport und Lagerung Anhang A: Gesetze, Verordnungen, Richtlinien Anhang B: Normen Literatur 10 von 35
11 Fragenkatalog 1: Grundlagen der Aufbereitung Verwenden wir dokumentierte und validierte Verfahren bei der Aufbereitung von Medizinprodukten (MP)? Existieren für alle Einzelschritte geeignete Standardarbeitsanweisungen bzw. Prozessvalidierungen? Erfolgt eine Risikobewertung und Einstufung der MP von uns? Werden die Herstellerangaben zur Aufbereitung berücksichtigt? Gibt es dazu eine Hygieneordnung der zuständigen Landesbehörde und von unserer medizinischen Einrichtung? 11 von 35
12 Aufbau der Empfehlung und Anlagen Neu hinzugekommen sind insgesamt acht mitgeltende Anlagen zur Konkretisierung von einzelnen Aspekten der zentralen Empfehlung. Es wurden somit jetzt verschiedene Empfehlungen, Stellungnahmen und Kommentare zu diesem speziellen Thema in einem Dokument vereint. 12 von 35
13 Aufbau der Empfehlung und Anlagen Die neuen mitgeltenden Anlagen behandeln im Einzelnen folgende Themen: Anlage 1: Zum Begriff geeignete validierte Verfahren Anlage 2: zu Abschnitt Prüfung der technisch-funktionellen Sicherheit 13 von 35
14 Aufbau der Empfehlung und Anlagen Anlage 3: Inbetriebnahme und Betrieb von Reinigungs- und Desinfektions- geräten (RDG) zur Aufbereitung von Medizinprodukten (Checkliste) Anlage 4: Inbetriebnahme und Betrieb von Kleinsterilisatoren zur Aufbereitung von Medizinprodukten (Checkliste) 14 von 35
15 Aufbau der Empfehlung und Anlagen Anlage 5: Übersicht über Anforderungen an Aufbereitungseinheiten für Medizinprodukte Anlage 6: Sachkenntnis des Personals 15 von 35
16 Fragenkatalog 2: Grundlagen der Aufbereitung Werden die baulich-funktionellen Anforderungen erfüllt und die technische Ausstattung bereitgestellt Haben wir eigene Aufbereitungsräume, geeignete Bereichs- /Zonentrennungen und Geräte? Verfügen die mit der Aufbereitung beauftragten Personen über die notwendige Sachkenntnis? 16 von 35
17 Aufbau der Empfehlung und Anlagen Anlage 7: Maßnahmen zur Minimierung des Risikos einer Übertragung der CJK/vCJK durch Medizinprodukte Anhang 1 zur Anlage 7: Hinweis auf den Endoskop-Pool an der Universitätsmedizin Göttingen oben: PrP C; unten PrPSc (path.) DIRECTORATE-GENERAL FOR RESEARCH AND INNOVATION, European Commission 17 von 35
18 Fragenkatalog 3: CJK/vCJK Führen wir Risikoeingriffe, die sich aus dem Verteilungsmuster pathologischen Prionproteins im menschlichen Organismus ableiten, durch? wenn ja, kennen wir die Zeichen einer möglichen oder klinisch wahrscheinlichen CJK/vCJK und die dann notwendigen prionenspezifischen Schutzmaßnahmen? treffen wir generelle Maßnahmen bei der Aufbereitung von Medizinprodukten zur Vermeidung der Übertragung von pathologischem Prionprotein bei unerkannten Trägern? kombinieren wir dabei wenigstens zwei auch für die Dekontamination bzw. Inaktivierung von Prionen (zumindest partiell) geeignete Verfahren? 18 von 35
19 Aufbau der Empfehlung und Anlagen Anlage 8: Anforderungen an die Hygiene bei der Aufbereitung flexibler Endoskope und endoskopischen Zusatzinstrumentariums (ersetzt die gleichnamige Empfehlung aus 2002) Mit drei neuen Anhängen: Anhang 6: Zur Aufbereitung flexibler Zystoskope und Bronchoskope Anhang 7: Aufbereitung von Ultraschallsonden zur Anwendung in der Gynäkologie Anhang 8: Aufbereitung von Ultraschallsonden mit Schleimhautkontakt 19 von 35
20 Was ist geblieben und was hat sich geändert? Validierung: Grundsätzliche Aussagen sind geblieben: Sterilisationsverfahren sind unter der Voraussetzung ihrer Anwendung bei rückstandsfrei gereinigten Medizinprodukten vollständig validierbar. Bei Reinigungs- und Desinfektionsverfahren sind insbesondere maschinelle Verfahren validierbar und vorrangig anzuwenden. 20 von 35
21 Beispiele für Ergänzungen/Präzisierungen Manuelle Reinigungs- und Desinfektionsverfahren, die z. B. im Rahmen der Vorreinigung von Medizinprodukten oder bei nicht maschinell zu reinigenden/desinfizierenden Medizinprodukten (Gruppe B) oder basierend auf einer Risikoanalyse zur Anwendung kommen, müssen stets nach dokumentierten Standardarbeitsanweisungen und mit auf Wirksamkeit geprüften, auf das Medizinprodukt abgestimmten (d.h. geeigneten und materialverträglichen) Mitteln und Verfahren validiert durchgeführt werden. 21 von 35
22 Beispiele für Ergänzungen Neu aufgenommen wurde: Die Anwendung manueller Verfahren setzt bei Verfügbarkeit maschineller Verfahren voraus, dass der Beleg über die Äquivalenz der Leistungsfähigkeit manueller und maschineller Verfahren erbracht wurde. In jedem Falle ist die standardisierte und reproduzierbare Reinigung mit nachgewiesener Wirkung (bei Gruppe B einschließlich der inneren Oberflächen) sicher zu stellen. Die Standardarbeitsanweisungen müssen die kritischen Verfahrensschritte ausdrücklich benennen. Diese sollen im Rahmen periodischer Prüfungen berücksichtigt werden, um die Wirksamkeit der jeweiligen Maßnahmen zu belegen. 22 von 35
23 Beispiele für Ergänzungen Neu aufgenommen wurde: Die Inhalte der Standardarbeitsanweisungen müssen nachfolgende Voraussetzungen berücksichtigen: Das Verfahren ist ausreichend genau spezifiziert. Die Spezifikation umfasst insbesondere eine genaue Beschreibung aller aufeinanderfolgenden Arbeitsschritte sowie der jeweils einzusetzenden Hilfsmittel. 23 von 35
24 Beispiele für Ergänzungen Neu aufgenommen wurde: Die Beschreibung der Arbeitsschritte enthält, mit Bezug auf die einzusetzenden Hilfsmittel, klar definierte Mindestvorgaben (einschl. zulässiger Toleranzen) zu den anzuwendenden Intensitäten, Spül- und Behandlungsdauern, Spülvolumina, Anzahl der Spülschritte, etc. Bei der Validierung werden worst case -Aspekte in Bezug auf die in der Beschreibung angegebenen Bedingungen eingesetzt. 24 von 35
25 Beispiele für Änderungen/Präzisierungen Die Qualität der Aufbereitung wird in Abhängigkeit vom jeweiligen Verfahren der Reinigung, Desinfektion und Sterilisation sichergestellt durch a) eine Validierung (bestehend aus Installations-, Betriebsund Leistungsqualifikation) b) periodische Routineprüfungen (z.b. täglich) c) chargenbezogene Routineprüfungen d) messtechnische Überwachung und Prüfung der Prozessparameter e) Wartung, Kalibrierung, ggf. Justierung, Instandsetzung und f) periodische Verfahrensprüfungen (erneute Leistungsbeurteilung) g) ereignisbezogene Verfahrungsprüfung (Leistungsbeurteilung aus besonderem Anlass). 25 von 35
26 Beispiele für Ergänzungen Neu aufgenommen wurde: Bei der Aufbereitung von Medizinprodukten ist entweder eine Spülung zwischen Reinigung und Desinfektion obligat, um die Desinfektionsleistung durch organisches Material und chemische Rückstände aus der vorherigen Reinigung nicht zu beeinträchtigen oder der Prozesschemikalienhersteller belegt eine ausreichende Desinfektion auch ohne Zwischenspülung. Bei der abschließenden chemischen/chemothermischen Desinfektion von semikritischen Medizinprodukten sind viruzide Desinfektionsverfahren/-mittel zu verwenden, deren Gutachten auf Grundlage der DVV/RKI-Leitlinie erstellt wurden. 26 von 35
27 Beispiele für Ergänzungen Neu aufgenommen wurde: Der Dekontamination von C. difficile dient die Kombination aus sorgfältiger Vor- und Hauptreinigung sowie eine Instrumentendesinfektion auf Basis von Glutaraldehyd und Peressigsäure RKI, Berlin Grundsätzlich erfolgt die Sterilisation nach sorgfältiger Reinigung und aus arbeitsschutzgründen notwendigen Desinfektion der Medizinprodukte. Heißluftsterilisation ( -desinfektion ) nur für semikritisch A (unverpackt) oder kritisch A-Produkte. 27 von 35
28 Beispiele für Ergänzungen Neu aufgenommen wurde: Bei der Heißluftsterilisation sind, im Gegensatz zu anderen Sterilisationsverfahren, die Masse der Güter, deren spezifische Wärme und spezifische Wärmeleitfähigkeit, die Verpackung und besonders unterschiedliche Beladungsmuster kritisch. Daher muss der Betreiber das Verfahren validieren, die Beladung (Masse der Instrumente) und die Verpackung definieren und standardisieren und dies sowie die Einhaltung der erforderlichen Temperatur-Zeit- Relationen fortlaufend dokumentieren. 28 von 35
29 Beispiele für Änderungen/Präzisierungen Kennzeichnung: Die Ergebnisse sind so zu dokumentieren, dass eine Rückverfolgbarkeit auf die jeweilige Charge (bei Medizinprodukten der Gruppen kritisch A und kritisch B) bzw. auf das aufbereitete Produkt (bei Medizinprodukten der Gruppe kritisch C) gewährleistet ist. Auch bei Medizinprodukten, bei denen die Aufbereitung mit einer Desinfektion endet, muss die erfolgte Durchführung des Prozesses für den Anwender erkennbar sein (QM). 29 von 35
30 Beispiele für Änderungen/Präzisierungen Chargendokumentation: Die Aufzeichnungen über die Aufbereitung von Medizinprodukten sind mindestens 5 Jahre aufzubewahren. Sonstige Rechtsvorschriften zu Aufbewahrungsfristen (z. B. Patientendokumentation) bleiben hiervon unberührt. Transport und Lagerung: Aufbereitete Medizinprodukte die steril zur Anwendung kommen brauchen stets eine Verpackung und sind staubgeschützt, sauber, trocken und frei von Ungeziefer bei Raumtemperatur zu lagern. 30 von 35
31 Beispiele für Ergänzungen Neu aufgenommen wurde: Die Lagerdauer ist abhängig von der Qualität des Verpackungsmaterials, der Dichtigkeit der Siegelnähte und den Lagerbedingungen. Davon abhängig sind auch Lagerfristen von über sechs Monaten denkbar. Keimarme (semikritische) Medizinprodukte müssen so gelagert werden, dass eine Rekontamination während der Lagerung vermieden wird. 31 von 35
32 Weitere Informationsquellen Medizinprodukte Infektionsschutz Infektions- und Krankenhaushygiene Empfehlungen der Kommission für Krankenhaushygiene und Infektionsprävention Medizinprodukte Dokumente Medizinprodukte Fachinformationen Fachinformationen Qualität 32 von 35
33 Weitere Informationsquellen Die vorherigen Folien enthielten nur einige Beispiele für Ergänzungen bzw. Änderungen in der aktualisierten Empfehlung und können nicht das Studium der gesamten Empfehlung ersetzen. Die aktualisierte Empfehlung und weiterführende Informationen erhalten Sie auch unter: Infektionsschutz Infektions- und Krankenhaushygiene Aufbereitung von Medizinprodukten 33 von 35
34 Weitere Informationsquellen Bei weiteren Fragen, die die Durchführung der Medizinprodukte-Betreiberverordnung betreffen, können Sie sich auch gerne an Ihre für die Medizinprodukteüberwachung zuständige Behörde wenden. Diese finden Sie z. B. über das DIMDI: Medizinprodukte Adressen Bitte beachten Sie: Das RKI ist weder Prüf-, noch Zulassungs- oder Überwachungsbehörde für den Rechtsbereich Medizinprodukte! 34 von 35
35 Vielen Dank für Ihre Aufmerksamkeit!
Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels
 Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
Professionelle Aufbereitung von Medizinprodukten Podiumsdiskussion DGSV Kongress 2014 zur KRINKO-BfArM-Empfehlung Validierung Leitung: Dr. M.-Th.Linner, Dr. W. Michels Grundaussagen zur Validierung (1)
Synopse der eingegangenen Stellungnahmen durch das Sekretariat der KRINKO und das BfArM
 Synopse der eingegangenen Stellungnahmen durch das Sekretariat der KRINKO und das BfArM (Bericht an die KRINKO 2008) Verschiedene Kreise stellen zum Teil konträre Forderungen, wie z.b. die Forderung nach
Synopse der eingegangenen Stellungnahmen durch das Sekretariat der KRINKO und das BfArM (Bericht an die KRINKO 2008) Verschiedene Kreise stellen zum Teil konträre Forderungen, wie z.b. die Forderung nach
Medizinprodukteaufbereitung aus Sicht der Bezirksregierung
 Medizinprodukteaufbereitung aus Sicht der Bezirksregierung Dr. Arno Terhechte Dezernat 24 Pharmazeutische Angelegenheiten Themen: Warum werden Betreiber inspiziert? Welche Betreibertypen werden überwacht?
Medizinprodukteaufbereitung aus Sicht der Bezirksregierung Dr. Arno Terhechte Dezernat 24 Pharmazeutische Angelegenheiten Themen: Warum werden Betreiber inspiziert? Welche Betreibertypen werden überwacht?
Deutsche Akkreditierungsstelle GmbH
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14103-01-02 nach DIN EN ISO/IEC 17025:2005 1 und den Richtlinien 90/385/EWG 2 und 93/42/EWG 3 als Prüflaboratorium Gültigkeitsdauer:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-14103-01-02 nach DIN EN ISO/IEC 17025:2005 1 und den Richtlinien 90/385/EWG 2 und 93/42/EWG 3 als Prüflaboratorium Gültigkeitsdauer:
Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis
 Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis Ute Wurmstich gilborn zahnärzte Kaltenweider Str. 11 D-30900 Wedemark Fachkunde I-III DGSV/SGSV 1 Grundsätzliche
Routine und Herausforderungen der Medizinprodukte Aufbereitung in einer modernen Zahnarztpraxis Ute Wurmstich gilborn zahnärzte Kaltenweider Str. 11 D-30900 Wedemark Fachkunde I-III DGSV/SGSV 1 Grundsätzliche
Änderungen der MPBetreibV 2014
 Änderungen der MPBetreibV 2014 3 Instandhaltung von Medizinprodukten (1) Die Instandhaltung von Medizinprodukten umfasst insbesondere Instandhaltungsmaßnahmen und die Instandsetzung. Instandhaltungsmaßnahmen
Änderungen der MPBetreibV 2014 3 Instandhaltung von Medizinprodukten (1) Die Instandhaltung von Medizinprodukten umfasst insbesondere Instandhaltungsmaßnahmen und die Instandsetzung. Instandhaltungsmaßnahmen
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ)
 Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Zertifizierung einer Zentralen Sterilgutversorgungsabteilung (FAQ) Marion Härtel Beraterin Zertifizierung ZSVA Expertin Medizinprodukte E-Mail: mp@herrderlage.com Tel: 030-53 000 466 Resultierend aus der
Regulative Aspekte der Aufbereitung chirurgischer Implantate
 Regulative Aspekte der Aufbereitung chirurgischer Implantate 35.Veranstaltung des Arbeitskreis Infektionsprophylaxe 16. Oktober 2012 in Potsdam 17.Oktober 2012 in Leipzig 1 Person Anja Fechner Dipl.-Ing.
Regulative Aspekte der Aufbereitung chirurgischer Implantate 35.Veranstaltung des Arbeitskreis Infektionsprophylaxe 16. Oktober 2012 in Potsdam 17.Oktober 2012 in Leipzig 1 Person Anja Fechner Dipl.-Ing.
MPG und VO zum 94. N. Buchrieser
 MPG und VO zum 94 N. Buchrieser Gesetze und Regelwerke EU-Direktive 93/42/EWG Medizinproduktegesetz Verordnung zum 94 MPG (ÖGSV-LL 11) RDG-Normen (ÖNORM EN ISO 15883 Teil 1-7) Sterilisatornormen (EN 285,
MPG und VO zum 94 N. Buchrieser Gesetze und Regelwerke EU-Direktive 93/42/EWG Medizinproduktegesetz Verordnung zum 94 MPG (ÖGSV-LL 11) RDG-Normen (ÖNORM EN ISO 15883 Teil 1-7) Sterilisatornormen (EN 285,
Medizinprodukterechtliche Stellungnahme zu Weisungsunabhängigkeitsbescheinigungen für Prüfungen im Rahmen der Aufbereitung von Medizinprodukten
 MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT KANZLEI DR. JÄKEL www.jaekel-law.de BERLINER STR. 37 T 03546 9349 528 15907 LÜBBEN (SPREEWALD) F 03546 9349 529 DR. CHRISTIAN JÄKEL dr@jaekel-law.de
MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT KANZLEI DR. JÄKEL www.jaekel-law.de BERLINER STR. 37 T 03546 9349 528 15907 LÜBBEN (SPREEWALD) F 03546 9349 529 DR. CHRISTIAN JÄKEL dr@jaekel-law.de
In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm der DGSV zur Einstufung
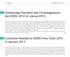 64 DGSV Zentralsterilisation 1/2013 Notwendige Korrektur des Flussdiagramms der DGSV 2012 im nuar 2013 In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm
64 DGSV Zentralsterilisation 1/2013 Notwendige Korrektur des Flussdiagramms der DGSV 2012 im nuar 2013 In der Ausgabe 6/2012 der Zentralsterilisation wurde die Empfehlung 77, das überarbeitete Flussdiagramm
9.5 Medizinprodukte-Betreiberverordnung - MPBetreibV
 9.5 -Betreiberverordnung - MPBetreibV Die -Betreiberverordnung (MPBetreibV) regelt das Errichten, Betreiben und Anwenden von n und von Zubehör für. Zubehör sind Gegenstände, Stoffe, Zubereitungen aus Stoffen
9.5 -Betreiberverordnung - MPBetreibV Die -Betreiberverordnung (MPBetreibV) regelt das Errichten, Betreiben und Anwenden von n und von Zubehör für. Zubehör sind Gegenstände, Stoffe, Zubereitungen aus Stoffen
Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen
 Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen F. H. H. Brill Dr. Brill + Partner GmbH Institut für Hygiene und Mikrobiologie, Hamburg, www.brillhygiene.com
Validierung manueller Aufbereitungsprozesse von Medizinprodukten gesetzliche und normative Grundlagen F. H. H. Brill Dr. Brill + Partner GmbH Institut für Hygiene und Mikrobiologie, Hamburg, www.brillhygiene.com
Anlage zur Akkreditierungsurkunde D-PL-18398-02-00 nach DIN EN ISO/IEC 17025:2005 3 und Richtlinie 93/42/EWG 1 und 90/385/EWG 2
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18398-02-00 nach DIN EN ISO/IEC 17025:2005 3 und Richtlinie 93/42/EWG 1 und 90/385/EWG 2 Gültigkeitsdauer: 17.12.2015 bis 04.03.2018
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-18398-02-00 nach DIN EN ISO/IEC 17025:2005 3 und Richtlinie 93/42/EWG 1 und 90/385/EWG 2 Gültigkeitsdauer: 17.12.2015 bis 04.03.2018
Ethische, hygienische und juristische Gesichtspunkte der Aufbereitung von Medizinprodukten
 Gemeinsame Stellungnahme des Vorstands der Deutschen Gesellschaft für Krankenhaushygiene (DGKH) und der Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten (ZLG) Ethische,
Gemeinsame Stellungnahme des Vorstands der Deutschen Gesellschaft für Krankenhaushygiene (DGKH) und der Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten (ZLG) Ethische,
Softwarevalidierung aus Anwendersicht. DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009
 Softwarevalidierung aus Anwendersicht DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009 Softwarevalidierung aus Anwendersicht Geräte mit automatischen Prozessabläufen zur Aufbereitung von Medizinprodukten
Softwarevalidierung aus Anwendersicht DGSV Kongress / Dr. B. Gallert / Fulda / 16.10.2009 Softwarevalidierung aus Anwendersicht Geräte mit automatischen Prozessabläufen zur Aufbereitung von Medizinprodukten
Qualitätsmanagement in der Gesundheitsversorgung, Medizinprodukten und in der Hygiene
 Qualitätsmanagement in der Gesundheitsversorgung, bei der Aufbereitung von Medizinprodukten und in der Hygiene Christiaan Meijer Vortrag auf der 35. Veranstaltung des Arbeitskreises Infektionsprophylaxe
Qualitätsmanagement in der Gesundheitsversorgung, bei der Aufbereitung von Medizinprodukten und in der Hygiene Christiaan Meijer Vortrag auf der 35. Veranstaltung des Arbeitskreises Infektionsprophylaxe
Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit?
 Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit? S. Werner, F. v. Rheinbaben HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
Derzeitige Medizinprodukte Beschaffung im Gesundheitswesen ein Systemrisiko für die Patientensicherheit? S. Werner, F. v. Rheinbaben HygCen Germany GmbH, Schwerin / Bochum 13.04.2016 DGKH Kongress Berlin
BAEHR Online- Hygieneplan. Hygieneplan? Ja klar, aber wie bekomm ich das am einfachsten, schnellsten. und sicher. hin?!
 Hygieneplan? Ja klar, aber wie bekomm ich das am einfachsten, schnellsten und sicher hin?! einfach, zeitsparend und sicher Unterstützung für Ihren betriebsspezifischen Hygieneplan BAEHR Online- Hygieneplan
Hygieneplan? Ja klar, aber wie bekomm ich das am einfachsten, schnellsten und sicher hin?! einfach, zeitsparend und sicher Unterstützung für Ihren betriebsspezifischen Hygieneplan BAEHR Online- Hygieneplan
Bekanntmachung. Übersicht über die Anlagen
 Bundesgesundheitsbl 2012 55:1244 1310 DOI 10.1007/s00103-012-1548-6 Springer-Verlag 2012 Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten Empfehlung der Kommission für Krankenhaushygiene
Bundesgesundheitsbl 2012 55:1244 1310 DOI 10.1007/s00103-012-1548-6 Springer-Verlag 2012 Anforderungen an die Hygiene bei der Aufbereitung von Medizinprodukten Empfehlung der Kommission für Krankenhaushygiene
Medizinprodukte-Sicherheitsplanverordnung
 Hygieneforum Sande 19.06.2014 Meldung von Vorkommnissen nach der Medizinproduke-Sicherheitsplanverordnung www.klinikum-bremen-ldw.de Klinikum Links der Weser Senator-Weßling-Str. 1 28277 Bremen Meldung
Hygieneforum Sande 19.06.2014 Meldung von Vorkommnissen nach der Medizinproduke-Sicherheitsplanverordnung www.klinikum-bremen-ldw.de Klinikum Links der Weser Senator-Weßling-Str. 1 28277 Bremen Meldung
Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen
 Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen Dr. med. univ. Sebastian Werner 1,2 1 HygCen Austria GmbH, Bischofshofen 2 Abteilung für Hygiene, Sozial und Umweltmedizin, Ruhruniversität
Nominative und gesetzliche Grundlagen zur Aufbereitung von Endoskopen Dr. med. univ. Sebastian Werner 1,2 1 HygCen Austria GmbH, Bischofshofen 2 Abteilung für Hygiene, Sozial und Umweltmedizin, Ruhruniversität
DGSV-Kongress vom 3.- 5. Oktober 2011. Neue Kompetenzen der ZSVA: Aufbereitung von flexiblen Endoskopen
 DGSV-Kongress vom 3.- 5. Oktober 2011 Neue Kompetenzen der ZSVA: Aufbereitung von flexiblen Endoskopen - Unterschiede in der Aufbereitung - Aufbereitungsverfahren mit chemo-thermischer Desinfektion - Materialveränderungen,
DGSV-Kongress vom 3.- 5. Oktober 2011 Neue Kompetenzen der ZSVA: Aufbereitung von flexiblen Endoskopen - Unterschiede in der Aufbereitung - Aufbereitungsverfahren mit chemo-thermischer Desinfektion - Materialveränderungen,
Qualitätsmanagement in der Gesundheits- versorgung, bei der Aufbereitung von Medizinprodukten und in der Hygiene
 Qualitätsmanagement in der Gesundheits- versorgung, bei der Aufbereitung von Medizinprodukten und in der Hygiene Christiaan Meijer! Vortrag auf dem Tübinger Forum am 29. März 2014 Mehr wissen. Weiter denken.
Qualitätsmanagement in der Gesundheits- versorgung, bei der Aufbereitung von Medizinprodukten und in der Hygiene Christiaan Meijer! Vortrag auf dem Tübinger Forum am 29. März 2014 Mehr wissen. Weiter denken.
Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation
 Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation Präsentation von Markus Geissmann anlässlich der 7èmes Journées Nationales Suissessursur la Stérilisation
Validierung der Software Anwendung für das Instrumentenmanagement und die Prozessdokumentation Präsentation von Markus Geissmann anlässlich der 7èmes Journées Nationales Suissessursur la Stérilisation
MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT. Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung
 KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung DGSV Kongress 2010 Fulda 08.10.2010 Inhalt Compliance
KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT Die Aufbereitung von Medizinprodukten - Haftungsvermeidung durch Haftungsverlagerung DGSV Kongress 2010 Fulda 08.10.2010 Inhalt Compliance
Kassenärztliche Vereinigung Sachsen-Anhalt Abteilung Qualitätssicherung und management Doctor-Eisenbart-Ring 2 39120 Magdeburg
 Ansprechpartner: Anke Schmidt Tel.: 0391 627-6453 Christin Richter Tel.: 0391 627-7454 oder per E-Mail: Hygiene@kvsa.de Anschaffung eines Reinigungs- und Desinfektionsgerätes (RDG) Reinigungs- und Desinfektionsgeräte
Ansprechpartner: Anke Schmidt Tel.: 0391 627-6453 Christin Richter Tel.: 0391 627-7454 oder per E-Mail: Hygiene@kvsa.de Anschaffung eines Reinigungs- und Desinfektionsgerätes (RDG) Reinigungs- und Desinfektionsgeräte
Zertifizierung des QM-Systems bei der Aufbereitung von Kritisch-C Produkten
 Christian Witte Zertifizierung des QM-Systems bei der Aufbereitung von Kritisch-C Produkten Zur aktuellen Differenz zwischen MPBetreibV und KRINKO/BfArM-Empfehlung Verordnung über die Änderung der MPBetreibV
Christian Witte Zertifizierung des QM-Systems bei der Aufbereitung von Kritisch-C Produkten Zur aktuellen Differenz zwischen MPBetreibV und KRINKO/BfArM-Empfehlung Verordnung über die Änderung der MPBetreibV
Chargendokumentation: High-End für die chirurgische Praxis
 Neue Materialien und Methoden 39 M. Keweloh Chargendokumentation: High-End für die chirurgische Praxis Einleitung: Abbildung 1 Startmaske. (Fotos: M. Keweloh) Nachweisbare Qualitätssicherung in chirurgischen
Neue Materialien und Methoden 39 M. Keweloh Chargendokumentation: High-End für die chirurgische Praxis Einleitung: Abbildung 1 Startmaske. (Fotos: M. Keweloh) Nachweisbare Qualitätssicherung in chirurgischen
Dieser Rahmenlehrplan ersetzt den Rahmenlehrplan für den Sachkundelehrgang in der bisher vorliegenden Fassung. Präambel
 Erwerb der Sachkenntnis gemäß 4(3) der Medizinproduktebetreiberverordnung (MPBetreibV) für die Instandhaltung von Medizinprodukten in der ärztlichen Praxis gültig ab Erscheinungsdatum und spätestens umzusetzen
Erwerb der Sachkenntnis gemäß 4(3) der Medizinproduktebetreiberverordnung (MPBetreibV) für die Instandhaltung von Medizinprodukten in der ärztlichen Praxis gültig ab Erscheinungsdatum und spätestens umzusetzen
Termine Nord. Lehrgang Fachkunde 1-1: 1. Woche 19.01. - 23.01.2015 2. Woche 26.01. - 30.01.2015 3. Woche 09.02. - 13.02.2015
 MMM Akademie Nord Termine Nord HH-Barmbek Lehrgang Fachkunde 1-1: 1. Woche 19.01. - 23.01.2015 2. Woche 26.01. - 30.01.2015 3. Woche 09.02. - 13.02.2015 Neu MMM Akademie Nord MMM Akademie Süd Informationen
MMM Akademie Nord Termine Nord HH-Barmbek Lehrgang Fachkunde 1-1: 1. Woche 19.01. - 23.01.2015 2. Woche 26.01. - 30.01.2015 3. Woche 09.02. - 13.02.2015 Neu MMM Akademie Nord MMM Akademie Süd Informationen
Empfehlung für die Überwachung der Aufbereitung von Medizinprodukten
 Empfehlung für die Überwachung der Aufbereitung von Medizinprodukten Rahmenbedingungen für ein einheitliches Verwaltungshandeln Erstellt von: Projektgruppe RKI-BfArM-Empfehlung der Arbeitsgruppe Medizinprodukte
Empfehlung für die Überwachung der Aufbereitung von Medizinprodukten Rahmenbedingungen für ein einheitliches Verwaltungshandeln Erstellt von: Projektgruppe RKI-BfArM-Empfehlung der Arbeitsgruppe Medizinprodukte
Umsetzung der Hygienerichtlinien
 Umsetzung der Hygienerichtlinien Andrea Percht, MBA Hygienefachkraft allgemein beeidete und gerichtlich zertifizierte Sachverständige für f r Hygiene Richtlinien Diese Leitlinie wurde auf Basis des Medizinproduktegesetzes
Umsetzung der Hygienerichtlinien Andrea Percht, MBA Hygienefachkraft allgemein beeidete und gerichtlich zertifizierte Sachverständige für f r Hygiene Richtlinien Diese Leitlinie wurde auf Basis des Medizinproduktegesetzes
Medizinproduktegesetz Medizinproduktebetreiberverordnung
 - Was müssen Betreiber tun? - Aufbereitung eine anspruchsvolle Aufgabe! J. Hanna Fachbereich Gesundheit Seite 1 Teil 1 - Was müssen Betreiber beachten? Seite 2 Alt: MedGV Neu: MPG Medizinprodukterecht
- Was müssen Betreiber tun? - Aufbereitung eine anspruchsvolle Aufgabe! J. Hanna Fachbereich Gesundheit Seite 1 Teil 1 - Was müssen Betreiber beachten? Seite 2 Alt: MedGV Neu: MPG Medizinprodukterecht
Anforderung an die hygienische Aufbereitung von Medizinprodukten in Nordrhein-Westfalen - Selbstauskunft -
 Anforderung an die hygienische Aufbereitung von Medizinprodukten in Nordrhein-Westfalen - - Einrichtung Name Adresse Tel. Fax E-mail Besichtigung Datum Teilnehmer Einrichtung Bezirksregierung Sonstige
Anforderung an die hygienische Aufbereitung von Medizinprodukten in Nordrhein-Westfalen - - Einrichtung Name Adresse Tel. Fax E-mail Besichtigung Datum Teilnehmer Einrichtung Bezirksregierung Sonstige
zu teamwork mit Haken und Ösen.
 vom Spagat der Verantwortlichkeit zur Rechtspflicht zu teamwork mit Haken und Ösen. Seminaris Medizinrecht seminaris.medizinrecht@t-online.de Hans-Werner Röhlig 46047 Oberhausen, Seilerstraße 106 Tel.:
vom Spagat der Verantwortlichkeit zur Rechtspflicht zu teamwork mit Haken und Ösen. Seminaris Medizinrecht seminaris.medizinrecht@t-online.de Hans-Werner Röhlig 46047 Oberhausen, Seilerstraße 106 Tel.:
Mindestinhalte von Validierungsberichten für Peroxid/ Peroxid-Plasma-Sterilisationsverfahren für Medizinprodukte
 Antworten und Beschlüsse des HAK Reinigung, Desinfektion u. Sterilisation Sterilisation RDS 004 Mindestinhalte von Validierungsberichten für Peroxid/ Peroxid-Plasma-Sterilisationsverfahren für Medizinprodukte
Antworten und Beschlüsse des HAK Reinigung, Desinfektion u. Sterilisation Sterilisation RDS 004 Mindestinhalte von Validierungsberichten für Peroxid/ Peroxid-Plasma-Sterilisationsverfahren für Medizinprodukte
ViFlow Prozessnetz als QM Handbuch in elektronischer Form
 ViFlow Prozessnetz als QM Handbuch in elektronischer Form Verpflichtung zur Qualitätssicherung 135a SGB V regelt die Verpflichtung zur Qualitätssicherung im Gesundheitswesen. Die Leistungserbringer sind
ViFlow Prozessnetz als QM Handbuch in elektronischer Form Verpflichtung zur Qualitätssicherung 135a SGB V regelt die Verpflichtung zur Qualitätssicherung im Gesundheitswesen. Die Leistungserbringer sind
Reinigung, Desinfektion, Pflege und Sterilisation von Turbinen, Hand- und Winkelstücken
 Reinigung, Desinfektion, Pflege und Sterilisation von Turbinen, Hand- und Winkelstücken Mikrobielle Kontamination von Übertragungsinstrumenten Nach Behandlung sind diese innen wie außen kontaminiert! Kontamination
Reinigung, Desinfektion, Pflege und Sterilisation von Turbinen, Hand- und Winkelstücken Mikrobielle Kontamination von Übertragungsinstrumenten Nach Behandlung sind diese innen wie außen kontaminiert! Kontamination
Arbeitskreis für Hygiene in Gesundheitseinrichtungen des Magistrats der Stadt Wien MA 15 Gesundheitsdienst der Stadt Wien STERILGUTVERSORGUNG
 Arbeitskreis für Hygiene in Gesundheitseinrichtungen des Magistrats der Stadt Wien MA 15 Gesundheitsdienst der Stadt Wien 18 Stand: 16.03.2016 STERILGUTVERSORGUNG Die internationale Normenreihe ÖNORM EN
Arbeitskreis für Hygiene in Gesundheitseinrichtungen des Magistrats der Stadt Wien MA 15 Gesundheitsdienst der Stadt Wien 18 Stand: 16.03.2016 STERILGUTVERSORGUNG Die internationale Normenreihe ÖNORM EN
Anhang B: Normen. Tabelle - Normen. 93/42/EWG DIN EN 285 Sterilisation Dampf-Sterilisatoren Groß- Sterilisatoren
 Anhang B: Normen Bei Befolgung der Angaben der aufgeführten Normen kann von der Erfüllung der anerkannten Regeln der Technik ausgegangen werden. Diese Zusammenstellung umfasst die unter dem Aspekt der
Anhang B: Normen Bei Befolgung der Angaben der aufgeführten Normen kann von der Erfüllung der anerkannten Regeln der Technik ausgegangen werden. Diese Zusammenstellung umfasst die unter dem Aspekt der
Tübinger Forum April 2012
 Tübinger Forum April 2012 Erstellung von Arbeitsanweisungen Praktische Beispiele Cornelia Hugo Akademie für Infektionsprävention 1 Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention
Tübinger Forum April 2012 Erstellung von Arbeitsanweisungen Praktische Beispiele Cornelia Hugo Akademie für Infektionsprävention 1 Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention
OP- Hygiene, Desinfektion und Sterilisation
 OP- Hygiene, Desinfektion und Sterilisation Studenten-Vorlesung, Bochum, 8. Juni 2010 Prof. Dr. Walter Popp Krankenhaushygiene Universitätsklinikum Essen Hufelandstr. 55, 45122 Essen Tel. 0201-723-4577
OP- Hygiene, Desinfektion und Sterilisation Studenten-Vorlesung, Bochum, 8. Juni 2010 Prof. Dr. Walter Popp Krankenhaushygiene Universitätsklinikum Essen Hufelandstr. 55, 45122 Essen Tel. 0201-723-4577
7. Desinfektion /Reinigung /Entsorgung /Sterilisation
 7. Desinfektion /Reinigung /Entsorgung /Sterilisation 7.3. Aufbereitung von Endoskopen Allgemein Personalschutz: Aufbereitung bei CJK Aufgrund konstruktiver Besonderheiten flexibler Endoskope und des endoskopischen
7. Desinfektion /Reinigung /Entsorgung /Sterilisation 7.3. Aufbereitung von Endoskopen Allgemein Personalschutz: Aufbereitung bei CJK Aufgrund konstruktiver Besonderheiten flexibler Endoskope und des endoskopischen
Erfahrungsbericht Aufbereitung der Aneurysma-Clips in der Zentralsterilisation. 08.06.2012 Seite 0
 Erfahrungsbericht Aufbereitung der Aneurysma-Clips in der Zentralsterilisation 08.06.2012 Seite 0 Übersicht Grundlagen Erfahrungen Herstellerangaben Aufbereitung Zusammenfassung Schlusswort 08.06.2012
Erfahrungsbericht Aufbereitung der Aneurysma-Clips in der Zentralsterilisation 08.06.2012 Seite 0 Übersicht Grundlagen Erfahrungen Herstellerangaben Aufbereitung Zusammenfassung Schlusswort 08.06.2012
Verfahrensanweisung zur Sauberkeit von Lagerschränken und -regalen, zum Umgang mit MP und Regelungen zur Lagerung von Sterilgut
 Entwurf Sitzmann 2/2011 Verfahrensanweisung zur Sauberkeit von Lagerschränken und -regalen, zum Umgang mit MP und Regelungen zur Lagerung von Sterilgut Bei erforderlicher Sterilität ist die Sterilisation
Entwurf Sitzmann 2/2011 Verfahrensanweisung zur Sauberkeit von Lagerschränken und -regalen, zum Umgang mit MP und Regelungen zur Lagerung von Sterilgut Bei erforderlicher Sterilität ist die Sterilisation
ZSVA & ISO 13485 (9001:2008) Anforderungen und Praxislösungen in der ZSVA
 & ISO 13485 (9001:2008) Anforderungen und Praxislösungen in der Iljias Mislimi Zentrale Sterilgutversorgungsabteilung () Diakonie-Klinikum Schwäbisch Hall ggmbh Oktober 2014 & ISO 13485 (9001:2008) Anforderungen
& ISO 13485 (9001:2008) Anforderungen und Praxislösungen in der Iljias Mislimi Zentrale Sterilgutversorgungsabteilung () Diakonie-Klinikum Schwäbisch Hall ggmbh Oktober 2014 & ISO 13485 (9001:2008) Anforderungen
Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2
 Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2 Ralph Ebersbach Vortrag auf dem 3. Berlin/Brandenburger Steritreff am 15. September 2012 in Berlin Mehr wissen. Weiter denken. Über HYBETA HYBETA
Validierung von Heißsiegelprozessen nach DIN EN ISO 11607-2 Ralph Ebersbach Vortrag auf dem 3. Berlin/Brandenburger Steritreff am 15. September 2012 in Berlin Mehr wissen. Weiter denken. Über HYBETA HYBETA
Die ambulante Medizin und
 J. Rathje, N. Enkling, M. Wolf, P. Jöhren Hygieneanforderungen an die zahnmedizinische Patientenversorgung CME-Beitrag Lernziele Der Leser sollte nach der Durchsicht des Artikels in der Lage sein, die
J. Rathje, N. Enkling, M. Wolf, P. Jöhren Hygieneanforderungen an die zahnmedizinische Patientenversorgung CME-Beitrag Lernziele Der Leser sollte nach der Durchsicht des Artikels in der Lage sein, die
9. Steri Fach Forum Am 3.März 2011 am LMU München Großhadern
 9. Steri Fach Forum Am 3.März 2011 am LMU München Großhadern Romana Frey Krankenschwester Fachkrankenschwester Operationsdienst Ausbildung zum Mentor Ausbildung Stationsleiter Stv. Leitung Gesamt OP Bereichsleitung
9. Steri Fach Forum Am 3.März 2011 am LMU München Großhadern Romana Frey Krankenschwester Fachkrankenschwester Operationsdienst Ausbildung zum Mentor Ausbildung Stationsleiter Stv. Leitung Gesamt OP Bereichsleitung
UV-Desinfektion von Ultraschallköpfen: Praxistestung
 UV-Desinfektion von Ultraschallköpfen: Praxistestung Priv. Doz. Dr. Magda Diab-El Schahawi Universitätsklinik für Krankenhaushygiene und Infektionskontrolle Med Uni Wien Literatur zu mangelnder Aufbereitung
UV-Desinfektion von Ultraschallköpfen: Praxistestung Priv. Doz. Dr. Magda Diab-El Schahawi Universitätsklinik für Krankenhaushygiene und Infektionskontrolle Med Uni Wien Literatur zu mangelnder Aufbereitung
Anlage zur Akkreditierungsurkunde D-ZM-16002-06-00 nach DIN EN ISO/IEC 17021:2011
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZM-16002-06-00 nach DIN EN ISO/IEC 17021:2011 Gültigkeitsdauer: 15.12.2014 bis 14.12.2019 Ausstellungsdatum: 15.12.2014 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZM-16002-06-00 nach DIN EN ISO/IEC 17021:2011 Gültigkeitsdauer: 15.12.2014 bis 14.12.2019 Ausstellungsdatum: 15.12.2014 Urkundeninhaber:
Leitlinie zur Validierung der manuellen Reinigung und manuellen chemischen Desinfektion von Medizinprodukten
 2013 Leitlinie zur Validierung der manuellen Reinigung und manuellen chemischen Desinfektion von Medizinprodukten DGKH Deutsche Gesellschaft für Krankenhaushygiene DGSV Deutsche Gesellschaft für Sterilgutversorgung
2013 Leitlinie zur Validierung der manuellen Reinigung und manuellen chemischen Desinfektion von Medizinprodukten DGKH Deutsche Gesellschaft für Krankenhaushygiene DGSV Deutsche Gesellschaft für Sterilgutversorgung
SACHKUNDEKURS ENDOSKOPIE
 SACHKUNDEKURS ENDOSKOPIE Hygiene + Aufbereitung in ambulanten Einrichtungen der Urologie. Überwachungen durch Aufsichtsbehörden 20. März 2013, Schwerin RECHTLICHER STELLENWERT VON LEITLINIEN Autor: Hans-Werner
SACHKUNDEKURS ENDOSKOPIE Hygiene + Aufbereitung in ambulanten Einrichtungen der Urologie. Überwachungen durch Aufsichtsbehörden 20. März 2013, Schwerin RECHTLICHER STELLENWERT VON LEITLINIEN Autor: Hans-Werner
ZWP extra. RKI/Hygiene. wichtige Neuerungen. 2/2013 August 9. Jahrgang
 ZWP extra 2/2013 August 9. Jahrgang wichtige Neuerungen RKI/Hygiene DRUCKLUFT ABSAUGUNG BILDGEBUNG ZAHNERHALTUNG HYGIENE DAS BESTE ist, wenn Sie von Viren sicher Abschied nehmen VOLL VIRUZID gemäß RKI-Empfehlung
ZWP extra 2/2013 August 9. Jahrgang wichtige Neuerungen RKI/Hygiene DRUCKLUFT ABSAUGUNG BILDGEBUNG ZAHNERHALTUNG HYGIENE DAS BESTE ist, wenn Sie von Viren sicher Abschied nehmen VOLL VIRUZID gemäß RKI-Empfehlung
Rechtliche Stellungnahme zur Aufbereitung von Medizinprodukten, insbesondere Einmalprodukten
 SOZIETÄT DR. REHBORN RECHTSANWÄLTE BERLIN - DORTMUND - KÖLN - LEIPZIG - MÜNCHEN Büro Berlin Kurfürstendamm 184 10707 Berlin Telefon: 030/88 77 69-0 Telefax: 030/88 77 69-15 Kathrin Möller 11 Yvonne Marckhoff
SOZIETÄT DR. REHBORN RECHTSANWÄLTE BERLIN - DORTMUND - KÖLN - LEIPZIG - MÜNCHEN Büro Berlin Kurfürstendamm 184 10707 Berlin Telefon: 030/88 77 69-0 Telefax: 030/88 77 69-15 Kathrin Möller 11 Yvonne Marckhoff
Umgang mit Explantaten
 Umgang mit Explantaten Aktuelle Entwicklung Implantate / Explantate Warum wird dieses Thema plötzlich so wichtig? Wem gehört das Explantat? Was muß berücksichtigt werden? Welche Aufgabe betrifft die ZSVA?
Umgang mit Explantaten Aktuelle Entwicklung Implantate / Explantate Warum wird dieses Thema plötzlich so wichtig? Wem gehört das Explantat? Was muß berücksichtigt werden? Welche Aufgabe betrifft die ZSVA?
Medizinprodukte-Überwachung im Land Bremen
 Medizinprodukte-Überwachung im Land Bremen Wiederaufbereitung in HNO- und urologischen Arztpraxen durch die Senatorin für Arbeit, Frauen, Gesundheit, Jugend und Soziales, Referat 34, als zuständige Behörde
Medizinprodukte-Überwachung im Land Bremen Wiederaufbereitung in HNO- und urologischen Arztpraxen durch die Senatorin für Arbeit, Frauen, Gesundheit, Jugend und Soziales, Referat 34, als zuständige Behörde
9. Steri Fach-Forum 3. März 2011 Klinikum der Universität München Großhadern
 9. Steri Fach-Forum 3. März 2011 Klinikum der Universität München Großhadern Sterilgutverpackung und Lagerung Normative Vorgaben/Interpretation Dr. Thomas Kießling TÜV Rheinland LGA Products GmbH Einleitung
9. Steri Fach-Forum 3. März 2011 Klinikum der Universität München Großhadern Sterilgutverpackung und Lagerung Normative Vorgaben/Interpretation Dr. Thomas Kießling TÜV Rheinland LGA Products GmbH Einleitung
zur Änderung der Richtlinie 93/42/EWG über Medizinprodukte
 17. Januar 2006 Positionspapier der Deutschen Krankenhausgesellschaft, Berlin und der Spitzenverbände der Krankenkassen AOK-Bundesverband, Bonn BKK Bundesverband, Essen Bundesverband der Innungskrankenkassen,
17. Januar 2006 Positionspapier der Deutschen Krankenhausgesellschaft, Berlin und der Spitzenverbände der Krankenkassen AOK-Bundesverband, Bonn BKK Bundesverband, Essen Bundesverband der Innungskrankenkassen,
Zertifizierungsstellen für Qualitätsmanagementsysteme
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 30.12.2009 Hinweis:
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 30.12.2009 Hinweis:
Beliehene gemäß 8 Absatz 1 AkkStelleG i.v.m. 1 Absatz 1 AkkStelleGBV
 . { DÄkkS Deutsche Akkreditierungsstelle Deutsche Akkreditierungsstelle GmbH Beliehene gemäß 8 Absatz 1 AkkStelleG i.v.m. 1 Absatz 1 AkkStelleGBV Akkreditierung Die Deutsche Akkreditierungsstelle GmbH
. { DÄkkS Deutsche Akkreditierungsstelle Deutsche Akkreditierungsstelle GmbH Beliehene gemäß 8 Absatz 1 AkkStelleG i.v.m. 1 Absatz 1 AkkStelleGBV Akkreditierung Die Deutsche Akkreditierungsstelle GmbH
Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen
 Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen Bibliografische Information der Deutschen Bibliothek Die Deutsche Bibliothek verzeichnet diese
Dietmar Kirchberg Das Medizinproduktegesetz: Was Pflegende wissen müssen Bestimmungen Beispiele Konsequenzen Bibliografische Information der Deutschen Bibliothek Die Deutsche Bibliothek verzeichnet diese
Umgebungs- und Hygieneprüfungen im Rahmen des Hygienemonitorings im Krankenhaus Prüfverfahren und Akzeptanzkriterien
 Umgebungs- und Hygieneprüfungen im Rahmen des Hygienemonitorings im Krankenhaus Prüfverfahren und Akzeptanzkriterien Dr. Julia Okpara-Hofmann Vortrag auf dem 115. Hygiene und Steri-Treff am 4. November
Umgebungs- und Hygieneprüfungen im Rahmen des Hygienemonitorings im Krankenhaus Prüfverfahren und Akzeptanzkriterien Dr. Julia Okpara-Hofmann Vortrag auf dem 115. Hygiene und Steri-Treff am 4. November
Medizinprodukte. Welches Ziel sollten Sie erreichen? Was sind Medizinprodukte (MP)? ZAHNMEDIZIN. Unternehmer
 Unternehmer ZAHNMEDIZIN Medizinprodukte Welches Ziel sollten Sie erreichen? Mitarbeiter, Patienten und Dritte ( Techniker, die ein Gerät instand setzen, oder Fremdfirmen, die die externe Aufbereitung von
Unternehmer ZAHNMEDIZIN Medizinprodukte Welches Ziel sollten Sie erreichen? Mitarbeiter, Patienten und Dritte ( Techniker, die ein Gerät instand setzen, oder Fremdfirmen, die die externe Aufbereitung von
Die Umsetzung des MPG in der Praxis. MP - Aufbereitung und Dokumentation
 Die Umsetzung des MPG in der Praxis MP - Aufbereitung und Dokumentation Entwicklung bis zu den aktuellen rechtlichen Grundlagen 13.12.2001 Medizin-Produkte-Gesetz MPG Neufassung 28.02.2002 MedizinProdukte-
Die Umsetzung des MPG in der Praxis MP - Aufbereitung und Dokumentation Entwicklung bis zu den aktuellen rechtlichen Grundlagen 13.12.2001 Medizin-Produkte-Gesetz MPG Neufassung 28.02.2002 MedizinProdukte-
Vorschlag zur Verfahrensweise bei der Überwachung ambulanter Behandlungseinrichtungen
 Vorschlag zur Verfahrensweise bei der Überwachung ambulanter Behandlungseinrichtungen Einleitung: Die ärztliche Praxis wird von verschiedenen Kontrollorganen überwacht. Diese Kontrollen dienen vor allem
Vorschlag zur Verfahrensweise bei der Überwachung ambulanter Behandlungseinrichtungen Einleitung: Die ärztliche Praxis wird von verschiedenen Kontrollorganen überwacht. Diese Kontrollen dienen vor allem
Prof. Dr. Reinier Mutters Institut für Medizinische Mikrobiologie und Hygiene Philipps-Universität Marburg Universitätsklinikum Gießen und Marburg
 Prof. Dr. Reinier Mutters Institut für Medizinische Mikrobiologie und Hygiene Philipps-Universität Marburg Universitätsklinikum Gießen und Marburg GmbH Bett ist eine der direkten Kontaktflächen kontaminiert
Prof. Dr. Reinier Mutters Institut für Medizinische Mikrobiologie und Hygiene Philipps-Universität Marburg Universitätsklinikum Gießen und Marburg GmbH Bett ist eine der direkten Kontaktflächen kontaminiert
Leitlinie zur Validierung maschineller Reinigungs- Desinfektionsprozesse. Aufbereitung thermolabiler Endoskope. supplement 3
 D 2596 F 19. Jahrgang 2011 3 supplement 3 Leitlinie zur Validierung maschineller Reinigungs- Desinfektionsprozesse zur Aufbereitung thermolabiler Endoskope D e u t s c h e G e s e l l s c h a f t f ü r
D 2596 F 19. Jahrgang 2011 3 supplement 3 Leitlinie zur Validierung maschineller Reinigungs- Desinfektionsprozesse zur Aufbereitung thermolabiler Endoskope D e u t s c h e G e s e l l s c h a f t f ü r
 Leistungsspektrum in Arztpraxen und ambulanten OP Zentren Chirurgie / Orthopädie - Bandnähte an großen und kleinen Gelenken - Gelenksspiegelungen - Hämorrhoidenentfernung - Leistenbrüche - Spaltung von
Leistungsspektrum in Arztpraxen und ambulanten OP Zentren Chirurgie / Orthopädie - Bandnähte an großen und kleinen Gelenken - Gelenksspiegelungen - Hämorrhoidenentfernung - Leistenbrüche - Spaltung von
Hygiene in der Praxis des niedergelassenen Arztes
 Hygiene in der Praxis des niedergelassenen Arztes - ordnungs- und haftungsrechtliche Aspekte - RA Dirk Benson Fachanwalt für Medizinrecht Haftungsrisiken bei Hygienenmängeln grds. Pat. beweisbelastet für
Hygiene in der Praxis des niedergelassenen Arztes - ordnungs- und haftungsrechtliche Aspekte - RA Dirk Benson Fachanwalt für Medizinrecht Haftungsrisiken bei Hygienenmängeln grds. Pat. beweisbelastet für
Validierung in der Praxis der Sterilgutversorgung
 Validierung in der Praxis der Sterilgutversorgung In Einrichtungen des Gesundheitswesen müssen die Aufbereitung von Medizinprodukten mit Validierten Verfahren erfolgen Qualitätsmanagementsysteme implementieren
Validierung in der Praxis der Sterilgutversorgung In Einrichtungen des Gesundheitswesen müssen die Aufbereitung von Medizinprodukten mit Validierten Verfahren erfolgen Qualitätsmanagementsysteme implementieren
Muster Nachweisdokumentation und Sicherheitsbewertungsbericht
 Muster Nachweisdokumentation und Sicherheitsbewertungsbericht auf Basis der "Verordnung (EG) Nr. 352/2009 der Kommission vom 24. April 2009 über die Festlegung einer gemeinsamen Sicherheitsmethode für
Muster Nachweisdokumentation und Sicherheitsbewertungsbericht auf Basis der "Verordnung (EG) Nr. 352/2009 der Kommission vom 24. April 2009 über die Festlegung einer gemeinsamen Sicherheitsmethode für
Kleindienst Consulting. Folie 1
 Systemgesteuerter Sterilgutkreislauf aus der Sicht von Anwender u. Kunden Real Time Dokumentation T-Q-M Optimierung der Prozessabläufe Kleindienst Consulting Folie 1 Von händischen zum High-tech Instrumenten
Systemgesteuerter Sterilgutkreislauf aus der Sicht von Anwender u. Kunden Real Time Dokumentation T-Q-M Optimierung der Prozessabläufe Kleindienst Consulting Folie 1 Von händischen zum High-tech Instrumenten
Leitfaden zu Gewinnung, Lagerung und Transport von Hygieneproben
 Leitfaden zu Gewinnung, Lagerung und Transport von Hygieneproben medizinisch chemisches Labor Dr. Mustafa, Dr. Richter OG Abteilung für Hygiene 5020 Salzburg, Bergstraße 14 tel: 0662 2205 fax: 0662 2205-421
Leitfaden zu Gewinnung, Lagerung und Transport von Hygieneproben medizinisch chemisches Labor Dr. Mustafa, Dr. Richter OG Abteilung für Hygiene 5020 Salzburg, Bergstraße 14 tel: 0662 2205 fax: 0662 2205-421
Neueste Entwicklungen in der Wiederaufbereitung von Medizinprodukten
 Neueste Entwicklungen in der Wiederaufbereitung von Medizinprodukten Freiburg, 11. Juni 2008 Andreas Schneider Steris AG, Pieterlen European Marketing Manager ZSVA Um was geht es?? Neuste Entwicklung bei
Neueste Entwicklungen in der Wiederaufbereitung von Medizinprodukten Freiburg, 11. Juni 2008 Andreas Schneider Steris AG, Pieterlen European Marketing Manager ZSVA Um was geht es?? Neuste Entwicklung bei
NORMEN Wunschvorstellung und Realität Ein Blick hinter die Kulissen
 NORMEN Wunschvorstellung und Realität Ein Blick hinter die Kulissen Mag. Dr. Tillo Miorini Institut für angewandte Hygiene ÖGSV Wozu Normen? Normen sollen den Stand der Technik repräsentieren Definieren
NORMEN Wunschvorstellung und Realität Ein Blick hinter die Kulissen Mag. Dr. Tillo Miorini Institut für angewandte Hygiene ÖGSV Wozu Normen? Normen sollen den Stand der Technik repräsentieren Definieren
VANGUARD Sterilgutversorgung: Häufig gestellte Fragen
 VANGUARD Sterilgutversorgung: Häufig gestellte Fragen 1. Wer ist die VANGUARD-Gruppe? VANGUARD ist eine international operierende Unternehmensgruppe, die sich auf innovative Dienstleistungen im Healthcare-Bereich
VANGUARD Sterilgutversorgung: Häufig gestellte Fragen 1. Wer ist die VANGUARD-Gruppe? VANGUARD ist eine international operierende Unternehmensgruppe, die sich auf innovative Dienstleistungen im Healthcare-Bereich
Wiederverwendung von Medizinprodukten und Einmalmedizinprodukten aus rechtlicher Sicht
 KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT IN KOOPERATION MIT BERLIN DÜSSELDORF Wiederverwendung von Medizinprodukten und Einmalmedizinprodukten aus rechtlicher Sicht 8. ZSVA-Forum
KANZLEI DR. JÄKEL MEDIZINRECHT ARZNEIMITTELRECHT MEDIZINPRODUKTERECHT IN KOOPERATION MIT BERLIN DÜSSELDORF Wiederverwendung von Medizinprodukten und Einmalmedizinprodukten aus rechtlicher Sicht 8. ZSVA-Forum
Zertifizierungsstellen für Qualitätsmanagementsysteme
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 15.08.2009 Hinweis:
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 15.08.2009 Hinweis:
Warum? Orthopäden; 5336. Dermatologen; 3342. Urologen; 2674. Chirurgen; 3976. Neurochirurgen; 491. Gynäkologen; 9875
 Können Medizinprodukte ohne CE-Kennzeichnung betrieben werden? Warum? Urologen; 2674 Neurochirurgen; 491 MKG; 1027 Allgemeinärzte/ praktische Ärzte; 40.246 Orthopäden; 5336 Chirurgen; 3976 Anästhesisten;
Können Medizinprodukte ohne CE-Kennzeichnung betrieben werden? Warum? Urologen; 2674 Neurochirurgen; 491 MKG; 1027 Allgemeinärzte/ praktische Ärzte; 40.246 Orthopäden; 5336 Chirurgen; 3976 Anästhesisten;
VDI-Richtlinie 5700 Risikomanagement der Aufbereitung von Medizinprodukten Maßnahmen zur Risikobeherrschung
 VDI-Richtlinie 5700 Risikomanagement der Aufbereitung von Medizinprodukten Maßnahmen zur Risikobeherrschung Prof. Dr.-Ing. Marc Kraft Fachgebiet Medizintechnik VDI und TU Berlin Fachgebiet Medizintechnik
VDI-Richtlinie 5700 Risikomanagement der Aufbereitung von Medizinprodukten Maßnahmen zur Risikobeherrschung Prof. Dr.-Ing. Marc Kraft Fachgebiet Medizintechnik VDI und TU Berlin Fachgebiet Medizintechnik
Fachkunde I Lehrgang. zur / zum. Technischen Sterilisationsassistentin / -assistenten. zur Aufbereitung von Medizinprodukten
 Fachkunde I Lehrgang zur / zum Technischen Sterilisationsassistentin / -assistenten zur Aufbereitung von Medizinprodukten Durch das Inkrafttreten des 2. Medizinprodukte-Änderungsgesetzes vom 01.01.2002,
Fachkunde I Lehrgang zur / zum Technischen Sterilisationsassistentin / -assistenten zur Aufbereitung von Medizinprodukten Durch das Inkrafttreten des 2. Medizinprodukte-Änderungsgesetzes vom 01.01.2002,
Aktuelle Ereignisse und Probleme im 17-ten Jahr nach der Einführung des MPG
 Aktuelle Ereignisse und Probleme im 17-ten Jahr nach der Einführung des MPG Sind in allen MP- Aufbereitungsabteilungen grundsätzliche Aspekte der Aufbereitung in Ordnung? Sind alle grundsätzlichen Probleme
Aktuelle Ereignisse und Probleme im 17-ten Jahr nach der Einführung des MPG Sind in allen MP- Aufbereitungsabteilungen grundsätzliche Aspekte der Aufbereitung in Ordnung? Sind alle grundsätzlichen Probleme
Abschnitt 1 Anwendungsbereich und Allgemeine Anforderungen an die Konformitätsbewertung 1 Anwendungsbereich
 13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
13.06.2007 Verordnung über Medizinprodukte - (Medizinprodukte-Verordnung - MPV)* vom 20. Dezember 2001 (BGBl. I S. 3854), zuletzt geändert durch Artikel 1 der Verordnung vom 16. Februar 2007 (BGBl. I S.
Zertifizierungsstellen für Qualitätsmanagementsysteme
 Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 01.05.2008 Hinweis:
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten Zertifizierungsstellen für Qualitätsmanagementsysteme Geltungsbereich DIN EN ISO 13485 : 2007 1 Stand 01.05.2008 Hinweis:
Hygienestrukturen in den Einrichtungen des Gesundheitswesens welche Kompetenz ist wo erforderlich?
 Hygienestrukturen in den Einrichtungen des Gesundheitswesens welche Kompetenz ist wo erforderlich? Karl-Heinz Stegemann -Fachkrpfl. für Hygiene und Infektionsprävention (RbP)- -Diplom-Pflegepädagoge- 1
Hygienestrukturen in den Einrichtungen des Gesundheitswesens welche Kompetenz ist wo erforderlich? Karl-Heinz Stegemann -Fachkrpfl. für Hygiene und Infektionsprävention (RbP)- -Diplom-Pflegepädagoge- 1
Anlage zur Akkreditierungsurkunde D-PL-13168-04-00 nach DIN EN ISO/IEC 17025:2005
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13168-04-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 22.07.2013 bis 21.07.2018 Ausstellungsdatum: 22.07.2013 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-PL-13168-04-00 nach DIN EN ISO/IEC 17025:2005 Gültigkeitsdauer: 22.07.2013 bis 21.07.2018 Ausstellungsdatum: 22.07.2013 Urkundeninhaber:
Medizinprodukterecht Umsetzung in der zahnärztlichen Praxis
 Medizinprodukterecht Umsetzung in der zahnärztlichen Praxis Zahnärztekammer Niedersachsen 03.06.2015 Behörde für Arbeits-, Umwelt- und Verbraucherschutz Dezernat 22 - Dipl.-Biol. Uta Schmidt / Dipl.-Ing.
Medizinprodukterecht Umsetzung in der zahnärztlichen Praxis Zahnärztekammer Niedersachsen 03.06.2015 Behörde für Arbeits-, Umwelt- und Verbraucherschutz Dezernat 22 - Dipl.-Biol. Uta Schmidt / Dipl.-Ing.
Wo liegt der Hygienelevel höher? OP Pharmaindustrie
 Wo liegt der Hygienelevel höher? OP Pharmaindustrie HFK Petra Dorfner HFK Susanna Grabmayer Wo liegt der Hygienelevel höher? Ziel Vorgaben Anforderungen Kontrollmöglichkeiten Gemeinsamkeiten/Unterschiede
Wo liegt der Hygienelevel höher? OP Pharmaindustrie HFK Petra Dorfner HFK Susanna Grabmayer Wo liegt der Hygienelevel höher? Ziel Vorgaben Anforderungen Kontrollmöglichkeiten Gemeinsamkeiten/Unterschiede
4 Medizinprodukte. 4.1 Aktive und nicht aktive Medizinprodukte. 4.2 Pflichten für Betreiber und Anwender von Medizinprodukten
 Medizinprodukte 4 4 Medizinprodukte 4 Medizinprodukte 4.1 Aktive und nicht aktive Medizinprodukte Definition Medizinprodukte Medizinprodukte sind Produkte zur medizinischen Zweckbestimmung, die vom Hersteller
Medizinprodukte 4 4 Medizinprodukte 4 Medizinprodukte 4.1 Aktive und nicht aktive Medizinprodukte Definition Medizinprodukte Medizinprodukte sind Produkte zur medizinischen Zweckbestimmung, die vom Hersteller
Hygienisch-mikrobiologische Überprüfung von flexiblen Endoskopen nach ihrer Aufbereitung
 » DGKH Hygienisch-mikrobiologische Überprüfung von flexiblen Endoskopen nach ihrer Aufbereitung Diese Empfehlung wird als Anlage in der noch nicht abgeschlossenen Leitlinie von DGKH, DGSV, DEGEA und AKI
» DGKH Hygienisch-mikrobiologische Überprüfung von flexiblen Endoskopen nach ihrer Aufbereitung Diese Empfehlung wird als Anlage in der noch nicht abgeschlossenen Leitlinie von DGKH, DGSV, DEGEA und AKI
Sicherstellung einer sachgerechten Aufbereitung von Medizinprodukten im niedergelassenen, ärztlichen Bereich
 Sicherstellung einer sachgerechten Aufbereitung von Medizinprodukten im niedergelassenen, ärztlichen Bereich Abschlussarbeit zum Fachkundelehrgang III für Leiter/innen der zentralen Sterilgutversorgung
Sicherstellung einer sachgerechten Aufbereitung von Medizinprodukten im niedergelassenen, ärztlichen Bereich Abschlussarbeit zum Fachkundelehrgang III für Leiter/innen der zentralen Sterilgutversorgung
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Materialien tierischen Ursprungs
 Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Materialien tierischen Ursprungs Geltungsbereich: Die vorliegenden Speziellen Regeln legen Anforderungen an Zertifizierungsstellen für
Spezielle Regeln für die Akkreditierung im Bereich Medizinprodukte Materialien tierischen Ursprungs Geltungsbereich: Die vorliegenden Speziellen Regeln legen Anforderungen an Zertifizierungsstellen für
Anlage zur Akkreditierungsurkunde D-ZE-16029-04-00 nach DIN EN ISO/IEC 17065:2013
 Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZE-16029-04-00 nach DIN EN ISO/IEC 17065:2013 Gültigkeitsdauer: 27.04.2016 bis 14.12.2019 Ausstellungsdatum: 27.04.2016 Urkundeninhaber:
Deutsche Akkreditierungsstelle GmbH Anlage zur Akkreditierungsurkunde D-ZE-16029-04-00 nach DIN EN ISO/IEC 17065:2013 Gültigkeitsdauer: 27.04.2016 bis 14.12.2019 Ausstellungsdatum: 27.04.2016 Urkundeninhaber:
PROTOKOLLE FÜR DIE VORDESINFEKTION, REINIGUNG UND STERILISATION ALLER ADAPTER VON PIERRE ROLLAND
 PROTOKOLLE FÜR DIE VORDESINFEKTION, REINIGUNG UND STERILISATION ALLER ADAPTER VON PIERRE ROLLAND E-Mail: satelec@acteongroup.com www.acteongroup.com Seite 1 von 8 Anweisungen für die Vordesinfektion, manuelle
PROTOKOLLE FÜR DIE VORDESINFEKTION, REINIGUNG UND STERILISATION ALLER ADAPTER VON PIERRE ROLLAND E-Mail: satelec@acteongroup.com www.acteongroup.com Seite 1 von 8 Anweisungen für die Vordesinfektion, manuelle
Übersicht Seminare 2015
 Glockenbruchweg 80 34134 Kassel Telefon: 0561 94175-0 www.pfaff-wassertechnik.de Übersicht Seminare 2015 Die Grünbeck Wasseraufbereitung GmbH bietet Ihnen bundesweit viele Seminare zu den Themen Wasseraufbereitung,
Glockenbruchweg 80 34134 Kassel Telefon: 0561 94175-0 www.pfaff-wassertechnik.de Übersicht Seminare 2015 Die Grünbeck Wasseraufbereitung GmbH bietet Ihnen bundesweit viele Seminare zu den Themen Wasseraufbereitung,
Medizinprodukterecht kompakt Anforderungen an Betreiber und Anwender. Dr. rer. nat. Isabella Nikolai-Gnisa - Bezirksregierung Köln
 Medizinprodukterecht kompakt Anforderungen an Betreiber und Anwender Dr. rer. nat. Isabella Nikolai-Gnisa - Bezirksregierung Köln Köln, 08. März 2013 Europäisches und nationales Medizinprodukterecht Zuständigkeit
Medizinprodukterecht kompakt Anforderungen an Betreiber und Anwender Dr. rer. nat. Isabella Nikolai-Gnisa - Bezirksregierung Köln Köln, 08. März 2013 Europäisches und nationales Medizinprodukterecht Zuständigkeit
Akkreditierungsumfang der Prüfstelle (EN ISO/IEC 17025:2005) HygCen Austria GmbH / (Ident.Nr.: 0196)
 1 2 3 4 5 6 7 8 02-030 11-001 16-009 16-010 17-008 DGHM Kapitel 14 DGHM Kapitel 15 DGHM Kapitel 17 2008-05 Prüfung der Reinigungswirkung chemothermischer Wäschedesinfektionsverfahren in den Wäschereien
1 2 3 4 5 6 7 8 02-030 11-001 16-009 16-010 17-008 DGHM Kapitel 14 DGHM Kapitel 15 DGHM Kapitel 17 2008-05 Prüfung der Reinigungswirkung chemothermischer Wäschedesinfektionsverfahren in den Wäschereien
MERKBLATT SPÜLEN, DESINFIZIEREN UND INBETRIEBNAHME VON TRINKWASSERINSTALLATIONEN
 MERKBLATT SPÜLEN, DESINFIZIEREN UND INBETRIEBNAHME VON TRINKWASSERINSTALLATIONEN Herausgeber: Zentralverband Sanitär Heizung Klima Rathausallee 6, 53757 St. Augustin Telefon: (02241) 9299-0 Telefax: (02241)
MERKBLATT SPÜLEN, DESINFIZIEREN UND INBETRIEBNAHME VON TRINKWASSERINSTALLATIONEN Herausgeber: Zentralverband Sanitär Heizung Klima Rathausallee 6, 53757 St. Augustin Telefon: (02241) 9299-0 Telefax: (02241)
