Eigenschaften der (Struktur)keramik
|
|
|
- Paulina Kalb
- vor 6 Jahren
- Abrufe
Transkript
1 Eigenschaften der (Struktur)keramik Vorteile: hohe Formstabilität niedrige Dichte hohe Härte chemische Beständigkeit Hochtemperaturbeständigkeit Biokompatibel Nachteile: begrenzte Duktilität niedrige Bruchdehnung niedrige Risszähigkeit streuende Festigkeitseigenschaften Thermoschockempfindlichkeit Woran liegt das? Bindung und Struktur 1
2 Bindung und Struktur Bindungstypen metallisch ionisch kovalent gemischt Typische Kristallstrukturen 2
3 Dichteste Kugelpackungen Kristallstruktur metallische Bindung (monoatomar) Kubisch flächenzentrierte EZ (Unit cell FCC) (Ag, Cu, Al, g-fe) Hexagonal dichtestgepackte EZ (Unit cell HCP) (Mg, Be, a-ti) Kubisch raumzentrierte EZ (Unit cell BCC) (W, Mo, Ta, a-fe) Quelle: W. Schatt, H. Worch: Werkstoffwissenschaft 3
4 Kristallstruktur ionische Bindung Zwei ineinander gestellte FCC Teilgitter (polyatomar) Die 8-ter Regel - Gilt für alle Bindungstypen! Quelle: IWE 4
5 Kristallstruktur ionische Bindung ionische Bindung - sterische Erklärung NaCl Ionenradienverhältnisse und Koordinationen Quelle: H. Salmang, H.Scholze: Keramik, Teil I 5
6 Kristallstruktur ionische Bindung r K /r A 0,85 0,51 0,45 Vergleich von experimentellen und berechneten Ionenabständen (nach Shannon und Prewitt / Werte in pm) Ionenradien bestimmen die Struktur Strukturvielfalt Eigenschaftsvielfalt Quelle: H. Salmang, H.Scholze: Keramik, Teil I 6
7 Kristallstruktur ionische Bindung ionische Bindung - physikalische Erklärung U e 2 z z N r 0 A BN 0 e r / CN 6 r 2,25N 0 h Coulomb, Born Meyer, van der Waals, Nullpunktsenergie U = Gitterenergie [J/mol] z = Ionenladung N 0 =Avogadro ρ = Abstoßungskoeffizient CN = Koordinierungszahl ν = Schwingungsfrequenz E = P an + P ab r 0 - Gleichgewichtsabstand Quelle: W. Schatt, H. Worch: Werkstoffwissenschaft 7
8 kovalent ionische Bindung Bindung:stark gerichtet geringe Symmetrie Die 8-ter Regel: Gilt für alle Bindungstypen! 8
9 kovalent ionische Bindung Typische Keramiken ionisch kovalent SiO 2 Si 3 N 4 SiC Elektronegativitätsdifferenz 1,54 1,14 0,65 Kovalenter Bindungsanteil [%] Mikrohärte [GPa] (fused quartz) 9
10 Ionischer Bindungsanteil kovalent ionische Bindung Keramiken weisen ionisch-kovalente Mischbindungen auf Mikrohärte [GPa] Elektronegativitätsdifferenz 10
11 Bindung - Bändermodell Bändermodell im Festkörper (für einen bestimmten Abstand r) Kann auf alle Bindungstypen übertragen werden! 11
12 Bindung - Bändermodell Hybridisierung Anti-Bindend Bindend Quelle: IWE 12
13 Bindung - Bändermodell Kristallrichtungs -Abhängigkeit der Bandstruktur Anisotropie wichtig für optische und elektrische Eigenschaften! Quelle: Handbook of Ceramics 13
14 Beispiel - Transparentkeramik sub-µm Sinterkorund (a-al 2 O 3 ) - hohe Festigkeit ( 4-pt = 700 MPa) - Transparenz - Anwendungen - Optik - Dental technology - Schneidwerkzeuge - Ballistik Dragunov test: Bändermodell a-al 2 O 3 (berechnet) Quelle: H. A. Rahnamaye Aliabad, Chin. Phys. B Vol. 24, No. 9 (2015) Al 2 O 3 beschichtetes Glas: d = 33 mm ~ 63 kg/m 2 Kugelsicheres Glas: d = 53 mm, ~ 108 kg/m 2 42% Gewichtseinsparung 14
15 Beispiel - Transparentkeramik Technologie: Hot Isostatic Pressing (HIP) P a P i - Nutzraum: D 300 mm x 450 mm P a >> P i P a = bar, P i 0 - Parameter: 2000 C, 2000 bar Ar 15
16 Kristall-Strukturen in der Keramik AB-Typen Zinkblende - Gitter Wurtzit - Gitter NaCl - Gitter eckenverknüpfte Tetraeder Schichtfolge: ABCABC ABAB Bsp: b- SiC Quelle: H. Salmang, H.Scholze: Keramik, Teil I Bsp: AlN Bsp: MgO, CaO, FeO 16
17 Kristall-Strukturen in der Keramik AB2-Typen SiO 2 TiO 2 CaF 2, ZrO 2, CeO 2 Kation KN Hoch-Cristobalit SiO 2 Tetraeder Rutil TiO 2 Oktaeder Fluorit CaF 2 Hexaeder Quelle: H. Salmang, H.Scholze: Keramik, Teil I 17
18 Kristall-Strukturen in der Keramik Tetraeder-Strukturen Möglichkeiten der Verknüpfung von [SiO 4 ] Tetraedern ( = Si 4+, = O 2- ) Quelle: H. Salmang, H.Scholze: Keramik, Teil I 18
19 Kristall-Strukturen in der Keramik Oktaeder-Strukturen flächenverknüpft (face sharing) kantenverknüpft (edge sharing) eckenverknüpft (corner sharing) hexagonales Bariumtitanat Rutil (AB 2 ) Perowskit (ABO 3 ) fig1_figure-3-cluster-aus-verknupften- Oktaedern-in-Subverbindungen-a-zwei
20 Kristall-Strukturen in der Keramik Oktaeder-Strukturen flächenverknüpft (face sharing) kantenverknüpft (edge sharing) eckenverknüpft (corner sharing) hexagonales Bariumtitanat Rutil (AB 2 ) Perowskit (ABO 3 ) Flächen-, kanten- und eckenverknüpfte Sauerstoffionenoktaeder im Ferroelektrikum BaTiO 3 (Perowskit-Struktur, e r = 2000) und in Rutil TiO 2 (e r = 100) 20
21 Kristall-Strukturen in der Keramik AB2-Typen Anwendungsbeispiel ZrO 2 = A-Kation: (kleines) Kation in jedem zweiten O- Würfel O-Anion: (großes) Anion bildet kubische Struktur Koordinationszahl: 8 (K) / 4 (A) Quelle:IWE 21
22 Verstärkungsmechanismen für Keramik Anwendungsbeispiel ZrO 2 - Verstärkungsmechanismen Umwandlungsstabilisierung für das System ZrO 2 Monoklin (RT) a = 515 nm b = 521 nm c = 532 nm b = Quelle: Salmang, Scholze: Keramik -8% Volumen- Änderung Tetragonal a = 364 nm c = 527 nm Kubisch (HT) a = 527 nm 22
23 Verstärkungsmechanismen für Keramik Umwandlungsstabilisierung für das System ZrO 2 Schmelze ca.2680 C Hochtemperaturform a-zro 2 (kubisch) ca.2300 C Hochtemperaturform b-zro 2 (tetragonal) Baddeleyit (RT) (monoklin) ca.1170 C r ~ 6,00 g/cm³ 8% Volumendehnung bei Abkühlung r ~ 5,56 g/cm³ Dilatometerkurven von ZrO 2 nach Curtis nicht-stabilisiertes reines ZrO 2 mit 5 mol-% CaO teilstabilisiertes ZrO 2 mit 19,8 mol-% CaO vollständig stabilisiertes ZrO 2 23
24 Verstärkungsmechanismen für Keramik Umwandlungsstabilisierung für das System ZrO 2 Phasendiagramm Yttriumoxid (Y 2 O 3 ) Zirkonoxid (ZrO 2 ) 24
25 Verstärkungsmechanismen für Keramik (a) Transformation zone ahead and around crack tip. K tip K a K s (b) Surface grinding induces the martensitic transformation, which in turn creates compressive surface layers and a concomitant increase in strength K s = shielding factor K s A' EV f T e w V f w Umwandlungs- Zone Quelle: Mechanical Properties, S. 384 Const (1) Umwandlungsdehnung 25
26 Kristall-Strukturen in der Keramik ABO 3 -Typen Quelle: IWE 26
27 Piezoelektrizität ABO 3 -Typen - Anwendungsbeispiel Ferroelektrika direkter piezoelektrischer Effekt: P j = d ij T i P j : Polarisation T i : (mech.) Spannung d ij : piezoelektrischer Verzerrungskoeffizient 27
28 Ferroelektrizität Anwendungsbeispiel Ferroelektrika Orientierungspolarisation Elementarzelle von Bariumtitanat (BaTiO 3 ) a) kubisch paraelektrisch (a = nm, T = 120 C > T C ), b) tetragonal ferroelektrisch (a = , c = nm, T = 20 C < T C ) 28
29 Ferroelektrizität Anwendungsbeispiel Ferroelektrika Polarisationskurve eines Ferroelektrikums Hysteresekurve Dehnungskurve eines Ferroelektrikums Schmetterlingskurve E C = Koerzitivfeldstärke, P S = Sättigungspolarisation P r = remanente Polarisation Permanenter Dipol 29
30 Ferroelektrizität Anwendungsbeispiel Ferroelektrika - Kondensatorwerkstoff (Dielektrikum) - Sensorik / Aktorik 30
31 Ferroelektrizität Anwendungsbeispiel Ferroelektrika T c T c Permittivität e vs. Temperatur Polarisation P vs. Temperatur Bei T C verschwindet P, aber nicht e! 31
32 Kristall-Strukturen in der Keramik AB 2 O 4 (AO B 2 O 3 )-Typen Spinell 32
33 Supraleiter AB 2 O 4 -Typen - Anwendungsbeispiel Supraleiter SBT = Strontium-Bismut-Tantalat (SrBi 2 Ta 2 O 9 ) Quelle: First principles study of polarization-strain coupling in SrBi2Ta2O9, Q. Yang et al., AIP Advances 3, (2013); doi: / YBCO = Yttrium-Barium-Kupferoxid (YBa 2 Cu 3 O 7 x ) 33
34 Supraleiter Keramische Supraleiter Oxidkeramische Supraleiter Metallische Supraleiter ( Fh Aalen) organische Supraleiter 34
35 Zusammenfassung Im Vergleich zu Metallen weisen Keramiken komplexere Strukturen auf In der Regel besitzen diese Strukturen eine geringere Symmetrie => weniger Gleitebenen, höhere Bindungsenergie Keramiken haben normalerweise keine Duktilität Bevor im Weiteren die mechanischen Eigenschaften behandelt werden, soll eine kurze Einführung in die elektrischen Eigenschaften erfolgen. 35
36 Ionen- und Elektronenleitung Ionen- und Elektronenleitung verschiedener Werkstoffe TiO 36
37 Ionen- und Elektronenleitung Elektrische Leitung, Stöchiometrie Warum sind Metalle Leiter (Bsp. Mg, Al)? Warum ist TiO 2 ein Isolator und thermodynamisch das stabilste Ti- Oxid? Warum ist Al 2 O 3 ein Isolator und thermodynamisch das stabilste Al-Oxid Welche Stöchiometrie haben Nb-Oxide, Zr-Oxide? Warum ist TiO ein elektronischer Leiter? Warum ist TiO 2-x, x<1 ein n-halbleiter? Warum ist ZnO ein Isolator? Warum ist ZnO 1-x ein n-hl? Leitfähigkeitsmechanismus LSM? Leitfähigkeitsmechanismus YSZ? 37
38 Ionen- und Elektronenleitung 38
39 Ionen- und Elektronenleitung Ionen- und Elektronenleitung verschiedener Werkstoffe TiO 39
40 Ionen- und Elektronenleitung Leitungsmechanismus Hopping-Leitung am Beispiel LaMnO 3 (Kathodenseite SOFC) hohe Temperatur notwendig! 40
41 Ionen- und Elektronenleitung Leitungsmechanismus Hopping-Leitung am Beispiel LaMnO 3 (Kathodenseite SOFC) Erhöhung der elektrischen Leitfähigkeit durch Dotierung mit Sr 2+ / Co 2+ 41
42 Ionen- und Elektronenleitung Ionenleitung im yttriumstabilisierten Zirkondioxid (YSZ) Ähnlicher Mechanismus wie für das Elektronen Hopping beim LSM aber beim YSZ findet ein Ionen-Hopping (Leerstellenwanderung) im chemischen Gradienten statt 42
43 Ionen- und Elektronenleitung Ionenleitung im yttriumstabilisierten Zirkondioxid (YSZ) 43
44 Ionen- und Elektronenleitung Ionenleitung im yttriumstabilisierten Zirkondioxid (YSZ) Leitfähigkeit in Abhängigkeit von der Dotierung 44
45 Ionen- und Elektronenleitung Ionenleitung im yttriumstabilisierten Zirkondioxid (YSZ) Leitfähigkeit in Abhängigkeit von der Temperatur 45
46 Ionen- und Elektronenleitung Anwendung Lambda-Sonde - Aufbau und Funktionsweise Abgas Pt 1 Pt 2 U U R T 4 F ln p p O2 II O2 I Lambda-Sonden Lambda < >1 R Gaskonstante F Faraday sche Konstante Die Sondenspannung (EMK) ist von der Temperatur (T) und den beiden O 2 - Partialdrücken im Abgas und Referenzgas abhängig. Pt wirkt als Katalysator (Oxidation bzw. Reduktion von Sauerstoff) 46
47 Sondenspannung / mv Ionen- und Elektronenleitung Anwendung Lambda-Sonde - Aufbau und Funktionsweise Regelung erfolgt um l=1 (stöchiometrische Verbrennung), da dort die stärkste Änderung des Sondensignals vorliegt. Regelung im Bereich <1 (fett) oder >1 (mager) mit diesem Sondentyp nicht möglich T-abhängigkeit >> Änderung der Sondenspannung Luft / Kraftstoff Verhältnis / l Temperaturabhängigkeit der l-sondenspannung 47
48 Ionen- und Elektronenleitung 48
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung
 Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Elementarzelle, Symmetrie, 7 Kristallsysteme, Zentrierte Elementarzellen, Salzstrukturen, NaCl-Struktur, AB-Strukturen, ZnS, CsCl, AB 2 -Strukturen,
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Elementarzelle, Symmetrie, 7 Kristallsysteme, Zentrierte Elementarzellen, Salzstrukturen, NaCl-Struktur, AB-Strukturen, ZnS, CsCl, AB 2 -Strukturen,
Thema heute: Aufbau fester Stoffe - Kristallographie
 Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Grundlagen der Chemie Polare Bindungen
 Polare Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektronegativität Unter der Elektronegativität
Polare Bindungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektronegativität Unter der Elektronegativität
A. N. Danilewsky 77. Inhalt von Kapitel 4
 A. N. Danilewsky 77 Inhalt von Kapitel 4 4 Kristallchemie... 78 4.1 Chemische Bindung und Koordination... 79 4.2 Konzept der dichtesten Kugelpackungen... 81 4.3 Strukturtypen... 84 4.3.1 Metalle... 84
A. N. Danilewsky 77 Inhalt von Kapitel 4 4 Kristallchemie... 78 4.1 Chemische Bindung und Koordination... 79 4.2 Konzept der dichtesten Kugelpackungen... 81 4.3 Strukturtypen... 84 4.3.1 Metalle... 84
Thema heute: Grundlegende Ionenstrukturen
 Wiederholung der letzten Vorlesungsstunde Einfache Metallstrukturen, Dichtestpackung von "Atomkugeln", N Oktaeder-, 2N Tetraederlücken, Hexagonal-dichte Packung, Schichtfolge ABAB, hexagonale Elementarzelle,
Wiederholung der letzten Vorlesungsstunde Einfache Metallstrukturen, Dichtestpackung von "Atomkugeln", N Oktaeder-, 2N Tetraederlücken, Hexagonal-dichte Packung, Schichtfolge ABAB, hexagonale Elementarzelle,
Wiederholung der letzten Vorlesungsstunde:
 Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Koordinationspolyeder, ionische Strukturen, NaCl, CsCl, ZnS, Elementarzelle, Gitter, Gitterkonstanten, 7 Kristallsysteme, Ionenradien, Gitterenergie
Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Koordinationspolyeder, ionische Strukturen, NaCl, CsCl, ZnS, Elementarzelle, Gitter, Gitterkonstanten, 7 Kristallsysteme, Ionenradien, Gitterenergie
Chemische Bindung. Wie halten Atome zusammen? Welche Atome können sich verbinden? Febr 02
 Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Chemische Bindung locker bleiben Wie halten Atome zusammen? positiv Welche Atome können sich verbinden? power keep smiling Chemische Bindung Die chemischen Reaktionen spielen sich zwischen den Hüllen der
Typische Eigenschaften von Metallen
 Typische Eigenschaften von Metallen hohe elektrische Leitfähigkeit (nimmt mit steigender Temperatur ab) hohe Wärmeleitfähigkeit leichte Verformbarkeit metallischer Glanz Elektronengas-Modell eines Metalls
Typische Eigenschaften von Metallen hohe elektrische Leitfähigkeit (nimmt mit steigender Temperatur ab) hohe Wärmeleitfähigkeit leichte Verformbarkeit metallischer Glanz Elektronengas-Modell eines Metalls
Wiederholung der letzten Vorlesungsstunde. Thema heute: Weitere Grundlegende Ionenstrukturen
 Wiederholung der letzten Vorlesungsstunde Einfache Ionengitter, abgeleitet von kubisch-dichten Ionenpackungen: NaCl, CaF 2, Li 2 O, inverse Strukturtypen, ZnS (Zinkblende), Li 3 Bi, Strukturvarianten:
Wiederholung der letzten Vorlesungsstunde Einfache Ionengitter, abgeleitet von kubisch-dichten Ionenpackungen: NaCl, CaF 2, Li 2 O, inverse Strukturtypen, ZnS (Zinkblende), Li 3 Bi, Strukturvarianten:
Quantenzahlen. Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale.
 Quantenzahlen Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale. l = 0, 1, 2, 3, (Orbital-)Symbol s, p, d, f, Zahl der Orbitale
Quantenzahlen Magnetquantenzahl m => entspricht der Zahl und Orien- (m = -l, -(l-1) 0 +(l-1), +l) tierung der Orbitale in jeder Unterschale. l = 0, 1, 2, 3, (Orbital-)Symbol s, p, d, f, Zahl der Orbitale
3. Struktur des Festkörpers
 3. Struktur des Festkörpers 3.1 Kristalline und amorphe Strukturen Amorphe Struktur - Atombindung ist gerichtet - unregelmäßige Anordnung der Atome - keinen exakten Schmelzpunkt, sondern langsames Erweichen,
3. Struktur des Festkörpers 3.1 Kristalline und amorphe Strukturen Amorphe Struktur - Atombindung ist gerichtet - unregelmäßige Anordnung der Atome - keinen exakten Schmelzpunkt, sondern langsames Erweichen,
Einfache Kristallstrukturen
 Einfache Kristallstrukturen Konstruktion von Kristallen: Kugelpackungen - hexagonal und kubisch dichteste Packungen - kubisch einfache Packung - kubisch innenzentrierte Packung Kristallstrukturen der Metalle
Einfache Kristallstrukturen Konstruktion von Kristallen: Kugelpackungen - hexagonal und kubisch dichteste Packungen - kubisch einfache Packung - kubisch innenzentrierte Packung Kristallstrukturen der Metalle
Grundlagen der Chemie
 1 Die Metallbindung Hartstoffe 75% aller chemischen Elemente sind. Typische Eigenschaften: 1. Die Absorption für sichtbares Licht ist hoch. Hieraus folgt das große Spiegelreflexionsvermögen. Das ist die
1 Die Metallbindung Hartstoffe 75% aller chemischen Elemente sind. Typische Eigenschaften: 1. Die Absorption für sichtbares Licht ist hoch. Hieraus folgt das große Spiegelreflexionsvermögen. Das ist die
Magische Kristalle Prof. Dr. R. Glaum
 Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Grundlagen der Chemie Metalle
 Metalle Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Metalle 75% aller chemischen Elemente sind Metalle. Typische
Metalle Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Metalle 75% aller chemischen Elemente sind Metalle. Typische
Einführung in die Kristallographie
 Einführung in die Kristallographie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Brennhausgasse 14 03731-39-2665 oder -2628 gerhard.heide@mineral.tu-freiberg.de
Einführung in die Kristallographie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Brennhausgasse 14 03731-39-2665 oder -2628 gerhard.heide@mineral.tu-freiberg.de
Übungsaufgaben zur Vorlesung Chemie der Materialien
 Übungsaufgaben zur Vorlesung Chemie der Materialien Aufgabe 1: a) Was ist die Referenz für die Mohs Härteskala? b) Ordnen Sie die folgenden Festkörper nach ihrer Härte auf der Skala: Korund, Graphit, CaF
Übungsaufgaben zur Vorlesung Chemie der Materialien Aufgabe 1: a) Was ist die Referenz für die Mohs Härteskala? b) Ordnen Sie die folgenden Festkörper nach ihrer Härte auf der Skala: Korund, Graphit, CaF
Metalloxide: Vom Rost zum High-Tech-Werkstoff
 Physik am Samstag, 01-07-2006 Metalloxide: Vom Rost zum High-Tech-Werkstoff ep4 Universität Ralph Claessen Experimentelle Physik IV Physikalisches Institut Universität Warum Metalloxide? Elementhäufigkeit
Physik am Samstag, 01-07-2006 Metalloxide: Vom Rost zum High-Tech-Werkstoff ep4 Universität Ralph Claessen Experimentelle Physik IV Physikalisches Institut Universität Warum Metalloxide? Elementhäufigkeit
Präparation. 1) Spaltung: Materialien: Alkalihalogenide (NaCl, KBr) Erdalkali (CaF 2. ) Oxide (MgO) Halbleiter (GaAs) Brechen Glas Bruchflächen amorph
 Oberflächenphysik 19.2. Vacuum technique [vapour pressure, Langmuir, pumps] 26.2. Structure, relaxations and reconstructions 4. 3. Diffractionsmethods: LEED, He atom scattering, grazing X-ray, ions 11.
Oberflächenphysik 19.2. Vacuum technique [vapour pressure, Langmuir, pumps] 26.2. Structure, relaxations and reconstructions 4. 3. Diffractionsmethods: LEED, He atom scattering, grazing X-ray, ions 11.
Konzepte der anorganischen und analytischen Chemie II II
 Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
Konzepte der anorganischen und analytischen Chemie II II Marc H. Prosenc Inst. für Anorganische und Angewandte Chemie Tel: 42838-3102 prosenc@chemie.uni-hamburg.de Outline Einführung in die Chemie fester
4.2 Metallkristalle. 4.2.1 Bindungsverhältnisse
 4.2 Metallkristalle - 75 % aller Elemente sind Metalle - hohe thermische und elektrische Leitfähigkeit - metallischer Glanz - Duktilität (Zähigkeit, Verformungsvermögen): Fähigkeit eines Werkstoffs, sich
4.2 Metallkristalle - 75 % aller Elemente sind Metalle - hohe thermische und elektrische Leitfähigkeit - metallischer Glanz - Duktilität (Zähigkeit, Verformungsvermögen): Fähigkeit eines Werkstoffs, sich
Anorganische Chemie III
 Seminar zu Vorlesung Anorganische Chemie III Wintersemester 01/13 Christoph Wölper Universität Duisburg-Essen Koordinationszahlen Ionenradien # dichteste Packung mit 1 Nachbarn -> in Ionengittern weniger
Seminar zu Vorlesung Anorganische Chemie III Wintersemester 01/13 Christoph Wölper Universität Duisburg-Essen Koordinationszahlen Ionenradien # dichteste Packung mit 1 Nachbarn -> in Ionengittern weniger
Chemische Bindung. Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung
 Chemische Bindung Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung 1 Was sind Ionen? Ein Ion besteht aus einem oder mehreren Atomen und hat elektrische Ladung Kationen
Chemische Bindung Ionenbindung (heteropolare Bindung) kovalente Bindung van-der-waals-bindung Metallbindung 1 Was sind Ionen? Ein Ion besteht aus einem oder mehreren Atomen und hat elektrische Ladung Kationen
Grundzüge der Keramik
 Grundzüge der Keramik Skript zur Vorlesung Ingenieurkeramik I Professur für nichtmetallische Werkstoffe ETH Zürich Jens Helbig Urs Schönholzer Ausgabe 2001 Titelbild Aluminate aus seltenen Erden in einer
Grundzüge der Keramik Skript zur Vorlesung Ingenieurkeramik I Professur für nichtmetallische Werkstoffe ETH Zürich Jens Helbig Urs Schönholzer Ausgabe 2001 Titelbild Aluminate aus seltenen Erden in einer
Kleines Repetitorium zur Vorlesung Werkstoffkunde für E-Techniker (Prof. Dr. A. Winnacker)
 Kleines Repetitorium zur Vorlesung Werkstoffkunde für E-Techniker (Prof. Dr. A. Winnacker) WET Kapitel 1 - Mechanische Eigenschaften von Festkörpern Skizzieren Sie ein Spannungs-Dehnungs-Diagramm (Bezeichnungen
Kleines Repetitorium zur Vorlesung Werkstoffkunde für E-Techniker (Prof. Dr. A. Winnacker) WET Kapitel 1 - Mechanische Eigenschaften von Festkörpern Skizzieren Sie ein Spannungs-Dehnungs-Diagramm (Bezeichnungen
Wie entstehen Gläser? Glasbildung ist verhinderte Kristallisation. Glas ist eine eingefrorene unterkühlte Schmelze. metastabil
 6.3 Gläser - seit 5000 Jahren - 100 Mio t/a - Deutschland: 3 Mio t Recycling-Anteil > 70% - 90% Kalk-Natron-Glas - auch metallische Gläser und andere Stoffe im Glaszustand Wie entstehen Gläser? Glasbildung
6.3 Gläser - seit 5000 Jahren - 100 Mio t/a - Deutschland: 3 Mio t Recycling-Anteil > 70% - 90% Kalk-Natron-Glas - auch metallische Gläser und andere Stoffe im Glaszustand Wie entstehen Gläser? Glasbildung
3.4. Leitungsmechanismen
 a) Metalle 3.4. Leitungsmechanismen - Metall besteht aus positiv geladenen Metallionen und frei beweglichen Leitungselektronen (freie Elektronengas), Bsp.: Cu 2+ + 2e - - elektrische Leitung durch freie
a) Metalle 3.4. Leitungsmechanismen - Metall besteht aus positiv geladenen Metallionen und frei beweglichen Leitungselektronen (freie Elektronengas), Bsp.: Cu 2+ + 2e - - elektrische Leitung durch freie
Erwin Riedel, Christoph Jan. Übungsbuch. Allgemeine und Anorganische Chemie. 3. Auflage DE GRUYTER
 Erwin Riedel, Christoph Jan Übungsbuch Allgemeine und Anorganische Chemie 3. Auflage DE GRUYTER Isolatoren Orbitale Elektronenaffinität Halbleiter Lewis-Formeln Leuchtdioden Formale Fragen 1. Atombau 3
Erwin Riedel, Christoph Jan Übungsbuch Allgemeine und Anorganische Chemie 3. Auflage DE GRUYTER Isolatoren Orbitale Elektronenaffinität Halbleiter Lewis-Formeln Leuchtdioden Formale Fragen 1. Atombau 3
Annette-Kolb-Gymnasium Traunstein Grundwissen der 9. Klasse für das Fach Chemie Aufgaben und Antworten
 1 Erkläre den Aufbau von Atomen und Ionen aus den Elementarteilchen: (Bsp. 23 Na, 1 H, 35 Cl - ). 2 Erläutere den Beriff Edelaskonfiuration und beschreibe, welche verschiedenen Mölichkeiten die Elemente
1 Erkläre den Aufbau von Atomen und Ionen aus den Elementarteilchen: (Bsp. 23 Na, 1 H, 35 Cl - ). 2 Erläutere den Beriff Edelaskonfiuration und beschreibe, welche verschiedenen Mölichkeiten die Elemente
Übungen zur Allgemeinen Geologie, Nebenfach. Erta Ale, Afrika
 Übungen zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Minerale anorganisch, (natürlich) Festkörper definierte chemische Zusammensetzung homogen definiert durch chemische Formel kristallin Physikalische
Übungen zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Minerale anorganisch, (natürlich) Festkörper definierte chemische Zusammensetzung homogen definiert durch chemische Formel kristallin Physikalische
3. Cluster und Nanopartikel. Cluster: Anzahl von Atomen und Struktur ist wohldefiniert Nanopartikel: Anzahl von Atomen nicht genau bestimmt
 3. Cluster und Nanopartikel Cluster: Anzahl von Atomen und Struktur ist wohldefiniert Nanopartikel: Anzahl von Atomen nicht genau bestimmt 1 Struktur ist grössenabhängig Bsp.: Au-Cluster Erst große Cluster
3. Cluster und Nanopartikel Cluster: Anzahl von Atomen und Struktur ist wohldefiniert Nanopartikel: Anzahl von Atomen nicht genau bestimmt 1 Struktur ist grössenabhängig Bsp.: Au-Cluster Erst große Cluster
Der Schmelzpunkt von Salzen
 Der Schmelzpunkt von Salzen Vergleich die Smp. der Salze (links). Welche Rolle könnten die Ionenradien bzw. die Ladung der enthaltenen Ionen spielen? Der Schmelzpunkt von Salzen ist i.d.r. sehr hoch. Er
Der Schmelzpunkt von Salzen Vergleich die Smp. der Salze (links). Welche Rolle könnten die Ionenradien bzw. die Ladung der enthaltenen Ionen spielen? Der Schmelzpunkt von Salzen ist i.d.r. sehr hoch. Er
Kristallstruktur der Metalle
 Bedeutung Metallische Werkstoffe sind in der Regel kristallin aufgebaut. Die vorliegende Kristallstruktur hat einen erheblichen Einfluss auf die Eigenschaften des Werkstoffs, wie z.b. die Festigkeit, Verformbarkeit,
Bedeutung Metallische Werkstoffe sind in der Regel kristallin aufgebaut. Die vorliegende Kristallstruktur hat einen erheblichen Einfluss auf die Eigenschaften des Werkstoffs, wie z.b. die Festigkeit, Verformbarkeit,
3.1 Der Schmelzpunkt. Ionische Verbindungen
 Materialwissenschaft I - Keramik-Kapitel 3 3-1 3 Das Bindungspotential und einige physikalische Eigenschaften Die Bindungskräfte zwischen den Ionen oder Atomen in einem Festkörper bestimmen viele seiner
Materialwissenschaft I - Keramik-Kapitel 3 3-1 3 Das Bindungspotential und einige physikalische Eigenschaften Die Bindungskräfte zwischen den Ionen oder Atomen in einem Festkörper bestimmen viele seiner
Einführung in die Technische Keramik. Bild 1: Anlaufspur einer Sommerski-Sprungschanze - ein Polymer / Keramik Verbundsystem
 2.2 Anforderungen an und Eigenschaften von keramischen Bauteilen Dr. Hans Hoppert ETEC Technische Keramik GmbH Lohmar Die Folien finden Sie ab Seite 74. Warum Keramik? Werkstoffe und ihre Eigenschaften
2.2 Anforderungen an und Eigenschaften von keramischen Bauteilen Dr. Hans Hoppert ETEC Technische Keramik GmbH Lohmar Die Folien finden Sie ab Seite 74. Warum Keramik? Werkstoffe und ihre Eigenschaften
Neue Glaskeramiken mit negativer thermischer Ausdehnung im System BaO-Al 2 O 3 -B 2 O 3
 Neue Glaskeramiken mit negativer thermischer Ausdehnung im System BaO-Al 2 O 3 -B 2 O 3 Christian Rüssel Ralf Keding Diana Tauch Otto-Schott-Institut Universität Jena Glaskeramiken System BaO-Al 2 O 3
Neue Glaskeramiken mit negativer thermischer Ausdehnung im System BaO-Al 2 O 3 -B 2 O 3 Christian Rüssel Ralf Keding Diana Tauch Otto-Schott-Institut Universität Jena Glaskeramiken System BaO-Al 2 O 3
Einführung in Werkstoffkunde
 Einführung in Werkstoffkunde Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Dr.-Ing. Norbert Hort norbert.hort@gkss.de Inhalte Über mich Einführung Aufbau von Werkstoffen Physikalische
Einführung in Werkstoffkunde Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Dr.-Ing. Norbert Hort norbert.hort@gkss.de Inhalte Über mich Einführung Aufbau von Werkstoffen Physikalische
Übungsblatt 3 (10.06.2011)
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 0 Übungsblatt (0.06.0 Wärmedämmung Ein Verbundfenster der Fläche A =.0 m besteht aus zwei Glasscheiben der Dicke d =.5 mm, zwischen
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 0 Übungsblatt (0.06.0 Wärmedämmung Ein Verbundfenster der Fläche A =.0 m besteht aus zwei Glasscheiben der Dicke d =.5 mm, zwischen
Einführung in Werkstoffkunde Aufbau von Werkstoffen
 Einführung in Werkstoffkunde Aufbau von Werkstoffen Dr.-Ing. Norbert Hort norbert.hort@gkss.de Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Inhalte Über mich Herstellung,
Einführung in Werkstoffkunde Aufbau von Werkstoffen Dr.-Ing. Norbert Hort norbert.hort@gkss.de Magnesium Innovations Center (MagIC) GKSS Forschungszentrum Geesthacht GmbH Inhalte Über mich Herstellung,
Phasendiagramme. Seminar zum Praktikum Modul ACIII
 Phasendiagramme Seminar zum Praktikum Modul ACIII Definition Phase Eine Phase ist ein Zustand der Materie, in dem sie bezüglich ihrer chemischen Zusammensetzung und bezüglich ihres physikalischen Zustandes
Phasendiagramme Seminar zum Praktikum Modul ACIII Definition Phase Eine Phase ist ein Zustand der Materie, in dem sie bezüglich ihrer chemischen Zusammensetzung und bezüglich ihres physikalischen Zustandes
Die Avogadro-Konstante N A
 Die Avogadro-Konstante N A Das Ziel der folgenden Seiten ist es, festzustellen, wie viele Atome pro cm³ oder pro g in einem Stoff enthalten sind. Chemische Reaktionen zwischen Gasen (z.b. 2H 2 + O 2 2
Die Avogadro-Konstante N A Das Ziel der folgenden Seiten ist es, festzustellen, wie viele Atome pro cm³ oder pro g in einem Stoff enthalten sind. Chemische Reaktionen zwischen Gasen (z.b. 2H 2 + O 2 2
0.3 Formeln, Gleichungen, Reaktionen
 0.3 Formeln, Gleichungen, Reaktionen Aussage von chemischen Formeln Formeln von ionischen Verbindungen - Metallkation, ein- oder mehratomiges Anion - Formel entsteht durch Ausgleich der Ladungen - Bildung
0.3 Formeln, Gleichungen, Reaktionen Aussage von chemischen Formeln Formeln von ionischen Verbindungen - Metallkation, ein- oder mehratomiges Anion - Formel entsteht durch Ausgleich der Ladungen - Bildung
2. Einführung in die Technische Keramik
 2. Einführung in die Technische Keramik 2.1 Werkstoffe, Eigenschaften und resultierende Anwendungen Heidrun Grycz Saint Gobain Advanced Ceramics Lauf GmbH Lauf a. d. Pegnitz Elke Vitzthum CeramTec AG Lauf
2. Einführung in die Technische Keramik 2.1 Werkstoffe, Eigenschaften und resultierende Anwendungen Heidrun Grycz Saint Gobain Advanced Ceramics Lauf GmbH Lauf a. d. Pegnitz Elke Vitzthum CeramTec AG Lauf
Stoffeigenschaften und Teilchenmodell
 Stoffeigenschaften und Teilchenmodell Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser
Stoffeigenschaften und Teilchenmodell Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser
22. Chemische Bindungen
 .05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
.05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
Grundlagen der Festkörperchemie
 Grundlagen der Festkörpercheie 1. Der feste Aggregatzustand Aggregatzustand Beständigkeit Ordnung Voluen For gas (g) - - - flüssig (l) + - Teilordnung fest (s) + + + akroskopisch subikrokopisch - ideales
Grundlagen der Festkörpercheie 1. Der feste Aggregatzustand Aggregatzustand Beständigkeit Ordnung Voluen For gas (g) - - - flüssig (l) + - Teilordnung fest (s) + + + akroskopisch subikrokopisch - ideales
Ideale und Reale Gase. Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig)
 Ideale und Reale Gase Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig) Wann sind reale Gase ideal? Reale Gase verhalten sich wie ideale Gase
Ideale und Reale Gase Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig) Wann sind reale Gase ideal? Reale Gase verhalten sich wie ideale Gase
Arten chemischer Bindungen
 Arten chemischer Bindungen Bindungsarten Atombindung (Kovalenzbindung) Ionenbindung Metallbindung Bindung in Komplexen Intermolekulare Wechselwirkungen polar unpolar Wasserstoffbrückenbindung Van-der-Waals-
Arten chemischer Bindungen Bindungsarten Atombindung (Kovalenzbindung) Ionenbindung Metallbindung Bindung in Komplexen Intermolekulare Wechselwirkungen polar unpolar Wasserstoffbrückenbindung Van-der-Waals-
Optische Eigenschaften metallischer und dielektrischer Dünnfilme bei der Ionenstrahlbeschichtung
 Optische Eigenschaften metallischer und dielektrischer Dünnfilme bei der Ionenstrahlbeschichtung C. Bundesmann, I.-M. Eichentopf, S. Mändl, H. Neumann, Permoserstraße15, Leipzig, D-04318, Germany 1 Inhalt
Optische Eigenschaften metallischer und dielektrischer Dünnfilme bei der Ionenstrahlbeschichtung C. Bundesmann, I.-M. Eichentopf, S. Mändl, H. Neumann, Permoserstraße15, Leipzig, D-04318, Germany 1 Inhalt
Fachinfo und Werkstoffüberblick
 Fachinfo und Werkstoffüberblick info@herbstkeramik.de Tel: 035026/91275 Dipl. Ing. (FH) Robin Herbst (unser kleines ABC der wichtigsten Begriffe, der von uns verwendeten Werkstoffe sowie der Materialeigenschaften)
Fachinfo und Werkstoffüberblick info@herbstkeramik.de Tel: 035026/91275 Dipl. Ing. (FH) Robin Herbst (unser kleines ABC der wichtigsten Begriffe, der von uns verwendeten Werkstoffe sowie der Materialeigenschaften)
Klausur Vertiefungsfach 2: Master
 I E H K Institut für Eisenhüttenkunde Rheinisch-Westfälische Technische Hochschule Aachen Klausur Vertiefungsfach 2: Master Stahlmetallurgie Univ.-Prof. Dr.-Ing. D. Senk 10.09.2012 Nachname, Vorname: Matrikel-Nr.:
I E H K Institut für Eisenhüttenkunde Rheinisch-Westfälische Technische Hochschule Aachen Klausur Vertiefungsfach 2: Master Stahlmetallurgie Univ.-Prof. Dr.-Ing. D. Senk 10.09.2012 Nachname, Vorname: Matrikel-Nr.:
Geochemie-I Fragenkatalog zur Klausurvorbereitung
 Geochemie-I Fragenkatalog zur Klausurvorbereitung 1) Chemische Eigenschaften der Elemente Wodurch ist ein Element charakterisiert/definiert? Was ist ein Isotop? Was bestimmt die chemischen Eigenschaften
Geochemie-I Fragenkatalog zur Klausurvorbereitung 1) Chemische Eigenschaften der Elemente Wodurch ist ein Element charakterisiert/definiert? Was ist ein Isotop? Was bestimmt die chemischen Eigenschaften
Bindung in Kohlenwasserstoffmolekülen
 Bindung in Kohlenwasserstoffmolekülen Die Kohlenstoffbindungen im Vergleich Bindung Bindungsstärke Differenz Bindungslänge [kj/mol] [pm] H-H 430 74 C-H 413-17 109 C-C 348 154 C=C 614 + 266 134 C C 839
Bindung in Kohlenwasserstoffmolekülen Die Kohlenstoffbindungen im Vergleich Bindung Bindungsstärke Differenz Bindungslänge [kj/mol] [pm] H-H 430 74 C-H 413-17 109 C-C 348 154 C=C 614 + 266 134 C C 839
EOS StainlessSteel 316L
 EOS StainlessSteel 316L Typische Anwedung StainlessSteel 316L ist eine korrosionsresistente, auf Eisen basierende Legierung. Bauteile aus Stainless Steel 316L entsprechen in ihrer chemischen Zusammensetzung
EOS StainlessSteel 316L Typische Anwedung StainlessSteel 316L ist eine korrosionsresistente, auf Eisen basierende Legierung. Bauteile aus Stainless Steel 316L entsprechen in ihrer chemischen Zusammensetzung
Bandstrukturen - leicht gemacht
 Bandstrukturen - leicht gemacht Eva Haas Stephanie Rošker Juni 2009 Projekt Festkörperphysik Inhaltsverzeichnis 1 Bandstrukturen 3 2 Energiebänder 3 3 Brillouin-Zonen - eine Übersicht 7 4 Beispiele 8 4.1
Bandstrukturen - leicht gemacht Eva Haas Stephanie Rošker Juni 2009 Projekt Festkörperphysik Inhaltsverzeichnis 1 Bandstrukturen 3 2 Energiebänder 3 3 Brillouin-Zonen - eine Übersicht 7 4 Beispiele 8 4.1
Chemische Bindungsanalyse in Festkörpern
 Fakultät Mathematik und Naturwissenschaften Fachrichtung Chemie und Lebensmittel Chemie Professur AC2 Dr. Alexey I. Baranov Chemische Bindungsanalyse in Festkörpern Sommersemester 2015 Bindung in Orbitaldarstellung:
Fakultät Mathematik und Naturwissenschaften Fachrichtung Chemie und Lebensmittel Chemie Professur AC2 Dr. Alexey I. Baranov Chemische Bindungsanalyse in Festkörpern Sommersemester 2015 Bindung in Orbitaldarstellung:
Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte Packung, Raumausfüllung, Ionenstrukturen - abgeleitet von Ionendichtestpackungen,
 Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Elektrische Leitung. Strom
 lektrische Leitung 1. Leitungsmechanismen Bändermodell 2. Ladungstransport in Festkörpern i) Temperaturabhängigkeit Leiter ii) igen- und Fremdleitung in Halbleitern iii) Stromtransport in Isolatoren iv)
lektrische Leitung 1. Leitungsmechanismen Bändermodell 2. Ladungstransport in Festkörpern i) Temperaturabhängigkeit Leiter ii) igen- und Fremdleitung in Halbleitern iii) Stromtransport in Isolatoren iv)
Einheiten und Einheitenrechnungen
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Chemie für Biologen Vorlesung im WS 200/05 V2, Mi 10-12, S0 T01 A02 Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen (Teil : 03.11.200) MILESS: Chemie für Biologen 66 Chemische
Kapitel 2. Eigenschaften des Siliziums und seiner Oxide
 Kapitel 2. Eigenschaften des Siliziums und seiner Oxide 2.1. Silizium Silizium ist nach dem Sauerstoff das meistverbreitete Element auf der Erde. Wegen seiner großen Sauerstoffaffinität kommt Silizium
Kapitel 2. Eigenschaften des Siliziums und seiner Oxide 2.1. Silizium Silizium ist nach dem Sauerstoff das meistverbreitete Element auf der Erde. Wegen seiner großen Sauerstoffaffinität kommt Silizium
VIOSIL SQ FUSED SILICA (SYNTHETISCHES QUARZGLAS)
 VIOSIL SQ FUSED SILICA (SYNTHETISCHES QUARZGLAS) Beschreibung VIOSIL SQ wird von ShinEtsu in Japan hergestellt. Es ist ein sehr klares (transparentes) und reines synthetisches Quarzglas. Es besitzt, da
VIOSIL SQ FUSED SILICA (SYNTHETISCHES QUARZGLAS) Beschreibung VIOSIL SQ wird von ShinEtsu in Japan hergestellt. Es ist ein sehr klares (transparentes) und reines synthetisches Quarzglas. Es besitzt, da
Viskosität und Formgebung von Glas
 Viskosität und Formgebung von Glas Stefan Kuhn Stefan.Kuhn@uni-jena.de Tel.: (9)48522 1.1 Zielstellung In diesem Praktikum soll der Flieÿpunkt der im Praktikumsversuch Schmelzen von Glas hergestellten
Viskosität und Formgebung von Glas Stefan Kuhn Stefan.Kuhn@uni-jena.de Tel.: (9)48522 1.1 Zielstellung In diesem Praktikum soll der Flieÿpunkt der im Praktikumsversuch Schmelzen von Glas hergestellten
Theoretische Modellierung von experimentell ermittelten Infrarot-Spektren
 Sitzung des AK-Thermophysik am 24./25. März 211 Theoretische Modellierung von experimentell ermittelten Infrarot-Spektren M. Manara, M. Arduini-Schuster, N. Wolf, M.H. Keller, M. Rydzek Bayerisches Zentrum
Sitzung des AK-Thermophysik am 24./25. März 211 Theoretische Modellierung von experimentell ermittelten Infrarot-Spektren M. Manara, M. Arduini-Schuster, N. Wolf, M.H. Keller, M. Rydzek Bayerisches Zentrum
Metallbindung und Metalle Ionenbindung und Salze
 Metallbindung und Metalle Ionenbindung und Salze Patrick Bucher 18. Juli 2011 Inhaltsverzeichnis 1 Metalle 1 1.1 Metallgitter und metallische Bindung...................... 2 1.2 Chemische Eigenschaften
Metallbindung und Metalle Ionenbindung und Salze Patrick Bucher 18. Juli 2011 Inhaltsverzeichnis 1 Metalle 1 1.1 Metallgitter und metallische Bindung...................... 2 1.2 Chemische Eigenschaften
Christian-Ernst-Gymnasium
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und en Element kann chemisch nicht mehr zerlegt werden Teilchen
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und en Element kann chemisch nicht mehr zerlegt werden Teilchen
Wiederholung: Duktilität
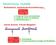 Wiederholung: Duktilität Bulkmaterial: prozentuale Bruchdehnung ε b lz l0 εb = l Dünne Schicht: 3-Punkt-Biegetest 0 l Z = Länge der Probe nach dem Bruch l 0 = Länge der Probe vor dem Bruch ε B = Bruchdehnung
Wiederholung: Duktilität Bulkmaterial: prozentuale Bruchdehnung ε b lz l0 εb = l Dünne Schicht: 3-Punkt-Biegetest 0 l Z = Länge der Probe nach dem Bruch l 0 = Länge der Probe vor dem Bruch ε B = Bruchdehnung
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig?
 1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
Grundwissen 9. Klasse Chemie
 Grundwissen 9. Klasse Chemie 1. Formelzeichen und Einheiten 2. Was versteht man unter der Stoffmenge und der Avogadro- Konstante N A? Eine Stoffportion hat die Stoffmenge n = 1 mol, wenn sie 6 * 10 23
Grundwissen 9. Klasse Chemie 1. Formelzeichen und Einheiten 2. Was versteht man unter der Stoffmenge und der Avogadro- Konstante N A? Eine Stoffportion hat die Stoffmenge n = 1 mol, wenn sie 6 * 10 23
Ferrofluide. Physikalische Grundlagen. http://en.wikipedia.org/wiki/file:ferrofluid_close.jpg
 Ferrofluide Physikalische Grundlagen http://en.wikipedia.org/wiki/file:ferrofluid_close.jpg Inhalt Definition Herstellung Maßnahmen zur Stabilisierung Abschätzung der Partikelgröße, Abstandsmechanismen
Ferrofluide Physikalische Grundlagen http://en.wikipedia.org/wiki/file:ferrofluid_close.jpg Inhalt Definition Herstellung Maßnahmen zur Stabilisierung Abschätzung der Partikelgröße, Abstandsmechanismen
Contents Inhalt. Evaporation and sputtering technical data Aufdampf- und zerstäubungstechnische Daten
 Contents Inhalt Evaporation and sputtering technical data Aufdampf- und zerstäubungstechnische Daten Application guidelines for special materials Anwendungshinweise für Spezialmaterialien Application matrix
Contents Inhalt Evaporation and sputtering technical data Aufdampf- und zerstäubungstechnische Daten Application guidelines for special materials Anwendungshinweise für Spezialmaterialien Application matrix
Grundwissen Chemie 9. Klasse SG
 Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Bauchemische Grundlagen Allgemeine Grundlagen
 Bauchemische Grundlagen Allgemeine Grundlagen Thomas A. BIER Institut für Keramik, Glas- und Baustofftechnik, Leipziger Straße 28, 09596 Freiberg, Inhalt des Moduls 1. Physiko- chemische Grundlagen der
Bauchemische Grundlagen Allgemeine Grundlagen Thomas A. BIER Institut für Keramik, Glas- und Baustofftechnik, Leipziger Straße 28, 09596 Freiberg, Inhalt des Moduls 1. Physiko- chemische Grundlagen der
Grundwissen Chemie 8I
 1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
Anorganische Chemie I Dr. Egbert Figgemeier. 04. Dezember 2006
 Anorganische Chemie I Dr. Egbert Figgemeier 04. Dezember 2006 Gruppe 14 C Si Ge Sn [Ed]2s 2 p 2 Pb Gruppe 14 Physikalische Eigenschaften Zunahme des metallischen Charakters innerhalb der Gruppe. Element
Anorganische Chemie I Dr. Egbert Figgemeier 04. Dezember 2006 Gruppe 14 C Si Ge Sn [Ed]2s 2 p 2 Pb Gruppe 14 Physikalische Eigenschaften Zunahme des metallischen Charakters innerhalb der Gruppe. Element
Glas - Chemische Eigenschaften Laugen Sa uren - konzentriert Sa uren - verdünnt
 Goodfellow GmbH Postfach 3 43 D-63 Bad Nauheim Telefon 0800 000 579 : Telefax 0800 000 580 Glas - hemische Eigenschaften Laugen Sa uren - konzentriert Sa uren - verdünnt MAOR bearbeitbare SiO 46/Al O3
Goodfellow GmbH Postfach 3 43 D-63 Bad Nauheim Telefon 0800 000 579 : Telefax 0800 000 580 Glas - hemische Eigenschaften Laugen Sa uren - konzentriert Sa uren - verdünnt MAOR bearbeitbare SiO 46/Al O3
Einführungskurs 7. Seminar
 ABERT-UDWIGS- UNIVERSITÄT FREIBURG Einführungskurs 7. Seminar Prof. Dr. Christoph Janiak iteratur: Riedel, Anorganische Chemie,. Aufl., 00 Kapitel.8.0 und Jander,Blasius, ehrb. d. analyt. u. präp. anorg.
ABERT-UDWIGS- UNIVERSITÄT FREIBURG Einführungskurs 7. Seminar Prof. Dr. Christoph Janiak iteratur: Riedel, Anorganische Chemie,. Aufl., 00 Kapitel.8.0 und Jander,Blasius, ehrb. d. analyt. u. präp. anorg.
Werkstoffkunde Chemische Bindungsarten
 Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
1.6. Die Ionenbindung
 1.6. Die Ionenbindung 1.6.1. Die Edelgasregel Die Edelgase gehen kaum Verbindungen ein und zeigen in ihrer Periode jeweils die höchsten Ionisierungsenergien. Ihre Elektronenkonfiguration mit jeweils Außenelektronen
1.6. Die Ionenbindung 1.6.1. Die Edelgasregel Die Edelgase gehen kaum Verbindungen ein und zeigen in ihrer Periode jeweils die höchsten Ionisierungsenergien. Ihre Elektronenkonfiguration mit jeweils Außenelektronen
GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie
 Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und Reaktionen Reinstoff Element Kann chemisch nicht mehr zerlegt
Christian-Ernst-Gymnasium Am Langemarckplatz 2 91054 ERLANGEN GRUNDWISSEN CHEMIE 9 - MuG erstellt von der Fachschaft Chemie C 9.1 Stoffe und Reaktionen Reinstoff Element Kann chemisch nicht mehr zerlegt
Vorlesung Anorganische Chemie
 Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 6 Entropie und Gibbs Enthalpie Gibbs-elmholtz-Gleichung Absolute Entropien Gibbs Standardbildungsenthalpien Kinetik
Vorlesung Anorganische Chemie Prof. Ingo Krossing WS 2007/08 B.Sc. Chemie Lernziele Block 6 Entropie und Gibbs Enthalpie Gibbs-elmholtz-Gleichung Absolute Entropien Gibbs Standardbildungsenthalpien Kinetik
Spiegelbeschichtungen in Dünnschichttechnik
 Spiegelbeschichtungen in Dünnschichttechnik WTT-CHost Workshop EMPA Dübendorf, 28. Juni 2006 Dr. Markus Michler, -NTB Dr. Markus Michler Spiegelbeschichtungen in Dünnschichttechnik Dübendorf, 28.Juni 2006
Spiegelbeschichtungen in Dünnschichttechnik WTT-CHost Workshop EMPA Dübendorf, 28. Juni 2006 Dr. Markus Michler, -NTB Dr. Markus Michler Spiegelbeschichtungen in Dünnschichttechnik Dübendorf, 28.Juni 2006
DGM Fachausschuss Hochtemperatur-Sensorik
 DGM Fachausschuss Hochtemperatur-Sensorik Holger Fritze Technische Universität Clausthal Institut für Energieforschung und Physikalische Technologien und Energie-Forschungszentrum Niedersachsen Energie-Campus,
DGM Fachausschuss Hochtemperatur-Sensorik Holger Fritze Technische Universität Clausthal Institut für Energieforschung und Physikalische Technologien und Energie-Forschungszentrum Niedersachsen Energie-Campus,
Fortsetzung der Erkundungen im Periodensystem
 Fortsetzung der Erkundungen im Periodensystem Wiederholung Für die chemischen Eigenschaften der Elemente sind die Elektronen der äußersten Schale verantwortlich Valenzorbitale Valenz- oder Außenelektronen
Fortsetzung der Erkundungen im Periodensystem Wiederholung Für die chemischen Eigenschaften der Elemente sind die Elektronen der äußersten Schale verantwortlich Valenzorbitale Valenz- oder Außenelektronen
Schweißen von Aluminiumwerkstoffen
 Schweißen von Aluminiumwerkstoffen Roland Latteier Wissenswerte Vergleich mit Stahl Vortragsgliederung Betriebliche Anforderungen Werkstoffbezeichnungen R. Latteier 2 Vortragsgliederung Erfahrung bei der
Schweißen von Aluminiumwerkstoffen Roland Latteier Wissenswerte Vergleich mit Stahl Vortragsgliederung Betriebliche Anforderungen Werkstoffbezeichnungen R. Latteier 2 Vortragsgliederung Erfahrung bei der
1 Elektrostatik 1.1 Ladung 1.1.1 Eigenschaften
 1 Elektrostatik 1.1 Ladung 1.1.1 Eigenschaften 1 Das heutige Bild vom Aufbau eines Atoms Größe < 10-18 m Größe 10-14 m Größe < 10-18 m Größe 10-15 m Größe 10-10 m 2 Ausblick: Ladung der Quarks & Hadronen
1 Elektrostatik 1.1 Ladung 1.1.1 Eigenschaften 1 Das heutige Bild vom Aufbau eines Atoms Größe < 10-18 m Größe 10-14 m Größe < 10-18 m Größe 10-15 m Größe 10-10 m 2 Ausblick: Ladung der Quarks & Hadronen
ELEKTROCHEMIE. Elektrischer Strom: Fluß von elektrischer Ladung. elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie.
 ELEKTROCHEMIE Elektrischer Strom: Fluß von elektrischer Ladung Elektrische Leitung: metallische (Elektronen) elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie Galvanische Zellen Elektrolyse Die
ELEKTROCHEMIE Elektrischer Strom: Fluß von elektrischer Ladung Elektrische Leitung: metallische (Elektronen) elektrolytische (Ionen) Zwei Haupthemen der Elektrochemie Galvanische Zellen Elektrolyse Die
Chemische Bindung. Chemische Bindung
 Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Hilfe!... Eine modulierte Struktur Ein Erfahrungsbericht. Internes Seminar, 15.11.2005
 Hilfe!... Eine modulierte Struktur Ein Erfahrungsbericht. Internes Seminar, 15.11.2005 Typisches Phasendiagramm A I -Zn/Cd: Das System Na Zn Quelle: Massalski NaZn 13 -Struktur Cd(1) Cd(1) d K(1) a Cd(2)
Hilfe!... Eine modulierte Struktur Ein Erfahrungsbericht. Internes Seminar, 15.11.2005 Typisches Phasendiagramm A I -Zn/Cd: Das System Na Zn Quelle: Massalski NaZn 13 -Struktur Cd(1) Cd(1) d K(1) a Cd(2)
Die Solarzelle. Passivated Emitter and Rear Locally diffused solar cell. 25% c-si Zelle erhältlich bei der University of New South Wales: ~1000EUR/W p
 Die Passivated Emitter and Rear Locally diffused solar cell 25% c-si Zelle erhältlich bei der University of New South Wales: ~1000EUR/W p Übersicht Definition des Problems Zellaufbau Absorber Emitter Oberflächenpassivierung
Die Passivated Emitter and Rear Locally diffused solar cell 25% c-si Zelle erhältlich bei der University of New South Wales: ~1000EUR/W p Übersicht Definition des Problems Zellaufbau Absorber Emitter Oberflächenpassivierung
Silbercoulometer / Elektrolyse. Bestimmung der Faraday schen Zahl mit dem Silbercoulometer
 Institut f. Experimentalphysik Technische Universität Graz Petersgasse 16, A-8010 Graz Laborübungen: Elektrizität und Optik 20. Mai 2010 Silbercoulometer / Elektrolyse Stichworte zur Vorbereitung: Elektrolytische
Institut f. Experimentalphysik Technische Universität Graz Petersgasse 16, A-8010 Graz Laborübungen: Elektrizität und Optik 20. Mai 2010 Silbercoulometer / Elektrolyse Stichworte zur Vorbereitung: Elektrolytische
2. Themenbereich: Farben und Kristalle. ? AGP-Versuche?
 Künstliche Edelsteine 2. Themenbereich: Farben und Kristalle? AGP-Versuche? AGP-Begleitvorlesung, 11.2014, C. Röhr Einleitung, Übersicht Hochdrucksynthese: Diamant Verneuil-Verfahren: Rubin, Saphir Czochralski-Verfahren:
Künstliche Edelsteine 2. Themenbereich: Farben und Kristalle? AGP-Versuche? AGP-Begleitvorlesung, 11.2014, C. Röhr Einleitung, Übersicht Hochdrucksynthese: Diamant Verneuil-Verfahren: Rubin, Saphir Czochralski-Verfahren:
Chemische Bindung. Ue Mol 1. fh-pw
 Ue Mol 1 Chemische Bindung Periodensystem - Atome - Moleküle Periodensystem(e) 3 Nichtmetalle - Metalloide 5 Eigenschaften der Elemente 6 Bindungstypen 7 Ionenbindung 8 Kovalente, homöopolare Bindung 10
Ue Mol 1 Chemische Bindung Periodensystem - Atome - Moleküle Periodensystem(e) 3 Nichtmetalle - Metalloide 5 Eigenschaften der Elemente 6 Bindungstypen 7 Ionenbindung 8 Kovalente, homöopolare Bindung 10
Festkörperchemie. VO, 2SWS / 3 ECTS-Punkte. (Prof. Herbert IPSER / Prof. Peter TERZIEFF )
 1. TEIL (H. Ipser) Festkörperchemie VO, 2SWS / 3 ECTS-Punkte (Prof. Herbert IPSER / Prof. Peter TERZIEFF ) CHEMISCHE BINDUNG IN FESTKÖRPERN Wiederholung der Grundtypen Metallische Bindung KRISTALLCHEMIE
1. TEIL (H. Ipser) Festkörperchemie VO, 2SWS / 3 ECTS-Punkte (Prof. Herbert IPSER / Prof. Peter TERZIEFF ) CHEMISCHE BINDUNG IN FESTKÖRPERN Wiederholung der Grundtypen Metallische Bindung KRISTALLCHEMIE
THERMISCHE AUSDEHNUNG
 INSTITUT FÜR ANGEWANDTE PHYSIK Physikalisches Praktikum für Studierende der Ingenieurswissenschaften Universität Hamburg, Jungiusstraße 11 THERMISCHE AUSDEHNUNG Unter thermischer Ausdehnung versteht man
INSTITUT FÜR ANGEWANDTE PHYSIK Physikalisches Praktikum für Studierende der Ingenieurswissenschaften Universität Hamburg, Jungiusstraße 11 THERMISCHE AUSDEHNUNG Unter thermischer Ausdehnung versteht man
Vorlesung am 7. Juni 2010
 Materialwissenschaften, SS 2008 Ernst Bauer, Ch. Eisenmenger-Sittner und Josef Fidler 1.) Kristallstrukturen 2.) Strukturbestimmung 3.) Mehrstoffsysteme 4.) Makroskopische Eigenschaften von Festkörpern
Materialwissenschaften, SS 2008 Ernst Bauer, Ch. Eisenmenger-Sittner und Josef Fidler 1.) Kristallstrukturen 2.) Strukturbestimmung 3.) Mehrstoffsysteme 4.) Makroskopische Eigenschaften von Festkörpern
Wasserchemie Modul 4
 Wasserchemie Modul 4 Ionenchromatographie / HPLC Plausibilitätstests tstests Ionensensitive Elektroden Chromatographie Trennung von Stoffgemischen Zwei nicht mischbare Phasen - stationäre Phase (Ionentauscher)
Wasserchemie Modul 4 Ionenchromatographie / HPLC Plausibilitätstests tstests Ionensensitive Elektroden Chromatographie Trennung von Stoffgemischen Zwei nicht mischbare Phasen - stationäre Phase (Ionentauscher)
Allgemeine Chemie. SS 2014 Thomas Loerting. Thomas Loerting Allgemeine Chemie
 Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Crashkurs Säure-Base
 Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Element. Verbindung. Reinstoff. Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
