5. Biochemie- Seminar
|
|
|
- Adolf Fuchs
- vor 8 Jahren
- Abrufe
Transkript
1 5. Biochemie- Seminar 5. Biochemie- Seminar Kohlenhydrate II und biologische Oxidation Verweise mit [L] beziehen sich auf Biochemie und Pathobiochemie von Löffler, Petrides, Heinrich; 8. Auflage. Glycogenbiosynthese und Glycogenabbau von Leif [L] Kap. 11.2; S. 368 Grundlagen Glycogen - nichtlineares Polymer aus D-Glucose-Einheiten; durch α-1,4- und α-1,6- Bindungen verknüpft - ist an Startermolekül Glycogenin gekoppelt - liegt im Zytoplasma als Granula (mit KH-Anteil und Proteinen); lässt sich außer in Erys in allen Zellen des Körpers nachweisen (z.t. in geringen Menge); besonders in: o Leberzellen bis 5-10% (nach KH-reicher Mahlzeit) g o Muskelzellen nicht über 1% 250g - C1-Atom ist wegen Aldehydgruppe reduzierend, C4-Atom ist nicht-reduzierend Kettenverlängerung am nicht-reduzierenden C4-Atom Biosynthese von Glycogen aus Glucose - [L] Abb normalerweise wird Glucose umgewandelt und an eine bestehende Glycogenkette ( Primer- Glycogen ) angehängt; hierzu muss jedoch zu einem früheren Zeitpunkt eine Glycogenkette aus dem Nichts ( de novo ) geschaffen worden sein dies schafft die Voraussetzung für die C1-C4-glykosidische Bindung - Aktivierung der Glc-1-P unter Verbrauch von 1 UTP - das Pyrophosphat wird im Anschluss sofort von einer Pyrophosphatase gespalten 4. de novo- Synthese - erklärt die Neuentstehung von Glycogenmolekülen - benötigt das Protein Glycogenin o zytosolisches Protein mit Glycosyltransferase- Aktivität - Glycogenin kann sich autokatalytisch an einem Tyrosylrest selbst glycosylieren (bis zu 8 Glycosylreste) an glycosyliertes Glycogenin lagert Glycogen-Synthase an, welche die weitere Glycosylierung vollzieht - 1 -
2 branching Enzyme - [L] Abb wenn Kette 6 11 Glieder lang ist werden Abzweigungen eingebaut durch das branching enzyme Amylo-1,4 1,6-Transglucosylase - überträgt eine min. 6 Reste lange Glucosekette über Schaffung einer 1,6-glycosidischen Bindung auf einen Glucoserest an der selben oder einer anderen Kette Verzweigungsstellen entstehen (typisch für Glycogen und Stärke) - der Prozess benötigt keine Energie in Form von ATP oder UTP - Pathobiochemie o durch einen Gendefekt kann es hier zu Fehlern kommen extrem lange Ketten o diese werden als körperfremd erkannt und es kommt zu einer Abwehrreaktion Leberzirrhose Abbau von Glycogen (Glycogenolyse) - [L] Abb Abspaltung durch phosphorolytische Spaltung [nicht hydrolytisch] am nicht-reduzierenden (C4) Ende des Glycogens - Cofaktor: PALP (Vit. B6) hierzu siehe Gluconeogenese aus Seminar 4 debranching enzyme - [L] Abb Glycogen-Phosphorylase kann 1,6-glykosidische Verzweigungen nicht spalten - Glycogen-Phosphorylase (s.o.) baut Ketten bis 4 Glucosemoleküle vor 1,6-Abzweigung ab - 3 Glucosemoleküle werden als Trisaccharideinheit von α(1,4) α(1,4)-glucantransferase des debranching Komplex an das Ende einer anderen Kette übertragen - Spaltung der 1,6-glycosidischen Bindung erfolgt hydrolytisch durch Amylo-1,6-Glucosidase des debranching enzyme Glucose wird frei - Pathobiochemie o Enymdefekt des debranching Komplex führt zu prall mit Glycogen gefüllter Leber Regulation - reziproke Kontrolle der Schlüsselenzyme Glycogen-Phosphorylase und Glycogen-Synthase allosterische Regulation in der Leber - Glucose inhibiert die Glycogen-Phosphorylase (kein Glycogen-Abbau nötig wenn genug Glucose vorhanden ist) allosterische Regulation im Muskel - AMP aktiviert die Phosphorylase - Glucose-6-Phosphat und ATP inhibieren die Phosphorylase - Anstieg von [Ca ++ ] i Ca ++ -Calmodulin-Komplex Teilaktivierung der Phosphorylase-Kinase, die dann mit sub-maximaler Geschwindigkeit arbeitet [die Glycogen-Phosphorylase aktiviert] - 2 -
3 hormonelle Regulation - Adrenalin/ Glucagon AC camp PKA o PKA aktiviert Phosphorylase-Kinase, diese wandelt Glycogen-Phosphorylase b [inaktiv] in Phosphorylase a [aktiv] um o PKA wandelt Glycogen-Synthase a [aktiv] in Synthase b [inaktiv] um - Insulin o o inhibiert Glucose-Synthase-Kinase 3 (GSK3) keine Inaktivierung der Glycogen- Synthase aktiviert eine Protein-Phosphatase dephosphoryliert inaktive Glycogen-Synthase Zusammenfassung Glycogenregulationsmechanismen der Leber - [L] Abb erhöhtes Glucoseangebot Insulin Glucagon/ Adrenalin Induktion der Glucokinase, Hemmung von Glc-6-Phosphatase Aktivierung Glycogensynthase - verringertes Glucoseangebot Insulin Glucagon/ Adrenalin [camp] i Hemmung von Glycogen-Synthase, Aktivierung von Glycogen-Phosporylase Glc-6-Phosphatase spaltet Glc-6-P zu Glucose Glycogenspeicherkrankheiten etliche verschiedene; wichtigste Form mit Anteil von ca. 40%: von-gierke-glycogenose (Typ I) - Defekt der Glucose-6-Phosphatase Leber-Glycogen kann nicht zu Glucose abgebaut werden - Risiko der Hypoglykämie schon im Kindesalter - vergrößerte Leber durch Glycogenspeicherung
4 Citratzyklus als Drehscheibe des Intermediärstoffwechsels dehydrierende Decarboxylierung von Pyruvat 1. Transport ins Mitochondrium mittels OH - -Antiport 2. dehydrierende Decarboxylierung durch Pyruvat-Dehydrogenase-Komplex [Cofaktoren mit * werden regeneriert, die anderen Cofaktoren werden verbraucht] - E1: Pyruvat-Dehydrogenase (TPP*) o Pyruvat bindet an TPP Decarboxylierung zu Hydroxyethyl-TPP und CO 2 o Oxidation von Hydroxyethyl-TPP zu Acetyl - E2: Dihydrolipoyl-Transacetylase (Liponamid*, CoA) o Acetyl wird an CoA gebunden Acetyl-Coa [geht in den Citratzyklus ein] und Lipoat - E3: Dihydrolipoyl-Dehydrogenase (FAD*, NAD) o Reoxidation von Lipoat [ Ausgangszustand wiederhergestellt] Regulation Regulation durch Interkonversion [Phosphorylierung/ Dephosphorylierung] - Acetyl-CoA, ATP, NADH, Fettsäuren inhibieren Kinase Phospho-PDH (inaktiv) - Mg ++, Ca ++ aktivieren Phosphatase Dephospho-PDH (aktiv) Pathobiochemie - Arsenit und Quecksilber machen den Dihydrolipinamid-Arm von E2 unwirksam - diese Vergiftung ähnelt einem Vitamin B 1 -Mangel Bedeutung des Citratzyklus - findet im Mitochondrium statt Transporter für Anknüpfung an zytosolische Stoffwechselvorgänge sind notwendig - wenn die Atmungskette zum Erliegen kommt läuft auch der Citratzyklus nicht, da dann die Reduktionsäquivalente fehlen katabole Funktion - generiert NADH, FADH zur ATP- Erzeugung in der Atmungskette - generiert GTP - die Energie für katabole Funktion kommt aus dem oxidativen Abbau von Acetyl-CoA anabole Funktion - Citratzyklus-Intermediate sind Ausgangsstoffe für Synthesen im Cytosol %21Citratcyclus-Ueberblick.svg - 4 -
5 Reaktionen des Citratzyklus 5. Biochemie- Seminar Kohlenhydrate II und biologische Oxidation Kondensationsreaktion - G 0 = -32,2 kj/mol Rkt. ist irreversibel - Aconitase enthält Eisen-Schwefel-Zentrum und dient im Zytosol der Eisenregulation - erste oxidative Decarboxylierung - zuerst wird das Hydrid entfernt [NAD NADH], dann decarboxyliert o G 0 = -7,1 kj/mol Rkt. ist irreversibel - zweite oxidative Decarboxylierung - strukturell und katalytisch fast identisch mit Pyruvat-Dehydrogenase-Komplex (s.o.) o gleiche Cofaktoren: TPP, CoA, Liponsäure, NAD +, FAD - G 0 = -34 kj/mol Rkt. ist irreversibel 5. - Substratkettenphosphorylierung Rückgewinnung von Oxalacetat aus Succinat Oxidation - Succinat-DH ist Teil der Atmungskette an der inneren Mitochondrien-Membran o FADH 2 überträgt Elektronen sie weiter auf Fe-S- Zentren o von dort direkt auf Ubichinon übertragen - stereospezifische Reaktion - C-Atom das in 7. das H 2 O erhielt wird oxidiert - G 0 = +30 kj/mol Rkt. nur möglich da Produkte sofort weiterreagieren - 5 -
6 Energiebilanz - aus Oxidation eines Acetyl-CoA-Moleküls entstehen 10 ATP - hohe Energieausbeute nur durch enge Verbindung mit oxidativen Phosphorylierung möglich - G 0 des gesamten Citratzyklus = -77,7 kj/mol enzymat. Reaktion H-Akzeptor ATP-Ausbeute Isocitrat-Dehydrogenase 1 NADH/H + 2,5 ATP α-ketoglutarat-dehydrogenase 1 NADH/H + 2,5 ATP Succinyl-CoA-Synthetase 1 GTP 1 ATP Succinat-Dehydrogenase 1 FADH 2 1,5 ATP Malat-Dehydrogenase 1 NADH/H + 2,5 ATP 10 ATP Regulation - Zelle energiereich kein Citratzyklus - Zelle energiearm Citratzyklus Citrat-Synthase [arbeitet aufgrund Substrat-Limitierung immer im unteren Leistungsbereich] - Citrat, ATP, NADH, Succinyl-CoA inhibieren - ADP aktiviert Isocitrat-Dehydrogenase - ATP, NADH inhibieren - ADP, NAD, Ca ++ aktivieren [Ca ++ steuert viele energieverbrauchende Prozesse, deshalb ist Ca++ ein Signal für baldigen Energiebedarf] α-ketoglutarat-dehydrogenase - ATP, NADH inhibieren - ADP, NAD, Ca ++ aktivieren amphibole Natur des Citratzyklus - neben oxidativen Abbau (katabolen Reaktionen) ist Citratzyklus auch Ausgang für versch. Biosynthesen (anabole Reaktionen) - Zwischenprodukte müssen durch Mitochondrienmembran ins Cytoplasma transportiert werden - einige Sequenzen des Citratzyklus auch im extramitochondrialen Raum o Citrat -Ketoglutarat o Fumerat Oxalacetat - große Bedeutung für: o Fettsäurebiosynthese o Hämbiosynthese o Gluconeogenese o Biosynthese nicht essentieller Aminosäuren - Fettsäurebiosynthese o Acetyl-CoA für FS-Biosynthese wichtig, kann aber nicht durch Mitochondrienmembran transportiert werden o auf Oxalacetat übertragen Citrat ins Cytoplasma durch ATP-Citratlyase gespalten - 6 -
7 Citrat + CoA-SH + ATP Oxalacetat + Acetyl-CoA + ADP +P i o ATP-Citratlyase viel in Geweben mit großer Kapazität zur Fettsäurebiosynthese (Leber, Fettgewebe) - Hämbiosynthese o Succinyl-CoA ist der Startpunkt für Hämbiosynthese o Kondensation mit Glycin -Aminolävulinat Hämsynthese - Gluconeogenese o Bildung von Oxalacetat aus Pyruvat o Biosynthese nicht essentieller Aminosäuren startet von Pyruvat bzw. Oxalacetat und -Ketoglutarat Anaplerotische Reaktionen - Intermediat-auffüllende Reaktionen 1. Pyruvat-Carboxylase - Carboxylierung ist Biotin-abhängig - bei geringen Konzentration von Acetyl-CoA aktiviert; hohe Aktivität u.a. in der Leber 2. Glutamat-Dehydrogenase 3. Malat-Enzym - Malat wird anschließend via H + -Symport ins Mitochondrium transportiert und dort umgewandelt - 7 -
8 Oxidative Phosphorylierung in deratmungskette und ATP-Synthese von Ferdi ATP Synthase - Enzymkomplex aus 17 unterschiedlichen Untereinheiten - In innerer Mitochondrienmembran verankert - Ragt in mitochondriale Matrix hinein - Unterscheidung in 4 Komponenten: F0-Teil: in mitochondriale Membran, viele Untereinheiten, enthält entscheidenden Rotor (bestehend aus ca. 10 c-untereinheiten, die im Kreis angeordnet sind, in der Mitte des Rotors ist γ- Untereinheit, seitlich a-untereinheit) plus fünf weitere UE mit ungeklärter Stiel: Funktion besteht aus zwei langen α-helices, welche zur γ- Untereinheit der ATP- Synthase gehören( wird durch Rotor in Bewegung gesetzt) F1- Teil: enthält 3 gleichartig gebaute katalytischen Zentren( bestehend aus je einer β UE und einer α UE) die im Ring angeordnet sind und durch Drehung der γ- Untereinheit, in der Mitte, die Möglichkeit erhalten ADP und Phosphat in ATP umzusetzen Stator: Dimer aus 2 β UE, entspricht zweiter Stiel der Drehung des F1- Teils verhindert, da im F0 Teil verankert - Funktionsweise ( ATP Synthese) - Dies ist die Kurzform, wer mehr wissen möchte siehe S. 500 Biochemie und Pathobiochemie, Löffler, Petrides,Heinrich 8. Auflage - durch F0-Teil strömen Protonen in die Matrix und versetzen Rotor in Drehung ( 1 Proton löst Bewegung einer c UE aus, für volle Drehung Anzahl der c- UE wichtig, für optimale Wirkungsweise bestimmte c- UE Anzahl wichtig. noch unbekannt) - Drehung überträgt sich auf γ- Untereinheit, nur diese dreht sich, nicht der ganze F1-Teil, Drehung gegen den Urzeigersinn - Drehung löst in β UE und α UE des F1-Teils Konformationsänderungen aus - Durch die Konformationsänderungen synthetisieren die 3 katalytischen Zentren ATP ( Prozess abwechselnd: 1. Bindung von ADP und Phosphat, loose 2. Schließung und Umsetzung von ADP und P in ATP, tight 3. Öffnung um ATP in Matrix freizusetzen), open - Bei Drehung des Rotors um 360 Grad kann F1-Teil genau 3 ATP synthetisieren - Schritte laufen an allen 3 Zentren gleichzeitig ab - Energie durch Protonenfluss wird dabei zur Konformationsänderungen vom O zum T verwendet Atmungskette - Allgemein: - Aufgabe: Aufrechterhaltung des mitochondriale Protonengradienten nicht etwa ATP Bildung - Bestehend aus 4 Atmungskettenkomplexe, in mitochondriale Innenmembran eingebettet - Komplexe 1,3 und 4, lagern sich zu Respirasomen zusammen, Respirasomen arbeiten als Protonenpumpen ( Aufbau Protonengradient), - Beziehen Energie aus Elektronen, die in festgelegter Reihenfolge durch 1,3, und 4 hindurchfließen - 8 -
9 - Alle Elektronen werden zuletzt vom Komplex 4 auf molekularen Sauerstoff ( aus Atemluft aufgenommen) übertragen, dazu parallele Aufnahme von Protonen, also jedes Sauerstoff- Molekül in 2 Wasser Moleküle umgesetzt - NADH = Überträger für Elektronen von der Nahrung zur Atmungskette( pro NADH exportiert Komplex 1 4 Elektronen, Komplex 3 4 Elektronen, Komplex 4 w Elektronen) ein NADH gibt 2 Elektronen ab und ermöglicht den Export von 10 Protonen sowie Synthese von 1 Wasser - Komplex 2 vermittelt Quereinstieg von Elektronen die nicht von NADH sondern von FADH2 kommen, allerdings nur Energie für die Komplexe 3 und 4 - Also: ein FADH2 gibt 2 Elektronen ab und ermöglicht den Export von 6 Protonen sowie Synthese von 1 Wasser - Außerdem wichtig für die Atmungskette: Coenzyme und prosthetische Gruppen - Coenzyme: kleine Moleküle die nicht aus Aminosäuren bestehen, aber die für die Funktion eines Enzyms essentiell sind, manche frei löslich: Bsp.: NADH - Prosthetische Gruppe: fest gebundene Coenzyme, z. Bsp. FAD an Komplex 2 Einzelne Komplexe in der Atmungskette - Siehe Tab. 15.2, S. 497 Biochemie und Pathobiochemie, Löffler, Petrides,Heinrich 8. Auflage - Komplex 1 - Synonym: NADH-Ubichinon-Oxidoreduktase - Nimmt Elektronen von NADH auf und überträgt sie auf Ubichinon - 43 Untereinheiten groß, L-Form, der größere Teil besteht aus hydrophoben Proteinen ( in der Innenmembran) kleinerer Teil besteht aus hydrophilen Proteinen ( in der Matrix) - Hydrophiler Teil nimmt Elektronen auf - NADH gibt Elektronen ab, welche auf Flavinmononukleotid(FMN) übertragen werden - Flavinmononukleotid nichtkovalent an Komplex 1 gebunden; dazu acht Eisen-Schwefelzentren am Komplex 1 an die die Elektronen hin und her springen und so durch den Komplex geschleust werden - 2 Typen Eisen-Schwefel Zentren: 2Fe/2 S-Typ und 4Fe/4s Typ, beide über Cystein mit Komplex 1 verbunden - Dann durchlaufen Elektroden hydrophoben Teil, genauer Weg noch ungeklärt - Dann Übertragung auf Ubichinon ( Coenzym Q ), dabei wird Energie frei, die noch ungeklärt den Transport von Protonen ermöglicht - Ubichinon: zentrale Sammelstelle für Elektronen in der Innenmembran, besteht aus hydrophober Seitenkette( hält Ubichinon in der Innenmembran) und einer Benzochinongruppe ( kann Elektron und Proton aufnehmen zur Bildung von Semichinon, dann Aufnahme eines weiteren Elektrons und Protons zur Bildung von Ubichinol, beide wichtig für Übertragung von Elektronen auf Komplex 3 und zur Elektronenübertragung von der Matrix in den Intermebranraum) - Hemmstoffe: viele Chinonanaloge Hemmstoffe, am bekanntesten: aus Leguminosen isolierbare Rotenon, aber auch hohe Konzentration von Barbituraten wie z. Bsp. Amytal wirken hemmend - Komplex 2 - Synonym: Succinat- Dehydrogenase, Succinat Ubichinon - Oxidoreduktase - Wesentlich kleiner als Komplex 1 - Teil des Citratzyklus ( bekommt Elektronen von Succinat, was zu Fumarat wird) - 9 -
10 - Keine Protonenpumpe obwohl er auch Elektronen auf Ubichinon überträgt - Ebenfalls membranständiger, hydrophober Teil und hydrophilem Teil in der Matrix - im hydrophilen Teil werden Elektronen auf Flavinadenindinukleotid ( FAD ), FAD kovalent an Komplex gebunden, hat zusätzlich zum FMN eine Adenosindiphosphatgruppe - weitere prosthetische Gruppen Komplex 2: drei Fe/S- Zentren und eine Hämgruppe im membranständigen Teil - Hemmstoffe: Malonat ( kompetitive Hemmung an Succinat Bindungsstelle, klassisch) - ETF-Ubichinon - Oxireduktase - Weiterer Enzymkomplex, wird immer von allen vernachlässigt und weint deswegen ganz viel, dabei ist seine Funktion durchaus mit der des Komplex 2 vergleichbar - in der Innenmembran, welcher festgebundenes FAD enthält, der Elektronen von vom Elektronen transferierenden Flavoprotein (ETF) übernimmt - ETF sammelt im mitochondriale Stoffwechsel Elektronen ein - Vom FADH2 der ETF UO werden Elektronen auf Ubichinon übertragen - Glycerin-3-phosphat-Dehydrogenase - Im Zytosol geht die Glykolyse los, in der NADH gebildet wird, welches zur Synthese von Glycerin-3-phosphat genutzt wird - In mitochondriale Innemembranraum wird dann mithilfe der G-3-p-D Elektronen für Ubichinon gewonnen - Komplex 3 - Enthält 11 Untereinheiten: u.a. Cytochrom b (hat 2 Hämgruppen gebunden), Cytochrom c1 (hat eine Häm Gruppe kovalent gebunden), Rieske-Eisen-Schwefel-Protein (hat ein Eisen- Schwefel Zentrum vom 2Fe/2S-Typ) - Komplex 3 nimmt Elektronen von Ubichinon auf und überträgt sie auf Cytochrom c ( dorthin werden alle Elektronen weitergeleitet, Cytochrom c besteht aus 104 AS, an der Außenseite der Innenmembran frei beweglich, enthält Hämgruppe die über Thioestergruppe mit 2 Cysteinen des Proteins kovalent gebunden ist, selten, nur noch Cytochrom c1 mit kovalenter Bindung) - Q-Zyklus: Reaktionsweg den Ubichinon-abhängigen Übertragung von Protonen aus der Matrix in den Intermembranraum, und das geht so - Also: Ubichinon nimmt an einem Innenmembrankomplex, Komplex 1 2 Elektronen auf und bekommt 2 Protonen mit dazu - Da Ubichinon Bindestellen an den Innenmebrankomplexen alle an der Innenseite der Innenmembran liegen, werden Protonen über die Matrix aufgenommen - Daraus entsteht Ubichinol, welches zur Bindestelle des Komplexes 3 wandert die an der Außenseite der Innenmembran liegt - Dort Abgabe von 2 Elektronen an Komplex 3 und 2 Protonen für den Intermebranraum - Effizienz wird verdoppelt indem jedes 2. Elektron innerhalb des Komplexes 3 an eine zweite Ubichinon Bindestelle bindet, welche an der Innenseite der Membran liegt, daraus entsteht wieder Ubichinol das wiederrum zu einer Bindungsstelle an Komplex 3 an der Außenseite der Innenmembran geht und die Elektronen an Komplex 3 und die Protonen an den Intermembranraum abgibt. Kann man doch gut verstehen oder? - Durch diesen Mechanismus zirkuliert ein erheblicher Teil der auf Komplex 3 übertragenen Elektronen im Q-Zyklus und trägt dadurch zum Transport von Protonen bei ( Export von 4 Protonen pro 2 Elektronen)
11 - Hemmstoffe: chinon-analoge HS: Myxothiazol und Stigmatellin blockieren das Ubihydrochinon Oxidationszentrum(Bindestelle an der Außenseite der Membran), Antimycin das Ubichinon Reduktionszentrum (Bindestelle an der Innenseite der Membran) - Komplex 4 - Synonym: Cytochrom c Oxidase - Nimmt Elektronen von Cytochrom C auf und überträgt sie auf Sauerstoff unter Bindung von Wasser - Übertragung von 2 Elektroden, exportieren von 2 Protonen ( noch nicht ganz geklärt) - Besteht aus 13 Polypeptiden sowie ein CuA-Zentrum mit 2 Kupferionen, einer Häm-a-Gruppe (Cytochrom a), einer Häm-a3-Gruppe ( Cytochrom a3) und ein CuB-Zentrum mi einem Kupferion - Zwischen Häm-a3 und CuB (werden beide von Histidin fixiert) bindet Sauerstoff, der mit der Atemluft aufgenommen wurde und nun hier zu Wasser umgesetzt wird = zentrale Struktur des Komplex 4, binukleäres Zentrum - Funktionsweise: von Cytochrom C wird ein Elektron auf ein Kupferion des CuA- Zentrum übertragen und von dort über Häm a auf Häm a3, hier werden Elektronen auf Sauerstoff übertragen - Die zur Bildung von 2 Wasser benötigten 4 Protonen werden aus der Matrix aufgenommen und NICHT exportiert - Indem Elektronen durch Komplex 4 fließen lösen sie Konformationsänderungen und Ladungsverschiebungen aus die außerhalb der Sauerstoffbindestelle, den Export von Elektronen bewirken. 2 Elektronen rein, Bildung 1 Wasser, dabei 2 Protonen verbraucht und 2 parallel exportiert - Hemmstoffe: Sauerstoff-ähnliche Moleküle, Komplexierung mit Eisen: CN-,N3, CO, ( NO,H2S) Energiebilanz der oxidativen Phosphorylierung - Der P/Q Quotient gibt an wie viel ATP pro verbrauchtem Sauerstoff gebildet wird - ATP ( = P ) Sauerstoffatom ( = O ), errechnet durch Kenntnis der Protonenlokations- Stöchiometrie - Zur Berechnung wichtig das ADP und P in die Mitochondrien rein und ATP raus geht - Pro gebildetem und exportiertem ATP gelangen also 4 1/3 Protonen in die Matrix zurück (s. o.) - Quotient NADH ( 10 Protonen) = 2,3 // Succinat über FAD direkt ( 6 Protonen) = 1,4 - Maximalwerte die in vivo sicher nicht erreicht werden - Wirkungsgrad der oxidativen Phosphorylierung liegt bei knapp 60 Prozent. - Ein NADH bildet maximal 4 ATP, da aber nur 2,3 entstehen = 60 Prozent - Energie zur Verfügung für Komplex 1 = 77 KJ/mol, Komplex 3 33 KJ/mol und Komplex KJ/mol, hier spiegelt sich Beitrag zum Ladungstransport über innere Mitochondrienwand wieder Regulation der Atmungskette - Substratoxidation und ATP-Bildung sind strikt gekoppelt - Darüber erfolgt Atmungskontrolle Britton Chance definiert 5 Fließgleichgewichtszustände
12 - Zustand 3, aktiver Zustand, alles in Masse da, maximale Geschwindigkeit - Zustand 4, kontrollierter Zustand, Sauerstoffverbrauch wird durch fehlendes ATP limitiert, protonenmotorische Kraft hat Maximalwert und bremst Elektronentransport der Atmungskettenkomplexe - Kontrolle hängt also von Dichtigkeit der inneren Mitochondrienmembran ab,denn auch bei fehlendem ADP kann durch Gabe eines Entkopplers ( Bsp. Dinitrophenol,?Nitrospray?, auch lipohile schwache organische Säuren, da sie sowohl in protonierter als auch deprotonierter Form frei über Membran diffundieren könne und so einen Zusammenbruch des Protonengradienten bewirken) Maximalwerte erreicht werden, da er Rückstrom von Protonen ermöglicht und so das elektrochemische Potential aufhebt - Interessanter Exkurs braunes Fettgewebe S. 503/504 Biochemie und Pathobiochemie, Löffler, Petrides, Heinrich 8. Auflage - In intakter Zelle wird Geschwindigkeit jedoch nicht über Verfügbarkeit von ADP geregelt, sondern komplexe Regulation, über verschiedene halbbewiesene Möglichkeiten: - 1.Möglichkeit - Einige Gewebe verfügen über Phosphokreatin-Kreatinsystem, zur kurzfristigen Auffüllung von ATP Speichern. - Gesteigertes Angebot von Reduktionsäquivalenten führt zu einer Erhöhung der Atmungsrate, ohne Änderung des ATP ADP Verhältnisses - Dabei vielleicht wichtig Isoformen des Thermogenins ( bei Aktivierung Erhöhung des Sauerstoffverbrauches ATP unabhängig) - 2.Möglichkeit : Erhöhung cytoplasmatisches Calcium, mehr Calcium in Mitochondrien, Citratzyklus - 3. Möglichkeit: Keine direkte Regulation über Sauerstoffverbrauch da Michaelis Konstante der sauerstoffverbrauchenden Cytochrom c-oxidase zu klein - 4. Möglichkeit: Vielleicht unter mikroaeroben Bedingungen existiert eine Kompetition mit NO - 5. Möglichkeit:. die Aktivität der Cytochrom c-oxidase in gewissem Maße über allosterische Nucleotid Bindungsstellen reguliert werden kann
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Kraftwerk Körper Energiegewinnung in unseren Zellen
 Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat
 Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase
 Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Pentosephosphat-Weg: alternativer Abbau von Glucose. Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet.
 Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Professionelle Seminare im Bereich MS-Office
 Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
KOHLENHYDRATE PYRUVAT-DEHYDROGENASE
 PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
Reaktionen der Zellatmung (1)
 ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Katalysatoren - Chemische Partnervermittlung im virtuellen Labor
 Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Die Atmungskette. 1. Einleitung und Funktion. Inhalt:
 Die Atmungskette Inhalt: 1. Einleitung und Funktion 2. Die einzelnen Komplexe der Atmungskette 3. Zusammengefasst: Die Vorgänge in der Atmungskette 4. Transporte durch die Mitochondrienmembran 5. Die Regulation
Die Atmungskette Inhalt: 1. Einleitung und Funktion 2. Die einzelnen Komplexe der Atmungskette 3. Zusammengefasst: Die Vorgänge in der Atmungskette 4. Transporte durch die Mitochondrienmembran 5. Die Regulation
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
schnell und portofrei erhältlich bei
 Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Übung 8. 1. Zellkommunikation. Vorlesung Bio-Engineering Sommersemester 2008. Kapitel 4. 4
 Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 05. 05. 08
Bitte schreiben Sie Ihre Antworten direkt auf das Übungsblatt. Falls Sie mehr Platz brauchen verweisen Sie auf Zusatzblätter. Vergessen Sie Ihren Namen nicht! Abgabe der Übung bis spätestens 05. 05. 08
12. Oxidative Phosphorylierung
 12. Oxidative Phosphorylierung 303 Zweck: Gewinnung von ATP Regeneration von NAD + und FAD Gesamtreaktionen: 3 ADP + 3 P i 3 ATP NADH + 0,5 O 2 + H + NAD + + H-O-H 2 ADP + 2 P i 2 ATP FADH 2 + 0,5 O 2
12. Oxidative Phosphorylierung 303 Zweck: Gewinnung von ATP Regeneration von NAD + und FAD Gesamtreaktionen: 3 ADP + 3 P i 3 ATP NADH + 0,5 O 2 + H + NAD + + H-O-H 2 ADP + 2 P i 2 ATP FADH 2 + 0,5 O 2
Atmung Übersicht. Atmung der Mitochondrien
 Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit
 Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit Frau Dr. Eva Douma ist Organisations-Beraterin in Frankfurt am Main Das ist eine Zusammen-Fassung des Vortrages: Busines
Eva Douma: Die Vorteile und Nachteile der Ökonomisierung in der Sozialen Arbeit Frau Dr. Eva Douma ist Organisations-Beraterin in Frankfurt am Main Das ist eine Zusammen-Fassung des Vortrages: Busines
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Parotis Pankreas. Dünndarm Bürstensaum. Amylose Amylopektin Glykogen. Maltose. Glucose. Isomaltose. Saccharose. Fructose. Lactose. Galaktose.
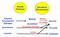 Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Foliensatz; Arbeitsblatt; Internet. Je nach chemischem Wissen können die Proteine noch detaillierter besprochen werden.
 03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
Schritt für Schritt Simulation Die Atmungskette
 KENNZEICHEN: KURS - SCHULE - - Schritt für Schritt Simulation Die Atmungskette Inhalt Übersicht über das Mitochondrium und die Mitochondrienmembran S.2 Zeichenerklärung S.3 Stichwortverzeichnis S.4 Leitfaden
KENNZEICHEN: KURS - SCHULE - - Schritt für Schritt Simulation Die Atmungskette Inhalt Übersicht über das Mitochondrium und die Mitochondrienmembran S.2 Zeichenerklärung S.3 Stichwortverzeichnis S.4 Leitfaden
Outlook. sysplus.ch outlook - mail-grundlagen Seite 1/8. Mail-Grundlagen. Posteingang
 sysplus.ch outlook - mail-grundlagen Seite 1/8 Outlook Mail-Grundlagen Posteingang Es gibt verschiedene Möglichkeiten, um zum Posteingang zu gelangen. Man kann links im Outlook-Fenster auf die Schaltfläche
sysplus.ch outlook - mail-grundlagen Seite 1/8 Outlook Mail-Grundlagen Posteingang Es gibt verschiedene Möglichkeiten, um zum Posteingang zu gelangen. Man kann links im Outlook-Fenster auf die Schaltfläche
Der Fettsäurestoffwechsel. Basierend auf Stryer Kapitel 22
 Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
APP-GFP/Fluoreszenzmikroskop. Aufnahmen neuronaler Zellen, mit freund. Genehmigung von Prof. Stefan Kins, TU Kaiserslautern
 Über die Herkunft von Aβ42 und Amyloid-Plaques Heute ist sicher belegt, dass sich die amyloiden Plaques aus einer Vielzahl an Abbaufragmenten des Amyloid-Vorläufer-Proteins (amyloid-precursor-protein,
Über die Herkunft von Aβ42 und Amyloid-Plaques Heute ist sicher belegt, dass sich die amyloiden Plaques aus einer Vielzahl an Abbaufragmenten des Amyloid-Vorläufer-Proteins (amyloid-precursor-protein,
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Das große ElterngeldPlus 1x1. Alles über das ElterngeldPlus. Wer kann ElterngeldPlus beantragen? ElterngeldPlus verstehen ein paar einleitende Fakten
 Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Das große x -4 Alles über das Wer kann beantragen? Generell kann jeder beantragen! Eltern (Mütter UND Väter), die schon während ihrer Elternzeit wieder in Teilzeit arbeiten möchten. Eltern, die während
Stellen Sie bitte den Cursor in die Spalte B2 und rufen die Funktion Sverweis auf. Es öffnet sich folgendes Dialogfenster
 Es gibt in Excel unter anderem die so genannten Suchfunktionen / Matrixfunktionen Damit können Sie Werte innerhalb eines bestimmten Bereichs suchen. Als Beispiel möchte ich die Funktion Sverweis zeigen.
Es gibt in Excel unter anderem die so genannten Suchfunktionen / Matrixfunktionen Damit können Sie Werte innerhalb eines bestimmten Bereichs suchen. Als Beispiel möchte ich die Funktion Sverweis zeigen.
SICHERN DER FAVORITEN
 Seite 1 von 7 SICHERN DER FAVORITEN Eine Anleitung zum Sichern der eigenen Favoriten zur Verfügung gestellt durch: ZID Dezentrale Systeme März 2010 Seite 2 von 7 Für die Datensicherheit ist bekanntlich
Seite 1 von 7 SICHERN DER FAVORITEN Eine Anleitung zum Sichern der eigenen Favoriten zur Verfügung gestellt durch: ZID Dezentrale Systeme März 2010 Seite 2 von 7 Für die Datensicherheit ist bekanntlich
Atmungskette inklusive Komplex II
 Atmungskette inklusive Komplex II Energiegewinnung durch oxidative Phosphorylierung GW2014 Das Prinzip der Oxidativen Phosphorylierung 14_01_01_harness_energy.jpg Chemiosmotische Kopplung 2016 1 1) 2)
Atmungskette inklusive Komplex II Energiegewinnung durch oxidative Phosphorylierung GW2014 Das Prinzip der Oxidativen Phosphorylierung 14_01_01_harness_energy.jpg Chemiosmotische Kopplung 2016 1 1) 2)
Im Folgenden wird Ihnen an einem Beispiel erklärt, wie Sie Excel-Anlagen und Excel-Vorlagen erstellen können.
 Excel-Schnittstelle Im Folgenden wird Ihnen an einem Beispiel erklärt, wie Sie Excel-Anlagen und Excel-Vorlagen erstellen können. Voraussetzung: Microsoft Office Excel ab Version 2000 Zum verwendeten Beispiel:
Excel-Schnittstelle Im Folgenden wird Ihnen an einem Beispiel erklärt, wie Sie Excel-Anlagen und Excel-Vorlagen erstellen können. Voraussetzung: Microsoft Office Excel ab Version 2000 Zum verwendeten Beispiel:
1 Lerncoach. Die Atmungskette (oxidative Phosphorylierung)
 126 Die Atmungskette (oxidative Phosphorylierung) Endoxidation.4 Die Atmungskette (oxidative Phosphorylierung) 1 Lerncoach Der folgende Abschnitt verdeutlicht Ihnen Schritt für Schritt das Prinzip der
126 Die Atmungskette (oxidative Phosphorylierung) Endoxidation.4 Die Atmungskette (oxidative Phosphorylierung) 1 Lerncoach Der folgende Abschnitt verdeutlicht Ihnen Schritt für Schritt das Prinzip der
ACDSee Pro 2. ACDSee Pro 2 Tutorials: Übertragung von Fotos (+ Datenbank) auf einen anderen Computer. Über Metadaten und die Datenbank
 Tutorials: Übertragung von Fotos (+ ) auf einen anderen Computer Export der In dieser Lektion erfahren Sie, wie Sie am effektivsten Fotos von einem Computer auf einen anderen übertragen. Wenn Sie Ihre
Tutorials: Übertragung von Fotos (+ ) auf einen anderen Computer Export der In dieser Lektion erfahren Sie, wie Sie am effektivsten Fotos von einem Computer auf einen anderen übertragen. Wenn Sie Ihre
AGROPLUS Buchhaltung. Daten-Server und Sicherheitskopie. Version vom 21.10.2013b
 AGROPLUS Buchhaltung Daten-Server und Sicherheitskopie Version vom 21.10.2013b 3a) Der Daten-Server Modus und der Tresor Der Daten-Server ist eine Betriebsart welche dem Nutzer eine grosse Flexibilität
AGROPLUS Buchhaltung Daten-Server und Sicherheitskopie Version vom 21.10.2013b 3a) Der Daten-Server Modus und der Tresor Der Daten-Server ist eine Betriebsart welche dem Nutzer eine grosse Flexibilität
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis Das komplette Material finden Sie hier: Download bei School-Scout.de
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Übungsbuch für den Grundkurs mit Tipps und Lösungen: Analysis Das komplette Material finden Sie hier: Download bei School-Scout.de
Was ist Sozial-Raum-Orientierung?
 Was ist Sozial-Raum-Orientierung? Dr. Wolfgang Hinte Universität Duisburg-Essen Institut für Stadt-Entwicklung und Sozial-Raum-Orientierte Arbeit Das ist eine Zusammen-Fassung des Vortrages: Sozialräume
Was ist Sozial-Raum-Orientierung? Dr. Wolfgang Hinte Universität Duisburg-Essen Institut für Stadt-Entwicklung und Sozial-Raum-Orientierte Arbeit Das ist eine Zusammen-Fassung des Vortrages: Sozialräume
Arbeiten mit UMLed und Delphi
 Arbeiten mit UMLed und Delphi Diese Anleitung soll zeigen, wie man Klassen mit dem UML ( Unified Modeling Language ) Editor UMLed erstellt, in Delphi exportiert und dort so einbindet, dass diese (bis auf
Arbeiten mit UMLed und Delphi Diese Anleitung soll zeigen, wie man Klassen mit dem UML ( Unified Modeling Language ) Editor UMLed erstellt, in Delphi exportiert und dort so einbindet, dass diese (bis auf
Z11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
Musterlösung - Übung 5 Vorlesung Bio-Engineering Sommersemester 2008
 Aufgabe 1: Prinzipieller Ablauf der Proteinbiosynthese a) Erklären Sie folgende Begriffe möglichst in Ihren eigenen Worten (1 kurzer Satz): Gen Nukleotid RNA-Polymerase Promotor Codon Anti-Codon Stop-Codon
Aufgabe 1: Prinzipieller Ablauf der Proteinbiosynthese a) Erklären Sie folgende Begriffe möglichst in Ihren eigenen Worten (1 kurzer Satz): Gen Nukleotid RNA-Polymerase Promotor Codon Anti-Codon Stop-Codon
Würfelt man dabei je genau 10 - mal eine 1, 2, 3, 4, 5 und 6, so beträgt die Anzahl. der verschiedenen Reihenfolgen, in denen man dies tun kann, 60!.
 040304 Übung 9a Analysis, Abschnitt 4, Folie 8 Die Wahrscheinlichkeit, dass bei n - maliger Durchführung eines Zufallexperiments ein Ereignis A ( mit Wahrscheinlichkeit p p ( A ) ) für eine beliebige Anzahl
040304 Übung 9a Analysis, Abschnitt 4, Folie 8 Die Wahrscheinlichkeit, dass bei n - maliger Durchführung eines Zufallexperiments ein Ereignis A ( mit Wahrscheinlichkeit p p ( A ) ) für eine beliebige Anzahl
icloud nicht neu, aber doch irgendwie anders
 Kapitel 6 In diesem Kapitel zeigen wir Ihnen, welche Dienste die icloud beim Abgleich von Dateien und Informationen anbietet. Sie lernen icloud Drive kennen, den Fotostream, den icloud-schlüsselbund und
Kapitel 6 In diesem Kapitel zeigen wir Ihnen, welche Dienste die icloud beim Abgleich von Dateien und Informationen anbietet. Sie lernen icloud Drive kennen, den Fotostream, den icloud-schlüsselbund und
Anlegen eines DLRG Accounts
 Anlegen eines DLRG Accounts Seite 1 von 6 Auf der Startseite des Internet Service Centers (https:\\dlrg.de) führt der Link DLRG-Account anlegen zu einer Eingabemaske, mit der sich jedes DLRG-Mitglied genau
Anlegen eines DLRG Accounts Seite 1 von 6 Auf der Startseite des Internet Service Centers (https:\\dlrg.de) führt der Link DLRG-Account anlegen zu einer Eingabemaske, mit der sich jedes DLRG-Mitglied genau
puls109 Sport und Ernährungsberatung
 Vitamine Das Wichtigste in Kürze Vitamine sind für alle Prozesse des Lebens extrem wichtig. Deshalb muss man die tägliche Mindestmenge zu sich nehmen. Durch Einseitige Ernährung kann ein Mangel entstehen.
Vitamine Das Wichtigste in Kürze Vitamine sind für alle Prozesse des Lebens extrem wichtig. Deshalb muss man die tägliche Mindestmenge zu sich nehmen. Durch Einseitige Ernährung kann ein Mangel entstehen.
Erweiterung der Aufgabe. Die Notenberechnung soll nicht nur für einen Schüler, sondern für bis zu 35 Schüler gehen:
 VBA Programmierung mit Excel Schleifen 1/6 Erweiterung der Aufgabe Die Notenberechnung soll nicht nur für einen Schüler, sondern für bis zu 35 Schüler gehen: Es müssen also 11 (B L) x 35 = 385 Zellen berücksichtigt
VBA Programmierung mit Excel Schleifen 1/6 Erweiterung der Aufgabe Die Notenberechnung soll nicht nur für einen Schüler, sondern für bis zu 35 Schüler gehen: Es müssen also 11 (B L) x 35 = 385 Zellen berücksichtigt
1/6. Welche Antwort ist richtig: Wie entsteht aus organischen Kohlenstoffverbindungen das gasförmige Kohlendioxid?
 1/6 Der Kohlenstoffkreislauf Arbeitsblatt B Material: Inhalte des Factsheets Grundlagen zum Klimawandel Der Wasserkreislauf (siehe Arbeitsblatt A) ist leicht erklärt: Wasser verdunstet, in höheren Schichten
1/6 Der Kohlenstoffkreislauf Arbeitsblatt B Material: Inhalte des Factsheets Grundlagen zum Klimawandel Der Wasserkreislauf (siehe Arbeitsblatt A) ist leicht erklärt: Wasser verdunstet, in höheren Schichten
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Metabolisierung des Aminosäure-Kohlestoffgerüstes
 Metabolisierung des Aminosäure-Kohlestoffgerüstes Abbau zu 7 wichtigen Molekülen: Pyruvat, Acetyl-CoA, Acetoacetyl-CoA, -Ketoglutarat, Succinyl-CoA, Fumarat, Oxalacetat >> also zu 4 Intermediaten des Citratzyklus,
Metabolisierung des Aminosäure-Kohlestoffgerüstes Abbau zu 7 wichtigen Molekülen: Pyruvat, Acetyl-CoA, Acetoacetyl-CoA, -Ketoglutarat, Succinyl-CoA, Fumarat, Oxalacetat >> also zu 4 Intermediaten des Citratzyklus,
PCD Europe, Krefeld, Jan 2007. Auswertung von Haemoccult
 Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Grundlagen der Informatik
 Mag. Christian Gürtler Programmierung Grundlagen der Informatik 2011 Inhaltsverzeichnis I. Allgemeines 3 1. Zahlensysteme 4 1.1. ganze Zahlen...................................... 4 1.1.1. Umrechnungen.................................
Mag. Christian Gürtler Programmierung Grundlagen der Informatik 2011 Inhaltsverzeichnis I. Allgemeines 3 1. Zahlensysteme 4 1.1. ganze Zahlen...................................... 4 1.1.1. Umrechnungen.................................
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
SUPERABSORBER. Eine Präsentation von Johannes Schlüter und Thomas Luckert
 SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
1. Kennlinien. 2. Stabilisierung der Emitterschaltung. Schaltungstechnik 2 Übung 4
 1. Kennlinien Der Transistor BC550C soll auf den Arbeitspunkt U CE = 4 V und I C = 15 ma eingestellt werden. a) Bestimmen Sie aus den Kennlinien (S. 2) die Werte für I B, B, U BE. b) Woher kommt die Neigung
1. Kennlinien Der Transistor BC550C soll auf den Arbeitspunkt U CE = 4 V und I C = 15 ma eingestellt werden. a) Bestimmen Sie aus den Kennlinien (S. 2) die Werte für I B, B, U BE. b) Woher kommt die Neigung
Anwendungsbeispiele Buchhaltung
 Kostenstellen in Webling Webling ist ein Produkt der Firma: Inhaltsverzeichnis 1 Kostenstellen 1.1 Was sind Kostenstellen? 1.2 Kostenstellen in der 2 Kostenstellen in Webling 2.1 Kostenstellen erstellen
Kostenstellen in Webling Webling ist ein Produkt der Firma: Inhaltsverzeichnis 1 Kostenstellen 1.1 Was sind Kostenstellen? 1.2 Kostenstellen in der 2 Kostenstellen in Webling 2.1 Kostenstellen erstellen
Lizenzen auschecken. Was ist zu tun?
 Use case Lizenzen auschecken Ihr Unternehmen hat eine Netzwerk-Commuterlizenz mit beispielsweise 4 Lizenzen. Am Freitag wollen Sie Ihren Laptop mit nach Hause nehmen, um dort am Wochenende weiter zu arbeiten.
Use case Lizenzen auschecken Ihr Unternehmen hat eine Netzwerk-Commuterlizenz mit beispielsweise 4 Lizenzen. Am Freitag wollen Sie Ihren Laptop mit nach Hause nehmen, um dort am Wochenende weiter zu arbeiten.
Behandlung von Diabetes
 04 Arbeitsanweisung Arbeitsauftrag Anhand des Foliensatzes werden die verschiedenen Behandlungsmethoden bei Diabetes Typ 1 und Typ 2 besprochen. Anschliessend werden noch kurz die Folgen bei einer Nichtbehandlung
04 Arbeitsanweisung Arbeitsauftrag Anhand des Foliensatzes werden die verschiedenen Behandlungsmethoden bei Diabetes Typ 1 und Typ 2 besprochen. Anschliessend werden noch kurz die Folgen bei einer Nichtbehandlung
Jedes Umfeld hat seinen perfekten Antrieb. Individuelle Antriebslösungen für Windenergieanlagen.
 Jedes Umfeld hat seinen perfekten Antrieb. Individuelle Antriebslösungen für Windenergieanlagen. 1 2 3 3 4 1 2 3 4 Generator Elektromechanische Bremse Azimutantriebe Rotorlock-Antrieb (im Bild nicht sichtbar)
Jedes Umfeld hat seinen perfekten Antrieb. Individuelle Antriebslösungen für Windenergieanlagen. 1 2 3 3 4 1 2 3 4 Generator Elektromechanische Bremse Azimutantriebe Rotorlock-Antrieb (im Bild nicht sichtbar)
Was ich als Bürgermeister für Lübbecke tun möchte
 Wahlprogramm in leichter Sprache Was ich als Bürgermeister für Lübbecke tun möchte Hallo, ich bin Dirk Raddy! Ich bin 47 Jahre alt. Ich wohne in Hüllhorst. Ich mache gerne Sport. Ich fahre gerne Ski. Ich
Wahlprogramm in leichter Sprache Was ich als Bürgermeister für Lübbecke tun möchte Hallo, ich bin Dirk Raddy! Ich bin 47 Jahre alt. Ich wohne in Hüllhorst. Ich mache gerne Sport. Ich fahre gerne Ski. Ich
Guide DynDNS und Portforwarding
 Guide DynDNS und Portforwarding Allgemein Um Geräte im lokalen Netzwerk von überall aus über das Internet erreichen zu können, kommt man um die Themen Dynamik DNS (kurz DynDNS) und Portweiterleitung(auch
Guide DynDNS und Portforwarding Allgemein Um Geräte im lokalen Netzwerk von überall aus über das Internet erreichen zu können, kommt man um die Themen Dynamik DNS (kurz DynDNS) und Portweiterleitung(auch
Selbst-Test zur Vorab-Einschätzung zum Vorkurs Chemie für Mediziner
 Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Repetitionsaufgaben Wurzelgleichungen
 Repetitionsaufgaben Wurzelgleichungen Inhaltsverzeichnis A) Vorbemerkungen B) Lernziele C) Theorie mit Aufgaben D) Aufgaben mit Musterlösungen 4 A) Vorbemerkungen Bitte beachten Sie: Bei Wurzelgleichungen
Repetitionsaufgaben Wurzelgleichungen Inhaltsverzeichnis A) Vorbemerkungen B) Lernziele C) Theorie mit Aufgaben D) Aufgaben mit Musterlösungen 4 A) Vorbemerkungen Bitte beachten Sie: Bei Wurzelgleichungen
Übung 11 Genregulation bei Prokaryoten
 Übung 11 Genregulation bei Prokaryoten Konzepte: Differentielle Genexpression Positive Genregulation Negative Genregulation cis-/trans-regulation 1. Auf welchen Ebenen kann Genregulation stattfinden? Definition
Übung 11 Genregulation bei Prokaryoten Konzepte: Differentielle Genexpression Positive Genregulation Negative Genregulation cis-/trans-regulation 1. Auf welchen Ebenen kann Genregulation stattfinden? Definition
Grundlagen der Physiologie
 Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Sie werden sehen, dass Sie für uns nur noch den direkten PDF-Export benötigen. Warum?
 Leitfaden zur Druckdatenerstellung Inhalt: 1. Download und Installation der ECI-Profile 2. Farbeinstellungen der Adobe Creative Suite Bitte beachten! In diesem kleinen Leitfaden möchten wir auf die Druckdatenerstellung
Leitfaden zur Druckdatenerstellung Inhalt: 1. Download und Installation der ECI-Profile 2. Farbeinstellungen der Adobe Creative Suite Bitte beachten! In diesem kleinen Leitfaden möchten wir auf die Druckdatenerstellung
= i (V) = d 2. v = d! p! n da v 1 = v 2 gilt auch d 1 ÿ p ÿ n 1 = d 2 ÿ p ÿ n 2 (III) p kürzen (Division durch p) d 1 ÿ n 1 = d 2 ÿ n 2 (IV) oder
 v = d! p! n da v 1 = v 2 (I) (II) gilt auch d 1 ÿ p ÿ n 1 = d 2 ÿ p ÿ n 2 (III) p kürzen (Division durch p) d 1 ÿ n 1 = d 2 ÿ n 2 (IV) oder i = Übersetzungsverhältnis n 1 n 2 = d 2 d 1 = i (V) Beispiel
v = d! p! n da v 1 = v 2 (I) (II) gilt auch d 1 ÿ p ÿ n 1 = d 2 ÿ p ÿ n 2 (III) p kürzen (Division durch p) d 1 ÿ n 1 = d 2 ÿ n 2 (IV) oder i = Übersetzungsverhältnis n 1 n 2 = d 2 d 1 = i (V) Beispiel
Elektrische Energie, Arbeit und Leistung
 Elektrische Energie, Arbeit und Leistung Wenn in einem Draht ein elektrischer Strom fließt, so erwärmt er sich. Diese Wärme kann so groß sein, dass der Draht sogar schmilzt. Aus der Thermodynamik wissen
Elektrische Energie, Arbeit und Leistung Wenn in einem Draht ein elektrischer Strom fließt, so erwärmt er sich. Diese Wärme kann so groß sein, dass der Draht sogar schmilzt. Aus der Thermodynamik wissen
Diese Ansicht erhalten Sie nach der erfolgreichen Anmeldung bei Wordpress.
 Anmeldung http://www.ihredomain.de/wp-admin Dashboard Diese Ansicht erhalten Sie nach der erfolgreichen Anmeldung bei Wordpress. Das Dashboard gibt Ihnen eine kurze Übersicht, z.b. Anzahl der Beiträge,
Anmeldung http://www.ihredomain.de/wp-admin Dashboard Diese Ansicht erhalten Sie nach der erfolgreichen Anmeldung bei Wordpress. Das Dashboard gibt Ihnen eine kurze Übersicht, z.b. Anzahl der Beiträge,
Vorgestellt von Hans-Dieter Stubben
 Neue Lösungen in der GGf-Versorgung Vorgestellt von Hans-Dieter Stubben Geschäftsführer der Bundes-Versorgungs-Werk BVW GmbH Verbesserungen in der bav In 2007 ist eine wichtige Entscheidung für die betriebliche
Neue Lösungen in der GGf-Versorgung Vorgestellt von Hans-Dieter Stubben Geschäftsführer der Bundes-Versorgungs-Werk BVW GmbH Verbesserungen in der bav In 2007 ist eine wichtige Entscheidung für die betriebliche
Anleitung über den Umgang mit Schildern
 Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
sm@rt-tan plus Flickerfeld bewegt sich nicht
 Technischer Hintergrund Um die Verwendung des Verfahrens Sm@rt-TAN plus des neuen sicheren TAN- Verfahrens so komfortabel wie möglich zu gestalten, wurde eine Möglichkeit geschaffen, die Angaben einer
Technischer Hintergrund Um die Verwendung des Verfahrens Sm@rt-TAN plus des neuen sicheren TAN- Verfahrens so komfortabel wie möglich zu gestalten, wurde eine Möglichkeit geschaffen, die Angaben einer
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Sowohl die Malstreifen als auch die Neperschen Streifen können auch in anderen Stellenwertsystemen verwendet werden.
 Multiplikation Die schriftliche Multiplikation ist etwas schwieriger als die Addition. Zum einen setzt sie das kleine Einmaleins voraus, zum anderen sind die Überträge, die zu merken sind und häufig in
Multiplikation Die schriftliche Multiplikation ist etwas schwieriger als die Addition. Zum einen setzt sie das kleine Einmaleins voraus, zum anderen sind die Überträge, die zu merken sind und häufig in
1. Einführung 2. 2. Erstellung einer Teillieferung 2. 3. Erstellung einer Teilrechnung 6
 Inhalt 1. Einführung 2 2. Erstellung einer Teillieferung 2 3. Erstellung einer Teilrechnung 6 4. Erstellung einer Sammellieferung/ Mehrere Aufträge zu einem Lieferschein zusammenfassen 11 5. Besonderheiten
Inhalt 1. Einführung 2 2. Erstellung einer Teillieferung 2 3. Erstellung einer Teilrechnung 6 4. Erstellung einer Sammellieferung/ Mehrere Aufträge zu einem Lieferschein zusammenfassen 11 5. Besonderheiten
Platinen mit dem HP CLJ 1600 direkt bedrucken ohne Tonertransferverfahren
 Platinen mit dem HP CLJ 1600 direkt bedrucken ohne Tonertransferverfahren Um die Platinen zu bedrucken, muß der Drucker als allererstes ein wenig zerlegt werden. Obere und seitliche Abdeckungen entfernen:
Platinen mit dem HP CLJ 1600 direkt bedrucken ohne Tonertransferverfahren Um die Platinen zu bedrucken, muß der Drucker als allererstes ein wenig zerlegt werden. Obere und seitliche Abdeckungen entfernen:
Südbaden-Cup. Ausstieg Champions
 Südbaden-Cup Ausstieg Champions Beschreibung Der Ausstieg aus dem Turnier dient Spielern die eine weite Anreise haben sich aus dem Turnier zu verabschieden um noch am gleichen Tag heimzureisen und einen
Südbaden-Cup Ausstieg Champions Beschreibung Der Ausstieg aus dem Turnier dient Spielern die eine weite Anreise haben sich aus dem Turnier zu verabschieden um noch am gleichen Tag heimzureisen und einen
Zahlenwinkel: Forscherkarte 1. alleine. Zahlenwinkel: Forschertipp 1
 Zahlenwinkel: Forscherkarte 1 alleine Tipp 1 Lege die Ziffern von 1 bis 9 so in den Zahlenwinkel, dass jeder Arm des Zahlenwinkels zusammengezählt das gleiche Ergebnis ergibt! Finde möglichst viele verschiedene
Zahlenwinkel: Forscherkarte 1 alleine Tipp 1 Lege die Ziffern von 1 bis 9 so in den Zahlenwinkel, dass jeder Arm des Zahlenwinkels zusammengezählt das gleiche Ergebnis ergibt! Finde möglichst viele verschiedene
Inhalt 1. Was wird gefördert? Bausparverträge
 Inhalt 1. Was wird gefördert? 2. Wie viel Prozent bringt das? 3. In welchem Alter ist das sinnvoll? 4. Wie viel muss man sparen? 5. Bis zu welchem Einkommen gibt es Förderung? 6. Wie groß sollten die Verträge
Inhalt 1. Was wird gefördert? 2. Wie viel Prozent bringt das? 3. In welchem Alter ist das sinnvoll? 4. Wie viel muss man sparen? 5. Bis zu welchem Einkommen gibt es Förderung? 6. Wie groß sollten die Verträge
Einfügen von Bildern innerhalb eines Beitrages
 Version 1.2 Einfügen von Bildern innerhalb eines Beitrages Um eigene Bilder ins Forum einzufügen, gibt es zwei Möglichkeiten. 1.) Ein Bild vom eigenem PC wird auf den Webspace von Baue-die-Bismarck.de
Version 1.2 Einfügen von Bildern innerhalb eines Beitrages Um eigene Bilder ins Forum einzufügen, gibt es zwei Möglichkeiten. 1.) Ein Bild vom eigenem PC wird auf den Webspace von Baue-die-Bismarck.de
Individuelle Formulare
 Individuelle Formulare Die Vorlagen ermöglichen die Definition von Schnellerfassungen für die Kontenanlage sowie für den Im- und Export von Stammdaten. Dabei kann frei entschieden werden, welche Felder
Individuelle Formulare Die Vorlagen ermöglichen die Definition von Schnellerfassungen für die Kontenanlage sowie für den Im- und Export von Stammdaten. Dabei kann frei entschieden werden, welche Felder
Stellvertretenden Genehmiger verwalten. Tipps & Tricks
 Tipps & Tricks INHALT SEITE 1. Grundlegende Informationen 3 2.1 Aktivieren eines Stellvertretenden Genehmigers 4 2.2 Deaktivieren eines Stellvertretenden Genehmigers 11 2 1. Grundlegende Informationen
Tipps & Tricks INHALT SEITE 1. Grundlegende Informationen 3 2.1 Aktivieren eines Stellvertretenden Genehmigers 4 2.2 Deaktivieren eines Stellvertretenden Genehmigers 11 2 1. Grundlegende Informationen
Oxidative Phosphorylierung
 BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
BICEMIE DER ERÄRUG II Grundzüge des Metabolismus xidative Phosphorylierung 24.04.2012 xidative Phosphorylierung xidative Phosphorylierung -Die Elektronen in AD und in FAD 2 (hohes Übertragungspotential)
XT Großhandelsangebote
 XT GROßHANDELSANGEBOTE XT Großhandelsangebote Die neuen XT- Großhandelsangebote bieten Ihnen eine große Anzahl an Vereinfachungen und Verbesserungen, z.b. Großhandelsangebote werden zum Stichtag automatisch
XT GROßHANDELSANGEBOTE XT Großhandelsangebote Die neuen XT- Großhandelsangebote bieten Ihnen eine große Anzahl an Vereinfachungen und Verbesserungen, z.b. Großhandelsangebote werden zum Stichtag automatisch
Atmung Respiration 1
 Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
Atmung Respiration 1 Atmung Die oxidative Phosphorylierung ist der letzte Schritt einer Serie von Energieumwandlungen, die insgesamt als Zellatmung oder einfach Atmung (Respiration) bezeichnet werden 2
DER SELBST-CHECK FÜR IHR PROJEKT
 DER SELBST-CHECK FÜR IHR PROJEKT In 30 Fragen und 5 Tipps zum erfolgreichen Projekt! Beantworten Sie die wichtigsten Fragen rund um Ihr Projekt für Ihren Erfolg und für Ihre Unterstützer. IHR LEITFADEN
DER SELBST-CHECK FÜR IHR PROJEKT In 30 Fragen und 5 Tipps zum erfolgreichen Projekt! Beantworten Sie die wichtigsten Fragen rund um Ihr Projekt für Ihren Erfolg und für Ihre Unterstützer. IHR LEITFADEN
Die Notare. Reform des Zugewinnausgleichsrechts
 Die Notare informieren Reform des Zugewinnausgleichsrechts Dr. Martin Kretzer & Dr. Matthias Raffel Großer Markt 28 66740 Saarlouis Telefon 06831/ 94 98 06 und 42042 Telefax 06831/ 4 31 80 2 Info-Brief
Die Notare informieren Reform des Zugewinnausgleichsrechts Dr. Martin Kretzer & Dr. Matthias Raffel Großer Markt 28 66740 Saarlouis Telefon 06831/ 94 98 06 und 42042 Telefax 06831/ 4 31 80 2 Info-Brief
Wasserkraft früher und heute!
 Wasserkraft früher und heute! Wasserkraft leistet heute einen wichtigen Beitrag zur Stromversorgung in Österreich und auf der ganzen Welt. Aber war das schon immer so? Quelle: Elvina Schäfer, FOTOLIA In
Wasserkraft früher und heute! Wasserkraft leistet heute einen wichtigen Beitrag zur Stromversorgung in Österreich und auf der ganzen Welt. Aber war das schon immer so? Quelle: Elvina Schäfer, FOTOLIA In
Beispiel Shop-Eintrag Ladenlokal & Online-Shop im Verzeichnis www.wir-lieben-shops.de 1
 Beispiel Shop-Eintrag Ladenlokal & Online-Shop. Als Händler haben Sie beim Shop-Verzeichnis wir-lieben-shops.de die Möglichkeit einen oder mehrere Shop- Einträge zu erstellen. Es gibt 3 verschiedene Typen
Beispiel Shop-Eintrag Ladenlokal & Online-Shop. Als Händler haben Sie beim Shop-Verzeichnis wir-lieben-shops.de die Möglichkeit einen oder mehrere Shop- Einträge zu erstellen. Es gibt 3 verschiedene Typen
Ernährungsinformationen0
 Ernährungsinformationen AllgemeinePunkte: SportlersolltenjedenTageinwertvollesFrühstückessen 3MahlzeitenproTag o Zwischenmahlzeitensollten gesund sein. Nüsse Obst/Gemüse Snacks(nurwennmankeinGewichtverlierenmöchte)
Ernährungsinformationen AllgemeinePunkte: SportlersolltenjedenTageinwertvollesFrühstückessen 3MahlzeitenproTag o Zwischenmahlzeitensollten gesund sein. Nüsse Obst/Gemüse Snacks(nurwennmankeinGewichtverlierenmöchte)
Kara-Programmierung AUFGABENSTELLUNG LERNPARCOURS. Abb. 1: Programmfenster. Welt neu erstellen; öffnen; erneut öffnen; speichern; speichern unter
 Kara-Programmierung AUFGABENSTELLUNG LERNPARCOURS Abb. 1: Programmfenster Welt neu erstellen; öffnen; erneut öffnen; speichern; speichern unter Programmfenster anzeigen Einstellungen öffnen Kara direkt
Kara-Programmierung AUFGABENSTELLUNG LERNPARCOURS Abb. 1: Programmfenster Welt neu erstellen; öffnen; erneut öffnen; speichern; speichern unter Programmfenster anzeigen Einstellungen öffnen Kara direkt
40-Tage-Wunder- Kurs. Umarme, was Du nicht ändern kannst.
 40-Tage-Wunder- Kurs Umarme, was Du nicht ändern kannst. Das sagt Wikipedia: Als Wunder (griechisch thauma) gilt umgangssprachlich ein Ereignis, dessen Zustandekommen man sich nicht erklären kann, so dass
40-Tage-Wunder- Kurs Umarme, was Du nicht ändern kannst. Das sagt Wikipedia: Als Wunder (griechisch thauma) gilt umgangssprachlich ein Ereignis, dessen Zustandekommen man sich nicht erklären kann, so dass
Abituraufgabe zur Stochastik, Hessen 2009, Grundkurs (TR)
 Abituraufgabe zur Stochastik, Hessen 2009, Grundkurs (TR) Eine Firma stellt USB-Sticks her. Sie werden in der Fabrik ungeprüft in Packungen zu je 20 Stück verpackt und an Händler ausgeliefert. 1 Ein Händler
Abituraufgabe zur Stochastik, Hessen 2009, Grundkurs (TR) Eine Firma stellt USB-Sticks her. Sie werden in der Fabrik ungeprüft in Packungen zu je 20 Stück verpackt und an Händler ausgeliefert. 1 Ein Händler
