Übungen zur Nomenklatur: Zeichne die Formeln auf ein leeres kariertes Blatt und benenne die einzelnen Formeln.
|
|
|
- Hannelore Peters
- vor 6 Jahren
- Abrufe
Transkript
1 Übungen zur Nomenklatur: Zeichne die Formeln auf ein leeres kariertes Blatt und benenne die einzelnen Formeln. Einfache Formeln, Verzweigungen, längste Kette, Nummerierung Nr Formel Name A1 Propan 3 2 A Butan A Butan A4 leicht 3 2 Methylpropan A Methylbutan A Methylbutan A7 2-Methylbutan 2 A8 2,2 Dimethylpropan A9 3 2 Methylbutan 2 Seite 1 von 9
2 A10 2,2,4 Trimethylpentan 2 A11 2,2,3,4 Tetramethylpentan A12 2,3,4 Trimethylhexan 2 A13 2,3,4,5 Tetramethylhexan A ,4,5 Trimethyl-3- propylhexan A15 2,2,3,3,4,4,5,5,6,6 Decamethylheptan A16 2,2,3,3,4,4,5,5,6,6 Decamethylheptan 3 3 Seite 2 von 9
3 A17 2,3,4,6,8,9 examethyldecan 2 2 Mittlere Formeln Alkane, Verzweigungen mit verschiedenen Alkylgruppen, verzweigte Seitenkette B1 =A ,4,5 Trimethyl-3- propylhexan B2 4 Ethyl-2,3-Dimethylheptan B3 2,3,5 Trimethyl-4- propyloctan B4 2,3 Dimethyl-4,5- Dipropylnonan B5 2 Trimethylheptan 4,5 Diethyl-2,3,4-2 2 Seite 3 von 9
4 B6 2 2 Trimethyloctan 4,5 Diethyl-2,3,4-2 2 B Ethyl-5-Propyl-2,3,4,6- Tetramethylheptan Ebenso 4 Ethyl-3-Propyl-2,4,5,6- Tetramethylheptan B Ethyl-3-Propyl-2,4,6- Trimethylheptan 2 2 B Butyl-4-Ethyl-2,3,4,9- Tetramethyl-6-Propyldecan B ,5 Diethyl-2,3,4- Trimethyloctan B ,4 Diethyl-3,4,6- Trimethyloctan Seite 4 von 9
5 B12 2,3,4,4,6 Pentamethylheptan 2 B13 2,2,4,4,5,6 examethylheptan 2 B14 2,3,4,6,7 Pentamethyl-4(2- Methylpropyl)-octan 2 2 B15 1 Methyl-2(1 Methylpropyl)- yclohexan B16 4(2-Methylbutyl)-2,3,4,6,7 Pentamethyloctan B17 4(2,3Dimethylbutyl)- 2,3,4,6,7 Pentamethyloctan 2 2 Seite 5 von 9
6 B18 2,3,6,7 Tetramethyl- 4,4 Di(2 Methylpropyl)octan Mittlere Formeln Alkene und Alkine mit Verzweigungen und verschiedenen Alkylgruppen, E/Z Konfiguration 1 (E)-3-Methylpent-2-en (Z)-3-Ethyl-4-Methylpent-2-en (Z)- 4-Methyl-3-propyl-pent-2- en 4 2 (Z) 3(1-Methylethyl)-5- Methylhex-2-en Längste Kette mit Doppelbindung; en höhere Priorität als Alkylrest kleinere Nummer en; 1. Unterschied entscheidet Priorität zwei Alternativen en kleiner als Zuerst niedrigste Summe, bei in exa-1-en-3,5-diin Zuerst niedrigste Summe, bei zwei Alternativen en kleiner als in epta-5-en-1,3-diin Seite 6 von 9
7 (E,Z) 3-Methylocta-2,6-dien (Z) 4(1-Methylethyl)-6- Methylhepta-3-en Längste Kette mit Doppelbindung; en höhere Priorität als Alkylrest kleinere Nummer en; 1. Unterschied entscheidet Priorität 9 2-exylbuta-1,3-dien ,4-Dimethylcyclopenta-1,3- dien 1-Methyl-4(2-Methylpropyl)- cyclopenta-1,3-dien (E)-2(2-Ethylbutyl)-Penta-1,3- dien Methyl-nona-2,6-dien-4-in epta-1,2,4,5-tetraen Seite 7 von 9
8 Formeln der Alkane, Alkene und Alkine mit Verzweigungen und verschiedenen Substituenten wie Alkohole, Aldehyde, Ketone, arbonsäuren D1 3 Butan-2,3-diol D2 3 3-ydroxybutan-2-on D3 3 Butandion D4 3-ydroxy-2-oxobutanal der 3-ydroxybutan-2-onal D5 2,3-Dihydroxybutanal D6 2,3-Dihydroxybutansäure D7 2-ydroxy-3-oxobutansäure der 2ydroxybutan-2-onsäure D8 2,3-Dioxobutansäure der Butandionsäure D9 2 3,4-Dimethylhexan-2-ol 3 D Ethyl-3-ydroxy-4,5- Dimethylhexan-2-on Kleinste Nummer on; hydroxy wegen on, Reihenfolge Alphabet Seite 8 von 9
9 D11 D12 Br 2 l Br F l F Brom-8-hlor-5-ethyl-7- Fluor-7-ydroxy-6-oxo-5- Propyl-octa-2-enal Nummer wegen al =1 höchste Priorität; Reihenfolge alphabetisch 1-Brom-1-hlor-4-ethyl-2- Fluor-2-ydroxy-4-Propyl-octa- 6-en-2-on Nummer wegen on =3 höchste Priorität; Reihenfolge alphabetisch D Pentandisäure D14 2-Amino-3-ydroxypropansäure 2 N D Ethansäurepropylester D16 D17 D18 D Seite 9 von 9
Systematische Nomenklatur
 Systematische Nomenklatur Je größer eine chemische Verbindung wird, desto komplizierter wird in der Regel deren Struktur, und desto schwieriger wird es, diese Verbindung eindeutig zu benennen. Dieses Problem
Systematische Nomenklatur Je größer eine chemische Verbindung wird, desto komplizierter wird in der Regel deren Struktur, und desto schwieriger wird es, diese Verbindung eindeutig zu benennen. Dieses Problem
I. Alkane Homologe Reihe, Nomenklatur
 Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
Organische Chemie Grundkurs (11. Klasse) Theorie und Übungen I. Alkane omologe Reihe, Nomenklatur omologe Reihe der Alkane Aufgabe: Setzen Sie die Tabelle fort Name Summenformel Struktur Rest Methan C
IUPAC Nomenklatur. Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten. Feld 2: Stammname der Verbindung
 Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten Feld 2: Stammname der Verbindung Feld 3: Grad der Ungesättigtheit Feld 4: funktionelle Gruppe mit höchster
Der Name eines Moleküls wird in 4 Felder aufgeteilt: Feld 1: Name und Position von Substituenten Feld 2: Stammname der Verbindung Feld 3: Grad der Ungesättigtheit Feld 4: funktionelle Gruppe mit höchster
Organik KOMPAKT Organik Blatt 1/5
 rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
rganik KMPAKT rganik Blatt 1/5 1 Elemente in organischen Verbindungen Kohlenstoff () Sauerstoff () Wasserstoff () Stickstoff (N) Phosphor (P) Schwefel (S) Kohlenstoff kommt immer in organischen Verbindungen
Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel!
 Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel! Prof. Dr. Ivo C. Ivanov Einführung (interaktive Vorlesung) Die genaue Benennung organischer Verbindungen nach
Nomenklatur organischer Verbindungen nach den IUPAC-Regeln Hier findest Du die Zauberformel! Prof. Dr. Ivo C. Ivanov Einführung (interaktive Vorlesung) Die genaue Benennung organischer Verbindungen nach
n Pentan 2- Methylbutan 2,2, dimethylpropan ( Wasserstoffatome sind nicht berücksichtigt )
 Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Grundwissen : 10 Klasse G8 Kohlenwasserstoffe Alkane Einfachbindung (σ -Bindung, kovalente Bindung ) : Zwischen Kohlenstoffatomen überlappen halbbesetzte p- Orbitale oder zwischen Kohlenstoff- und Wasserstoffatomen
Benennung (Nomenklatur) von Alkanen. zusammengestellt von W. Habelitz-Tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S.
 Benennung (Nomenklatur) von Alkanen zusammengestellt von W. abelitz-tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S. 34 + 35 istorische Entwicklung ursprünglich: Trivialnamen für viele Stoffe, z.
Benennung (Nomenklatur) von Alkanen zusammengestellt von W. abelitz-tkotz in Anlehnung an Galvani 3, Oldenbourg-Verlag, S. 34 + 35 istorische Entwicklung ursprünglich: Trivialnamen für viele Stoffe, z.
Kennsilbe. -an. -en -in. -yl. -ol. -al (VI) -on. (VII) -säure (VIII)
 Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Hinweise und Übungen zur Nomenklatur (Benennung) organischer Verbindungen Die Vielfalt organischer Verbindungen ist im Gegensatz zur anorganischen hemie durch wenige Elemente aber zahlreiche Strukturmöglichkeiten
Systematische Nomenklatur
 Systematische Nomenklatur IUPAC-Nomenklatur Alle Verbindungen sind Derivate der längsten im Molekül vorkommenden Kohlenstoff-Kette. Von der Kette abzweigende Gruppen werden als Vorsilben angefügt. Die
Systematische Nomenklatur IUPAC-Nomenklatur Alle Verbindungen sind Derivate der längsten im Molekül vorkommenden Kohlenstoff-Kette. Von der Kette abzweigende Gruppen werden als Vorsilben angefügt. Die
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
L.9 Organische Chemie I
 L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
L.9 rganische hemie I 9.1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan und iso-butan):
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Alkane und Cycloalkane
 Systematik und Nomenklatur Alkane und ycloalkane einfachstes Alkan: Methan 4 Summenformel Strukturformel schrittweise Verlängerung um eine - 2 - Einheit homologe Reihe rganische hemie I 1 Alkane Gesättigte
Systematik und Nomenklatur Alkane und ycloalkane einfachstes Alkan: Methan 4 Summenformel Strukturformel schrittweise Verlängerung um eine - 2 - Einheit homologe Reihe rganische hemie I 1 Alkane Gesättigte
Station 1: Nomenklatur von Alkanen
 Station 1: Nomenklatur von Alkanen Station 1: Nomenklatur von Alkanen 1. a) 3-Ethyl-2-methylpentan e) 2,2-Dimethylpropan b) 3-Ethyl-2-methylpentan f) 2,3,5-Trimethylhexan c) 2,3,5-Trimethylhexan g) 2,3-Dimethylbutan
Station 1: Nomenklatur von Alkanen Station 1: Nomenklatur von Alkanen 1. a) 3-Ethyl-2-methylpentan e) 2,2-Dimethylpropan b) 3-Ethyl-2-methylpentan f) 2,3,5-Trimethylhexan c) 2,3,5-Trimethylhexan g) 2,3-Dimethylbutan
Z 8 EINFÜHRUNG IN DIE ORGANISCHE CHEMIE 1) DEFINITIONEN 2) ELEMENTE UND BINDUNGEN. Organische Chemie. Kunstoffe. Farbstoffe
 EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
Homologe Reihe der Alkane. Benennung der Alkane. Konstitutionsisomerie. Isomerie. Was versteht man unter der Homologen Reihe der Alkane?
 Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Grundwissen hemie: NTG 10 1/24 omologe eihe der Alkane Was versteht man unter der omologen eihe der Alkane? Grundwissen hemie: NTG 10 2/24 Benennung der Alkane Benenne die ersten zwölf Vertreter aus der
Organische Chemie. Einstieg. Chemie-Formeldarstellungen. Formeldarstellungen der Chemie: Bei Ionenverbindungen: Verhältnisformeln. , AlF 3. etc.
 Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Organische Chemie Einstieg Chemie-Formeldarstellungen Formeldarstellungen der Chemie: Textuelle Darstellungen: Bei Ionenverbindungen: Verhältnisformeln Bsp: NaCl; CaBr 2, AlF 3 etc. Bei Molekülverbindungen:
Kohlenstoffverbindungen
 Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Kohlenstoffverbindungen Zusammenfassung Im 19. Jahrhundert begann man die Zusammensetzung von Naturstoffen zu untersuchen. Dieser Zweig der hemie wird Organische hemie genannt. Ursprünglich glaubte man,
Clara Schumann -Gymnasium Grundlagen der organischen Chemie
 1 lara Schumann -Gymnasium Grundlagen der organischen hemie Ein Leitprogramm für den Grundlagen-hemieunterricht der Sekundarstufe II Dr. Daniel Bürgisser Neue Kantonsschule Aarau Revision 2003 Modifiziert:
1 lara Schumann -Gymnasium Grundlagen der organischen hemie Ein Leitprogramm für den Grundlagen-hemieunterricht der Sekundarstufe II Dr. Daniel Bürgisser Neue Kantonsschule Aarau Revision 2003 Modifiziert:
Vorlesung 5. Alkane. Experimentalchemie, Prof. H. Mayr 20 Achtung Lückentext. Nur als Begleittext zur Vorlesung geeignet. Anzahl C-Atome im n-alkan
 Vorlesung 5. Alkane Verbindungen aus Kohlenstoff und Wasserstoff, die nur Einfachbindungen enthalten, nennt man gesättigte Kohlenwasserstoffe. Sie sind ein auptbestandteil von Erdgas und Erdöl. Liegen
Vorlesung 5. Alkane Verbindungen aus Kohlenstoff und Wasserstoff, die nur Einfachbindungen enthalten, nennt man gesättigte Kohlenwasserstoffe. Sie sind ein auptbestandteil von Erdgas und Erdöl. Liegen
1. Nomenklatur (Fettgedruckt...IUPAC Namen) 1.1. Alkane
 rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG. omenklatur (Fettgedruckt...IUPA amen).. Alkane Die längste Kohlenstoffkette wird bestimmt und daraus ergibt sich der ame Alkan:
rganisch-chemisches Proseminar für Molekulargenetiker und Mikrobiologen AAG. omenklatur (Fettgedruckt...IUPA amen).. Alkane Die längste Kohlenstoffkette wird bestimmt und daraus ergibt sich der ame Alkan:
Zur Benennung organischer Moleküle
 Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Zur Benennung organischer Moleküle Beispiele und Übungen Funktionelle Gruppen Es sind Atomgruppen in organischen Verbindungen. Sie verändern die Stoffeigenschaften und das Reaktionsverhalten des Ausgangskohlenwasserstoffs.
Skript zur Vorlesung Organische Chemie (Prof. M. Albrecht) an der RWTH Aachen
 Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
Skript zur Vorlesung rganische hemie (Prof. M. Albrecht) an der WT Aachen Erstellt von: Michael Müller Erstellungsdatum: 23.01.2004 e-mail: michael.mueller@rwth-aachen.de Nomenklatur und Isomerie organischer
I. Theoretischer Teil. 2. Synthese aryl-substituierter Cyclopentadiene Praktischer Nutzen von Pentaarylcyclopentadienderivaten 4
 Inhaltsverzeichnis I. Theoretischer Teil 1. Einleitung und Problemstellung 1 2. Synthese aryl-substituierter Cyclopentadiene 4 2.1. Praktischer Nutzen von Pentaarylcyclopentadienderivaten 4 2.2. Palladium-katalysierte
Inhaltsverzeichnis I. Theoretischer Teil 1. Einleitung und Problemstellung 1 2. Synthese aryl-substituierter Cyclopentadiene 4 2.1. Praktischer Nutzen von Pentaarylcyclopentadienderivaten 4 2.2. Palladium-katalysierte
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Übungsbeispiele Kapitel Organische Verbindungen
 Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
Übungsbeispiele 26. 1. 2016 Kapitel rganische Verbindungen 10) (9 Punkte) Schreiben Sie Valenzstrichformeln für folgende Substanzen: 3-Methyl-1-hepten, 2E-Nonen-4,5-diol-6-on, 2,3-Dihydroxybutandisäure,
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
Grundwissen 10. Klasse NTG 1
 Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Grundwissen 10. Klasse NTG 1 1. rganische hemie = Kohlenstoffchemie rganische Verbindungen sind Kohlenstoffverbindungen. Ausnahmen:, 2, Kohlensäure, arbonate; 2. Eigenschaften organischer Verbindungen
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Einführung in die Organische Chemie. Benjamin Grimm
 Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Einführung in die Organische Chemie Benjamin Grimm Gliederung Einführung: Begriff der organischen Chemie Synthese organischer Stoffe: Cracken von Erdöl Organische Stoffklassen Isomerie Orbitalmodell: Hybridisierung
Die Kohlenwasserstoffe und ihre Nomenklatur
 Die Kohlenwasserstoffe und ihre Nomenklatur Ein Leitprogramm für die hemie Autor Beratung Dr. Georg Graf Prof. Dr. Antonio Togni, ETZ Leitprogramm Nomenklatur Adressaten Gymnasiasten ab 2. Schuljahr im
Die Kohlenwasserstoffe und ihre Nomenklatur Ein Leitprogramm für die hemie Autor Beratung Dr. Georg Graf Prof. Dr. Antonio Togni, ETZ Leitprogramm Nomenklatur Adressaten Gymnasiasten ab 2. Schuljahr im
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
F.-94,3 C, Kp.68,6 C, D.0,660 Heptan CH 3. F.28,5 C, Kp.303 C, D.0,775(30 ) Nonadecan CH 3. F.32 C, Kp.330 C, D.0,772(40 ) Eicosan CH 3
 Kohlenwasserstoffe 1 Alkane Unverzweigte Alkane Methan CH 4 F.-184 C, Kp.-164 C, LW.0 Ethan CH 3 F.-172 C, Kp.-88,5 C, LW.47 Propan CH 3 F.-190 C, Kp.-42,1 C Butan CH 3 F.-135 C, Kp.0,6 C Pentan CH 3 F.-131
Kohlenwasserstoffe 1 Alkane Unverzweigte Alkane Methan CH 4 F.-184 C, Kp.-164 C, LW.0 Ethan CH 3 F.-172 C, Kp.-88,5 C, LW.47 Propan CH 3 F.-190 C, Kp.-42,1 C Butan CH 3 F.-135 C, Kp.0,6 C Pentan CH 3 F.-131
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Grundwissen Chemie 10. Klasse SG
 Grundwissen hemie 10. Klasse SG Molekülstruktur und Stoffeigenschaften Elektronegativität - Abkürzung: EN - relatives Maß für die Fähigkeit eines Atoms, in einer chemischen Bindung das Bindungselektronenpaar
Grundwissen hemie 10. Klasse SG Molekülstruktur und Stoffeigenschaften Elektronegativität - Abkürzung: EN - relatives Maß für die Fähigkeit eines Atoms, in einer chemischen Bindung das Bindungselektronenpaar
Grundwissen Chemie Jahrgangsstufe 10 (NTG)
 Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Grundwissen Chemie Jahrgangsstufe 10 (NTG) Die organische Chemie ist die Chemie des Kohlenstoffs und seiner Verbindungen. Kohlenstoffkreislauf ATMSPHÄE (C 2 ) BISPHÄE (Lebewesen) LITHSPHÄE HYDSPHÄE (Gesteine)
Vorlesung Chemie für Biologen: Klausur 1 WS Sa
 1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
1 Vorlesung Chemie für Biologen: Klausur 1 WS 02-03 Sa 07.12.02 Name:... Ihre Unterschrift:... Vorname:... Matrikel-Nr.:... Studienbeginn: SS: WS:...... Tutor der Übungen: (Dort Klausureinsicht.) Punkteschlüssel
Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik
 Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik 34 Geben Sie die systematischen Namen jeder der folgenden Verbindungen an: Welche der Verbindungen aus Übung besitzen E- und
Kapitel 3 Alkene Struktur, Nomenklatur, Reaktivität Thermodynamik und Kinetik 34 Geben Sie die systematischen Namen jeder der folgenden Verbindungen an: Welche der Verbindungen aus Übung besitzen E- und
Grundwissen Chemie 10. Jahrgangsstufe
 Grundwissen Chemie 10. Jahrgangsstufe 1. Kohlenwasserstoffe - Alkane gesättigte Kohlenwasserstoffe (nur Einfachbindungen) mit der allgemeinen Summenformel C n H 2n+2 homologe Reihe (= Gruppe chemisch verwandter
Grundwissen Chemie 10. Jahrgangsstufe 1. Kohlenwasserstoffe - Alkane gesättigte Kohlenwasserstoffe (nur Einfachbindungen) mit der allgemeinen Summenformel C n H 2n+2 homologe Reihe (= Gruppe chemisch verwandter
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Übungsaufgaben: Alkohole und Aldehyde/Ketone
 Übungsaufgaben: Alkohole und Aldehyde/Ketone 15.12.06 1. Alkohol und Schwefelsäure Propan-1-ol wird mit bzw. in Gegenwart von verdünnter Schwefelsäure zur Reaktion gebracht. Geben Sie die Reaktionen für
Übungsaufgaben: Alkohole und Aldehyde/Ketone 15.12.06 1. Alkohol und Schwefelsäure Propan-1-ol wird mit bzw. in Gegenwart von verdünnter Schwefelsäure zur Reaktion gebracht. Geben Sie die Reaktionen für
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2.1 Homologe Reihe, Nomenklatur, Konstitution, Konformation CH 2
 Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler. Alkane.1 omologe Reihe, Nomenklatur, Konstitution, Konformation.1.1 omologe Reihe
Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler. Alkane.1 omologe Reihe, Nomenklatur, Konstitution, Konformation.1.1 omologe Reihe
Rupprecht-Gymnasium München Fachschaft Chemie
 Rupprecht-Gymnasium München Fachschaft Chemie Grundwissen der 10. Klasse NTG In der Jahrgangsstufe 10 erwerben die Schüler folgendes Grundwissen: Sie kennen die wichtigsten Alkane, Alkene und Alkine, können
Rupprecht-Gymnasium München Fachschaft Chemie Grundwissen der 10. Klasse NTG In der Jahrgangsstufe 10 erwerben die Schüler folgendes Grundwissen: Sie kennen die wichtigsten Alkane, Alkene und Alkine, können
Stoffklasse Alkane Alkene/Alkine Aromaten
 Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
Stoffklasse Alkane Alkene/Alkine Aromaten funktionelle Gruppe Bezeichnung Einfachbindung Doppel-/Dreifachbindung aromatisches System Präfix Alkyl- Alkenyl/Alkinyl- Phenyl- Suffix -alkan -en/-in -Benzol
Nomenklatur. 2. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen. 3,3,4,4-Tetramethylheptan
 Nomenklatur Alkane. Ermittle die längte Kohlenstoffkette Stammname 8 8 8 -Methyloctan -Ethyloctan -Propyloctan. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen
Nomenklatur Alkane. Ermittle die längte Kohlenstoffkette Stammname 8 8 8 -Methyloctan -Ethyloctan -Propyloctan. Nummerierung der Kette dergestalt, dass die Substituenten möglichst niedrige Ziffern bekommen
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
1. Nennen Sie die drei wichtigen Bindungstypen und die zwei wichtigen Typen von Atomverbänden.
 6. Bindungslehre 6.2 Wie verbinden sich Atome? 1. Nennen Sie die drei wichtigen Bindungstypen und die zwei wichtigen Typen von Atomverbänden. 6.3 Metallbindung 1. Nennen Sie fünf charakteristische Eigenschaften
6. Bindungslehre 6.2 Wie verbinden sich Atome? 1. Nennen Sie die drei wichtigen Bindungstypen und die zwei wichtigen Typen von Atomverbänden. 6.3 Metallbindung 1. Nennen Sie fünf charakteristische Eigenschaften
2. Alkane. Allgemeines Nomenklatur + Konstitutionsisomerie Konformationsisomerie Industrielle Bedeutung Synthetische Darstellung Reaktionen der Alkane
 2. Alkane Allgemeines Nomenklatur + Konstitutionsisomerie Konformationsisomerie Industrielle Bedeutung Synthetische Darstellung Reaktionen der Alkane OC I Lehramt F. H. Schacher 1 Allgemeines Kohlenwasserstoffe
2. Alkane Allgemeines Nomenklatur + Konstitutionsisomerie Konformationsisomerie Industrielle Bedeutung Synthetische Darstellung Reaktionen der Alkane OC I Lehramt F. H. Schacher 1 Allgemeines Kohlenwasserstoffe
1. Methan 2 1.1. Eigenschaften und Zusammensetzung 2 1.2. Molekülstruktur 2 1.3. Vorkommen und Bedeutung 2
 A l k a n e 1. Methan 2 1.1. Eigenschaften und Zusammensetzung 2 1.2. Molekülstruktur 2 1.3. Vorkommen und Bedeutung 2 2. Die homologe Reihe der Alkane 2 2.1. Beispiele: Butan, exan und Eicosan (Paraffin)
A l k a n e 1. Methan 2 1.1. Eigenschaften und Zusammensetzung 2 1.2. Molekülstruktur 2 1.3. Vorkommen und Bedeutung 2 2. Die homologe Reihe der Alkane 2 2.1. Beispiele: Butan, exan und Eicosan (Paraffin)
Ein Alkan, dem ein H-Atom fehlt, wird Alkyl-Rest genannt. Der Name ergibt sich aus dem Alkan, jedoch mit der Endung yl:
 Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Organische Chemie Unter organischer Chemie versteht man die Chemie der Kohlenwasserstoffe und ihre Derivate. Die C- Atome verbinden sich durch Kovalentebindung (Einfach-, Doppel- und Dreifachbindungen)
Chemie. für die Berufsmaturität. Günter Baars. Chemie. Baars. Unter Mitarbeit von Franz Heini, Markus Isenschmid und Doris Kohler
 www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
www.hep-verlag.ch/chemie-bm-ergaenzungen Franz eini Studium der Biologie mit ebenfach Biochemie. öheres Lehramt für das Fach Biologie. Unterrichtstätigkeit an der KDMS und an Gymnasien in Fribourg. Lehrer
ORGANISCHE CHEMIE. Prof. Dipl.-Ing. Manfred SUSSITZ. Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt
 ORGANISCHE CHEMIE Prof. Dipl.-Ing. Manfred SUSSITZ Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt 1. Kohlenwasserstoffe KW Kohlenstoff "Kohlenstoff ist in organischen Verbindungen
ORGANISCHE CHEMIE Prof. Dipl.-Ing. Manfred SUSSITZ Kernfragen: Mündliche Reifeprüfung: Alpen-Adria-Gymnasium Völkermarkt 1. Kohlenwasserstoffe KW Kohlenstoff "Kohlenstoff ist in organischen Verbindungen
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Organische Verbindungen 4. Nomenklatur organischer Stoffe (Kl. 9/10) Die Nomenklatur organischer Verbindungen ein Übungszirkel
 Organische Verbindungen 4. Nomenklatur organischer Stoffe (Kl. 9/10) 1 von 28 Die Nomenklatur organischer Verbindungen ein Übungszirkel Ein Beitrag von Günther Lohmer, Leverkusen Mit Illustrationen von
Organische Verbindungen 4. Nomenklatur organischer Stoffe (Kl. 9/10) 1 von 28 Die Nomenklatur organischer Verbindungen ein Übungszirkel Ein Beitrag von Günther Lohmer, Leverkusen Mit Illustrationen von
Nomenklatur von Alkyl Substituenten
 Organic Chemistry 4 th Edition Paula Yurkanis uice Chapter 2 Alkane: Kohlenwasserstoffe, die nur Einfachbindungen aufweisen Allgemeine Fmel: C n 2n+2 Eine Einführung In Organische Verbindungen Nomenklatur
Organic Chemistry 4 th Edition Paula Yurkanis uice Chapter 2 Alkane: Kohlenwasserstoffe, die nur Einfachbindungen aufweisen Allgemeine Fmel: C n 2n+2 Eine Einführung In Organische Verbindungen Nomenklatur
Grundwissen der 10.Klasse NTG
 Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Vergleichende Reaktionsmechanismen
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Vergleichende Reaktionsmechanismen 1. rdnen Sie die angegebenen Reaktionen einem Reaktionstyp zu und formulieren Sie den Reaktionsmechanismus. Radikalische
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME 1 Vergleichende Reaktionsmechanismen 1. rdnen Sie die angegebenen Reaktionen einem Reaktionstyp zu und formulieren Sie den Reaktionsmechanismus. Radikalische
Organische Chemie. Kohlenwasserstoffe. Alkane. Alkane
 1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
CHE 172.1: Organische Chemie für die Life Sciences
 1 CE 172.1: rganische Chemie für die Life Sciences Prof Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und
1 CE 172.1: rganische Chemie für die Life Sciences Prof Dr. J. A. Robinson 9. Alkohole, Ether und Phenole In diesem Kapitel werden wir als Schwerpunkte folgendes betrachten ; 1) Struktur, Reaktionen und
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
hemie für Biologen Vorlesung im WS 2004/05 V2, Mi 10-12, S04 T01 A02 Paul ademacher Institut für Organische hemie der Universität Duisburg-Essen (Teil 8: 01.12.2004) MILESS: hemie für Biologen 142 Nomenklatur
Organische Chemie Chemielaboranten 1-12
 Organische Chemie Chemielaboranten 1-12 1.2 Alkene Alkene- und Cycloalkene sind aliphatische respektive cycloaliphatische, ungesättigte Kohlenwasserstoffe mit einer oder mehreren Doppelbindungen. Die Endung
Organische Chemie Chemielaboranten 1-12 1.2 Alkene Alkene- und Cycloalkene sind aliphatische respektive cycloaliphatische, ungesättigte Kohlenwasserstoffe mit einer oder mehreren Doppelbindungen. Die Endung
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Kohlenwasserstoffe. Homologe Reihe. Alkane. Alkene. HGA-Grundwissen Chemie-10. Klasse NTG
 GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
Grundkompetenzen organische Chemie
 Grundkompetenzen organische Chemie Nachfolgende Themen geben einen Überblick über die Inhalte der 10. Jahrgangsstufe, die auch in der berstufe benötigt werden. Dieser Grundwissenskatalog dient nur der
Grundkompetenzen organische Chemie Nachfolgende Themen geben einen Überblick über die Inhalte der 10. Jahrgangsstufe, die auch in der berstufe benötigt werden. Dieser Grundwissenskatalog dient nur der
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Stationenlernen Chemie im Paket. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stationenlernen Chemie im Paket Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 59149 Stationenlernen:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stationenlernen Chemie im Paket Das komplette Material finden Sie hier: School-Scout.de Titel: Bestellnummer: 59149 Stationenlernen:
4-Butyl-2,5-dimethylheptan 5-Ethyl-4,8-dimethylundecan
 Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Übungsaufgaben zur Vorlesung Chemie für Biologen, WS 2005/2006 Themenbereich rganische Chemie 1. Warum ist der Kohlenstoff mehr als jedes andere Element dafür prädestiniert, komplexe Molekülverbindungen
Prüfungsvorbereitung organische Chemie
 Prüfungsvorbereitung organische hemie 2L Alle diese Aufgaben lehnen sich an Aufgaben zur gestreckten Abschlussprüfung für hemielaboranten Teil 1 an. Sie sind jedoch umformuliert und von den Stoffsystemen/Zahlenwerten
Prüfungsvorbereitung organische hemie 2L Alle diese Aufgaben lehnen sich an Aufgaben zur gestreckten Abschlussprüfung für hemielaboranten Teil 1 an. Sie sind jedoch umformuliert und von den Stoffsystemen/Zahlenwerten
Organische Experimentalchemie für Mediziner, Zahnmediziner und Naturwissenschaftler
 rganische Experimentalchemie für Mediziner, Zahnmediziner und Naturwissenschaftler Vorlesung: Mo-Fr. 8:00-8:45 Uhr Klausur: Abschlussklausur I Fr. 15.01.2016 18:15 19:45 Abschlussklausur II Fr. 05.02.2016
rganische Experimentalchemie für Mediziner, Zahnmediziner und Naturwissenschaftler Vorlesung: Mo-Fr. 8:00-8:45 Uhr Klausur: Abschlussklausur I Fr. 15.01.2016 18:15 19:45 Abschlussklausur II Fr. 05.02.2016
tetraedrisch trigonal - planar linear H 105 H 107 trigonal pyramidal
 BLK - SINUS hemie, bayerisches Schulset 4; Pilotschule: EvB Gymnasium, Buckenhofer Str. 5, 91080 Spardorf erleitung des räumlichen Baues von Molekülen mit ilfe des Valenzelektronenpaar-Abstoßungs-Modells
BLK - SINUS hemie, bayerisches Schulset 4; Pilotschule: EvB Gymnasium, Buckenhofer Str. 5, 91080 Spardorf erleitung des räumlichen Baues von Molekülen mit ilfe des Valenzelektronenpaar-Abstoßungs-Modells
Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen
 2. Alkane Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen 2.1 unverzweigte Alkane Formel: C n 2n+2 = -(C 2 ) n - homologe Reihe n Name Formel Schmp.
2. Alkane Alkane = aliphatische Kohlenwasserstoffe, Paraffine Organische Verbindungen ohne funktionelle Gruppen 2.1 unverzweigte Alkane Formel: C n 2n+2 = -(C 2 ) n - homologe Reihe n Name Formel Schmp.
Beuth Hochschule für Technik Berlin, Studiengang Pharma- und Chemietechnik Tutorium Organische Chemie 1 (SS 2011), Tutor: Sascha Behne
 IUPAC-Nomenklatur 1.) Zeichnen Sie die Struktur von: a) 4-(1-Methylethyl)heptan b) 2,3,4,4-Tetramethylhexan c) cis-1,2-dimethylcyclohexan d) 6-Brom-7-(chlormethyl)nonan-2,3-diol e) Isopren f) trans-1,2-diethylcyclopropan
IUPAC-Nomenklatur 1.) Zeichnen Sie die Struktur von: a) 4-(1-Methylethyl)heptan b) 2,3,4,4-Tetramethylhexan c) cis-1,2-dimethylcyclohexan d) 6-Brom-7-(chlormethyl)nonan-2,3-diol e) Isopren f) trans-1,2-diethylcyclopropan
10.1. Was versteht man unter einem Orbital? 10.2
 10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
10.1 Was versteht man unter einem Orbital? Ein Orbital ist ein dreidimensionaler Aufenthaltsraum für maximal 2 Elektronen, in dem diese sich mit 99% Wahrscheinlichkeit aufhalten. Je nach Energiestufe ist
Grundlagen der organischen Chemie: Gesättigte Kohlenwasserstoffe
 Grundlagen der organischen Chemie: Gesättigte Kohlenwasserstoffe Patrick Bucher 13. August 2011 Inhaltsverzeichnis 1 Einführung in die organische Chemie 1 1.1 Die Einteilung der organischen Verbindungen..................
Grundlagen der organischen Chemie: Gesättigte Kohlenwasserstoffe Patrick Bucher 13. August 2011 Inhaltsverzeichnis 1 Einführung in die organische Chemie 1 1.1 Die Einteilung der organischen Verbindungen..................
3. AUFBAU ORGANISCHER VERBINDUNGEN - ISOMERIEN
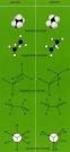 3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
3 AUFBAU ORGANISER VERBINDUNGEN - ISOMERIEN Die Bindungsverhältnisse und die Geometrien von Kohlenwasserstoffen lassen sich mit ilfe des ybrdisierungskonzepts verstehen und anschaulich darstellen (siehe
Organische Chemie. 1. Formuliere die Startreaktion und die Reaktionskette bei der Umsetzung von Ethan mit Chlor. Wie heisst dieser Reaktionstyp?
 Organische Chemie 1. Formuliere die Startreaktion und die Reaktionskette bei der Umsetzung von Ethan mit Chlor. Wie heisst dieser Reaktionstyp? 2. Chlorwasserstoff reagiert mit 1-Buten. Formuliere den
Organische Chemie 1. Formuliere die Startreaktion und die Reaktionskette bei der Umsetzung von Ethan mit Chlor. Wie heisst dieser Reaktionstyp? 2. Chlorwasserstoff reagiert mit 1-Buten. Formuliere den
Lösungen zu Übung 22
 rganische hemie I Lösungen zu Übung 22 1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan
rganische hemie I Lösungen zu Übung 22 1. Schreiben Sie die Konstitutionsformeln für die 4 Isomere der Summenformel 4 9 auf. Zur Summenformel 4 10 existieren zwei verschiedene Konstitutionsisomere (n-butan
Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester am
 Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester 2014 am 18.06.2014 Name: Matrikelnummer: Studiengang: Unterschrift: Aufgabe 1 2 3 4 5 6 7 8 9 10 Gesamt max. Punktzahl 10 10
Übungsklausur zur Vorlesung Organische Chemie für Biologen im Sommersemester 2014 am 18.06.2014 Name: Matrikelnummer: Studiengang: Unterschrift: Aufgabe 1 2 3 4 5 6 7 8 9 10 Gesamt max. Punktzahl 10 10
Chemie 10 NTG. In der Jahrgangsstufe 10 erwerben die Schüler folgendes Grundwissen:
 In der Jahrgangsstufe 10 erwerben die Schüler folgendes : 1. Sie kennen die wichtigsten Alkane, Alkene und Alkine, können sie benennen, ihre Bindungsverhältnisse und Molekülstrukturen beschreiben und sind
In der Jahrgangsstufe 10 erwerben die Schüler folgendes : 1. Sie kennen die wichtigsten Alkane, Alkene und Alkine, können sie benennen, ihre Bindungsverhältnisse und Molekülstrukturen beschreiben und sind
Orbital. Elektronenpaarabstoßungsmodell. räumliche Grundstrukturen 1. räumliche Grundstrukturen 2
 Orbital Der Raum, in dem sich ein Elektron mit größtmöglicher Wahrscheinlichkeit aufhält. Dieses Modell ermöglicht eine Vorhersage der räumlichen Struktur eines Moleküls. Elektronenpaarabstoßungsmodell
Orbital Der Raum, in dem sich ein Elektron mit größtmöglicher Wahrscheinlichkeit aufhält. Dieses Modell ermöglicht eine Vorhersage der räumlichen Struktur eines Moleküls. Elektronenpaarabstoßungsmodell
Chemie für Biologen WS 2005/6. Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen
 hemie für Biologen WS 2005/6 Arne Lützen Institut für Organische hemie der Universität Duisburg-Essen (Teil 10: Organische hemie gesättigte Kohlenwasserstoffe) Sonderstellung des Elements Elektronegativität
hemie für Biologen WS 2005/6 Arne Lützen Institut für Organische hemie der Universität Duisburg-Essen (Teil 10: Organische hemie gesättigte Kohlenwasserstoffe) Sonderstellung des Elements Elektronegativität
Magdalena Drozdowska Romanowska. in Zusammenarbeit mit Burkhard Paudtke
 Magdalena Drozdowska Romanowska in Zusammenarbeit mit Burkhard Paudtke Inhaltsverzeichnis Kapitel 1. Kohlenwasserstoffe 1.1. Einführung 1.2. Alkane.. 1.3. Alkene.. 1.4. Alkine... 1.5. Mehrfach ungesättigte
Magdalena Drozdowska Romanowska in Zusammenarbeit mit Burkhard Paudtke Inhaltsverzeichnis Kapitel 1. Kohlenwasserstoffe 1.1. Einführung 1.2. Alkane.. 1.3. Alkene.. 1.4. Alkine... 1.5. Mehrfach ungesättigte
Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe
 1 Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe Warm Up 1) Erweitern Sie die Ihnen bekannten Regeln der Nomenklatur für Alkene und benennen danach folgende Verbindungen. Die Regel zur
1 Übungssblatt 3: Alkene und weitere cyclische Kohlenwasserstoffe Warm Up 1) Erweitern Sie die Ihnen bekannten Regeln der Nomenklatur für Alkene und benennen danach folgende Verbindungen. Die Regel zur
Organische Chemie - 4 - Kohlenstoff als Bindungspartner. Kapitel 4: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen
 Organische hemie - 4 - Kohlenstoff als Bindungspartner 1 Kapitel 4: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen Organische hemie - 4 - Kohlenstoff als Bindungspartner 2 nhalt Kapitel
Organische hemie - 4 - Kohlenstoff als Bindungspartner 1 Kapitel 4: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen Organische hemie - 4 - Kohlenstoff als Bindungspartner 2 nhalt Kapitel
Alkane einfache Kohlenwasserstoffe
 Dr. Anja Dombrowski andlungsorientierter hemieunterricht an Stationen Sekundarstufe uf I Anja Dombrowski Downloadauszug aus dem Originaltitel: andlungsorientierter hemieunterricht an Stationen Dieser Download
Dr. Anja Dombrowski andlungsorientierter hemieunterricht an Stationen Sekundarstufe uf I Anja Dombrowski Downloadauszug aus dem Originaltitel: andlungsorientierter hemieunterricht an Stationen Dieser Download
Inhaltsverzeichnis. Teil I Volle Kraft voraus: Die Chemie des Kohlenstoffs 23. Einführung 17. Kapitel 1 Die wundervolle Welt der organischen Chemie 25
 Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Inhaltsverzeichnis Inhaltsverzeichnis Über den Autor 7 Einführung 17 Über dieses Buch 18 Konventionen in diesem Buch 19 Törichte Annahmen über den Leser 19 Wie dieses Buch aufgebaut ist 20 Teil I: Es war
Prof. Dr. Urs Séquin: Organische Chemie für Studierende der Medizin 1
 rof. Dr. Urs équin: rganische hemie für tudierende der Medizin 1 Übersicht über die wichtigsten Verbindungsklassen und ihre funktionellen Gruppen Verbindungsklasse allgemeine Form; Beispiel ame ( = Kohlenstoffrest,
rof. Dr. Urs équin: rganische hemie für tudierende der Medizin 1 Übersicht über die wichtigsten Verbindungsklassen und ihre funktionellen Gruppen Verbindungsklasse allgemeine Form; Beispiel ame ( = Kohlenstoffrest,
Stoffklassen in der Organischen Chemie. Nomenklaturfragen. Isomerie und sterischer Bau
 Stoffklassen in der Organischen Chemie Nomenklaturfragen Isomerie und sterischer Bau 1 Stoffklassen in der organischen Chemie Kohlenwasserstoffe Kohlenwasserstoffe mit Substituenten Y (eteroatom oder funktionelle
Stoffklassen in der Organischen Chemie Nomenklaturfragen Isomerie und sterischer Bau 1 Stoffklassen in der organischen Chemie Kohlenwasserstoffe Kohlenwasserstoffe mit Substituenten Y (eteroatom oder funktionelle
Organische Stofflehre
 Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Organische hemie hemielaboranten 1-01 Organische Stofflehre 1 Kohlenwasserstoffe Die Kohlenwasserstoffe, abgekärzt KW, sind die einfachsten organischen Verbindungen. Sie bestehen nur aus den Elementen
Chemisches Grundwissen und Erläuterungen Klasse 10
 Chemisches Grundwissen und Erläuterungen Klasse 10 für den naturwissenschaftlich technologischen Zweig Kohlenwasserstoffe gesättigte Kohlenwasserstoffe, die C-Atome haben im Molekül jeweils nur einen Bindungspartner,
Chemisches Grundwissen und Erläuterungen Klasse 10 für den naturwissenschaftlich technologischen Zweig Kohlenwasserstoffe gesättigte Kohlenwasserstoffe, die C-Atome haben im Molekül jeweils nur einen Bindungspartner,
Vom Alkohol zum Oxidationsprodukte der Alkohole
 Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die Nomenklatur organischer Verbindungen - ein Übungszirkel - als veränderbare WORD-Datei Das komplette Material finden Sie hier:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die Nomenklatur organischer Verbindungen - ein Übungszirkel - als veränderbare WORD-Datei Das komplette Material finden Sie hier:
Kapitel 04: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen
 Kapitel 04: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen Organische hemie - 04 - Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen 2 nhalt Kapitel 04: Kohlenstoff als Bindungspartner
Kapitel 04: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen Organische hemie - 04 - Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen 2 nhalt Kapitel 04: Kohlenstoff als Bindungspartner
Kapitel 04: Kohlenstoff als Bindungspartner in Alkanen, Alkenen und Alkinen
 1 2 nhalt...1 nhalt... 2 Wdh. Klasse 10: Die Atombindung bei Wasserstoff & Kohlenstoff...4 Kohlenstoff als Bindungspartner... 5 Die homologe Reihe der Alkane... 6 Die Namen der homologen Reihe von Alkanen
1 2 nhalt...1 nhalt... 2 Wdh. Klasse 10: Die Atombindung bei Wasserstoff & Kohlenstoff...4 Kohlenstoff als Bindungspartner... 5 Die homologe Reihe der Alkane... 6 Die Namen der homologen Reihe von Alkanen
5.10 Stereochemie E/Z, D/L, R/S E/Z Nomenklatur D/L Nomenklatur COOH
 Stereochemie E/Z, D/L, R/S SPF SB_A KME 191 5.10 Stereochemie E/Z, D/L, R/S 5.10.1 E/Z Nomenklatur Die (E)-(Z) Isomerie beschreibt die beiden Möglichkeiten der Anordnung von Substituenten an Doppelbindungen.
Stereochemie E/Z, D/L, R/S SPF SB_A KME 191 5.10 Stereochemie E/Z, D/L, R/S 5.10.1 E/Z Nomenklatur Die (E)-(Z) Isomerie beschreibt die beiden Möglichkeiten der Anordnung von Substituenten an Doppelbindungen.
Organische Chemie I/II. Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter!
 Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
Organische Chemie I/II Name: Fachprüfung Vorname: 5. Februar 2003, 15 30-18 30 h Matr.-Nr.: Raum 250 Schreiben Sie bitte Ihre Lösungen ausschließlich auf diese Aufgabenblätter! Jede Aufgabe wird mit 10
9. Alkohole, Ether und Phenole
 Friday, February 2, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 9. Alkohole, Ether und Phenole Bis jetzt haben wir fast bei jedem Kapitel eine neue funktionelle Gruppe und auch eine wichtige neue
Friday, February 2, 2001 Allgemeine Chemie B II Page: 1 Inhalt Index 9. Alkohole, Ether und Phenole Bis jetzt haben wir fast bei jedem Kapitel eine neue funktionelle Gruppe und auch eine wichtige neue
