Fundamentals of Biochemistry
|
|
|
- Erna Franke
- vor 6 Jahren
- Abrufe
Transkript
1 Donald Voet Judith G. Voet Charlotte W. Pratt Fundamentals of Biochemistry Second Edition Chapter 7: Protein Function: Myoglobin and Hemoglobin Copyright 2006 by John Wiley & Sons, Inc. Proteinfunktion: Myoglobin und Hämoglobin 1. Myoglobin A. Myoglobin Struktur B. Myoglobin Funktion 2. Hämoglobin A. Hämoglobin Struktur B. Sauerstoffbindung zu Hämoglobin 3. Kooperativität A. Mechanismen der Kooperativität in Hämoglobin B. Allosterische Proteine 4. Abnormale Hämoglobine 1
2 1. Myoglobin A. Struktur von Myoglobin Strukturaufklärung des Pottwal-Myoglobins wurde 1959 von John Kendrew gemacht. Später wurde die Struktur verschiedener Spezies und auch von Hb Mutationen durchgeführt. Das Hämoglobin wurde zum besterforschten Protein überhaupt. Myoglobin aus 8 Helices (A-H). ellipsoid Helices zwischen 7 und 26 AS lang meistens α-helices Enden der Helices A, C, E und G bilden 310 -Helix Bezeichnung von Resten: B5 = 5. AS in B-Helix (N-term nach C-term) FG3= 3. AS im Interhelicalen Segment zw. F u. G NA = nicht helicales aminoterminales Segment HC= nicht helicales carboxyterminales Segment Manchmal auch kombinierte Bezeichnung Glu EF6(83)= Glu 83 im interhelicalen Segment EF 6. AS. 2
3 Die Hämgruppe B. Myoglobin Funktion Räumliche Darstellung des OxyMb distales His proximales His H-Brücke Häm in hydrophobe Tasche eingebettet. DesoxyMb -> sechste koord. Stelle von Fe(II) unbesetzt. Fe(II) rückt auch weiter aus Porphyrinebene Distales His senkt Autooxidationsrate und erhöht Sauerstoffaffinität -> nicht ersetzbar durch andere AS Fe durch O2 Bindung vor Oxidation geschützt -> paradox Oxidation von Häm-Fe in Desoxyform jedoch Säurekatalysiert. Protonen werden durch Fe reduziert und diese reduzieren O2 zu Superoxid. Das distale His wirkt als Protonenfalle und schützt somit Fe vor oxitation. Die Sauerstoffsättigung verändert die Konformation von Mb nur geringfügig. Struktur von Oxy und Desoxy Mb gleich. 3
4 Sauerstoff-Bindungskurve von Myoglobin Sättigungsgrad von Myoglobin Partialdruck Umgebung Andere Sauerstoff-Transportproteine Leghämoglobin in Leguminosen (Pflanzenz. B. Klee)Diese Pflanzen die in Symbiose sind mit Bakterien welche Stickstoff fixieren. Das Abfangen des O2 durc legämoglobin erhöht die Effizienz der Stickstoff fixierung. Hämocyanin in Invertebraten und hat keine Hämgruppe in hoher Konzentration in der Hemolymph Flüssigkeit (vergleichbar mit Blut in Vertebraten). 4
5 2. Hämoglobin A. Hämoglobin Struktur Funktion des Hämoglobins Sauerstoff wird zur Energiegewinnung gebraucht. In kleinen Organismen gelangt O2 durch Diffusion zum Gewebe. In grossen Organismen (Schichtdicke der Gewebe >1mm) aktiver Transport nötig (Löslichkeit des O2 zu niederig). Sauerstoff bindende Proteine haben sich entwickelt. Hämoglobin = Hb (Fe mit Häm), Hämocyanin (Cu haltig), Hämerythrin (Fe haltig, ohne Häm). Fische der Antarktis einzige Vertebraten ohne Hämoglobin. O2 ist bei -1.9 C ausreichend löslich, deshalb haben diese Fische farbloses Blut. Myoglobin = Mb in Muskel erleichtert O2 transport in arbeitendem Muskel und dient in Wassersäugern als O2 Speicher. Häm Häm Mb und jede der 4 Untereinheiten von Hb enthalten nicht kovalent gebundenes Häm, das auch in Cytochromen vorkommt. Oxygenierung ändert Elektonenkonfiguration von Häm-Fe(II) Farbwechsel des Blutes von dunkel purpur (venöses Blut) zu leuchtend rot (arterielles Blut). CO, NO, H2S binden besser als O2 Toxizität Oxidation von Fe(II) zu Fe(III) Methämoglobin (MetHb) Metmyoglobin (MetMb). Keine Bindung von O2, H2O sättigt Fe(III) ab braune Farbe von trockenem Blut His Rest In Erythrocyten reduziert Methämoglobinreduktase Fe(III) zu Fe(II). 5
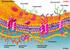
6 β1 α2 Nicht identische UE im Hb ausgeprägte Wechselwirkungen α1 β1 Kontakt 35 AS α1 β2 Kontakt nur 19 AS αβ-heterodimere -> hydrophobe WW Homodimere -> keine WW da durch Flüssigkeit gefüllten Kanal getrennt α1 β2 Unterschiedliche Quartärstruktur von Desoxy- und Oxy- Hämoglobin Desoxy-Form = T-Zustand β1 α2 β2 Oxy-Form = R-Zustand α2 α1 t-zustand β2 Tertiärstruktur UE Oxygenierung verengt Kanal β1 α1 r-zustand Tertiärstruktur UE DesoxyHb Kristall zerplatzt an der Luft α1 β2 Kontakt nur 19 AS dagegen α1 β1 Kontakt 35 AS -> stärkerer Kontakt unverändert d.h. Veränderung entlang α1 β2 Kontakt -> Verdrehung von α1 β1 Dimer um ca. 15 gegen α2 β2 Dimer 6
7 Blick von rechts auf vorherige Darstellung -> α1 β1 Dimer gefärbt dargestellt α2 β2 Dimer nur Umriss Durch Oxygenierung verschieben sich die 2 α β Dimere gegeneinander OxyHb ist kompakter als DesoxyHb Beachte: Lage von His FG4(97)β (schwarz) relativ zu gelb markierten AS. B. Sauerstoffbindung zu Hämoglobin Hämoglobin bindet O2 kooperativ. Die Hill-Gleichung beschreibt die sigmoidale O2Bindungskurve von Hämoglobin. [S] n Ys = K + [S] n Ys = Sättigungsgrad K = Dissoziationskonstante (p50) S = Ligandkonz., hier po2 n = Hill-Koeffizient n=1 nicht kooperative Bindung wie in Myoglobin n>1 pos. kooperativ wie in Hämoglobin n<1 neg. kooperativ 2.8 hyperbolische Bindungskurve mit demselben p50 wie Hb 7
8 Graphische Auswertung der Hill-Gleichung Hill-Auftragung log YO2 = nlogpo2 - nlogp50 1-YO2 po2 = p Torr 30 Torr viertes O2 bindet mit 100 höherer Affinität an Hämoglobin als erstes O2 3. Kooperativität A. Mechanismen der Kooperativität in Hämoglobin Einwandern von Fe(II) in PorphyrinEbene löst T-> R Transformation aus t-zustand Fe(II) 60 pm aus Porph. Ebene.-> pyramidale durchgebogen O2-Bindung ändert Elektr.konfig. von Fe -> Fe-N porph. -Bindung kontrahiert -> Fe in Phorphyrinebene und O 2 Bindung F-Helix muss Lage verändern, damit HisF8 dem Porphyrinring nicht zu nahe kommt. Dadurch wird Fe- O 2-Bindung stabilisiert. 8
9 Versetzen von 3 Seitenketten. Äquivalenter Satz von H-Brücken. Wie ein Schalter, nur 2 Zustände. Die Kooperativität der Sauerstoffbindung an Hämoglobin ergibt sich aus dem T -> R Übergang Bindung von Sauerstoff erfordert eng abgestimmte Molekülbewegungen: 1) Fe(II) gleitet nur in Porphyrinringebene wenn gleichzeitig sich die räumliche Orientierung vom proximalen His sich ändert. 2) Das proximale His ist fest mit Nachbarn verbunden -> Neuorientierung nur möglich wenn sich F-Helix über Porphyrinebene bewegt. 3) F-Helix kann sich nur dann bewegen wenn α1-β2 und α2-β1 Kontakte sich um eine Windung verschieben 4) Die Unbeweglichkeit der α1-β1 und α2-β2 Kontakte erzwingt die Konformationänderung in 3) -> Untereinheiten oder Dimere können Konformation nicht unabhängig voneinander ändern. Da nur 2 stabile α1-β2 (bzw. α2-β1) Kontakte möglich -> Quartärstruktur von Hb nur in 2 Zustandsformen Was heisst Kooperativität? 1. UE bindet O2 muss aber in t-zustand verharren da andere UE ohne O2 im t-zustand. Je mehr O2 gebunden desto höher O2 Affinität da UE im r-zustand. 9
10 T-Zustand durch Ionenbindungen stabilisiert, brechen auf bei Übergang zu R-Zustand R-Zustand durch Bindung von Sauerstoff stabilisiert. Warum T-Zustand aber stabiler als R-Zustand? C-terminale AS sind im R-Zustand flexibel im TZustand aber nicht, sie sind über Ionenbrücken stabilisiert. Netzwerk von ionischen WW und H-Brücken am Carboxyende der α und β Untereinheiten. deprotoniert bei Bohr effekt Alle diese Bindungen werden beim T-> R Übergang geöffnet Kohlendioxidtransport und Bohr-Effekt Hb transportiert neben O2 auch CO2 im Blut. O2 Bindung (physiolog. ph) Konformationsänderung von Hb (nicht aber Mb). Acidität von Hb erhöht sich und Protonen werden freigesetzt. Wenn diese Protonen durch erhöhen des ph abgefangen werden Erhöhung der O2 Bindungskapazität. = Bohr-Effekt Der Bohr-Effekt erleichtert den O2 Transport Aus O2 wird CO 2 (gelöst). CO 2 wird zu Hydrogencarbonat (langsame Reaktion). Wird in Erythrocyten beschleunigt von Carboanhydrase). CO2 wird im Blut als Hydrogencarbonat transportiert (kein ausperlen von CO 2 möglich). Gewebe po2 niedrig Lunge po2 hoch Einfluss des ph auf die O 2-Bindungskurve des Hb arbeitender Muskel ph tiefer mehr O2 wird abgegeben. 10
11 Rolle von Hb beim Transport von O2 von Lunge zu Gewebe Bedeutung von BPG für die O2 - Bindung Gereinigtes Hb hat höhere Affinität zu O2 als Vollblut. Unter anderem ist dafür D-2,3-Bisphosphoglycerat (BPG= 2,3 DPG) verantwortlich. BPG bindet stärker an DesoxyHb als an OxyHb. Es stabilisiert DesoxyHb. Selbe Funktion hat bei Vögeln Inositol hexakisphosphat (IHP) und bei Fischen und Amphibien Adenosintriphosphat (ATP). Modulation O2 Affinität von Hb in Säugern: 1) H + 2) CO2 3) Cl 4) BPG 11
12 Ohne BPG wird nur wenig O2 freigesetzt BPG erhöht p50 Wert Einfluss von BPG und CO2 von isoliertem Hb im Vergleich zu Vollblut 12
13 Regulation des Sauerstofftransportes Glykolyse Bindung von BPG an Desoxyhämoglobin BPG senkt Sauerstoffaffinität des Hb verbindet β UE über Salzbrücken und stabilisiert somit T-Form Bei Übergang in R-Form wird BPG herausgedrückt da sich Kanal verengt. Fötales Hb (HbF) hat anstelle von HisH143 ein ungeladenes Serin. BPG kann DesoxyHb nicht stabilisieren im Fötus -> höhere Sauerstoffaffinität. Salz- und H-Brücken 13
14 Bei Höhenanpassung steigt die BPG-Konzentration an Anpassung an Höhe führt zur Vermehrung von Erythrocyten. Nach einem Tag ist bereits der Anstieg von BPG zu beobachten, welches die Erythrocyten nicht verlassen kann. Verminderung der O 2 Bindungsaffinintät. Anstieg von BPG auch in Patienten mit Hypoxie, z.b. Anämien, kardiopulmonare Insuffizienz Fötales Hämoglobin (HbF) hat eine niedrige BPG-Affinität und bindet O2 besser als mütterliches Hämoglobin (HbA) O2 Versorgung des Fetus wird dadurch erst effizient. Höhenadaption gewährleistet dass Sauerstoffversorgung sich nicht vermindert. 14
15 B. Allosterische Proteine Organismen müssen auf Veränderungen in der Umgebung reagieren. Dies erfordert einen hohen Grad von Kontrolle biochemischer Mechanismen. Regulation ist auf jedem Niveau des Organismus möglich: -molekulare Ebene (Reaktionsgeschwindigkeiten, Genexpression) -zelluläre Ebene (Signaltransduktion) -organismische Ebene (Verhalten) Die meisten Erkrankungen können auf eine Störung der Kontrollmechanismen zurückgeführt werden. Liganden-Bindung kann durch allosterische Wechselwirkungen kontrolliert werden. Hämoglobin ist ein gutes Beispiel für eine solche Regulation die auf kooperativen Wechselwirkungen beruht. Die Bindung eines Liganden an eine spezifische Koordinationsstelle wird durch das Binden eines anderen Liganden (Effektor oder Modulator) an eine andere Stelle des Proteins beeinflusst. Sind Liganden identisch=homtroper Effekt, unterschiedlich=heterotroper Effekt. Diese Effekte können sowohl positiv als auch negativ sein. Hämoglobin zeigt positiv homotrope (O2 Bindung) und negativ heterotrope (BPG, CO2, H+, Cl-) Effekte. Allosterische Effekte ergeben sich aus Wechselwirkungen zwischen Untereinheiten oligomerer Proteine. Diese Effekte sind schwer zu beschreiben -> Modelle Im Folgenden Modelle für die allosterische Regulation der Sauerstoffaffinität in Hb. Symmetriemodell allosterischer Regulation Annahmen: 1. Allosterisches Protein = Oligomer aus gleichen symmetrisch angeordneten Untereinheiten (Protomeren). 2. Jedes Protomer kann in mindestens 2 Zuständen vorliegen die miteinander im Gleichgewicht sind (Hb in R- oder T- Zustand) unabhängig davon ob Ligand gebunden oder nicht. 3. Ligand kann jeden Konformationszustand binden.konformattionsänderungen können nur Affinität des Liganden beeinflussen. 4. Molekulare Symmetrie bleibt während Konformationswechsel erhalten. Also keine Oligomere von Hb die gleichzeitig r- und t-protomere enthalten. 15
16 C. Sequentielles Modell Symmetrie Modell geht von Lock and Key Mechanismus aus Sequentielles Modell geht von Induced fit aus -> verschiedene Dissoziationskonstanten vrgl. Adair-Gleichung Induced fit -> flexible Wechselwirkung zwischen Ligand und Protein -> Konformationsänderung -> Erhöhen der Affinität. Mit Röntgenstrukturanalyse einige Konformationsänderungen beobachtet -> stützen Induced fit Modell. Ligandenbindung -> Konformationsänderung in der UE -> kooperative WW beeinflussen benachbarte UE durch diese Konformationsänderung -> Affinität für Ligand wird verändert. Dieser Mechanismus ist abhängig von der Stärke der Kopplung der einzelnen UE. Starke Kopplung -> konzertierte Kopplung (-> Symmetrie Modell), schwache Kopplung -> sequentielle Konformationsänderung der einzelnen UE. 16
17 Sequentielles Modell der Allosterie Die Kopplung zwischen den Untereinheiten ist gering -> die Symmetrie der Oligomeren wird nicht aufrecht gehalten. Hb besteht nicht aus identischen Untereinheiten wie es das Symmetrie-Modell verlangt, sie sind jedoch genug ähnlich, dass in erster Näherung die Voraussagen des Symmetrie-Modelles zutreffen. Die Ligandenbindung im T-Zustand bewirkt ein kleine Konformationsänderung wie es das induced fit Modell vorhersagt. Dieses Phänomen wurde auch durch Röntgenstrukturanalyse bestätigt. Das partiell belegte Hb bleibt zunächst im T-Zustand. Die Fe-Atome der α-ue sind jedoch gegenüber dem DesoxyHb um 15pm zum Porphyrinring hin verschoben. -> Solche Veränderungen in der Tertiärstruktur erzeugen die für den T->R Übergang erforderliche Spannung 17
18 4. Abnormale Hämoglobine Über 400 Hämoglobin mutanten bekannt. Bei 95% nur eine einzige AS ausgetauscht. Solche Mutationen werden Hämoglobinopathien genannt. Dagegen werden Störungen in der Hämoglobinsynthese als Thalassämien bezeichent. A. Molekulare Pathologie des Hämoglobins 1. Austausch von AS an der Oberfläche Änderungen von oberflächlich gelegenen AS sind oft unauffällig, da Oberflächen AS keine spezielle Funktion haben. Ausnahme: Sichelzellenanämie (HbS, siehe später). HbE ist die häufigste Mutante nach HbS. Glu B8(26)ß -> Lys, d.h. saure AS wird durch basische ersetzt. Da aber an Oberfläche und keine spezifische Funktion -> keine Folgen 2. Austausch intern gelegener AS Austausch interner AS führt meist zu Destabilisierung von Hämoglobin -> Abbauprodukte, speziell zerfallenes Häm kleben an Zellmembran der Erythrocyten -> vorzeitige Lyse. Träger instabiler Hämoglobine haben hämolytische Anämie 18
19 kleinste Konformationsänderung im Zentrum kann zum Verlust der Bindung von Häm führen -> Funktionslosigkeit Hb Hammersmith Phe CD1(42)ß -> Ser Häm wird herausgelöst Hb Bristol Val E11(67)ß -> Asp Häm wird herausgelöst Hb Bibba Leu H19(136)α -> Pro Helix wird gebrochen -> instabil Hb Savanna Gly B6(24)ß -> Val Überkreuzung B und E Helix gestört Hb Philly Tyr C1(35) α >Phe α1 ß1 Kontakt gestört Molekularer Hintergrund der Sichelzell-Anämie Erythrocyten haben Sichelähnliche Form -> weniger Flexibel -> führt zu fatalen Blockaden des Blutflusses. Durchblutung in Peripherie verschlechtert -> gestörte Blutzirkulation. Mutation führt zur Verklumpung der deformierten Erythrocyten -> Homozygote Träger leiden an hämolytischer Anämie. In Afrika 25% der Bevölkerung heterozygote Träger von HbS GluA3(6)ß -> Val. Bietet Schutz gegen Malaria. Grund: Malaria Parasit benötigt eine bestimmte Kalium-Ionen Konzentration für seine Entwicklung die in normalen EC vorhanden ist. Die HbS Mutation senkt die Kalium-Ionen Konzentration in den SichelZellen und der Parasit kann nicht überleben. Normale EC HbS HbA Sichelförmige EC 19
20 Die HbS-Fasern werden durch intermolekulare Kontakte stabilisiert Anordnung der DesoxyHb Kontakte zwischen Asp73 und Glu 23 auch in HbA -> genügt alleine nicht um Fasern zu Bilden. Jedoch ist auch dieser Kontakt wichtig. Weitere Kontakte -> mischen von Hb verschiedener Mutanten Hb Harlem Glu3 -> Val,Asp73 -> Asn -> höhere Konz. von HbH/S nötig für Polymerisation als für HbA/S Hb Kole-Bu Asp 73 -> Asn Polymerisation auch verzögert. Asp73 wichtig für intermolekulare Kontakte von HbS. Hb Memphis Glu23 -> Gln α UE von HbMemphis und ß-UE von HbS gelieren langsamer. HbS GluA3(6)ß -> Val Glu macht keinen Kontakt OxyHb keine hydrophobe Tasche HbS bildet Fasern die verantwortlich sind für die Sichelfrom der EC. Die EC können platzen und die Fasern treten aus. Fasern des HbS die aus einem Erythrocyten austreten. 20
21 Der Beginn der HbS - Gelbildung ist ein komplexer Prozess Zeitverlauf der Gelbildung von HbS Initiation der Gelbildung durch Temperatursprung von 0 auf 20 C Konz. Abhängigkeit der Gelbildung von DesoxyHb bei 30 C Faserbildung tritt mit einer Zeitlichen Verzögerung auf. Abhängig von: Sauerstoffpartialdruch (T->R Übergang) HbS Konzentration Temperatur n 1 / td = k (ct / cs ) td = Verzögerungszeit ct = total HbS Konzentration cs = Löslichkeit von HbS k,n = Konstanten Zweistufenprozess: 1. Bildung eines Nucleus von HbS Molekülen homogener Nukleationsprozess hohe Konzentrationsabhängigkeit 2. Gebildete Fasern = Nukleationskeime heterogener Nukleationsprozess rasche Beendigung der Gelierung = kinetische Hypothese episodenhaftes Auftreten von Krisen -> Stocken Blutstrom Oxygenierung -> Fasern aufgelöst -> keine Fasern in arteriellem Blut -> Kapillargebiet in 0.5-2s durchströmt -> HbS kann ausfallen wenn aber td > Transitzeit keine Unterbrechung des Blutstroms. td kann verkürzt werden bei Fieber, O2 Mangel oder Dehydratisierung -> Krisen. erhöht Anteil an HbF (wie ist unbekannt) -> andere dynamik in der Faserbildung dauert länger als Aufenthaltsdauer im peripheren Gewebe. 21
22 22
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 1. Funktion des Hämoglobins Sauerstoff
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 4. Allosterische Regulation Organismen
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 4. Allosterische Regulation Organismen
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 3. Anormale Hämoglobine Über 400
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation 3. Anormale Hämoglobine Über 400
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9)
 Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation A. Struktur von Myoglobin Strukturaufklärung
Hämoglobin: Proteinfunktion und Mikrokosmos (Voet Kapitel 9) 1. Funktion des Hämoglobins 2. Struktur und Mechanismus 3. Anormale Hämoglobine 4. Allosterische Regulation A. Struktur von Myoglobin Strukturaufklärung
Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasse
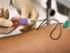 Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Hämoglobin Allgemeines: Konzentration des Hämoglobins im Blut: 160 g/l Verpackung im Erythrocyten -> kolloidosmotisch unwirksam -> beeinträchtigt nicht den Wasseraustausch im Kapillarbereich Durch die
Atmung II Atemgastransport Pathophysiologie
 Atmung II Atemgastransport Pathophysiologie Einführung Äußere und Innere Atmung Atemgastransport Normwerte Atemgastransport Das Blut Eine wesentliche Aufgabe des Blutes ist der Atemgastransport : Das Blut
Atmung II Atemgastransport Pathophysiologie Einführung Äußere und Innere Atmung Atemgastransport Normwerte Atemgastransport Das Blut Eine wesentliche Aufgabe des Blutes ist der Atemgastransport : Das Blut
Mechanismus der Enzymkatalyse
 Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Mechanismus der Enzymkatalyse Allgemeine Prinzipien Annäherung des Substrats an das aktive Zentrum des Enzyms Enzym und Substrat treten in Wechselwirkung: Bildung des [ES]-Komplexes. Konformationsänderung
Kardiopulmonale Homöostase
 Kapitel 2 Kardiopulmonale Homöostase Primäre Funktion des Blutes im Rahmen der Atmung Transport von O 2 aus der Lunge zum peripheren Gewebe, CO 2 aus der Peripherie zu den Lungen, H + vom Gewebe zu den
Kapitel 2 Kardiopulmonale Homöostase Primäre Funktion des Blutes im Rahmen der Atmung Transport von O 2 aus der Lunge zum peripheren Gewebe, CO 2 aus der Peripherie zu den Lungen, H + vom Gewebe zu den
Biologie. Anorganische Chemie. Bioanorganische Chemie
 Eine kleine Einführung in die Bioanorganische Chemie illustriert am Sauerstofftransport Jorge Ferreiro Montag, 8.12.2008 OACP II, ETH Zürich Wie lässt sich die Anorganische Chemie mit der Biologie verbinden,
Eine kleine Einführung in die Bioanorganische Chemie illustriert am Sauerstofftransport Jorge Ferreiro Montag, 8.12.2008 OACP II, ETH Zürich Wie lässt sich die Anorganische Chemie mit der Biologie verbinden,
Atemgastransport im Blut
 Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid
Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid
Woche 1: Grundlagen - Spezialfall Hämoglobin Woche 2: Proteinanalytik - Enzymregulation
 Woche 1: Grundlagen - Spezialfall Hämoglobin Woche 2: Proteinanalytik - Enzymregulation Vorlesung Medizinische Biochemie (13.04.18) Hauptakteure der Sauerstoffversorgung: Hämoglobin und Myoglobin für den
Woche 1: Grundlagen - Spezialfall Hämoglobin Woche 2: Proteinanalytik - Enzymregulation Vorlesung Medizinische Biochemie (13.04.18) Hauptakteure der Sauerstoffversorgung: Hämoglobin und Myoglobin für den
Aufgabe 6 (Quartärstruktur)
 Aufgabe 6 (Quartärstruktur) Fragestellung Folgende Fragestellungen sollen beim Hämocyanin-Hexamer von Limulus polyphemus (1lla_Hexamer.pdb) untersucht werden: - Welche Symmetrien sind erkennbar? - Wenn
Aufgabe 6 (Quartärstruktur) Fragestellung Folgende Fragestellungen sollen beim Hämocyanin-Hexamer von Limulus polyphemus (1lla_Hexamer.pdb) untersucht werden: - Welche Symmetrien sind erkennbar? - Wenn
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Biochemische UE Alkaline Phosphatase.
 Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Biochemische UE Alkaline Phosphatase peter.hammerl@sbg.ac.at Alkaline Phosphatase: Katalysiert die Hydrolyse von Phosphorsäure-Estern: O - O - Ser-102 R O P==O O - H 2 O R OH + HO P==O O - ph-optimum im
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Funktion von Proteinen:
 Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
2. Tertiärstruktur. Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen.
 2. Tertiärstruktur Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen. 2) Verstehen warum nicht polare Reste im inneren eines Proteins
2. Tertiärstruktur Lernziele: 1) Verstehen wie Röntgenstrukturanalyse und NMR Spektroskopie gebraucht werden um Proteinstrukturen zu bestimmen. 2) Verstehen warum nicht polare Reste im inneren eines Proteins
Aufgabe 5 (Supersekundärstruktur)
 Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
Aufgabe 5 (Supersekundärstruktur) Fragestellung Bei der Untereinheit des Arthropodenhämocyanins aus Limulus polyphemus werden folgende Fragestellungen untersucht: - Welche Supersekundärstrukturen gibt
1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss
 1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur - Eigenschaften eines Proteins werden durch
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur - Eigenschaften eines Proteins werden durch
Km: Michaelis-Konstante: Entspricht der Substratkonzentration, bei der die Hälfte der maximalen Gescwindigkeit (vmax) erreicht wird
 BioMol II Klausur 1. Kinetik 1.1 Michaelis-Menten Michaelis-Menten-Gleichung stellt einen Zusammenhang her zwischen der Konzentration des Substrates und der entsprechenden Geschwindigkeit der Reaktion.
BioMol II Klausur 1. Kinetik 1.1 Michaelis-Menten Michaelis-Menten-Gleichung stellt einen Zusammenhang her zwischen der Konzentration des Substrates und der entsprechenden Geschwindigkeit der Reaktion.
SS Thomas Schrader. der Universität Duisburg-Essen. (Teil 8: Redoxprozesse, Elektrochemie)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Sauerstofftransport im Blut. von Ralph Althoff Christoph Mittmann
 Sauerstofftransport im Blut von Ralph Althoff Christoph Mittmann Gliederung des Vortrags 1.) Geschichtliches 2.) Eigenschaften des Blutes 3.) Aufbau des Blutes 4.) Der Sauerstofftransporter 5.) Die Chemie
Sauerstofftransport im Blut von Ralph Althoff Christoph Mittmann Gliederung des Vortrags 1.) Geschichtliches 2.) Eigenschaften des Blutes 3.) Aufbau des Blutes 4.) Der Sauerstofftransporter 5.) Die Chemie
1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur
 Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 4. Protein-Stabilisierung Proteine sind
Dreidimensionale Struktur von Proteinen (Voet Kapitel 7) 1. Sekundärstruktur 2. Faserproteine 3. Globuläre Proteine 4. Protein Stabilisierung 5. Quartärstruktur 4. Protein-Stabilisierung Proteine sind
Membranen. U. Albrecht
 Membranen Struktur einer Plasmamembran Moleküle gegeneinander beweglich -> flüssiger Charakter Fluidität abhängig von 1) Lipidzusammensetzung (gesättigt/ungesättigt) 2) Umgebungstemperatur Biologische
Membranen Struktur einer Plasmamembran Moleküle gegeneinander beweglich -> flüssiger Charakter Fluidität abhängig von 1) Lipidzusammensetzung (gesättigt/ungesättigt) 2) Umgebungstemperatur Biologische
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Physiologie der Atmung. Cem Ekmekcioglu
 Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
Physiologie der Atmung Cem Ekmekcioglu Übersicht über den Transportweg des Sauerstoffes beim Menschen Schmidt/Thews: Physiologie des Menschen, 27.Auflage, Kap.25, Springer (1997) Klinke, Pape, Silbernagl,
-Übersicht. 2. G-Protein-gekoppelte Rezeptoren. 5. Na + -K + -Pumpe REZEPTOREN. 1. Allgemeine Definition: Rezeptoren. 3. Tyrosin-Kinase Rezeptoren
 REZEPTOREN -Übersicht 1. Allgemeine Definition: Rezeptoren 2. G-Protein-gekoppelte Rezeptoren 3. Tyrosin-Kinase Rezeptoren Beispiel: Insulin 4. Steroidhormone 5. Na + -K + -Pumpe EINFÜHRUNG Definition
REZEPTOREN -Übersicht 1. Allgemeine Definition: Rezeptoren 2. G-Protein-gekoppelte Rezeptoren 3. Tyrosin-Kinase Rezeptoren Beispiel: Insulin 4. Steroidhormone 5. Na + -K + -Pumpe EINFÜHRUNG Definition
Gliederung. Puffersysteme. Wofür Puffersysteme? Wofür Puffersysteme? Wofür Puffersysteme? ph-verhältnisse im Körper. Puffersysteme
 Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
Gliederung Puffersysteme Referat von Christian Rubbert Wofür Puffersysteme? ph-verhältnisse im Körper Puffersysteme Wofür Puffersysteme? Verschiedene Vorgänge im Körper, z.b.: Wofür Puffersysteme? Enzym
UAufgabe 12: (evolutiv konservierte Aminosäuren)
 UAufgabe 12: (evolutiv konservierte Aminosäuren) Aufgabenstellung Wählen Sie zur Darstellung evolutiv konservierter Aminosäure-Positionen in "1lla" eine ihnen sinnvoll erscheinende Anfärbung. Exportieren
UAufgabe 12: (evolutiv konservierte Aminosäuren) Aufgabenstellung Wählen Sie zur Darstellung evolutiv konservierter Aminosäure-Positionen in "1lla" eine ihnen sinnvoll erscheinende Anfärbung. Exportieren
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Hemmung der Enzym-Aktivität
 Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+
![Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ Elektronenspektrum von [Ti(H 2 O) 6 ] 3+](/thumbs/66/55543366.jpg) Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Elektronenspektrum von [Ti(H 2 O) 6 ] 3+ 3 2 1 15 20 25 30 1000 cm -1 e g hv t 2g Deutung der Elektronenspektren Absorption bestimmter Frequenzen des eingestrahlten Lichts durch: Elektronenübergang zwischen
Tyrosinkinase- Rezeptoren
 Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen. Abb. aus Stryer (5th Ed.)
 Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen Die verschiedenen Ribosomen-Komplexe können im Elektronenmikroskop beobachtet werden Durch Röntgenkristallographie wurden
Elektronenmikroskopie zeigte die Existenz der A-, P- und E- trna-bindungsstellen Die verschiedenen Ribosomen-Komplexe können im Elektronenmikroskop beobachtet werden Durch Röntgenkristallographie wurden
Hemmung der Enzym-Aktivität
 Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Literatur: Proteine Struktur und Struktur-Funktions-Beziehungen. Proteins Structure and structure-function relationships
 Biochemie II LVA 166.163 (WS 2015) Vortragender: Ao.Univ.Prof. Dr. Ewald Srebotnik ewald.srebotnik@tuwien.ac.at Modul 1: Proteine Struktur und Struktur-Funktions-Beziehungen Proteins Structure and structure-function
Biochemie II LVA 166.163 (WS 2015) Vortragender: Ao.Univ.Prof. Dr. Ewald Srebotnik ewald.srebotnik@tuwien.ac.at Modul 1: Proteine Struktur und Struktur-Funktions-Beziehungen Proteins Structure and structure-function
Verfahren zu Strukturvorhersagen in vereinfachten Modellen. Tobias Voigt Sommerakademie 2002 St. Johann
 Verfahren zu Strukturvorhersagen in vereinfachten Modellen Tobias Voigt Sommerakademie 2002 St. Johann Einführung! Sequenzierung von Proteinen und Nukleinsäuren ist heute Routine! Die räumliche Struktur
Verfahren zu Strukturvorhersagen in vereinfachten Modellen Tobias Voigt Sommerakademie 2002 St. Johann Einführung! Sequenzierung von Proteinen und Nukleinsäuren ist heute Routine! Die räumliche Struktur
Versuch: Enzyme (LDH)
 Versuch: Enzyme (LDH) 25.11.02 Seiten im Campell, Tierphysbuch (Penzlin) und Eckert Zusammenfassung Campbell S. 105-113 Zusammenfassung Eckert S. 77 89 Zusammenfassung Penzlin S. 50 ff. Allgemein: Temperatur
Versuch: Enzyme (LDH) 25.11.02 Seiten im Campell, Tierphysbuch (Penzlin) und Eckert Zusammenfassung Campbell S. 105-113 Zusammenfassung Eckert S. 77 89 Zusammenfassung Penzlin S. 50 ff. Allgemein: Temperatur
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Schweizerische Maturitätsprüfung Gruppe / Kandidat/in Nr:... Fächerübergreifender Teil Biologie
 Gruppe / Kandidat/in Nr:... Name/Vorname:... Schwerpunktfach Teil BIOLOGIE UND CHEMIE Fächerübergreifender Teil Biologie Verfasser: Richtzeit: Hilfsmittel: Hinweise: G. Rutz, M. Lüscher 30 Minuten (von
Gruppe / Kandidat/in Nr:... Name/Vorname:... Schwerpunktfach Teil BIOLOGIE UND CHEMIE Fächerübergreifender Teil Biologie Verfasser: Richtzeit: Hilfsmittel: Hinweise: G. Rutz, M. Lüscher 30 Minuten (von
0.1 Eiweißstoffe (Proteine)
 1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
Aspekte der Eisenresorption. PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse Binningen
 Aspekte der Eisenresorption PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse 19 4102 Binningen Chemische Eigenschaften Fe-II wird leichter aufgenommen als Fe-III wegen der besseren
Aspekte der Eisenresorption PD Dr. F.S. Lehmann Facharzt für Gastroenterologie FMH Oberwilerstrasse 19 4102 Binningen Chemische Eigenschaften Fe-II wird leichter aufgenommen als Fe-III wegen der besseren
Chemie 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter Wasser (= 1000g)?
 Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Musterprüfung für die Zwischenprüfung Chemie Klasse: MPA / PSW 09 Datum: Fr. 21. Mai. 2010 12:20 13:05 1. Wie viele Neutronen hat es im Isotop 14 6 C? 2. Wie viele Mol Wassermoleküle hat es in einem Liter
Aminosäurenanalytik. Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE
 Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Vertiefendes Seminar zur Vorlesung Biochemie I. Bearbeitung Übungsblatt 6
 Vertiefendes Seminar zur Vorlesung Biochemie I 04.12.2015 Bearbeitung Übungsblatt 6 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 04.12.2015 Bearbeitung Übungsblatt 6 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!!
 Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine Bildung der Disulfidbrücke
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine Bildung der Disulfidbrücke
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Die Bindung in Übergangsmetallkomplexenn. Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth
 Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Die Bindung in Übergangsmetallkomplexenn Klassische Koordinationschemie (Alfred Wernersche) Valenzstruktur-Theorie (Valenzbindungsth heorie) Ligandenfeld-Theorie H 3 3+ H 3 H 3 Cr H 3 H 3 H 3 Molekülorbital-Theorie
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Freie Elektronen bilden ein Elektronengas. Feste positive Aluminiumionen. Abb. 1.1: Metallbindung: Feste Atomrümpfe und freie Valenzelektronen
 1 Grundlagen 1.1 Leiter Nichtleiter Halbleiter 1.1.1 Leiter Leiter sind generell Stoffe, die die Eigenschaft haben verschiedene arten weiterzuleiten. Im Folgenden steht dabei die Leitfähigkeit des elektrischen
1 Grundlagen 1.1 Leiter Nichtleiter Halbleiter 1.1.1 Leiter Leiter sind generell Stoffe, die die Eigenschaft haben verschiedene arten weiterzuleiten. Im Folgenden steht dabei die Leitfähigkeit des elektrischen
Atmungsphysiologie II.
 Atmungsphysiologie II. 29. Gasaustausch in der Lunge. 30. Sauerstofftransport im Blut. 31. Kohlendioxidtransport im Blut. prof. Gyula Sáry Gasaustausch in der Lunge Gasdiffusion findet durch die Kapillarmembrane
Atmungsphysiologie II. 29. Gasaustausch in der Lunge. 30. Sauerstofftransport im Blut. 31. Kohlendioxidtransport im Blut. prof. Gyula Sáry Gasaustausch in der Lunge Gasdiffusion findet durch die Kapillarmembrane
Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
 Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Coulomb-Gesetz, Ionen- (Kristall-)strukturen, NaCl, CsCl, ZnS, Elementarzelle, 7 Kristallsysteme Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
Wiederholung der letzten Vorlesungsstunde: Ionenbindung, Coulomb-Gesetz, Ionen- (Kristall-)strukturen, NaCl, CsCl, ZnS, Elementarzelle, 7 Kristallsysteme Themen heute: Reaktionsgleichungen, chemische Gleichgewichte
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Aminosäuren. Seitenkette. -Kohlenstoffatom. Karboxilgruppe. Aminogruppe
 Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Proteine Aminosäuren 16 Seitenkette -Kohlenstoffatom Aminogruppe Karboxilgruppe Die Gruppen der Aminosäuren 17 Bildung der Peptidbindung Die strukturellen Ebenen der Proteine 18 Primär Struktur Aminosäuer
Prionen. Prionen (K. Berendes, S. Lingan)
 Prionen Gliederung 1. Struktur eines Proteins und ihre Analyse 2. Allgemeines 3. Infektionsformen 4. Prionkrankheiten bei Mensch und Tier 5. BSE 6. Creutzfeldt-Jakob-Krankheit 7. Therapieansätze 1. Struktur
Prionen Gliederung 1. Struktur eines Proteins und ihre Analyse 2. Allgemeines 3. Infektionsformen 4. Prionkrankheiten bei Mensch und Tier 5. BSE 6. Creutzfeldt-Jakob-Krankheit 7. Therapieansätze 1. Struktur
Vorname: Frage 1. Nennen Sie drei Metalle, die :für den Menschen essentiell sind und als Mengenelemente Körper vorkommen (3 P) Frage 2
 1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Transkription und Translation sind in Eukaryoten räumlich und zeitlich getrennt. Abb. aus Stryer (5th Ed.)
 Transkription und Translation sind in Eukaryoten räumlich und zeitlich getrennt Die Initiation der Translation bei Eukaryoten Der eukaryotische Initiationskomplex erkennt zuerst das 5 -cap der mrna und
Transkription und Translation sind in Eukaryoten räumlich und zeitlich getrennt Die Initiation der Translation bei Eukaryoten Der eukaryotische Initiationskomplex erkennt zuerst das 5 -cap der mrna und
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
4.1. Eigenschaften von Enzymen
 4. Enzyme 106 107 4.1. Eigenschaften von Enzymen Enzyme sind Proteine, die chemische Reaktionen beschleunigen (Biokatalysatoren) Herausragende Merkmale verglichen mit anderen Katalysatoren: drastische
4. Enzyme 106 107 4.1. Eigenschaften von Enzymen Enzyme sind Proteine, die chemische Reaktionen beschleunigen (Biokatalysatoren) Herausragende Merkmale verglichen mit anderen Katalysatoren: drastische
Die Freie Aktivierungsenthalpie
 Die Freie Aktivierungsenthalpie E A G k Ae RT e = = RT G: Freie Aktivierungsenthalpie G = H T S e G RT = e S R e H RT e S R A H E A Katalyse: der aktivierte Übergangskomplex H E A Katalysatoren beeinflussen
Die Freie Aktivierungsenthalpie E A G k Ae RT e = = RT G: Freie Aktivierungsenthalpie G = H T S e G RT = e S R e H RT e S R A H E A Katalyse: der aktivierte Übergangskomplex H E A Katalysatoren beeinflussen
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Praktikum Physikalische Chemie I 30. Januar Aktivierungsenergie. Guido Petri Anastasiya Knoch PC111/112, Gruppe 11
 Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Praktikum Physikalische Chemie I 30. Januar 2016 Aktivierungsenergie Guido Petri Anastasiya Knoch PC111/112, Gruppe 11 1 Aufgabenstellung Für die Reaktion von Saccharose mit Wasser zu Glucose und Fructose
Aufgabe 10: (Konformationsänderungen)
 Aufgabe 10: (Konformationsänderungen) Aufgabenstellung Was passiert durch die Oxygenierung auf der Ebene der Tertiärstruktur, was auf Ebene der Quartärstruktur? Mit dem Programm Swiss-pdb-viewer soll dies
Aufgabe 10: (Konformationsänderungen) Aufgabenstellung Was passiert durch die Oxygenierung auf der Ebene der Tertiärstruktur, was auf Ebene der Quartärstruktur? Mit dem Programm Swiss-pdb-viewer soll dies
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
und Reinstruktur Die Sekundärstruktur ist die Anordnung der Aminosäurenkette, wobei man in zwei Arten unterscheidet: o Faltblatt- oder β- Struktur
 Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Aufbau von Proteinen insbesondere unter Betrachtung der Primär-,, Sekundär-,, Tertiär-,, Quartär-,, Supersekundär- und Reinstruktur Primärstruktur Unter Primärstruktur versteht man in der Biochemie die
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus)
 Kinetik Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus) Klassifizierung chem. Reaktionen nach kinetischen Aspekten a) Reaktionsmolekularität: wie viele Teilchen
Kinetik Kinetik: a) Reaktionsgeschwindigkeit (zeitlicher Verlauf) b) Reaktionsweg (Mechanismus) Klassifizierung chem. Reaktionen nach kinetischen Aspekten a) Reaktionsmolekularität: wie viele Teilchen
Bioorganische Chemie Enzymatische Katalyse 2011
 Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Ringvorlesung Chemie B - Studiengang Molekulare Biotechnologie Bioorganische Chemie Enzymatische Katalyse 2011 Prof. Dr. A. Jäschke INF 364, Zi. 308, Tel. 54 48 51 jaeschke@uni-hd.de Lehrziele I Kenntnis
Anionenaustausch. Definition Anionen-Austausch-Kapazität (AAK): AAK = Σ austauschbar gebundenene Anionen
 Anionenaustausch Definition Anionen-Austausch-Kapazität (AAK): AAK = Σ austauschbar gebundenene Anionen Ursache der Anionensorption positive Ladungen (Protonierung von Al/Fe-OH-Gruppen; unspezifische Sorption)
Anionenaustausch Definition Anionen-Austausch-Kapazität (AAK): AAK = Σ austauschbar gebundenene Anionen Ursache der Anionensorption positive Ladungen (Protonierung von Al/Fe-OH-Gruppen; unspezifische Sorption)
Komplexbildung. CoCl 3 5 NH 3. CoCl 3 6 NH 3. CoCl 3 4 NH 3 Alfred Werner The Nobel Prize in Chemistry 1913
 Komplexbildung CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner 1866-1919 The Nobel Prize in Chemistry 1913 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH
Komplexbildung CoCl 3 6 NH 3 CoCl 3 5 NH 3 CoCl 3 4 NH 3 CoCl 3 4 NH 3 Alfred Werner 1866-1919 The Nobel Prize in Chemistry 1913 Komplexbildung Beispiel wässrige Lösungen von Aluminium(III) Al 3+ + 3 OH
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Praktikumsrelevante Themen
 Praktikumsrelevante Themen RedoxReaktionen Aufstellen von Redoxgleichungen Elektrochemie Quantitative Beschreibung von RedoxGleichgewichten Redoxtitrationen 1 Frühe Vorstellungen von Oxidation und Reduktion
Praktikumsrelevante Themen RedoxReaktionen Aufstellen von Redoxgleichungen Elektrochemie Quantitative Beschreibung von RedoxGleichgewichten Redoxtitrationen 1 Frühe Vorstellungen von Oxidation und Reduktion
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
LeWis» ph-wert Berechnungen «Kapitel 5
 Additum 5. Wässrige Lösungen mehrprotoniger Säuren und Basen Ziel dieses Kapitels ist es, eine weitere Anwendungsmöglichkeit des bisher erlernten Vorgehenskonzepts vorzustellen. Die Berechnung von ph-werten
Additum 5. Wässrige Lösungen mehrprotoniger Säuren und Basen Ziel dieses Kapitels ist es, eine weitere Anwendungsmöglichkeit des bisher erlernten Vorgehenskonzepts vorzustellen. Die Berechnung von ph-werten
Die α (alpha)-thalassämien- Informationen für Patienten
 Die Alpha Thalassämien Seite 1 von 1 Die α (alpha)-thalassämien- Informationen für Patienten Erstellung Prüfung Prof. Dr. med. Roswitha Dickerhoff Prof. Dr. med. R. Dickerhoff Gültigkeitsbeginn 01.05.2013
Die Alpha Thalassämien Seite 1 von 1 Die α (alpha)-thalassämien- Informationen für Patienten Erstellung Prüfung Prof. Dr. med. Roswitha Dickerhoff Prof. Dr. med. R. Dickerhoff Gültigkeitsbeginn 01.05.2013
Themengebiet: 1 HA + H 2 O A - + H 3 O + H 3 O + : Oxonium- oder Hydroxoniumion. Themengebiet: 2 B + H 2 O BH + + OH - OH - : Hydroxidion
 1 1 Säuren sind Protonendonatoren, d.h. Stoffe, die an einen Reaktionspartner ein oder mehrere Protonen abgeben können; Säuredefinition nach Brönsted Im Falle von Wasser: HA + H 2 O A - + H 3 O + H 3 O
1 1 Säuren sind Protonendonatoren, d.h. Stoffe, die an einen Reaktionspartner ein oder mehrere Protonen abgeben können; Säuredefinition nach Brönsted Im Falle von Wasser: HA + H 2 O A - + H 3 O + H 3 O
Signale und Signalwege in Zellen
 Signale und Signalwege in Zellen Zellen müssen Signale empfangen, auf sie reagieren und Signale zu anderen Zellen senden können Signalübertragungsprozesse sind biochemische (und z.t. elektrische) Prozesse
Signale und Signalwege in Zellen Zellen müssen Signale empfangen, auf sie reagieren und Signale zu anderen Zellen senden können Signalübertragungsprozesse sind biochemische (und z.t. elektrische) Prozesse
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
Die Zelle. Membranen: Struktur und Funktion
 Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
2.2 Intermolekulare Wechselwirkungen
 2.2 Intermolekulare Wechselwirkungen -15-2.2 Intermolekulare Wechselwirkungen Die Bildung der hier vorgestellten molekularen Aggregate beruht auf schwachen Wechselwirkungen zwischen Atomen oder Molekülen.
2.2 Intermolekulare Wechselwirkungen -15-2.2 Intermolekulare Wechselwirkungen Die Bildung der hier vorgestellten molekularen Aggregate beruht auf schwachen Wechselwirkungen zwischen Atomen oder Molekülen.
3. Übung Grundlagen der Hauptgruppenchemie
 Allgemeine und Anorganische Chemie 3. Übung Grundlagen der Hauptgruppenchemie Aufgabe 1: Beschreiben Sie die Herstellung von Schwefelsäure nach dem Kontaktverfahren mit Hilfe von chemischen Gleichungen
Allgemeine und Anorganische Chemie 3. Übung Grundlagen der Hauptgruppenchemie Aufgabe 1: Beschreiben Sie die Herstellung von Schwefelsäure nach dem Kontaktverfahren mit Hilfe von chemischen Gleichungen
Denaturierung von Proteinen
 Denaturierung von Proteinen = Auflösen der konformationsstabilisierenden Wechselwirkungen, wodurch die Konformation reversibel oder irreversibel zerstört wird durch Erhitzen, Einwirkung von Scherkräften,
Denaturierung von Proteinen = Auflösen der konformationsstabilisierenden Wechselwirkungen, wodurch die Konformation reversibel oder irreversibel zerstört wird durch Erhitzen, Einwirkung von Scherkräften,
Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte)
 Datum: 06.12.2010 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte) Modulnr.: FMI-BI0027 iermit bestätige ich meine Prüfungstauglichkeit.
Datum: 06.12.2010 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte) Modulnr.: FMI-BI0027 iermit bestätige ich meine Prüfungstauglichkeit.
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
1 Einleitung. Einleitung 1
 Einleitung 1 1 Einleitung Die Supramolekulare Chemie ist die Chemie der intermolekularen Bindung. Sie beschäftigt sich mit Strukturen und Funktionen von Einheiten, die durch Assoziation zweier oder mehrerer
Einleitung 1 1 Einleitung Die Supramolekulare Chemie ist die Chemie der intermolekularen Bindung. Sie beschäftigt sich mit Strukturen und Funktionen von Einheiten, die durch Assoziation zweier oder mehrerer
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik
 Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
Metabolismus Umwandlung von Stoffen und Energie nach den Gesetzen der Thermodynamik Der Metabolismus oder Stoffwechsel ist die Gesamtheit der in einem Organismus ablaufenden (bio)chemischen Prozesse Der
= Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s]
![= Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s] = Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s]](/thumbs/94/122358469.jpg) Ache2 Kapitel 14: Chemische Kinetik (Geschwindigkeit) Reaktionsgeschwindigkeit Beeinflussung: 1. Aggregatszustände der Reaktanten: Je öfters Moleküle zusammenstossen, desto schneller reagieren sie. (Oberflächenvergrösserung
Ache2 Kapitel 14: Chemische Kinetik (Geschwindigkeit) Reaktionsgeschwindigkeit Beeinflussung: 1. Aggregatszustände der Reaktanten: Je öfters Moleküle zusammenstossen, desto schneller reagieren sie. (Oberflächenvergrösserung
Pressemitteilung. Neue Placebo-kontrollierte Doppelblind-Studie bestätigt: Entsäuerung mit Basica Direkt bringt mehr Energie
 Pressemitteilung Neue Placebo-kontrollierte Doppelblind-Studie bestätigt: Entsäuerung mit Basica Direkt bringt mehr Energie In der heutigen Zeit muss man leistungsfähig sein für alle Anforderungen, die
Pressemitteilung Neue Placebo-kontrollierte Doppelblind-Studie bestätigt: Entsäuerung mit Basica Direkt bringt mehr Energie In der heutigen Zeit muss man leistungsfähig sein für alle Anforderungen, die
Falschfaltung von Proteinen
 Falschfaltung von Proteinen - Aggregation - domain swapping - amyloidogene Strukturen Was determiniert die Faltung von Proteinen? Einfachstes System: Zwei-Zustandsmodell N U Energie U dg ÜS dg* N Molekulare
Falschfaltung von Proteinen - Aggregation - domain swapping - amyloidogene Strukturen Was determiniert die Faltung von Proteinen? Einfachstes System: Zwei-Zustandsmodell N U Energie U dg ÜS dg* N Molekulare
Grundwissen Chemie 8. Klasse NTG
 Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
