Rolle der Aminosäuren im Stoffwechsel
|
|
|
- Ralf Gerhardt
- vor 8 Jahren
- Abrufe
Transkript
1 Rolle der Aminosäuren im Stoffwechsel freie AS aus zugeführtem Protein und hydrolysiertem Körperprotein = 0.05 % 70 g Im Gegensatz zu Fettsäuren und Glucose sind freie AS NICHT speicherbar % davon im Muskel!
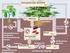
2 Resorption und Verteilung der Aminosäuren im Organismus Darm: Verlust essentieller AS, besonders Thr (Bestandteil proteolyse-resistenter Mucine in endothelialen Schleimschichten!) Mucosa: Glu, Gln, Asp Energie Arg Citrullin Niere: Arg-Synthese zentrale Rolle der Leber: Proteinbiosynthese und -abbau Ketosäuren Fettsäuren, Glucose Ammoniak Harnstoff genaue Menge nicht resorbierter AS unbekannt Muskulatur: nimmt v.a. verzweigtkettige AS auf: Val, Leu, Ile
3 Aminosäuren - Hauptabbauwege Aminosäuren Transaminierung α-ketosäuren dehydrierende Decarboxylierung Fettsäure-Thioester (Acetyl-CoA) oxidative Desaminierung (Glutamat-DH) NH 3 Harnstoffzyklus Niere - Urin Fettsäuren Citrat-Zyklus: je nach Stoffwechsellage Abbau zu CO 2 + H 2 0 oder Aufbau von Kohlenhydraten, Fetten... Decarboxylierung biogene Amine Oxidation (Aminoxidasen)
4 AS-Abbau: 1. Stickstoff (N 2 ) - Abspaltung Generelles: nicht benötigte AS werden abgebaut (normal: < 50 %) bei Säugern: AS-Abbau Abbau hauptsächlich in der Leber aber auch periphere Organe können AS zum Energiegewinn (ATP-Bildung) zu CO 2, H 2 O und NH 3 abbauen in Energieübertragungswegen kommen keine Stickstoffhaltigen Verbindungen vor Aminogruppe entfernen durch Transaminierung und oxidative Desaminierung Ammoniak (NH 3 ) ist cytotoxisch muss entgiftet werden
5 Die zentralen Aminoäuren und ihre zugehörigen α-ketosäuren (α-ks) sind am häufigsten an Umbaureaktionen (Transaminierungen) beteiligt hohe intrazelluläre Konzentration dieser AS: 10- bis 50-fach erhöht gegenüber Plasma
6 Transaminierung Prinzip der Reaktion: AS α-kg α-ks Glu Aminogruppe (-NH 2 ) wird auf α-ketoglutarat (α-kg; = 2-Oxo-glutarat) übertragen: AS α-ks abhängig von Pyridoxalphosphat (PALP) reversibel AS-Synthese aus α-ks ABER: für für Lysin (Lys, K) K) und Threonin (Thr, T): T): keine Aminotransferasen
7 Die beiden wichtigsten Aminotransferasen Aspartat- Aminotransferase (AST, ASAT, GOT = Glutamat-Oxalacetat- Transaminase) Alanin- Aminotransferase (ALT, ALAT, GPT = Glutamat-Pyruvat- Transaminase) hohe Konzentration dieser Enzyme in in Leber, Myocard, Hirn Isoformen in in Cytosol und Mitochondrien Diagnostik
8 Pyridoxalphosphat (PLP, PALP) Vitamin B6 = Pyridoxal leicht sauer leicht basisch substituiertes Pyridin Aldehydgruppe bildet kovalente Schiff-Basen: prosthetische Gruppe (Coenzym) z.b. in Aminotransferasen
9 Mechanismus der PALP-abhängigen Transaminierung an der Aldehydgruppe des PALP: protoniertes PALP wirkt als Elektronenfalle Amino-Stickstoff wird nicht frei!
10 PALP-abhängige Reaktionen Spaltung der Bindung a), b) oder c) c) Aldolasen: Aldolspaltung (Glycin vom Rest der AS abgespalten) a) Aminotransferasen: Transaminierung (AS + α-kg α-ks + Glu) b) Decarboxylasen: Decarboxylierung (AS Amin + CO 2 ) weitere Reaktionen: Dehydratasen = Desaminasen: α-,ß-eliminierung (AS α-ks + NH 3 ) PALP-abhängige Reaktionen: im AS-Stoffwechsel, in der Hämoglobin- Biosynthese, bei der GABA-Biosynthese, im Glycogen-Abbau
11 PALP-abhängige Decarboxylierung Spaltung zwischen α-c α-c und und Carboxylgruppe Freisetzung des des Amins Amins und und CO CO 2 2 DAO Ox Säure Aminosäure Cystein (Cys, C) Asparaginsäure (Asp, D) Glutaminsäure (Glu, E) Histidin (His, H) Dihydroxy-Phenylalanin (DOPA) Tryptophan (Trp, W) 5-Hydroxy-Tryptophan Amin Cysteamin ß-Alanin γ-aminobuttersäure (GABA) Histamin Dopamin Tryptamin Serotonin Vorkommen Coenzym A Coenzym A Neurotransmitter Mediator, Hormon Neurotransmitter Hormon Neurotransmitter
12 α-,ß-eliminierung und Aldolspaltung Spaltung der der Bindungen zwischen α-c α-c und und seinem seinem H sowie sowie ß-C ß-C und und seinem seinem Substituenten Eliminierung von von Wasser (bzw. (bzw. H 2 2 S) S) Iminosäure spontane Hydrolyse zu zu α-ks α-ks + NH NH 3 3 Spaltung der der Bindung zwischen α-c α-c und und ß-C ß-C Glycin Glycin vom vom Rest Rest der der Aminosäure abgetrennt [Aminoacrylat] Abbau von Ser, Cys zu Pyruvat Thr zu α-ketobutyrat auch Met, Gly, His ß-, γ-eliminierung bei Homoserin, Homocystein Folat Tetrahydrofolat (FH 4 ) (sind Coenzyme der Purin- und Pyrimidinsynthese und des Met-Stoffwechsels)
13 Oxidative Desaminierung wichtigste Reaktion: Glutamat-Dehydrogenase (GLDH): Gleichgewichtsreaktion; allosterische Aktivierung (ADP, GDP) Aminogruppe als NH 3 freigesetzt ( ) oder NH 3 wird fixiert ( ) Zwischenprodukt Schiff-Base (Iminosäure) wie bei Transaminierung mitochondriales Enzym hohe Konzentration der GLDH in in der Leber ( Diagnostik)
14 Hyperaktive GLDH führt zu Hypoglykämischer Hyperinsulinämie Mutationen im GLDH-Gen: gain-of-function : erhöhter Umsatz von Glu keine Hemmung durch ATP/GTP a) ATP-Synthese = ATP/ADP-Quotient steigt Insulin-Ausschüttung Blutglucosespiegel sinkt b) erhöhter NH 3 -Spiegel (Hyperammonämie)
15 Die wichtigsten NH 3 liefernden Reaktionen oxidative Desaminierung (GLDH) andere Aminosäure-Desaminierungen z.b. basische AS, α-,ß-eliminierung, Lyasen Aminoxidasen (Mono-, Diaminoxidasen = MAO, DAO) Transaminierung von Glutamin Q: Q + α-ks + H 2 0 α-kg + AS + NH 4 + Purinnucleotid-Desaminasen Pyrimidinabbau: (d)cmp-desaminase, Ringspaltungen U, T molekulare Ursache für für Neurotoxizität von NH 3 :: Hemmung des Citratcyclus durch α-kg-mangel im im Gehirn.
16 Ammoniak NH 3 ~ 25% des im Körper gebildeten Ammoniaks entsteht im Darm. bei normalem Blut-pH (7.4): 98% NH 4 + und 2% NH 3 : NH 3 + H 2 0 NH OH - NH 3 toxisch: freie Diffusion durch Nervenzellmembran in Muskulatur wird NH 3 z.t. aufgenommen nur die arterielle Ammoniakkonzentration korreliert mit der im ZNS, nicht die venöse! Entgiftung & Ausscheidung als Harnstoff
17 Ammoniak-Entgiftung I Vermeidung der NH 3 -Freisetzung: = Übertragung von Aminogruppen auf Ketoverbindungen durch: Aspartatzyklus Transaminierungen: - Aminogruppen auf α-kg übertragen Aspartatzyklus: - ist verknüpft mit Harnstoff-, AMP- und Purinbiosynthese - Aminogruppen auf Citrullin bzw. Nukleotide (X) übertragen
18 Ammoniak-Entgiftung II kovalente Fixierung von NH 3 durch: GLDH (mitochondrial) Rückreaktion; zentrale Rolle des Glutamats ABER: Glutamat kann Blut- Hirn-Schranke nicht passieren! Glutaminsynthetase (ebenfalls mitochondrial) Harnstoffzyklus Harnstoff aus der Leber in die Niere Ausscheidung mit Urin
19 Periphere Gewebe reichen Stickstoff an Leber extrahepatische Zellen: Transaminierungen, GLDH Glutamat Glutamin-Synthetase (besonders Gehirn): Glutamin ist ist DER Transporter von Amino-Stickstoff zu zu Leber, Niere Muskelzellen nutzen außerdem die Alanin-Aminotransferase - Rückreaktion, um Alanin aus Pyruvat herzustellen: Alanin ist ist die AS mit der zweithöchsten Plasmakonz.
20 Glukose-Alanin-Zyklus: Zusammenspiel von Muskel und Leber Glukose-Alanin-Zyklus hat besondere Bedeutung im arbeitenden Muskel Gln hauptsächlich aus Asp und Glu erzeugt = Transporter für Kohlenstoffgerüste aus der Proteolyse Niere: Glutaminase I, II NH 4 + im Urin
21 Entgiftung des NH 3 im Harnstoffzyklus mol (30-90 g) Harnstoff / Tag Fixierung: NH 3 + CO 2 CO 2 diffundiert ins Mito Carbo-Anhydrase (CA) HCO 3 - Ornithin/Citrullin Antiport Krebs- Henseleit- Zyklus N-Acetylglutamat = allosterischer Aktivator (essentiell; Schnellregulation) Bilanz: NH 4+ + HCO ATP + Asp + 2 H 2 O Harnstoff + 2 ADP + AMP + P i + Fumarat
22 Zusammenspiel des Harnstoffzyklus mit anderen Stoffwechselwegen GLDH E α-kg + NH 3 (Glutaminase Q E + NH 3 ) = NADH-liefernde Reaktionen
23 Störungen des Harnstoffzyklus Symptome Hyperammonämie Enzephalopathie respiratorische Alkalose Ursachen genetische Enzymdefekte: Inzidenz ca. 1:25.000, früher: Stickstoffreduktionskost, Zufuhr von α-ketosäuren erworbene Lebererkrankungen wie Leberzirrhose akutes Leberversagen z.b. durch Knollenblätterpilz- oder Paracetamolvergiftung.
24 Enzymdefekte im Harnstoffzyklus AsL R-ase OTC-Mangel Mangel: Carbamoyl-P diffundiert ins Cytoplasma Pyrimidinsynthese Orotacidurie (Diagnose) AsS OTC CPS I Krankheit Defektes Enzym Folge Behandlung Hyperammonämie I (kongenitale Ammoniak-Intox.) CPS I Stickstoff- Anhäufung als Glycin und Glutamin Hyperammonämie II Citrullinämie Argininbernsteinsäurek. (Argininosuccinaturie) Argininosuccinat- Lyase (AsL) OTC Argininosuccinat- Synthetase (AsS) Stickstoff- Anhäufung als Citrullin Ornithin fehlt (Argininosuccinat- Ausscheidung) proteinarme Diät mit viel Arg Orn- Synthese steigern Diät ohne Arginin Hyperargininämie Arginase (R-ase) Arginin angehäuft, Orn fehlt N-Acetylglutamat- N-Acetyl-glutamat- CPS I inaktiv Synthasemangel Synthetase (allosterisch) proteinarme Diät mit Benzoat + Phenylacetat Konjugation von Glycin und Glutamin Ausscheidung siehe Hyperammonämie I
25 Einschränkung des Harnstoffzyklus durch Leberinsuffizienz gesund z.b. durch Infektion, Alkohol, Medikamente Leberfunktion auf % eingeschränkt Insuffizienz! häufig Fibrosen Bluthochdruck der Pfortader (portale Hypertens.) Bildung von Umgehungskreisläufen (Anastomosen) Ammoniakspiegel steigt hepatische Enzephalopathie (Ammoniakvergiftung des Gehirns) Coma hepaticum
26 Diagnostik von Lebererkrankungen Enzyme des Aminosäurestoffwechsels: Messung der Plasmakonzentrationen Störungen des Gallengangsystems: γ-glutamyl-transpeptidase (γ-gt) epitheliales Enzym erhöhte Plasmakonzentration Leberschäden: Aminotransferasen (Transaminasen): Isoenzyme in Cytosol und Mitochondrien normale höchste Aktivitäten: Alanin-Aminotransferase (ALT) im Cytosol, Aspartat-Aminotransferase (AST) v.a. im Mito Glutamat-Dehydrogenase (GLDH) im Mitochondrium Diagnostik: AST/ALT < 1: normal, aber auch bei Entzündung leichte Leberschäden: Anstieg ALT schwere Leberschäden: AST und GLDH
27 Harnstoff, NH 3 und Säure-Basen-Haushalt Fixierung von NH 4+ und HCO 3- im Harnstoffzyklus gekoppelt ACIDOSE: Protonenüberschuss im Blut (ph < 7.37) Leber: weniger Hydrogencarbonat HCO 3- Harnstoffsynthese ; NH 4+ : in Glutamin (Gln) fixiert Niere: aus Glutamin NH 4+ freigesetzt Ausscheidung ALKALOSE: Protonenmangel im Blut (ph > 7.44) Leber: mehr HCO 3- NH 4+ benötigt: Hydrolyse von Gln Harnstoffsynthese ; Niere: Glukoneogenese gestoppt (keine Gln-Desaminierung) keine Kopplung von H + an NH 3 Protoneneinsparung Niere
28 Zusammenfassung Stationen der Ammoniakentsorgung: Gewebe: Fixierung von NH 3 in Glu und Gln Leber: Harnstoffzyklus Niere: Freisetzung von NH 3 aus Gln, Ausscheidung von Harnstoff (Urea) und NH 4 +
29 Aminosäureabbau: 2. Kohlenstoffgerüste Die 20 Standard-AS werden über 7 Moleküle in den CC eingespeist: Citrat- Cyclus Fettsäuren Hämsynthese
30 Abbau essentieller und bedingt essentieller AS nach Entfernung der Amino (NH 2 -)-Gruppe dehydrierende Decarboxylierung Amino- glucogenes ketogenes * * säure Abbauprodukt Abbauprodukt Bemerkungen Lysin - 2x Acetyl-CoA irreversible Transaminierung Methio- Succinyl-CoA - abhängig von Vitamin B6, B12 nin Cys Pyruvat und Folsäure Threo- Succinyl-CoA Acetaldehyd 2 Wege: α, ß-Eliminierung nin Gly Pyruvat Acetyl-CoA oder Aldolspaltung Isoleucin Succinyl-CoA Acetyl-CoA Valin Succinyl-CoA - Leucin - Acetyl-CoA, über ß-Hydroxy-ß-methylglutaryl-CoA Acetoacetat (HMG-CoA) * Cholesterolsynthese Tyrosin Fumarat Acetoacetat Tetrahydrobiopterin-, Ascorbinsäure-abhängig Phenylalanin Tyrosin Fumarat Acetoacetat Trp Alanin Pyruvat 2x Acetyl-CoA PLP-abhängig Histidin α-ketoglutarat - PLP-abhängig Cystein Pyruvat - historisch: Bildung von von Glukose bzw. bzw. Acetoacetat im im diabetischen Tier Tier
31 Methionin: abhängig von 3 Vitaminen Remethylierung (Vit. B12) Mangel durch N 2 0 (Narkose): Synthase inaktiv neurologische Schäden = SAM; AdoMet; aktives Methionin (Folsäure) Transmethylierung Propionyl- CoA CoA 5 α-ketobutyrat + Cystein Pyruvat 5 = Transsulfurierung mit PALP (aus Vit. B6) Enzymdefekte Homocystinurie bzw. Cystathionurie
32 2 Wege für den Abbau von Threonin Aldolspaltung α-,ß-eliminierung α-ketobutyrat Propionyl- CoA
33 Essentielle AS der Aspartat- und Pyruvatfamilie - Bedeutung essentielle AS: Aspartatfam. Lys, Met, Thr; Pyruvatfam. Val, Ile, Leu Lysin: mögliche Vorstufe von Carnitin (mito. Fettsäure-Carrier) Hydroxy-Lysin: Bestandteil von Kollagen Methionin: S-Adenosylmet = aktives Methyl : wichtigster Methylgruppendonator für N- oder O-Methylierung (C1- Übertragung; z.b. Bildung von Kreatin) Pathobiochemie: Homocystinurie (beim Met-Abbau): Endothelschädigung, Arteriosklerose Acidose durch gestörten Abbau von Propionyl-CoA (Abbau von Met, Thr, Val, Ile)
34 Abbau verzweigtkettiger Aminosäuren (Pyruvat-Familie) verzweigtkettige AS (Val, Ile, Leu) v.a. in Muskel (Skelett, Herz) und Niere, auch im Gehirn abgebaut die anderen essentiellen AS in der Leber dehydrierende Decarboxylierung zu Fettsäure-CoA-Thioestern Threonine Propionyl-CoA-Carboxylase Biotin-abhängig Enzymdefekt/Biotinmangel: Propionylacidämie L-Methylmalonyl-CoA-Isomerase Vit. B12 (Cobalamin)-abhängig Enzymdefekt/Vit. B12-Mangel: Methylmalonacidämie
35 Verzweigtketten- (Ahornsirup-) krankheit Transaminierung dehydrierende Decarboxylierung Enzymdefekt in in dehydrierender Decarboxylierung zentralnervöse Störungen, Azidose Körperflüssigkeiten und und Atemluft: würzig-süßlicher Geruch sofortige Diät: Diät: arm arm an an Val, Val, Ile, Ile, Leu Leu (sind essentiell!)
36 Aromatenfamilie I: Abbau von Phenylalanin Phenylalanin-Hydroxylase 1. Hydroxylierungen, Biopterin-abhängig (Tyrosin = Abbauprodukt von Phenylalanin) 2. oxidative Ringspaltung Hydroxylierung Transaminierung Hydroxylierung Decarboxylierung (Vit. C abhängig) ox. Ringspaltung Isomerisierung
37 Aromatenfamilie II: Bedeutung v. Phe und Tyr Vorstufen von Pigmenten (Melanin; Synthesestörung: Albinismus), Neurotransmittern (Noradrenalin) und Hormonen (Adrenalin, Thyroxin) Phenylketonurie (PKU): Phenylketonurie (PKU): häufigste Störung des AS-Stoffwechsels 1: (heterozygot: 1:50!) > 240 Mutationen der Phenylalanin-Hydroxylase Phe-Abbau auf alternativen Wegen (neuro)tox. Produkte frühe Diagnose! Phe-arme Diät bis mindestens 10 Jahre
38 Aromatenfamilie III: Tryptophan Tryptophan = Indolyl-Alanin Abbau: Biopterin-abhängig 1. oxidative Spaltung der Ringe 2. Abtrennung Ala-Seitenkette Alanin + Acetoacetat Tryptophan verstärkt Proteinbiosynthese in in der der Leber (ist (ist dort dort normalerweise die die am am geringsten konzentrierte AS) AS) Provitaminfür für Nicotinsäure-Synthese ( ( NAD(P)) Pellagra = kombinierter Tryptophan- und und Vitaminmangel (Niacin) Vorstufe biogener Amine: Serotonin (5-Hydroxytryptamin), Melatonin (Epiphysenhormon), Tryptamin
39 Histidin Stickstoff #1 als NH 3 abgespalten (Histidase) Stickstoff #2 als Formiminogruppe auf Tetrahydrofolat übertragen PALP-abhängige Decarboxylierung biogenes Amin Histamin: Freisetzung NO in Gefäßendothel Relaxation glatter Gefäßmuskeln allergische Reaktion! 3-Methyl-Histidin in in Actin, Myosin im im Urin: Indikator für für Muskelprotein-Abbau
40 Cystein (Serinfamilie) im Extrazellularraum als Cystin (oxidierende Umgebung) : Abbau durch α-,ß-eliminierung: Disulfid [Aminoacrylat] Vorstufe von Taurin (Aminoethylsulfonsäure) Konjugation von Gallensäuren (Taurocholsäure) Cystinurie AS-Transporterstörung (rbat-gen), betrifft auch Lys, Arg, Orn (Diaminocarbonsäuren), ebenfalls vermehrte Ausscheidung von Homocystein
41 Abbau nicht- und semiessentieller AS Amino- glucogenes ketogenes Bemerkungen säure Abbauprodukt Produkt Arginin Ornithin Glu - über Glutamat-Semialdehyd α-ketoglutarat Prolin Glu α-ketoglutarat - über Glutamat-semialdehyd Glutamin Glu α-ketoglutarat - Aminogruppendonator; Glutaminase Glutamat α-ketoglutarat - Zentralsubstanz im AS- Stoffwechsel, Neurotransmitter! Asparagin Asp Oxalacetat Aminogruppendonator; Asparaginase Aspartat Oxalacetat, Fumarat - Glycin Pyruvat - Alanin Pyruvat - wichtigste glucogene AS Serin (Glycin) Pyruvat - liefern letztlich alle Oxalacetat (C4-Gerüst) glucogen aber: Pyruvat AcetylCoA Fettsäuren Abbau in in fast allen Geweben
42 Bedeutung nichtessentieller Aminosäuren Aspartat/Asparagin, Glutamat/Glutamin Transaminierungen... Prolin: als Hydroxyprolin (Hyp) in Kollagen (ca. 25 %) Hyp im Urin = Maß für Kollagen-Stoffwechsel Arginin: - Freisetzung von NO (+ Citrullin) durch NO-Synthase siehe auch Histamin! - Vorstufe für Polyamine (Spermin, Spermidin) stabilisieren DNA - Ausgangsstoff für Kreatinsynthese (Kreatinphosphat = Energiereserve im Muskel) Glycin: Biosynthese von Häm (+ Succinyl-CoA) und Purinen Serin: - Vorstufe für Purinbasen, Phospholipide, Cystein - Hydroxymethylgruppe (C1-Verbindung) kann auf Tetrahydrofolsäure übertragen werden Alanin: D- und L-Form in Murein-Zellwand der Bakterien
43 C1-Verbindungen im AS-Stoffwechsel Biotin = Vit. H Harnstoffderivat bindet CO 2 an Position N1, überträgt es auf Pyruvat, Acetyl-CoA, Propionyl-CoA C1-Einheiten werden geliefert von: von: Methionin aktiviert (Ado (Ado-Met) überträgt Methyl (-CH (-CH 3 3 )) auf auf Histidin, DNA; DNA; bei bei Synthese von von Kreatin, Adrenalin, Cholin Glycin Methylen (-CH (-CH 2 2 -) -) Serin Serin Methyl Übertragung auf auf Tetrahydrofolat Histidin Formimino (-CH=NH) Synthese von von Methionin, Thyminnucleotiden
44 Der vollständige Abbau von AS zu zu CO 2 + H NH 3 liefert Energie (ca kj/g) essentielle AS nichtessentielle AS Zahlenwerte = ATP-Äquivalente Glucose: Stearinsäure (C18): Ethanol: 38 ATP-Äquivalente (17 kj/g) 148 ATP-Äquivalente (39 kj/g) 114 ATP-Äquivalente (30 kj/g)
45 Zusammenfassung: AS im Stoffwechsel Synthese von Körperprotein: Verfügbarkeit essentieller AS! Energie liefernde Substrate: tgl. Umsatz 4.4g/kg bzw mmol/kg übertrifft Fett- bzw. Kohlenhydratumsatz; AS am Energiegewinn mit 15-20% beteiligt glucogene AS Glucosehomöostase Quelle für für Stickstoff und organischen Schwefel für für Biosynthesen zellulärer AS-Pool gespeist aus endogenem Proteinabbau und AS aus Nahrung
46 Aminosäure-Stoffwechsel unter verschiedenen äußeren Bedingungen myotrop (anabol): AS von Leber Muskel; positive N 2 -Bilanz durch: Insulin (AS-Transportsysteme!), Testosteron, Somatotropin; mtor bewirkt Anschalten der Ribosomenbiogenese und Translation hepatotrop (negative Stickstoff-Bilanz): Proteinabbau zuerst in Gastrointestinaltrakt, Leber, Niere, Pankreas Muskel (größtes Organ) verliert höchste Absolutmenge an Protein durch Aktivierung von Calpainen und Proteasom Nahrungskarenz = Glukose fehlt; Acetyl-CoA glucogene Substanz; Lactat, Pyruvat keine Netto-Neusynthese von Glukose Proteinabbau: Alanin Transport Muskel Leber: Glukoneogenese Glycin in die Niere Guconeogenese Hypoalaninämie (Muskelabbau reduziert) Verlust von > 50% der Muskelmasse Tod Stress, Infektionen, Verletzungen, Tumoren, AIDS höhere Stickstoffausscheidung (Verlust von Körperprotein) Kachexie
47 Proteinqualität Biologische Wertigkeit Fehlen einer essentiellen AS Proteinbiosynthese unterschiedliche Verdaubarkeit (%) Muttermilch 95 Kartoffel 71 Ei Fisch Rindfleisch Kuhmilch Gelatine Soja Hefe Hafer Reis Mais Weizen pflanzliche Proteine im im menschlichen Organismus oft oft unvollständig hydrolysiert gemischte Mahlzeit: essentielle AS AS ergänzen: Getreide (arm (arm an an Lys, Lys, ausreichend Trp) Trp) + Bohnen (arm (arm an an Trp, Trp, ausreichend Lys) Lys)
48 Protein-Energie-Malnutrition (PEM) Kwashiorkor: Entwöhnungskrankheit zu wenig Protein: essentielle AS fehlen Hypoalbuminämie ( Wasserbauch ) Marasmus (grch.: verwelken) zu wenig Protein Hypoalbuminämie (Ödeme) generell zu wenig Energiezufuhr
Proteinstoffwechsel. Bildung der Aminosäuren. Protein-Abbau der Körperproteine. Protein-Abbau der Nahrungsproteine. Verwertung der Aminosäuren
 Bildung der Aminosäuren Körperproteine 10000 g Nahrungsproteine Proteinstoffwechsel Proteolyse (300 400 g/d) AminosäurePool Verdauung (50 100 g/d) 100 g Vortragender: Dr. W. Helliger Neusynthese aus z.b.
Bildung der Aminosäuren Körperproteine 10000 g Nahrungsproteine Proteinstoffwechsel Proteolyse (300 400 g/d) AminosäurePool Verdauung (50 100 g/d) 100 g Vortragender: Dr. W. Helliger Neusynthese aus z.b.
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Metabolisierung des Aminosäure-Kohlestoffgerüstes
 Metabolisierung des Aminosäure-Kohlestoffgerüstes Abbau zu 7 wichtigen Molekülen: Pyruvat, Acetyl-CoA, Acetoacetyl-CoA, -Ketoglutarat, Succinyl-CoA, Fumarat, Oxalacetat >> also zu 4 Intermediaten des Citratzyklus,
Metabolisierung des Aminosäure-Kohlestoffgerüstes Abbau zu 7 wichtigen Molekülen: Pyruvat, Acetyl-CoA, Acetoacetyl-CoA, -Ketoglutarat, Succinyl-CoA, Fumarat, Oxalacetat >> also zu 4 Intermediaten des Citratzyklus,
Nichtessentielle Aminosäuren. Stoffwechsel Nahrungskarenz
 Nichtessentielle Aminosäuren Stoffwechsel Nahrungskarenz Einleitung 11 nichtessentielle AS Können von Säugetierzellen selbstsynthetisiert werden. Im Vergleich zu essentiellen AS einfache Synthesewege Nichtessentiell
Nichtessentielle Aminosäuren Stoffwechsel Nahrungskarenz Einleitung 11 nichtessentielle AS Können von Säugetierzellen selbstsynthetisiert werden. Im Vergleich zu essentiellen AS einfache Synthesewege Nichtessentiell
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aminosäuren & Ketosäuren BIOGENE AMINE
 BIOGENE AMINE Von Mohammed Jaber BIOGENE AMINE: Biogene Amine sind AS ohne COOH-Gruppe! Und warum sind sie so wichtig? Von Mohammed Jaber und Proteine BIOGENE AMINE: Durch die Abspaltung der COOH- Gruppe
BIOGENE AMINE Von Mohammed Jaber BIOGENE AMINE: Biogene Amine sind AS ohne COOH-Gruppe! Und warum sind sie so wichtig? Von Mohammed Jaber und Proteine BIOGENE AMINE: Durch die Abspaltung der COOH- Gruppe
Aminosäuren - Proteine
 Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Aminosäuren - Proteine ÜBERBLICK D.Pflumm KSR / MSE Aminosäuren Überblick Allgemeine Formel für das Grundgerüst einer Aminosäure Carboxylgruppe: R-COOH O Aminogruppe: R-NH 2 einzelnes C-Atom (α-c-atom)
Pharmazeutische Biologie Grundlagen der Biochemie
 Pharmazeutische Biologie Grundlagen der Biochemie Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Aminosäure... chirale Moleküle
Pharmazeutische Biologie Grundlagen der Biochemie Prof. Dr. Theo Dingermann Institut für Pharmazeutische Biologie Goethe-Universität Frankfurt Dingermann@em.uni-frankfurt.de Aminosäure... chirale Moleküle
Energie aus Aminosäuren - Wundermittel Protein?
 Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Foliensatz; Arbeitsblatt; Internet. Je nach chemischem Wissen können die Proteine noch detaillierter besprochen werden.
 03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
03 Arbeitsauftrag Arbeitsauftrag Ziel: Anhand des Foliensatzes soll die Bildung und der Aufbau des Proteinhormons Insulin erklärt werden. Danach soll kurz erklärt werden, wie man künstlich Insulin herstellt.
8. Aminosäuren - (Proteine) Eiweiß
 8. Aminosäuren - (Proteine) Eiweiß Proteine sind aus Aminosäuren aufgebaut. Aminosäuren bilden die Grundlage der belebten Welt. 8.1 Struktur der Aminosäuren Aminosäuren sind organische Moleküle, die mindestens
8. Aminosäuren - (Proteine) Eiweiß Proteine sind aus Aminosäuren aufgebaut. Aminosäuren bilden die Grundlage der belebten Welt. 8.1 Struktur der Aminosäuren Aminosäuren sind organische Moleküle, die mindestens
Was ist denn NAD / NADP??
 Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Aliphatische Aminosäuren. Aromatische Aminosäuren
 Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Prof. Dr..-U. eißig rganische Chemie I 17.1 Aliphatische Aminosäuren systematischer ame (Trivialname) truktur Vorkommen, Bedeutung 2-Aminoethansäure (α-aminoessigsäure, Glycin) 3 C 2 C 2 α Proteine, Peptide
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
1. Fragentyp A Welche der folgenden Aminosäuren ergibt beim Abbau Propionyl-CoA? A) Isoleucin B) Tyrosin C) Glutaminsäure D) Glycin E) Asparaginsäure
 1. Fragentyp A Welche der folgenden Aminosäuren ergibt beim Abbau Propionyl-CoA? A) Isoleucin B) Tyrosin C) Glutaminsäure D) Glycin E) Asparaginsäure 2. Fragentyp D Welche der folgenden Aussagen ist (sind)
1. Fragentyp A Welche der folgenden Aminosäuren ergibt beim Abbau Propionyl-CoA? A) Isoleucin B) Tyrosin C) Glutaminsäure D) Glycin E) Asparaginsäure 2. Fragentyp D Welche der folgenden Aussagen ist (sind)
Energiestoffwechsel --- Aminosäuren. Prof. Dr. Martin van der Laan
 Energiestoffwechsel --- Aminosäuren Prof. Dr. Martin van der Laan Stoffwechsel von Aminosäuren (Überblick) Aminosäure N 3 + R C α Desaminierung Transaminierung Decarboxylierung CO 2 N 3 + R C (Biogenes)
Energiestoffwechsel --- Aminosäuren Prof. Dr. Martin van der Laan Stoffwechsel von Aminosäuren (Überblick) Aminosäure N 3 + R C α Desaminierung Transaminierung Decarboxylierung CO 2 N 3 + R C (Biogenes)
Peptide Proteine. 1. Aminosäuren. Alle optisch aktiven proteinogenen Aminosäuren gehören der L-Reihe an: 1.1 Struktur der Aminosäuren
 1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
1. Aminosäuren Aminosäuren Peptide Proteine Vortragender: Dr. W. Helliger 1.1 Struktur 1.2 Säure-Basen-Eigenschaften 1.2.1 Neutral- und Zwitterion-Form 1.2.2 Molekülform in Abhängigkeit vom ph-wert 1.3
Lösungsblatt zu Aufbau von Aminosäuren
 Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
Lösungsblatt zu Aufbau von Aminosäuren 1. Zeichnen Sie die allgemeine Formel einer α-aminosäure, welche am α-c- Atom eine Seitenkette R trägt. 2. Welche der zwanzig natürlich vorkommenden L-α-Aminosäuren
COOH. Die Aminosäuren tragen laborübliche Abkürzungen, so stehen z. B. Gly für Glycin oder Phe für Phenylalanin.
 Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
 Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Aminosäuren mit sauren Seitengruppen Asparaginsäure (Asp,D) pk S der α-carbonsäure = 1,88; pk S der β-carbonsäure = 3,65 Die beiden Carbonsäuregruppen unterscheiden sich auch in ihrer chemischen Reaktivität
Modul 8: Bioinformatik A. Von der DNA zum Protein Proteinsynthese in silicio
 Modul 8: Bioinformatik A. Von der DNA zum Protein Proteinsynthese in silicio Ein Wissenschaftler erhält nach einer Sequenzierung folgenden Ausschnitt aus einer DNA-Sequenz: 5 ctaccatcaa tccggtaggt tttccggctg
Modul 8: Bioinformatik A. Von der DNA zum Protein Proteinsynthese in silicio Ein Wissenschaftler erhält nach einer Sequenzierung folgenden Ausschnitt aus einer DNA-Sequenz: 5 ctaccatcaa tccggtaggt tttccggctg
Pure Whey Protein Natural
 Wie Ihnen das Pure Whey Protein Natural dabei hilft, sich um Ihr Wohlbefinden zu kümmern. Proteine sind essentiell für den reibungslosen Ablauf der Funktionen im menschlichen Körper. Sie werden beim Wachstum,
Wie Ihnen das Pure Whey Protein Natural dabei hilft, sich um Ihr Wohlbefinden zu kümmern. Proteine sind essentiell für den reibungslosen Ablauf der Funktionen im menschlichen Körper. Sie werden beim Wachstum,
Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit
 Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit glukosespiegel: enge Regelung zum Schutz vor Unterund Überzuckerung (Hypo- bzw. Hyperglykämie) abhängig von Nahrungszufuhr und Stoffwechsel bei
Die Bedeutung der Kohlenhydrate für Leistung und Gesundheit glukosespiegel: enge Regelung zum Schutz vor Unterund Überzuckerung (Hypo- bzw. Hyperglykämie) abhängig von Nahrungszufuhr und Stoffwechsel bei
Aminosäuren. Die Mischung macht's. Die Proteinfabrik. ANKUBERO GmbH. Verschiedene Aminosäuren und Proteine
 Aminosäuren ANKUBERO GmbH Lieber Kunde, lieber Interessent, Die Mischung macht's Verschiedene Aminosäuren und Proteine Aufgeteilt in drei Hauptgruppen unterscheidet man essenzielle, semi-essenzielle oder
Aminosäuren ANKUBERO GmbH Lieber Kunde, lieber Interessent, Die Mischung macht's Verschiedene Aminosäuren und Proteine Aufgeteilt in drei Hauptgruppen unterscheidet man essenzielle, semi-essenzielle oder
Application Notes. Aracus
 Application Notes Aracus membrapure GmbH Wolfgang Küntscher Str. 14 16761 Hennigsdorf / Berlin Mail: info@membrapure.de Tel.: 03302 / 201 20 0 Fax: 03302 / 201 20 21 Index Physiological Extended 54 amino
Application Notes Aracus membrapure GmbH Wolfgang Küntscher Str. 14 16761 Hennigsdorf / Berlin Mail: info@membrapure.de Tel.: 03302 / 201 20 0 Fax: 03302 / 201 20 21 Index Physiological Extended 54 amino
15. Aminosäuren, Peptide und Proteine
 15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
15. Aminosäuren, Peptide und Proteine 1 Proteine (Polypeptide) erfüllen in biologischen ystemen die unterschiedlichsten Funktionen. o wirken sie z.b. bei vielen chemischen eaktionen in der atur als Katalysatoren
Das beste Essen für Sportler
 Das beste Essen für Sportler Schön, dass Sie hier sind! Einflussfaktoren auf die sportliche Leistungsfähigkeit Talent Regeneration Alter Ernährung Umfeld/Umwelt Gesundheit Training Motivation Lebensmittelkreis
Das beste Essen für Sportler Schön, dass Sie hier sind! Einflussfaktoren auf die sportliche Leistungsfähigkeit Talent Regeneration Alter Ernährung Umfeld/Umwelt Gesundheit Training Motivation Lebensmittelkreis
2. Prinzipien der Pflanzenstärkung durch Blattanwendung von L Aminosäuren
 Aminosäuren und Peptide für die Pflanzenstärkung von Dr. Helmut Wolf, Protan AG 1. Einführung 2. Prinzipien der Pflanzenstärkung durch Blattanwendung von L Aminosäuren 3. Wirtschaftlichkeit der Blattanwendung
Aminosäuren und Peptide für die Pflanzenstärkung von Dr. Helmut Wolf, Protan AG 1. Einführung 2. Prinzipien der Pflanzenstärkung durch Blattanwendung von L Aminosäuren 3. Wirtschaftlichkeit der Blattanwendung
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Aminosäuren und Proteine
 Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
Beispiele zur Multiple-Choice Prüfung in OC
 1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
Stoffwechsel von Aminosäuren (AS)
 Kapitel: Aminosäuren 1 Stoffwechsel von Aminosäuren (AS) Repetition Die Aminosäuren besitzen im Stoffwechsel der Zellen vier Funktionen: Aminosäuren sind die 20 Bausteine für die Biosynthese der Proteine.
Kapitel: Aminosäuren 1 Stoffwechsel von Aminosäuren (AS) Repetition Die Aminosäuren besitzen im Stoffwechsel der Zellen vier Funktionen: Aminosäuren sind die 20 Bausteine für die Biosynthese der Proteine.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler
 Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Vorlesung Biophysik I - Molekulare Biophysik Kalbitzer/Kremer/Ziegler 23.10. Zelle 30.10. Biologische Makromoleküle I 06.11. Biologische Makromoleküle II 13.11. Nukleinsäuren-Origami (DNA, RNA) 20.11.
Biochemie Übungsblatt Nr Fettsäuresynthese:
 Fettsäuresynthese: 1) Mit Hilfe des mitochondriale ACP? AcetylCoA Carrboxylase (Biothin als prosth. Gruppe) AcetylCoA + Kohlendioxid + ATP MalonylCoA + ADP + P 2)? Reguliert durch Insulin (Insulin hemmt
Fettsäuresynthese: 1) Mit Hilfe des mitochondriale ACP? AcetylCoA Carrboxylase (Biothin als prosth. Gruppe) AcetylCoA + Kohlendioxid + ATP MalonylCoA + ADP + P 2)? Reguliert durch Insulin (Insulin hemmt
Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom
 Johann Wolfgang Goethe-Universität Frankfurt am Main Deckblatt Fachbereich Biowissenschaften Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom 08.12.2008 Name: Vorname:
Johann Wolfgang Goethe-Universität Frankfurt am Main Deckblatt Fachbereich Biowissenschaften Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom 08.12.2008 Name: Vorname:
ERBOTIN PF. Erbsenproteinisolat. GUSTAV PARMENTIER GmbH
 ( 80% Protein) Geschmacksneutral Hohe Löslichkeit Hohe Emulgierfähigkeit Gute Wasser- und Fettbindefähigkeit Hochwertiger Proteinlieferant Isoliertes Erbsenprotein - ein hochfunktionelles. Das isolierte
( 80% Protein) Geschmacksneutral Hohe Löslichkeit Hohe Emulgierfähigkeit Gute Wasser- und Fettbindefähigkeit Hochwertiger Proteinlieferant Isoliertes Erbsenprotein - ein hochfunktionelles. Das isolierte
10 BIOGENE-AMINE 4 NICHT-PROTEINOGENE- AS. 20 PROTEINOGENE AS glucoplastisch/ketoplastisch 8 ESSENTIELLE AS
 Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Inhaltsverzeichnis. Das Warnecke-Konzept Mein Weg zum Ziel Ausgeglichene Energiezufuhr Sport als Ergänzung
 Inhaltsverzeichnis Das Warnecke-Konzept Mein Weg zum Ziel Ausgeglichene Energiezufuhr Sport als Ergänzung Powerstoff Eiweiß In einer Studie aus dem Jahr 2004 wurde gezeigt, dass Aminosäuren, die kleinen
Inhaltsverzeichnis Das Warnecke-Konzept Mein Weg zum Ziel Ausgeglichene Energiezufuhr Sport als Ergänzung Powerstoff Eiweiß In einer Studie aus dem Jahr 2004 wurde gezeigt, dass Aminosäuren, die kleinen
- Biochemieklausur Name: Matrikelnr.:
 07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
07.02.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Protein - Eiweiß Der Baustoff des Lebens
 Protein - Eiweiß Der Baustoff des Lebens Überblick 1. Protein Allgemein 2. Die biologische Wertigkeit 3. Arten von Protein 3.1 tierisches Protein 3.2 pflanzliches Protein 4. Der Proteinmythos 5. Gute Proteinquellen
Protein - Eiweiß Der Baustoff des Lebens Überblick 1. Protein Allgemein 2. Die biologische Wertigkeit 3. Arten von Protein 3.1 tierisches Protein 3.2 pflanzliches Protein 4. Der Proteinmythos 5. Gute Proteinquellen
Bachelor Studiengang Ernährungswissenschaften Seminar Biochemie der Ernährung (Modul BE2.3) Übersicht Seminarthemen
 Biochemie der Ernährung (Modul BE2.3) Prof. Dr. Stefan Lorkowski 1 Bachelor Studiengang Ernährungswissenschaften Seminar Biochemie der Ernährung (Modul BE2.3) Übersicht Seminarthemen Biosynthese von Aminosäuren
Biochemie der Ernährung (Modul BE2.3) Prof. Dr. Stefan Lorkowski 1 Bachelor Studiengang Ernährungswissenschaften Seminar Biochemie der Ernährung (Modul BE2.3) Übersicht Seminarthemen Biosynthese von Aminosäuren
Das Nahrungsmittel Ei Lehrerinformation
 Lehrerinformation 1/7 Arbeitsauftrag Die Sch erhalten eine umfassende Betrachtung der Inhaltsstoffe inkl. intensiver Befassung mit der Nahrungsmittelpyramide und der Wichtigkeit des Eis in diesem Zusammenhang.
Lehrerinformation 1/7 Arbeitsauftrag Die Sch erhalten eine umfassende Betrachtung der Inhaltsstoffe inkl. intensiver Befassung mit der Nahrungsmittelpyramide und der Wichtigkeit des Eis in diesem Zusammenhang.
-Klausur Biochemie Name: Matrikelnr.: 1. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist.
 4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
Allgemeine Pathologie. Störungen im Kupfer- Stoffwechsel
 Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
Allgemeine Pathologie Störungen im Kupfer- Stoffwechsel Physiologie (1): - das Übergangsmetall Kupfer ist als essentielles Spurenelement Bestandteil einer Reihe wichtiger Enzyme: - Ferro-oxidase I (Coeruloplasmin),
6. DNA -Bakteriengenetik
 6. DNA -Bakteriengenetik Konzepte: Francis Crick DNA Struktur DNA Replikation Gentransfer in Bakterien Bakteriophagen 2. Welcher der folgenden Sätze entspricht der Chargaff-Regel? A) Die Menge von Purinen
6. DNA -Bakteriengenetik Konzepte: Francis Crick DNA Struktur DNA Replikation Gentransfer in Bakterien Bakteriophagen 2. Welcher der folgenden Sätze entspricht der Chargaff-Regel? A) Die Menge von Purinen
Aminosäurebestimmung im Kochschinken
 1. Gegenstand der Untersuchung Es wurden 4 verschiedene Kochschinken eines Discounters hinsichtlich deren Gehalt an freien und NPN-gebundenen sowie möglichen Zusätzen untersucht. Darüber hinaus dienen
1. Gegenstand der Untersuchung Es wurden 4 verschiedene Kochschinken eines Discounters hinsichtlich deren Gehalt an freien und NPN-gebundenen sowie möglichen Zusätzen untersucht. Darüber hinaus dienen
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Behandlung von Diabetes
 04 Arbeitsanweisung Arbeitsauftrag Anhand des Foliensatzes werden die verschiedenen Behandlungsmethoden bei Diabetes Typ 1 und Typ 2 besprochen. Anschliessend werden noch kurz die Folgen bei einer Nichtbehandlung
04 Arbeitsanweisung Arbeitsauftrag Anhand des Foliensatzes werden die verschiedenen Behandlungsmethoden bei Diabetes Typ 1 und Typ 2 besprochen. Anschliessend werden noch kurz die Folgen bei einer Nichtbehandlung
Fette und ihre Funktionen. Müssen Fette sein?
 Fette und ihre Funktionen Müssen Fette sein? Ja! Fette sind: Wichtiger Bestandteil unserer täglichen Nahrung Energieträger Nummer 1 Quelle für essentielle n Vehikel für die Aufnahme fettlöslicher Vitamine
Fette und ihre Funktionen Müssen Fette sein? Ja! Fette sind: Wichtiger Bestandteil unserer täglichen Nahrung Energieträger Nummer 1 Quelle für essentielle n Vehikel für die Aufnahme fettlöslicher Vitamine
Ringvorlesung Bio(an)organische Chemie. Kofaktoren und Vitamine Die Moleküle des Lebens. Armin Geyer. Fachbereich Chemie Philipps-Universität
 Ringvorlesung Bio(an)organische Chemie Kofaktoren und Vitamine Die Moleküle des Lebens Armin Geyer Fachbereich Chemie Philipps-Universität 15. Apr. 2005 Inhalt Definition und Übersicht Antioxidantien:
Ringvorlesung Bio(an)organische Chemie Kofaktoren und Vitamine Die Moleküle des Lebens Armin Geyer Fachbereich Chemie Philipps-Universität 15. Apr. 2005 Inhalt Definition und Übersicht Antioxidantien:
Proteinbedarf und Proteinqualität
 Proteinbedarf und Proteinqualität für Patienten im Akutspital und für geriatrische Patienten Symposium Nestlé Health Science 2018 Dr. C. Römer-Lüthi 1 Generell gültige Grundlagen Dr.C.Römer-Lüthi 2 Wozu
Proteinbedarf und Proteinqualität für Patienten im Akutspital und für geriatrische Patienten Symposium Nestlé Health Science 2018 Dr. C. Römer-Lüthi 1 Generell gültige Grundlagen Dr.C.Römer-Lüthi 2 Wozu
52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat
 2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
1.6 ph-werte. Einführung Chemie Seite 19
 Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Organische Chemie der biologischen Stoffwechselwege
 Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Aminosäurenanalytik. Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE
 Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Aminosäurenanalytik Probenvorbereitung Eiweißfällung, Oxidation und Hydrolyse Karl-Heinz Jansen SYKAM CHROMATOGRAPHIE Proteinfällung 2 Proteinfällung 3 Proteinfällung 4 Proteinfällung 5 Proteinfällung
Stoffwechsel - Energiebereitstellung - Biomoleküle
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
-Klausur Biochemie Name: Matrikelnr.:
 25.07.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
25.07.207 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Häm. Biosynthese Pathophysiologie der Biosynthese
 Häm Biosynthese Pathophysiologie der Biosynthese Häm = Porphyrin farbige Verbindung, konjugiertes Ringsystem 4 Pyrrolringe ubiquitär in Tier- und Pflanzenreich prosthetische Gruppe von Hämoproteinen Mensch
Häm Biosynthese Pathophysiologie der Biosynthese Häm = Porphyrin farbige Verbindung, konjugiertes Ringsystem 4 Pyrrolringe ubiquitär in Tier- und Pflanzenreich prosthetische Gruppe von Hämoproteinen Mensch
BIOCHEMIE des Stoffwechsels ( )
 BIOCHEMIE des Stoffwechsels (772.114) 11. Einheit Protein und Aminosäure Stoffwechsel Abbau von Proteinen aus der Nahrung Abbau von zellulären Proteinen Transaminasen und Glutamat-Dehydrogenase Harnstoff-Cyclus
BIOCHEMIE des Stoffwechsels (772.114) 11. Einheit Protein und Aminosäure Stoffwechsel Abbau von Proteinen aus der Nahrung Abbau von zellulären Proteinen Transaminasen und Glutamat-Dehydrogenase Harnstoff-Cyclus
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Aminosäurestoffwechsel I. Grundlagen und Ammoniak-Stoffwechsel COO- +H 3 C R. Johannes Schmidt; Matthias Schnepper
 Aminosäurestoffwechsel I Grundlagen und Ammoniak-Stoffwechsel OO- 3 N R Johannes Schmidt; Matthias Schnepper Einführung Gliederung: Struktur und Einteilung der Aminosäuren Grundzüge des Aminosäurestoffwechsels
Aminosäurestoffwechsel I Grundlagen und Ammoniak-Stoffwechsel OO- 3 N R Johannes Schmidt; Matthias Schnepper Einführung Gliederung: Struktur und Einteilung der Aminosäuren Grundzüge des Aminosäurestoffwechsels
Soja-Lebensmittel - Quelle von hochwertigem Eiweiß
 Soja-Lebensmittel - Quelle von hochwertigem Eiweiß Thesenpapier des wissenschaftlichen Beirats der ENSA Einleitung Eiweiß ist ein wichtiger Grundnährstoff, der für das Wachstum und die Reparatur aller
Soja-Lebensmittel - Quelle von hochwertigem Eiweiß Thesenpapier des wissenschaftlichen Beirats der ENSA Einleitung Eiweiß ist ein wichtiger Grundnährstoff, der für das Wachstum und die Reparatur aller
Campherchinon (teuer)
 chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
chiral pool alle chiralen, nicht racemischen Verbindungen aturstoffe - müssen enantiomerenrein verfügbar sein - müssen leicht und rein isolierbar sein dann sind diese billig im andel verfügbar alle Verbindungen,
-Klausur Biochemie Name:
 -Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Die Pyrimidinsynthese
 Die Pyrimidinsynthese Bei der Pyrimidinsynthese wird zunächst der 6-Ring, also die Base zusammengefügt. Erst anschließend kommt es zum Anknüpfen der Ribose. Lokalisation: Zytoplasma Der Ausgang, der
Die Pyrimidinsynthese Bei der Pyrimidinsynthese wird zunächst der 6-Ring, also die Base zusammengefügt. Erst anschließend kommt es zum Anknüpfen der Ribose. Lokalisation: Zytoplasma Der Ausgang, der
DIE BEDEUTUNG DER AMINOSÄUREN IM SPITZENSPORT
 DIE BEDEUTUNG DER AMINOSÄUREN IM SPITZENSPORT Dr. Jürgen Spona Vitalogic (www.vitalogic.at) Vitalstoffe Vitamine Spurenelemente Kohlenhydrate, Fette AMINOSÄUREN 2 3 Amino Acids State of the Art 4 Verdauungsorgane
DIE BEDEUTUNG DER AMINOSÄUREN IM SPITZENSPORT Dr. Jürgen Spona Vitalogic (www.vitalogic.at) Vitalstoffe Vitamine Spurenelemente Kohlenhydrate, Fette AMINOSÄUREN 2 3 Amino Acids State of the Art 4 Verdauungsorgane
Ernährungsinformationen0
 Ernährungsinformationen AllgemeinePunkte: SportlersolltenjedenTageinwertvollesFrühstückessen 3MahlzeitenproTag o Zwischenmahlzeitensollten gesund sein. Nüsse Obst/Gemüse Snacks(nurwennmankeinGewichtverlierenmöchte)
Ernährungsinformationen AllgemeinePunkte: SportlersolltenjedenTageinwertvollesFrühstückessen 3MahlzeitenproTag o Zwischenmahlzeitensollten gesund sein. Nüsse Obst/Gemüse Snacks(nurwennmankeinGewichtverlierenmöchte)
Die spezifische Vitaminkombination in nur einer Tablette.
 Die spezifische Vitaminkombination in nur einer Tablette. Die gezielte Vitaminergänzung bei medikamentös behandelter Epilepsie. Schließen Sie Ihre Vitaminlücken ganz gezielt. Hinweis EPIVIT ist ein ernährungsmedizinisch
Die spezifische Vitaminkombination in nur einer Tablette. Die gezielte Vitaminergänzung bei medikamentös behandelter Epilepsie. Schließen Sie Ihre Vitaminlücken ganz gezielt. Hinweis EPIVIT ist ein ernährungsmedizinisch
LIPIDE. Eine kleine Geschichte
 Eine kleine Geschichte Das Acyl,der Bus, steht ahnungslos auf dem Triacylglycerin-Parkplatz rum Plötzlich, oh weh, bekommt die Zelle ein Signal: Achtung! Achtung! Wir brauchen Energie Nur, wo ist denn
Eine kleine Geschichte Das Acyl,der Bus, steht ahnungslos auf dem Triacylglycerin-Parkplatz rum Plötzlich, oh weh, bekommt die Zelle ein Signal: Achtung! Achtung! Wir brauchen Energie Nur, wo ist denn
Schließen Sie gezielt Vitaminlücken bei Epilepsie.
 Schließen Sie gezielt Vitaminlücken bei Epilepsie. Weitere Fragen zum Thema Vitaminlücken bei Epilepsie beantworten wir Ihnen gerne: Desitin Arzneimittel GmbH Abteilung Medizin Weg beim Jäger 214 22335
Schließen Sie gezielt Vitaminlücken bei Epilepsie. Weitere Fragen zum Thema Vitaminlücken bei Epilepsie beantworten wir Ihnen gerne: Desitin Arzneimittel GmbH Abteilung Medizin Weg beim Jäger 214 22335
ORGANISCHE CHEMIE. Aminosäuren und Proteine
 RGAISE EMIE Aminosäuren und Proteine Aminosäuren (AS) R 2 arbonsäuren mit einer Aminogruppe Die (etwa) 20 proteinogenen Aminosäuren sind alle α-aminosäuren (Aminogruppe an -2), unterscheiden sich durch
RGAISE EMIE Aminosäuren und Proteine Aminosäuren (AS) R 2 arbonsäuren mit einer Aminogruppe Die (etwa) 20 proteinogenen Aminosäuren sind alle α-aminosäuren (Aminogruppe an -2), unterscheiden sich durch
Wie oft soll ich essen?
 Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Wie oft soll ich essen? Wie sollen Sie sich als Diabetiker am besten ernähren? Gesunde Ernährung für Menschen mit Diabetes unterscheidet sich nicht von gesunder Ernährung für andere Menschen. Es gibt nichts,
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
puls109 Sport und Ernährungsberatung
 Vitamine Das Wichtigste in Kürze Vitamine sind für alle Prozesse des Lebens extrem wichtig. Deshalb muss man die tägliche Mindestmenge zu sich nehmen. Durch Einseitige Ernährung kann ein Mangel entstehen.
Vitamine Das Wichtigste in Kürze Vitamine sind für alle Prozesse des Lebens extrem wichtig. Deshalb muss man die tägliche Mindestmenge zu sich nehmen. Durch Einseitige Ernährung kann ein Mangel entstehen.
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte)
 Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Besser leben mit Gicht. Seite 3 Seite 4 Seite 5 Seite 6. Zu starke Schweißbildung. besser natürlich behandeln. Gicht-Telegramm
 Besser leben mit Gicht GT II-2014 Seite 3 Seite 4 Seite 5 Seite 6 Purinrechner jetzt auf i-phone und Android Warnung vor dem Einsatz von NSAR wie Diclofenac Zu starke Schweißbildung besser natürlich behandeln
Besser leben mit Gicht GT II-2014 Seite 3 Seite 4 Seite 5 Seite 6 Purinrechner jetzt auf i-phone und Android Warnung vor dem Einsatz von NSAR wie Diclofenac Zu starke Schweißbildung besser natürlich behandeln
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Getreide-Vitamine. Definition Funktion Vitaminarten Ernährung Vitamine im Korn Vitamine im Brot Vertiefung II-4 II-4
 II-4 II-4 Was sind Vitamine? Vitamine steuern in allen Lebensformen nahezu gleiche Abläufe. Chemisch betrachtet handelt um völlig unterschiedliche Stoffgruppen. Der Begriff Vitamin enthält die Bezeichnung
II-4 II-4 Was sind Vitamine? Vitamine steuern in allen Lebensformen nahezu gleiche Abläufe. Chemisch betrachtet handelt um völlig unterschiedliche Stoffgruppen. Der Begriff Vitamin enthält die Bezeichnung
Folsäure. Struktur = Pteroylglutamat; PteGLU n
 Folsäure Struktur = Pteroylglutamat; PteGLU n Biochemische Wirkungsweise Übertragung von C1-Einheiten; Wirksame Form ist das Tetrahydrofolat (H 4 -Folat), das durch Serin in das N 5,N 10 -Methylentetrahydrofolat
Folsäure Struktur = Pteroylglutamat; PteGLU n Biochemische Wirkungsweise Übertragung von C1-Einheiten; Wirksame Form ist das Tetrahydrofolat (H 4 -Folat), das durch Serin in das N 5,N 10 -Methylentetrahydrofolat
24-STUNDEN-SAMMELURIN
 Blutfarbstoffs (Hämoglobin), wird normalerweise nicht mit dem Urin ausgeschieden. Erst bei einer erhöhten Konzentration im Blutserum enthält auch der Urin Bilirubin dies ist der Fall, wenn eine Funktionsstörung
Blutfarbstoffs (Hämoglobin), wird normalerweise nicht mit dem Urin ausgeschieden. Erst bei einer erhöhten Konzentration im Blutserum enthält auch der Urin Bilirubin dies ist der Fall, wenn eine Funktionsstörung
Funktionelle Gruppen Amine
 sind Stickstoff-Derivate, die als schwache organische Basen gelten. Funktionelle Gruppen Einfachstes Amin, Methanamin. Ammoniak besitzt drei -Atome, die formal durch organische este ersetzt werden können.
sind Stickstoff-Derivate, die als schwache organische Basen gelten. Funktionelle Gruppen Einfachstes Amin, Methanamin. Ammoniak besitzt drei -Atome, die formal durch organische este ersetzt werden können.
Inhalt. Ganzheitliche Gesundheit... 9. Ernährung Der Mensch ist was er isst... 23. Möchten Sie lange gesund und jung bleiben?... 3
 Link zum Titel: Detlef Pape, Gesund - Vital - Schlank, Deutscher Ärzte-Verlag 2002 Inhalt Geleitwort................................................................ 1 Zum Anfang..............................................................
Link zum Titel: Detlef Pape, Gesund - Vital - Schlank, Deutscher Ärzte-Verlag 2002 Inhalt Geleitwort................................................................ 1 Zum Anfang..............................................................
Allgemeine Ernährungsrichtlinien für SpitzensportlerInnen
 Allgemeine Ernährungsrichtlinien für SpitzensportlerInnen Univ. Prof. Dr. Paul Haber Univ. Prof. Dr. Paul Haber 1 5 Ernährungsbilanzen Bilanz: Differenz zwischen Zufuhr (mit Ernährung) und Verbrauch oder
Allgemeine Ernährungsrichtlinien für SpitzensportlerInnen Univ. Prof. Dr. Paul Haber Univ. Prof. Dr. Paul Haber 1 5 Ernährungsbilanzen Bilanz: Differenz zwischen Zufuhr (mit Ernährung) und Verbrauch oder
Wirkung und Nachweis von Alkohol im menschlichen Körper
 Wirkung und Nachweis von Alkohol im menschlichen Körper Agenda Wirkung des Alkohols auf den menschlichen Körper Messsysteme Anwendungsempfehlungen zu Atemalkoholmessgeräten 0 Alkohol und Drogentestgeräte
Wirkung und Nachweis von Alkohol im menschlichen Körper Agenda Wirkung des Alkohols auf den menschlichen Körper Messsysteme Anwendungsempfehlungen zu Atemalkoholmessgeräten 0 Alkohol und Drogentestgeräte
Parotis Pankreas. Dünndarm Bürstensaum. Amylose Amylopektin Glykogen. Maltose. Glucose. Isomaltose. Saccharose. Fructose. Lactose. Galaktose.
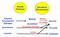 Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 12.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 12.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
BIOINF1110 Einführung in die Bioinforma7k. 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on
 BIOINF1110 Einführung in die Bioinforma7k 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Zentrum für Bioinforma7k Tübingen Proteine Zentrales Dogma DNA Transkription mrna
BIOINF1110 Einführung in die Bioinforma7k 5. Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Zentrum für Bioinforma7k Tübingen Proteine Zentrales Dogma DNA Transkription mrna
Was weiß ich über Ernährung im Hobbysport?
 Was weiß ich über Ernährung im Hobbysport? 1 Was weiß ich über Sport? 2 Botschaft Nummer 1 Leistung und Leistungssteigerungen sind bis ins hohe Alter möglich! 3 Marathoner Sprinter 4 Botschaft Nummer 2
Was weiß ich über Ernährung im Hobbysport? 1 Was weiß ich über Sport? 2 Botschaft Nummer 1 Leistung und Leistungssteigerungen sind bis ins hohe Alter möglich! 3 Marathoner Sprinter 4 Botschaft Nummer 2
- Biochemieklausur Name: Matrikelnr.:
 08.07.20 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
08.07.20 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
BIOINF1110 Einführung in die Bioinforma7k. Molekulare Maschinen Proteinstrukturen und ihre Funk/on
 BIOINF1110 Einführung in die Bioinforma7k Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Angewandte Bioinforma0k Zentrum für Bioinforma0k Tübingen Proteine 2 Zentrales Dogma
BIOINF1110 Einführung in die Bioinforma7k Molekulare Maschinen Proteinstrukturen und ihre Funk/on Oliver Kohlbacher Angewandte Bioinforma0k Zentrum für Bioinforma0k Tübingen Proteine 2 Zentrales Dogma
Die spezifische Vitaminkombination in nur einer Tablette.
 Die spezifische Vitaminkombination in nur einer Tablette. Die gezielte Vitaminergänzung bei medikamentös behandeltem Morbus Parkinson. Schließen Sie Ihre Vitaminlücken ganz gezielt. Hinweis PARKOVIT ist
Die spezifische Vitaminkombination in nur einer Tablette. Die gezielte Vitaminergänzung bei medikamentös behandeltem Morbus Parkinson. Schließen Sie Ihre Vitaminlücken ganz gezielt. Hinweis PARKOVIT ist
Chemische Evolution. Biologie-GLF von Christian Neukirchen Februar 2007
 Chemische Evolution Biologie-GLF von Christian Neukirchen Februar 2007 Aristoteles lehrte, aus Schlamm entstünden Würmer, und aus Würmern Aale. Omne vivum ex vivo. (Alles Leben entsteht aus Leben.) Pasteur
Chemische Evolution Biologie-GLF von Christian Neukirchen Februar 2007 Aristoteles lehrte, aus Schlamm entstünden Würmer, und aus Würmern Aale. Omne vivum ex vivo. (Alles Leben entsteht aus Leben.) Pasteur
